Utforsk rent sølv og sølvlegeringer som brukes til smykker
En omfattende guide til rent sølv og sølvlegeringsmaterialers egenskaper og funksjoner
Sølv har en forlokkende hvit glans, høy kjemisk stabilitet og estetisk samleverdi, noe som gjør det svært populært blant folk (spesielt kvinner), og det har derfor fått tittelen "kvinnenes metall". Det er mye brukt til smykker, pyntegjenstander, sølvtøy, servise, gratulasjonsgaver, medaljer og minnemynter. Sølvsmykker har et stort marked i utviklingsland, og sølvservise er populært blant familier. Minnemynter i sølv er utsøkt designet, utstedes i begrenset antall og har en verdibevarende og verdiøkende funksjon, noe som gjør dem svært ettertraktet blant myntsamlere og investorer.

Innholdsfortegnelse
Seksjon Ⅰ Grunnleggende egenskaper ved sølv
1. Fysiske egenskaper ved sølv
Sølv er et grunnstoff i gruppen IB i 5. periode i det periodiske system, med grunnstoffsymbolet Ag, atomnummer 47 og relativ atommasse 107,870. Sølv har en svært høy refleksjonsevne for synlig lys, 92%-96% i bølgelengdeområdet 380-780 nm, den høyeste blant alle metalliske grunnstoffer, og betydelig høyere enn andre edelmetallelementer (Figur 4-1). Derfor fremstår sølv som lyst
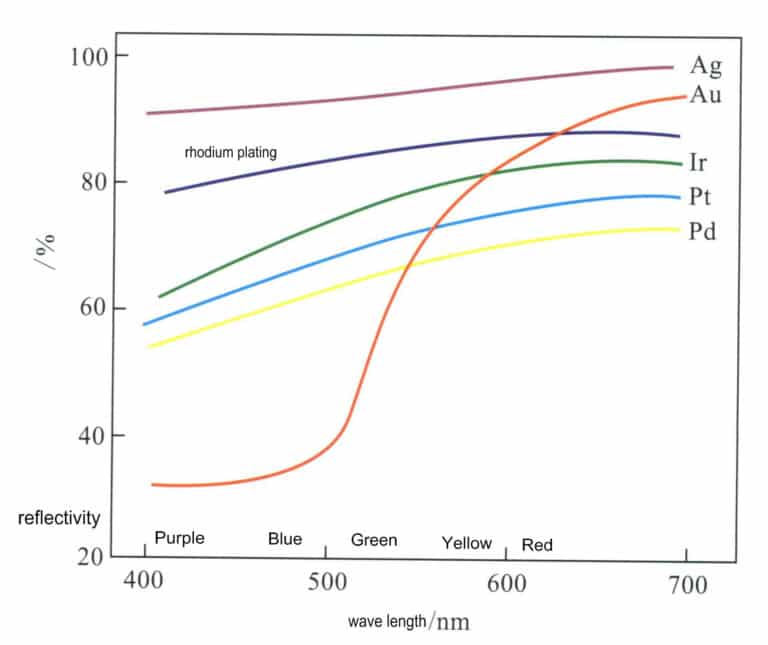
De viktigste fysiske egenskapene til sølv er vist i tabell 4-1. Ved romtemperatur er tettheten til sølv 10,49 g/cm3og etter hvert som temperaturen øker, synker sølvets tetthet til 9,35 g/cm3 rett før det smelter. Sølv er den beste lederen av elektrisitet og varme blant alle metaller, noe som gjør det vanskeligere å 3D-printe og lasersveise, ettersom varmen som tilføres lokalt, raskt ledes ut i omgivelsene, noe som gjør det vanskelig å konsentrere varmen.
Tabell 4-1 De viktigste fysiske egenskapene og indeksverdiene til sølv
| Fysiske egenskaper | Indeksverdier | Fysiske egenskaper | Indeksverdier |
|---|---|---|---|
| Fargekoordinater | L* = 95,8, a* =-0,7, b* = 5,3 | Lineær ekspansjonskoeffisient (0-100 ℃) | 19.2 x 10-6/℃ |
| Tetthet (20 ℃) | 10,49 g/cm3 | Resistivitet (25 ℃) | 1.59 x 10-6Ω⸳cm |
| Smeltepunkt | 961.78 | Spesifikk varmekapasitet (25℃) | 25,41 J/(mol⸳K) |
| Kokepunkt | 2177 | Fusjonsvarme | 11,30 kJ/mol |
| Damptrykk (smelting) | 0,38 Pa | Fordampningsvarme | 284,6 kJ/mol |
| Varmeledningsevne (25 ℃) | 433 W/(m⸳K) | Debye-temperatur ϴd | 215 K |
| Termisk diffusivitet (0 ℃) | 1.75 m2/s | Magnetisk susceptibilitet | -0.15 x 10-6 cm3/g |
2. Kjemiske egenskaper ved sølv
Sølv har ikke reaktive kjemiske egenskaper, og den kjemiske stabiliteten er bedre enn for metaller som jern og kobber. Det reagerer ikke med oksygen, hydrogen, inerte gasser og organiske gasser ved romtemperatur, og selv ved høye temperaturer reagerer det ikke med hydrogen eller inerte gasser, noe som gjør det utsatt for korrosjon og misfarging.
Sølv har en sterk affinitet for svovel, og i atmosfærer som inneholder skadelige stoffer som H2S, SO2COS (karbonylsulfid), og i vandige løsninger som inneholder sulfider, er det utsatt for korrosjon og danner uløselig svart Ag2S-forbindelser på overflaten, og korrosjonsatferden viser for det meste elektrokjemiske egenskaper. Når sølv blir liggende i luften, danner overflaten gradvis svart Ag2S, noe som fører til at smykker blir matte og misfargede. Denne egenskapen ved sølv har stor innvirkning på dets verdi som edelmetall. Ag2S kan brytes ned til metallisk sølv og SO2 når den varmes opp i luften.
Ved romtemperatur løser sølv seg i salpetersyre og konsentrert svovelsyre, men er uløselig i saltsyre og fortynnet svovelsyre. Ved oppvarming oppløses det i saltsyre, svovelsyre, salpetersyre og kongevann. I likhet med gull reagerer sølv lett med kongevann og mettede klorerte syrer; sølv danner et AgCl-nedfall, som kan brukes til å skille gull og sølv.
I likhet med gull har sølv god korrosjonsbestandighet i alkaliske oppløsninger og smeltede alkalimetaller, noe som gjør det til et vanlig smeltedigelmateriale for smeltet NaOH og KOH.
Sølv kan langsomt kombineres med halogener ved romtemperatur, men under oppvarmingsforhold kan sølv reagere svært raskt med halogener og danne sølvhalogenider. Sølv oppløses i visse kompleksdannere som er mettet med luft (for eksempel cyanider av alkalimetaller fra gruppe ⅠA og jordalkalimetaller fra gruppe ⅡA, oksygenholdige cyanidløsninger og sure tioureaoppløsninger som inneholder Fe3+ ), og danner stabile komplekser (Tabell 4-2).
Tabell 4-2 Sølvets oppførsel i ulike korrosive medier
| Etsende medier | Middels tilstand | Temperatur | Graden av korrosjon av sølv | |||
|---|---|---|---|---|---|---|
| Etsende medier | Middels tilstand | Temperatur | Nesten ingen korrosjon | Lett korrosjon | Moderat korrosjon | Alvorlig korrosjon |
| Svovelsyre | 98% | 18℃ | Ja | |||
| Svovelsyre | 98% | 100℃ | Ja | |||
| Salpetersyre | 0,1 mol/L | Romtemperatur | Ja | |||
| Salpetersyre | 70% | Romtemperatur | Ja | |||
| Salpetersyre | Smoke (>90%) | Romtemperatur | Ja | |||
| Saltsyre | 36% | 18℃ | Ja | |||
| Saltsyre | 36% | 100℃ | Ja | |||
| Hydrofluorsyre | 40% | Romtemperatur | Ja | |||
| kongevann | 75%HCl + 25%HNO3 | Romtemperatur | Ja | |||
| Hydrogensulfid | Luftfuktighet | Romtemperatur | Ja | |||
| Fosforsyre | > 90% | Romtemperatur - 100 °C | Ja | |||
| Klor | Tørt klor | Romtemperatur | Ja | |||
| Klor | Våt klor | Romtemperatur | Ja | |||
| Sitronsyre | Romtemperatur - 100 °C | Ja | ||||
| Kvikksølv | Romtemperatur | Ja | ||||
| Jern(I II)kloridoppløsning | Romtemperatur | Ja | ||||
| Sod iumhydroksidløsning | Romtemperatur | Ja | ||||
| Ammoniakkløsning | Romtemperatur | Ja | ||||
| Kaliumcyanidoppløsning | Romtemperatur ~ 100 ℃ | Ja | ||||
| Smeltet natriumhydroksid | 350℃ | Ja | ||||
| Smeltet natriumperoksid | 350℃ | Ja | ||||
| Smeltet natriumsulfat | 350℃ | Ja | ||||
Sølv kan danne forbindelser med ulike stoffer og finnes i form av monovalente ioner i disse forbindelsene, for eksempel AgNO3, Ag2O, AgCl, AgBr, AgCN, Ag2SO4osv. AgNO3 brukes ofte som hovedsalt for cyanidfri forsølvning og er en kilde til sølvioner. Sølvnitratløsning inneholder et stort antall sølvioner, noe som gjør den svært oksidativ, lett nedbrytes i lys, kan forårsake proteinkoagulering og har visse etsende effekter på huden, så den bør oppbevares i brune flasker. Ag2O er et svartbrunt pulver med dårlig termisk stabilitet, som spaltes til sølv og oksygen ved oppvarming. AgCl er uløselig i vann, men lett løselig i KCN, NaCN og andre stoffer. AgCl suspendert i fortynnet svovelsyre kan lett reduseres til sølv av negativt ladede metaller som sink, jern osv., og denne enkle metoden er mye brukt til raffinering av sølv.
AgBr har de samme egenskapene som AgCl, løser seg i ammoniumsalter, tiosulfater, sulfitter og cyanidløsninger, og kan lett reduseres til metallisk sølv. De lysfølsomme egenskapene til sølvhalogenider er de viktigste egenskapene; under påvirkning av lys brytes de ned til sølv og frie halogener. Denne egenskapen utnyttes til å produsere fotografisk film, fotopapir og sensibiliserte membraner.
3. Mekaniske egenskaper
De viktigste mekaniske egenskapene til rent sølv er vist i tabell 4-3. Rent sølv er veldig mykt, med god duktilitet og smidighet, nest etter gull i duktilitet, og kan presses til tynne plater og trekkes til fine tråder; 1 gram sølv kan trekkes til en 1800 meter lang tråd og valses til folie med en tykkelse på 10 μm. Men når sølv inneholder små mengder urenheter som Sb, Bi og Pb, blir det sprøtt, og duktiliteten reduseres betydelig, med effekten av Pb som den mest uttalte.
Tabell 4-3 viser de viktigste mekaniske egenskapene til glødet rent sølv.
| Mekaniske egenskaper | Indeksverdier | Mekaniske egenskaper | Indeksverdier |
|---|---|---|---|
| Brinell-hardhet HB/N/mm2 | 25 | Krympningshastighet i tverrsnitt /% | 80 ~ 95 |
| Strekkfasthet /MPa | 140 ~ 160 | Elastisk modul E/GPa | 82 |
| Strekkgrense /MPa | 20 ~ 25 | Skjæremodul G/GPa | 28 |
| Forlengelseshastighet /% | 40 ~ 50 | Kompresjonsmodul B/GPa | 101.8 |
Rent sølv kan styrkes gjennom kaldbearbeiding Figur 4-2. Bearbeidingshastigheten påvirker de mekaniske egenskapene til sølv. Den første prosesseringshastigheten for glødet rent sølv kan nå 99%. Etter hvert som bearbeidingshastigheten øker, øker hardheten, strekkfastheten og flytegrensen til sølv, mens forlengelseshastigheten raskt avtar, og arbeidsherdingshastigheten viser et mønster med først rask og deretter langsom. På grunn av rent sølvs lave stablingsfeilenergi er imidlertid ikke den arbeidsherdende effekten betydelig, og styrken og hardheten etter bearbeiding forblir veldig lav, noe som gjør det vanskelig å oppfylle styrkekravene for å sette smykker.
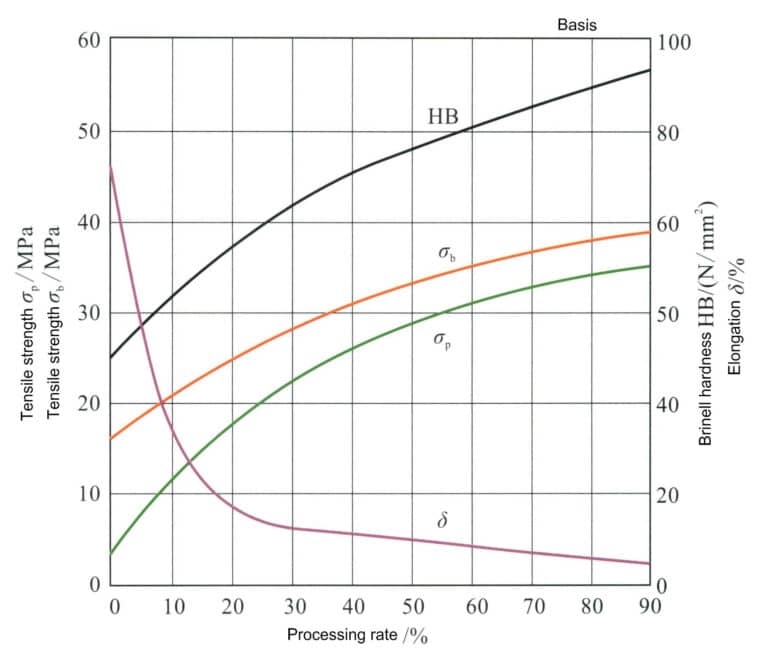
Den lave stablingsfeilenergien til rent sølv betyr at den arbeidsherdende effekten ikke er betydelig, og styrken og hardheten etter bearbeiding forblir svært lav, noe som gjør det vanskelig å oppfylle styrkekravene for innfatning av smykker. De mekaniske egenskapene til sølv i den bearbeidede herdede tilstanden endres raskt etter glødebehandling. Når glødetemperaturen øker, reduseres hardheten til rent sølv gradvis ved forskjellige prosesseringshastigheter, men reduksjonshastigheten må være mer konsistent. Når prosesseringshastigheten er under 50%, reduseres hardheten raskest ved en glødetemperatur på 200 °C; når prosesseringshastigheten er over 70%, reduseres hardheten raskest ved en glødetemperatur på 100 °C (Figur 4-3).
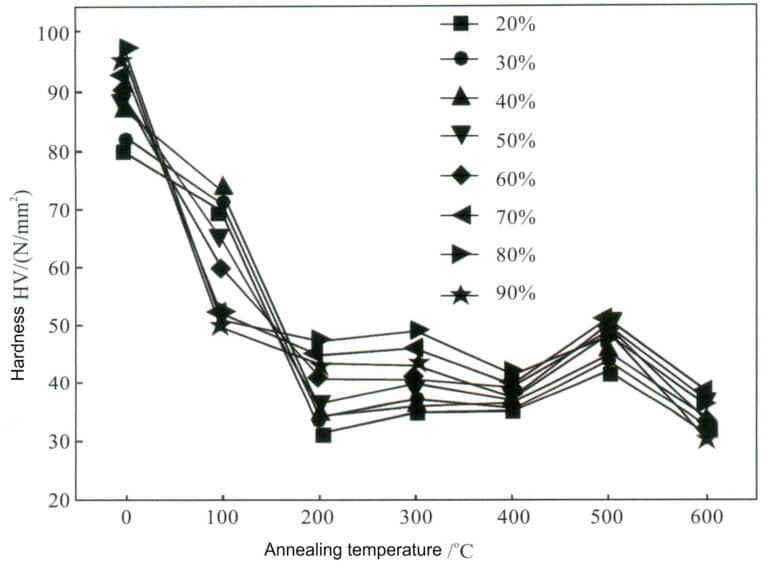
Et annet kjennetegn ved rent sølv i bearbeidet tilstand er at det er utsatt for "naturlig aldringsmykning", noe som betyr at styrken og hardheten til den bearbeidede profilen eller produktet gradvis reduseres under naturlig plassering, noe som er ugunstig for bruk av smykker. Oppmykningen av rent sølv under naturlig aldring er faktisk forårsaket av utvinning eller til og med dannelse av omkrystalliserte strukturer. Forskning viser at endringen i styrken til rent sølv etter kald deformasjon er relatert til materialets renhet, deformasjonsmengde, aldringstemperatur og plasseringstid. Polykrystallinsk rent sølv kan til og med oppleve naturlig aldringsmykning ved temperaturer under 20 ℃; mykningshastigheten avhenger av deformasjonen og urenhetsinnholdet i rent sølv. Omfanget av behandlingsdeformasjonen påvirker også i stor grad aldringsmykningen. Sølv med en renhet på 99,999% begynner å mykne etter å ha blitt deformert med 99% og holdt i 10 timer ved 20 °C, mens det etter 50% deformasjon kan opprettholdes i 100 timer ved 20 °C før det begynner å mykne.
4. Prosessytelse
Sølv har et relativt lavt smeltepunkt og kan smeltes ved hjelp av flamme-, induksjons- og motstandsoppvarming. Under smelting av sølv oppstår det imidlertid ofte et fenomen som kalles "sølvregn", som kjennetegnes av metallsprut, noe som fører til betydelige tap. Når sølv smeltes i et miljø med dårlige atmosfæriske forhold eller vakuum, er flyktigheten til sølv relativt høy, og den er enda høyere i en oksiderende atmosfære enn i en reduserende atmosfære.
Sølv er utsatt for dannelse av porøsitetsdefekter under støping, og prinsippet for dannelsen av dem er nært knyttet til sølvets egenskaper. I følge støpedannelsesteorien er hovedårsaken til generering av porøsitet at under størkningsprosessen reduseres løseligheten av gass i det smeltede metallet med temperaturfallet, noe som fører til gassovermetning, nedbør og boblevekst, som ikke blir utvist i tide, noe som resulterer i porer. Porene i sølvstøpegods er relatert til oksygenet som absorberes av det smeltede metallet. Fra det binære fasediagrammet Ag-O (figur 4-4) kan man se at når den mettede oksygensølvsmelten størkner, begynner den å størkne ved ca. 951 °C under sølvsmeltepunktet (961,78 °C), og størkningen er fullført ved ca. 931 °C.
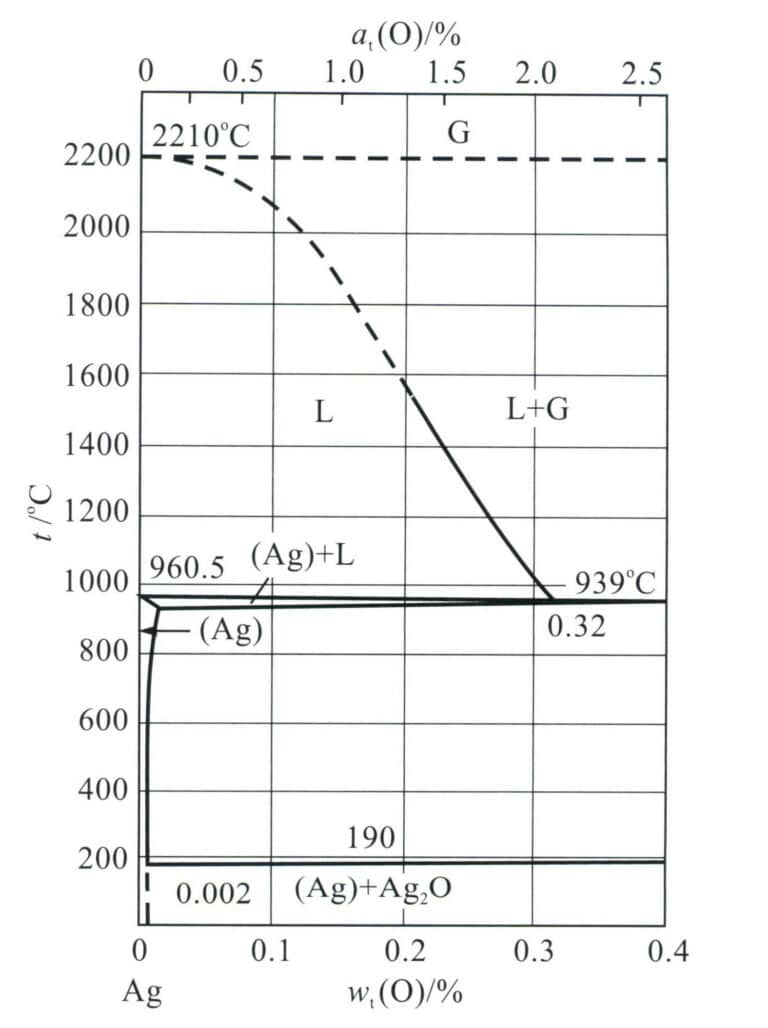
Merk: G representerer gassfasen; (Ag) +L representerer tofaseregionen fast-væske,
hvor (Ag) representerer den sølvbaserte faste løsningen, og L representerer væskefasen.
Tabell 4-4 viser løseligheten av oksygen oppløst som atomer i sølv i en oksygenatmosfære på 1 atm. Løseligheten av oksygen i smeltet sølv rett over smeltepunktet er høyest, ca. 3200 x 10-6og når 21 ganger sitt eget volum. Når temperaturen øker, øker sølvvæskens overopphetingsgrad, og oksygenets løselighet avtar.
Når sølvvæsken størkner, reduseres løseligheten av oksygen i fast sølv betydelig. Løseligheten av oksygen i fast sølv ved 931 °C når sitt maksimum, omtrent 60 x10-6. Når temperaturen synker, synker løseligheten av oksygen i fast sølv raskt, og ved romtemperatur kan sølv knapt absorbere oksygen. Løseligheten av oksygen er ikke bare relatert til temperatur, men også til partialtrykket av oksygen. Når partialtrykket av oksygen øker, øker løseligheten, og reaksjonen mellom sølv og oksygen endres også.
Tabell 4-4 viser løseligheten av oksygen i sølv i en oksygenatmosfære på 1 atm.
| Temperatur /℃ | Temperatur /℃ | 200 | 400 | 600 | 800 | 973 | 1024 | 1075 | 1125 |
|---|---|---|---|---|---|---|---|---|---|
| Oksygeninnhold | x10-6 | 0.03 | 1.4 | 10.6 | 38.1 | 3050 | 2950 | 2770 | 2640 |
| Oksygeninnhold | mm3/g | - | - | - | - | 2135 | 2056 | 1939 | 1849 |
Under størkning vil stoffer som er oppløst i sølvvæsken, for eksempel O, N og H, bli utskilt til fast-væske-grensesnittet. Når metningsløseligheten er overskredet, vil de frigjøres. Dannelsen av gassporer består av to stadier: kjernedannelse og vekst. Kjernedannelsen må overvinne de kombinerte effektene av atmosfærisk trykk, metallets statiske trykk og tilleggstrykk fra overflatespenning. Først når trykket i gassen som utfelles, overstiger den totale verdien av de ytre trykkene, kan det dannes en boblekjerne. Boblen vokser videre, og når den blir stor nok, øker oppdriftskraften som virker på den, noe som får den til å stige og løsne. Når boblens fuktingsvinkel med faststoffoverflaten er ϴ> 90, er den lett å løsne; når ϴ< 90, er den ikke lett å løsne. Hvis dendrittveksten under størkning er større enn stigningshastigheten, vil de voksende dendrittene omslutte boblene fullstendig og danne gassporer.
Sølv har en myk tekstur, noe som gjør det velegnet til håndlagde smykker. I tradisjonell sølvsmykkeproduksjon brukes rent sølv i stor utstrekning til å lage filigran- og vevde smykker, ofte ved hjelp av teknikker som hamring og gravering for å danne dekorative mønstre på smykkets overflate. I moderne smykkeproduksjon brukes også kaldbearbeidingsteknikker som valsing, trekking, stempling og hydraulisk pressing i stor utstrekning til å bearbeide sølvsmykker, der man utnytter den utmerkede duktiliteten til rent sølv. Teknikker som spinning, dyptrekking og dypstempling brukes ofte til å lage sølvskåler, sølvkopper og annet kunsthåndverk.
Del II Renhet og klassifisering av sølvsmykker
1. Renhetsmerking av sølvsmykker
For sølvsmykker angis renheten med en kombinasjon av tusendels renhet og sølv, Ag eller S (S er forkortelsen for sølv på engelsk). For eksempel kan sølvsmykker som inneholder 92,5%, merkes med et renhetsmerke som 925 sølv, 925Ag, 925 S eller 925. For sølvsmykker med en renhet som ikke er lavere enn 99%, er renhetsmerket merket som finsølv, 990 sølv, 990 Ag eller S 990. Det som vanligvis omtales som tusendels sølv på markedet (med et sølvinnhold som ikke er lavere enn 99,9%), er ensartet merket som rent sølv.
2. Klassifisering av sølvsmykkers renhet
Sølv er mye brukt i produksjonen av smykker, håndverk og andre dekorative gjenstander. Basert på renheten av sølv, kan det deles inn i smykkesølv med høy renhet og smykkesølv med vanlig renhet.
2.1 Smykkesølv med høy renhet
Som navnet antyder, refererer smykkesølv med høy renhet til sølv med en høy renhetsgrad, som kan deles inn i flere kategorier:
(1) Rent sølv.
Teoretisk sett skal sølvinnholdet være 100%. Men på samme måte som "gull ikke er helt rent", er heller ikke sølv det. Selv med dagens vitenskapelige og teknologiske nivå er det svært vanskelig å smelte sølv med en renhet på 100%, og man kan bare komme i nærheten av denne renhetsverdien. Rent sølv er også kjent som "finsølv", og det har fått navnet sitt på grunn av de unike mønstrene som dannes på overflaten under smelte-, raffinerings- og kondenseringsprosessene. Når det gjelder smykkematerialer, er det verken nødvendig eller praktisk å forfølge sølvets renhetsgrad. Derfor klassifiseres sølv med en renhet som ikke er lavere enn 99,6% i bransjen generelt som finsølv. Sølv med et innhold som ikke er lavere enn 99,9% kalles rent sølv.
(2) 990 finsølv.
Sølvinnholdet må være minst 990 ‰. 990‰ finsølv ble tidligere ofte brukt som standardsølv for sirkulasjon og handel. Det kan brukes som sikkerhet for eiendom, som sølvbacking for bedriftskonsortier og som medium for handelsutveksling.
Rent sølv og 990-sølv har en høyere kvalitet, noe som gjør dem mykere i konsistensen. De brukes vanligvis bare til sølvsmykker uten utsmykning, og det er vanligst med sølvsmykker i tradisjonell stil.
2.2 Smykkesølv av vanlig renhet
Smykkesølv av vanlig renhet ved å tilsette en liten mengde andre metaller til rent sølv eller sterlingsølv, noe som resulterer i en hardere tekstur av sølv. Denne typen sølv er vanligvis basert på Ag-Cu-legeringer, ettersom kobber har fysiske og kjemiske egenskaper som ligner på sølvets, noe som kan gi farget sølv seighet og opprettholde god duktilitet. I tillegg kan noen legeringselementer til en viss grad undertrykke den sløvende effekten av luft på sølvsmykker. Derfor er overflateglansen til mange fargede sølvpynt mindre utsatt for endring sammenlignet med rent sølv og sterlingsølv. Vanlig renhet smykker sølv inkluderer hovedsakelig følgende kategorier:
(1) 980 sølv.
Angir et sølvinnhold på 98%, med et renhetsmerke på 980 S. Dette fargede sølvet er litt hardere enn rent sølv og sterlingsølv, og brukes mest til å lage verdibevarende smykker.
(2) 958 sølv.
Det har et sølvinnhold på 95,8%, den andre standardlegeringen for sølvsmykker i 1100-tallets England, kjent som Britannia-sølv. Det har lavere hardhet og egner seg ikke til innfatning av edelstener.
(3) 925 sølv.
Angir et sølvinnhold på 92,5%, kjent som "sterlingsølv", når bare Cu brukes som legeringselement. Dette er den første standardlegeringen for smykkesølv i England på 1100-tallet, som fortsatt er i bruk i dag, med en historie på over 800 år, og som er allment akseptert og brukt over hele verden. Dette sølvet har en viss hardhet og seighet, noe som gjør det egnet til å lage ringer, halskjeder, brosjer, hårnåler og andre smykker, og det egner seg godt til innfatning av edelstener.
(4) 900 sølv.
Sølvinnholdet er 90%, med god styrke og hardhet. Opprinnelig ble det hovedsakelig utviklet for å lage sølvmynter, men det er også kjent som myntsølv og senere brukt til å lage smykker.
(5) 800 sølv.
Angir et sølvinnhold på 80%; dette sølvet har høy hardhet og god elastisitet, noe som gjør det egnet til å lage håndklokker, krageklemmer og andre smykker.
Det finnes sølv med lavere renhetsgrad, for eksempel 700 sølv, 600 sølv og 500 sølv. Det er verdt å merke seg at sølv ikke har like stabile kjemiske egenskaper som gull, spesielt når det utsettes for luft, noe som kan føre til at det anløper og mister glansen. Derfor har sølv alltid hatt lav status i edelmetallsmykker, klassifisert som lavverdige edelmetallsmykker med en lavere verdi enn platina og gull.
Del III Legering av rent sølv og sølv
1. Dekorativt rent sølv
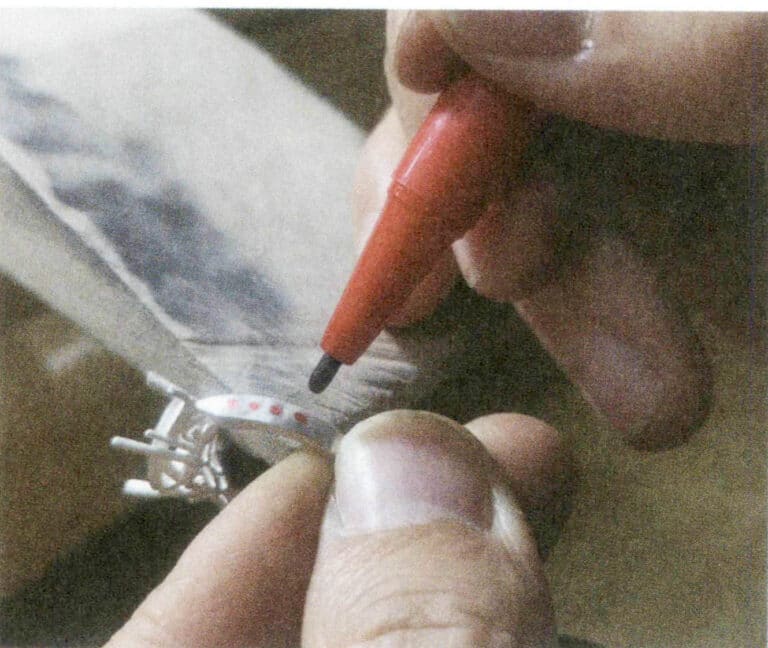
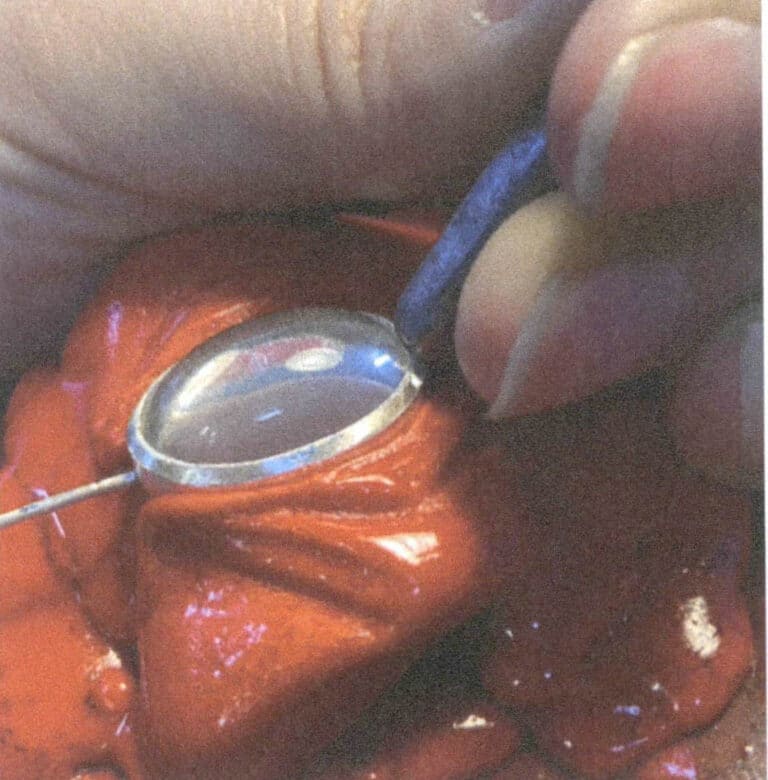
Kulturen med tradisjonelle håndlagde sølvsmykker har en tusenårig historie. Tradisjonelle sølvsmykker bruker hovedsakelig håndverksteknikker som hamring, støping, filigran og gravering, noe som krever myke og lettformede materialer. Materialet er derfor hovedsakelig rent sølv, og formene og mønstrene består hovedsakelig av vinranker, blomster, lykkebringende dyr og lykkebringende tegn. Denne tradisjonelle håndverkskulturen har gått i arv frem til i dag og har fortsatt et visst marked (figur 4-5).

Smykkebedrifter kjøper vanligvis rene sølvkorn eller rene sølvbarrer som råmateriale når de produserer sølvsmykker (Figur 4-6. Figur 4-7).


For å sikre kvaliteten på rene sølvprodukter er det nødvendig å ta utgangspunkt i kilden til råmaterialkvalitetene. Rent sølv er delt inn i tre kvaliteter basert på kjemisk sammensetning: IC-Ag99,99, IC-Ag99,95 og IC-Ag99,90. Bransjestandarden "Silver Granules" (YS/T 856-2012) spesifiserer kravene til spesifikasjonene for sølvgranulat, med en partikkelstørrelse på 1-15 mm, og den kjemiske sammensetningen må oppfylle de internasjonale standardkravene for sølvblokker. Den internasjonale standarden "Silver Ingots" spesifiserer tydelig den kjemiske sammensetningen og urenhetsinnholdet i disse tre klassene av rene sølvblokker, som vist i tabell 4-5.
Tabell 4-5 Krav til den kjemiske sammensetningen av rene sølvbarrer
| Karakter | wt (Ag) (≥)% | Innhold av urenheter (wt≤)/% | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Karakter | wt (Ag) (≥)% | Cu | Pb | Fe | Sb | Se | Te | Bi | Pd | Totalt antall urenheter |
| IC-Ag99.99 | 99.99 | 0.0025 | 0.001 | 0.001 | 0.001 | 0.0005 | 0.0008 | 0.0008 | 0.001 | 0.01 |
| IC-Ag99.95 | 99.95 | 0.0250 | 0.015 | 0.002 | 0.002 | - | - | 0.001 | - | 0.05 |
| IC-Ag99. 90 | 99.90 | 0.0500 | 0.025 | 0.002 | - | - | - | 0.002 | - | 0.10 |
Som nevnt tidligere er styrken og hardheten til tradisjonelle rene sølvsmykker svært lav. Selv med kaldprosessering kan arbeidsherdingsnivået være høyere på grunn av at sølv er et metall med lav stablingsfeilenergi. Dessuten er rent sølv i herdet tilstand utsatt for naturlig aldring, noe som gjør det lett å deformere og slites under daglig bruk. På grunn av den lave styrken er det også uegnet til innfatning av edelstener, noe som gjør det vanskelig å skape design med tredimensjonal effekt. I tillegg er rent sølv utsatt for matthet og misfarging i luften.
For å forbedre manglene ved rent sølvmateriale er det nødvendig å modifisere det ved hjelp av legering eller spesielle prosesseringsteknikker, slik at det modifiserte materialet oppfyller de tilsvarende smykkestandardene samtidig som det har god omfattende ytelse i fysiske, kjemiske, mekaniske og prosesseringsaspekter.
2. Mikrolegert sølv
Industrien har utviklet høyrent sølv som motstår naturlig aldring, mykgjøring og sløvhet ved hjelp av mikrolegeringsmetoder, eller skapt smykker av sølv med høy hardhet og høy renhet ved hjelp av spesielle behandlingsteknikker.
2.1 Mikrolegert sølv
Forskning har vist at tilsetning av sporlegeringselementer til rent sølv kan forbedre styrken og herdehastigheten, undertrykke utvinningsprosessen til en viss grad, heve omkrystalliseringstemperaturen og forbedre legeringens herdeegenskaper og motstand mot naturlig aldringsmykning. Hvis man for eksempel tilsetter spor av sjeldne jordartsmetaller (Y, La, Ce) til rent sølv med en renhet på 99,96% i mengder mindre enn 0,11%, får man en sølvloddelegering som har bedre korrosjonsbestandighet og høyere motstand mot aldringsmykning sammenlignet med rent sølv, noe som gjør den egnet som materiale for sølvsmykker (figur 4-8).
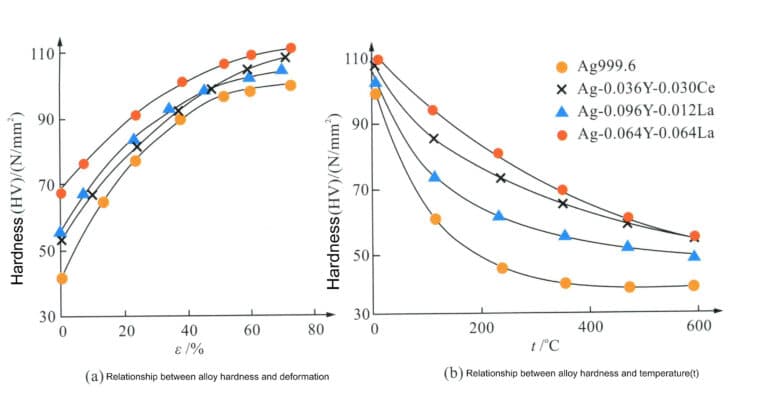
På samme måte resulterer tilsetning av 0,01% Mn til vanlig rent sølv, med en prosesseringshastighet på 97%, i en strekkfasthet på 340 MPa og en hardhet på HV103 for Mn-mikrolegert rent sølv, som kan forbli stabilt i 365 dager ved 25 ℃, mens vanlig rent sølv går tilbake til styrken og hardhetsnivået før deformasjon på mindre enn 30 dager, og styrken og hardheten er i utgangspunktet gjenopprettet til nivået før deformasjon (figur 4-9). Tilsetning av Mn kan effektivt forfine sølvkornet, øke antall korngrenser, forbedre deformasjonsmotstanden og spille en rolle i å styrke og stabilisere mekaniske egenskaper.
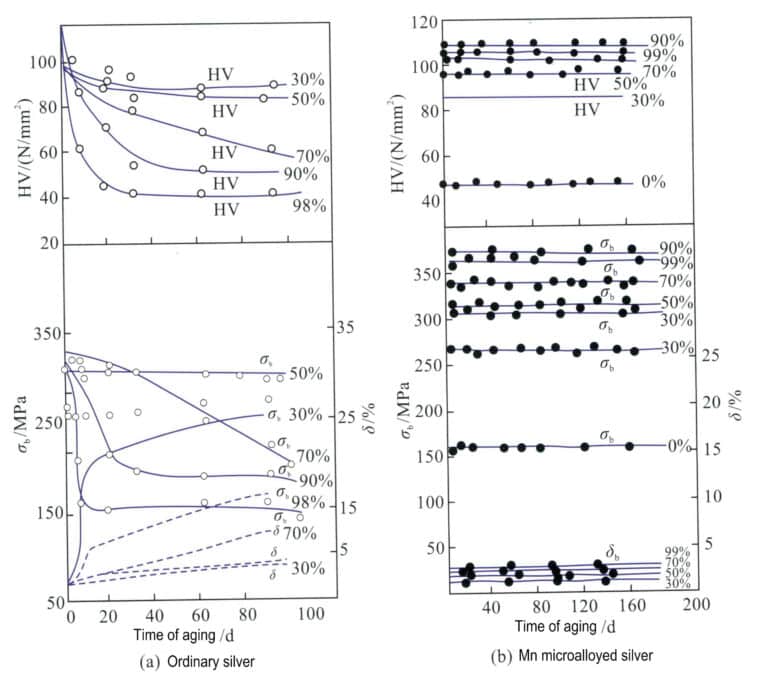
σb. Strekkfasthet; δ. Forlengelse; HV. Mikro Vickers-hardhet; Vanlig rent sølv; Mn mikrolegert rent sølv
2.2 Elektroformet hardt sterlingsølv
Den elektroformede prosessen med hardt 999-sølv er en smykkedannende teknikk basert på prinsippet om elektrokjemisk deponering. Ved å forbedre formuleringen av elektroformingsløsningen og parametere som pH-verdi, arbeidstemperatur, innhold av organisk blekemiddel og omrøringshastighet, forbedres den indre strukturen i sølvet, slik at man oppnår en tett struktur nær nanokrystaller, noe som øker sølvets styrke og hardhet betydelig. Det representerer et gjennombrudd og en innovasjon innen tradisjonelle sterlingsølvsmykker.
Sølvinnholdet i elektroformet hardt 999 sølv er ikke mindre enn 99,9%, og oppfyller kvalitetsstandarden for 999 sølv, men hardheten er mer enn tre ganger så høy som for vanlige 999 sølvsmykker. Det har en hardhet som kan sammenlignes med 925 sølv, noe som forbedrer rene sølvsmykkers deformasjon og slitestyrke betydelig og oppfyller kravene til edelsteninnlegg. På grunn av smykkets hule indre er volumet dessuten fire ganger så stort som for vanlige rene sølvsmykker med samme vekt, noe som gjør det mulig å skape tredimensjonale og levende former. Produktet har en god tredimensjonal effekt og har en kombinasjon av ren sølvkvalitet, 925 sølvs hardhet og tradisjonelle sølvsmykker med 1/3 vekt (figur 4-10).

3. Sølvlegeringssystemer for smykker
Styrkeegenskapene til mikrolegert sølv er i stor grad avhengig av kald deformasjonsherding. Når smykkene utsettes for varme under prosesser som sveising og polering, reduseres imidlertid hardheten raskt, noe som gjør det vanskelig å oppfylle produksjons- og brukskravene. Derfor er den viktigste tilnærmingen i markedet for sølvsmykker å redusere sølvets finhet gjennom legering for å oppnå en sølvlegering med god ytelse, og sølvlegeringer som inneholder 92,5% er de mest brukte. Teoretisk sett kan alle elementer som kan oppløses i sølv, gi en forsterkende effekt, men graden av forsterkning varierer mellom ulike legeringselementer. Dessuten har mange elementer en alvorlig tendens til å segregere ved korngrensene i sølv. Ved mikrolegering for å styrke sølv er mengden som tilsettes svært liten og kan fungere som fordelaktige legeringselementer. Men når innholdet overstiger løselighetsgrensen, kan det føre til at sølvet blir sprøtt. De vanligste legeringselementene for sølvlegeringer inkluderer hovedsakelig Cu, Zn, Pd, Pt, Sn, In, Si, Ge og andre.
3.1 Ag-Cu-legering
Fasediagrammet for den binære legeringen Ag-Cu er vist i figur 4-11. Ag-Cu-legeringen er en eutektisk legering med et kobberinnhold ved et eutektisk punkt på 28,1%, som inntreffer ved 779 °C. Den maksimale løseligheten av kobber i sølv er 8,8%. Innenfor dette området, når kobberinnholdet øker, synker legeringens smeltepunkt helt til det når legeringens eutektiske temperatur. Derfor forbedrer tilsetning av kobber til sølv støpeegenskapene. Etter størkning danner Ag-Cu-legeringen ikke-blandbare sølvrike og kobberrike faste oppløsninger, noe som øker legeringens styrke betydelig. Aldringsbehandling av legeringen i fast form ved lave temperaturer kan gi ytterligere utfellingsforsterkning. Dermed kan kobber gi en merkbar forsterkende effekt i sølv og øke omkrystalliseringstemperaturen.
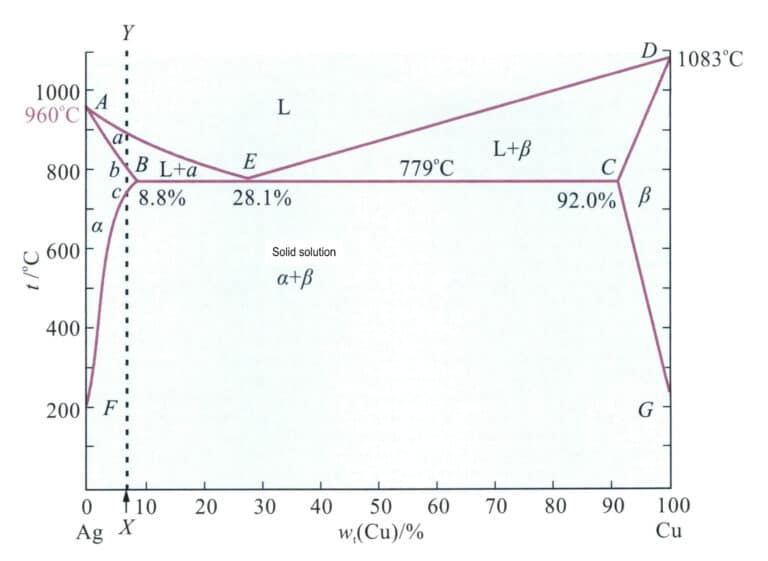
Merk: 960 ℃ representerer smeltepunktet for rent sølv; 1083 ℃ representerer smeltepunktet for rent kobber; 8,8% er den maksimale løseligheten av kobber i sølv; 28,1% er kobberinnholdet ved det eutektiske punktet; 779 ℃ er den eutektiske temperaturen; 92.0% indikerer at den maksimale løseligheten av sølv i kobber er 100%-92,0% = 8,0%; punkt A punkt E representerer liquiduslinjen; a er den sølvbaserte faste løsningen; 0 er den kobberbaserte faste løsningen; G representerer temperaturen der løseligheten av sølv i kobber synker til 0 under likevektsforhold.
De viktigste mekaniske egenskapene til legeringen er vist i tabell 4-6. Etter hvert som Cu-innholdet øker, forbedres Ag-Cu-legeringens styrke og hardhet, mens forlengelsen synker tilsvarende.
Tabell 4-6 viser de viktigste mekaniske egenskapene til Ag-Cu-legeringen.
| Legeringskvalitet | Hardhet HB/(N/mm)2) | Strekkfasthet/MPa | Forlengelse/% | |||
|---|---|---|---|---|---|---|
| Legeringskvalitet | Annea ledet staten | Bearbeidet tilstand | Glødet tilstand | Bearbeidet tilstand | Annea ledet staten | Bearbeidet tilstand |
| 95%Ag-5%Cu | 50 | 119 | 240 | 450 | 43 | 5 |
| 92,5%Ag-7,5%Cu | 57 | 118 | 260 | 470 | 41 | 4 |
| 90%Ag-10%Cu | 64 | 125 | 270 | 450 | 35 | 4 |
| 87,5%Ag-12,5%Cu | 70 | 127 | 260 | - | 38 | 4 |
| 80%Ag-20%Cu | 79 | 134 | 310 | 500 | 35 | 4 |
| 75%Ag-25%Cu | 82 | 135 | 320 | 540 | 33 | 4 |
Etter tilsetning av Cu til sølv har fargen en viss innvirkning. Etter hvert som Cu-innholdet øker, reduseres Ag-Cu-legeringens refleksjonsevne for synlig lys gradvis (Figur 4-12), og fargen på legeringen endres gradvis fra sølvhvit til lys rosa, rosa og til og med rød.
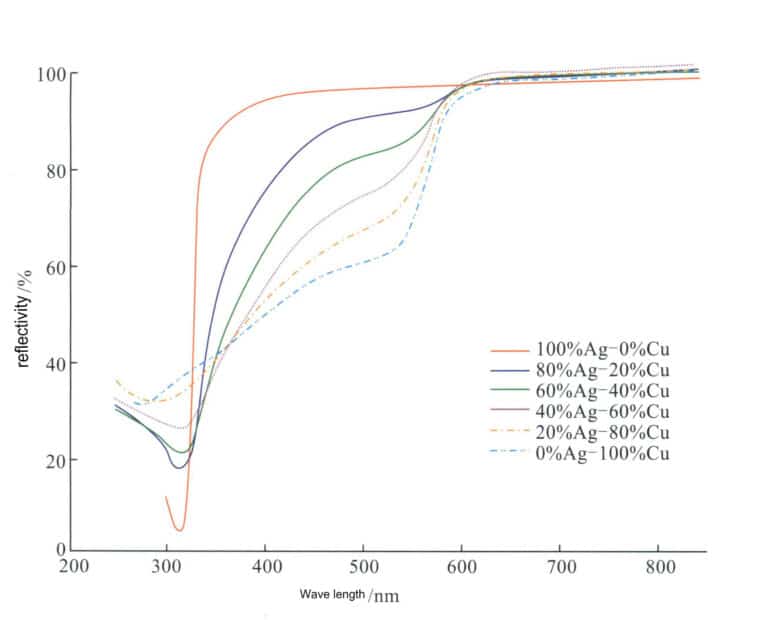
Cu er det mest brukte legeringselementet i Ag, og den tradisjonelle sølvfargen er en binær legering med Cu som legeringselement, med hovedkvaliteter inkludert 980 sølv, 925 sølv, 900 sølv og 800 sølv. Sølvlegeringene i det nåværende markedet er også i utgangspunktet basert på Ag-Cu-legeringen som basislegering. Selv om kobber kan forbedre sølvets styrke, hardhet og støpeegenskaper, forbedrer det ikke sølvets motstand mot mørkfarging og misfarging. På grunn av legeringens tofasestruktur oppstår det dessuten en korrosjonsmikrobatterieffekt i korrosive miljøer, noe som gjør korrosjonsbestandigheten dårligere enn for en enfaset sølvoppløsning i fast form.
3.2 Ag-Pd-legering
Forskning viser at tilsetning av en viss mengde edle metaller til sølv effektivt forbedrer sølvets motstandskraft mot mørkfarging og misfarging. Pd er det foretrukne edelmetallelementet i sølv, og figur 4-13 viser fasediagrammet for den binære legeringen Ag-Pd.
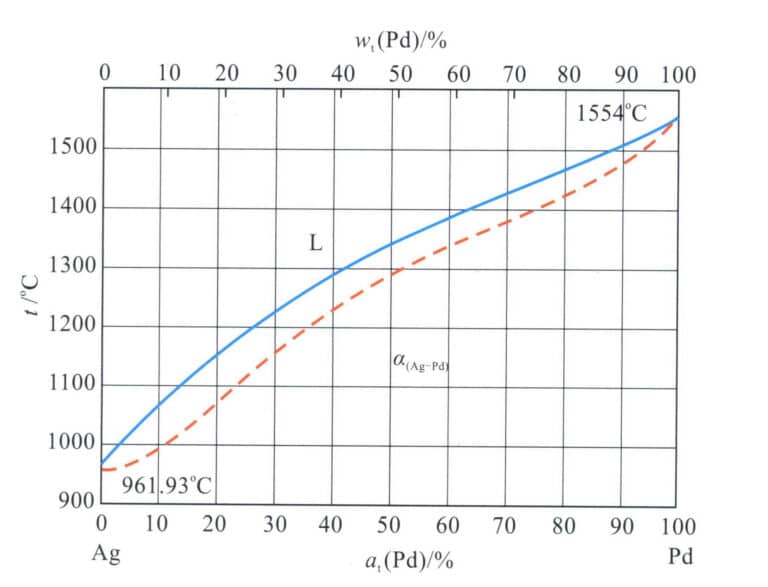
Legeringen er uendelig løselig i flytende og faste faser, og danner en kontinuerlig fast løsning. Derfor er den forsterkende effekten av palladium på sølv generelt beskjeden, som vist i tabell 4-7. Kald deformasjon kan forbedre legeringens styrke og hardhet til en viss grad. Den kan likevel ikke fullt ut oppfylle styrkekravene til innebygde smykker, noe som gjør det nødvendig å tilsette andre legeringselementer for ytterligere forsterkning.
Tabell 4-7 De viktigste egenskapene til den glødede legeringen
| Legeringskvalitet | Smeltetemperatur /℃ | Tetthet /(g/cm3) | Hardhet HV/(N/mm2) | Strekkfasthet /MPa | Varmeledningsevne /[W/(cm⸳K)] |
|---|---|---|---|---|---|
| 95%Ag - 5%Pd | 980 ~ 1020 | 10.5 | 28 | 170 | 2.20 |
| 90%Ag - 10%Pd | 1000 ~ 1060 | 10.6 | 35 | 210 | 1.42 |
| 80%Ag - 20%Pd | 1070 ~ 1150 | 10.7 | 45 | 260 | 0.92 |
Palladium forbedrer effektivt sølvets motstandskraft mot anløping på grunn av sulfid. Når palladiuminnholdet øker, reduseres tendensen til at sølvet anløper og misfarges på grunn av sulfid betydelig. Legeringens smeltepunkt øker imidlertid, krystalliseringsintervallet utvides også, og palladium er utsatt for gassabsorpsjon under smelting, noe som øker vanskeligheten med smelting og støping, noe som krever smelting under vakuum eller inert gassbeskyttelse.
På grunn av den kontinuerlige økningen i prisen på palladium, øker tilsetning av palladium kostnadene for sølvlegeringer betydelig. Derfor har bruken av palladium i sølv gått kraftig ned de siste årene, og eksisterende bruksområder er hovedsakelig basert på små tilsetninger.
Copywrite @ Sobling.jewelry - Tilpasset smykkeprodusent, OEM og ODM smykkefabrikk
Del IV Sterlingsølv og modifikasjoner av dette
Sterling stammer fra navnet til en tysk myntprodusent, Easterlings, på 1100-tallet. Han tok med seg avanserte teknikker for fremstilling av sølvmynter og sølvlegeringer til England under Henrik II, og skapte en sølvlegering som besto av 92,5%Ag og 7,5%Cu. Denne legeringen ble mye brukt og ble det første merket av sølvlegering i 1100-tallets England. Til ære for denne myntmakeren fikk legeringen navnet sterlingsølv. Til å begynne med refererte sterlingsølv spesifikt til legeringen 92,5%Ag-7,5%Cu, men senere ble legeringen utvidet til å bli en generell betegnelse for alt 925-sølv. Siden 1100-tallet har sterlingsølv vært mye brukt i sølvtøy og sølvsmykker, og det har gjennomgående fungert som en standardlegering, og er den eldste dekorative sølvlegeringen i historien.
1. Kjennetegn ved sterlingsølv
1.1 Mekaniske egenskaper
I henhold til figur 4-11 tilsvarer sammensetningen av sterlingsølvregeringen den stiplede linjen XY, og skjæringspunktene med fasegrensen er A, B, C. Området fra punkt B til punkt C er en enkelt fast løsning, og etter langsom avkjøling under punkt C vil en kobberrik fast oppløsningsfase utfelle fra den faste løsningen. Oppvarming av sterlingsølv til 800 °C for behandling av fast oppløsning gir en enkelt fast oppløsning, noe som kan gi legeringen utmerket duktilitet og bearbeidbarhet. Tabell 4-6 viser at styrken og hardheten til fast oppløsning i sterlingsølv er betydelig høyere enn for rent sølv. Kaldbearbeiding av sterlingsølv i fast oppløsning kan oppnå en god arbeidsherdende effekt (figur 4-14).
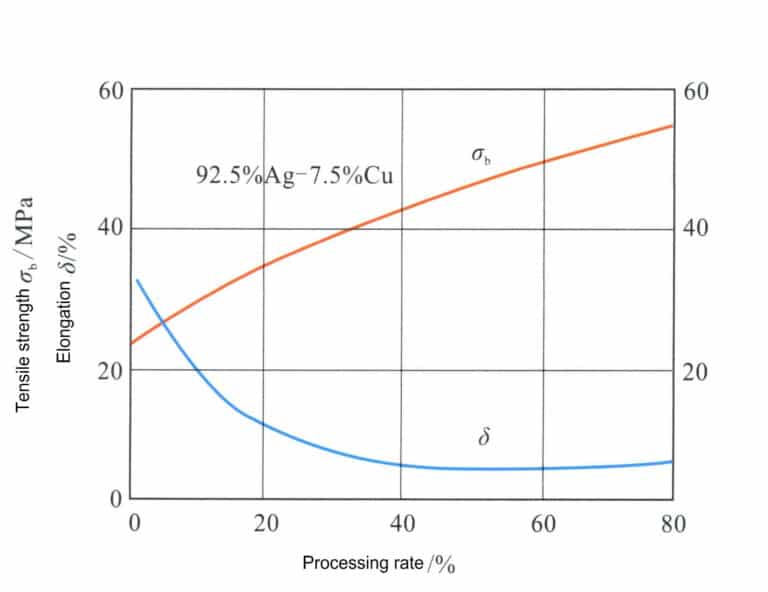
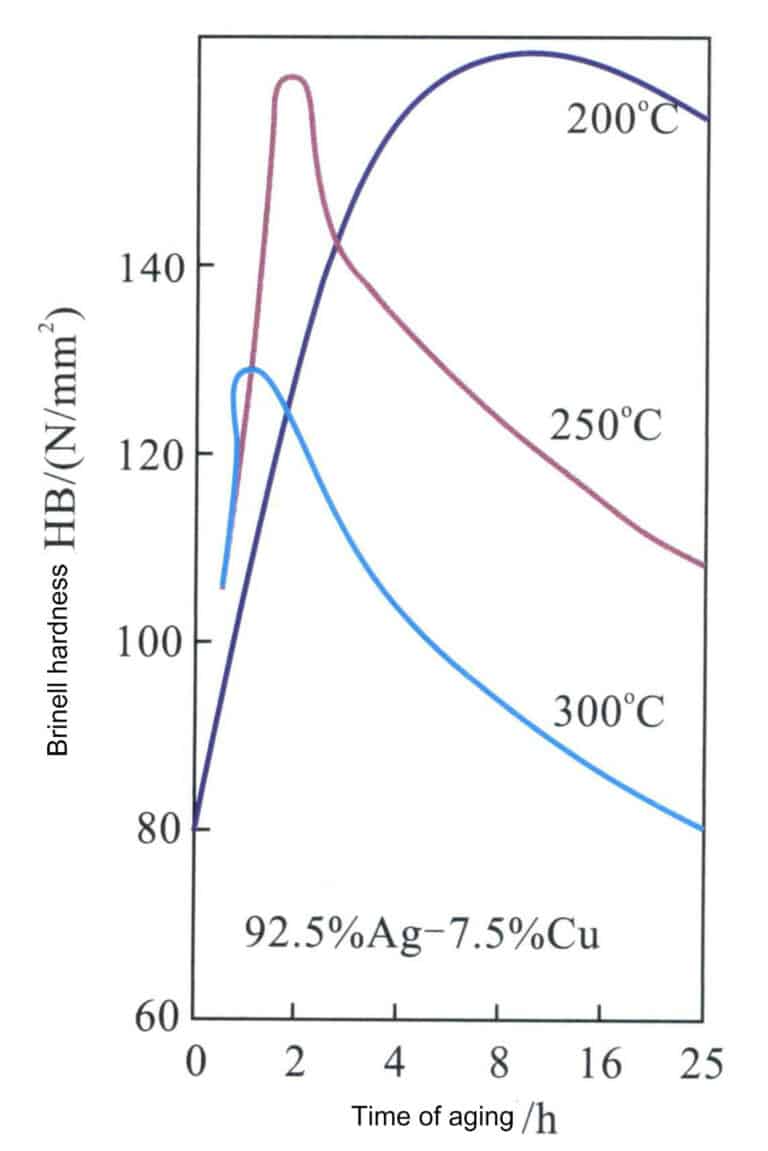
Et fremtredende trekk ved sterlingsølvregering er dens utmerkede aldersherdende egenskaper, som kan endres gjennom aldringsbehandling (figur 4-15). Den faste løsningen av sterlingsølv gjennomgår aldringsbehandling ved 200-300 ℃, og når aldringstemperaturen er 200 ℃, er den høyeste oppnådde hardheten nær HV160, sammenlignbar med den for 18K gulllegering; det kreves imidlertid en lengre aldringstid for å nå denne toppverdien. Når aldringstemperaturen øker, forkortes tiden for å oppnå topp hardhet kraftig, men topphardheten synker også tilsvarende. Når aldringstemperaturen når 300 ℃, har effekten av aldersherding blitt betydelig redusert.
1.2 Kjennetegn ved støping
Likvidustemperaturen til sterlingsølv er 898 °C, og legeringen har et lavt smeltepunkt, noe som gjør den egnet for smelting i en grafittdigel.
Sterlingsølv absorberer imidlertid store mengder oksygen i smeltet tilstand, noe som skaper problemer ved smelting og støping. Denne egenskapen gjør legeringen utsatt for fordampning ved høye temperaturer eller forårsaker betydelige tap under avkjølingsprosessen ved høy temperatur på grunn av sprut. Hvis sterlingsølv ikke beskyttes under smeltingen, og det ikke brukes tilstrekkelige deoksideringsmidler, kan oksygen lett akkumuleres, noe som fører til oksidasjon av kobber, og smykkestøpegods er utsatt for defekter som porøsitet og oksiderte inneslutninger. Det oksiderte kobberet i støpegodset kan forårsake to typer problemer: (1) hele støpegodset kan ha oksiderte kobberinneslutninger, som danner harde flekker når inneslutningene er nær overflaten og stikker ut på den polerte overflaten; (2) oksiderte kobberinneslutninger nær krympekaviteter vises som flekkete, uklare flekker på den polerte overflaten, som er dype og vanskelige å rense av. Anta at sterlingsølvsmelten er sterkt overopphetet eller ikke beskyttet i lang tid. I så fall vil kobberet oksidere kraftig og danne en tyktflytende væskeoverflate, noe som reduserer smeltens flyteevne og fører til ufullstendig fylling i noen små områder av støpeobjektet, og ofte resulterer i underfylling. Overflaten nær støpeområdet ser rød ut. I tillegg er krystalliseringsintervallet for sterlingsølv relativt stort og når 90 ℃, med betydelige forskjeller mellom de flytende og faste fasekomponentene, med en tendens til pastalignende størkning, med alvorlig dendritisk vekst, samtidig som det har lavere flytbarhet, noe som fører til en større tendens til krympeporøsitet.
For å unngå akkumulering av oksygen i sterlingsølvsmelten er det avgjørende å unngå kontakt mellom det smeltede metallet og atmosfæren så mye som mulig under smelte- eller støpeprosessen. Derfor bør følgende punkter noteres.
(1) Under smelting av elektrisk ovn brukes vakuumbeskyttelse, eller inerte gasser som argon eller nitrogen brukes til beskyttelse, noe som kan eliminere oksygen i smeltekammeret og redusere oksidasjonen av det smeltede metallet.
(2) Når du bruker en brannpistol til smelting, bør flammen justeres til en reduserende gul flamme som dekker hele væskeoverflaten for å forhindre at det smeltede metallet absorberer oksygen. Ved smelting i elektrisk smelteovn kan det noen ganger legges til en reduserende flamme ved munningen av smeltedigelen for å dekke det smeltede metallet.
(3) Dryss trekull eller vannfri borsyre på overflaten av det smeltede metallet; de flyter på overflaten av sølvvæsken og kan beskytte sølvvæsken på to måter: a. ved å danne en barriere mellom det smeltede metallet og luften; b. ved å redusere kobberoksid. Denne metoden er uegnet for sentrifugalstøpemaskiner, men fungerer svært godt på manuelt betjente vakuumstøpemaskiner.
(4) I metoden ovenfor er det også viktig å styrke beskyttelsen av det smeltede metallet under helleprosessen. Spesielt når du bruker en vakuumstøpemaskin for å helle, siden det er en manuell helling under vakuumforhold, er det nødvendig å beskytte strømmen av smeltet metall. Vanligvis brukes en reduserende flamme; når gipsformen plasseres, antennes flammen, og flammen må dekke hellingsporten til formen, noe som kan eliminere luften inne i formen.
1.3 Polering av fenomenet "rød flekk"
Sterlingsølv danner ofte mørkerøde flekker på overflaten under polering, noe som påvirker lysstyrken og estetikken til den polerte overflaten, samt vedheftingen av det galvaniserte laget. Dette fenomenet er mer uttalt på overflatene til produkter som har gjennomgått termisk behandling, for eksempel gløding og sveising.
Etter å ha varmet opp sterlingsølvblokken ved 700 °C i 1,5 timer, ble oksidasjonstilstanden observert i mikroskop, noe som avslørte at legeringen ikke bare dannet et oksidlag på overflaten, men også utviklet en indre oksidasjonssone under overflaten (figur 4-16).

Sterlingsølv tilhører Ag-Cu-legeringen. Når legeringen kommer i kontakt med oksygen i luften ved høye temperaturer, skjer selektiv oksidasjon av Cu først etter at temperaturen overstiger 400 K. Når prøven senkes ned i fortynnet svovelsyre, kan overflatelaget av kobberoksid fjernes. Derfor, etter at prøven er lett polert, kan den presentere en sølvhvit farge. Etter ytterligere polering dukker det imidlertid opp mørkerøde flekker på den polerte overflaten, noe som ødelegger refleksjonsegenskapene til den polerte sølvoverflaten (Figur 4-17), noe som indikerer at det fortsatt finnes oksidasjonsprodukter av Cu i dette området.

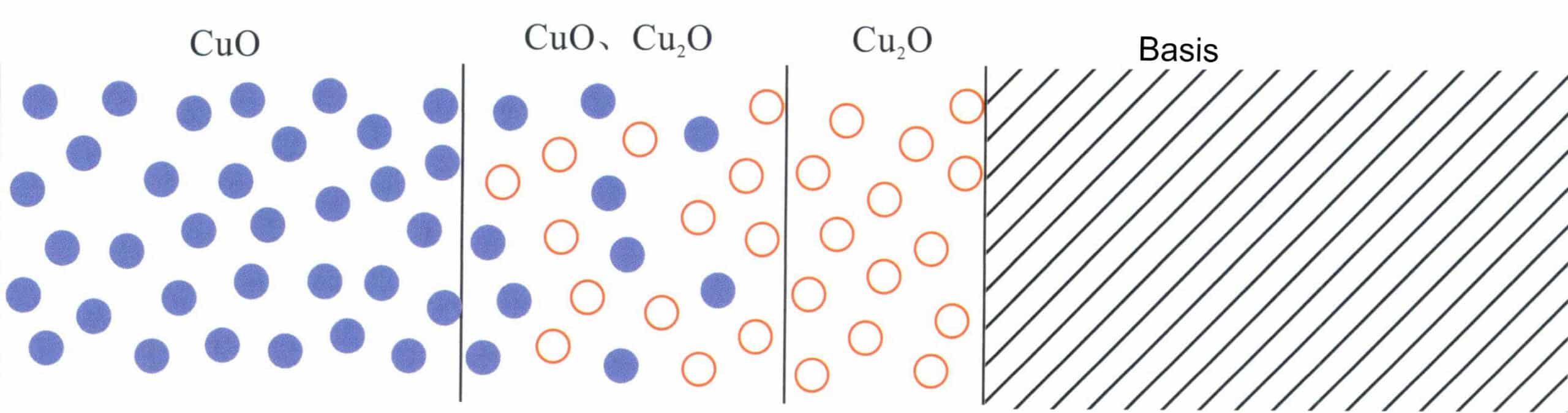
Når kobber kommer i kontakt med oksygen i luften ved høye temperaturer, for eksempel under varmvalsing, gløding eller sveising, oksiderer overflaten på kobberemnet først og danner rød Cu2O og oksiderer deretter videre til svart CuO. Oksidasjonen av kobber er ikke begrenset til overflaten av sølvlegeringer, men kan trenge ned til en viss dybde (figur 4-18). I henhold til teorien om legeringers oksidasjonskinetikk ved høy temperatur, når to diffunderer samtidig med Cu, må det være en akkumulering av Cu2O-utfellingsfasen i den indre oksidasjonssonen, og legeringen som ikke har gjennomgått indre oksidasjon ved den indre oksidasjonsfronten, vil vise uttømming av Cu. Ag har en sterk evne til å absorbere oksygen og transportere oksygen til det indre av metallet ved høye temperaturer. Derfor er oksygendiffusjon dominerende, og permeabiliteten er mye høyere enn for Cu. Oksygen kan derfor trenge inn i legeringsoverflatens underlag og danne interne oksidutfellinger. Det må finnes en direkte vei fra oksidet til legeringsoverflaten for å fjerne underlagets kobberoksid gjennom syreetsing. Kobberinnholdet i sterlingsølv er bare 7,5%, og strukturen er en fast tofaseløsning uten dannelse av et oksidnettverk, noe som betyr at det ikke er noen direkte vei inn i det indre under nedsenking i syre, slik at det indre Cu2O for å forbli intakt. Resultatet er at overflaten på den oksiderte sterlingsølvprøven fortsatt har svarte og uregelmessige flekker, såkalte "røde flekker".
Forskning har vist at alvorlighetsgraden av de røde flekkene på overflaten av sterlingsølv er nært knyttet til oppvarmingstemperaturen og oppvarmingstiden (figur 4-19). Jo høyere oppvarmingstemperatur og jo lengre oppvarmingstid, desto tykkere blir oksidfilmen på overflaten, og desto dypere trenger det indre oksidlaget inn i underlaget, noe som gjør det vanskelig å fjerne med konvensjonelle poleringsmetoder.

1.4 Fenomenet mørkere fargeendring
Sølv i seg selv er utsatt for mørkfarging og misfarging. Tilsetning av Cu-elementer i sterlingsølv forbedrer ikke legeringens tendens til misfarging. Sterlingsølvslegeringen har dessuten en tofasestruktur i både støpt og eldre tilstand, bestående av en sølvrik fast oppløsning og en kobberrik fast oppløsning, som er to inkompatible faser. Potensialforskjellen mellom disse to fasene danner lokale mikrobatterireaksjoner, noe som øker den elektrokjemiske korrosjonsytelsen til sterlingsølvslegeringen og reduserer korrosjonsbestandigheten. Derfor er sterlingsølvsmykker utsatt for korrosjon og misfarging, noe som påvirker sølvsmykkernes utseendekvalitet alvorlig.
2. Legeringselementenes innflytelse på sterlingsølv
Sterlingsølv har en tendens til å utvikle røde flekker ved polering og matt misfarging, og er dessuten utsatt for metallurgiske og støpemessige feil under smelting, noe som gjør det nødvendig med modifikasjonsbehandling. Dette innebærer legering for å forbedre den generelle ytelsen samtidig som de gode mekaniske egenskapene opprettholdes. Vanlige legeringselementer inkluderer Si, Zn, Sn, Ce, Ge og andre.
2.1 Silisium(Si)s påvirkning på sterlingsølv
Tradisjonelle sterlingsølvslegeringer har en tendens til å absorbere gass under smelting og støping, noe som gjør dem utsatt for oksidasjon og resulterer i større gassporer i støpegodset. Øverst er det gassutløpskanaler på grunn av absorpsjon av størkningsgass, ledsaget av oksiderte inneslutninger, og det finnes også inneslutninger i støpegodset. Ved å tilsette en liten mengde silisium til sterlingsølv kan man effektivt forbedre gassabsorpsjonstendensen og oksidasjonsmotstanden, noe som resulterer i bedre støpekvalitet, reduserte defekter av gassporer og inneslutninger og forbedret overflatekvalitet etter polering. Fra et termodynamisk perspektiv er Gibbs frie energiverdi for silisiumdannende oksider høyere enn for kobberoksider. Etter tilsetning av en passende mengde silisium reagerer derfor silisiumet i det smeltede metallet fortrinnsvis med oksygen, noe som reduserer gassporefeilene. På grunn av silisiumdioksydets lave tetthet og høye viskositet kan det fjernes fra overflaten av det smeltede metallet ved hjelp av flussmiddel når det flyter opp til overflaten. Silisiumet som tilsettes sterlingsølv, bidrar også til å forbedre legeringens motstandskraft mot oksidasjon og sulfidmisfarging.
Etter hvert som Si-innholdet øker, blir kornstrukturen gradvis grovere, noe som forverrer overflatepoleringseffekten og fører til en "appelsinskall"-effekt på overflaten. Når silisiuminnholdet overstiger en viss verdi, øker legeringens sprøhet betydelig, noe som gjør den utsatt for sprekkdannelser under bearbeiding.
2.2 Påvirkning av sink (Zn) på sterlingsølv
Zn kan senke smeltepunktet for sterlingsølv, øke smeltens flytbarhet, redusere krympedefekter og gjøre støpestrukturen tettere, men det har ingen betydelig effekt på kornstørrelsen. Som et oksygenaktivt element reagerer Zn, når det tilsettes sterlingsølv, fortrinnsvis med oksygen i det smeltede metallet, noe som kan bidra til å redusere oksidasjonen av det smeltede metallet på grunn av absorbert oksygen. Men når sinkinnholdet er for høyt, kan det lett øke mengden oksiderte inneslutninger i det smeltede metallet.
Forskjellen i atomstørrelse mellom Zn og Ag er 7,76%, Cu, og forskjellen i atomstørrelse med Ag er 11,50%, Zn. Den forsterkende effekten av Ag er mindre sterk enn den av Cu. Når Zn delvis erstatter Cu i sterlingsølv, reduseres støpe- og glødet hardhet. Når Zn-innholdet overstiger 3,36%, er støpehardheten til sterlingsølv bare rundt HV50, noe som gjør det vanskelig å oppfylle kravene til smykkeinnlegg og krav til slitestyrke. Zn har en negativ effekt på legeringens prosesseringsytelse, og reduserer plastisiteten. For høyt Zn-innhold vil føre til problemer som delaminering, avskalling og sprekkdannelser under bearbeiding.
Elektrodepotensialet til Zn er lavere enn Ag og Cu, og det vil spontant dannes en passiveringsfilm på Sterling Silver-overflaten, noe som bremser elektrokjemisk korrosjon og forbedrer legeringens motstandskraft mot sulfidmisfarging og oksidasjon. Etter hvert som Zn-innholdet øker, øker også sterlingsølvet. Tykkelsen på oksidfilmen reduseres gradvis. Likevel, når Zn-innholdet overstiger 3,5%, er Sterling sølv mer utsatt for oksidasjonsinneslutninger, noe som er skadelig for dets elektrokjemiske korrosjonsbestandighet og anti-sulfid misfarging ytelse.
2.3 Effekten av Stannum (Sn) på sterlingsølv
Ved å tilsette Sn til sterlingsølv kan man senke legeringens smeltepunkt, øke smeltens flytbarhet og redusere legeringens krymping, noe som resulterer i en tettere støpestruktur. En liten mengde Sn kan også forfine legeringens struktur, men når Sn-innholdet overstiger 2%, blir legeringens struktur merkbart grovere, og det dannes relativt store dendritter som krymper og segregeres.
I sterlingsølvslegeringer forbedrer delvis erstatning av Cu med Sn generelt legeringens opprinnelige hardhet i støpt tilstand. Etter hvert som Sn-innholdet øker, stiger legeringens hardhet først og synker deretter. Når Sn-innholdet nærmer seg 1%, når hardheten sin maksimale verdi, men legeringens duktilitet påvirkes betydelig, noe som kan føre til sprekkdannelse under kaldbearbeiding.
Sn er også et oksygenaktivt grunnstoff. En viss mengde Sn kan danne en tett oksidfilm på legeringens overflate og beskytte underlaget. Sn kan forbedre den elektrokjemiske korrosjonsbestandigheten til sterlingsølv. Etter hvert som Sn-innholdet øker, forbedres legeringens elektrokjemiske korrosjonsbestandighet. Når Sn-innholdet overstiger 2%, forbedres legeringens sulfidmisfarging og oksidasjonsmotstand betydelig.
2.4 Påvirkningen av Cerium (Ce) på sterlingsølv
Tilsetningen av det sjeldne jordartsmetallet Ce til sterlingsølv har en betydelig innvirkning på sølvets struktur. Ce kan effektivt rense metallvæsken og redusere gassinnholdet. Når Ce-innholdet er under 0,05%, kan det foredle kornstrukturen, hovedsakelig fordi Ce fungerer som en kornforedler under størkningsprosessen av metallvæsken, noe som reduserer graden av krympeporøsitet og forbedrer tettheten under gløding; Ce kan også hindre migrering av korngrenser og dermed opprettholde en fin kornstruktur.
Spormengder av Ce kan forbedre de mekaniske egenskapene til sterlingsølv, øke styrken og hardheten, forbedre duktiliteten og forbedre legeringens arbeidsherdende effekt. Når Ce-innholdet økes ytterligere, er det en tendens til segregering ved korngrensene, noe som forverrer legeringens bearbeidingsytelse og gjør den mer utsatt for oksidasjonsinneslutninger.
Etter tilsetning av spormengder av Ce kan den elektrokjemiske korrosjonsbestandigheten, oksidasjonsflekkmotstanden og sulfidmisfargingsmotstanden til sterlingsølv forbedres kraftig. Når Ce-innholdet overstiger 0,075%, vil korrosjonsbestandigheten til sterlingsølv avta.
2.5 Ge-virkningen på sterlingsølv
Når Ge tilsettes sterlingsølv, og innholdet er mellom 0,2% og 0,8%, er støpehardheten til sterlingsølv høyere, og arbeidsherdingsytelsen, elektrokjemisk korrosjonsbestandighet og misfargingsmotstand er alle forbedret sammenlignet med sterlingsølv, noe som gjenspeiler bedre totalytelse. Når Ge-innholdet er for lavt, er ytelsesforbedringen av sterlingsølv ikke signifikant; men når innholdet er for høyt, kan det lett føre til grovkorning av legeringen, noe som fører til en nedgang i legeringens generelle ytelse.
Del V Misfarging og beskyttelse av sølv
Sølv og dets legeringsmaterialer er mye brukt i smykkeindustrien, og de har en betydelig egenskap: de gjennomgår lett anløp og misfarging. Etter at sølvlegeringer misfarges, reduseres overflateglansen sterkt, noe som påvirker smykkekvaliteten på smykkene og øker vanskeligheten med legeringsbehandlingen.
1. Årsaken til at sølv anløper
Det kjemiske potensialet til rent sølv er +0,799 V, noe som er relativt høyt sammenlignet med standardpotensialet til hydrogen, noe som klassifiserer det som et inert metall. Under normale forhold reagerer det ikke kjemisk med syrer eller baser, og reagerer bare med sterke oksiderende konsentrerte syrer (som konsentrert salpetersyre og varm konsentrert svovelsyre). Sølvsmykker vil imidlertid gradvis anløpe etter å ha blitt brukt en stund eller til og med når de legges i en oppbevaringsboks i en viss tid, og tradisjonelt sterlingsølv er spesielt utsatt for anløping. Årsakene til at sølv anløper kan oppsummeres som følger.
1.1 Misfarging av sølvsulfid
Sølv og sølvlegeringer er utsatt for korrosjon og misfarging i miljøer som inneholder H2S, SO2og COS. Sølv er svært følsomt for H2S-gass, og når konsentrasjonen av H2S i atmosfæren når 0,2 x 10-9 (volumfraksjon), er det tilstrekkelig til å korrodere sølv, noe som resulterer i dannelsen av svart Ag2S, nemlig:
4Ag + 2 H2S + O2 = 2Ag2S + 2H2O
Hastigheten av sølvsulfid misfarging i en atmosfære av H2S følger Wagners diffusjonskinetiske mekanisme, og når innholdet av H2S øker eller når H2S sameksisterer med andre gasser som NO2, O2øker misfargingen av sølvsulfid. SO2 i luften kan også omdannes til S2-for å danne Ag2S, noe som forårsaker misfarging av sølv. Følsomheten for SO2 er ikke like høy som for H2S, men når SO2 sameksisterer med andre gasser som NO2 og O2vil også hastigheten på sulfidmisfargingen intensiveres.
Sølv er svært følsomt overfor oksygenholdige sulfidløsninger. Misfargingen skjer langsomt når sølvet senkes ned i en oksygenfri Na2S-løsning. Men hvis prøven tas ut og natriumsulfidløsningen som er festet til sølvoverflaten, kommer i kontakt med oksygen, vil sølvprøven raskt vise tydelig misfarging. Jo lenger den eksponeres for luft, desto mer alvorlig blir misfargingen. Rekkefølgen på fargeforandringene er sølv, hvitt → gult → brunt → blått. Dette skyldes at standard elektrodepotensialet til Ag (0,779 V) er lavere enn O (1,229 V). Ag er termodynamisk ustabilt når oksygen er til stede, først ved O2 blir oksidert til Ag+ og deretter kombinere med Ag+ og S2-for å danne en uløselig forbindelse Ag2S. Jo høyere konsentrasjonen av sulfider er, desto mer alvorlig blir misfargingen. Den kjemiske reaksjonen av sølv i oksygenholdig Na2S vandig løsning er:
4Ag + 2H2O + O2 + 2S2-= 2Ag2S↓+4OH–
Ag-Cu-legeringer er mer utsatt for sulfiddannelse og produserer svart Cu2 S fordi Cu lettere sulfiderer enn Ag; dermed misfarges de lettere enn rent sølv.
1.2 Elektrokjemisk korrosjon i fuktige miljøer
I fuktige omgivelser kan ujevnheter i sølvoverflaten (ujevn legeringssammensetning eller fysiske forhold som indre spenninger, glatt overflate osv.) føre til forskjellige potensialer i ulike områder av metalloverflaten under vannfilmen, noe som skaper en potensialforskjell mellom disse områdene. To tilstøtende områder med ulike potensialer kobles sammen, og vannfilmen fungerer som en elektrolytt for transport av ioner, mens metallet fungerer som en leder for transport av elektroner, slik at det dannes en elektrisk syklus. Dette skaper effekten av et kortslutningsbatteri, og det dannes mange mikrobatterier av korrosjon på metalloverflaten. Den støpte strukturen i sterlingsølv består vanligvis av en tofasestruktur som består av en sølvrik fast løsning og en kobberrik fast løsning. I fuktige omgivelser blir den kobberrike faste oppløsningsfasen anoden i korrosjonsmikrobatteriet, noe som gjør legeringen mer utsatt for korrosjon og misfarging. Sølv av høyere kvalitet kan også gjennomgå elektrokjemisk korrosjon på grunn av urenheter, og i fuktige miljøer som inneholder salt, omdannes sølvoverflaten ofte til sølvklorid, et gråbrunt, klebende stoff som ligner jord.
1.3 Effekten av ultrafiolett lys på misfarging av sølv
Lys, som en ekstern energikilde, kan fremme ioniseringen av metallioner, og dermed akselerere reaksjonen mellom sølv og det korrosive mediet, det vil si akselerere misfargingsreaksjonen av sølv. Når overflaten av det forsølvede laget bestråles med lys med forskjellige bølgelengder, vises resultatene i tabell 4-8. Det kan sees at det sølvbelagte laget er utsatt for misfarging etter å ha absorbert ultrafiolett lys, og evnen til den bestrålte lysbølgelengden til å forårsake misfarging øker når bølgelengden avtar.
Tabell 4-8 Effekten av bestrålt lysbølgelengde og bestrålingstid på misfargingen av det sølvbelagte laget
| Bestrålt lys bølgelengde/nm | Bestrålingstid / timer | ||||
|---|---|---|---|---|---|
| Bestrålt lys bølgelengde/nm | 6 | 12 | 18 | 24 | 48 |
| 253.7 | Uendret | Fokal makula | Gulbrun | Brun-svart | Helt i svart |
| 365.0 | Uendret | Uendret | Uendret | Gul | - |
| Sollys | Uendret | Uendret | Uendret | Lokalisert makula | - |
I henhold til resultatene av røntgenfotoelektronspektroskopi og Auger-spektroskopianalyse består fargeforandringen i det sølvbelagte laget under ultrafiolett lys hovedsakelig av Ag2O, AgO, AgCl og tilsvarende sølvforbindelser.
2. Måter å forebygge misfarging av sølv på
Når det gjelder misfarging av sølv og sølvlegeringer, har det blitt forsket mye både nasjonalt og internasjonalt på hvordan man kan forbedre sølvets misfargingsmotstand. Når det gjelder å fremme misfargingsmotstand, kan forskningen oppsummeres i to hovedkategorier: overflatebehandling av sølvlegeringer og utvikling av misfargingsresistente sølvlegeringer.
2.1 Overflatemodifiseringsteknologi for å forhindre misfarging av sølv
Overflatemodifisering innebærer bruk av kjemiske eller fysiske metoder for å danne en inert film på overflaten av sølvsmykker, isolere sølvsubstratet fra korrosive medier i omgivelsene, blokkere reaksjonene mellom lys, oksidanter, korrosive medier og sølv, og forhindre misfarging. Avhengig av hvilken type film som dannes, kan overflatemodifisering kategoriseres i flere hovedtyper: elektroplettering, nedsenking, kjemisk passivering, elektrokjemisk passivering, organisk adsorpsjonspassivering, harpiksbelegg og selvmonterte filmer.
Rhodiumplettering er den mest brukte overflatemodifiseringsmetoden for sterlingsølvsmykker. Ved å belegge en tynn film av rhodium på overflaten av smykkene, kan et lyst, speillignende utseende oppnås, og rhodiumlaget har høy hardhet og god kjemisk stabilitet, noe som kan forbedre slitestyrken og misfargingsmotstanden til sølvsmykker. På grunn av produksjonskostnadene og overflatens lysstyrkeeffekt er rhodiumlaget på smykker vanligvis veldig tynt og kan lett slites av under bruk, og mister sin beskyttende effekt.
Kjemisk passivering eller elektrokjemisk passivering kan danne en uorganisk passiveringsfilm på overflaten av sølv. Kromatpassivering er en vanlig kjemisk passiveringsmetode for sølvsmykker, som genererer et lag av sølvoksid og sølvkromat i en sur eller alkalisk oppløsning som inneholder seksverdige kromforbindelser. Elektrokjemisk passivering utnytter prinsippet om katodisk reduksjon til å generere et filmlag bestående av sølvkromat, kromsyre, basisk sølvkromat og basisk kromsyre på overflaten av sølv. Disse filmlagene har gode passiveringseffekter, kan redusere den frie energien i legeringsoverflaten og forhindre misfarging uten å ha noen vesentlig innvirkning på utseendet til sølvhåndverket. Problemene er imidlertid at filmlaget må være mindre tett, har dårlig mekanisk stabilitet, kompleks struktur, vanskeligheter med å dekke kanter og miljøpåvirkning.
Ved å bruke metoder som nedsenking, sprøyting og belegg for å danne en organisk beskyttende film på sølvoverflaten kan man forbedre sølvets antiflakk-egenskaper, og det er gjort mye forskning på dette området både nasjonalt og internasjonalt. Benzotriazol, tetrazolium og ulike svovelholdige forbindelser kan danne komplekser på sølv. Det kan dannes komposittfilmer, og noen vannløselige polymerer tilsettes for å lage filmmidler, men det resulterende filmlaget må være tettere, og anti-tarniseffekten kan være bedre. Noen beskyttelsesmidler er oljeløselige antiflakkmidler basert på parafin og langkjedede kvartære ammoniumsalter, som kan danne et fast smørende lag på overflaten av sølv, noe som gir en god antiflakkeeffekt. De har imidlertid dårlig motstand mot løsningskorrosjon, og bruk av varm bensin som løsemiddel utgjør en betydelig risiko. I tillegg, etter å ha belagt et lag voks på overflaten, vil legeringens lysstyrke og refleksjonsevne reduseres kraftig. Sprøyting av akryllakk, polyuretanlakk og organisk silikonlakk på overflaten av sølvlegeringer kan forbedre anti-tarnish-evnen. Likevel må belegget også ha tilstrekkelig tykkelse til å gi en viss antiflammende effekt, noe som også kan påvirke utseendet på sølvhåndverkssmykker.
Tradisjonelle beskyttelsesmidler fungerer ikke godt når det gjelder å beskytte hullene på sølvsmykker, mens molekylære selvmonteringssystemer som alkyltioler, organsilaner og Schiff-baser kan danne beskyttende filmer på overflaten av sølvsmykker. Disse filmene har egenskaper som tett og ensartet struktur, upåvirket av substratoverflatens form, fri for metalliske urenheter og påvirker ikke substratets utseende, noe som demonstrerer utmerket antifargingsevne for sølv, noe som gjør dem til en av de lovende prosessene for overflatebehandling av anløpte sølvsmykker.
Overflatemodifiseringsprosesser har egenskaper som lave kostnader, enkle og praktiske prosesser og en viss antifargingseffekt. På grunn av den tynne filmen som dannes, vil det eksponerte sølvsubstratet likevel komme i kontakt med korrosive medier og anløpe når det blir riper i det.
2.2 Sølvlegeringer med anti-tarnish ved hjelp av total legering
Allerede i 1927 foreslo National Bureau of Standards i USA etter forskning at det ikke finnes noen annen måte å fullstendig forhindre sulfidasjonsreaksjonen av sølv på, med mindre det legeres med andre edelmetallelementer. For å undertrykke dannelsen av sølvsulfider er det nødvendig å danne legeringer med 40% palladium, 70% gull eller 60% platina. Det er imidlertid ingen tvil om at det fortsatt er en nødvendig og effektiv metode å forbedre sølvlegeringers anløpsmotstand ved hjelp av legeringer. Mange land over hele verden arbeider fortsatt med å utvikle nye typer sølvlegeringer som er motstandsdyktige mot anløpeflekker, og har oppnådd noen forskningsresultater. De viktigste legeringselementene som danner anlakkbestandige sølvlegeringer kan klassifiseres i tre kategorier.
(1) Legering med edle metaller.
Blant alle edelmetallelementene har sølv relativt aktive kjemiske egenskaper. Ved å tilsette edelmetallelementer med høyere kjemisk potensial, som Au, Pd og Pt, kan man forbedre elektrodepotensialet til sølvlegeringer og øke deres anløpsmotstand. Ved å tilsette 5% Pd til sterlingsølv ble for eksempel sølvlegeringens anløpsmotstand betydelig forbedret, og etter ti dager i en klor- eller ammoniakkatmosfære viste legeringen ingen misfarging eller korrosjon av betydning. Legeringen har en forlengelse på mellom 15%-26%, og den kan produseres ved hjelp av konvensjonelle støpe- og mekaniske formingsmetoder. På samme måte, i serien av anløpsbestandige sølvlegeringer som inneholder platina, når Pt-innholdet er 1%, er anløpsmotstanden mer enn tre ganger så stor som for sterlingsølv; når den inneholder Pt 3,5%, er anløpsmotstanden mer enn seks ganger så stor som for sterlingsølv; når den inneholder Pt 5%, er anløpsmotstanden mer enn åtte ganger så stor som for sterlingsølv. Sølvlegeringer som inneholder platina kan raffinere kornstørrelsen betydelig samtidig som hardheten økes; legeringen har også utmerket plastisitet; det forbedrer legeringens lysstyrke, nærmer seg fargen på platina og forhindrer utseendet på røde flekker. Legering med edle metaller øker materialkostnadene for anløpsbestandig sølv betydelig, og markedsapplikasjonen er relativt begrenset.
(2) Legering med sjeldne jordartsmetaller.
Mange studier har vist at tilsetning av spormengder av sjeldne jordartsmetaller til sølv eller sølvlegeringer bidrar til å forbedre legeringens motstandskraft mot sulfideringsmisfarging. De mest brukte sjeldne jordartsmetallene er yttrium (Y), cerium (Ce), lantan (La) osv. For eksempel, når sjeldne jordartselementer tilsettes rent sølv hvis innholdet av sjeldne jordarter er under 0,11%, kan det utvise bedre sulfidasjonsmisfargingsmotstand enn rent sølv. Tilsetningen av sjeldne jordartselementer forfiner kornstørrelsen på den kalddeformerte omkrystalliseringsstrukturen, og den spredte sølv-sjeldne jordforbindelser andre fase dannet gjennom fragmentering og reaggregering styrker effektivt sølvlegeringen og forbedrer legeringens termiske stabilitet, og viser en høy motstand mot aldringsmykning. De fleste sølvlegeringer som er utviklet på hjemmebane, har sjeldne jordartsmetaller som legeringselementer.
(3) Legering med andre oksygenaktive elementer.
Adding oxygen-active elements such as Zn, Si, Sn, In, and Ge to the Ag-Cu alloy can improve the sulfidation and oxidation discoloration resistance of silver alloys. This is currently the most common type of tarnish-resistant silver alloy on the market. Italy, the United States, Germany, and others have developed various tarnish-resistant silver alloy fillers, achieving sulfidation discoloration effects that reach more than five times that of sterling silver. The principle of its tarnish resistance: these elements belong to oxygen-active elements, and their oxides have lower free energy than copper oxides, with a stronger affinity for oxygen, allowing for the formation of more stable oxides. Before forming Ag2S, these oxides form a dense protective film layer, acting as a barrier to protect the silver matrix.
Section VI Performance Evaluation and Common Issues of Tarnish-Resistant Silver
1. Performance Evaluation of Anti-tarnish Silver
Various anti-discoloration silver filling materials have appeared on the market, with performance varying widely. Adopting appropriate methods to evaluate their performance is necessary, providing a basis for selecting suitable filling materials.
1.1 Evaluation Methods for Anti-Discoloration Performance
Anti-discoloration performance is one of silver alloys’ most important performance indicators, mainly including resistance to sulfide discoloration and oxidative red spots, which must be tested through experiments.
1.1.1 Evaluation Method for Resistance to Sulfide Discoloration
According to the conditions and locations used in the experiment, it is divided into outdoor and laboratory testing methods.
(1) Outdoor testing method
The outdoor testing method involves placing silver alloy samples in a real environment to observe the time the samples remain unchanged in color and the specific phenomena of color change that occur to evaluate the alloy’s resistance to color change. This method can more accurately reflect the alloy’s resistance to color change, but it has its own drawbacks: (1) The time to obtain test results is relatively long; for example, in certain environments, alloys with good corrosion resistance may take years to yield results; (2) The reproducibility of the results is low. Due to differences in regions and times, the natural environment will vary to some extent. Therefore, the results of the same alloy tested in different regions will differ significantly; even in the same region at different times, the test results will also vary.
Due to the long testing time in natural environments, accelerated corrosion methods are sometimes used to obtain results more quickly. For example, they are placing the alloy in harsh environments such as near electroplating workshops or boiler flue gas or exposing it to ultraviolet radiation in the atmosphere for testing. However, these methods are easily affected by environmental pollution and other factors, leading to significant differences in the degree of similarity, authenticity, and reproducibility of the test results compared to natural corrosion color change. Therefore, they are not advisable.
(2) Laboratory testing method
According to the corrosive media used in laboratory tests, it can be divided into two methods: liquid phase tests and gas phase tests.
(2.1) Liquid phase test method.
The more commonly used methods are the sulfide solution and artificial sweat immersion methods. The former involves immersing the sample in a solution of sodium sulfide or ammonium sulfide at a certain concentration, using the Tuccillo-Nielsen method, which is quite general. The sample is fixed on a rotating wheel and is periodically immersed in a solution of concentration 0.5% or 2% Na2S solution at a speed of 1r/min. It can effectively detect the discoloration resistance of silver alloys under the action of oxygenated sodium sulfide solution. The latter involves preparing artificial sweat according to relevant standards, immersing the sample in sweat with a certain pH value and temperature, usually around pH 6.5, at a temperature of 30℃ or 37℃. During the immersion test, it is necessary to maintain the stability of the solution temperature, and the sample and the comparison sample should be tested under the same conditions. The color changes of the comparison sample after different immersion times can be accurately measured using a colorimeter to determine the degree of discoloration of the sample.
(2.2) Gas phase test method.
Using gas phase test methods to examine the discoloration resistance of silver alloys and silver coatings has become quite common, forming international and domestic standards. Gas phase tests can be conducted in static or flowing gas. The gas contains substances that can cause discoloration of silver alloy materials, such as H2S, SO2, Cl2, and NO2, which can be a single gas or a mixture of two or more gases; the gas can be introduced or generated through chemical reactions. Common gas phase test methods mainly include:
A. H2S test method. This method uses H2S to conduct accelerated corrosion tests, widely used in the electronics industry for evaluating the discoloration resistance of electronic components and electrical contact materials, with multiple international and national standards. These standards include those using high-concentration H2S atmospheres as well as low-concentration ones. However, there is no specific test standard for discoloration resistance in the jewelry industry, leading to various practices, some referencing electronic industry standards for testing, while others choose their testing conditions. A typical testing method is the Thioacetamide (TAA) method, which is a strict standard for measuring silver jewelry, corresponding to the international standard Metallic Coatings-Thioacetamide corrosion test (TAA test) (BS EN ISO 4538-1995). Due to the high concentration of H2S atmosphere, some silver alloy surfaces are prone to discoloration, and the corrosion film layer may become loose and peel off, which can affect the accuracy and reproducibility of the results to some extent. The discoloration conditions of different types of silver alloys after H2S corrosion for 3 hours are compared as shown in Figure 4-20, where the concentration of H2S is 13 x 10-6, relative humidity is 75%, and temperature is 30℃.

B. SO2 Test method. SO2 Can accelerate the corrosion of silver alloys, typical methods include the “Corrosion Test of Metals and Other Inorganic Coatings under Condensation Conditions of Sulfur Dioxide”, which uses a certain volume, heated closed acrylic test chamber, introducing a certain concentration of SO2 gas, tested over three cycles (non-continuous exposure). Using a single SO2 gas for corrosion testing has a longer test cycle, and assessing the corrosion results between samples is somewhat difficult.
C. Mixed gas test method. The corrosion products of this method are relatively close to actual conditions, and the test results are relatively stable. This method is conducted in a specially designed test environment, with humidity at 75%, the temperature at 25℃, H2S, and concentrations of 0.8mg/L, SO2, and 3mg/L, updated three times per hour. Japan invented a mixed gas accelerated corrosion method for testing the corrosion status of silver alloys in electronic devices, composed of air, H2S, and NO2, where H2S is the main factor causing discoloration, and NO2 acts as a catalyst to accelerate the reaction between silver and H2S, allowing the formation of corrosion products in a shorter time.
1.1.2 Evaluation method for anti-oxidation red spot performance
There are generally two methods to evaluate silver alloys’ anti-oxidation red spot performance. (1) Place the sample in an electric furnace for heating, controlling the atmosphere, heating temperature, and insulation time, then take a cross-section of the sample to observe the oxidation film under a microscope (Figure 4-21). Polish the sample and observe the red spot condition on the polished surface. This method can stably control test conditions, and the test accuracy is relatively good. (2) Heat the sample with a torch to a certain temperature, then stop heating and let the sample cool naturally to room temperature, repeating the above operation several times, taking a cross-section of the sample to observe the oxidation film condition, and polishing to observe the red spot condition on the sample surface; this method has a larger human factor.

1.2 Evaluation of Process Performance
Silver alloys used for making jewelry need to have good resistance to sulfide discoloration and oxidation spots and require good mechanical and process performance, which often presents contradictions in joint development. Some alloying elements are beneficial for discoloration resistance. Still, when their content reaches a certain level, they may negatively impact the alloy’s casting and processing performance, leading to a decline in the overall performance of the alloy; In contrast, some alloying elements can improve the mechanical properties of silver, they may not be favorable for its discoloration resistance. Therefore, when selecting discoloration-resistant silver alloys, it is necessary to evaluate their discoloration resistance while fully considering the performance requirements of the alloy for different processing techniques. For example, the melting method can affect the oxidation resistance of the alloy; the same alloy can yield different results when melted using a torch, induction heating in the atmosphere, or melted in a protective atmosphere or vacuum; similarly, jewelry production may use casting methods, stamping methods, or welding methods, each of which has a different emphasis on the process performance requirements of the alloy, requiring separate evaluations from the perspectives of castability ability, cold working performance, welding performance, etc., and fully consider the process operability of the alloy to avoid operational issues that may arise from a too-narrow process range.
1.3 Evaluation of Safety and Cost-Effectiveness
The silver alloy used for jewelry must meet safety requirements, and the content of toxic and harmful impurity elements must not exceed international standards. Additionally, the silver alloy’s comprehensive performance and material cost should be evaluated in terms of cost-effectiveness.
2. Common issues with anti-tarnish silver for jewelry
The issues with anti-tarnish silver for jewelry in the market mainly include the following aspects.
2.1 Insufficient anti-tarnish performance
When jewelry companies discuss the silver jewelry business, the most direct question from customers is how long the silver jewelry can remain untarnished. Many customers require it to remain untarnished for at least one year, but companies need help guaranteeing this. Besides the influence of usage environment and storage methods, a significant reason is that the anti-tarnish performance of the alloy itself is not outstanding. Silver alloys containing precious metal elements like Pd and Pt have better anti-tarnish performance, but their relatively high prices deter many companies, as customers often need to specify the use of such alloys or pay extra for them. The market is predominantly occupied by anti-tarnish silver alloys that use oxygen-active element alloying. Theoretically, the dense oxide film formed by these elements should prevent the internal metal from further sulfiding and oxidizing, thereby improving the silver alloy’s resistance to sulfide and oxidative discoloration. However, it should be noted that the microstructure of the base alloy, the distribution of alloying elements in the base, and the structure and mechanical properties of the surface oxide film can significantly affect the structure of the oxide film. If the formed alloy oxide film is unevenly distributed, loose and coarse, or has micro-cracks, it will not provide effective protection. In other words, different alloys with different component ratios will yield different anti-tarnish results. Even if the same alloy manufacturer uses the same alloy formula, if the company does not strictly adhere to the specified melting and casting process standards during production, the results may also vary.
2.2 The problem of insufficient hardness
Many companies have reported that the hardness of tarnish-resistant silver alloys is much lower than that of sterling silver, making them relatively easy to deform and unable to meet the requirements for mold making, elastic parts, etc. This is indeed the case. For silver alloys that improve tarnish resistance with Pd, Pt precious metal elements, due to their similar crystal structure to silver and high solubility, the strengthening effect is poor, and the initial hardness is generally low. Zn is commonly used as the main alloying element for tarnish-resistant silver alloys alloyed with other elements, and the strengthening effect could be better. Therefore, most tarnish-resistant silver alloys have low as-cast hardness, usually below HV60, which is insufficient for jewelry products with certain strength requirements. Although alloys can increase hardness through deformation processing, only casting processes can be used for the production of most set jewelry, making deformation methods unsuitable. Of course, some alloys can improve hardness through aging treatment, but they are often not used or misused in actual production because jewelry-making involves a multi-process craft. During the mold-making stage, gemstone setting stage, and even polishing stage, the workpiece may undergo welding or heating, usually done by operators using flame heating, with heating temperature, heating time, and cooling speed being quite arbitrary, making it generally difficult to achieve the effects expected by alloy suppliers. Additionally, once the jewelry has been set with gemstones, it is no longer suitable to use aging treatment methods to increase hardness, as high-temperature quenching can easily damage the gemstones.
Therefore, from a practical application perspective, it is necessary to improve the alloys’ as-cast and annealed hardness. From China’s resource advantages, rare earth elements should be worth considering.
2.3 Issues related to casting
The vast majority of jewelry is formed through casting, and several jewelry companies have established their casting departments. Companies generally only purchase filler from alloy suppliers and then buy pure silver to prepare the required silver alloy. During the casting production process, many companies are often troubled by various casting issues such as porosity, sand holes, shrinkage, inclusions, and cracks, which affect the normal order of production and increase production costs.
Sterling silver, with Cu as the main alloying element, is prone to defects such as porosity and oxidized inclusions if not protected during melting, increasing the molten metal’s viscosity. The oxidized film formed at the front of the molten metal increases surface tension, leading to increased filling resistance and affecting forming performance. The resulting defects, such as porosity and inclusions, significantly increase the difficulty of subsequent polishing.
Silver alloys primarily composed of Pd, Pt, and other precious metal elements have a higher melting point, increasing the likelihood of porosity. This is because jewelry mainly uses gypsum molds, and gypsum has poor thermal stability; the higher the alloy’s melting point, the greater the possibility of thermal decomposition of gypsum, leading to porosity in the castings.
Different anti-tarnish silver alloys contain different types and amounts of oxygen-active elements, exhibiting varying casting performances. Si oxide has a low density and high viscosity, making it easy to float to the surface of the molten metal and be removed with the help of flux, which is beneficial for fluidity and filling performance. However, excessive Si can lead to thermal cracking and polishing issues; removing Zn and Sn oxides is more difficult. For silver alloys containing a large amount of low-melting-point oxygen-active elements (such as Zn, Sn, In ), using a torch for melting can easily produce volatiles and oxidized inclusions, and using induction heating can also lead to similar problems due to overheating. A small amount of rare earth added can improve filling properties. Still, the amount of rare earth increases to a certain extent. In that case, the formed rare earth oxides will increase the viscosity of the molten metal, counteracting the purifying effect of the rare earth and negatively affecting casting performance.
Among the issues above, porosity is one of the most prominent problems. The porosity generation is closely related to the properties of the silver alloy itself. As mentioned earlier, silver has a typical characteristic of absorbing a large amount of oxygen in the molten state, causing the molten metal to splash at high temperatures, resulting in significant losses easily. During the solidification process of casting, the solubility of gas in the molten metal decreases with the drop in temperature, leading to gas supersaturation, precipitation, and enlargement, forming bubbles that fail to be discharged in time, resulting in porosity (Figure 4-22).

From the mechanism of pore formation, it can be seen that there are mainly two approaches to reduce or avoid pore defects: (1) minimize the amount of gas entering the molten metal; (2) take measures to release the gas in the molten metal before pouring.
(1) Reduce the gas entering the molten metal.
First, the quality of the raw materials must be controlled. The raw materials should be dry and clean, not damp or oily. The purchased pure silver materials come in forms such as granules, bars, and plates, with granules being the most common. Since granules are formed by metal droplets rapidly cooling in water, they can sometimes be hollow and even contain water inside, which can introduce a large amount of gas during melting. They must be thoroughly dried or pre-melted into ingots before use. If the surface of the raw materials has oil or other organic impurities, it will also introduce gas, especially when reusing scrap from stamped jewelry, which often adheres to oil. It should be degreased and cleaned thoroughly before use. The ratio of new and reused materials should be reasonably controlled when mixing materials. Each time the raw materials are melted and cast, they will be contaminated, including gas absorption, reaction with gypsum molds, and residual inclusions. Therefore, the amount of reused materials should generally be controlled within 50%.
Secondly, effective protective measures should be taken during melting. Different enterprises have different production conditions, and the melting methods used also vary. Common melting methods include gas-oxygen flame, acetylene oxygen flame, high-frequency induction furnace, and medium-frequency induction furnace. When melting in the open atmosphere, the molten metal will inevitably absorb gas; the larger the liquid surface and the longer the contact time, the greater the tendency to absorb gas, mainly oxygen from the air. When using flame melting, it also includes oxygen brought in by the oxidizing flame. Therefore, protective measures should be taken during the melting process to reduce the amount of gas absorption if silver is melting in the atmosphere; crushed charcoal, graphite sheets, or dehydrated borax can be used as a cover. If flame melting is used, it should be adjusted to an orange-yellow reducing flame, and the melting time should be a manageable length. If conditions permit, priority should be given to vacuum induction melting, which can be done under low vacuum with protective gas. This involves evacuating the melting chamber first, then backfilling it with nitrogen or argon as protective gas, followed by heating and melting. Nitrogen is cheaper, but it has a certain solubility in silver, which poses a risk of causing pores; argon is more expensive but is more stable in silver and should be prioritized.
(2) Promote gas release in the molten metal before pouring.
Under atmospheric conditions, molten silver inevitably absorbs gas. To avoid the formation of gas pores, the molten metal should undergo degassing treatment before pouring, allowing as much gas dissolved in the silver liquid as possible to be released. Two methods can be adopted:
A. Using floating gas bubbles for degassing. By blowing fine, dense argon bubbles into the bottom of the molten metal using a breathable plug, it does not react with the molten metal and becomes floating gas bubbles. The bubbles serve as a vacuum space for the gases dissolved in the molten metal, allowing the dissolved gases to diffuse into the floating bubbles, becoming gaseous molecules that rise with the bubbles. When the floating bubbles rise to the surface of the molten metal, the gas inside the bubbles escapes into the atmosphere, achieving the goal of reducing the gas content in the molten metal.
B. Using condensation method for degassing. The silver liquid is slowly cooled to the solidification temperature, causing most of the dissolved oxygen and other gases to precipitate due to the decrease in solubility with the drop in temperature, thus achieving the purpose of degassing. It is then rapidly heated back to the pouring temperature for casting. For silver liquids with poor raw material quality and high gas content, multiple cycles of condensation and remelting can be performed to improve their quality.
2.4 Issues in cold processing
Issues in cold processing in the production process of silver jewelry, common cold deformation processing techniques include cold volume forging such as cold heading, cold extrusion, stamping, etc., and sheet metal stamping such as stretching, blanking, trimming, punching, etc. Material rolling, such as cold rolling, roll forming, etc., and the following issues are often encountered during processing.
(1) Surface sand holes of profiles.
The surface quality of profiles depends not only on the surface quality of the ingot but is also closely related to the surface quality of the rollers. When the roller surface has scratches or local damage, it will be replicated on the profile surface; when dust or other debris accumulates on the roller surface, it will be pressed into the profile surface, worsening the surface quality of the profile (Figure 4-23). Therefore, during production, the roller surface should be frequently wiped to prevent dust and other impurities from accumulating and scratching the rollers or being pressed into the strip surface. The rollers should be covered when not in use to protect the surface. The diameter of the finished product rollers should be small and highly polished or electroplated to achieve a mirror effect.

(2) Annealing defects.
This includes blistering, abnormal grain growth, and incomplete annealing.
A. Blistering. Blistering on the surface of sheets and strips is caused by gas holes within the ingot or reactions between the ingot and the atmosphere during annealing. The pressure increases when the bubbles are heated, causing the metal surrounding the bubble to expand and form blisters (Figure 4-24). This issue can generally be avoided by controlling the casting or annealing conditions. For example, it enhances deoxidation during the melting process, reduces the dissolved oxygen content and oxidation in the molten metal, controls the annealing temperature, and avoids using hydrogen-rich annealing atmospheres.
B. Abnormal grain growth. Silver will exhibit significant grain growth when the annealing temperature is too high or the annealing time at high temperature is too long (Figure 4-25). Excessively coarse grains affect mechanical properties and severely impact the surface quality of processed jewelry. Therefore, the annealing process should be reasonably formulated based on the size and quality of the profile.
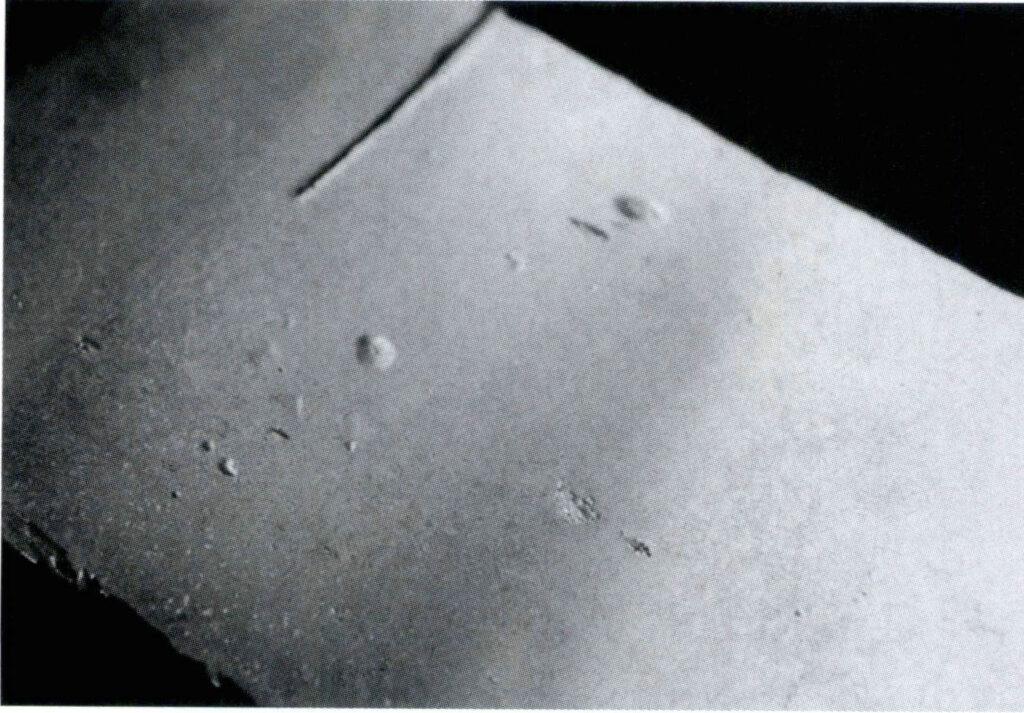
Figure 4-24 Bubbles appearing on the surface of silver profiles after annealing

Figure 4-25 Abnormal grain growth caused by improper annealing of silver
C. Incomplete annealing. Different silver alloy materials have different recrystallization temperatures. If the annealing temperature is too low, the amount loaded into the furnace is too large, or uneven heating is applied with a torch, incomplete annealing may occur. In this case, residual stress will remain within the profile, affecting subsequent processing and leading to defects such as cracks.
2.5 Issues related to polishing
Jewelry has high requirements for surface quality, and most jewelry must undergo polishing to achieve a mirror-like finish. Polishing of anti-tarnish silver alloys often encounters several typical problems, such as orange peel surface, dents, scratches, and comet tails. When the alloy’s grain is coarse, it is prone to forming an orange peel surface; when there are shrinkage or porosity defects in the alloy, it is likely to form polishing dents; when high hardness segregated phases or inclusions appear within the alloy’s grain structure, it is easy to form polishing scratches and comet tails.
To achieve a good surface polishing effect, in addition to correctly executing the polishing operation process, the properties of the alloy itself also have an important impact. Grain refinement and improvement of casting performance are the main ways to enhance polishing performance.