Quelles sont les principales méthodes et applications du plaquage platine dans l'industrie moderne ?
Techniques de plaquage platine : solutions, alliages et applications en joaillerie
Introduction :
Vous vous interrogez sur le plaquage platine ? Ce guide couvre tous les aspects, des bases aux techniques avancées. Découvrez différentes solutions de plaquage, notamment à base de chlorure et de sulfate, et apprenez à les optimiser. Explorez les solutions de plaquage minces et épaisses pour diverses applications. Les alliages de platine vous intriguent ? Nous abordons les plus courants comme le Pt-Au, le Pt-Co et le Pt-Ir. De plus, plongez-vous dans le plaquage chimique pour des applications uniques. Que vous soyez créateur de bijoux, détaillant ou fabricant sur mesure, ce guide complet vous aidera à sublimer vos produits grâce au plaquage platine.

Table des matières
Section I Aperçu
Le platine possède un numéro atomique de 78 dans le tableau périodique, son symbole chimique est Pt, sa masse atomique relative est de 195,7 et sa densité est de 21,09 g/cm³.3 (20℃), et un point de fusion de 1768℃.
Certains paramètres principaux du platine sont présentés dans le tableau 3-1.
Tableau 3-1 Quelques paramètres principaux du platine
| Paramètres caractéristiques | Valeur caractéristique |
|---|---|
|
Nom de l'élément, symbole de l'élément, numéro atomique Classification Groupe, Période Densité, dureté Couleur Masse atomique relative Rayon atomique rayon de liaison covalente valence chimique structure cristalline point de fusion point d'ébullition Chaleur de vaporisation Chaleur de dissolution Capacité thermique spécifique Conductivité conductivité thermique |
Platine, Pt, 78 Métal de transition 10(Ⅷ),6 21090kg/m3, 3.5 blanc grisâtre 195.084 13h35 128 heures 2、4 Cubique à faces centrées 2041. 4K ( 1768,3℃ ) 4098K (3825℃) 510 kJ/mol 19,6 kJ/mol 130J/(kg • K) 9. 66X 106m ・Ω 71,6 W/(m·K) |
Section II Galvanoplastie du platine
Tableau 3-2 Applications industrielles des revêtements de placage au platine
| Produit | Matériaux | Épaisseur du placage/μm | Produit | Matériaux | Épaisseur du placage/μm |
|---|---|---|---|---|---|
|
Composants aérospatiaux Composants aéronautiques Plateaux de cloison de sécurité Électrodes |
Superalliages contenant du niobium SUS347 Titane SUS316 |
10 10 5 10 |
Électrodes Électrodes Électrodes - |
Titane maille de titane Fil de tungstène - |
2 à 7 2 à 7 10 - |
Tableau 3-3 Sels de platine typiques
| sels 2,4-valents | sels de platine typiques |
|---|---|
| sels de Pt(II) |
Acide chloroplatinique : H2PtCl6 • 6H2O Nitrite de platine diammine : Pt(NH3)2(NON2)2 sulfate de nitrite de platine : H2Pt(NO2)2SO4 |
| sels de Pt(IV) | Hydroxyplatinate de sodium : Na2Pt(OH)6 · 2H2O |
1. Diverses solutions de plaquage de platine
Tableau 3-4 Compositions et conditions de traitement de diverses solutions de placage de platine
| Conditions de composition et de procédé | Chlorure | sulfite de diammonium | DNS | sels hydroxybasiques | Acide phosphorique | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N° 1 | N° 2 | N° 3 | N° 4 | N° 5 | N° 6 | N° 7 | N° 8 | N° 9 | N° 10 | N° 11 | N° 12 | N° 13 | N° 14 | |
| Acide chloroplatinique H2PtCl6/(g/L) | 10 à 50 | |||||||||||||
| Chloroplatinate d'ammonium (NH4)2PtCl6/ (g/L) | 15 | |||||||||||||
| nitrite de diammine platine Pt(NH3)2(NON2)2/(g/L) | 8~16. 5 | 20 | 6~20 | 8 | 6~20 | 16.5 | ||||||||
| sulfate de nitrite de platine H2Pt(NO2)2SO4/ (g/L) | 10 | |||||||||||||
| Hydroxyplatinate de sodium Na2Pt(OH)6 ・ 2H2O/(g/L) | 20 | 18.5 | ||||||||||||
| Acide hydroxyplatinique H2Pt (OH)6/ (g/L) | 20 | |||||||||||||
| Hydroxyplatinate de potassium K2Pt(OH)6/ (g/L) | 20 | |||||||||||||
| Chlorure de platine PtCl4· 5H2O/(g/L) | 7.5 | |||||||||||||
| Ammoniac (28%)/(g/L) | ||||||||||||||
| Acide chlorhydrique/(g/L) | 180~300 | |||||||||||||
| Citrate de sodium (g/L) | 100 | 20~25 | ||||||||||||
| Chlorure d'ammonium/(g/L) | 4~5 | |||||||||||||
| Nitrate d'ammonium (g/L) | 100 | |||||||||||||
| Nitrite de sodium/(g/L) | 10 | |||||||||||||
| Acide fluoroborique/(g/L) | 50~100 | |||||||||||||
| Fluoborate de sodium/(g/L) | 80~120 | |||||||||||||
| Acide sulfonique/(g/L) | 20~100 | |||||||||||||
| Acide phosphorique/(g/L) | 80 | 10~100 | ||||||||||||
| Acide sulfurique/(g/L) | 10~100 | pH2 | ||||||||||||
| Acétate de sodium/(g/L) | 70 | |||||||||||||
| carbonate de sodium/(g/L) | 100 | |||||||||||||
| Hydroxyde de sodium/(g/L) | 10 | 5.1 | ||||||||||||
| Oxalate de sodium/(g/L) | 5.1 | |||||||||||||
| sulfate de sodium/(g/L) | 30.8 | |||||||||||||
| Hydroxyde de potassium/(g/L) | 15 | |||||||||||||
| Phosphate d'ammonium hydrogéné)(g/L) | 20 | |||||||||||||
| Hydrogénophosphate de sodium/(g/L) | 100 | |||||||||||||
| Sulfate de potassium (g/L) | 40 | |||||||||||||
| Température de la solution de placage (°C) | 45~90 | 80~90 | 90~95 | 70~90 | 65~100 | 75~100 | 75~100 | 80~90 | 30~70 | 75 | 65~80 | 75 | 70~90 | 70~90 |
| Densité de courant (A/dm)2) | 3.0 | 0.5~1.0 | 0.3~2.0 | 2~5 | 0.2~2 | 0.5~0.3 | 0.5~0.3 | 0.5 | 2.5 | 0.8 | 0.8 | 0.75 | 0.3~1 | 0.3~1 |
| Rendement du courant/% | 15~20 | 70~10 | 10 | 14~18 | 15 | 15 | 15 | 35~40 | 10~15 | 100 | 80 | 100 | 10~50 | 15~50 |
(1) Solution de plaquage au chlorure
La première solution de placage de platine techniquement réussie utilisait l'acide chloroplatinique (H₂O₃).2PtCl6・6H2O) comme sel de base. Une électrode de Pt soluble a été utilisée, dans les conditions suivantes : acide chloroplatinique (10 à 15 g/L), acide chlorhydrique (180 à 300 g/L), température de la solution de placage de 45 à 90 °C et densité de courant de 2,5 à 3,5 A/dm².2L'efficacité du courant cathodique est de 15% à 20%. Le film de placage obtenu à partir de cette solution peut atteindre 20 µm d'épaisseur sans fissures et présente une bonne ductilité. Cependant, le pH doit être maintenu dans une plage étroite afin d'éviter l'hydrolyse de la solution de placage. L'hydrolyse débute lorsque le pH de la solution atteint 2,2.
(2) Solution de placage de diamminonitrite
Pour assurer la concentration de platine divalent et empêcher son oxydation en Pt(IV), il est nécessaire d'ajouter une quantité appropriée de composés aminés afin de former un complexe avec le Pt(II). Le composant principal de cette solution de placage est le diamminotritoplatine Pt(NH₃)₂.3)2(NON2)2Ce sel, souvent appelé sel Pt-P (II), a été découvert par W. Keitel en 1931 (solution de placage n° 3 du tableau 3-4). L’augmentation de la concentration en nitrite dans la solution affecte la dissociation du complexe de platine et, par conséquent, le comportement de la solution de placage. Après ébullition, NH₃4On ajoute OH pour réagir avec NaNO3 pour générer du NH34NON2 Pour rétablir l'efficacité initiale du courant, on produit du Pt-P, qui se décompose ensuite en azote et en hydrogène gazeux. De cette manière, la quasi-totalité des composants non métalliques du sel Pt-P dans la solution de placage se vaporise et disparaît, ce qui prolonge la durée de vie de cette solution par rapport aux solutions de placage chlorées. L'avantage de cette solution de placage réside dans la relative facilité d'ajustement de sa composition.
AB Triper et al. ont utilisé le PR comme source d'énergie, atteignant une vitesse d'électrodéposition de 5 μm/h. Les conditions étaient les suivantes : 5 à 6 A/dm².2Le temps d'électrolyse cathodique est de 5 s et le temps d'électrolyse anodique de 2 s. La solution de placage n° 4 du tableau 4-3 a été décrite dans le brevet français de Lacroix de 1967. Cette solution permet d'obtenir une épaisseur de revêtement allant jusqu'à 7,5 µm. La solution de placage n° 5 est issue d'un brevet américain (US PAT. 2984603, 2984604) déposé en 1961, qui consiste à ajouter de l'acide sulfonique à la solution de placage de sel de platine-phosphore. La solution n° 6 contient de l'acide phosphorique, tandis que la solution n° 7 utilise un mélange d'acide phosphorique et sulfurique comme base, conformément au brevet français de 1960 (Fr PAT. 1299226). Les auteurs ont utilisé des anodes insolubles et ont appliqué avec souplesse des méthodes essentielles telles que l'agitation.
Le procédé n° 8 utilise de l’acétate de sodium et du carbonate de sodium en remplacement des sels d’ammonium, ce qui permet d’obtenir un rendement de courant maximal et d’améliorer la stabilité de la solution de placage. Le revêtement obtenu est lisse et uniforme, avec une épaisseur pouvant atteindre 10 µm, sans piqûres ni fissures.
Au Japon, cette solution de placage est largement utilisée dans l'industrie. Voici un exemple :
|
Platine (nitrite de diammineplatine) nitrate d'ammonium nitrite de sodium Hydroxyde d'ammonium |
10 g/L 100 g/L 10 g/L 35 g/L |
Température de la solution Densité de courant efficacité actuelle - |
90~92℃ 1A/dm2 10%~20% - |
(3) Solution de placage à l'acide nitrosulfurique de platine
Cette solution de placage ne contient ni ammoniac ni amines, mais utilise de l'acide nitrosulfurique de platine [H2Pt (OH)6 · 2H2O) comme ingrédient de base. La préparation de la solution de placage implique l'utilisation de sels nitrés, de sels de potassium de chlorure de platine ou d'acide sulfurique de platine (K)2Pt(NO2)3Cl, K2Pt (NO2)2Cl2 ou K2Pt (NO2)2SO4Une faible densité de courant est utilisée pour un placage brillant, et de l'acide sulfurique est ajouté pour ajuster le pH en dessous de 2,0. Des compositions représentatives sont présentées dans le tableau 3-4, n° 9. Cette solution de placage permet d'obtenir des couches de placage relativement épaisses.
(4) Solution de placage de métaux à base de sels d'acide hydroxyplatinique alcalin
Dans une solution de placage alcaline typique, on utilise un sel de sodium ou de potassium de l'acide hydroxyplatinique tel que Na2Pt(OH)6 ou K2Pt(OH)6 La solution de placage utilisée présente des compositions représentatives (voir tableau 3-4, n° 11). La température de la solution de placage est de 75 °C et la densité de courant de 0,8 A/dm².2, et le rendement actuel peut atteindre 100%, et l'anode utilise des matériaux en Ni ou en acier inoxydable.
Le procédé n° 10 a été proposé par AR Powell en 1913 et un brevet britannique a été obtenu (Brit PAT. 363569). Un revêtement brillant comparable à la solution de placage au rhodium peut être obtenu.
On peut obtenir un certain nombre de couches minces à partir de cette solution de placage. Lorsque la concentration en Pt est inférieure à 3 g/L, le rendement faradique chute brutalement. Une densité de courant peut atteindre 2,5 A/dm².2 Lorsque la concentration est élevée (12 g/L), et à une température de solution de 65 à 70 °C, l'efficacité du courant peut atteindre environ 801 T/min. Cependant, une augmentation supplémentaire de la température n'améliore pas significativement le résultat.
(5) Solution de phosphatation
Dès 1855, Roseleuer proposa le procédé au phosphate. Cette solution de placage utilise un sel de coordination de chlorure de platine tétravalent, des phosphates de métaux alcalins et des sels d'ammonium comme sels conducteurs. En 1949, W. Pfanhauser proposa la solution de placage n° 14 qui, dans ces conditions, permet d'obtenir un revêtement de 0,5 µm.
Druve a présenté des résultats expérimentaux obtenus avec la même solution de placage. Le principal inconvénient de cette solution réside dans la difficulté de son réglage. Les précipités qui se forment lors de la préparation de la solution doivent se dissoudre lentement. L'utilisation de phosphate d'ammonium est nécessaire pour éviter les revêtements poreux et spongieux. Le phosphate d'ammonium facilite la dissolution du complexe de platine. Dans certaines conditions, un sel jaune insoluble se forme à la surface de l'anode dans la solution de placage, constituant une couche isolante probablement composée d'hydroxyplatinate d'ammonium.
(6) Placage au platine à base de sulfate
Le plaquage de platine sur titane ou tantale ne pose pas de problème, même s'il n'est pas brillant. Cependant, pour le plaquage d'objets décoratifs, la brillance devient primordiale et le risque de fissures est à prendre en compte. Masashi et al. ont proposé l'utilisation d'une solution de plaquage au sulfate pour pallier ce problème. Cette solution consiste à dissoudre un sel de platine dans du sulfate, à ajouter du sulfite et à ajuster le pH à moins de 2 avec de l'acide sulfurique. L'ajout de sulfite rend le potentiel du platine plus négatif que celui des ions hydrogène, ce qui garantit une faible teneur en hydrogène dans la couche de platine et, par conséquent, une faible contrainte interne et une brillance élevée. Toutefois, une concentration trop élevée de sulfite peut entraîner la réduction du platine. À un pH supérieur à 2, le sulfite s'hydrolyse facilement, tandis qu'un pH inférieur à 2 contribue à stabiliser le complexe de platine.
Le prétraitement pour le plaquage est le suivant : alcalin → dégraissage électrolytique → trempage dans l'acide et électrolyse cathodique de 2 min.
Le processus de placage est présenté dans le tableau 3-5.
Tableau 3-5 Conditions du procédé de platine dans la série d'acide sulfurique
| Conditions de composition et de procédé | N° 1 | N° 2 |
|---|---|---|
|
HAuCl4 (compté comme Au) K2SO4 K2SO3 pH (ajusté avec de l'acide sulfurique) température Densité de courant Temps de placage Épaisseur du placage Couche de placage |
10 g/L 50 g/L 1,0 g/L 1.0 75℃ 2A/dm2 60 min 7 μm Luminosité |
10 g/L 100 g/L 2,0 g/L 2.0 65℃ 1 A/dm2 100 min 5/μm Belle apparence, bonne adhérence |
Dans le tableau 3-5 n° 1, un revêtement dichroïque de Pt-Au peut être obtenu en pré-plaquant de l'or flash sur le substrat, en plaquant une couche épaisse de platine de 7 μm et en plaquant 2 μm d'or sur le platine.
2. Solution de placage mince
3. Solution de placage épais
(1) Placage décoratif
Comme mentionné précédemment, les produits plaqués platine, tels que les montures de lunettes et les boîtiers de montres, ont vu le jour en raison de l'importance accordée à la marque platine. L'épaisseur du plaquage est généralement inférieure à 5 µm.
Récemment, une autre technologie a fait son apparition dans le domaine des objets décoratifs : l'électroformage.
L'épaisseur des produits électroformés est généralement de 100 à 150 µm. Leur évidement permet de réduire leur poids et leur coût. Lors du placage avec des solutions ordinaires et par des méthodes d'électroplacage conventionnelles, des fissures apparaissent dès que l'épaisseur du placage dépasse 10 µm, ce qui représente un défi technique.
(2) Applications industrielles
Le placage au platine de pièces en acier inoxydable pour l'aéronautique est désormais utilisé en pratique. Le procédé est le suivant :
Tableau 3-6 Performances des matériaux d'anode en platine
| Propriétés | Pt | Ti | Nb | Ta |
|---|---|---|---|---|
|
Densité (20℃)/(g/cm3) Point de fusion/°C Dureté (après traitement thermique) Conductivité thermique/[W/(m·K)] Résistivité/μΩ·cm Coefficient de dilatation linéaire (x105)/[mm/(mm·K)]
|
21. 45 1769 37 à 42 (Vickers) 71. 6 10. 6 9. 1 |
4. 54 1668 120 (Brennel) 16.8 48 8. 5 |
8. 57 2468 84 (Vickers) 67. 4 13. 1 7. 1 |
16. 6 2996 E-60 (Rockwell) 54. 8 12.4 6. 5 |
Généralement, l'épaisseur de la couche de platine est d'environ 2 µm, ce qui induit une densité de courant élevée. Dans des conditions telles que les courts-circuits lors du contact avec la cathode, et lors d'opérations impliquant du bifluorure d'ammonium, de l'acide fluoroborique, des bases fortes et des solutions à forte concentration de cyanure, la consommation de platine s'accélère. Il est donc nécessaire d'en prolonger au maximum la durée de vie, ce qui peut être réalisé en augmentant le rapport surface anode/surface cathode. Lors du dépôt de platine sur des électrodes en titane, le titane peut d'abord être rendu rugueux par sablage, puis activé à l'acide pour éliminer la couche d'oxyde superficielle, avant le dépôt électrolytique de platine.
Le processus de vieillissement typique des anodes en titane plaquées platine se déroule comme suit : ① le film d’oxyde de titane présent aux défauts de la plaque de platine est détruit ; ② le titane commence à se dissoudre ; ③ l’interface platine-titane subit une corrosion par piqûres à mesure que la dissolution progresse, et le film de platine se détache. Si ce phénomène se produit pendant le plaquage à l’or, il entraînera une augmentation soudaine de l’écart d’épaisseur de la couche d’or. En pratique, face à de tels problèmes, il est préférable d’inspecter l’anode.
4. Autres améliorations apportées à la solution de placage
(1) Améliorations apportées au prétraitement
Il existe également des méthodes pour améliorer l'adhérence entre le sodium et ses alliages et la couche de platine en optimisant le prétraitement. Kamata a proposé dans un brevet une technique de décapage acide à pH 1, suivie d'un dépôt de platine de l'épaisseur requise dans une solution alcaline. La solution de décapage acide contient principalement de l'acide chloroplatinique (0,3 à 3 g/L, exprimé en platine) et une concentration en ions halogénures de 5% à 15% (fraction massique). Le pH doit être maintenu en dessous de 1 ; une valeur supérieure entraîne une diminution de l'activité du titane et une mauvaise adhérence. À l'inverse, une concentration trop faible en ions halogénures peut empêcher l'élimination complète du film passif à la surface du titane, ce qui affecte également l'adhérence de la couche de platine. Les conditions de décapage sont une température de la solution de 40 à 80 °C et une densité de courant de 5 à 25 A/dm².2Les conditions et les résultats du plaquage au platine sont présentés dans le tableau 3-7.
Tableau 3-7 Conditions de placage au platine et leurs résultats (les valeurs de concentration sont entre parenthèses)
| Numéro de série | solution de placage par impact | solution de plaquage platine | Épaisseur du placage/μm | Test de stripping | ||
|---|---|---|---|---|---|---|
| ion platine/(g/L) | Ion halogène (fraction massique)/% | ion platine/(g/L) | pH | |||
|
1 2 3 4 5 6 7 8 9 |
H2PtCl6 (0. 1) H2PtCl6 (0. 1) H2PtCl6 (0. 1) H2PtCl6 (1. 0) H2PtCl6 (1. 0) H2PtCl6 (1.0) H2PtCl6 (5.0) H2PtCl6 (5.0) H2PtCl6( 5. 0) |
HCl (5) HCl (5) HCl (5) HCl (10) HCl (10) HCl (10) HCl (20) HCl (20) HCl (20) |
K2Pt(OH)6 (5) K2Pt(OH)6 (10) K2Pt(OH)6 ⑸ dinitrate de platine (5) dinitrate de platine (10) Dinitramide de platine (20) K2Pt(OH)6 ⑸ K2Pt(OH)6 (10) K2Pt(OH)6 (20) |
12. 0 13. 0 13. 5 12. 0 13. 0 13. 5 12.0 13. 0 13. 5 |
10 15 20 10 15 20 10 15 20 |
Bon Bon Bon Bon Bon Bon Bon Bon Bon |
(2) Placage du platine à l'aide d'une solution de placage neutre
L'utilisation d'une solution de placage quasi neutre est avantageuse pour le dépôt de motifs, car elle évite l'emploi de métaux alcalins comme le sodium et, par conséquent, les effets néfastes liés à leur accumulation. La solution de placage au platine proposée par Otani répond à cette condition. Le tableau 3-8 présente la composition de cette solution et les résultats des essais réalisés dans ses conditions de mise en œuvre.
Tableau 3-8 Composition et conditions de traitement de la solution de placage de platine neutre
| Ingrédients et leurs conditions de traitement | N° 1 | N° 2 | N° 3 |
|---|---|---|---|
|
Dinitrodiammine platine (concentration en Pt)/(g/L) Glycine/(mol/L) Acide iminodiacétique/(mol/L) Acide diaminotriacétique/(mol/L) pH Température/°C Densité de courant (A/dm)2) Vitesse de précipitation (μm/min) Rendement du courant/%
|
12 0. 57 - - 5.0 70 1. 0 0. 3 80 |
12 - 0. 3 - 5. 0 70 1. 0 0. 2 65 |
12 - 0. 1 0. 1 5. 0 70 1. 0 0. 1 65 |
Cette solution de placage étant proche de la neutralité, elle est favorable au placage de motifs et n'affectera pas négativement le film de contre-placage.
Kamata, du Japon, a également étudié l'effet des métaux alcalino-terreux comme agents de brillance. Il a constaté que les métaux alcalino-terreux, tels que le calcium, le baryum et le magnésium, ont un effet brillant sur les solutions de placage alcalines. La concentration optimale d'ions alcalino-terreux est de (2 × 100) × 10-6Le degré de luminosité est également contrôlé en faisant varier la concentration d'ions de métaux alcalino-terreux ajoutés.
Les principaux composants et conditions de fonctionnement de la solution de placage sont les suivants :
| Principaux composants de la solution de placage |
KOH 40 g/L Pt [ajouté sous forme de K2Pt(OH)620 g/L Ca [ajouté sous forme de CaCl2 solution aqueuse] Quantité adéquate |
| Conditions de fonctionnement |
pH 13,5 Température 80℃ Densité de courant 3A/dm2 Plaque de cuivre calandré en métal de base Épaisseur du placage : 20 μm |
Tableau 3-9 Effet de la concentration en ions Ca sur la brillance de la couche de placage de platine
| Concentration en ions Ca/x10-6 | Apparence | Concentration en ions Ca/x10-6 | Apparence |
|---|---|---|---|
|
0 0. 1 0. 3 0. 5 0. 7 1. 0 |
Non brillant Non brillant Non brillant Non brillant Non brillant Semi-brillant |
1. 5 2. 0 2. 5 3. 0 5. 0 - |
Semi-brillant Semi-brillant Semi-brillant Semi-brillant Miroir brillant - |
Copywrite @ Sobling.Jewelry - Fabricant de bijoux sur mesure, usine de bijoux OEM et ODM
Section III Placage en alliage de platine
(1) Alliage platine-iridium
L'alliage Pt-Ir électrodéposé peut être utilisé sur les électrodes pour la production de carbonate de sodium et l'électroplacage.
Les conditions du processus de placage pour l'alliage proposé par Kamada et al. sont présentées dans le tableau 3-10.
Tableau 3-10 Conditions de procédé de galvanoplastie de l'alliage Pt-Ir
| Conditions de composition et de procédé | N° 1 | N° 2 |
|---|---|---|
|
hexachlorure de sodium et d'iridium acide borique malonate disodique tétrachloroplatinate de sodium Oxalate de potassium tétrabromoplatinate de sodium pH Température Densité de courant |
10 g/L 40 g/L 0,02 mol/L 0,5 à 3 g/L - - 5 85℃ 0,5 A/dm2 |
10 g/L 40 g/L - - 0,02 mol/L 0,5 à 3 g/L 2 85℃ 0,5 A/dm2 |
Le procédé de galvanoplastie consiste d'abord à déposer par évaporation une couche d'or de 1 µm sur une feuille de laiton, puis à retirer l'or par un autre dépôt, et enfin à déposer un alliage Pt-Ir. Le revêtement ainsi obtenu présente une bonne dureté, une bonne adhérence, une bonne résistance à la chaleur et une excellente connectivité pour les connexions filaires métalliques, avec un rendement de courant atteignant 1001 TP3T.
Concernant cette solution de placage, si le pH est trop bas, la densité de courant est insuffisante pour une utilisation pratique ; si le pH est trop élevé, des précipités d'hydroxyde se forment facilement. Si la température est trop basse, le dépôt de l'alliage est difficile ; si la température est trop élevée, la solution de placage s'évapore rapidement, ce qui nuit à sa conservation. Si la densité de courant est trop faible, la vitesse de dépôt est trop lente ; si elle est trop élevée, la réaction cathodique conduit principalement à un dégagement d'hydrogène.
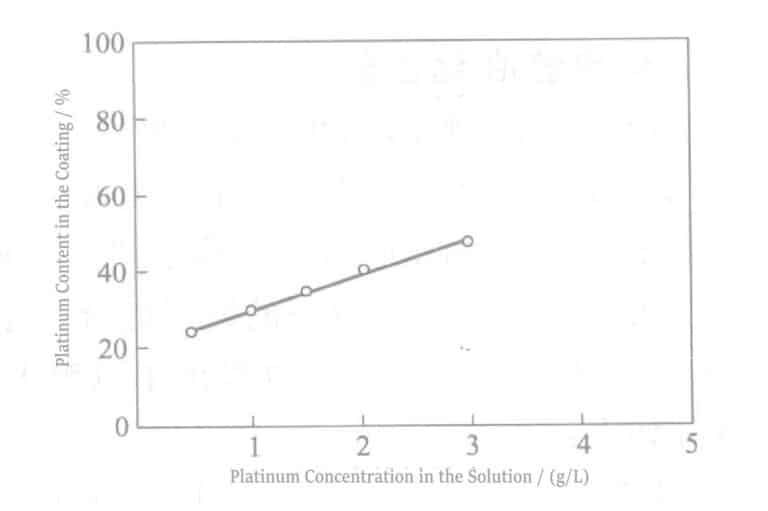
Parallèlement, la composition de l'alliage dans le film de placage peut également être contrôlée en ajustant le rapport de concentration métallique dans la solution de placage. La figure 3-1 illustre la variation de la composition du revêtement d'alliage en fonction du rapport de concentration métallique dans la solution de placage.
Comme on peut le constater sur la figure, dans la plage de concentration expérimentale, le rapport de composition Pt-Ir dans la couche de placage a une relation linéaire avec le rapport de concentration des ions métalliques dans la solution de placage.
(2) Galvanoplastie d'alliage platine-fer
Les alliages contenant du fer sont généralement utilisés comme matériaux magnétiques. Plus la densité d'enregistrement est élevée, meilleures sont les performances. Les alliages platine-fer présentent une forte anisotropie magnétique, une bonne résistance à la corrosion et à l'usure, et devraient améliorer les performances des films magnétiques.
Katsutsugu Koda a proposé une formule de solution de placage présentant une bonne stabilité et permettant un dépôt électrolytique continu. Les ions ferreux (fer trivalents) présents dans la solution de placage ont tendance à former des gels, ce qui nuit à l'aspect de la couche déposée et réduit la concentration de fer divalent, affectant ainsi la stabilité de la solution. Le fer trivalent est généré selon la réaction suivante :
Pt4+ + 2e–→ Pt2+
2Fe2+ → 2Fe3+ + 2e–
D'après la formule ci-dessus, et compte tenu de la stabilité des ions ferreux, les ions platine tétravalents ont un effet négatif, ce qui a conduit à l'invention du platine divalent pour remplacer le platine tétravalent. La pratique a démontré que le platine divalent peut être utilisé en électrodéposition.
Le tableau 3-11 présente les conditions de procédé et les résultats de l'électrodéposition d'un alliage binaire Pt-Fe. On constate que le rapport atomique des métaux dans le revêtement d'alliage Pt-Fe obtenu pour les échantillons n° 1 à n° 3 est proche de la valeur optimale. Un rapport atomique de 50:1Pt:3T est optimal pour la réalisation de films magnétiques destinés à l'enregistrement.
Tableau 3-11 Conditions de procédé pour le placage d'alliage binaire Pt-Fe et leurs résultats
| Conditions de composition et de procédé | N° 1 | N° 2 | N° 3 | N° 4 | N° 5 | |
|---|---|---|---|---|---|---|
| sel de platine | Type | Pt(NH3)2(NON2)2 | [Pt(NH3)4]Cl2 | Pt(NH3)2(NON2)2 | Pt(NH3)2(NON2)2 | Na[Pt(C2O4)2 |
| Contenu | 5 g/L | 5 g/L | 5 g/L | 5 g/L | 10 g/L | |
| sel de fer | Type | FeSO4 • 7H2O | FeSO4 • 7H2O | FeSO4 • 7H2O | FeSO4 • 7H2O | FeSO4 • 7H2O |
| Contenu | 2 g/L | 30 g/L | 30 g/L | 10 g/L | 20 g/L | |
| Antioxydants | Type | sulfite de sodium | chlorure d'hydroxyammoniacal | Acide L-ascorbique | hydrate d'acide citrique | sulfate d'hydroxyammoniacal |
| Contenu | 5 g/L | 3 g/L | 3 g/L | 40 g/L | 50 g/L | |
| agent complexant | Type | citrate de triammonium | EDTA-2Na | citrate de triammonium | EDTA-2Na | oxalate de sodium |
| Contenu | 50 g/L | 10 g/L | 15 g/L | 2 g/L | 30 g/L | |
| Additifs | Type | - | phosphate dihydrogéné de potassium | phosphate dihydrogéné de potassium | Phosphate d'ascorbyle de potassium | - |
| Contenu | - | 15 g/L | 15 g/L | 5 g/L | - | |
| Température de la solution de placage | 40℃ | 30℃ | 60℃ | 50℃ | 70℃ | |
| pH | 8 | 2 | 3 | 4 | 8 | |
| Densité de courant | 1A/dm2 | 2A/dm2 | 1A/dm2 | 1A/dm2 | 1,5 A/dm2 | |
| Composition du placage (atomisation) | Pt | 51% | 49% | 55% | 72% | 37% |
| Fe | 49% | 51% | 45% | 28% | 63% | |
| Aspect de la couche plaquée | O | O | O | O | O | |
(3) Électroplacage d'alliage platine-cobalt
Le film d'alliage Pt-Co présente une densité d'enregistrement magnétique très élevée, ce qui est particulièrement intéressant pour les supports d'enregistrement magnétique de grande capacité. Ses performances sont optimales lorsque son rapport atomique est de 1:1.
Koda a également étudié les alliages Pt-Co (voir tableau 3-12).
Tableau 3-12 Conditions de procédé et résultats du placage d'alliage binaire Pt-Co
| Conditions de composition et de procédé | N° 1 | N° 2 | N° 3 | N° 4 | N° 5 | |
|---|---|---|---|---|---|---|
| sel de platine | Type | Pt(NH3)2(NON2)2 | [Pt(NH3)4]Cl2 | Pt(NH3)2(NON2)2 | Pt(NH3)2(NON2)2 | Na[Pt(C2O4)2 |
| Contenu | 2 g/L | 5 g/L | 5 g/L | 2 g/L | 10 g/L | |
| sel de fer | Type | CoSO4 • 7H2O | CoSO4 • 7H2O | CoSO4 • 7H2O | CoSO4 • 7H2O | CoSO4 • 7H2O |
| Contenu | 30 g/L | 30 g/L | 2 g/L | 45 g/L | 20 g/L | |
| Tampon(1) | Type | EDTA-2Na | citrate de triammonium | citrate de triammonium | acide borique | oxalate d'ammonium |
| Contenu | 30 g/L | 5 g/L | 50 g/L | 30 g/L | 30 g/L | |
| Tampon(2) | Type | citrate de triammonium | - | - | EDTA-2Na | - |
| Contenu | 5 g/L | - | - | 2 g/L | - | |
| sel conducteur | Type | acide sulfamique | sulfate d'ammonium | sulfate d'ammonium | acide sulfamique | sulfate d'ammonium |
| Contenu | 15 g/L | 15 g/L | 15 g/L | 20 ml/L | 15 g/L | |
| Antiprécipitant | Type | - | Ammoniac | - | - | - |
| Contenu | - | 3 g/L | - | - | - | |
| Température de la solution de placage | 60℃ | 50℃ | 40℃ | 50℃ | 70℃ | |
| pH | 3 | 2 | 4 | 3 | 4 | |
| Densité de courant | 1A/dm2 | 2A/dm2 | 4A/dm2 | 3A/dm2 | 4A/dm2 | |
| Composition du placage (atomisation) | Pt | 65% | 49% | 30% | 40% | 37% |
| Fe | 35% | 51% | 70% | 60% | 63% | |
| Aspect de la couche plaquée | O | O | O | O | O | |
Le rapport atomique de l'alliage du revêtement obtenu à partir du n° 2 du tableau 3-11 est d'environ 50%.
Hu Zhongmin et al. ont également proposé une formule d'alliage Pt-Co pour le placage. Ses principaux composants sont les suivants :
|
Pt(NH3)2(NON2)2 (sous forme de Co) 0,2 à 15 g/L CoSO4 (sous forme de cobalt) 5 à 70 g/L (Maintenir Co:Pt = 30:1) |
|
pH 1,2 (ajusté avec NH₄⁺)2SO3H) Température 70℃ Densité de courant 2A/dm2
|
(4) Alliage platine-rhodium
Le revêtement en alliage Pt-W présentant une capacité catalytique d'oxydation supérieure à celle du platine, l'intérêt pour le placage en alliage Pt-W s'est accru. Matsunori Sawada et al. ont proposé une formule d'alliage platine-tungstène permettant d'obtenir un aspect uniforme, une bonne capacité catalytique et une bonne stabilité de la solution de placage.
On obtient une solution de placage stable en ajoutant des acides organiques ou des sels d'acides organiques aux composants principaux, puis en laissant vieillir le mélange.
Les acides organiques utilisés peuvent être l'acide acétique, l'acide citrique, l'acide oxalique, l'acide tartrique, etc. Les composants et concentrations représentatifs sont les suivants :
H2PtCl4 2 g/L (en Pt)
Na2WO4 • 2H2O 25 g/L (en poids)
Citrate de sodium 5 g/L
Acide citrique 5 g/L
sulfate de sodium 15 g/L
Conditions de vieillissement : 60 °C × 8 h
Conditions de placage : 65 °C, 6 mA/cm²2 , 10 min
Matériau de placage : treillis métallique en acier inoxydable d'un diamètre de 0,3 mm
Les traitements de pré-placage sont :
Dégraissage électrolytique → Rinçage à l'eau → Trempage dans l'acide chlorhydrique → Rinçage à l'eau → Placage or flash → Trempage dans l'acide sulfurique → Rinçage à l'eau → Galvanoplastie d'alliage Pt-W
Supposons qu'aucun traitement de vieillissement ne soit appliqué et que le dépôt soit effectué immédiatement à l'aide de la solution de placage préparée. Dans ce cas, le co-dépôt de tungstène sera instable, d'autant plus que le dépôt initial sera faible. La solution de placage se stabilisera progressivement avec l'utilisation, et le co-dépôt de tungstène augmentera. Une couche de placage stable contenant du tungstène peut être obtenue si le traitement de vieillissement décrit ci-dessus est appliqué.
(5) Galvanoplastie d'un alliage platine-nickel
Hu Zhongmin a proposé les principaux composants de la formule de l'alliage Pt-Co pour électroplacage comme suit :
(5) Galvanoplastie d'un alliage platine-nickel
Hu Zhongmin a proposé les principaux composants de la formule de l'alliage Pt-Co pour électroplacage comme suit :
|
Pt(NH3)2(NON2)2 (sous forme de Pt) 0,2 à 15 g/L sulfamate de nickel (exprimé en Ni) 5 à 70 g/L (maintenir Ni:Pt=30:1) Acide sulfamique en quantité suffisante |
|
pH 1~1,4 (ajusté avec de l'acide sulfamique) Température 70°C Densité de courant 2A/dm2 |
Section IV Placage chimique du platine
Outre son utilisation en joaillerie, en catalyse et dans les matériaux réfractaires, le platine peut également servir d'électrode en couche mince pour les composants semi-conducteurs. L'obtention de couches minces de platine par dépôt chimique est une approche récente. Les agents réducteurs sont généralement l'hydrazine ou l'hydrate d'hydrazine ; l'hypophosphite est parfois utilisé.
Raitian raffine les sels de platine en faisant passer du dioxyde de carbone dans une solution de complexe d'hexaammineplatine [Pt(NH₃)₂].3)6(OH)4], provoquant la précipitation du sel de platine et permettant une électroplacage du platine stable et rapide.
La méthode de raffinage spécifique consiste à faire passer du dioxyde de carbone dans une solution de complexe d'hexaammineplatine [Pt(NH₃)₂]⁺.3)6(OH)4On laisse reposer pendant environ 3 heures pour obtenir un précipité de sel de platine. Ce précipité est ensuite filtré, lavé et séché, puis le carbonate est dissous dans un acide organique afin d'obtenir un sel de platine raffiné pour la galvanoplastie. L'utilisation de sels organiques permet d'éviter la contamination par des ions inorganiques. Les ions halogénures ont tendance à s'adsorber sur les pièces à plaquer, ce qui réduit la vitesse de dépôt et provoque un noircissement du film de platine. La présence d'ions sulfate et nitrate peut également engendrer des problèmes d'aspect. Les acides organiques utilisés sont des acides sulfoniques, tels que l'acide méthanesulfonique ou l'acide éthanesulfonique, ou des acides carboxyliques organiques de faible masse moléculaire, tels que l'acide acétique ou l'acide propionique.
Pour faciliter la volatilisation et l'élimination du dioxyde de carbone, la solution peut être maintenue sous pression réduite lors de la dissolution du précipité de carbonate de platine avec un acide organique.
Solution de placage et conditions de traitement :
Pt(NH3)6(CH3COO)4 (sous forme de Pt dissous dans l'acide acétique) 3 g/L
Hydrate d'hydrazine 3 mL/L
Ester de glycérol (agent de nivellement) 20×10-6
pH (ajusté avec de l'ammoniaque) 11
Température 60℃
Pièces plaquées Plaque d'oxyde d'aluminium (activée)
Vitesse de dépôt : 1,8 µm/h
L'agent de nivellement peut être du polyoxyéthylène dodécyl éther, et l'agent réducteur peut être remplacé par de l'hypophosphite.
Utilisant également l'hydrate d'hydrazine comme agent réducteur, la formule de Koslov Alexander est la suivante :
Pt(NH3)2(NON2)2 (sous forme de Pt) 2 g/L
Hydrate d'hydrazine (agent réducteur) 3 g/L
NH2OH – HC1 (stabilisant) Quantité adéquate
pH (ajusté avec de l'acide acétique) 3
Température 50℃
Vitesse de dépôt : 0,1 µm/h
Tableau 3-13 Essai de placage chimique Pt
| Objet | Test 1 | Test 2 | Test 3 |
|---|---|---|---|
| Caractéristiques du test | La membrane échangeuse d'ions imprégnée de 5% (NH4)4PtCl2 La solution a été placée dans une solution de 1 g/L d'hydroborure de sodium + 1 mg/L de carbonate de magnésium à 50 °C pendant 1 h. | Membrane échangeuse d'ions imprégnée de 5% (NH4)4PtCl2 La solution a été placée dans une solution de 1 g/L d'hydroborure de sodium + 10 mg/L de sulfate de magnésium à 30 °C pendant 1 h. |
HPtCl4 1 g/L Hydroborure de sodium 1 g/L Carbonate de calcium 10 ml/L 80 °C, 1 h Réaction de la plaque d'aluminium dans la solution ci-dessus par immersion |
| Matériau de base | membrane échangeuse de cations | membrane échangeuse de cations | plaque d'aluminium |
| Épaisseur du platine | 0,1 mm | 0,1 mm | 0,1 mm |
| diamètre des particules de platine | En dessous de 10 μm | En dessous de 10 μm | En dessous de 10 μm |
| résistance de surface | 10Ω/cm | 10Ω/cm | 10Ω/cm |
Cette réaction nécessite des métaux alcalino-terreux ; ceux-ci peuvent se dissoudre avec l’agent réducteur (comme dans les expériences 1 et 2) ou être ajoutés à la solution de placage (comme dans l’expérience 3). Cependant, leur mécanisme d’action reste mal compris. Plus la couche de placage est compacte, moins elle présente de défauts, tels que des fissures, ce qui garantit une résistance relativement faible et, par conséquent, la qualité de l’électrode.
Kenji Takahashi a proposé un procédé de placage chimique utilisant un sel d'ammonium de platine tétravalent comme sel principal. La formule générale de ce sel de platine est [Pt(NH₄)₂]⁺.3)6X. Dans cette formule, X peut être un ion halogénure, OH⁻.– groupe, SO42-, etc.
Sa composition est :
Sel de platine (sel d'ammonium platine tétravalent) (en platine) 0, 5〜5,0 g/L
Ammoniac (28%) 10〜100 g/L
Eau et hydrazine (agent réducteur) 0,5 à 5 g/L
pH 10 à 12,5
Température de la solution de placage : 50 à 70 °C