Cómo mejorar sus joyas con técnicas de tratamiento de superficies
Dominio de los tratamientos superficiales para joyería: Del pulido a la nanopulverización
El proceso de tratamiento de superficies de joyería es un tratamiento técnico que utiliza diversos métodos, como físicos, químicos, electroquímicos y mecánicos, para cambiar la textura, el color y el tacto de la superficie del accesorio, evitar la corrosión, embellecer la decoración y prolongar su vida útil. Enriquece enormemente el efecto decorativo de los productos accesorios, amplía los medios disponibles para el diseño de accesorios, presenta un estilo más vibrante y diverso para la joyería y ofrece a los consumidores opciones más personalizadas. Mejora significativamente el efecto superficial, la vida útil y el valor añadido económico de los accesorios.
Existen muchos tipos de procesos de tratamiento de superficies para la joyería moderna popular, siendo los métodos más utilizados principalmente el pulido, la galvanoplastia, el chapado químico, las películas de conversión electroquímica química, la deposición física de vapor, el esmalte, la resina epoxi y la nano pulverización de superficies.

Opciones de color del chapado
Índice
Sección I Tecnología de pulido
1. Pulido mecánico
El pulido mecánico consiste en tratar la superficie de las joyas utilizando maquinaria de pulido y medios abrasivos. Los métodos habituales de pulido mecánico incluyen las siguientes categorías.
(1) Muela de tela para pulir
El pulido con rueda de tela se realiza con una rueda de pulido montada en una máquina. La pasta de pulido se aplica periódicamente a la superficie de trabajo de la rueda de pulido. Por el contrario, la superficie de la pieza que se está procesando se presiona con fuerza contra la superficie de trabajo de la rueda de pulido, que se encuentra en un estado de rotación a alta velocidad. Con la ayuda de las fibras de la rueda de pulido y la pasta de pulido, la superficie de la pieza que se está procesando consigue un aspecto de espejo (Figura 11-1). Actualmente se cree que el principio de las pulidoras de rueda de tela es que la alta temperatura generada por la fricción entre la rueda de pulido que gira a alta velocidad y la superficie de la pieza que se está procesando puede causar la deformación plástica de la superficie de la pieza, rellenando los huecos microscópicos en la superficie de la pieza que se está procesando; al mismo tiempo, la alta temperatura generada durante el pulido también puede formar rápidamente una capa muy fina de película de óxido en la superficie de la pieza que se está procesando. La superficie expuesta del sustrato se oxida de nuevo al eliminar esta capa de película de óxido. El proceso continúa en este ciclo hasta que se completa el pulido, lo que da como resultado una superficie plana y lisa.
(2) Pulido por vibración
Se instala con un motor vibratorio en el disco vibratorio de la pulidora vibratoria, y el disco vibratorio se conecta a la base mediante muelles vibratorios. Cuando se pone en marcha la pulidora vibratoria, el motor vibratorio genera una fuerte fuerza de excitación, impulsando los medios de molienda en el disco vibratorio para producir un movimiento en tres direcciones: vibración vertical, volteo de adentro hacia afuera y rotación en espiral en el sentido de las agujas del reloj, creando así un efecto de molienda en la superficie de la joya para lograr un acabado pulido (Figura 11-2 ).

Figura 11-1 Pulido con disco de tela

Figura 11-2 Pulido por vibración
(3) Pulido con rodillo
Su principio de funcionamiento es el siguiente: Cuatro rodillos hexagonales están montados uniformemente en la circunferencia del cuerpo giratorio. Los rodillos giran con el cuerpo giratorio a la vez que giran alrededor de su eje bajo la acción del sistema de ruedas dentadas (en sentido contrario). El movimiento planetario de los rodillos hace que, debido a la fuerza centrífuga, el material que se encuentra en su interior permanezca siempre en un lado de la pared exterior de los rodillos, creando una capa de flujo en la superficie. Dentro de esta capa de flujo, las piedras de esmerilado y las piezas generan un movimiento relativo, realizando un corte fino y presionando sobre la superficie de la pieza, consiguiendo así una superficie pulida en la pieza (Figura 11-3).
(4) Pulido vórtex
Su principio de funcionamiento es: utilizando la fuerza centrífuga generada por la rotación a alta velocidad de la plataforma giratoria inferior, se produce una fuerte fricción entre la pieza de trabajo y el abrasivo bajo la acción de una ranura fija, formando una operación de vórtice en espiral, provocando una fricción rotacional a alta velocidad y un volteo en espiral de la pieza de trabajo y el abrasivo. Esto permite eliminar las rebabas de las joyas pulidas y pulirlas uniformemente en muy poco tiempo, consiguiendo un efecto de pulido ideal. La base de la pulidora es un disco giratorio dentro de un contenedor, con la parte superior del contenedor abierta y las paredes del contenedor sin girar. La separación entre el recipiente y el disco puede ser inferior a 0,05 mm, lo que permite utilizar las partículas de cáscara de nuez más finas (Figura 11-4).

Figura 11-3 Pulido con rodillo

Figura 11-4 Pulido Vortex
(5) Pulido por arrastre
Al trabajar, la pieza se arrastra sobre el medio de pulido mientras no se mueve. Cada pieza de trabajo tiene su propia posición de apoyo, las superficies entre las piezas de trabajo no entrarán en contacto, evitando así daños en la superficie. En comparación con los métodos de pulido tradicionales, crea un mayor movimiento relativo y una mayor fuerza de procesamiento, reduciendo significativamente el tiempo de procesamiento. Tiene grandes ventajas para piezas de trabajo pesadas. El método de pulido por arrastre es especialmente adecuado para anillos pesados, cierres y cajas de reloj, y también para muchas otras piezas de trabajo que pueden suspenderse en soportes fijos (Figura 11-5).

Tabla 11-1 Características de los distintos procesos de pulido
| Métodos de pulido | Medio de pulido | Medio de molienda | Ventajas | Desventajas | Pieza adecuada |
|---|---|---|---|---|---|
| Pulido por vibración | Virutas de madera, trozos de porcelana, partículas de cáscara de nuez, harina de maíz, bolas de acero | Cerámica, plástico | Artículos baratos, grandes, piezas estampadas | Con el largo tiempo de procesamiento, la baja presión, las hendiduras y el escaso efecto de alisado, es imposible lograr resultados ideales durante el procesamiento en seco. | Cadena pequeña, cadena mecánica |
| Pulido de cañones | Cubo de madera, aguja de madera, partículas de cáscara de nuez, harina de maíz, bola de acero | Cerámica, plástico | Barato | Largo tiempo de procesamiento, procesamiento inconveniente, la superficie tiene polvo, la superficie está prensada | Diversas piezas de joyería |
| Pulido vórtex | Partículas de cáscara de nuez, trozos de porcelana, plástico | Cerámica, plástico | Con alta eficiencia y corto tiempo de procesamiento, la máquina completa la carga de trabajo 70%, menos procesos, joyas limpias, fácil manejo, alta calidad de la superficie. | Sólo puede manipular piezas ligeras (20 g como máximo) y no puede procesar engastes de piedras preciosas de cadena pequeña. | La mayoría de las joyas, productos industriales y cajas de relojes |
| Pulido de arrastre | Partículas de cáscara de nuez | Gránulo de cáscara de nuez | Puede pulir piezas grandes y pesadas sin impactos ni colisiones, con un tiempo de procesamiento corto, un manejo sencillo y una alta calidad de superficie. | Sin molienda húmeda | Varias piezas de joyería que se pueden fijar en un estante |
2. Pulido químico
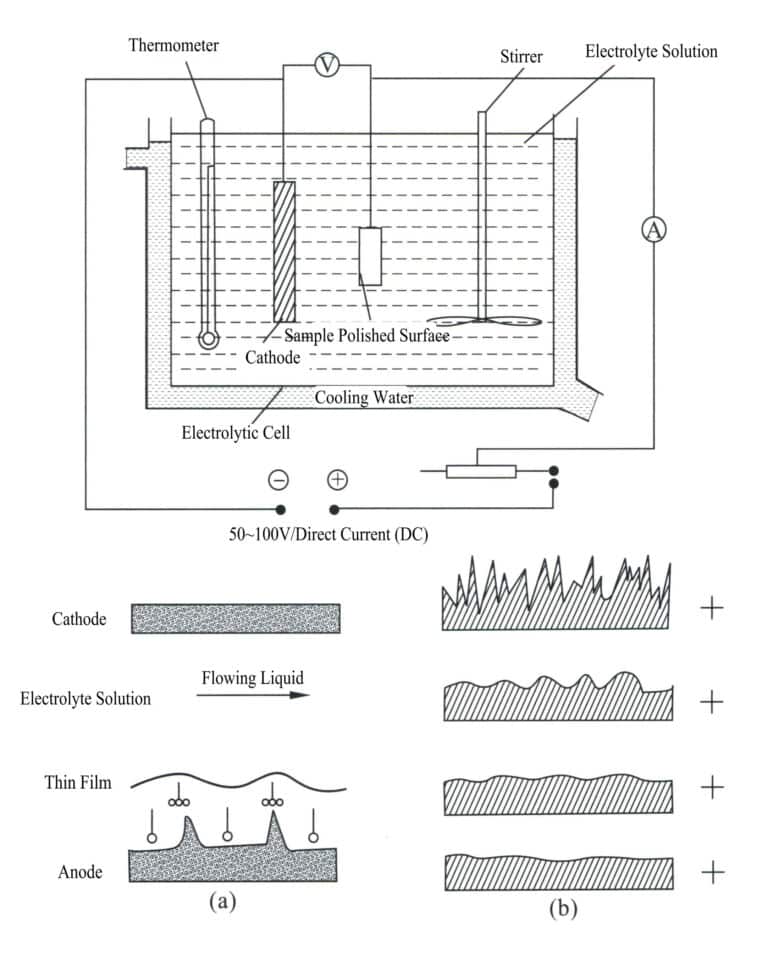
3. Pulido electroquímico
Sección II Proceso de galvanoplastia
1. Conocimientos básicos de galvanoplastia para joyería
(1) Tipos de galvanoplastia para joyería
Según la finalidad del revestimiento, la galvanoplastia para joyería puede dividirse en revestimientos protectores y revestimientos decorativos.
- Recubrimientos protectores. El objetivo principal es evitar la corrosión del metal. Pertenecen a esta categoría los revestimientos de uso común, como las capas galvanizadas y de estaño. Los metales negros suelen protegerse con capas galvanizadas en condiciones atmosféricas generales, mientras que las capas de estaño se utilizan generalmente para proteger metales negros que entran en contacto con ácidos orgánicos.
- Revestimientos decorativos. Principalmente con fines decorativos, pero también con un cierto nivel de protección. Los revestimientos compuestos suelen formar varias capas, ya que es difícil encontrar un único revestimiento que cumpla los requisitos de los revestimientos decorativos. Normalmente, primero se aplica una capa base sobre el sustrato, seguida de una capa superficial y, a veces, también se aplica una capa intermedia. Por ejemplo, la galvanoplastia de metales preciosos y la galvanoplastia de imitación de oro se utilizan ampliamente, sobre todo en algunas joyas valiosas y pequeñas joyas de ferretería, con un uso y un volumen de producción relativamente altos. Se trata principalmente de metales preciosos electrodepositados y diversas aleaciones.
Según la relación electroquímica entre el revestimiento y el metal del sustrato durante la corrosión, la galvanoplastia decorativa puede dividirse en revestimientos anódicos y catódicos.
- Revestimiento anódico. Se refiere al revestimiento que actúa como ánodo y se disuelve primero cuando se forma una microbatería de corrosión con el metal del sustrato, como el cincado sobre hierro. Este tipo de revestimiento no sólo proporciona protección mecánica al sustrato, sino que también ofrece protección química.
- Revestimiento catódico. Se refiere al revestimiento que actúa como cátodo cuando forma una microbatería de corrosión con el metal del sustrato. Por ejemplo, el estañado sobre hierro. Este tipo de revestimiento sólo puede proporcionar protección mecánica al sustrato; una vez que el revestimiento se daña, deja de proteger el sustrato y acelera su velocidad de corrosión.
(2) El proceso básico de la galvanoplastia metálica
La electrodeposición es un proceso electroquímico y redox. Durante la electrodeposición, el componente metálico actúa como cátodo, el metal o aleación a recubrir actúa como ánodo soluble o se utiliza una malla de titanio como ánodo insoluble, conectada a los terminales negativo y positivo de la fuente de alimentación, y sumergida en un electrolito que contiene los componentes del recubrimiento. Bajo la acción de la corriente, puede obtenerse una capa de deposición en la superficie del ornamento (Figura 11-7).
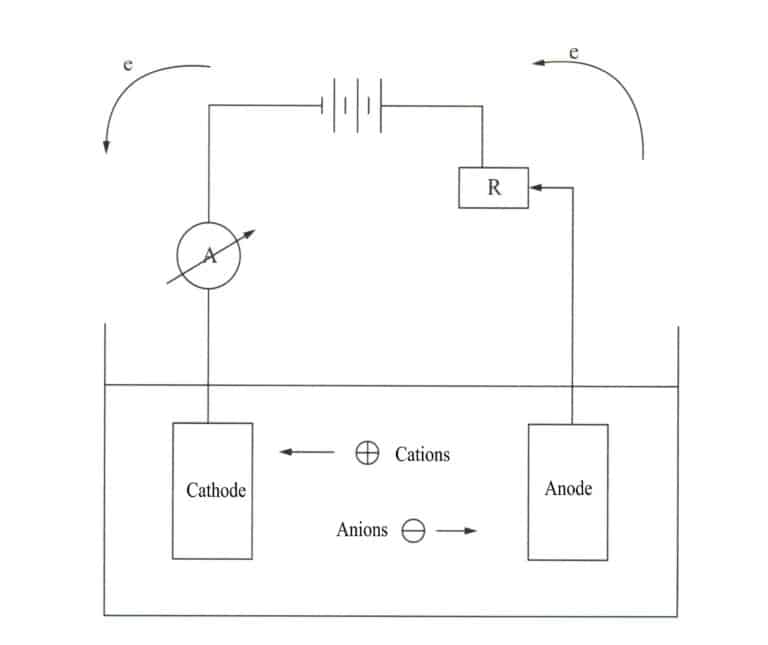
El proceso de galvanoplastia reduce el metal o sus iones complejos a metal en el cátodo. Dado que el metal chapado tiene una estructura cristalina como los metales ordinarios, el proceso de galvanoplastia también se conoce como proceso de electrocristalización. Incluye los tres pasos siguientes.
- Proceso de transferencia de masa. Los iones metálicos o los iones de complejos metálicos son transportados continuamente a la superficie del electrodo desde el electrolito a través de pasos como la difusión, la convección y la electromigración.
- Proceso electroquímico. Los iones metálicos o los iones de complejos metálicos se deshidratan y adsorben en la superficie del cátodo para liberar electricidad y reducirse a átomos metálicos.
- Proceso de cristalización. Los átomos metálicos se disponen en el cátodo para formar cristales metálicos de una forma determinada, y la cristalización suele producirse por nucleación y crecimiento.
La finura de los cristales viene determinada por la velocidad de nucleación y la velocidad de crecimiento. Si la tasa de nucleación es más rápida que la de crecimiento, se producirán más cristales, lo que dará lugar a granos más finos y densos; a la inversa, los granos serán más gruesos.
2. Cobre electrodepositado y aleaciones de cobre
El cobreado es rosado, uniforme y delicado, con distintas tonalidades según el proceso. En galvanoplastia, el cobreado se utiliza ampliamente, principalmente como capa base y capa intermedia, y también puede utilizarse como capa superficial, como el chapado en oro de imitación.
Los procesos de revestimiento de cobre utilizados actualmente incluyen principalmente el revestimiento de cobre con cianuro, sulfato ácido y pirofosfato. Entre ellos, la solución de revestimiento de cobre con cianuro es muy tóxica, contamina gravemente el medio ambiente, perjudica la salud humana y se ha incluido en la lista de procesos que deben eliminarse. Además, en los últimos años también se han desarrollado y aplicado el cobreado con aminosulfonato, el cobreado con aminas orgánicas, el cobreado con citrato-tartrato y el cobreado con HEDP.
En los años 70, la investigación se centró en sustituir la galvanoplastia con cianuro por la galvanoplastia sin cianuro, lo que dio lugar a la galvanoplastia de cobre con pirofosfato y sulfato. Sin embargo, no podían aplicarse directamente sobre sustratos de acero como capa base.
2.1 Cobreado con sulfato
La galvanoplastia de cobre con sulfato se utiliza ampliamente en la galvanoplastia decorativa de protección, la galvanoplastia de plásticos y la galvanoplastia gruesa de cobre para la electroformación de placas de circuitos impresos. Se puede dividir en dos tipos: uno es una solución de revestimiento de alto contenido en cobre y bajo contenido en ácido que se utiliza para la galvanoplastia de piezas, que tiene un revestimiento liso y brillante con buena tenacidad; el otro es una solución de revestimiento de alto contenido en ácido y bajo contenido en cobre que se utiliza para la galvanoplastia de placas de circuitos impresos, que tiene una excelente capacidad de dispersión y cobertura, por lo que es muy adecuada para el revestimiento de orificios, con un revestimiento uniforme y delicado.
(1) Componentes principales de la solución de revestimiento
① Sulfato de cobre. Es la sal principal que proporciona el Cu2+ para la electrodeposición. Si la concentración es demasiado baja, se reducirá el límite superior de la densidad de corriente, disminuirá la velocidad de deposición y se verá afectado el brillo del revestimiento. Cuando la concentración es demasiado alta, se reducirá la capacidad de dispersión de la solución de revestimiento, y debido al límite de solubilidad del sulfato de cobre, se precipitarán cristales de sulfato de cobre, siendo apropiado 180~220g/L.
② Ácido sulfúrico. Su función principal es aumentar la conductividad de la solución. Cuando la concentración es demasiado baja, provoca una oxidación incompleta del cobre del ánodo, produciendo Cu2O, lo que produce "polvo de cobre" o rebabas en el revestimiento. Al mismo tiempo, disminuye la capacidad de dispersión de la solución de revestimiento. Cuando la concentración de ácido sulfúrico es adecuada, el rango de densidad de corriente del revestimiento es amplio, el revestimiento es brillante y la capacidad de nivelación alcanza resultados óptimos. Si la concentración de ácido sulfúrico es demasiado alta, afecta al brillo y a la nivelación del revestimiento.
③ Iones cloruro. Son activadores anódicos que pueden ayudar a que el ánodo se disuelva normalmente, inhibir la producción de Cu+Si la concentración de iones de cloruro es demasiado baja, se forman revestimientos dendríticos. Si la concentración de iones cloruro es demasiado baja, se forman revestimientos dendríticos, con la zona de alta corriente propensa a quemarse, y es probable que el revestimiento desarrolle picaduras o agujeros de alfiler. Si la concentración de iones cloruro es demasiado alta, aparece una capa de película blanca gelatinosa en la superficie del ánodo y, por mucho abrillantador que se añada, el revestimiento no será brillante. La concentración adecuada de iones cloruro es de 40~100ml/L.
④ Aditivos. Una excelente combinación de aditivos puede producir soluciones de metalizado estables, altos índices de cualificación del producto y una gran eficacia de trabajo. En la actualidad, se han comercializado muchos aditivos y sus materiales. Los requisitos de los aditivos varían en función del tipo de revestimiento. Por ejemplo, los recubrimientos decorativos ponen más énfasis en el brillo, la velocidad y la nivelación del recubrimiento; los recubrimientos decorativos protectores se centran más en la nivelación y la flexibilidad del recubrimiento; los recubrimientos de placas de circuitos requieren un excelente rendimiento en la zona de baja corriente, una distribución uniforme del recubrimiento y ductilidad del recubrimiento, entre otros. Los aditivos de cobreado constan principalmente de cuatro partes: portadores, abrillantadores, agentes niveladores y agentes humectantes.
- Transportista: Un buen portador puede maximizar la eficacia de los agentes abrillantadores y niveladores. Los portadores se formulan principalmente a partir de tensioactivos, y es imposible conseguir el mejor efecto con un solo material, como los compuestos de poliéter, los compuestos aniónicos tetraéter de etilendiamina, etc.
- Agentes abrillantadores y niveladores: Los compuestos orgánicos de polisulfuro, los polisulfuros orgánicos, los sulfonatos orgánicos de polisulfuro, los tintes orgánicos, etc., tienen efectos abrillantadores y niveladores en combinación con portadores. Ambos efectos pueden aparecer en el mismo material, centrándose los colorantes más en la capacidad de nivelación.
- Humectantes: pueden mejorar la acción humectante de la solución de revestimiento. Se suelen utilizar tensioactivos no iónicos o aniónicos, como polietilenglicol, emulgentes OP, etc. El cobre ácido brillante utiliza agitación por aire y sólo puede elegir agentes humectantes de baja espuma.
(2) Reacción del electrodo de cobreado con ácido sulfúrico
Cátodo: Cu2+ + 2e=Cu φ0Cu2+/Cu = +0.34V
Cu2+ + e=Cu+ φ0Cu2+/Cu+ = +0.17V
Cu+ + e=Cu φ0Cu+/Cu = +0.51V
Debido al potencial de electrodo estándar del Cu2+ al ser mucho más positivo que el hidrógeno, el gas hidrógeno no se liberará en el cátodo, pero cuando no esté suficientemente reducido, aparecerá Cu+. Desde la perspectiva del potencial de electrodo estándar, es más probable que se produzca la reacción de reducción a Cu, y la reducción de Cu dará lugar a un revestimiento rugoso, que debe evitarse.
Ánodo: El ánodo de cobre en solución de ácido sulfúrico experimenta una disolución anódica, proporcionando los iones de cobre necesarios en la solución de revestimiento, a saber: Cu-2e=Cu2+.
Al mismo tiempo que Cu2+ se genera, se genera inevitablemente Cu+a saber: Cu-e=Cu+. Cuando Cu+ aparece y entra en la solución; si hay suficiente ácido sulfúrico y aire en la solución, Cu+ puede oxidarse, a saber:4Cu++O2+4H+=4Cu2++2H2O, Cuando la concentración de ácido sulfúrico en la solución es insuficiente, Cu+ se hidrolizará, a saber:2Cu++2H2O=2CuOH+2H+=Cu2O+H2O. En este momento, Cu2O se depositará en el cátodo por electroforesis, produciendo rebabas. Debido a la inestabilidad del Cu+también pueden producirse reacciones de desproporción, a saber:2Cu+=Cu2++Cu, y el Cu generado también se depositará en el revestimiento por electroforesis, produciendo polvo de cobre, rebabas y rugosidades. Por lo tanto, durante el proceso de galvanoplastia, la aparición de Cu+ debe evitarse en la medida de lo posible; el uso de ánodos de cobre que contengan fósforo y la agitación de la solución de revestimiento con aire pueden resolver el problema.
2.2 Cobreado con pirofosfato
El cobreado con pirofosfato no puede aplicarse directamente sobre sustratos de hierro y zinc. Se utiliza sobre todo en sustratos de aleación de zinc antes del revestimiento de cobre con sulfato ácido para proteger el sustrato de la corrosión ácida fuerte y garantizar la calidad de la combinación de revestimiento. También se utiliza en procesos de galvanoplastia de metalización de plásticos, pero su aplicación en galvanoplastia de hardware es limitada.
Los cristales brillantes de cobreado con ácido fosfórico tienen una buena capacidad de dispersión y cobertura. La eficiencia de la corriente catódica es alta, pero el uso a largo plazo puede provocar la acumulación de fosfato, lo que reduce la velocidad de deposición.
(1) Componentes principales de la solución de revestimiento
- Pirofosfato de cobre. Es la sal principal de la solución de revestimiento, aportando iones de cobre. Si el contenido de cobre es demasiado bajo, disminuye la densidad de corriente, lo que da lugar a un brillo y nivelación deficientes del revestimiento; si el contenido de cobre es demasiado alto, reducirá la polarización catódica, lo que dará lugar a un revestimiento rugoso. El contenido de cobre en la solución de revestimiento debe mantenerse en una determinada proporción con el pirofosfato potásico.
- Pirofosfato de potasio. Es el principal agente complejante, y cuando el valor de pH es 8, la forma principal del complejo es [Cu(P2O7)2]6-manteniendo [P2O74-]:[Cu2+Si la relación es demasiado grande, se reduce la eficacia de la corriente, se producen agujeros en el revestimiento y la solución de revestimiento tiende a enturbiarse.
- Aminoácido cítrico. Es un agente complejante auxiliar y despolarizador de ánodos. Puede mejorar la disolución del ánodo, aumentar la capacidad de dispersión de la solución de revestimiento e incrementar el brillo del revestimiento. Si el contenido es demasiado bajo, la disolución del ánodo será deficiente, la capacidad de dispersión de la solución de revestimiento disminuirá y se producirá "polvo de cobre". Por lo general, el contenido adecuado es de unos 10~30g/L.
(2) Reacción del electrodo de cobreado con pirofosfato
Reacción catódica:[Cu(P2O7)2]6- + 2e6- = Cu + 2P2O74-
2H2O + e = H2 + 2OH–
Reacción anódica:Cu + 2P2O74- -2e = [Cu(P2O7)2]6-
Cuando el ánodo se pasiva, se libera oxígeno:4OH– - 4e = O2 + 2H2O
Cuando la oxidación anódica es incompleta, el Cu + ocurre: Cu - e = Cu+
Las dos últimas reacciones deben controlarse cuidadosamente para evitar que se produzcan.
2.3 Galvanoplastia de imitación de oro
En los últimos años, debido al desarrollo de la galvanoplastia decorativa en la construcción, la ferretería, la iluminación y los ornamentos, el chapado en oro de imitación se ha utilizado ampliamente.
(1) Principales categorías de galvanoplastia de imitación de oro
El chapado en oro de imitación puede estar hecho de aleaciones de cobre-zinc, cobre-estaño o cobre-estaño-zinc, o el postprocesado de aleaciones de cobre-zinc puede producirlo para crear un efecto de oro realista. El efecto de oro de imitación puede conseguir colores como el oro de 18K, 4K y rosa. Las aleaciones de cobre-estaño (bronce) pueden dividirse en tres categorías en función del contenido de estaño: bronce con bajo contenido de estaño, con un contenido de estaño de 5%~15%, que tiene un aspecto entre rosa y amarillo dorado; bronce con contenido medio de estaño, con un contenido de estaño de 15%~40%, que tiene un aspecto amarillo; y bronce con alto contenido de estaño, con un contenido de estaño de 40%~50%, que tiene un aspecto blanco plateado.
El chapado en oro tiene un tiempo de galvanoplastia muy corto, y su brillo depende principalmente de la capa subyacente como soporte, normalmente chapada en una capa de níquel brillante u otro chapado blanco y brillante. El chapado en latón también puede servir como base de una fina capa decorativa de oro y como capa protectora y lubricante. El latón es propenso a decolorarse con el aire, por lo que debe someterse a un tratamiento antidecoloración cuando se utiliza como capa superficial o base de la capa fina de oro, como rociarlo con un revestimiento orgánico o recubrirlo con pintura electroforética catódica. En los últimos años, para evitar las alergias cutáneas al níquel en el chapado de joyas, se puede utilizar la aleación de cobre-zinc blanco como sustituto de bajo grado del chapado de níquel, y también puede servir de base para el cromo y para los recubrimientos blancos y blancos requeridos en las decoraciones metálicas de juguete.
La clave para obtener una aleación mediante la codeposición simultánea de dos metales es que sus potenciales de deposición deben estar próximos, y la polarización catódica debe garantizar que los dos metales se depositen en la proporción deseada. Los iones complejos presentes en la solución cianurada son principalmente Cu(CN)32- y Zn(CN)42-. La estabilidad de los iones de cianuro de cobre es mucho mayor que la de los iones de cianuro de zinc, y la polarización catódica del cobre es mucho mayor que la del zinc. Por lo tanto, para conseguir un revestimiento que cumpla los requisitos, es necesario controlar estrictamente el cianuro total, el cianuro libre, la relación cobre-zinc, el valor de pH y factores como la temperatura, la densidad de corriente y la agitación.
(2) Flujo del proceso de galvanoplastia de oro de imitación
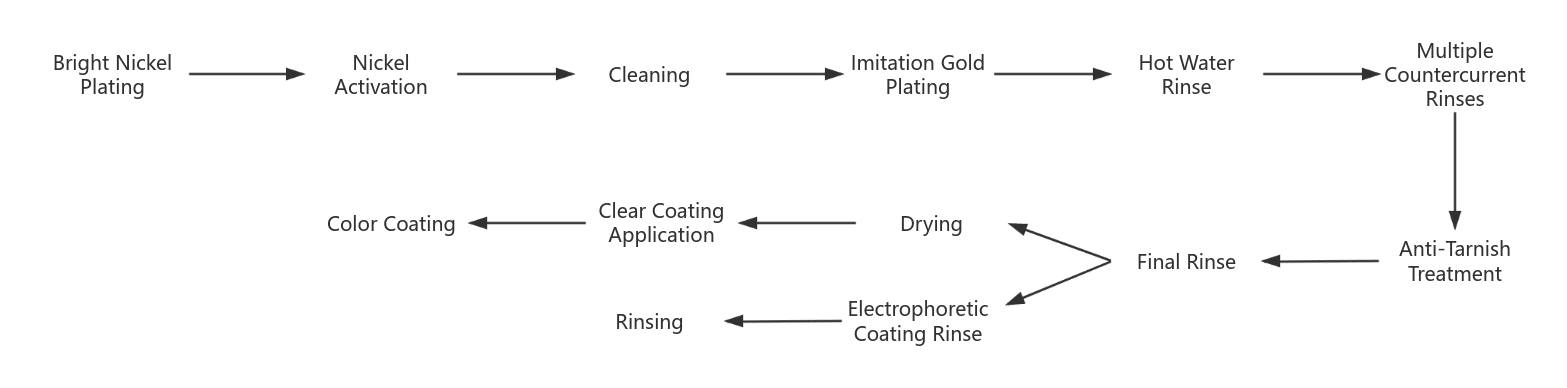
El chapado en oro de imitación de aleación de cobre plantea dos grandes retos: por un lado, cómo mantener el brillo del chapado y evitar la decoloración del chapado de aleación de cobre; por otro, cómo conseguir un efecto realista. Por lo tanto, un proceso de galvanoplastia y un tratamiento posterior razonables resultan cruciales. El proceso de galvanoplastia de imitación de oro más utilizado es el siguiente:
- Antes de recubrir la pieza con níquel brillante, debe someterse a un tratamiento previo. Al final, el niquelado brillante tiene un tono blanquecino, que puede realzar el brillo de la capa de oro de imitación.
- La activación del níquel tiene por objeto eliminar la capa de pasivación de la superficie de níquel brillante para mejorar la fuerza de unión con la capa superficial. El método consiste en el tratamiento catódico en la solución electrodesengrasante durante 3~5 minutos, seguido de la activación con ácido sulfúrico 5% después de aclarar con agua y enjuagar a fondo antes de entrar en el tanque de chapado en oro de imitación.
- Tras el recubrimiento galvánico de imitación de oro, la superficie de la pieza se limpia con agua caliente y se enjuaga con lavado a contracorriente.
- Tratamiento antidecoloración destinado a evitar que el revestimiento se decolore tras el lavado. Entre los procesos de pasivación habituales se encuentran el dicromato potásico o el benzotriazol.
- La electroforesis catódica se trata con pintura de electroforesis catódica de tipo acrílico o con revestimientos transparentes como barniz de tipo acrílico o se rocía o sumerge con revestimientos transparentes de silicona orgánica.
- Barniz o pintura colorante. Para crear un efecto de imitación de oro realista en apariencia y compensar las deficiencias del tono del chapado en oro de imitación, puede aplicarse un revestimiento transparente de color dorado.
3. Níquel galvánico
3.1 Níquel brillante
El níquel brillante es uno de los revestimientos más utilizados en la actualidad. Se basa en el níquel watt, al que se añaden aditivos para conseguir un niquelado brillante y liso.
(1) Componentes principales de la solución de revestimiento
① Níquel. Las fuentes de iones de níquel pueden ser sulfato de níquel, cloruro de níquel, aminosulfonato de níquel, etc. Los iones de níquel son el componente principal de la solución de revestimiento, generalmente con un contenido de 52~70g/L. Una concentración elevada de iones de níquel permite aumentar la densidad de corriente. Mejora la velocidad de deposición, pero si la concentración es demasiado alta, la capacidad de dispersión de la solución de metalizado disminuye, lo que puede provocar que no se produzca metalizado en zonas de baja corriente. Si la concentración de iones de níquel es demasiado baja, la velocidad de deposición disminuye y, en casos graves, la zona de corriente alta puede quemarse.
② Buffer. El ácido bórico es el mejor tampón en la solución de niquelado, y su concentración mínima efectiva no es inferior a 30g/L; generalmente, la toma en la solución de niquelado es apropiadamente de 40~.50g/L. El ácido bórico también puede mejorar la polarización catódica, mejorar la conductividad de la solución y mejorar las propiedades mecánicas del revestimiento.
③ Agentes humectantes. Durante el proceso de galvanoplastia, se libera hidrógeno en el cátodo. Los agentes humectantes pueden reducir la tensión superficial de la solución galvánica, aumentando el efecto humectante de la solución sobre la superficie de la pieza, dificultando que las burbujas de hidrógeno generadas durante la galvanoplastia permanezcan en la superficie del cátodo, evitando así la formación de poros y manchas. Los agentes humectantes se componen de tensioactivos, que pueden clasificarse en agentes humectantes de alta espuma y agentes humectantes de baja espuma. Los agentes humectantes de alta espuma incluyen el dodecil sulfato sódico, mientras que los agentes humectantes de baja espuma incluyen el dietilhexil sulfato sódico.
④ Agentes abrillantadores. Incluidos los agentes abrillantadores primarios, los agentes abrillantadores secundarios y los agentes abrillantadores auxiliares.
- Abrillantador primario: Su función principal es refinar el tamaño de grano y reducir la sensibilidad de la solución de niquelado a las impurezas metálicas, con una dosificación general de aproximadamente 1~10g/L, una capa de niquelado contiene aproximadamente 0,03%S. Los abrillantadores primarios típicos incluyen sacarina, difenil sulfonio amonio (BB1), tolueno sulfonio amonio, ácido bencenosulfónico, ácido 1,3,6 naftaleno sulfónico, ácido benceno sulfónico y ácido benceno sulfónico sódico (BSS), etc.
- Los abrillantadores secundarios crean un brillo notable en el revestimiento, pero también introducen tensión y fragilidad en el revestimiento y sensibilidad a las impurezas. La dosificación debe controlarse estrictamente y, cuando se utilizan junto con abrillantadores primarios, pueden producir un revestimiento totalmente brillante. Entre los abrillantadores secundarios típicos figuran el 1,4-butanodiol, el alcohol propargílico, el hexanol, la piridina, la tiourea, etc.
- Abrillantadores auxiliares: Ayudan a abrillantar el revestimiento, mejoran la capacidad de cobertura del revestimiento y reducen la sensibilidad de la solución de revestimiento a las impurezas metálicas. Los abrillantadores auxiliares típicos incluyen alil sulfonato sódico, vinil sulfonato sódico, propargil sulfonato sódico, etc.
⑤ Aditivos de materias primas niqueladas. Los distintos productos intermedios se combinan en función de sus respectivas características de rendimiento, lo que da lugar a varios tipos.
- Abrillantador de baño (agente suavizante): compuesto principalmente por agentes abrillantadores primarios y auxiliares.
- Agente abrillantador (agente abrillantador principal): Compuesto por uno o más componentes, siendo el principal un agente abrillantador secundario, complementado por otros componentes.
- Tensioactivos: Existen dos tipos: de baja espuma y de alta espuma.
- Agentes de purga: tales como eliminadores de hierro, eliminadores de cobre, eliminadores de zinc, agentes de posicionamiento de zona baja, etc.
(2) Reacción del electrodo
Cátodo: Ni2+ + 2e = Ni 2H+ + 2e = H2
Ánodo: Ni = Ni2+ + 2e 4OH– = 2H2O + O2 + 4e
3.2 Níquel Negro Galvanizado y Gunmetal Satinado
El niquelado negro y gunmetal (perla negra) se utiliza principalmente para revestimientos ópticos y revestimientos decorativos antiguos, generalmente chapados sobre revestimientos brillantes de níquel, cobre, bronce y zinc, con un espesor no superior a 2μm. Este tipo de revestimiento es duro y quebradizo, con escasa resistencia a la corrosión, y la superficie del revestimiento debe protegerse con barniz.
La aparición de los colores negro y bronce de cañón se debe a los diferentes materiales ennegrecedores de la solución de revestimiento. La capa de niquelado negro contiene una mayor cantidad de fases no metálicas, como el niquelado negro que contiene cinc, que generalmente tiene una fracción másica de níquel de 40%~60%, cinc de 20%~30%, azufre de 10%~15%, y materia orgánica de alrededor de 10%, por lo que es una mezcla de níquel, cinc, sulfuro de níquel, sulfuro de cinc y materia orgánica.
La temperatura de trabajo de la solución de revestimiento, el valor de pH y la densidad de corriente afectan a la oscuridad del revestimiento. Si el revestimiento no es oscuro o tiene colores o parece amarillo, compruebe primero la conductividad, luego si la corriente es demasiado alta o demasiado baja; si la temperatura es demasiado alta, y luego compruebe si las concentraciones de tiocianato, sulfato de zinc, molibdato de amonio, etc., en la solución de revestimiento son insuficientes.
3.3 Níquel perlado galvánico
El níquel perlado (níquel satinado) tiene una cristalización fina, baja porosidad, baja tensión interna, buena resistencia a la corrosión y un tono suave. No deja marcas al tocarlo con la mano, es apreciado y querido en galvanoplastia decorativa, se utiliza mucho como capa base de cromo, plata y oro, y puede emplearse directamente para capas superficiales, sobre todo en aplicaciones como relojes y joyería.
El proceso principal de la galvanoplastia de níquel satinado consiste en añadir a la solución de revestimiento determinadas sustancias orgánicas, como aniones y sustancias anfóteras, que, en condiciones electrolíticas, forman precipitados con un diámetro similar al de las partículas coloidales. Estos precipitados se depositan junto con el níquel en el cátodo, produciendo un recubrimiento de níquel satinado con un brillo nacarado. Seleccionando los tipos y concentraciones de aditivos, se puede controlar el diámetro de los precipitados. El proceso del níquel perlado se compone casi en su totalidad de aditivos comerciales patentados.
El defecto que suele aparecer en el níquel perlado son los "puntos brillantes", que pueden resolverse eliminando los contaminantes y agitando a fondo la solución de revestimiento antes de usarla.
4. Plata galvanoplástica y aleaciones de plata
El símbolo del elemento plata es Ag, la masa atómica relativa es 107,9; el potencial de electrodo estándar es 0,799 V, y el equivalente electroquímico es 4,025/(A.h)
Los revestimientos de plata y aleaciones de plata tienen una excelente conductividad, baja resistencia al contacto, soldabilidad y grandes propiedades reflectantes y decorativas. Se utilizan mucho en vajillas, instrumentos musicales, joyería, etc., como revestimientos decorativos.
La capa plateada reacciona con el azufre del aire, formando óxido de plata y sulfuro de plata negro. También puede ennegrecerse fácilmente en contacto con materiales que contienen azufre, como plásticos y caucho, y el oxígeno del aire contribuye al oscurecimiento. La decoloración de la capa plateada afecta gravemente al aspecto de los componentes y repercute en la soldabilidad y el rendimiento eléctrico del revestimiento.
Las soluciones de plateado siguen basándose principalmente en el plateado con cianuro, que produce una capa blanca fina y pura con buena capacidad de dispersión y cobertura, y el proceso es relativamente estable. Sin embargo, tiene un alto contenido en cianuro y es muy tóxico. Se han llevado a cabo investigaciones nacionales e internacionales sobre procesos de plateado sin cianuro, y en la actualidad se dispone de suministros comerciales, como el plateado NS, el plateado con niacina, el plateado con tiosulfato, el plateado con dibutiril imida y el plateado con ácido imidazol-sulfónico, entre otros. El plateado sin cianuro ha progresado lentamente debido a su aspecto menos delicado que el plateado con cianuro, su mantenimiento menos conveniente y el suministro inconsistente de materias primas.
4.1 Plateado con cianuro
Desde la primera patente de plateado en 1840 hasta ahora, el plateado con cianuro tiene más de 160 años de historia. El plateado con cianuro siempre ha dominado la generación del plateado. El desarrollo del baño de plata con cianuro en la década de 1970 introdujo abrillantadores que aplicaban directamente una capa de plata brillante a partir de la solución de baño, eliminando el proceso de pulido, mejorando la eficacia y ahorrando una gran cantidad de plata. El baño de plata brillante se ha convertido en la corriente principal del baño de plata con cianuro.
(1) Componentes principales de la solución cianurada de revestimiento de plata
Plata. Es la sal principal en la solución de revestimiento, existiendo como iones complejos de cianuro de plata. La fuente de plata puede ser AgNO3AgCl, AgCN, KAg(CN)2pero AgNO3 y el AgCl se convierte mejor en AgCN o KAg(CN)2y se añade a la solución de revestimiento. La Ag en la solución de revestimiento se mantiene a 20~40g/L. Si la concentración de plata es demasiado alta, el revestimiento se cristaliza de forma gruesa y aparece amarillo; si la concentración de plata es demasiado baja, el rango de densidad de corriente es demasiado estrecho y la velocidad de deposición disminuye.
② Cianuro de potasio. Es un agente complejante; además de formar complejos con Ag, una cierta cantidad de cianuro potásico libre es beneficiosa para la estabilidad de la solución de revestimiento, la disolución normal del ánodo y la capacidad de dispersión de la solución de revestimiento. Los datos, en general, se refieren sobre todo al KCN libre. Si su concentración es demasiado alta, la velocidad de deposición de la solución de revestimiento es lenta; si la concentración es demasiado baja, la capa de revestimiento es propensa a amarillear, y el ánodo de plata se pasiva fácilmente, lo que da lugar a una velocidad de deposición lenta.
③ Hidróxido de potasio, carbonato de potasio. Puede mejorar la conductividad de la solución de revestimiento, contribuir a la capacidad de dispersión de la solución de revestimiento y aumentar el brillo del revestimiento.
④ Tartrato de sodio. Puede reducir la polarización del ánodo, evitar la pasivación y promover la disolución del ánodo de plata.
⑤ Agentes abrillantadores. La adición de agentes abrillantadores puede conseguir un revestimiento totalmente brillante y ampliar el rango de densidad de corriente, pero es necesario seleccionar los agentes abrillantadores adecuados para los revestimientos de plata utilizados con distintos fines. En el caso de los revestimientos decorativos, el requisito de espesor no es elevado, pero los requisitos de color del revestimiento (blancura y brillo) son especialmente altos, por lo que no es adecuado utilizar aditivos que contengan metales. Para los revestimientos funcionales utilizados en aplicaciones eléctricas y electrónicas, los requisitos de grosor del revestimiento y rendimiento eléctrico son mayores, y algunos pueden tener en cuenta los requisitos de dureza del revestimiento, lo que permite añadir sales metálicas como el antimonato potásico.
Los abrillantadores no metálicos suelen contener azufre, que puede producir un plateado blanco brillante, pero su vida útil no es lo suficientemente larga. Se descomponen si no se utilizan rápidamente en la solución de revestimiento. Los abrillantadores metálicos, como el antimonio, el selenio, el telurio, el cobalto y el níquel, pueden mejorar el brillo del chapado y aumentar la dureza, por lo que son más adecuados para el chapado de plata dura.
(2) Reacción del electrodo de revestimiento de plata cianurada
Cátodo:
El ion complejo de cianuro de plata se reduce directamente en el cátodo: Ag(CN)2- + e = Ag + 2CN–
Reacción adversa: 2H2O + 2e = H2 + 2OH–
Ánodo:
Utilizando ánodo de plata soluble: Ag + 2CN– = Ag(CN)2- + e
Cuando se utilizan ánodos insolubles:4OH– = 2H2O + O2 + 4e
La eficiencia de corriente del plateado con cianuro es alta, con eficiencias de corriente tanto catódica como anódica cercanas a 100%.
4.2 Decoloración del baño de plata
Las joyas chapadas en plata, cuando se exponen al aire o se utilizan durante algún tiempo, entran en contacto con gases nocivos o sustancias que contienen azufre en el aire, lo que provoca que el chapado se corroa y decolore, afectando gravemente al aspecto de la joya. Las principales causas son las siguientes.
- La propia capa plateada puede reaccionar fácilmente y volverse amarilla en una atmósfera húmeda que contenga sulfuros y, en casos graves, puede volverse negra.
- Funcionamiento incorrecto del proceso de plateado. Una limpieza inadecuada después del plateado deja restos de sales de plata en la superficie, y esta plata ionizada es propensa a la decoloración. La solución de revestimiento está contaminada o no es lo suficientemente pura, con iones metálicos como cobre, hierro y zinc, lo que da lugar a una baja pureza de la capa de revestimiento. Una operación inadecuada da lugar a una capa de metalizado rugosa con una elevada porosidad. Las superficies con alta porosidad son propensas a acumular humedad y medios corrosivos.
- Embalaje y almacenamiento inadecuados tras el baño de plata. Las razones de la decoloración incluyen principalmente: en primer lugar, las joyas bañadas en plata están expuestas directamente a la luz, lo que provoca que los átomos de plata se vean afectados por los rayos ultravioleta, transformándose en iones de plata, lo que acelera la velocidad de decoloración; en segundo lugar, el almacenamiento en un ambiente húmedo y a alta temperatura es propenso a la decoloración; en tercer lugar, un mal sellado del embalaje puede provocar que los materiales de embalaje reaccionen con el baño de plata.
4.3 Proceso de tratamiento antidecoloración con capas plateadas
Para evitar que la capa de plata se decolore, en la producción se suelen utilizar procesos de pasivación de la capa de plata, que suelen incluir los siguientes métodos: pasivación química, pasivación electroquímica, inmersión en agentes antidecoloración, galvanoplastia con metales preciosos e inmersión en películas protectoras orgánicas.
(1) Pasivación química
Después de lavarlas a fondo con agua, las piezas chapadas que no hayan recibido un baño de plata brillante deben tratarse inmediatamente con ácido crómico.
- Tratamiento con ácido crómico. Anhídrido crómico:80~85g/L; cloruro sódico:15~20g/L; temperatura: temperatura ambiente; tiempo: 5~15 segundos. Tras el tratamiento con ácido crómico, se forma una película amarilla relativamente suelta en la superficie del revestimiento de plata.
- Proceso de decapado. Agua amoniacal: 300~500ml/L; temperatura ambiente; tiempo: 20~30 segundos.
- Idemitsu. Fracción de masa de ácido nítrico o ácido clorhídrico de 5%~10%; temperatura ambiente; tiempo: 5~20 segundos. Después de que la capa de plateado se someta a los procesos anteriores, se somete a un pasivado químico para conseguir mejores resultados. La capa de película de pasivación química es muy fina, lo que tiene poco efecto en la resistencia de contacto. Aún así, la estructura de la película de pasivación no es lo suficientemente densa, y su capacidad para evitar la decoloración no es fuerte, por lo que la pasivación electroquímica puede llevarse a cabo a continuación.
(2) Pasivación electroquímica
Puede realizarse después de la pasivación química o directamente después del plateado brillante. Se utiliza la capa de plateado como cátodo y el acero inoxidable como ánodo. Mediante la electrólisis, se forma una película relativamente densa en forma de aguja en la superficie de la capa de plata, que tiene una mayor resistencia a la decoloración que la película de pasivación química. Si la pasivación química se combina con la electrólisis, el efecto es aún mejor.
(3) Agente protector contra contactos eléctricos por inmersión
Disolver el agente protector en un disolvente orgánico y sumergirlo durante 1~2 minutos a cierta temperatura, lo que tiene un efecto protector sobre la superficie.
(4) Galvanoplastia de metales preciosos
Galvanoplastia de oro, rodio, paladio, aleación de paladio y níquel (80% ), espesor de 0,1~0,2μm.
(5) Película protectora orgánica
El grosor suele ser superior a 5μm, y el efecto protector es mejor. Los revestimientos protectores transparentes a base de acrílico o silicona pueden ser de inmersión (pulverización) o pintura electroforética acrílica catódica. Los requisitos de la película protectora orgánica incluyen principalmente una buena densidad de recubrimiento, una alta transparencia, una dureza de recubrimiento no inferior a HV4 y una buena adherencia al sustrato.
5. Oro galvánico y aleaciones de oro
La masa atómica relativa del oro es 197, el potencial de electrodo estándar del oro monovalente es +1,68 V, el equivalente electroquímico del oro trivalente es +1,5 V, y el equivalente electroquímico del Au+ es de 7,357 g/(A.h) y el equivalente electroquímico de Au3+ es de 2,44977 g/(A.h).
El oro tiene una estabilidad química extremadamente alta y no lo corroen ni el ácido clorhídrico, ni el ácido sulfúrico, ni el ácido nítrico, ni el ácido fluorhídrico, ni los álcalis. La conductividad eléctrica del oro sólo es superada por la de la plata y el cobre. La conductividad térmica del oro es 70% de la de la plata, y el oro tiene una excelente ductilidad. Debido a su estabilidad química, conductividad y buena soldabilidad, el oro se utiliza ampliamente en la industria de la decoración.
El chapado en oro decorativo se utiliza generalmente para joyería artesanal, que requiere que el chapado tenga buen color, brillo, resistencia al desgaste y no se decolore. La pureza del chapado puede dividirse en oro puro y oro K. El oro puro tiene un contenido de oro superior a 99,9% y los tipos de oro K más utilizados son 22K, 18K y 14K. El oro fino puede aplicarse directamente sobre sustratos como níquel, cobre y bronce, mientras que el oro grueso requiere una capa base previa.
El chapado en oro comenzó a principios del siglo XIX, con la aparición de patentes para aplicaciones de chapado en oro a finales de la década de 1840 basadas en soluciones de chapado alcalino a base de cianuro. Debido a la extrema toxicidad del cianuro, tanto a nivel nacional como internacional, se ha investigado continuamente para desarrollar soluciones de chapado en oro sin cianuro y con bajo contenido en cianuro, lo que ha dado lugar a la aparición del chapado en oro puro ácido, el chapado en oro duro ácido, el chapado en oro neutro y el chapado en oro sin cianuro. Las soluciones de chapado en oro pueden dividirse en cuatro tipos: alcalinas con cianuro, ácidas con bajo contenido en cianuro, neutras con bajo contenido en cianuro y sin cianuro. En general, las soluciones de chapado en oro con bajo contenido en cianuro y sin cianuro siguen presentando ciertas lagunas en cuanto a estabilidad y efectos de chapado en comparación con las soluciones de chapado en oro con cianuro alcalino.
5.1 Dorado con cianuro
(1) Dorado alcalino cianurado
① Principales componentes de la solución alcalina cianurada de chapado en oro. La solución de chapado en oro alcalino cianurado tiene una buena capacidad de dispersión, es una solución de chapado estable, es fácil de manejar y mantener, y puede incorporar fácilmente diferentes elementos de aleación, como Cu, Ni, Co, Ag, Cd, etc. para producir aleaciones de oro de diferentes tonalidades. Por ejemplo, la adición de níquel puede producir un color dorado ligeramente blanco, la adición de Cu y Cd produce oro rosa; la adición de Ag puede dar lugar a un chapado en oro verde claro. Controlando la concentración de elementos de aleación en la solución de revestimiento y las condiciones de trabajo, se puede conseguir casi cualquier tonalidad deseada de revestimiento de oro. La porosidad del chapado en oro con cianuro es relativamente alta, y su resistencia al desgaste y a la corrosión es escasa. Debido al alto contenido de cianuro en el chapado en oro, su uso ha disminuido significativamente en los últimos años; sin embargo, en la industria de la joyería, el chapado en oro con cianuro sigue siendo el tipo más común. Los principales componentes de la solución alcalina de chapado en oro con cianuro son los siguientes.
- Cianuro potásico de oro (contiene 68,3% de oro ). Es la sal principal de la solución de revestimiento y la fuente de oro en la capa de revestimiento. La capa de revestimiento aparecerá roja y áspera si el contenido de Au es demasiado bajo. La calidad del cianuro potásico de oro es muy importante y debe tenerse cuidado al seleccionarlo y utilizarlo. El cianuro potásico de oro debe disolverse en agua desionizada antes de añadirlo a la solución de revestimiento.
- Cianuro potásico (cianuro sódico). Se trata de un agente complejante que puede estabilizar la solución de revestimiento y permitir que el proceso del electrodo se desarrolle con normalidad. Si el contenido es demasiado bajo, la solución de revestimiento se vuelve inestable, lo que da lugar a un revestimiento rugoso con poco color.
- Fosfato. Es un tampón que estabiliza la solución de metalizado y mejora el brillo del revestimiento.
- Carbonato. Es una sal conductora que puede mejorar la conductividad de la solución de revestimiento y aumentar su capacidad de dispersión. Sin embargo, si no se añade carbonato al abrir el depósito y la solución es alcalina, con el tiempo, el CO2 del aire se acumularán en la solución de revestimiento. Cuando la acumulación de carbonatos es excesiva, puede provocar que el revestimiento se vuelva áspero y produzca manchas.
- La composición de las aleaciones de Cu, Ni, Co, Ag y Cd se añade principalmente con sales de cianuro, y también las hay que se añaden con sales de EDTA. Sus concentraciones deben controlarse adecuadamente para obtener revestimientos de aleación de 14K, 16K, 18K y 23K de diferentes proporciones. Además, los revestimientos de oro-plata de 16K y los de oro-cobre-cadmio de 18K pueden utilizarse como capas intermedias en combinaciones de revestimiento de oro grueso y revestirse hasta el espesor requerido.
② Reacción del electrodo del chapado en oro alcalino con cianuro. La sal principal de la solución cianurada de chapado en oro es el cianuro potásico de oro KAu(CN)2. El ion complejo de cianuro Au(CN)2– se encuentra en la solución y se descarga en el cátodo, generando una capa de chapado en oro.
Cátodo:[Au(CN)2]– + e = Au + 2CN–
Reacción adversa:2H+ + 2e = H2
Ánodo:
Utilizando ánodo de plata soluble: Au + 2CN– - e = [Au(CN)2]–
Cuando se utilizan ánodos insolubles:2H2O - 4e = 4H+ + O2
Una parte de CN– que queda en la solución es oxidado por el oxígeno del ecosistema inicial, y los posibles productos incluyen CNO–DIRECTOR DE OPERACIONES–CO32-NH3(CN)2etc., que se acumulan en la solución y se convierten en contaminantes.
(2) Proceso de chapado en oro con cianuro ácido
La base de una solución ácida de chapado en oro de microcianuro es que los iones complejos de cianuro de oro no se descomponen a un pH de 3,1. El pH de la solución ácida de chapado en oro es de 3,5~5,5. El chapado en oro puro es brillante, uniforme, delicado y tiene un tono rojo amarillento. Si se añaden elementos de aleación como Co, Ni, Sb, Cu, Cd y otros a la solución de chapado, se obtienen aleaciones de oro que cumplen los requisitos de la industria decorativa en cuanto a tonalidades, como las capas de chapado en oro de 22,5~23,5 de 1N14, 2N18, 3N.
En la producción, el chapado en oro ácido se divide principalmente en dos tipos: oro fino y oro grueso. El chapado en oro fino incluye el pre-oro y el oro decorativo. El oro previo requiere una excelente adhesión al sustrato y a la capa de oro, mientras que la solución de chapado de oro previo evita la contaminación de la solución de chapado de oro grueso. El oro decorativo puede ser oro puro o una aleación de oro, en función de los requisitos de aspecto. Las soluciones de chapado en oro grueso incluyen soluciones de chapado en oro ordinarias y de alta velocidad. La solución de chapado puede chaparse hasta el grosor requerido según sea necesario. Los principales componentes de la solución de chapado en oro de cianuro ácido son los siguientes:
- Cianuro de potasio. Con un contenido suficiente, la sal principal puede producir un chapado en oro brillante y finamente cristalino. Un contenido insuficiente da lugar a un estrecho intervalo de densidad de corriente, con un chapado de color rojo, áspero y muy poroso.
- Citrato. Tiene efectos complejantes, asociadores y amortiguadores. Si la concentración es demasiado alta, la eficacia de la corriente disminuye y la solución es propensa al envejecimiento; si la concentración es demasiado baja, la capacidad de dispersión de la solución de revestimiento es deficiente.
- Fosfato. Un agente tampón que puede estabilizar la solución de revestimiento y mejorar el brillo del revestimiento.
- El cobalto, el níquel, el antimonio, el cobre, el cadmio, la plata, etc., son elementos de aleación que pueden mejorar la dureza y el aspecto del revestimiento, y su concentración debe controlarse estrictamente.
5.2 Dorado sin cianuro
En los años 60, se utilizaba en la producción el chapado en oro sin cianuro, con soluciones de chapado que contenían sulfitos, tiosulfatos, haluros, ácido te-succínico, etc., pero la más utilizada era la solución de chapado de sulfito con [Au(SO3)2]3- como anión complejo.
Las características de la solución de revestimiento de sulfito son: la solución de revestimiento tiene buena dispersión y capacidad de cobertura, la capa de revestimiento tiene buena nivelación y ductilidad (el alargamiento puede alcanzar 70%~90%), puede alcanzar brillo de espejo, y la pureza de la capa de revestimiento es alta, con buena soldabilidad. Rápida velocidad de sedimentación, pocos poros. El revestimiento tiene buena adherencia a metales de níquel, cobre y plata.
La desventaja de la solución de revestimiento de sulfito es que su estabilidad no es tan buena como la de la solución de revestimiento de cianuro, y la resistencia al desgaste del oro duro es pobre. Actualmente, este proceso tiene una pequeña cuota de mercado, pero tiene potencial.
6. Galvanoplastia de rodio
El chapado en rodio es de color blanco plateado, tiene un fuerte brillo superficial, no se ve afectado por gases corrosivos como el dióxido de carbono y los sulfuros de la atmósfera, y tiene una gran estabilidad frente a ácidos y bases, mostrando una fuerte resistencia a la corrosión. La dureza del chapado en rodio es diez veces superior a la del chapado en plata, con una buena resistencia al desgaste. Como capa decorativa de rodio, tiene un tinte ligeramente azulado en blanco, un lustre brillante, resistencia al desgaste y una gran dureza, lo que lo convierte en el revestimiento decorativo de más alto grado. Debido a la gran dureza y fragilidad del rodio, si el revestimiento es demasiado grueso, puede desprenderse fácilmente. Por lo tanto, para la bisutería en general, es habitual chapar primero plata, paladio o níquel como capa base antes del chapado en rodio.
La solución de chapado de rodio contiene sulfatos, fosfatos o aminosulfonatos, los sulfatos más utilizados. Su solución de chapado es fácil de mantener, tiene una alta eficiencia de corriente y una rápida velocidad de deposición, por lo que es adecuada para el procesamiento de joyas.
(1) Componentes principales de la solución de revestimiento de sulfato de rodio
- Sulfato de rodio. Es la sal principal de la solución de revestimiento, y cuando el contenido de rodio es adecuado, puede producir un revestimiento brillante finamente cristalino. Si el contenido es demasiado alto, el revestimiento no será blanco y será áspero; si el contenido es demasiado bajo, el revestimiento se volverá amarillo y tendrá poco brillo. Generalmente, el contenido de rodio se controla entre 1,6~2,2.g/L.
- Ácido sulfúrico. Su función principal es mantener la estabilidad de la solución de revestimiento y aumentar la conductividad, y un bajo contenido de ácido sulfúrico afectará al brillo de la capa de revestimiento.
(2) Reacción del electrodo de rodiado
Reacción anódica:4OH - 4e = 2H2O + O2 ↑
Reacción catódica: Rh2+ + 2e = Rh
Reacción catódica lateral:2H+ + 2e = H2 ↑
Sección III Proceso de revestimiento químico
1. Características del revestimiento químico
En comparación con la galvanoplastia, la galvanoplastia química presenta las siguientes ventajas.
(1) El metalizado químico se adapta a diversos materiales de sustrato, incluidos metales, semiconductores y materiales no metálicos.
(2) El espesor del revestimiento químico es uniforme y constante, independientemente de la forma o complejidad de la pieza; siempre que se tomen las medidas técnicas adecuadas, se puede obtener un revestimiento uniforme en la pieza.
(3) En el caso del metalizado químico autocatalítico, pueden obtenerse recubrimientos de cualquier espesor, e incluso es posible el electroconformado. Los revestimientos obtenidos por metalizado químico tienen excelentes propiedades químicas, mecánicas y magnéticas (como revestimientos densos y alta dureza).
Sin embargo, el revestimiento químico también tiene algunas desventajas: en primer lugar, la vida útil de la solución de revestimiento químico es relativamente corta; en segundo lugar, la velocidad de revestimiento es lenta, y sólo por debajo de la velocidad de revestimiento crítica puede garantizarse la calidad del revestimiento.
2. Principio del revestimiento químico
El revestimiento químico es un proceso de deposición de metales en el que los iones metálicos se reducen en la superficie metálica mediante autocatálisis por agentes reductores apropiados en la solución. Se trata de una reacción química redox que implica la transferencia de electrones y un proceso de deposición química sin fuente de energía externa. Este tipo de deposición química puede dividirse en tres categorías.
(1) Revestimiento de sustitución
Colocar un metal con fuertes propiedades reductoras (el sustrato, la pieza a recubrir) en una solución de otra sal metálica con fuertes propiedades oxidantes. El metal del sustrato actúa como un fuerte agente reductor, y los electrones que dona son aceptados por los iones metálicos de la solución, depositándose en la superficie del sustrato para formar un recubrimiento. Este proceso también se denomina metalizado por inmersión. Por ejemplo, el cobre desplazando a la plata, en el que la pieza de cobre como sustrato desplaza a la plata de la solución, y la capa de plata depositada cubre la superficie de cobre. La reacción de reducción se detiene inmediatamente cuando está totalmente cubierta, lo que da lugar a un recubrimiento muy fino. Dado que la reacción se basa en la corrosión del metal del sustrato, la fuerza de adherencia del recubrimiento al sustrato es relativamente pobre. No hay muchos sistemas adecuados para el proceso de metalizado por inmersión en cuanto a sustrato y solución de metalizado, por lo que la aplicación de este proceso es limitada.
(2) Metalizado de contactos
Después de que el metal que se va a bañar en oro entre en contacto con otro metal auxiliar, se sumerge en una solución de sales metálicas, y el potencial del metal auxiliar debe ser inferior al del metal depositado. Una vez que la pieza metálica y el metal auxiliar se sumergen en la solución, forman una batería primaria, en la que el metal auxiliar es el ánodo debido a su fuerte actividad, disolviendo y liberando electrones. Por el contrario, la pieza metálica es el cátodo, donde los iones metálicos de la solución se reducen y se depositan en forma de capa metálica sobre la pieza. Este método carece de importancia en la aplicación práctica, pero puede utilizarse para iniciar el chapado químico sobre sustratos activos no catalíticos.
(3) Método de reducción
En primer lugar, la solución de revestimiento químico contiene iones metálicos para el revestimiento y, a continuación, se añaden electrones proporcionados por un agente reductor adecuado para reducir los iones metálicos y depositar un revestimiento metálico. Esta reacción de revestimiento químico debe estar bien controlada en cuanto a velocidad; de lo contrario, la deposición en toda la solución carece de sentido. El método de reducción consiste en depositar un revestimiento metálico sobre una superficie activa con capacidad catalítica. Debido a la capacidad autocatalítica de la capa depositada durante el proceso de chapado, esta técnica puede depositar continuamente para formar un recubrimiento de un cierto espesor que tenga valor práctico, que es el verdadero significado del proceso de "chapado químico". El método para conseguir la deposición de metales utilizando un agente reductor sobre una superficie activa autocatalítica es el único proceso de deposición húmeda que puede sustituir a la galvanoplastia.
3. Dorado químico
El chapado químico en oro puede dividirse en tipo reductor y tipo de desplazamiento, dependiendo de si se utiliza un agente reductor en la solución de chapado. La solución de chapado químico de oro de tipo reductor incluye sal de oro, agente complejante, agente reductor, tampón de pH y otros aditivos. Su reacción utiliza el agente reductor para reducir el oro, que luego se deposita uniformemente sobre el sustrato para conseguir el espesor deseado. Generalmente, se puede depositar una capa de oro más gruesa, con un espesor de alrededor de 1μm. El chapado químico en oro por desplazamiento se lleva a cabo sin un agente reductor externo. Debido a la diferencia de potencial entre metales, un metal más activo puede desplazar un metal menos activo de la solución a través de una reacción de desplazamiento. Por ejemplo, en el baño de oro por desplazamiento sobre un sustrato de níquel, la diferencia de potencial entre el oro y el níquel permite al níquel desplazar el oro de la solución de baño a la superficie de la capa de níquel. El potencial estándar del oro es de 1,68 V, mientras que el potencial estándar del níquel es de sólo -0,25 V, lo que indica una diferencia de potencial significativa. Cuando el sustrato de níquel se sumerge en la solución de chapado en oro por desplazamiento, se produce una reacción de desplazamiento y una capa de oro sustituye rápidamente a la superficie de níquel. Sin embargo, los átomos de oro tienen un volumen mayor, lo que da lugar a una disposición relativamente suelta en la superficie de níquel con muchos poros. Por lo tanto, en el subsiguiente proceso de inmersión en oro, a medida que se prolonga el tiempo, los iones de oro de la solución de chapado siguen experimentando reacciones de desplazamiento con los átomos de níquel a través de los poros de la superficie de la capa de oro.
(1) Composición y condiciones de proceso de la solución de dorado químico
La solución química de chapado en oro contiene compuestos de iones de oro (es decir, sales de oro), agentes complejantes, tampones de pH, agentes reductores, estabilizadores y otros componentes principales.
① Sales de oro y agentes complejantes. Entre los compuestos de iones de oro adecuados se encuentran las sales cianuradas de oro KAu(CN)2KAu(CN)4compuestos de oro hidrosolubles HAuCl4KAuCl4NH4AuCl4, Na3Au(SO3)2, Na3Au(S2O3)2, and gold compounds Au(OH)3 with lower solubility. They can be used alone or in combination. The gold ion concentration is generally 0.001~0.1mol/L. If the gold ion concentration is below 0.001mol/L, practical gold deposition rates cannot be achieved; if the gold ion concentration is above 0.1mol/L, gold precipitates are likely to form, and gold compounds cannot fully exert their role in chemical plating, leading to the waste of gold, which is economically unfavorable. The addition of complexing agents to the plating solution aims to form complexes with the metal components in the solution while acting as a buffer to suppress changes in the pH of the plating solution. Available complexing agents include EDTA·2Na, K2SO3, Na2SO3, K2S2O3 and others.
② Reducing agents and additives. The main reducing agents currently used in research include dimethylamine borane (DMAB), sodium hypophosphite, hydrazine, borohydrides, hydrazine borane, thiourea, sodium ascorbate, and titanium trichloride, among others.
③ Process conditions. The pH value of the plating solution is generally 5~9, with an optimal range of 6~8. A lower pH value improves the adhesion of the gold plating layer, but excessively low pH values can easily produce harmful gases and corrosion. A high pH value makes the plating solution strongly alkaline, which can dissolve the coating on the surface of the plated item. Depending on the type and concentration of gold ion compounds and complexing agents, it is appropriate to select alkaline solutions NaOH, KOH, NH4OH or inorganic acid solutions H2SO4, H3PO4, H3BO3 to adjust the pH value of the plating solution. The plating temperature is generally 50~90℃, the best being 60~85℃. A lower operating temperature is particularly suitable for items that are not heat-resistant, and it can also save energy and ensure safe operation.
(2) Cyanide-Free Chemical Gold Plating
Developing cyanide-free chemical gold plating, which replaces CN– in the gold plating solution with non-cyanide alternatives, is an important direction in chemical gold plating. It represents a significant advancement based on cyanide gold plating and has seen considerable domestic and international development in recent years. The current cyanide-free gold plating solutions mainly include sulfite gold plating, thiosulfate gold plating, halide gold plating, and thiocyanate gold plating, among which sulfite gold plating has better practical value. The following mainly introduces the sulfite gold plating system.
Sulfite system: In 1842, sulfite gold salt was first used as a gold source for cyanide-free electroplating of gold; it was later applied in chemical gold plating solutions, referred to as sulfite gold plating solutions. The reducing agents used in this gold plating solution include sodium hypophosphite, formaldehyde, hydrazine, borohydrides, DMAB, sodium ascorbate, thiourea and its derivatives, and phenyl compounds, among others. To obtain a practical cyanide-free gold plating solution, a small amount of stabilizers needs to be added to the plating solution, such as EDTA, triethanolamine, NTA, benzotriazole, 2-mercaptobenzothiazole, etc. These additives can form complex chelating agents with the monovalent gold ions in sulfite gold salt, thereby improving the stability of the plating solution.
4. Chemical Nickel Plating
The chemical nickel plating layer is independent of the coating thickness and the shape of the part and has high hardness, good wear resistance, natural lubricity, and excellent corrosion resistance, which is why it is known as the “designer’s coating.” Designers can find suitable options in the coating system based on the properties required for the parts.
Composition and Process Conditions of Chemical Nickel Plating Solution
The chemical nickel plating solution is crucial for the chemical plating process’s stability and the coating’s quality. Since the development of chemical plating, many types of plating solutions have been developed. Among them, the most commonly used solution combines nickel sulfate as the main salt and sodium hypophosphite as the reducing agent, along with appropriate additional components to adjust stability, complexation, and other properties.
(1) Nickel salts. There are mainly two types: nickel sulfate and nickel chloride. During the plating process, if the concentration of nickel salts is too low, the reaction rate is slow, making it difficult to form a plating layer. If the concentration is too high, it leads to some nickel ions being free in the plating solution, reducing the stability of the solution, which can easily result in a rough plating layer and even trigger the decomposition of the plating solution. Therefore, it is essential to maintain an appropriate content of nickel salts in the plating solution and to accurately analyze and appropriately supplement the nickel salt content during the process.
(2) Reducing agent. The common reducing agent is sodium hypophosphite. The role of the reducing agent is to catalyze dehydrogenation to provide lively primary hydrogen atoms to reduce the nickel ions to metallic nickel. The reducing agent’s content significantly impacts the deposition rate; increasing the concentration of the reducing agent can accelerate the deposition rate, but the concentration of the reducing agent should not be too high. Otherwise, the plating solution is prone to self-decomposition, which destroys the stability of the plating solution, and the deposition rate will also reach a limit value.
(3) Complexing agents. Commonly used complexing agents include glycolic acid, malic acid, tartaric acid, citric acid, and lactic acid. Adding complexing agents controls the deposition rate of nickel ions. The addition of complexing agents must consider the ability to complex all nickel ions and the deposition rate of the plating solution to maintain an appropriate ratio of the components. Complexing agents can reduce the concentration of free ions and the equilibrium potential in the solution while also adsorbing on the plated parts’ surface, enhancing the plated parts’ surface activity and accelerating the release of hydrogen ions from hypophosphite. Using composite complexing agents can effectively improve the stability of the plating solution and the deposition rate and make the surface of the coating bright and dense.
(4) pH value adjusters and buffers. The pH value of the plating solution has a significant impact on the deposition rate, reducing agent utilization and coating performance. Since H+ is a byproduct of the reduction reaction, the pH value of the plating solution will decrease as the reaction proceeds. Therefore, adjusting and controlling the pH value during chemical plating is crucial. pH value adjusters are usually NaOH, KOH or alkaline compounds such as carbonates, ammonia, etc. If it is necessary to lower the pH value, inorganic or organic acids must be added. Adding buffers prevents instability in the deposition rate caused by drastic changes in pH value during the deposition reaction. The anions of the buffer combine to form weak acid molecules with very low ionization, thus controlling the drastic changes in the pH value of the plating solution.
(5) Estabilizadores. During the plating process, active crystalline cores inevitably form in the plating solution for various reasons, causing the solution to decompose and fail. By adding stabilizers, these active crystalline cores can be poisoned, losing their self-catalytic effect, thus preventing the decomposition of the plating solution. Stabilizers have become a technical secret in the chemical nickel plating process. Common stabilizers include lead ions, tin sulfides, etc.
(6) Promoters. The addition of complexing agents to the chemical nickel plating solution generally leads to a decrease in deposition rate. If added in excess, it can cause the deposition rate to become very slow or even unusable. Small amounts of organic acids are often added to the plating solution to increase the deposition rate, and these organic acids are referred to as promoters.
(7) Temperature. Temperature is the most important parameter affecting the deposition rate of chemical nickel plating. The catalytic reaction of chemical nickel plating generally can only be achieved under heating conditions, and many individual reaction steps of chemical nickel plating only show a significant deposition rate above 50℃. The operating temperature of the acidic plating solution for chemical nickel-phosphorus alloy is generally around 85~95℃, while general alkaline chemical plating solutions can deposit within a moderate temperature range. As the temperature increases, the deposition rate accelerates. However, raising the plating solution temperature will accelerate the increase of hypophosphite, making the plating solution unstable. During operation, the plating solution should be stirred evenly, and care should be taken to prevent local overheating of the plating solution, maintaining a stable working temperature to avoid severe self-decomposition of the plating solution and adverse consequences such as delamination of the coating.
(8) pH value. With the increase of the pH value of the plating solution, the deposition rate accelerates, and the solubility of phosphite decreases, which can easily lead to the self-decomposition of the plating solution. Suppose the pH value of the plating solution is too high. In that case, the reaction of hypophosphite oxidizing to phosphite accelerates, and the catalytic reaction turns into a spontaneous reaction, causing the plating solution to fail quickly. As the pH value increases, the phosphorus content in the coating decreases. When the pH value is too low, the reaction cannot proceed, such as in acidic plating solutions, when the pH value<3, it isn’t easy to deposit a nickel-phosphorus alloy coating.
(9) The effect of stirring. The diffusion process influences the chemical nickel plating process, and stirring the chemical plating solution helps to increase the transfer rate of reactants to the workpiece surface while also facilitating the removal of reaction products. Essentially, stirring alters the chemical composition and pH value within the diffusion layer at the workpiece/solution interface. Stirring methods include mechanical stirring, magnetic stirring, ultrasonic dispersion, and chemical dispersion methods. Additionally, when chemical nickel plating is conducted under heating conditions, the large amount of hydrogen gas released can create a “self-stirring” effect. Among these, mechanical stirring is simple and easy to implement, generally using external shear and impact forces to fully disperse particles in the medium; however, it does not effectively address the overall stirring of the plating solution, especially at the bottom of the beaker. Magnetic stirring utilizes a magnetic rotor to generate stirring through rotation in the plating solution. It is very effective for stirring the solution at the bottom, making it beneficial for composite plating solutions containing settling particles. However, magnetic stirrers typically only heat the bottom of the plating tank, and this heating method can easily cause local overheating of the bottom solution, which may adversely affect the plating solution’s stability and the coating’s performance. Ultrasonic dispersion has been widely recognized and effective in recent years, utilizing ultrasound’s high energy and cavitation effect to crush aggregated microparticles for dispersion. However, due to the immense energy of ultrasound, this dispersion should be applied intermittently during plating. Better results can be achieved if supplemented with a certain intensity of mechanical stirring.
5. Chemical Copper Plating
Chemical copper plating technology is mainly applied to non-metal surfaces such as plastics and wood in decorative items. Whether for decorative or functional plastic electroplating, most require chemical copper plating to ensure a good conductive base layer and achieve a good coating. Compared to other methods of metalizing plastic surfaces, chemical copper plating is the most economical and simplest method.
(1) Common Methods of Chemical Copper Plating
The chemical copper plating solution mainly consists of copper salts, reducing agents, complexing agents, stabilizers, adjusting agents, and other components. Currently, the widely used chemical copper plating solution uses copper sulfate as the main salt and formaldehyde as the reducing agent, mainly composed of two parts: one is a solution containing copper sulfate, potassium sodium tartrate, sodium hydroxide, sodium carbonate, and nickel chloride; the other is a solution containing the reducing agent formaldehyde. These two solutions must be prepared separately in advance and then mixed for use. In alkaline solutions, formaldehyde mainly exists as methylene glycol and its anions. During the chemical copper plating process, formaldehyde rapidly undergoes a disproportionation reaction, producing its redox products and leading to premature aging of the plating solution. Since no coordinating agents exist in the plating solution, only a small amount of these oxides can be dissolved while most continue accumulating. A typical plating solution formula and working conditions are 5g/L copper sulfate, 25g/L potassium sodium tartrate, 7g/L sodium hydroxide, 10ml/L formaldehyde, and time 20~30 seconds.
(2) Chemical Copper Plating on Non-Metallic Surfaces
With the expansion of the application field of chemical copper plating, the technology for chemical copper plating on non-metal surfaces has also gradually matured. For example, maskless producing the copper interconnection wires on ceramic substrates has been achieved by combining laser micro-etching technology with chemical plating. On this basis, a chemical copper plating method has been further established and implemented on the surfaces of non-metallic materials such as ceramics without the need for catalytic activation. This method simplifies the chemical copper plating process, has good coating performance, stable plating solution, and fast plating speed; it also saves precious metals and reduces production costs. Chemical metal plating is one of the main methods for metalizing plastic surfaces.
After the plastic is metalized, it can be further processed through chemical plating or electroplating to obtain plastic products with wear resistance, heat resistance, thermal stability, and special functions.
Chemical copper plating is also applied to the surface treatment of wooden materials, and the treated materials have better decorative and corrosion-resistant properties, which can enhance the added value of the products. Japan has made certain progress in researching wood copper plating and gold plating processes in recent years. The treatment objects are mainly wood from commonly used tree species such as Japanese cedar, and the test materials include wood chips and small square timber. The treatment process first involves ultrasonic treatment of the test materials in aqueous and organic solvent immersion solutions, degreasing and removing components that hinder the plating film, then sealing the resin channels with polyethylene glycol toluene solution, attaching the catalyst, and finally performing chemical plating, which requires several drying steps.
Despite the significant development of the chemical copper plating process, the following aspects still need further improvement: the relationship between the stability of chemical copper plating and plating speed; the kinetic study of chemical copper plating in multi-complex systems; the impact of additives on coating performance; the relationship between the microstructure of the coating and the surface morphology of the substrate; alternatives to formaldehyde, etc.
Copywrite @ Sobling.Jewelry - Fabricante de joyería personalizada, fábrica de joyería OEM y ODM
6. Chemical Plating Example: Electroplating of Leaf Veins
Leaf vein electroplating, also known as leaf decoration electroplating, first selects artistic, hard, and dense-veined leaves. After removing chlorophyll to expose the leaf veins undergo surface metallization and electroplating processing.
These leaves have been shaped and processed to maintain their original, realistic appearance and reflect the elegance and luxury after electroplating (Figure 11-8).

The main processes of leaf vein decorative electroplating are divided into three parts: leaf vein treatment, surface metallization (chemical plating), and decorative electroplating.
(1) Leaf Vein Treatment
Place the freshly picked leaves in an alkaline aqueous solution for soaking to remove chlorophyll, allowing the surface to display a relatively intact natural leaf vein pattern. The soaking solution is prepared with sodium hydroxide. After soaking for several days, chlorophyll can be removed, but this method takes a long time, and the degree of corrosion is difficult to control. Adding some sodium carbonate to the sodium hydroxide solution and heating it to a boil can quickly remove chlorophyll, with the leaves changing from green to yellow-green ideal. After washing the boiled leaves, if there are still traces of chlorophyll remaining on the veins, a soft brush must gently scrub along the veins, ensuring that the veins remain intact as a standard.
(2) Surface Metallization
Surface metallization is a treatment method that makes the surface of general non-metal materials conductive, preparing for the next electroplating step, which can be achieved through sensitization, activation, reduction, and chemical plating. Chemical nickel plating makes the surface of the leaf veins conductive, with the basic formula and process conditions being 26~28g/L nickel sulfate, 35g/L sodium hypophosphite, 20g/L citric acid, and other appropriate amounts. The operating process conditions are pH value being 4.6~4.8 and temperature at 90℃.
(3) Decorative Electroplating
After bright copper plating, mid-term production can be carried out: use spot welding to configure hanging parts, such as positioning pins, hooks, and other hangers. The material for the hanging parts is generally fine purple copper wire. Before spot welding, soak the fine copper wire in an acid solution for a short time (less than 30 seconds), and then cover it with solder for spot welding.
(4) Bright Electroplated Nickel
The nickel plating process, which is mainly used to prevent the penetration of copper and gold plating, refers to the previous one.
(5) Electroplated Gold
Finally, a thick gold plating is applied to the surface.
Section IV Chemical and Electrochemical Conversion Film Process for Popular Jewelry
Chemical and electrochemical conversion film technology is a technique that uses chemical or electrochemical means to bring metal into contact with a specific chemical treatment solution, thereby forming a layer on the metal surface that has good adhesion and can protect the base metal from the effects of water and other corrosive media, can improve the adhesion and aging resistance of organic coatings, or can impart decorative properties to the surface.
In the jewelry industry, chemical and electrochemical conversion film technology has been widely applied, forming colored films or interference films through surface conversion, creating various decorative colors and surface coloring effects, improving the appearance of materials, and enhancing corrosion resistance. This includes surface coloring treatments for copper jewelry, stainless steel jewelry, titanium jewelry, aluminum jewelry, and silver jewelry.
1. Chemical Coloring Process of Copper and Copper Alloy Ornaments
Copper alloy coloring is mainly applied to craft jewelry. Most copper compounds have intense colors, and the decorative colors on the surface of copper and its alloys almost cover the entire color spectrum through chemical coloring. Currently, the ones that are accepted by the market and can be produced on an industrial scale are primarily green (copper carbonate), black (copper sulfide), blue (alkaline copper ammonia complex), black (copper oxide), and red (cuprous oxide).
(1) The Chemical Reaction Mechanism of Surface Coloring
The surface coloring of copper and its alloys is the interaction of metallic copper with the coloring solution, forming an oxide layer, sulfide layer, and other compound films on the metal surface. Different coloring effects can be achieved by selecting different coloring formulas and conditions. For example, sulfur-based solutions that can be utilized include sulfides (such as potassium sulfide, ammonium sulfide, etc.), sodium thiosulfate, polysulfides (such as potassium persulfate), etc. The coloring principle is based on the characteristic reaction of sulfur with copper to produce copper sulfide, and under different reaction conditions and the participation of other components in the formula, colors such as black, brown, dark antique copper, blue, and purple can be formed. The interaction of copper with ammonia and chromium, along with the participation of other ions in the formula, can also produce various coloring effects under different reaction conditions. The addition of oxidants in the coloring formula can promote the reaction, but excessive oxidants can affect the quality of the oxide film.
(2) Chemical Coloring Process of Copper
- The color is antique copper. Immerse pure copper or copper-plated ornaments (the thickness of the copper plating must be greater than 5μm) in the coloring solution below and shake continuously. It will quickly turn brown and deepen over time. When it reaches a certain thickness, oxygen will start to precipitate; at this point, it should be removed, cleaned, and dried for polishing, or the colored piece can be rubbed with leather scraps in a drum. The surface layer of the convex part is ground away to reveal some of the original copper color. The parts will exhibit a gradient of color from light to dark from the convex to the concave surfaces, creating an elegant antique style. This antique color tone is favored in craft ornaments on the international market. The typical process specification for achieving antique copper color is 40~120g/L basic copper carbonate, 200ml/L ammonia, reacting at room temperature for 5~15 minutes.
- Copper coloring blue. Optional copper coloring blue process scheme: 130g/L copper sulfate, 13g/L ammonium chloride, 30ml/L ammonia, and 10ml/L acetic acid react for several minutes at room temperature.
- Copper coloring green. Optional copper coloring green process schemes: 32g/L calcium chloride, 32g/L copper nitrate, 32g/L ammonium chloride, react for a few minutes under 100℃.
- Copper coloring ancient green. Optional copper coloring ancient green process specifications: 5~10g/L sulfuric acid brocade, 10~15g/L ammonium sulfate, 25~30g/L sodium thiosulfate, water 200 ml, react for several minutes under 30~50℃.
- Copper coloring brown. Optional copper coloring brown process specifications: 6g/L copper sulfate, 4g/L copper acetate, 1g/L alum, react for 10 minutes under 95~100℃.
- Copper coloring golden yellow. Optional copper coloring golden yellow process schemes: 0.8g/L potassium sulfide, 1g/L ammonium sulfide, 0.3g/L barium sulfide, 4g/L sodium sulfide, 0.13g/L potassium permanganate, and 0.7g/L hydrogen peroxide react for several minutes at room temperature.
- Copper coloring red. Optional copper red process scheme: 25g/L copper sulfate, 200g/L sodium chloride, react for 5~10 minutes under 50℃.
- Copper coloring black. Optional copper blackening process schemes: 5~12.5g/L potassium sulfide and 20~200g/L ammonium chloride, which react for several minutes at room temperature.
(3) Chemical Coloring Process of Copper Alloys
Coloring with brass is relatively simple, with copper alloys followed by bronze, aluminum, and band bronze. The chemical coloring of copper alloys is widely used in craft jewelry.
- Copper alloy coloring red. Optional copper alloy red process schemes: 2g/L iron nitrate, 2g/L sodium sulfite, react for a few minutes under 75℃.
- Copper alloy coloring orange. Optional copper alloy orange process schemes: 25g/L sodium hydroxide and 50g/L copper carbonate, which react for a few minutes under 60~75℃.
- Copper alloy coloring brown. Optional process scheme for brown copper alloy: 12.5g/L barium sulfide, reacting for several minutes under 50℃.
- Copper alloy coloring chocolate color. Optional processes for copper alloy with chocolate color: 25g/L copper sulfate, 25g/L ammonium nickel sulfate, 25g/L potassium chlorate, react for a few minutes under 100℃.
- Copper alloy coloring ancient green color. Optional processes for achieving the ancient green color of copper alloy: 350g/L ammonium chloride, 200g/L copper acetate, react for a few minutes under 100℃.
- Copper alloys coloring blue. Optional processes for blue copper alloys: 2g/L sodium sulfite, 1g/L lead acetate, react for a few minutes under 100℃.
- Copper alloy coloring black. Optional process scheme for blackening copper alloy: 25g/L copper sulfate, a small amount of ammonia, reacts for a few minutes under 80~90℃.
(4) Factors Affecting Coloring Effects
The chemical coloring of copper and copper alloy jewelry is sometimes unstable, and the main factors affecting the coloring effect are the following three.
① The influence of substrate composition. Generally speaking, substrates with a high copper content are more likely to achieve a pure and attractive appearance. As the copper content decreases, the presence of other alloying elements, which are more reactive than copper, will affect the purity of the corrosion products and the color of the copper coating. For example, the corrosion products of zinc, tin, aluminum, etc., will mix white hydroxides into the film layer, causing the film layer to appear white. In this case, the content of stabilizers can be appropriately increased. When a β phase is present in the material’s metallographic structure, due to its poor corrosion resistance, severe pitting will occur, resulting in a large accumulation of zinc hydroxide at the pit openings, leading to obvious white spots and rendering the material unusable. At this time, reducing the stabilizer content can achieve good results.
② The impact of the workpiece surface condition. For deep-drawn or deep-stretched parts, in areas of severe deformation, 80% mechanical energy is stored in the form of crystal defects such as dislocations and vacancies, which have high chemical reactivity, leading to localized color differences. Stress relief annealing can be used to eliminate these issues. Additionally, the consistency of the surface roughness of the parts also has a certain impact on color consistency.
③ The impact of special climatic conditions. The coloring of copper alloy jewelry after applying the coloring solution may experience instability due to changes in climate during the color development reaction in the air. There may be insufficient or excessive reaction time for special climates, which requires appropriate control of the coloring time to resolve.
2. The Coloring Process of Silver and its Alloy Jewelry
The coloring treatment of silver and its alloys is mainly used for decorative craft jewelry, forming sulfides on its surface, which can create shades of black, blue-black, light gray, dark gray-green, gray-green, ancient silver, yellow-brown, green-blue, and so on.
(1) Silver Coloring Ancient Silver Color
Selectable silver alloy antique silver color process scheme: 25g/L potassium sulfide, 38g/L ammonium chloride, and 2g/L barium sulfide react at room temperature until the desired tone is reached.
(2) Silver Coloring Black
Selectable silver alloy with black process scheme: 15g/L potassium sulfide, 40g/L ammonium chloride, and a small amount of ammonia water react under 80℃ until the desired tone is reached.
(3) Silver Coloring Blue-Black
Selectable silver alloy with blue-black color process scheme: 2g/L potassium sulfide, 6g/L ammonium chloride, reacting under 60~80℃ until the desired hue is reached.
(4) Silver Coloring Blue and Yellow
Selectable silver alloy with blue-yellow process scheme: 1.5g/L potassium sulfide, reacting under 80℃ until the desired hue is reached.
(5) Silver Coloring Green
Selectable silver alloy with blue-green process scheme: 300g/L hydrochloric acid and 100g/L iodine react at room temperature until the desired hue is reached.
(6) Silver Coloring Yellow-Brown
Selectable silver alloy yellow-brown process scheme: 5g/L barium sulfide reacts at room temperature until the desired hue is reached.
3. Coloring Process of Zinc and its Alloy Jewelry
The surface conversion film formed by chromate passivation treatment of zinc and its alloys also has coloring functions, generally resulting in various colors such as rainbow, grass green, brownish yellow, green, military green, and black.
(1) Zinc Coloring Black
Selectable zinc blackening process: For 10~15 minutes, 40~50g/L copper sulfate and 30~40g/L potassium chloride react at room temperature.
(2) Zinc turns red
Selectable zinc red process scheme: copper sulfate, tartaric acid, and ammonia react at room temperature for minutes.
(3) Zinc Coloring Red
Selectable zinc coloring red craft scheme: 60g/L copper sulfate, 80g/L sodium carbonate, 60ml/L potassium bitartrate, react at room temperature for 3~5 minutes.
(4) Zinc Alloy Coloring Gray
Selectable zinc alloy gray coating process scheme: 20~25g/L copper sulfate, 50ml/L ammonia, 30g/L ammonium chloride, react for 3~5 minutes under 20~25℃.
(5) Zinc Alloy Coloring Green
Selectable zinc alloy green process scheme: 80~100g/L potassium dichromate, 25~30g/L sulfuric acid, 150g/L hydrochloric acid, react for 0.5~1 minutes under 30~40℃.
(6) Zinc Alloy Coloring Black
Selectable zinc alloy blackening process: 140~160g/L copper sulfate and 80~90g/L potassium chlorate react for 3~5 minutes under 20~25℃.
4. The Oxidation Coloring Process of Stainless Steel Jewelry
Stainless steel anodizing refers to forming an anodized color layer on the surface of stainless steel. It utilizes the colorless and transparent oxide film to create color through light interference, resulting in a durable hue formed by this film layer.
Typical methods for coloring stainless steel through oxidation include chemical and oxidation coloring methods. Chemical coloring methods include the Inco method and the Acheson method. The Inco method involves immersing the steel in a high-temperature sulfuric acid solution for coloring. In contrast, the Acheson method involves electrolysis in a medium-temperature solution to form a thin oxide film on the stainless steel surface, with color controlled by changing the thickness of the oxide film. The oxidation coloring method involves heating in the atmosphere or a controlled atmosphere to form an oxide film; this method is simple, but it is difficult to control the color, so it is limited to small stainless steel ornaments.
(1) Inco Method
In 1972, Inco established the color management and color-enhancing film technology for the acidic solution oxidation method, and its processing steps are as follows:
Pre-treatment → Water washing→Color development treatment→Water washing→Hard film treatment→Water washing→Drying
After pretreatment, the stainless steel plate is immersed in a 80~85℃ mixed solution of chromic acid and sulfuric acid. This treatment can form a chromium-based oxide film on the surface of the stainless steel, which can vary in thickness from hundreds to thousands depending on the treatment time. Due to light interference, colors can appear in the order of tea color: blue, gold, purple, green, etc. The growth of the oxide film, that is, the color change, can alter the immersion potential of the stainless steel, mastering this potential change for color management is the first feature of the Inco method (color development process). However, the color development film is porous at this stage and has poor wear resistance. Therefore, cathodic electrolysis should continue in a mixed aqueous chromic acid and phosphoric acid solution to strengthen the color development film. This treatment can seal the pores of the porous color development film, significantly improving wear and corrosion resistance. This is the second characteristic of the Inco process (hard film treatment).
Due to some issues with the process, the color in this technology is difficult to control, and the management requirements for raw materials are strict.
(2) Acheson Method
In 1985, Kawasaki Steel successfully developed the alternating current electrolysis method, also known as the Acheson method. This method involves electrolyzing stainless steel in a mixed solution of chromic acid and sulfuric acid below 60℃, forming an oxide film on the surface. Due to the repeated alternating anode electrolysis for a specified number of times, coloration and film hardening can occur simultaneously. Color control can be achieved by controlling the total electric charge. Stainless steel colored using the Acheson method has bright colors and can display unique colors such as bronze and yellow.
The color of the stainless steel surface mainly depends on factors such as the chemical composition of the surface film, its microstructure, surface smoothness, film thickness, and the angle of incident light. Generally, thin oxide films display blue or brown, medium thickness films show golden yellow or red, thick films appear green, and the thickest ones appear black. Overall, the coloring process of stainless steel is relatively difficult, with high process requirements, and its color uniformity is not easy to control.
5. Anodizing Treatment of Aluminum Alloy Jewelry
Aluminum alloy jewelry are widely colored using the anodizing method. Aluminum is one of the easiest metals to color. Through anodizing treatment, a thick and dense oxide film layer is formed on the aluminum surface, significantly changing the corrosion resistance of the aluminum alloy and improving hardness, wear resistance, and decorative performance. The methods for coloring aluminum oxide films mainly include electrolytic coloring, chemical dyeing, and electrolytic dyeing.
(1) Electrolytic Coloring Method
Electrolytic coloring is the process of anodizing and coloring completed in the same solution, directly forming a colored oxide film on aluminum alloys. Therefore, the electrolytic coloring method is also known as the one-step electrode coloring method. Electrolytic coloring is caused by the selective absorption of certain wavelengths of light by the film layer while the remaining wavelengths are reflected. The selective absorption is related to the oxidation state of the alloying elements in the film layer or the state of the electrolyte composition combined with the substances in the oxide film.
(2) Chemical Coloring Method
The anodic oxide film of aluminum jewelry can be impregnated and colored with inorganic or organic dyes. The coloring agents are deposited in the upper part of the pores of the oxide film. The most suitable oxide film for coloring is obtained through sulfuric acid anodization.
(3) Electrolytic Coloring Method (Two-Step Electrolytic Coloring Method)
After anodizing aluminum or aluminum alloys, they are immersed in a solution of more expensive metal salts, and coloring is achieved by using alternating current for polarization or direct current for cathodic polarization. Under the action of the electric field, metal ions are reduced and deposited at the bottom of the pores in the oxide film, resulting in the coloring of aluminum and its alloys.
Section V Physical Vapor Deposition Process
Physical Vapor Deposition is abbreviated as PVD. Physical Vapor Deposition is a physical vapor reaction growth method, and the deposition process occurs under vacuum or low-pressure gas discharge conditions. The source of the deposited material is a solid material, which, after “evaporation or sputtering,” generates a new solid material deposition layer on the surface of the part that is completely different in performance from the substrate.
Physical vapor deposition technology is increasingly applied to jewelry, with surface decorative coatings for crafts. The colors of the coatings are diverse, including deep gold, light gold, coffee, antique bronze, gray, black, gray-black, and multicolored, which can significantly improve the appearance color of craft jewelry and enhance characteristics such as wear resistance and corrosion resistance.
1. Classification of Physical Vapor Deposition Processes
Physical vapor deposition processes are divided into several types, including vacuum evaporation coating, ion plating, and magnetron sputtering coating, with the latter two belonging to the category of plasma vapor deposition. The deposition of the film layer occurs under low-pressure plasma gas discharge conditions, where the film layer particles gain higher energy in the electric field, resulting in significant improvements in the organization, structure, and adhesion of the film layer compared to vacuum evaporation coating. With the development of high technology, various new technologies for ion plating and magnetron sputtering coating have gradually matured and are continuously promoted and applied in various fields.
(1) Vacuum Evaporation Coating
Vacuum evaporation coating (evaporation) is vaporizing and evaporating the coating material through high-temperature heating under vacuum conditions and depositing it on the substrate surface to form a solid thin film. Evaporation technology is one of the earlier developed technologies in vacuum coating technology. Compared to sputtering and ion plating, the evaporation method is relatively simple, but under appropriate process conditions, it can produce very pure, thin film coatings with specific structures and properties. Therefore, evaporation technology still plays an important role in optics, semiconductor devices, and plastic metallization fields.
The vacuum evaporation coating has the following technical characteristics:
- The vacuum evaporation coating process includes the evaporation of the coating material, the transport of vapor atoms, and the nucleation and growth of vapor atoms on the substrate surface, which consists of evaporation, transport, and deposition.
- The deposition vacuum of vacuum evaporation coating is high, generally at 10-3~10-5Pa. The film layer particles hardly collide with gas molecules or other metal vapor atoms, reaching the workpiece directly.
- The energy of the film layer particles reaching the workpiece is the thermal energy carried during evaporation. Since the workpiece is not biased in vacuum evaporation coating, the metal atoms rely solely on the vaporization heat during evaporation, which is approximately 0.1~0.2eV. Therefore, the energy of the film layer particles is low, the bonding strength between the film layer and the substrate is small, and it isn’t easy to form compound coatings.
- The vacuum evaporation coating layer is formed under a high vacuum, and the layer particles in the vapor are atoms state, forming small cores on the surface of the workpiece, growing into a dense structure.
- The vacuum evaporation coating layer is obtained under high vacuum conditions. Generally, the coating can only be deposited on the side of the workpiece facing the evaporation source. In contrast, the side and back of the workpiece hardly receive any coating, resulting in poor coating quality.
(2) Magnetron Sputtering Coating
Under certain vacuum conditions, bombarding the surface of a material with charged particles of tens of electron volts or higher kinetic energy allows the atoms of the bombarded material to gain enough energy to escape the binding of the original material lattice and enter the gas phase. This technology is called sputtering technology. The sputtered gas phase elements are used for deposition to form a film, and this deposition process is referred to as sputter coating, as shown in Figure 11-9. When depositing hard coatings, the workpiece needs to be connected to a negative bias power supply called magnetron sputtering ion plating or bias sputtering.
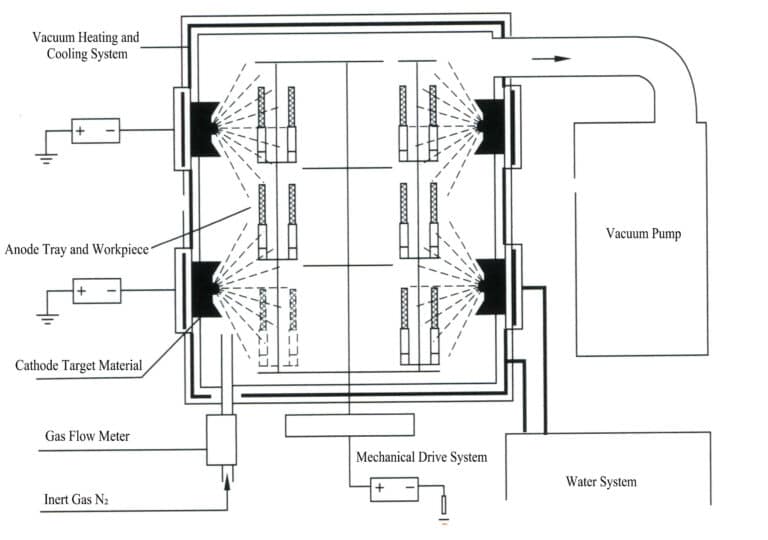
Sputter coating is currently the most widely used coating technology in PVD technology, with the following advantages:
- The quality of the sputtered coating is good, and the adhesion to the substrate is very strong.
- The application range of sputter coating is wide and suitable for various materials, and high melting point materials can also be easily sputtered.
- The thickness distribution of the sputter-coated film is relatively uniform.
- The sputtering coating process has good repeatability, is easy to achieve process control automation, and can be produced continuously on a large scale.
(3) Ion Plating
Ion plating is a process that takes place under vacuum conditions, using gas discharge to partially ionize gas or evaporated materials. While the gas ions or ions of the evaporated materials bombard the surface, the evaporated material or its reaction products are deposited onto the substrate.
In the following aspects, Ion plating combines the fast deposition rate of evaporation plating with the surface cleaning characteristics of ion bombardment in sputtering plating.
- The film layer has good adhesion to the substrate and dense film structure.
- It can improve the film’s ability to cover complex shaped surfaces, also known as the diffraction capability during the film deposition process.
- The controllable parameters of the film layer organization are numerous, the overall energy of the film layer particles is high, and it is easy to perform reactive deposition, allowing for the acquisition of compound coatings at lower temperatures.
2. The Application of PVD Coating Technology in the Jewelry Industry
2.1 Zirconium Nitride Decorative Coating
(1) Pre-Treatment for Coating
The vacuum coating process requires a high level of cleanliness for the sample surface and the vacuum furnace chamber, which is necessary for obtaining high-quality film layers. Therefore, the samples must be cleaned, and the vacuum furnace must be cleaned before coating.
Cleaning the sample surface is key to film formation. The sample surface must be clean and free of rust spots and oil stains, so the sample should be strictly cleaned before entering the furnace to remove oil, dirt, rust, and moisture. The cleaned sample should not be touched by hand to prevent secondary contamination.
The pre-treatment process flow for workpiece coating is as follows:
- Ultrasonic cleaning (1% metal cleaning agent), temperature: 50℃, time: 3 minutes.
- Ultrasonic cleaning (5% metal cleaning agent), temperature: 50℃, time: 2 minutes.
- Hot water cleaning, temperature: 50℃, time: 30 seconds.
- Rinse with cold water at room temperature for 30 seconds.
- Rinse with deionized water at room temperature for 20 seconds.
- Alcohol dehydration.
- Drying or air drying.
- Cleaning of the vacuum furnace. Wipe the dirt, attachments, and deposits inside the vacuum furnace with a dry cloth, and use a scraper to remove attachments from the corners.
(2) Coating Process Flow
① Pre-evacuation. After the sample is placed in the vacuum chamber, close the furnace door, turn on the mechanical pump for rough pumping, and when the vacuum reaches 0.1 Pa, turn on the oil diffusion pump for fine pumping. The vacuum process ends when the vacuum in the chamber reaches 6.5×10-3Pa.
② Glow discharge cleaning. The function of glow discharge cleaning involves many electrons moving toward the anode during the cleaning process. The high-speed movement of electrons ionizes the argon gas in the vacuum chamber, creating a glow phenomenon and generating softer argon ion movement. The moving argon ions, under the influence of the biased electric field, bombard the surface of the workpiece, colliding and removing the adsorbed gases and impurity atoms from the surface, exposing a clean surface of the workpiece material. At the same time, it increases the micro-roughness of the workpiece surface, which is beneficial for enhancing the bonding strength between the film layer and the workpiece. After introducing a certain argon gas flow to raise the pressure to 4×100Pa in the furnace, the bias power supply applied to the workpiece is turned on (the voltage and pulse duty cycle are adjustable). Here, the bias value is positive, and argon ions are used to clean the furnace wall, target surface, workpiece, and turntable. The cleaning time is determined based on the material and cleanliness of the workpiece.
③ Main bombardment. The role of the main bombardment is to apply a negative bias to the workpiece, which accelerates a large number of target material ions that are sputtered out. Positively charged target material ions move towards the workpiece under the influence of the negative bias, forming high-speed ion clusters with considerable energy. These ion clusters perform a certain degree of cleaning, activation, and implantation on the workpiece. The effect of the main bombardment: a large number of metal ions are implanted into the surface of the workpiece, and the implanted ions cause lattice restructuring with the substrate. Some metal ions with slightly lower energy levels produce a diffusion layer due to smaller implantation forces. Ions moving toward the workpiece may collide with it, and some will sputter and eject due to lower energy levels or differing incident angles. These ions will then collide with the next moving ions, forming secondary energy-level ions that ultimately deposit on the surface of the workpiece.
After cleaning, the vacuum chamber continues to evacuate to achieve 6.5×10-3Pa. Then, a certain flow rate of argon gas is introduced to achieve a total pressure of 0.3 Pa in the furnace; the values of pulse bias and duty cycle are adjusted (specific values depend on the requirements of the film layer); the power (voltage, current) of the cathode target’s intermediate frequency power supply is set to a certain value; the sample is subjected to main bombardment, with the bombardment time determined by process requirements.
④ Adding nitrogen gas for deposition coloring. At the end of the main bombardment process, an appropriate flow of reaction gas N2 will be introduced (at this time, the vacuum degree will slightly decrease). Manually adjust the nitrogen flow meter’s potentiometer to control the nitrogen flow based on the partial pressure of nitrogen (percentage) displayed by the mass spectrometer. At this time, the pulse bias, duty cycle, and the power (voltage, current) values of the cathode target’s intermediate frequency power supply can be adjusted according to process requirements; the sample is subjected to deposition coloring, and the deposition time is determined based on process requirements. In this way, metal ions will move towards the workpiece under appropriate bias, and during the movement, they will collide with the reaction gas to form a metallic compound film. At the same time, the movement speed will also decrease and deposit on the surface of the workpiece.
⑤ Passivation. The role of passivation is that the freshly coated film layer is a relatively active structure with a certain temperature. If it comes into contact with the atmosphere immediately, it will react again, causing a color change. Therefore, after the coating is completed, it should be cooled down, and a suitable amount of argon gas should be introduced, which protects the surface film layer of the workpiece with inert gas, allowing the film layer to be more stable with the temperature decreasing; on the other hand, it allows the target surface to absorb a large amount of argon gas and become saturated, thereby maintaining a fresh target surface and preventing the target surface from absorbing other gases after being filled with atmosphere, thus protecting the sputtering target surface from contamination. The maximum argon gas flow during the filling process is about 2 minutes.
⑥ Inflatable cooling. When the temperature of the vacuum chamber drops to 120℃, it introduces air to atmospheric pressure.
⑦ Opening the furnace and take out the sample. Open the furnace door, put on clean gloves to remove the sample, and seal the sample for color measurement, film thickness measurement, and Auger semi-quantitative analysis.
(3) Color Control of Zirconium Nitride Film
As a decorative ZrN gold-like film, the color of the film layer is particularly crucial. Due to the numerous process parameters of the medium-frequency reactive magnetron sputtering technology, many factors affect the film’s color. Under certain other process parameters, the nitrogen partial pressure and sputtering power are vital in the film’s color. As the nitrogen partial pressure increases, the color of the ZrN film changes from silver-white→light yellow→gold yellow→reddish gold→deep red. As the sputtering power increases, the color of the ZrN film changes from deep yellow→gold yellow →light yellow. By comparing the colors of ZrN films with those of gold and gold alloys, the desired gold yellow can be obtained by adjusting the nitrogen partial pressure during deposition.
2.2 Titanium Nitride Decorative Coating
(1) Magnetron Sputtering Technology for the Deposition of Titanium Nitride Process
① Install the workpiece. After installing the workpiece on the workpiece fixture, close the coating chamber.
② Vacuum extraction. Start the vacuum pump, and when the vacuum degree reaches 6 Pa, open the diffusion high spring and extract the vacuum to achieve 6×10-3Pa.
③ Baking heating. Turn on the baking heating power supply to heat the workpiece to the predetermined temperature.
④ Bombardment purification. Introduce working gas into the coating chamber, maintain a vacuum degree of 1~3Pa, bombardment voltage of 1000~3000 V, the workpiece generates glow discharge, argon ions bombard and purify the workpiece, bombardment for 10~20 minutes.
⑤ Titanium nitride deposition. First, deposit the base layer, reduce the workpiece bias to about 500 V, introduce argon gas, and adjust the vacuum to 0.3~0.5Pa. Turn on the magnetron sputtering target power supply. A glow discharge occurs on the target surface, and a high-density flow of argon ions ejects titanium atoms from the target surface. Next, deposit the titanium nitride coating, requiring the introduction of nitrogen gas, with the vacuum maintained within the range of 0.5~0.7Pa. Due to the balanced metal ionization rate of the magnetron sputtering being only 5%~10%, the reactivity of the metal is relatively low, resulting in a narrow process range (nitrogen content) for obtaining nitrogenized needle-like compounds coating. Compared to glow discharge, to achieve high-quality titanium nitride coatings, it is essential to strictly control the amount of titanium sputtering and the argon-nitrogen ratio. Otherwise, the deposition rate will be very low, and the color will be difficult to control.
⑥ Remove the workpiece. When the film thickness reaches the specified requirements, inflate the coating chamber, open the coating chamber, and remove the workpiece.
(2) The Effect of Process Parameters on the Properties of Titanium Nitride Films
① The effect of deposition temperature on the properties of nitride thin films. The deposition temperature affects the hardness and structure of TiN coatings; the hardness and adhesion of the TiN film deposited near 500℃ are the highest. Excessive and high temperatures are detrimental to the surface hardness of the TiN film. If the deposition temperature is too low, it reflects a short pre-sputtering time or low sputtering energy, affecting the film’s density, leading to insufficient nucleation of the TiN film and coarsening of the structure, resulting in a decrease in hardness. Conversely, if the deposition temperature is too high, it can cause overheating on the sample surface. Suppose the deposition temperature exceeds the tempering temperature of the substrate material. In that case, it will reduce substrate hardness, preventing a good bond with the film and causing a decrease in film hardness. Therefore, increasing the deposition temperature is beneficial for improving the hardness of the TiN film, provided that the sample surface does not overheat.
② The effect of deposition voltage on the properties of titanium nitride films. As the deposition voltage increases, the fracture morphology of the prepared TiN films becomes finer, and the microhardness and the deposition rate of the films increases. Increasing the discharge voltage under the same deposition conditions also means enhancing the plasma intensity, which promotes the chemical reactions in a direction favorable for product formation. Therefore, increasing the deposition voltage can increase the deposition rate of TiN films.
③ The effect of the workpiece on the performance of titanium nitride films. The quality of the film’s performance on the workpiece is not only related to the properties of the film itself but also to the properties of the workpiece material, especially the hardness of the workpiece material. Hard films exhibit their superior wear resistance only on relatively hard substrate materials. If the hardness of the substrate material varies, the bonding strength between the TiN film and the substrate will also differ. The greater the substrate hardness, the better the bonding between the TiN film and the substrate. In practical applications, efforts should be made to maintain a high hardness of the substrate material under certain deposition temperature conditions to improve the quality of the film. The smaller the surface roughness of the substrate, the higher the bonding strength between the titanium nitride film and the substrate, with polishing being the best for substrate surface roughness.
Section VI Enamel Craftsmanship
Enamel is a beautiful and colorful craft art made by attaching various colored glazes to a metal base (using materials such as gold, silver, copper, titanium, etc.) and firing it at high temperatures. Enamel colors are vibrant, have a gem-like luster and texture, resist corrosion, wear, and high temperatures, are waterproof and moisture-proof, are hard and solid, and do not age or deteriorate. Enamel has a long history of application in craft jewelry; in ancient centuries, it was used in the design of various decorative items for jewelry boxes, and by the 15th century, watchmakers incorporated it into watchmaking, adding bright colors to watches. The meticulous firing methods of enamel are intriguing, and its rich color expressiveness has pushed it to the forefront of fashion trends. Enamel jewelry wins with color and often attracts the attention of jewelry designers, especially when enamel is used for surface decoration on metal jewelry, greatly enhancing the artistic expressiveness of the pieces.
Enamel is commonly known as “Shaoqing” in southern China, “Shaolan” in northern China, and “shippō-yaki” in Japan.
The processing methods of jewelry enamel are divided into three types: painted enamel, champlevé enamel, and cloisonné enamel.
(1) Painted Enamel
The enamel painting craft originated in Western Europe and France and was brought to Guangdong by European merchants and missionaries during the Kangxi period of the Qing Dynasty. The art of painted enamel was first manufactured in Guangdong, where it is commonly referred to as “Shaoqing,” “Guang enamel,” or “Foreign enamel.” The emperor and ministers quickly appreciated and valued this exceptionally exquisite craft upon its arrival in China. During the Qing Dynasty, Emperors Kangxi, Yongzheng, and Qianlong established enamel workshops in both the Beijing Imperial Palace and Guangdong, and they frequently selected outstanding enamel painters from Guangdong to serve in the capital, producing large quantities of enamelware and enamel jewelry for royal use.
Painted enamel is the most difficult of the three main types of enamel techniques. The biggest advantage of painting directly on metal is that the patterns and lines can be richer, allowing for more detailed and complex designs that are unrestrained. However, omitting the step of using metal wire to outline will greatly increase the difficulty of firing the enamel. First, there is the issue of color mixing between different colors; without metal wire to separate the different colors, if the enamel materials are not mixed properly, it can lead to a chaotic situation of color bleeding.
Making painted enamel involves applying several layers of white glaze, or porcelain white, onto a metal base. Porcelain white is a white solid that must be ground into powder and mixed with appropriate water. A small brush can be applied evenly on the metal base. The firing temperature for porcelain is generally between 720~820℃. After sintering, a white base plate is obtained, and various colors of enamel are painted on this base plate, intricately depicting patterns like in oil painting. The biggest issue is color mixing; if the colors are mixed too much, the patterns will become blurred after sintering, ruining the artwork. Therefore, after depicting a section, it must be sintered first. The next section can be painted, followed by another sintering, which must be repeated until the work is completed. Sometimes, it requires dozens of repetitions of sintering, and if it gets damaged at any point, the entire piece will be ruined, making the craft of painted enamel highly valuable.

(2) Cloisonné Enamel
The cloisonné enamel technique is relatively complex, yet it is the most familiar and proudest enamel craft for the Chinese, with the famous “Jingtai Blue” being a type of cloisonné enamel. Its characteristic is that metal wires are first used on a metal base to outline the pattern, fixed with a natural adhesive, and then welded onto the metal base. Different colors of enamel glaze are then filled into the outlined contours made from finely ground minerals and metal oxides. The metal pieces are placed in a special furnace at a temperature of 800℃ for firing, causing the glaze to change color due to the high temperature. Since different metal oxides require different temperatures to change color, the enamel pieces may undergo multiple firings. Finally, the metal wires are smoothed, and a colorless transparent protective agent is applied for protection.

(3) Champlevé Enamel
The technique is similar to cloisonné enamel. The surface patterns of metal ornaments are formed using techniques such as engraving, stamping, or etching. First, patterns are carved on the metal base, leaving grooves within the carved outlines. To create vivid patterns with lines of varying thickness, the enamel painter grinds the enamel paint into a powder, mixes it with a small amount of water, and then fills the grooves with enamel, brushing a thin layer of painted patterns. Once completed, it is left to air dry and then placed in a high-temperature kiln above for firing, with each layer of paint needing to be fired for 40~60 seconds in the high-temperature kiln of 800℃. After multiple repetitions of filling with enamel and firing and polishing, a smooth and lustrous work is ultimately formed.

Section VII Resin Casting Process
The resin casting process is widely used in popular jewelry. According to the nature of the resin, it is divided into two main categories: soft resin and hard resin. Soft resin has a lower hardness and is not suitable for grinding and polishing but can be used for surface coating of craft jewelry; hard resin has a high hardness and can be processed by grinding and polishing to achieve a smooth and shiny effect.
Generally, epoxy resin crystal drop glue is used, which is composed of high-purity epoxy resin, curing agents, and other substances. Its cured product has the characteristics of being water-resistant, chemically resistant, and crystal clear. In addition to providing good protection for the surface of craft ornaments, this crystal drop glue can also enhance the surface gloss and brightness. Adding various pigments to the glue can form a rich color series, further enhancing the surface decorative effect, making it suitable for surface decoration and protection of crafts made from materials such as metal, ceramics, glass, and acrylic.
Epoxy resin has a surface effect similar to enamel and is often used as a faux enamel product, sometimes referred to as “soft enamel.” However, there are significant differences between the two. Enamel is made from enamel pigments fired at high temperatures; it is very hard and stable, has good durability, and does not age or deteriorate, but is prone to metal oxidation and softening, making it unsuitable to use for ornaments inlaid with gemstones; resin belongs to the category of organic compounds made from plastic. Products of this type of plastic resin do not need to be sintered in a high-temperature furnace to achieve color. It is sufficient to apply liquid color resin on the metal and let it air dry naturally or dry it in a baking box, making the production simple and not harmful to the metal, suitable for the final treatment of inlaid gemstone jewelry. However, due to the material properties of the resin, it is not durable, not heat-resistant, and is prone to corrosion and wear. After a certain period, it is likely to show aging, fading, and loss of luster. It is of lower grade and does not retain value. The basic process of resin is as follows.
- First, prepare the necessary tools and equipment, such as weighing instruments, glue adjusting tools, workpiece carriers, drying equipment, and the workpieces for the dripping glue operation.
- Place or adjust the balance scale (electronic scale), oven, workpiece carrier, and workbench level.
- Weigh A glue using a dry and clean wide-mouth flat container while proportionally weighing B glue (generally at a weight ratio of 3:1)
- Use a round glass rod (or round wooden stick) to stir the AB mixture to the left, right, or in a clockwise or counterclockwise direction. At the same time, the container (vessel) is preferably tilted at an angle of 45° and continuously rotated, stirring for about 1~2 minutes.
- Pour the mixed AB glue into a soft plastic bottle with a pointed nozzle for dripping, and drop the glue onto the desired accessory position.
- When the area of the resin drop is slightly larger, or the amount of resin is relatively more, to accelerate the elimination of bubbles in the glue, a gas torch fueled by liquefied gas can be used to promote defoaming. During defoaming, the torch’s flame should be adjusted to a complete combustion state, and the flame should ideally be kept about 25 cm away from the surface of the workpiece. The movement speed of the torch should not be too fast or too slow; a moderate speed should be maintained.
- After the bubbles are eliminated, the workpiece can be placed horizontally in the oven for heating and curing. The temperature should first be adjusted to 40℃ around 30 minutes and then raised to 60~70℃ until the glue is fully cured.

Section VIII Etching Technology
Etching is the process of removing unwanted metal to a certain depth using chemical methods. Its principle is similar to the production of circuit boards, where the metal parts to be retained are covered with an acid-resistant coating, and then an acidic solution is used to etch away the unwanted metal parts; the processing of negative patterns is exactly the opposite of that of positive patterns.
The etching process is suitable for the processing and producing antique-style crafts and jewelry with special surface style requirements. In recent years, the export volume of metal paintings, crafts, and hollow art pieces processed by etching methods in our country has greatly increased, becoming a new branch of craft jewelry.
Etching processes can be divided into chemical etching, electrolytic etching, laser etching, and ultrasonic etching.
1. Chemical Etching Process
Cover the areas that need not be etched with a corrosion-resistant coating, then immerse the workpiece in a special etching solution. The formula for the solution is shown in the table 11-2. Ensure that the areas to be etched are in full contact with the solution, and if necessary, heating and stirring can be applied. Control the etching time based on the required etching depth and the etching rate obtained from experiments to achieve the desired etching result.
Table 11-2 Partial Metal Etching Solution Formulas
| Ingredients and process conditions | Etching stainless steel | Etching copper alloy | Etching aluminum |
|---|---|---|---|
| Ferric chloride | 600 ~ 800 | 600 ~ 650 | 450 ~ 550 |
| Hydrochloric acid/(g・L -1) | 80 ~ 120 | ||
| Phosphoric acid/(g・L -1) | 20 ~ 30 | ||
| Copper sulfate/(g・L -1) | 200 ~ 300 | ||
| Sulfuric acid/(g・L -1) | 90 ~ 100 | 10 ~ 20 | |
| Nitric acid/(g・L -1) | 8 ~ 12 | ||
| Etching accelerator/(g・L -1) | 80 ~ 100 | ||
| Temperatura/℃ | 10 ~ 45 | 15 ~ 50 | 20 ~ 40 |
| Time/min | 15 ~ 20 | 10 ~ 15 | 10 ~ 20 |
2. Electrolytic Etching
Section IX Nano ~ Spraying Plating Technology

1. The Principle of Nano ~ Spraying and Plating
2. Characteristics of Nano ~ Spraying Plating
(1) Green and environmentally friendly. No three waste emissions, non ~ toxic and harmless, no harmful heavy metals.
(2) Low investment and low cost. Compared to electroplating, the equipment investment is small, and there is no need to equip a wastewater treatment system.
(3) The operation is both safe and simple, with high efficiency. There will be no harm if the operator accidentally sprays it on their hands or other body parts. There is no need for water electroplating treatment and complex preliminary conductive layer treatment.
(4) It can be positioned for spray plating and can spray plate in different colors on the same product. Various colors at will.
(5) The processed parts are not limited by size and shape, are not restricted by various materials, can be recycled, and save resources.
(6) The application range of color diversity is extensive. The sprayed products can be coated with gold, silver, chrome, nickel, or sand ~ colored mirror effects. They can also be coated with various other colors, such as golden yellow, brass color, antique gold yellow, cannon copper color (red, yellow, purple, green, blue), and other high ~ gloss effects. It can be sprayed on various materials such as metal, resin, plastic, glass, ceramics, acrylic, and wood, and can be widely used in various surface decoration industries such as crafts and jewelry.
(7) Products made with nano ~ spraying have excellent adhesion, impact resistance, corrosion resistance, weather resistance, wear resistance, scratch resistance, and good rust prevention capabilities.
















