Co potřebujete vědět o zlacení a slitinách zlata
Ultimátní průvodce technikami a řešeními zlacení šperků
Úvod:
Jaké jsou různé typy roztoků pro zlacení a jejich vlastnosti? Jak můžete pro pokovování použít různé sloučeniny zlata? Proč zvolit pro své projekty tenké nebo silné zlacení? Tato komplexní příručka pokrývá vše od základů roztoků pro zlacení, včetně kyselých, neutrálních a bezkyanidových možností, až po podrobné postupy pro tenké a silné zlacení. Seznamte se s historií a moderními technikami používanými v tomto odvětví, které jsou ideální pro výrobce šperků, designéry a maloobchodníky, kteří chtějí vylepšit své výrobky odolnými a krásnými zlatými povrchovými úpravami.
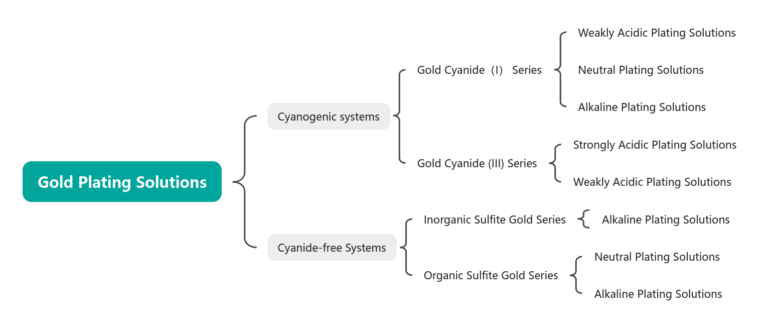
Klasifikace roztoků pro zlacení
Obsah
Oddíl I Přehled
V roce 1800 vynalezl profesor Lugi V. Brougnatell z Itálie techniku zlacení. V následujících více než 100 letech bylo v Evropě populární galvanické pokovování niklem, mědí a mosazí, přičemž jen několik galvanických továren provádělo zlacení hodinek, osobních ozdob a kovového nádobí, aby uspokojily požadavky několika bohatých lidí. Ve Spojených státech se mezitím hlavní pozornost soustředila na zlacení související s jemným zpracováním drahokamů.
V roce 1913 Frary zavedl relativně komplexní systém galvanického pokovování zlatem a stal se průkopníkem moderního galvanického pokovování.
V roce 1950 společnost EC Rinker jako první vyvinula technologii zlacení přidáním stopového množství stříbra do roztoků pro zlacení.
Následně byly vyvinuty a široce používány kyselé roztoky pro zlacení na bázi organických kyselin.
V roce 1952 E. A. Parker jako průkopník v aplikaci kyanidu draselného a zlata a uvedl, že přidání slabých organických kyselin (jako je kyselina citronová, kyselina vinná atd.) do pokovovacích roztoků kyanidu draselného a zlata částečně neutralizovaných alkalickými amonnými solemi může udržet pokovovací roztok stabilní při pH = 3.
V roce 1959 EC Rinker popsal technologii kyselého zlacení v rozmezí pH 3~5.
Technologie galvanického pokovování zlata se následně dočkala rozsáhlejšího a hloubkového výzkumu, včetně principů nanášení a analýzy fyzikálně-chemických vlastností.
S rostoucí poptávkou po moderní průmyslové výrobě dozrálo a stalo se praktickým mnoho aplikovaných technologií zlacení.
1. Typy a vlastnosti roztoků pro zlacení
Tabulka 1-1 Klasifikace roztoků pro zlacení
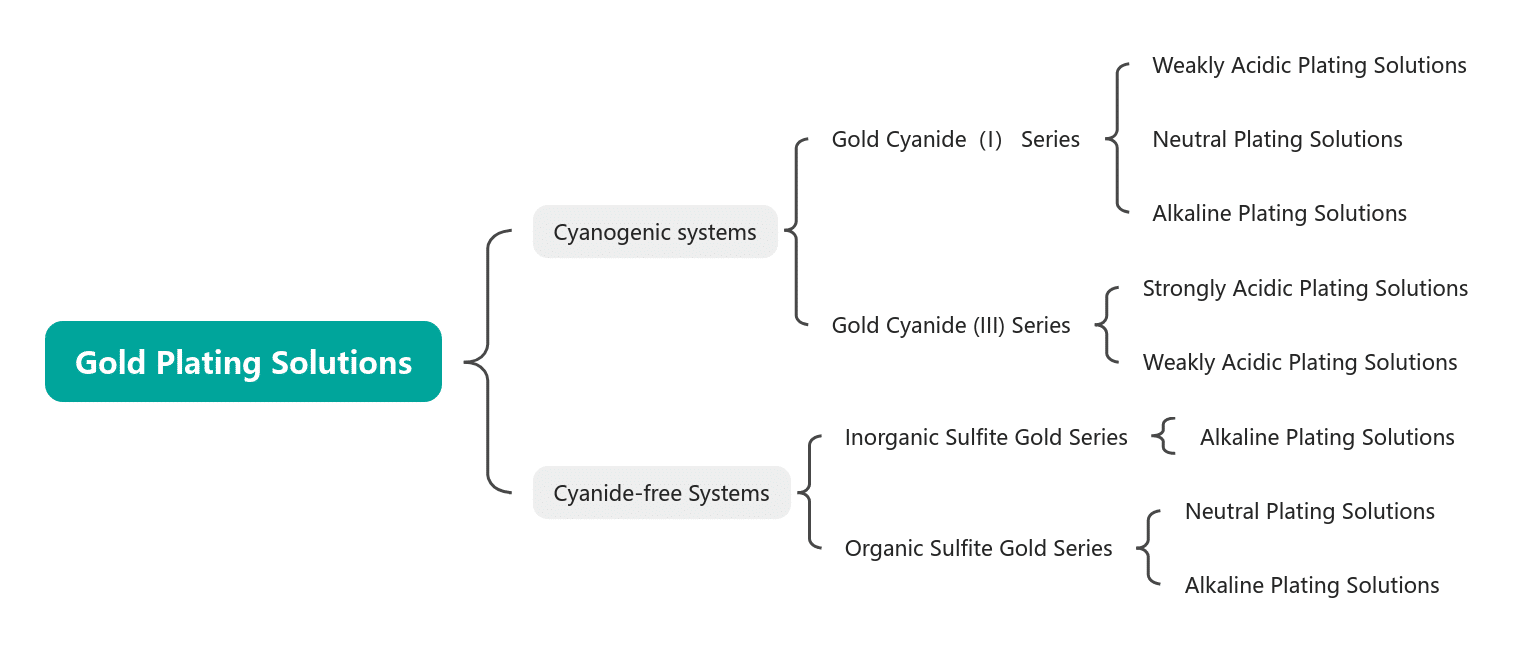
Tabulka 1-2 Charakteristiky různých typů roztoků pro zlacení
| Roztok pro galvanické pokovování | Zlatý ligand | Kyselost a zásaditost | pH | Vzhled | Zařízení |
|---|---|---|---|---|---|
| Kyselé zlacení Tvrdé zlacení | KAu(CN)2 | Slabě kyselý | 3~5 | Lesk | Konektory, kontakty, svorky, ozdobné díly |
| Neutrální zlacení Měkké zlacení Pletení z čistého zlata | KAu(CN)2 | Neutrální | 6~9 | Bez lesku | Deska plošných spojů, polovodičová |
| Kyanidové zlacení | KAu(CN)2 | Alkalické | 10~13 | Lesk | Dekorativní díly |
| Zlacení bez kyanidu | Na3Au(SO3)2 | Neutrální | 6 až 8 | Bez lesku | Zlaté obvodové vzory, desky plošných spojů |
| Alkalické | 8~12 | Lesk |
2. Sloučeniny zlata používané ke zlacení
Zlato má mnoho valenčních stavů, z nichž nejstabilnější jsou sloučeniny s valencí +3, následované sloučeninami s valencí +2, zatímco sloučeniny s valencí +5 se snadno rozkládají. Zlato(I) ve vodném roztoku má několik stabilních ligandů, jako jsou typické koordinační soli dihalogenaurátů(I), koordinační soli dikyanoaurátů, thiosíranové soli zlata(I) atd., z nichž kyanidy jsou velmi stabilní s konstantou stability K=4×1028Proto se sloučeniny zlata(I) a zlata(III) používají nejčastěji a jsou nejběžnější, zatímco sloučeniny zlata(II) a zlata(V) jsou také stále více chápány a používány.
Kyanid zlatodraselný (I) je dosud nejrozšířenější a nejběžnější hlavní solí pro zlacení. V posledních letech se častěji používají roztoky kyanidu zlatodraselného (III) a siřičitanu zlatosodného (I) pro pokovování.
1.1 Kyanid draselný a zlatožlutý, KAu(CN)2 (dále jen „kyanid draselno-zlatistý“)
(1) Relativní molekulová hmotnost hmotnost: 288,10. Mezi metody přípravy patří chemické metody a elektrolytické metody.
(2) Vlastnosti: Kyanid draselno-zlatistý připravený touto metodou je bezbarvý krystalický, snadno rozpustný ve vodě, mírně rozpustný v ethanolu a nerozpustný v acetonu a hexadekanolu. Snadno se rozkládá při zahřívání v kyselém prostředí, je stabilní na světle na vzduchu a jeho stabilita je výrazně vyšší než u podobných ligandů kyanidu mědi a stříbra.
(3) Metody přípravy
① Chemická metoda
a. Rozpouštění zlata: Vložte čisté zlato do zředěné lučavky královské (objemový poměr vody k lučavce královské je 1:4) a zahřívejte do rozpuštění → Po úplném rozpuštění bloku zlata snižte teplotu → Opakovaně po kapkách přidávejte kyselinu chlorovodíkovou, dokud se nepřestane tvořit hnědý oxid dusičitý → Pomalu zahušťujte, dokud se roztok nezmění na tmavě červenohnědý a neobjeví se drobný rolující lesklý redukovaný zlatý prášek.
b. Neutralizační reakce: Roztok ochlaďte na přibližně 25 °C. Za míchání → přikapejte nasycený roztok hydroxidu sodného → dokud se nevytvoří hnědočervená polotuhá látka → přidávejte kyanid draselný, dokud se roztok nestane bezbarvým a průhledným (s malým množstvím sražených agregovaných částic zlatého prášku).
c. Okyselení (příprava kyanidu zlata): Roztok se ochladí na přibližně 25 °C → Za míchání se po kapkách přidává kyselina chlorovodíková → dokud se nevytvoří jasně žlutozlatá sraženina kyanidu → Zamíchá se a nechá se zrát při nízké teplotě → Nechá se odstát, aby se vytvořily vrstvy, přirozeně se ochladí na pokojovou teplotu, odstraní se horní odpadní kapalina, přefiltruje se a žlutá sraženina se promyje teplou vodou.
d. Syntéza kyanidu draselného a zlata: Vložte kyanid zlata do malého množství vody → Za míchání přidejte odměřené množství nasyceného roztoku kyanidu draselného → dokud se roztok nestane bezbarvým a průhledným → Přefiltrujte, abyste odstranili zlatý prášek → Zahustěte → Ochlaďte, aby se krystalizoval → Odstraňte matečný louh → Usušte bílý krystalický kyanid draselného a zlata při 80 °C → Uzavřete a zabalte.
Při použití této metody k přípravě kyanidu draselného a zlata je výrobní zařízení jednoduché a dokáže účinně oddělit stopové nečistoty ve zlatě a připravit kyanid draselného a zlata vyšší čistoty.
② Membránová elektrolýza: Metoda Sovětský svaz jako první použil elektrolýzu s mikroporézní keramickou membránou k výrobě různých kovů a kovových sloučenin. Domácí i zahraniční společnosti obecně používají k výrobě kyanidu draselného a zlata elektrolýzu s organickými membránami. Tato metoda elektrolýzy však souvisí s problémem koroze organických membrán alkalickými elektrolyty a produkty koroze značně poškozují vysoce kvalitní integrované obvody, desky plošných spojů s vysokou hustotou a vrstvy zlata na kontaktech (společnost Suzhou University Special Chemical Reagent Industrial Company úspěšně vyvinula praktickou aplikaci).
1.2 Thiokyanát draselný (III), K[Au(CN4)]·H2O
(1) Relativní molekulová hmotnost: 358.15.
(2) Vlastnosti: Bezbarvé krystaly, snadno rozpustné ve vodě, se při zahřátí nad 200 °C stanou bezvodou solí, tají za červeného žáru a při vyšších teplotách se rozkládají.
(3) Způsoby přípravy:
① Zahřejte kyanid draselný-zlato v roztoku kyanidu draselného;
② Rozpusťte chlorid zlatý v K3[Fe(CN)6];
③ Rozpusťte dikyanid zlata(III) v K3[Fe(CN)6];
④ Zpracujte kyanid draselný-zlato bromem a výsledný K[Au(CN)2Br2] reaguje s kyanidem draselným v methanolu za vzniku produktu.
1.3 Chlorid zlata
(1) Chlorid zlata(I), AuCl
① Relativní molekulová hmotnost: 232,46.
② Vlastnosti: světle žluté nehygroskopické krystaly se začínají pomalu rozkládat při zahřátí nad 150 °C. Rozkládá se ve vodě a ethanolu a rozpouští se v roztoku chlorových alkalických kyselin za vzniku dichlorátu zlatého.
③ Způsob přípravy: Chlorečnan zlatý (HAuCl4, III) se umístí do vysokého vakua a zahřeje na 156 °C, aby se rozložil a získal produkt.
(2) Chlorid zlata (III), HAuCl4
① Relativní molekulová hmotnost: 303,37.
② Vlastnosti: Červené jehličkovité krystaly, bod tání 229 °C, bod varu 254 °C (rozklad), hygroskopické, vodný roztok je červenohnědý, tvoří H2[AuCl3O] v kyselém roztoku. V neutrálním vodném roztoku se pomalu rozkládá za vzniku zlata. Odpařením vodného roztoku vzniká oranžová krystalická dihydrátová sůl, rozpustná v ethanolu a etheru.
③ Způsob přípravy: Při teplotě mezi 225~250℃ se plynný chlór nechá projít zlatým práškem o tlaku 120~127 kPa (900-950 mmHg) za účelem přípravy. Alternativně rozpusťte zlato v lučavce královské, opakovaně přidávejte kyselinu chlorovodíkovou k odstranění kyseliny dusičné, poté pomalu zahřívejte při nízké teplotě k odstranění přebytečné kyseliny chlorovodíkové, zahustěte, ochladte a krystalizujte, čímž získáte produkt.
1.4 Oxid zlata(III), Au2O3
(1) Relativní molekulová hmotnost: 441,93.
(2) Vlastnosti: Černý (hnědý) prášek nebo krystalická polymerní struktura, sloučenina zlata obklopená atomy kyslíku tvořící planární tetrakoordinovaný komplex. Na slunečním světle se pomalu rozkládá, při zahřátí na 110 °C začíná uvolňovat kyslík, při 160 °C se stává oxidem zlata(I) a při 250 °C ztrácí veškerý kyslík, čímž se stává amfoterním oxidem nerozpustným ve vodě, ale rozpustným v kyselině chlorovodíkové a alkalických vodných roztocích.
(3) Způsob přípravy: Rozpusťte zlato v lučavce královské, opakovaně přidávejte kyselinu chlorovodíkovou a zahřívejte (5krát), aby se odstranila kyselina dusičná, přidávejte uhličitan sodný, dokud se nevznikne zásaditá sraženina, promyjte vodou, odstředěte, proveďte elektrodialýzu po dobu 2 týdnů a poté sušte při 140~150℃, aby se získal produkt.
Sekce II Tenké zlacení
Galvanické pokovování tenkým zlatým roztokem neboli kartáčovací zlatý roztok se liší od bleskového zlatého roztoku (strike plating). Kartáčovací zlatý roztok je obvykle založen na alkalických kyanidových kapalinách, přičemž existuje mnoho typů od čistého zlata až po slitiny, jako jsou pokovovací roztoky kyanidu draselného s různými ligandovými systémy. Některé společnosti také používají své vlastní speciálně vyvinuté pokovovací roztoky. Bleskové zlaté roztoky jsou většinou kyselé a mohou sloužit jako základní pokovovací vrstva pro silné vrstvy zlata, přičemž k vytvoření tenké vrstvy zlata se používá vyšší proudová hustota v krátkém čase, čímž se zlepší disperze a adheze horní silné vrstvy zlata.
Tabulka 1-3 ukazuje složení a provozní podmínky některých reprezentativních roztoků pro tenké zlacení kartáčem. Mezi nimi fosfát působí jako pufr a také jako vodivostní činidlo. Z nově připraveného roztoku pro zlacení lze dosáhnout dobrého povlaku, ale po elektrifikaci se v roztoku pro zlacení rychle tvoří nečistoty, které způsobují, že se na pokovené vrstvě snadno objevují barevné rozdíly. Hlavním důvodem je, že když teplota roztoku pro zlacení stoupá, kyanid podléhá rozkladné reakci. Proto je nutné roztok pro zlacení po určité době používání ošetřit, obvykle filtrací s aktivním uhlím.
Tabulka 1-3 Různá reprezentativní řešení pro tenké zlacení štětcem
| Komponenty | Řešení pro pokovování čistým zlatem | Hamiltonova barva | Bílá 1 | Bílá 2 | Zelenkavě zlatá | Červené zlato | ||
|---|---|---|---|---|---|---|---|---|
| Žlutý | Růžová | Zelená | ||||||
| KAu (CN)2/(g/l) | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 0.41 | 0.33 | 2 | 0.82 |
| Volný KCN/(g/l) | 7.5 | 7.5 | 2.0 | 2.0 | 15 | 15 | 7.5 | 4 |
| K2HPO4/(g/l) | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
| K2Ni(CN)4/(g/l) | - | 0.26 | 0.26 | 0.26 | 1.1 | - | - | 0.21 |
| K2Cu(CN)3/(g/l) | - | 0.13 | 1.1 | - | - | - | - | 2.64 |
| K2Ag(CN)2/(g/l) | - | - | - | 0.05 | - | - | 0.26 | - |
| K2Sn(OH)6/(g/l) | - | - | - | - | - | 2.11 | - | - |
| Teplota pokovovacího roztoku / ℃ | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 65 ~ 70 | 65 ~ 70 | 55 ~ 70 | 55 ~ 70 |
| Hustota proudu/(A/dm2) | 1 ~ 4 | 1 ~ 3.5 | 2 ~ 5 | 1 ~ 4 | 3 ~ 6 | 3 ~ 5 | 1 ~ 3 | 3 ~ 4 |
Při galvanickém pokovování čistého zlata ovlivňují jiné kovy než zlato v pokovovacím roztoku významně barvu pokovované vrstvy. Měď zbarvuje pokovenou vrstvu znatelně do červena, nikl a zinek ji zbarvují do běla a olovo snadno způsobuje, že se na povrchu pokovené vrstvy usazují černé, skvrnité, drsné, šedohnědé látky. Barvu pokovených vrstev ze slitiny zlata lze proto dosáhnout přidáním různých kovů. V reálných procesech galvanického pokovování však není snadné dosáhnout ideálního barevného tónu.
Anoda roztoku pro zlacení obvykle používá nerozpustné anodové materiály, jako je nerezová ocel a černé platinovo-titanové síťové desky, a v závislosti na roztoku pro zlacení lze použít i uhlíkové desky. Po určitém proudu spotřebovaném roztokem pro zlacení by měl být pravidelně analyzován, aby se doplnila koncentrace zlatých iontů, ligandů a dalších aktivních složek. Pro automatický výpočet a doplnění denní práce lze použít ampérhodinový měřič. Během procesu tenkého zlacení dochází také k velkému odběru roztoku pro galvanické zlacení, který je nutné předem vypočítat, aby se doplnila spotřeba a ztráta času. Průběh procesu tenkého zlacení je znázorněn na obrázku 1-1.

V průběhu procesu je koncentrace roztoku pro bleskové zlacení přibližně 1/5 až 1/3 koncentrace hlavního pokovovacího roztoku (povrchové vrstvy nebo vrchní vrstvy zlata). Poté, co je povrch pokovené součásti zcela pokryt extrémně tenkou vrstvou zlata, se tato součást umístí do hlavního pokovovacího roztoku, aby se vrstva zlata pokovila požadovaným barevným odstínem.
Zbytky kyanidu na povrchu zlacené vrstvy mohou tvořit vodní skvrny, které ovlivňují vzhled a elektrické vlastnosti pokovení. Proto je nutné pokovené díly po zlacení důkladně vyčistit a vysušit. Kromě zahřívání pro sušení lze k dehydrataci použít speciální produkty s organickými rozpouštědly. Například dehydratace a sušení bezvodým ethanolem neovlivní barvu zlacené vrstvy a rychlost schnutí je také vysoká.
Vrstva zlatého pokovení štětcem je velmi tenká a obvykle se jich tloušťka kontroluje pod 0,1 μm. Na tenkou vrstvu zlata se při použití jako povrchová vrstva pokovení nanášejí různé organické ochranné filmy, které zabraňují snadnému opotřebení a změně barvy. Nejčastěji používanou organickou ochranou je akrylová melaminová pryskyřice s tvrdostí filmu přibližně odpovídající tvrdosti tužky 3H~4H a tloušťkou 10~15 μm. Pro elektroforetické pokovování se často používá aniontová akrylová melaminová pryskyřice.
Protože tenká vrstva zlatého pokovení rychle a rychle vytvoří jednotnou a konzistentní barvu, proces pokovování obvykle využívá pohyb katody nebo tryskové míchání pokovovacího roztoku. Řízením teploty pokovovacího roztoku, koncentrace iontů zlata a hustoty proudu se regulují podmínky pro potlačení barevných rozdílů v pokovované vrstvě.
Sekce III Silné zlacení
Tabulka 1-4 Složení a provozní podmínky pokovovacího roztoku a vlastnosti pokovovací vrstvy
| Zlatá sloučenina | Typy galvanického pokovování | Vodivé soli | pH slitiny kovu | Složení | Struktura sraženiny | Charakteristika |
|---|---|---|---|---|---|---|
| Chlorid draselný a zlato | Slabá kyselost | Kyselina citronová, oregano-fosforečná, kyselina aminosulfonová, kyselina vinná, kyselina šťavelová | Čisté zlato, kobalt, nikl, železo, indium, cín 3,0~5,0 | Kyselina citronová + citrát sodný 80~100 g/l Kyanid draselný a zlato 8 g/l Sulfamát nikelnatý 3,0 g/l Octan zinečnatý 0,5 g/l | Vrstevnatá struktura s eutektickou vrstvou organického polymeru mezi vrstvami | Dokáže získat jasné a tvrdé sraženiny; pokovovací roztok se snadno upravuje a je možné provádět pokovování za nízkých teplot. |
| Neutrální | Kyselina fosforečná, kyselina sírová, kyselina boritá, organické kyseliny | Čisté zlato, sraženina, krystalový modifikátor: titan, selen 5,0 ~ 8,0 | Kyanid draselný a zlatý 2 ~16 g/l Citrát draselný 120 ~150 g/l Fosforečnan draselný 10~50 g/l Síran amonný 20~150 g/l Jeden z Ti, Ce, Te, Bi 0,01~40 mg | Sloupcovité nebo jehličkovité krystaly, méně časté srážení nečistot | Vrstva čistého zlata 99.99%; vysrážená praktická měkká, pololesklá nebo matná silná vrstva pokovování; akumulace nečistot ovlivňuje životnost pokovovacího roztoku. | |
| Alkalické | Kyanid, uhličitan, kyselina pyroforová | Čisté zlato, stříbro, kadmium, zinek, antimon 8,5 až 13,0 | Čisté zlato, stříbro, kadmium, zinek, antimon 8,5 až 13,0 | Hranice zrn s precipitací kyanidových polymerů | Lze získat velmi rovnoměrnou silnou vrstvu zlata o tloušťce přibližně 300 μm; lze získat pokovovací vrstvu z čistého zlata až po slitinu 9K; necitlivost na nečistoty, snadná manipulace s pokovovacím roztokem |
(1) Úloha polyethyleniminu – organických sloučenin s vysokou molekulovou hmotností polyaminu: Organické sloučeniny se selektivně adsorbují v Helmholtzově dvojité elektrické vrstvě, čímž se zesiluje polarizační efekt. Během procesu elektrolytického nanášení se organické látky kontinuálně adsorbují na aktivní růstové body, čímž inhibují nanášení a pohyb zlata po povrchu katody, což vede k hladkému a lesklému povrchu. Určité množství organické hmoty, která se ko-deponuje do mřížky nanesených krystalů, však vážně nepříznivě ovlivňuje fyzikální vlastnosti pokovené vrstvy, zejména její odolnost proti opotřebení. Obecně se to zlepšuje přidáním dalších kovů za účelem ko-depozice, která zlepšuje nepříznivé účinky organických látek.
(2) Úloha dalších polokovů, jako je arsen, thalium, selen a olovo: Přidání polokovů nejenže vytváří dobrou lesklou vrstvu zlatého pokovení z kyanidového roztoku zlatého pokovení, ale také dosahuje velmi lesklé vrstvy zlatého pokovení ze sulfitového roztoku zlatého pokovení. Obecně platí, že další množství pod 10-6 může vyvolat velmi zřetelný charakteristický efekt.
Princip zjasňování polokovů: polokovové látky se rovnoměrně adsorbují na povrchu katody, katalyzují, podporují nukleaci krystalů zlata, generují více růstových bodů a podporují rovnoměrnou krystalizaci a depozici.
(3) Úloha eutektika přechodných kovů kobaltu, niklu, železa atd.: Vrstva lesklého zlatého pokovení legovaná kobaltem a niklem obsahuje určité množství uhlíku. Pokud je obsah uhlíku nižší než 0,1%, nelze dosáhnout vrstvy lesklého zlatého pokovení, a to ani v případě, že kobalt podléhá eutektické reakci.
Izotop 14Experimenty s C prokázaly, že uhlík pochází z komplexního ligandu kobalt-kyanid. Rozpuštěním vrstvy zlatého pokovení obsahujícího kobalt a nikl v kyselém roztoku lučavky královské lze oddělit látky obsahující uhlík. Pod mikroskopem připomíná materiál ošetřený lučavky královskou plast. Tento membránovitý polymer vytváří na povrchu pokovené vrstvy velký kontaktní odpor.

1. Alkalické zlacení
Ze všech roztoků pro pokovování zlatem je alkalický kyanidový roztok pro pokovování zlatem nejstarším elektrolytickým roztokem pro pokovování zlatem. Alkalický kyanidový roztok pro pokovování zlatem se široce používá pro pokovování čistého zlata, zlatých slitin a dekorativního zlacení a lze jej použít i pro funkční elektronické zlacení. Pokovovací roztok se obvykle skládá z kyanidu draselného, volného kyanidu, uhličitanu draselného atd. Při pokovování zlatých slitin lze podle potřeby přidávat různé kovové soli.
Zlatění alkalickým kyanidovým roztokem zlatění vede k dobré rovnoměrnosti povlaku a smáčivosti a je velmi vhodné pro pokovování slitin zlata s nízkým obsahem zlata. Dokáže pokovovat vrstvy zlata od nízkých hodnot K do vysokých hodnot K. Pokovovací roztok má vysoký obsah volného kyanidu, takže je méně náchylný k nečistotám. Volný kyanid může rozpouštět zlato, takže pokovené předměty musí být po vyjmutí z pokovovací lázně ihned vyčištěny; jinak zbytky pokovovacího roztoku na povrchu způsobí vady, jako je například vlnitý vzhled.
Zlaté pokovování bez kyanidu se používá hlavně pro destičky, integrované obvody budičů pro displeje z tekutých krystalů, zlaté svařovací plošky pro obaly a obvody, svorky a další kontaktní body substrátu. U destiček zapojení s fotocitlivými rezistovými filmy je výška rohu zlatých svařovacích plošek několik desítek mikrometrů a tloušťka je 15~20 μm. Vyrobený CN- v kyanidovém zlacovacím roztoku může korodovat fotocitlivý rezistový film a ochranný film kolem substrátu; proto se většinou používají pokovovací roztoky bez kyanidu a slabě kyselé pokovovací roztoky.
Alkalické zlaticí roztoky jsou převážně kyanidové zlaticí roztoky s přidanými kovy od binárních po kvartérní; praktické vrstvy zlaceného zlata jsou binární nebo ternární slitiny zlata. Reprezentativní složení a provozní podmínky alkalických zlacených roztoků jsou uvedeny v tabulce 1-5.
Tabulka 1-5 Složení a provozní podmínky roztoku pro pokovování alkalickou slitinou zlata
| Druhy slitin | Složení a provozní podmínky | |
|---|---|---|
| Binární slitiny | Slitina zlata a mědi |
Kyanid draselný a zlatý 12 g/l Kyanid draselný-měďnatý 7 g/l Thiokyanid draselný 10 g/l 2-Pyridinkarboxylová kyselina 8 g/l pH 8 (upraveno pomocí KOH) 70 °C, 0,4 A/dm²2 |
| Slitina zlata a stříbra |
Kyanid draselný a zlatý 15 g/l Kyanid draselno-stříbrný 3 g/l Kyanid draselný-nikelnatý 20 g/l Kyanid kobaltu draselný 10 g/l Kyanid draselný 80 g/l Hydroxid amonný 20 g/l 15 °C, 0,6 A/dm²2 |
|
| Slitina zlata a cínu |
Kyanid draselný a zlatý 30 g/l Dusičnan cínatý 7 g/l Pyrofosforečnan draselný 100 g/l Pokojová teplota, 1 A/dm²2 |
|
| Ternární slitiny | Slitina zlata, mědi a kadmia |
Kyanid draselný a zlatý 15 g/l Kyanid draselný-měďnatý 200 g/l Kyanid draselný-kadmia 5 g/l Kyselina L-glutamová 50 g/l 70 °C, 1 A/dm²2 pH 8 (upraveno pomocí KOH) Au:Cu:Cd=70:15:15 |
1.1 Pokovování slitinou zlata a stříbra
Tabulka 1-6 Složení roztoku pro pokovování slitinou zlata a stříbra
| Složení a provozní podmínky | Parametry | Složení a provozní podmínky | Parametry |
|---|---|---|---|
| Chlorid draselno-zlatý (vypočteno jako Au)/(g/l) | 8 | Povrchově aktivní látka | Malé množství |
| Chlorid draselno-střibrný (vypočteno jako Ag)/(g/l) | 2.5 | Teplota /℃ | 27 |
| Volný thiokyanát draselný/(g/l) | 100 | Hustota proudu /(A/dm2) | 1 |
| Aminová sůl/(g/l) | 5 |

Koncentrace volného kyanidu draselného by neměla být nižší než 90 g/l, obecně by měla být vyšší než 100 g/l, což je vhodnější hodnota. Překročení 120 g/l zvyšuje polarizaci, potlačuje usazování stříbra, zvyšuje rychlost usazování zlata a vytváří vysoce kvalitní vrstvu zlata.
Obsah zlata se upravuje podle hodnoty K zlaté slitiny regulací koncentrace zlata a stříbra v pokovovacím roztoku. Například, pokud je koncentrace stříbra v pokovovací vrstvě slitiny 2,5 g/l, musí být koncentrace zlata regulována v rozmezí 7~10 g/l, aby se dosáhlo 18karátového zlata.
Vliv koncentrace stříbra: když je koncentrace stříbra nízká, rozsah jasu pokovené vrstvy je široký a obsah zlata je vysoký.
Vliv koncentrace aminu: Při přidání množství aminu na 30 g/l se rychlost nanášení zlata nemění, ale ve srovnání s nepřidáním aminu se zvyšuje jas pokovené vrstvy. Při zvýšení množství přidaného aminu na 50 g/l se rychlost nanášení zlata zvyšuje, což způsobuje jev „hoření“ v oblastech s vysokou proudovou hustotou. Hlavním účelem přidání aminu je snížení napětí v silných vrstvách pokovování zlatem. Přidání ligandů, jako je triethylentetramin (10~30 g/l), do roztoků pro pokovování ze slitin zlata a stříbra s lesklým povrchem může vést k lepším výsledkům.
Obrázek 1-4 ukazuje vztah mezi teplotou pokovovacího roztoku, hustotou proudu a rychlostí nanášení zlata. Tvrdost nanesené vrstvy zlata je Hv.25170~210. Povrchové a průřezové podmínky vrstvy zlatého pokovení: po přímém nanesení zlata o tloušťce 4 μm na vrstvu niklového pokovení byla odloupnutá zlatá vrstva pozorována pod elektronovým rastrovacím mikroskopem. Výsledky jsou znázorněny na obrázcích 1-5 a 1-6, což ukazuje, že povrch a průřez vrstvy pokovení nemají póry a jsou husté. Krystalinita vrstvy zlatého pokovení byla testována rentgenovou difrakcí po přímém nanesení asi 10 μm zlata na měděný plech. Vrchol základní měděné vrstvy nebyl detekován; byly změřeny pouze vrcholy vrstvy pokovení ze slitiny zlata a stříbra a krystalizace rostla v rovině (111).

Obrázek 1-5 Stav povrchu pokovování slitinou zlata a stříbra

Obrázek 1-6 Organizační struktura povlaků ze slitin zlata a stříbra
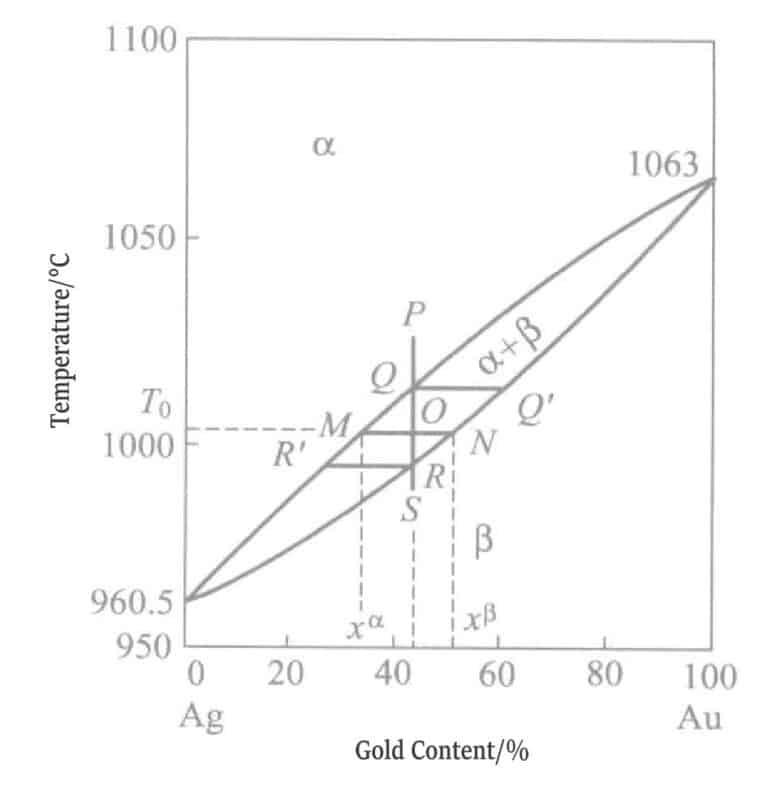
Stav slitin řady zlato-stříbro je znázorněn na obrázku 1-7, patří do pevného roztoku s plným poměrem a zlato i stříbro mají strukturu fcc (plošně centrovanou kubickou) s atomovými poloměry 1,44 Å (1 Å = 10-10m). Mřížka se proto nedeformuje.
E. Raub také provedl rentgenové difrakční studie na vrstvách zlatého pokovení a potvrdil, že slitiny řady zlato-stříbro tvoří pouze jeden typ pevného roztoku a mají vynikající odolnost proti korozi.
EA Parker uvedl, že tato řada slitin zlata a stříbra má vynikající odolnost proti korozi a vodivost, je velmi cenná pro výrobu součástí komunikačních zařízení a její jedinečný zlatozelený odstín a odolnost proti korozi ji činí vhodnou jako základní vrstvu pro silné zlacení.
1.2 Pozlacená slitina mědi
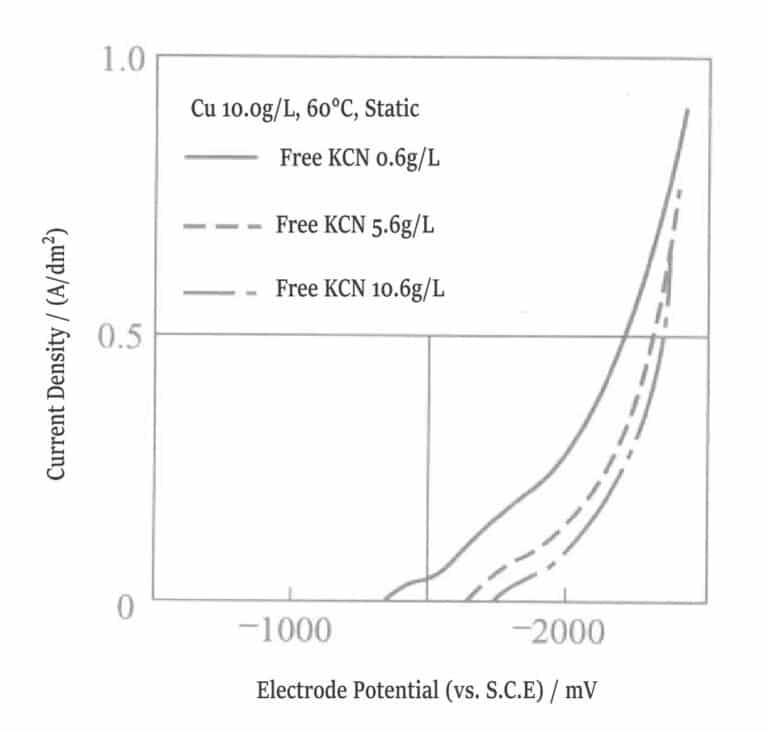
Obrázek 1-8 Polarizační křivka roztoku pro pokovování mědí
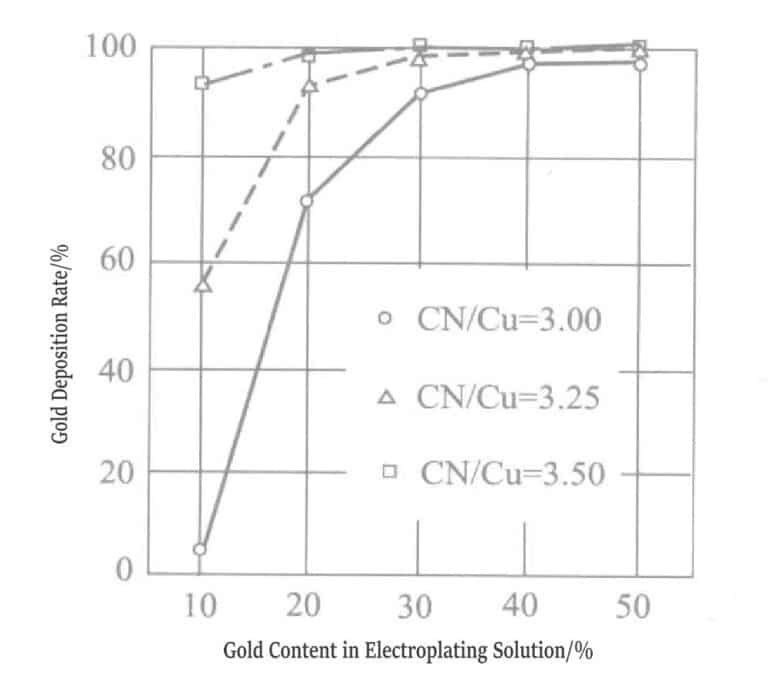
Obrázek 1-9 Změny vysrážených složek ve vrstvě pokovení ze slitiny zlata a stříbra
Tabulka 1-7 Složení a provozní podmínky roztoku pro pokovování slitinou
| Složení a provozní podmínky | Parametry | Složení a provozní podmínky | Parametry |
|---|---|---|---|
| KAu(CN)2/(g/l) | 7.5 ~ 9.0 | Na2SEO4/(g/l) | 0.5 |
| K2Cu(CN)2/(g/l) | 130 | Teplota elektrolytu/℃ | 60 |
| K2Cd(CN)4/(g/l) | 0.4 ~ 2 | Hustota proudu/(A/dm2) | 0.75 |
| KCN/(g/l) | 15 |
Přidání solí niklu do roztoku pro pokovování slitiny zlata a mědi zvyšuje tvrdost pokovené vrstvy. Pokud je pH pokovovacího roztoku blízké kyselému, zvyšuje se množství usazeného niklu. Pokovená vrstva obsahující kadmium má barvu podobnou růžovému zlatu a vykazuje velmi ušlechtilý dekorativní tón.
Zlatá vrstva obsahující 18karátový kadmium je pevný roztok s vysokou tvrdostí, mezí kluzu, pevností v tahu a vynikající odolností proti korozi. Bohužel kvůli problémům s ochranou životního prostředí je používání kovů, jako je kadmium, omezeno úmluvami Mezinárodní organizace pro ochranu životního prostředí a musí být přísně kontrolováno v rámci povolených stopových množství. Kadmium je stále více regulováno a obecně se používá pouze při velmi speciálních barevných úpravách, pokovování slitinami a galvanickém tvarování dutého zlata o tloušťce 200~300 μm, kde se používá pouze při pokovování slitinami 18karátového zlata, mědi a kadmia.
2. Kyselé zlacení
Kyselý roztok pro zlacení je stabilní v rozmezí pH přibližně 3 a je schopen ukládat nikl nebo kobalt, které nepodléhají elektrolýze v alkalických roztocích pro zlacení, a vytvářet povlaky ze slitin zlato-nikl nebo zlato-kobalt. Jemné krystaly povlaku se nedeformují ani nedislokují a neobsahují žádné dutiny, což umožňuje dlouhodobý stabilní růst.
Povlak nanesený z kyselého pokovovacího roztoku má lesklý vzhled a nazývá se lesklý pokovovací roztok. Povlak z kyselého pokovovacího roztoku má vysokou tvrdost a je také známý jako roztok pro tvrdé zlacení (tabulka 1-8). Různé kovy přidávané do organických kyselých pokovovacích roztoků se nazývají kovové zjasňovače.
Tabulka 1-8 Hlavní složky a varianty kyselého roztoku pro zlacení
| Složení a provozní podmínky | Referenční parametry | Podmínka roztoku pro pokovování |
|---|---|---|
| KAu(CN)2 (g/l) | 4 ~ 6 (vypočteno jako Au) | Vysoká koncentrace (cca 16 g/l), vhodná pro vysokorychlostní zlacení |
| Hydrát kyseliny citronové (g/l) | 50 až 100 | Přidejte kyselinu citronovou jako ligand pro vrták a jako pufr pro pokovovací roztok nebo přidejte jiné kobaltové ligandy |
| CoSO44 • 7 hodin2O/(g/l) | 0,1 〜 3,0 (vypočteno jako Co) | Obecně se přidává kobalt a pokovování. Při legování Au-Ni se přidává kyselina sírová (vypočteno jako Co). |
| pH | 3,5 〜 4,5 | Proudová účinnost je vysoká při vysokém pH, ale snadno se vytváří mlha |
| Teplota/℃ | 30 až 40 | Vysoká teplota kapaliny snadno vytváří mlhu |
Tabulka 1-9 Vlastnosti kyselého roztoku pro zlacení
| Vliv hodnoty pH | Vlastnosti pokovovacího roztoku | Aplikace | |
|---|---|---|---|
| pH 3 | pH 3 ~ 5 | ||
|
① Slitiny zlata a kobaltu, zlata a niklu ② Kobalt a nikl jsou vysoce aktivní a více se srážejí; přepětí pro vývoj vodíku je nízké, proudová účinnost se zvyšuje, účinnost pokovování je nízká |
① Eutektická lesklá, tvrdá slitina; vysoký potenciál vývoje vodíku, nízká proudová účinnost, vysoká účinnost pokovování ② V pokovovacím roztoku není přítomen žádný volný kyanid ③ Během srážení zlata z KAu(CN)2, součást CN- tvoří HCN, který difunduje do ovzduší a ovlivňuje životní prostředí |
① Během srážení zlata z KAu(CN) není přítomen žádný volný kyanid2, CN- tvořící HCN ②S prodlužující se dobou galvanického pokovování v důsledku akumulace K+, zvýšení pH pokovovacího roztoku ③ Pokovovací roztok je kyselý; Na Pt/Ti anodě je vysoký potenciál vývoje vodíku a organické karboxylové kyseliny, jako je kyselina citronová, podléhají Kolbeho reakci za vzniku viskózních polymerů, takže k potlačení této reakce je zapotřebí anodová deska s velkou plochou. |
① Dekorativní galvanické pokovování ② Kromě odstranění kobaltu a niklu lze pro úpravu barvy přidat také indium, zinek a železo |
Pokud v pokovovacím roztoku není přítomen žádný volný kyanid, kyanid draselný-zlato ukládá zlato a komplexní ionty kyanidu (CN – ) tvoří HCN, který vstupuje do atmosféry a difunduje.
V galvanické nádrži se zlaté destičky jako anody používají jen zřídka; obecně se používají destičky z nerezové oceli nebo Pt/Ti destičky. V kyselých pokovovacích roztocích je přepětí při vývoji kyslíku na anodě vysoké a karboxylové kyseliny, jako je kyselina citronová, mají tendenci na anodě podléhat Kolbeho reakcím. Metody, jako je zvětšení plochy anody, mohou zabránit tvorbě lepkavých polymerních usazenin.
Společné nanášení niklu a kobaltu zvyšuje tvrdost kyanidové zlacené vrstvy. Po pájení reflow při 260 °C se prudce zvyšuje kontaktní odpor. Přidání alifatických sloučenin, jako je ethanol, do pokovovacího roztoku může zabránit změnám kontaktního odporu po pájení reflow a výrazně zvýšit rozsah proudové hustoty pokovovacího roztoku. Například při pokovování zlatem flexibilních desek plošných spojů (měď) může přidání merkapto sloučenin zabránit rozpouštění měděných trubek a stabilně a dlouhodobě pokovovat silnou vrstvu zlata.2.1 Pokovování slitinami zlata a kobaltu
Kyselé zlacení se obecně provádí pomocí roztoků organických kyselin zlacení z řady kyseliny citronové a citrátu. Ligand, kyanid draselný a zlato, se ve vodném roztoku organické kyseliny disociuje za vzniku volného kyanidu, čímž se roztok stává galvanickou lázní s pH přibližně 3. Podle potřeby se přidávají různé složky, jako například ligandy jiné než kyselina citronová, včetně EDTA. Jako regulátor pH se používá hydrogensíran sodný. Mezi vodivé soli patří hydrogenfosforečnan draselný, dihydrogenfosforečnan, hydrogenfosforečnan amonný, pyrofosforečnan sodný atd. Mezi použité pufry patří síran draselný, síran sodný atd. Podmínky galvanického pokovování: koncentrace zlata 1~8 g/l, proudová hustota 0,3~10 A/dm²2, teplota pokovovacího roztoku 25~40℃. Obecně se při pokovování silné vrstvy zlata nevyskytují žádné nežádoucí jevy, jako je zamlžování. Zjasňovač v pokovovacím roztoku vyžaduje přidání pouze malého množství přechodných kovů nebo metaloidů. Kobalt a nikl jsou reprezentativní kovové zjasňovače.
R. Duva a kol. navrhli řešení zlacení uvedené v tabulce 1-10 v patentu a úspěšně si přihlásili mnoho dalších patentů na kyselé zlacení.
Tabulka 1-10 Složení reprezentativních kyselých roztoků pro zlacení
| Složení a provozní podmínky | 1 | 2 |
|---|---|---|
| Kyselina citronová + citrát sodný / (g/l) | 80 | 80 |
| Zlato (kyanid draselný a zlato) / (g/l) | 8 | 8 |
| Nikl (síran nikelnatý) / (g/l) | 3 | |
| Zinek (octan zinečnatý) / (g/l) | 0.5 | |
| Indium (síran) / (g/l) | 5 | |
| Kobalt (síran) / (g/l) | 3 | |
| pH | 4 až 5 | 3~4 |
| Teplota /℃ | 21 | 21 |
| Hustota proudu / (A/dm1) | 1 | 1 |
| K① hodnota | 23 | 21 |
① Národní norma GB 11887-89 stanoví, že obsah zlata v 1K je 4,166% („K“ je zkratka anglického slova carat a německého slova karat).
21K = 21×4. 166% = 87. 486% (875 ‰)
24karátové zlato se často mylně označuje jako ryzí zlato nebo se označuje jako „1000 ‰“ se skutečným obsahem zlata 99 991 TP3T, což odpovídá 23,988 K (mezinárodní organizace zakazují označování jako „ryzí zlato“, „zlato 9999“ a „24karátové zlato“).
Existuje mnoho názorů na roli kobaltu v pokovovacích roztocích. Eisenmann analyzoval obsah draslíku, kobaltu, uhlíku, dusíku a dalších prvků ve vrstvě zlatého pokovení a zjistil, že poměr těchto prvků odpovídá poměru KCo[Au(CN)2]3 molekuly. Proto byl učiněn závěr, že v pokovovacím roztoku působí jako zjasňovač, spíše než že samotný kobalt poskytuje zjasňující účinek. V pokovovacím roztoku se tvoří v Helmholtzově dvojité vrstvě a za typických pokovovacích podmínek se rozpouští pouze minimálně. Po vytvoření ligandu vykazuje elektrochemické chování podobné organickým zjasňovačům a je adsorbován katodicky. Tento přechodný kov vykazuje zjasňující účinky v širokém rozsahu pH, což je v souladu s kobaltem a dalšími přechodnými kovy, které vykazují zjasňující účinky pouze v kyselých pokovovacích roztocích.
Teoreticky by poměr draslíku, kobaltu, uhlíku a dusíku v pokovené vrstvě měl být 1:1:6:6, ale tyto poměry se značně liší. Poměr draslíku a kobaltu se pohybuje v rozmezí (1,0:0,4) až (1,0:5,5) v závislosti na stavu pokovovacího roztoku a provozních parametrech; poměr kobaltu a uhlíku se pohybuje mezi (1:3) až (1:10), zatímco poměr uhlíku a draslíku zůstává v podstatě stabilní na hodnotě 3:1.
Výše uvedené výsledky nevyvracejí skutečnost, že KCo[Au(CN)2]3 je hlavním zjasňovačem v roztoku pro zlacení a současně byly v roztoku pro zlacení detekovány také kobalt, CoOOH nebo kyanid kobaltu. Vznik KCo[Au(CN)2]3 lze také vysvětlit mnoha vlastnostmi kyselého roztoku pro zlacení, například považovat tuto sloučeninu pouze za jednoduchý meziprodukt v procesu galvanického pokovování, přičemž další reakce představují proces zjasňování. Stručně řečeno, předpokládá se, že k zjasnění vrstvy zlatého pokovování přispívají faktory, jako je redukce draslíku a kobaltu, soli kyanidových ligandů a tvorba polymerů.
Složení reprezentativních lesklých, nízkopásmových a otěruvzdorných roztoků zlacení je uvedeno v tabulce 1-11. Teoretické předpoklady jsou zcela v souladu s roztokem zlacení v silné koordinační síle koordinační skupiny kobaltu z ligandu KCo[Au(CN)2]3 disociace ligandu kobaltových iontů, což vede ke vzniku KCo[Au(CN)2]3, vznik výskytu role zjasnění. Pokud je přidána ve formě kobaltové soli EDTA, celkové množství kobaltu KCo[Au(CN)2]3 byla 6 g/l.
Tabulka 1-11 Složení reprezentativních roztoků pro lesklé, nízkopásmové a otěruvzdorné zlacení
| Prvek | Hmotnostní poměr/% | Atomový poměr /% | Prvek | Hmotnostní poměr/% | Atomový poměr /% |
|---|---|---|---|---|---|
| K | 0. 26 | 1.3 | Co | 0.24 | 0.80 |
| C | 0.24 | 3.94 | Celkový | 1.00 | 9.70 |
| N | 0.26 | 3.66 |
Všechny elektrolyty pro zlacování obsahují silně koordinující kyanidové ligandy (s výjimkou systému siřičitanových solí zlata). Kyanokobaltový ion [Co(CN)6–] je jedním z nejstabilnějších koordinačních solných komplexů známých mezi ligandy a kyanidová sůl koordinovaná s Co(III) je téměř netoxická.
Pokud se v kyselém roztoku pro pokovování zlatem nachází volný kyanid, bude se vytvářet HCN, takže koncentrace volného kyanidu musí být velmi nízká. Pokud se však pH zvýší, koncentrace volného kyanidu v roztoku pro pokovování se zvýší. Při analýze kobaltu v roztoku pro pokovování je nutné rozlišovat mezi „neaktivním kobaltem“ a „aktivním kobaltem“, přičemž prvním je Co(III) a druhým Co(II).
Při změně provozních podmínek pokovovacího roztoku je třeba dbát na následující aspekty.
(1) pH má mnoho vlivů na pokovovací roztok.
Při vysoké hodnotě pH 5,0 se zvyšuje koncentrace volného kyanidu, což podporuje tvorbu koordinační soli kyano kobaltu(III) a zvyšuje rozpustnost KCo[Au(CN)2]3, čímž se snižuje jas pokovené vrstvy. Dodávka kobaltu v Helmholtzově dvojité elektrické vrstvě (obrázek 1-3) je ovlivněna koordinační schopností ligandů, která závisí na pH pokovovacího roztoku. Vzhledem k tomu, že pH pokovovacího roztoku neustále stoupá, vyžadují kyselé pokovovací roztoky neustálé přidávání pufrovacích činidel.
Při nízkém pH se přednostně vybíjejí vodíkové ionty, což má za následek nižší proudovou účinnost pokovovacího roztoku.
(2) Teplota pokovovacího roztoku: S rostoucí teplotou pokovovacího roztoku se zvyšuje rozpustnost KCo[Au(CN)2]3 zvyšuje se a jas pokovené vrstvy klesá.
Teplota také ovlivňuje koordinační pevnost. Když se teplota pokovovacího roztoku zvýší, zvýšení koncentrace solí zlata a kobaltu může tento efekt účinně snížit.
(3) Vysokorychlostní pokovování: Roztoky pro vysokorychlostní pokovování vyžadují pravidelné úpravy. Aby se zabránilo lokálnímu snížení koncentrace na katodě (koncentrační polarizace), měly by být koncentrace zlata a kobaltu udržovány pod horní hranicí. Ze stejného důvodu by se mělo míchání provádět u roztoků s vysokou koncentrací a při pokovování s vysokou proudovou hustotou se používá tryskové míchání. Vysoké teploty mohou zesílit účinek míchání. Hlavní charakteristikou vysokorychlostního pokovování je vysoká proudová hustota jak na anodě, tak na katodě. Zjasňovače na bázi přechodných kovů mohou dosáhnout optimálního výkonu při vysoké proudové hustotě na obou elektrodách. Je však třeba vzít v úvahu následující situace:
① Hodnota pH pokovovacího roztoku rychle stoupá.
② Společnost3+ se generuje rychle.
③ Koordinační soli kyanidu kobaltnatého(III) se snadno tvoří.
④ Organické ligandy podporují oxidaci pokovovacího roztoku.
V průběhu let bylo vyvinuto mnoho pokovovacích roztoků obsahujících organické přísady, které zvyšují rozsah hustoty proudu pokovovacích roztoků na bázi kobaltu a zlata a slitin niklu a zlata, čímž se dosahuje vysokorychlostního pokovování při nižších koncentracích.
(4) Aktuální účinnost: Proudová účinnost je poměr (%) proudu spotřebovaného při skutečném procesu zlacení k celkovému použitému proudu. Ostatní redukční reakce spotřebovávají zbývající proud.
Používání Co3+ + e– =Co2+Z pohledu spotřeby proudu lze chápat, že tvorba a adsorpce KCo[Au(CN)2]3 zvýšené polarizační účinky, což vede k podpoře výboje vodíku.
Důležité podmínky, které napomáhají vzniku KCo[Au(CN)2]3, jako je nízká hodnota pH, vysoká koncentrace volného Co2+a nízká teplota pokovovacího roztoku snižují proudovou účinnost.
Použití vhodných ligandů může regulovat efektivní koncentraci kobaltu a tvorbu KCo[Au(CN)2]3, což má za následek lesklou pokovenou vrstvu a optimální proudovou účinnost.
(5) Přidávání kovů, tedy kovových zjasňovačů, brání tvorbě KCo[Au(CN)2]3Například olovo brání tvorbě zjasňovačů adsorpcí, čímž snižuje proudovou účinnost.
(6) Míchání: Ve srovnání s pokovovacími roztoky jiných kovů, vzhledem k dostupnosti zlatých surovin, ceně a dalším nákladovým faktorům a skutečnosti, že většina proudu v procesu pokovování je spotřebována přenosem elektronů ve vodivých solích s vysokou koncentrací, se pokovovací roztoky obecně používají s nejnižší možnou koncentrací.
Au(CN)2– není při elektroforéze přitahován ke katodě a je dodáván do Helmholtzovy dvojité vrstvy (obrázek 1-3) difuzí; proto je míchání důležitou podmínkou pro dodávání koordinační soli zlata a zjasňovačů ke katodě.
Míchání může zlepšit proudovou účinnost, ale zároveň dále zvýší proudovou účinnost v oblastech s vysokou proudovou hustotou, což zhorší rovnoměrnost pokovovací vrstvy.
S pokrokem v technologii lokálního pokovování se problém špatné disperze pokovované vrstvy postupně zmenšoval. V současné době se běžně používají přísady k rozšíření rozsahu proudové hustoty a zlepšení rovnoměrnosti pokovování.
Kopírování @ Sobling.Jewelry - Výrobce šperků na zakázku, továrna na šperky OEM a ODM
2.2 Pokovování slitinou zlata a niklu

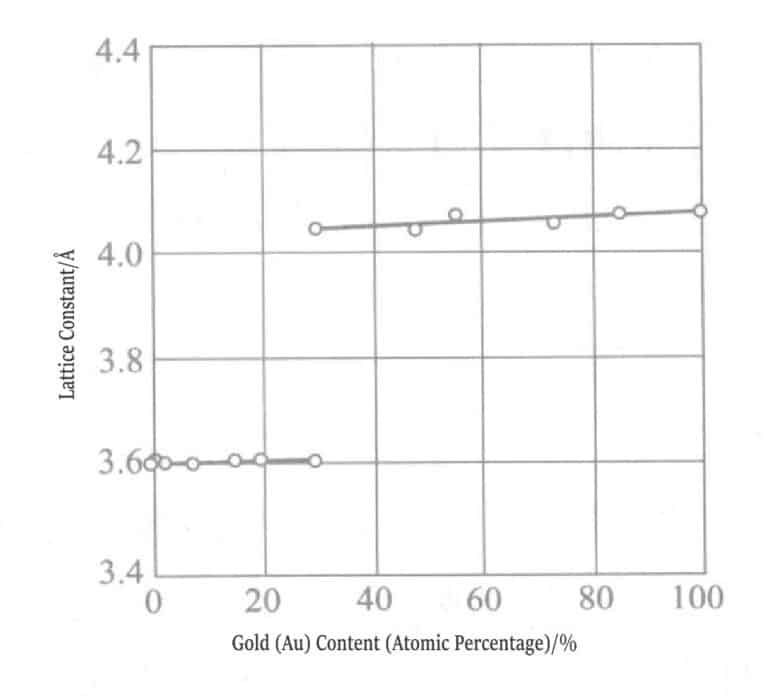
Obrázek 1-11 Obsah niklu a mřížková konstanta povlaku ze slitiny zlato-nikl

Obrázek 1-12 Obsah niklu a mřížková konstanta povlaku ze slitiny zlato-nikl
Byl měřen vztah mezi obsahem niklu a mřížkovou konstantou v alkalických a kyselých pokovovacích roztocích pro galvanicky pokovené vrstvy slitin zlata a niklu. Nikl tvoří pevný roztok se zlatem při maximálním obsahu 5% a při překročení 5% se nikl sráží jako jednoduchá směs.
Srovnávací testy byly provedeny také na pokovovacích vrstvách ze slitin zlata a niklu a ze slitin zlata a kobaltu a výsledky ukázaly, že vlastnosti obou slitin zlata se výrazně liší. Obrázky 1-13 a 1-14 ukazují, že obsah uhlíku, kobaltu a niklu ve slitinách zlata stejného složení se mění s teplotou pokovovacího roztoku. Obsah kobaltu klesá s rostoucí teplotou pokovovacího roztoku a křivky uhlíku a kobaltu jsou rovnoběžné, takže molární poměr uhlíku ke kobaltu je přibližně fixní na 4.
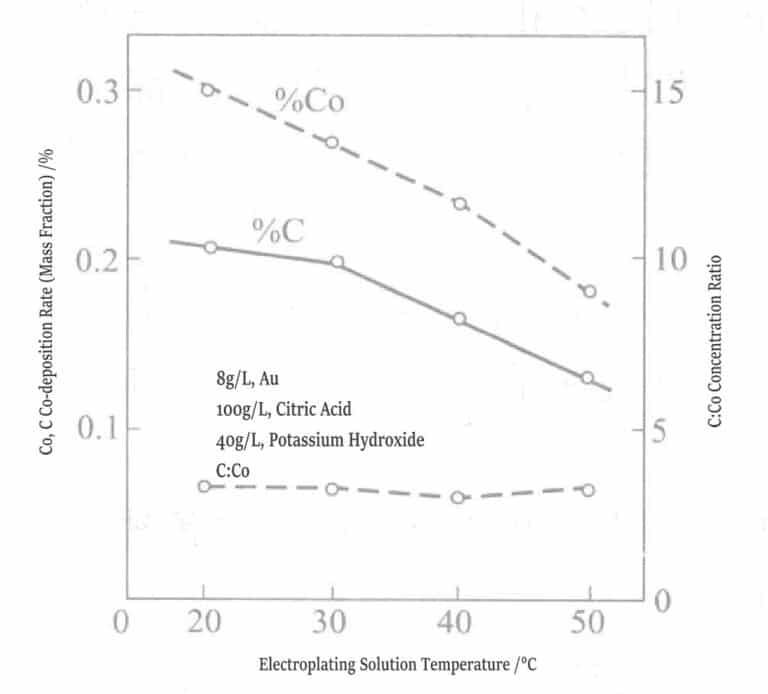
Obrázek 1-13 Vztah mezi teplotou pokovovacího roztoku a rychlostí společné depozice kobaltu a uhlíku
(0,5 g/l, pH 3,5, 1 l/dm2 )
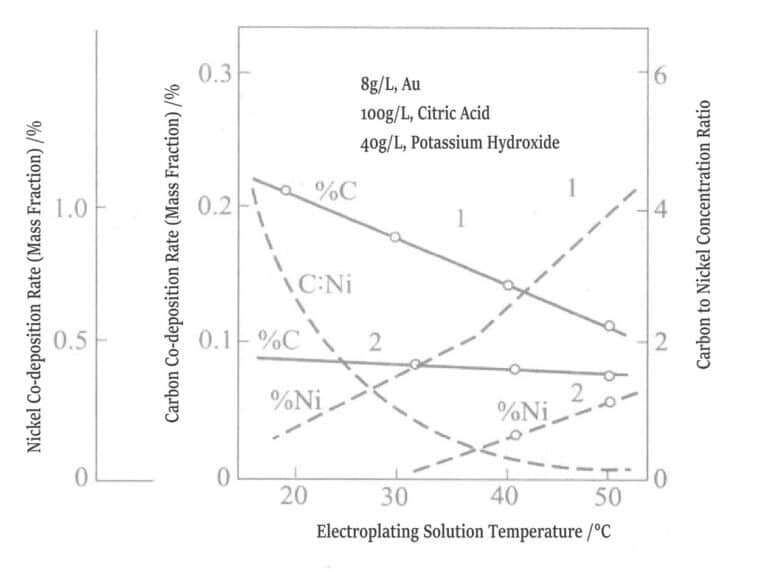
Obrázek 1-14 Vztah mezi teplotou pokovovacího roztoku a společným ukládáním niklu a uhlíku
1–0,5 g/l, pH 3,5, 1 l/dm²2 2–0,5 g/l, Ni, pH 4,5, 1 Å/dm²2
Obrázek 1-15 ukazuje vliv pH na ko-depozici niklu. Pokud je pH regulováno nad 4,5, ko-depozice niklu v pokovené vrstvě je nulová, zatímco pod pH 4,5 je pokovená vrstva lesklá.
Když se do zlacecí vrstvy přimísí další nečistoty, zvyšuje se tahové napětí pokovené vrstvy. Obrázek 1-16 ukazuje vztah mezi teplotou pokovovacího roztoku ze slitiny zlata a niklu a hodnotou napětí v pokovené vrstvě.
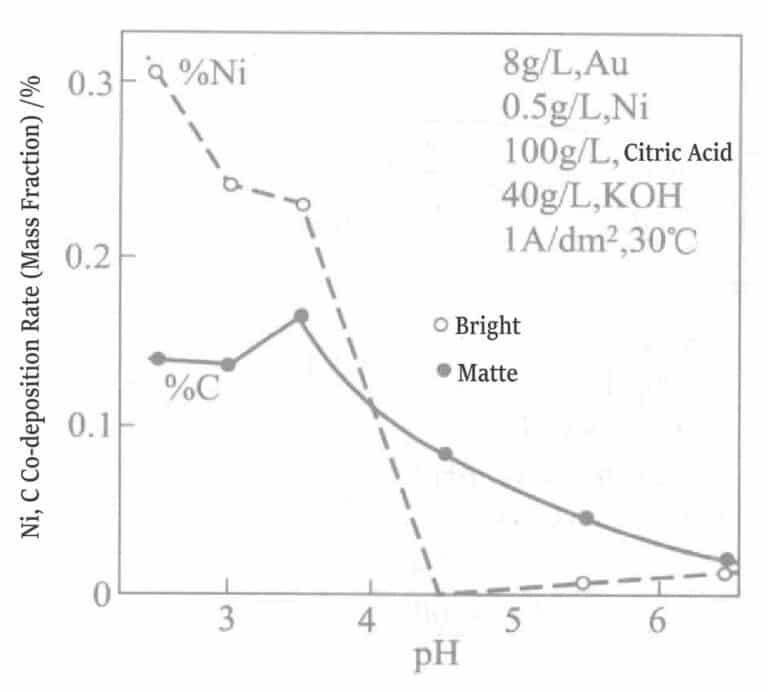
Obrázek 1-15 Vliv pH na rychlost společné depozice niklu a uhlíku
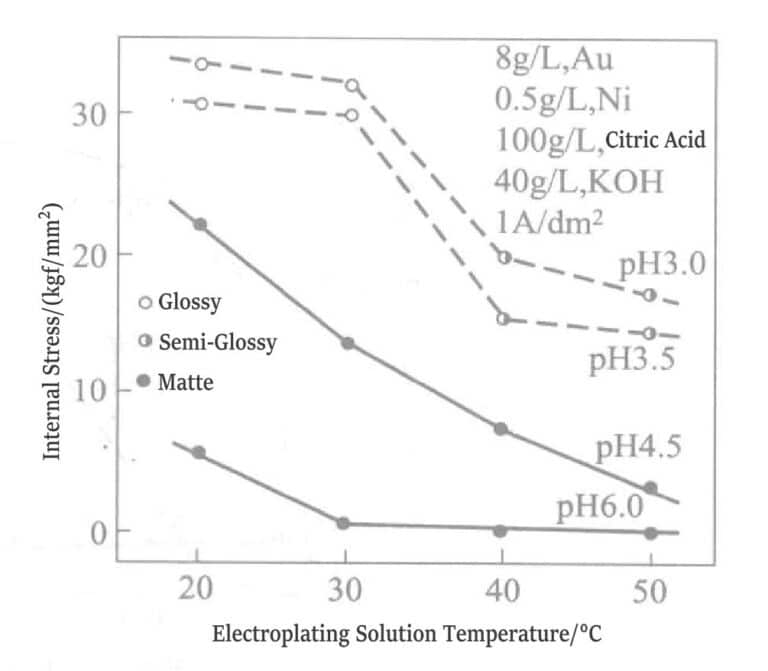
Obrázek 1-16 Vztah mezi hodnotou vnitřního napětí, pH a teplotou pokovovacího roztoku (1 kgf/mm2 =980,665 Pa)
S rostoucí tloušťkou těchto zlacených vrstev se snadno tvoří trhliny. Pevnost v tahu pokovené vrstvy ze slitiny zlata a niklu je znázorněna na obrázku 1-17. Pevnost v tahu je výrazně ovlivněna tloušťkou a kvalitní pokovenou vrstvu bez trhlin lze pokovit pouze do tloušťky 2~3 μm.
Pokud je pH pod 5, může pokovovací roztok generovat ligandy. V současné době je vazebná síla mezi citrátem a niklem (Ni2+ ) je silnější než kyanid. Obrázky 1-18 ukazují různé podmínky pokovovacího roztoku. Pokud se nikl přidá ve formě K2Ni(CN)4, obsah uhlíku v pokovovací vrstvě prudce stoupá. Obsah niklu v pokovovací vrstvě stoupá z koncentrace vyšší než 0,3 g/l v pokovovacím roztoku. Pokud je koncentrace niklu v pokovovacím roztoku nižší než 0,3 g/l, pokovovací vrstva je matná; nad 0,3 g/l se stává lesklou. Pokud se však nikl přidá do pokovovacího roztoku jako síran nikelnatý, může se lesklý efekt dosáhnout i při koncentraci niklu nižší než 0,3 g/l. Důvodem je, že nikl již prošel kodepozicí na určité koncentrační úrovni.

Obrázek 1-17 znázorňuje vztah mezi tloušťkou zlatého pokovení a pevností v tahu.
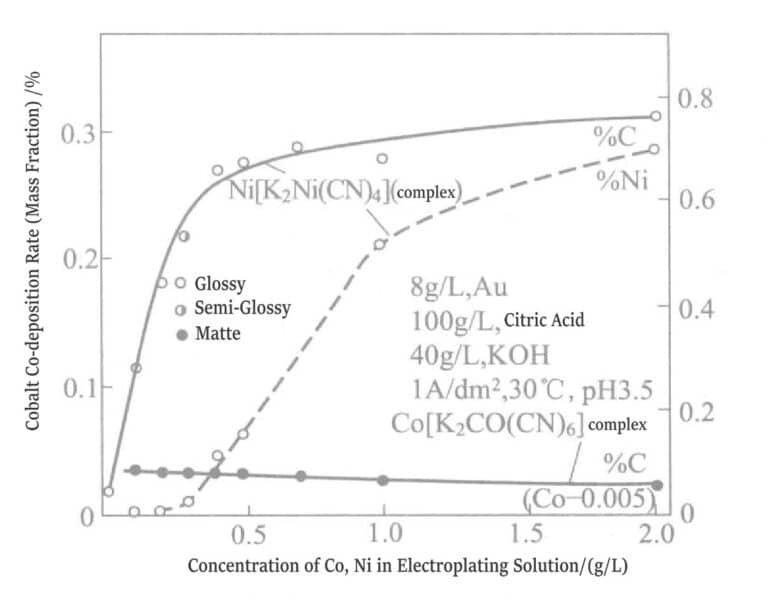
Obrázek 1-18 Vliv komplexních iontů na koncentrace kobaltu a niklu v pokovovacím roztoku a rychlosti společné depozice kobaltu, niklu a uhlíku.
(1) Složení a provozní podmínky pokovovacího roztoku: Barva pokovené vrstvy je klíčem k dekorativnímu zlacení. V kyselých organokyselých pokovovacích roztocích se jako hlavní složky používají následující: soli zlata, organické kyseliny, soli niklu, zjasňovače a látky snižující pnutí. Soli zlata, jako je kyanid draselný a zlato. Mezi organické kyseliny patří kyselina citronová, kyselina hydroxybutandiová a kyselina vinná. Mezi soli niklu patří soli niklu kyseliny amidosulfonové, kyseliny citronové, kyseliny sírové, kyseliny glukonové, kyseliny mravenčí, kyseliny borité, kyseliny fosforečné atd. Mezi zjasňovače (kovy) patří indium, kobalt, zinek, kadmium, antimon atd.
Mezi látky zmírňující stres patří hořčík, vápník, α-bipyridin, alkylbenzensulfonát sodný, triethylentetramin, hydrazinsulfát, kyselina amidosulfonová atd.
(2) Faktory ovlivňující barvu pokovených vrstev ze slitiny zlata a niklu: Tabulka 1-12 uvádí dva typy pokovovacích roztoků: barvy pokovovacích vrstev, stabilita pokovovacího roztoku, fyzikální vlastnosti atd.
① Vliv citrátu niklu: Koncentrace citrátu niklu vypočtená jako nikl v pokovovacím roztoku se pohybuje v rozmezí 15 g/l, 20 g/l, 25 g/l, 30 g/l, čímž se upravuje barva vrstvy zlatého pokovení. Při koncentraci citrátu niklu 15 g/l je pokovovaná vrstva jasně zlatožlutá; při koncentraci 20–30 g/l se barva nemění. Při přidání 1 g/l kobaltu ve formě síranu kobaltu se barva nemění, ale jas pokovené vrstvy ano. Po samostatné změně teploty pokovovacího roztoku na 35 °C, 40 °C, 45 °C, 55 °C se barva pokovené vrstvy stále nezměnila.
Tabulka 1-12 Složení a provozní podmínky dvou roztoků pro pokovování zlatem a niklem
| Složení a provozní podmínky | Roztok niklování s kyselinou citronovou | Roztok pro pokovování sulfamátem niklu |
|---|---|---|
| Kyselina citronová /(g/l) | 150 | 150 |
| Citrát draselný /(g/l) | 100 | 100 |
| Sulfamát niklu (jako Ni)/(g/l) | 15 | |
| Nikl (jako Ni)/(g/l) s kyselinou citronovou | 25 | |
| Síran kobaltnatý (jako Co)/(g/l) | 1 | 0.5 |
| Kyanid draselný a zlato (jako Au) /(g/l) | 2 | 2 |
| Kyanid draselný KCN/(g/l) | 1 | 1 |
| pH | 4.2 | 4.2 |
| Teplota /℃ | 40 | 40 |
② Vliv aminosulfonátu niklu: V pokovovacím roztoku je koncentrace aminosulfonátu niklu 5 g/l, 10 g/l, 15 g/l, 20 g/l, počítáno jako nikl; s přidáním 0,5 g/l kobaltu (síranu kobaltnatého) a 2,5 g/l zlata (kyanidu draselného a zlata) se barva pokovované vrstvy výrazně mění. Při koncentraci niklu 5 g/l je pokovená vrstva jasně zlatožlutá; při koncentraci 10 g/l je světle zlatá. Při porovnání pokovených vrstev nanesených pomocí dvou solí niklu vykazuje pokovená vrstva z roztoku citrátu niklu jasně zlatožlutou barvu. Naproti tomu pokovená vrstva z roztoku aminosulfonátu niklu je mírně načernalá.
③ Účinek síranu nikelnatého: Po určité době se v roztoku pokovování síranem nikelnatým vytvoří sraženina hydroxidu nikelnatého, která je nevhodná k použití.
④ Proudová účinnost: Vztah mezi proudovou hustotou a proudovou účinností pro dva pokovovací roztoky je znázorněn na obrázku 1-19. Při proudové hustotě 0,5 A/dm²21,0 A/dm²21,5 A/dm²2Mezi roztokem citrátového niklování a roztokem aminosulfonového niklování není žádný rozdíl a proudová účinnost obou je 22%~23%.
⑤ Poměr nanášení zlata: Obsah zlata v pokovené vrstvě roztoku citrátového niklu je o 1%~3% (hmotnostní podíl) vyšší než obsah zlata v pokovené vrstvě roztoku aminosulfonového niklu (obrázek 1-20).
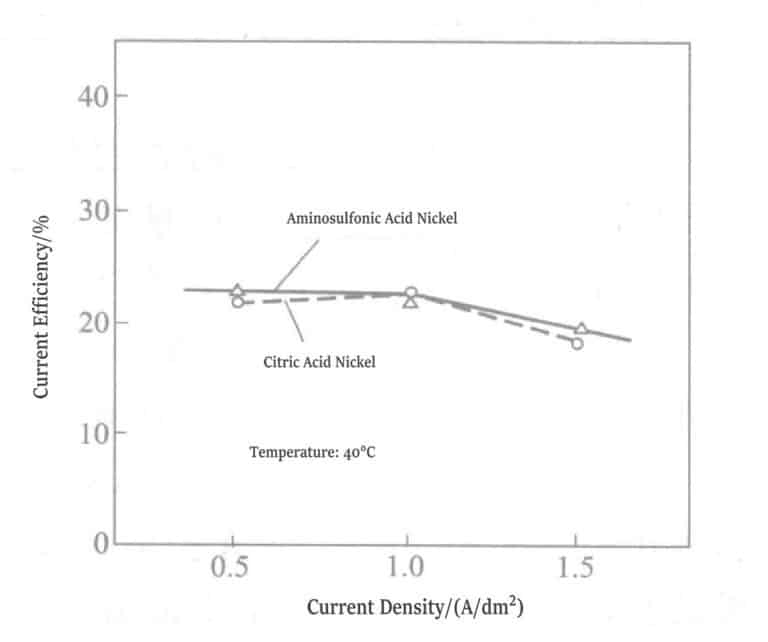
Obrázek 1-19 Vztah mezi hustotou proudu a proudovou účinností
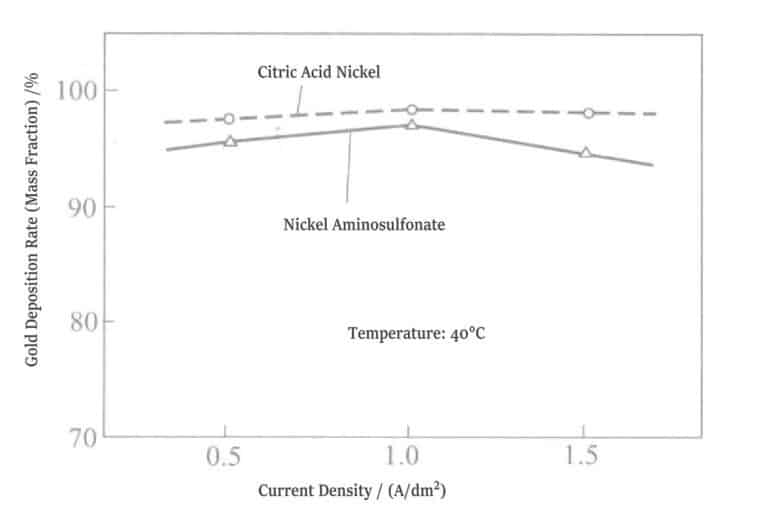
Obrázek 1-20 Vztah mezi poměrem usazování niklové soli a zlata
Tabulka 1-13 Tvrdost průřezů dvou typů pokovovacích vrstev
| Typ | Zatížení/gf① | Tvrdost Hv |
|---|---|---|
| Roztok pro pokovování citrátem niklu | 25,50 | 280 ~ 310 |
| Roztok pro pokovování kyselinou niklsulfamovou | 25,50 | 210 ~ 240 |
| ① lgf=9,80665×10-3N. | ||
Povrch dvou pokovených vrstev o tloušťce 50 μm je bez trhlin, hladký a pololesklý. Pokud je obsah niklu (hmotnostní podíl) v pokovené vrstvě ze slitiny zlata a niklu přibližně 5%, tvrdost se obvykle pohybuje kolem Hv 200. Vzhledem k velké tloušťce pokovené vrstvy vzniká vnitřní pnutí, takže naměřený výsledek překračuje Hv 200. Tvrdost pokovené vrstvy z roztoku aminosulfonátu je nízká, což je ovlivněno nejen tloušťkou pokovené vrstvy, ale také účinkem samotného aminosulfonátu na snížení pnutí.
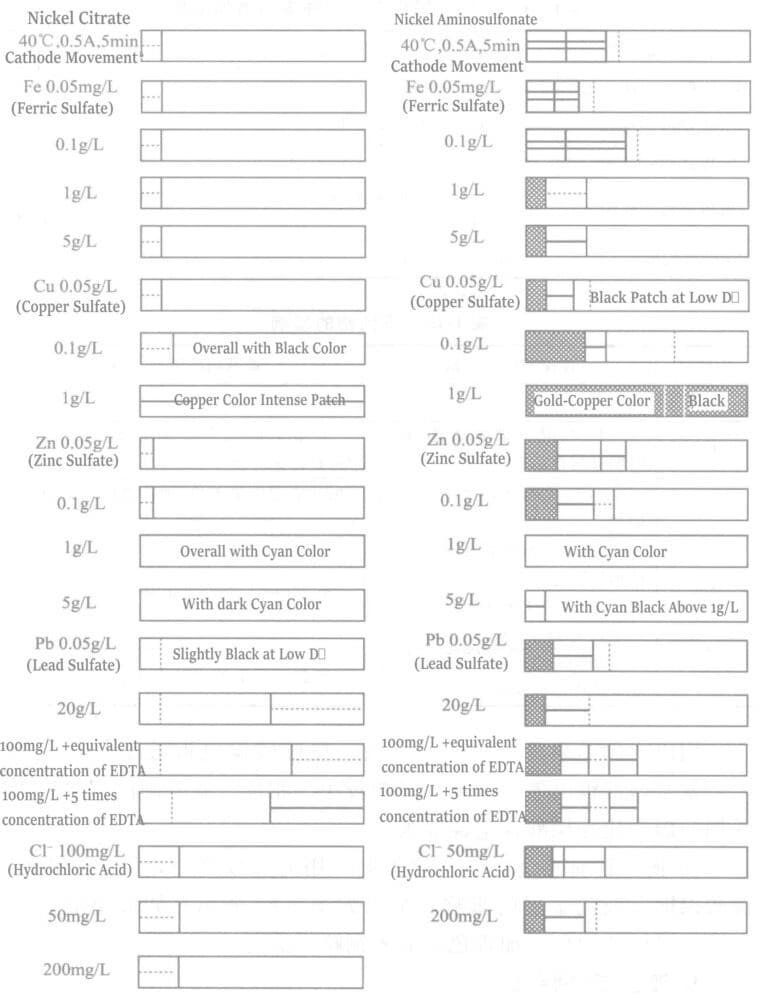
⑦ Vliv nečistot: Experimentální pokovovací roztok a provozní podmínky pro vliv nečistých kovů na vzhled pokovené vrstvy jsou uvedeny v tabulce 1-14. Lesklý nikl byl nanesen v testovací nádrži pro tenkovrstvé baterie za účelem provedení testů tenkovrstvých bateriových desek. Výsledky obou pokovovacích roztoků jsou uvedeny na obrázku 1-21 a shrnutí výsledků je uvedeno v tabulce 1-15.
Tabulka 1-14 Typy a koncentrace přidaných sloučenin nečistých kovů
| Nečisté sloučeniny | Přidaná částka |
|---|---|
| Fe ve formě síranu železnatého | 0,05 g/l, 0,1 g/l, 1 g/l, 5 g/l |
| Cu ve formě síranu měďnatého | 0,05 g/l, 0,1 g/l, 1 g/l |
| Zn ve formě síranu zinečnatého | 0,05 g/l, 0,1 g/l, 1 g/l, 5 g/l |
| Pb ve formě síranu olovnatého | 100 mg+krát (molární poměr) EDTA 5 mg/l, 20 mg/l, 100 mg+ ekvivalentní mol EDTA |
| Cl ve formě kyseliny chlorovodíkové | 50 mg/l, 200 mg/l |
Tabulka 1-15 Vlivy nečistot
| Nečistoty | Roztok pro pokovování citrátem niklu | Roztok niklování aminosulfonovou kyselinou |
|---|---|---|
| Fe | Žádný účinek až do 5 g/l | |
| Cu | Při 0,1 g/l: Celý povrch se jeví jako černý; při 1 g/l: Objevuje se zřetelná měděná sraženina. | Při 0,5 g/l: V oblastech s nízkou proudovou hustotou dochází k černéní; při 1 g/l: Povrch ztrácí lesk. |
| Zn | Do 0,1 g/l: Žádný pozorovatelný účinek; Nad 0,1 g/l: Objevuje se modrozlatožluté zbarvení s modravým odstínem, který se úměrně zesiluje se zvyšující se koncentrací. | |
| Pb | Přibližně 5 mg/l: V oblastech s nízkou proudovou hustotou se projevuje mírné zčernání. Při přibližně 20 mg/l: Po zavedení EDTA-2Na se objeví zakalený vzhled. | Do 20 mg/l: Nebyl pozorován žádný významný vliv. |
| Cl | Při 200 mg/l: Okrajové zvýšení zákalu omezené na oblasti s vysokou proudovou hustotou. | Kolem 200 mg/l: V podstatě žádný detekovatelný vliv. |
Při porovnání výše uvedených výsledků pro dva typy pokovovacích roztoků je roztok pro niklování kyselinou citronovou silně ovlivněn olovem. Naproti tomu olovo ovlivňuje roztok pro niklování kyselinou aminosulfonovou méně. Naopak měď ovlivňuje roztok pro niklování kyselinou aminosulfonovou více než roztok pro niklování kyselinou citronovou.
⑧ Vliv mědi a zinku na barvu vrstvy zlatého pokovení: K měření vlivu mědi a zinku na vrstvu zlatého pokovení roztokem kyseliny citronové a niklu byl použit leskoměr a výsledky jsou uvedeny na obrázku 1-22. Pokud se do roztoku zlatého pokovení přimíchá zinek, barva pokovené vrstvy se zvýší do azurové barvy; pokud se přimíchá měď, vykazuje mírný černý nádech.

2.3 Pokovování slitinou zlata, niklu a india
Tabulka 1-16 Složení a provozní podmínky roztoku pro pokovování slitinou zlato-nikl-indium
| Složení a provozní podmínky | Parametry | Složení a provozní podmínky | Parametry |
|---|---|---|---|
| Kyanid draselný a zlato/(g/l) | 11.7 | Indium (síran india)/(g/l) | 5 |
| Kyselina citronová / (g/l) | 85 | pH | 3.8 |
| Citrát draselný / (g/l) | 140 | Teplota galvanického roztoku / ℃ | 38 |
| Nikl (citrát nikelnatý) / (g/l) | 4.5 | Hustota proudu / (A/dm2) | 1 |
2.4 Pokovená hypoalergenní slitina zlata
Kovy jako nikl a kobalt se již dlouho běžně používají k úpravě tvrdosti, odolnosti proti opotřebení, odolnosti proti korozi a barvy zlacených vrstev. Nikl a kobalt způsobují v lidském těle alergické reakce a země v Evropě a Americe již zavedly restriktivní předpisy týkající se používání niklu a kobaltu. Proto byly vyvinuty hypoalergenní zlacecí roztoky.
Přidáním solí železa a titanu do roztoků pro pokovování zlatými slitinami lze dosáhnout stejného jasného efektu jako u solí niklu a kobaltu. Přidáním vodivých solí, slabých organických kyselin, jako je kyselina vinná a kyselina citronová, solí obecných kovů, solí osmia atd. lze vyřešit problém s alergií na kovy. Tyto roztoky pro pokovování zlatými slitinami nezpůsobují alergie u lidského těla. Přesto je dosažení hladkosti běžných pokovovacích vrstev obtížné a při tloušťce přesahující 3 μm se objevují praskliny. Úprava žlutých a bílých tónů je také poměrně obtížná.
Nahrazením niklu a kobaltu, které způsobují alergie, železem, přidáním vodivých solí india a použitím pufrů pro úpravu pH má vrstva pokovení ze slitiny zlata stejný jas, přilnavost a stabilitu, stejně jako stejnou tloušťku a tónové charakteristiky jako vrstvy pokovení ze slitin zlato-nikl nebo zlato-kobalt.
Zdrojem zlatých iontů je kyanid draselno-zlatý nebo kyanid draselno-zlatý. Pokud je koncentrace příliš nízká, proudová účinnost je nízká, pokovená vrstva se jeví jako zamlžená a je náchylná ke vzniku prasklin; pokud je příliš vysoká, zvyšuje se viskozita roztoku pro pokovování zlatem a pokovená vrstva je náchylná ke spálení.
Pokud je koncentrace železnatých nebo železitých iontů příliš nízká, zlato se nemůže stabilně usazovat a vrstva zlatého pokovení má sklon k zamlženému červenému hoření. Pokud je příliš vysoká, může docházet ke vzniku velkých trhlin, což ztěžuje dosažení silné vrstvy pokovení.
Přidání pouze železa způsobuje nadměrné vnitřní napětí ve vrstvě zlatého pokovení, což zvyšuje náchylnost k prasklinám a brání tvorbě hladké vrstvy slitiny. Přidání india může zmírnit napětí ve vrstvě zlatého pokovení, což umožňuje silnější zlacení, a lze jej také použít k úpravě tónu čistého zlata.
Pokud je koncentrace iontů india příliš nízká, pravděpodobně se objeví trhliny; pokud je příliš vysoká, snižuje se proudová účinnost a nanášení zlaté vrstvy se stává nestabilním.
Anorganické nebo organické kyseliny mohou být vybrány z kyseliny fosforečné, kyseliny pyrofosforečné, kyseliny borité, kyseliny wolframové, kyseliny šťavelové, kyseliny vinné, kyseliny citronové, kyseliny jablečné, kyseliny mléčné, kyseliny jantarové, kyseliny hydroxyoctové a kyseliny glukonové.
Pokud je koncentrace vodivých solí a pH pufrů příliš nízká, vodivost je špatná a pH pufrování je nedostatečné, což způsobuje nestabilní usazování vrstvy zlatého pokovování; pokud je příliš vysoká, zvyšuje se viskozita pokovovacího roztoku, což zvyšuje pravděpodobnost vzniku trhlin.
pH 1,5 až 7,0. Pod 1,5 je proudová účinnost nízká a depozice nestabilní. Nad 7,0 se snadno tvoří sraženiny železa a india, což způsobuje abnormální depozici vrstvy zlata.
Změna koncentrace výše uvedených složek, přidání povrchově aktivních látek, dalších pomocných látek atd. může zlepšit barvu, odolnost proti korozi a opotřebení nanesené vrstvy zlatého pokovení. Následující příklady to ilustrují:
Po konvenční předúpravě měděného plechu použijte pokovovací roztok uvedený v tabulce 1-17, pH 4, teplotu 40 °C a hustotu proudu 2 A/dm².2 pokovit zlatou slitinou.
Tabulka 1-17 Řešení pro pokovování zlatými slitinami a vrstva pokovování zlatými slitinami
| Složení a výsledky | Použité chemikálie | Č. 1 | Č. 2 | Č. 3 | Č. 4 | Č. 5 | Č. 6 | Č. 7 | Č. 8 |
|---|---|---|---|---|---|---|---|---|---|
| Zlato/(g/l) | Kyanid draselný a zlatý | 5 | 5 | 5 | 5 | 5 | |||
| Kyanid draselný a zlatý (III) | 5 | 5 | 5 | 5 | |||||
| Železo /(g/l) | Železitý ion | 5 | 5 | 5 | 5 | 5 | |||
| Železitý ion | 5 | 5 | 5 | 5 | 5 | ||||
| Indium /(g/l) | 5 | 5 | 5 | 5 | 5 (titan) | ||||
| Vodivá sůl a pH pufr /(g/l) | Kyselina šťavelová | 100 | 20 | 100 | 10 | 100 | |||
| Kyselina vinná | 100 | 20 | 10 | ||||||
| Kyselina citronová | 100 | 20 | |||||||
| Kyselina boritá | 20 | ||||||||
| Kyselina wolframová | 20 | 10 | 10 | ||||||
| Kyselina fosforečná | 20 | ||||||||
| Výsledek | Tloušťka jasu/μm | Nad 5 | <1 | <1 | <1 | <1 | |||
| Rychlost sedimentace / (μm/min) | 0. 15 ~ 0. 25 | Nelze určit | |||||||
| Charakteristika | Lesklé galvanické pokovování | Trhliny a abnormální srážky | |||||||
V roztoku pro pokovování slitinou zlata a železa lze přidáním india, vodivých solí a pH pufrů dosáhnout jasné vrstvy pokovování ze slitiny zlata o tloušťce nad 5 μm a tón lze upravit od žluté po bílou.
Č. 5 ~ č. 8 je výsledek bez přidání india. Rychlost pokovování je nestabilní, vrstva pokovování vytváří mnoho trhlin, povrch je abnormální (spálený, zamlžený) a dosažení lesklé vrstvy zlatého pokovování o tloušťce nad 1 μm je nemožné. Použití thalia místo india také způsobuje praskliny ve vrstvě zlatého pokovování a abnormální usazování. Takové pokovovací roztoky nemají praktické využití. Tabulka 1-17 ukazuje vlastnosti roztoků pro pokovování zlatými slitinami a vrstev zlatého pokovování.
Vzhledem k alergenním vlastnostem niklu a kobaltu a omezením prodeje nebo vývozu se v pokovovacích roztocích ze slitin zlata používají železo a indium jako náhrada niklu a kobaltu. Vlastnosti pokovovacích vrstev jsou stejné, což eliminuje alergenní problémy kovů, jako je nikl a kobalt. Nanesená pokovovací vrstva v pokovovacím roztoku je stabilní a lze upravit praktický barevný tón.
3. Neutrální zlacení
Neutrální zlacení se nazývá měkké zlacení nebo čisté zlacení. Vyznačuje se vysokou čistotou nanesené vrstvy zlata, bez lesku a s nízkou tvrdostí. Používá se hlavně pro zlacení vrstev v pouzdrech integrovaných obvodů. Roztok pro zlacení se skládá z zlaté soli, kyanidu draselného a zlata, pufrovacích činidel s neutrálním pH, jako je citrát, fosfát a směsi těchto solí. Tyto soli navíc také zvyšují vodivost roztoku pro zlacení.
Charakteristika neutrálního pokovovacího roztoku: Přidání stopového množství krystalizačního modifikátoru může změnit precipitační strukturu pokovované vrstvy, což má za následek citronově žlutý barevný odstín. Při nedostatečném přídavku je vzhled červenohnědý nebo spálený; při nadměrném přídavku dochází ke společnému srážení, které snižuje čistotu pokovované vrstvy.
3.1 Dekorativní zlacení
Tabulka 1-18 Složení a provozní podmínky roztoku pro pokovování slitinou zlata a mědi (I)
| Složení a provozní podmínky | Parametry | Složení a provozní podmínky | Parametry |
|---|---|---|---|
| Kyanid draselný a zlato/(g/l) | 7 | pH | 6. 8 až 75 |
| Na2HPO4 (hydrogenfosforečnan disodný)/(g/l) | 28 | Teplota roztoku pro galvanické pokovování/℃ | 65 ~ 75 |
| Cu[Na]2Cu(CN)3]/(g/l) | 7 | Hustota proudu/(A/dm2) | 0,5 až 1 |
| Fe (kyanid železnatý)/(g/l) | 3 |
Tabulka 1-19 Složení a provozní podmínky roztoku pro pokovování slitinou zlata a mědi (II)
| Složení a provozní podmínky | Parametry | Složení a provozní podmínky | Parametry |
|---|---|---|---|
| Kyanid draselný a zlato/(g/l) | 0. 7~1. 5 | pH | 8.5 |
| Cu(EDTA měďnatá sůl)/(g/l) | 8 | Teplota roztoku pro galvanické pokovování/℃ | 53 〜 57 |
| Na2EDTA (bez EDTA) (g/l) | 16 | Hustota proudu/(A/dm2) | 1 ~ 1. 5 |
Jedná se o roztoky pro pokovování zlatými slitinami běžně používané v Evropě. Pokovená vrstva je zcela pevný roztok obsahující značné množství mědi, ale není náchylná ke změně barvy. Zkouška provzdušňováním kyselinou dusičnou vykazuje vynikající odolnost proti korozi.
Vrstva pokovování slitinou zlata a mědi z roztoku EDTA pokovování se tepelně zpracovává při teplotě 300~400℃ za účelem získání Au-Cu.3 intermetalická sloučenina s velmi vysokou tvrdostí. Obrázek 1-23 ukazuje polarizační křivku pokovovacího roztoku v tabulce 1-4.
3.2 Funkční zlacení
Tabulka 1-20 Složení a provozní podmínky vysoce čistého neutrálního zlacecího roztoku
| Složení a provozní podmínky | Č. 1 | Č. 2 | Č. 3 | Č. 4 | Č. 5 |
|---|---|---|---|---|---|
| Kyanid draselný a zlato/(g/l) | 10. až 31. | 10 až 20 | 7. až 18. | 6 | 8.2 |
| Dihydrogenfosforečnan sodný/(g/l) | 60 | - | 82 | - | - |
| Pyrofosforečnan draselný/(g/l) | - | - | - | - | 150 |
| Citrát/(g/l) | 60 | 60 až 125 | 50 až 75 | 90 | - |
| Citrát draselný | Citrát draselný | Citrát amonný | Rozpustná sůl kyseliny | ||
| Pentahydrát thiosíranu sodného/(g/l) | 5 až 10 | - | - | - | - |
| Triethylfosfát/(g/l) | - | 30 až 60 | - | - | - |
| Aminotrimethylfosfát/(g/l) | - | - | - | 80 | - |
| Benzylalkohol (hmotnostní zlomek)/% | - | - | - | - | 0. 05 |
| pH | 5,5 až 8,0 | 6 〜 8 | 5 ~ 6. 5 | 6.0 | 7 ~ 8 |
| Teplota /℃ | 60 | 60 | 45 až 100 | 65 | 60 |
| Hustota proudu /(A/dm2) | 0,1 až 1,5 | 0. 1 ~ 0. 3 | 0. 1 ~ 0. 4 | 0. 1 ~ 0. 5 | 0. 1 |
4. Pokovování sulfitovým zlacením
Od roku 1970 je praktické zlacení pomocí siřičitanových solí zlata. Komplexní soli siřičitanu zlatého(I) podléhají [Au(SO3)2]3-⇌Au++2SO32- disociace.
Stabilita tohoto typu komplexního iontu je mnohem nižší než u kyanidových komplexů, s konstantou stability přibližně 1010, takže stabilita je 1028 krát horší než [Au(CN)2–] .
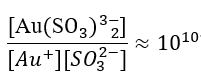
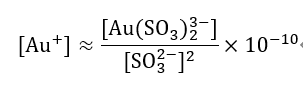
Am je aminoskupina alifatického aminu.
Anion disociuje podle následujícího vzorce:
Au(Am)2(TAK3)2]3- ⇌[Au(Am)2]+ + 2(SO3)2- (1-2)
A také [Au(Am)2]+ ⇌Au+ + 2:00 (1-3)
Tabulka 1-21 Složení roztoku pro galvanické pokovování siřičitanem zlatým
| Složení | Parametry |
|---|---|
| Zlato [iminokoordinovaná sůl siřičitanu sodného a zlata(I)]/(g/l) | 12 |
| Siřičitan sodný (volný)/(g/l) | 50 |
| Citrát sodný/(g/l) | 50 |
| Tetraboritan sodný/(g/l) | 10 |
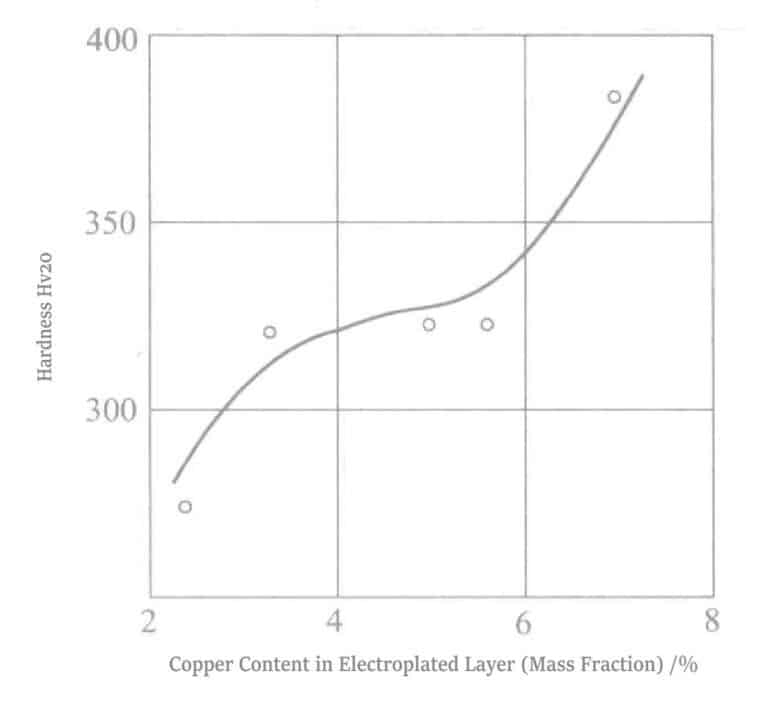
Siřičitan zlatý se obecně používá k pokovování ternárních slitin zlata Au-Pd-Cu během galvanického pokovování zlatých slitin. Jeho výhody jsou: 1. Pokovená vrstva se jeví růžová; 2. Tvrdost dosahuje až Hv 400; 3. Vynikající odolnost proti opotřebení; 4. Vynikající odolnost proti korozi. Nevýhody jsou: 1. Poměr nanášení slitiny se mění nerovnoměrně s hustotou proudu a teplotou; 2. Anoda podléhá redukci a nanášení během dlouhodobého pokovování.
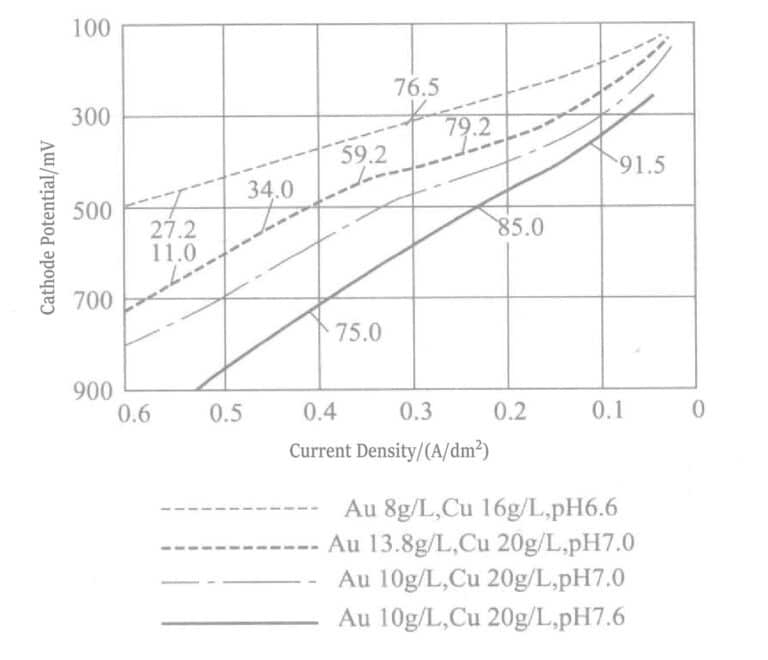
Yoshimura a kol. použili podmínky v tabulce 1-22, s různými koncentracemi mědi 0,0021~0,0211 mol/l, teplotou pokovovacího roztoku 25 °C, 50 °C a hustotou proudu 0,230 A/dm².2 pro pokovování. Vzhled, tvrdost, odolnost proti opotřebení a další hodnoty naneseného povlaku jsou uvedeny v tabulce 1-23. Ve srovnání s velikostí zrna 337 Å pokovené vrstvy ze slitiny zlata a palladia je velikost zrna 161~231 Å pokovené vrstvy ze slitiny zlata, palladia a mědi menší, s tvrdostí pokovování 400 Hv a dobrou odolností proti opotřebení. Existuje související patent pro pokovenou vrstvu ze slitiny zlata, palladia a mědi.
Tabulka 1-22 Složení roztoku pro galvanické pokovování slitiny Au-Pd-Cu Jednotka: mol/l
| Složení | Parametr | Složení | Parametr |
|---|---|---|---|
| Au(SO3 )2 3- | 0.0204 | Na2TAK3 | 0.1983 |
| Pd(en)2 2+ | 0.0236 | NaAsO2 | 0.0115 |
| EDTA-2Na | 0.2109 | CuSO44 | 0,0021 〜 0,0211 |
Tabulka 1-23 Porovnání tvrdosti a odolnosti proti opotřebení ze slitiny Au-Pd-Cu a slitiny Au-Ni
| Složení galvanického roztoku, depoziční poměr/% | Tvrdost VHN | Odolnost proti opotřebení |
|---|---|---|
| Au : Ni | ||
| 92 : 8 | 237 | 20 |
| Au: Pd: Cu | ||
| 87: 3: 10 | 362 | 26 |
| 80: 5: 15 | 437 | 33 |
| 79: 8: 13 | 383 | 28 |
| 75: 9: 16 | 400 | 28 |