Vad du behöver veta om guldplätering och guldlegeringar
Den ultimata guiden till förgyllningstekniker och lösningar för smycken
Inledning:
Vilka olika typer av guldpläteringslösningar finns det och deras egenskaper? Hur kan man använda olika guldföreningar för plätering? Varför välja tunn eller tjock guldplätering för dina projekt? Denna omfattande guide täcker allt från grunderna i guldpläteringslösningar, inklusive syra-, neutral- och cyanidfria alternativ, till detaljerade processer för tunn och tjock guldplätering. Lär dig om historien och moderna tekniker som används i branschen, perfekt för smyckesmakare, designers och återförsäljare som vill förbättra sina produkter med hållbara och vackra guldfinisher.
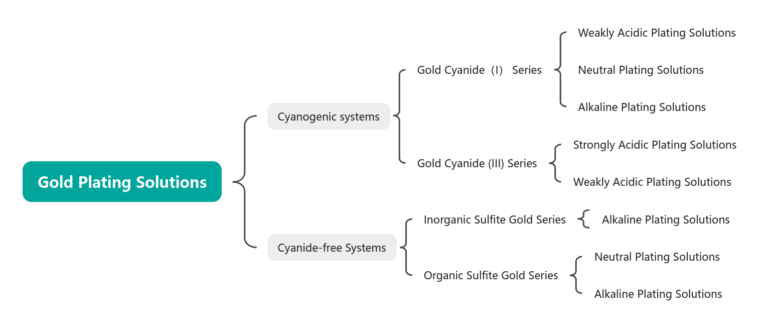
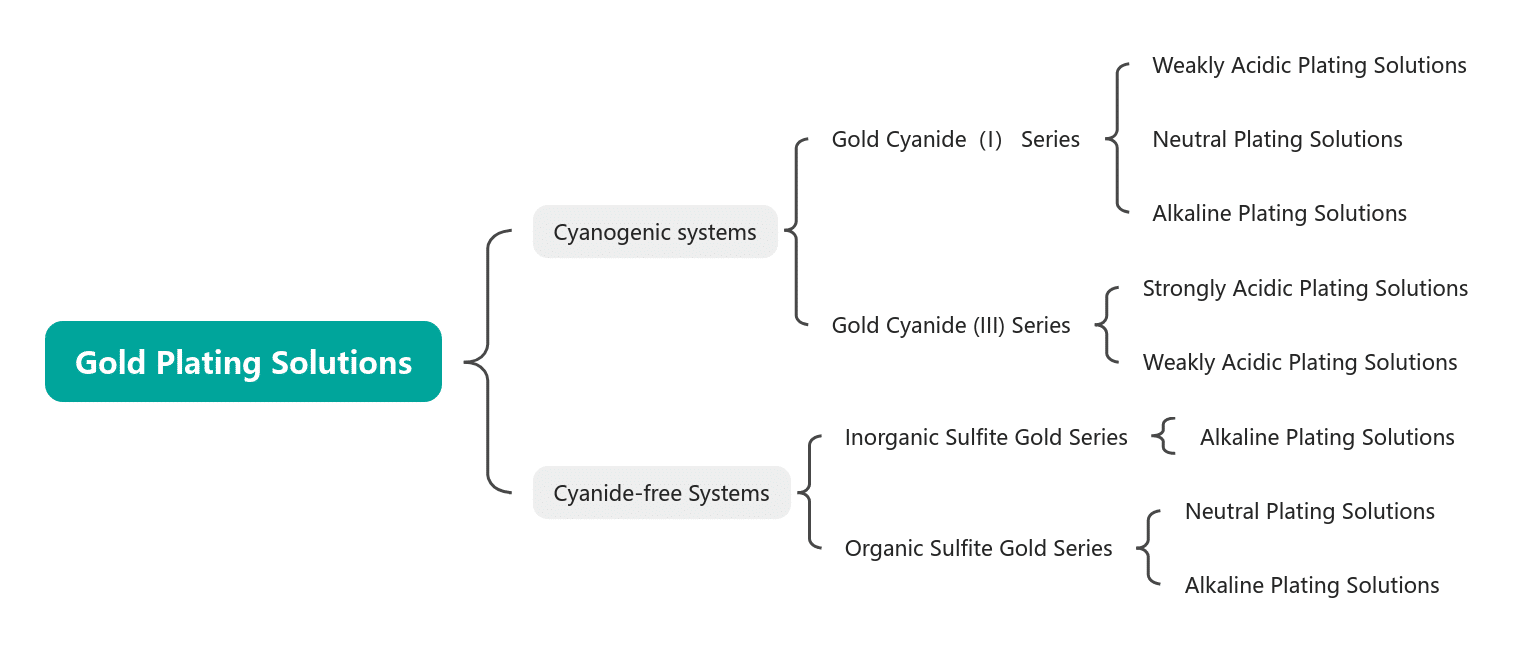
Klassificering av guldpläteringslösningar
Innehållsförteckning
Avsnitt I Översikt
År 1800 uppfann professor Lugi V. Brougnatell från Italien förgyllningstekniken. Under de följande mer än 100 åren var elektroplätering av nickel, koppar och mässing populärt i Europa, med endast ett fåtal elektropläteringsfabriker som utförde förgyllning av klockor, personliga prydnadsföremål och metallporslin för att möta behoven hos ett fåtal rika personer. Samtidigt låg huvudfokus i USA på förgyllning relaterad till bearbetning av fina ädelstenar.
År 1913 etablerade Frary ett relativt omfattande system för guldelektroplätering, vilket var pionjär inom modern elektroplätering.
År 1950 var EC Rinker den första som utvecklade en teknik för blank guldplätering genom att tillsätta spårmängder av silver till guldpläteringslösningar.
Därefter utvecklades sura förgyllningslösningar baserade på organiska syror och användes i stor utsträckning.
År 1952 var EA Parker pionjär inom tillämpningen av kaliumguld(I)cyanid och rapporterade att tillsats av svaga organiska syror (såsom citronsyra, vinsyra etc.) till kaliumguld(I)cyanidpläteringslösningar som delvis neutraliserats med alkaliska ammoniumsalter kunde hålla pläteringslösningen stabil vid pH=3.
År 1959 avslöjade EC Rinker sur guldpläteringsteknik inom intervallet pH 3~5.
Efteråt fick elektropläteringstekniken för guld mer omfattande och djupgående forskning, inklusive analys av deponeringsprinciper och fysikalisk-kemiska egenskaper.
Med den ökande efterfrågan på modern industriell produktion har många tillämpade förgyllningstekniker mognat och blivit praktiska.
1. Typer och egenskaper hos guldpläteringslösningar
Tabell 1-1 Klassificering av guldpläteringslösningar
Tabell 1-2 Egenskaper hos olika typer av guldpläteringslösningar
| Elektropläteringslösning | Guldligand | Surhet och alkalinitet | pH-värde | Utseende | Apparat |
|---|---|---|---|---|---|
| Syraguldplätering Hårdguldplätering | KAu(CN)2 | Svagt sur | 3~5 | Glans | Kontaktdon, kontakter, terminaler, dekorativa delar |
| Neutral guldplätering Mjuk guldplätering Ren guldflätning | KAu(CN)2 | Neutral | 6~9 | Ingen glans | Kretskort, halvledare |
| Cyanidförgyllning | KAu(CN)2 | Alkalisk | 10~13 | Glans | Dekorativa delar |
| Cyanidfri guldplätering | Na3Au(SO3)2 | Neutral | 6〜8 | Ingen glans | Guldkretsmönster, kretskort |
| Alkalisk | 8~12 | Glans |
2. Guldföreningar som används för förgyllning
Guld har många valenstillstånd, bland vilka +3-valensföreningarna är de mest stabila, följt av +2-valensföreningar, medan +5-valensföreningar sönderfaller lätt. Guld(I) i vattenlösning har flera stabila ligander, såsom typiska dihalogenoaurat(I)-syrakoordinationssalter, dicyanoauratkoordinationssalter, tiosulfatguld(I)-syrasalter, etc., bland vilka cyanider är mycket stabila, med en stabilitetskonstant K=4×1028Därför används guld(I)- och guld(III)-föreningar mest och är de vanligaste, medan guld(II)- och guld(V)-föreningar också förstås och tillämpas i allt större utsträckning.
Hittills är kaliumguld(I)cyanid det mest använda och vanligaste huvudsaltet för förgyllning. Kaliumguld(III)cyanid och natriumguld(I)sulfitpläteringslösningar har använts allt oftare under senare år.
1.1 Kaliumguld(I)cyanid, KAu(CN)2 (nedan kallad kaliumguldcyanid)
(1) Relativ molekylär massa: 288,10. Beredningsmetoder inkluderar kemiska metoder och elektrolysmetoder.
(2) Egenskaper: Kaliumguldcyaniden som framställs med denna metod är färglös kristallin, lättlöslig i vatten, något löslig i etanol och olöslig i aceton och hexadekanol. Den sönderfaller lätt vid upphettning i sura förhållanden, är ljusstabil i luften och dess stabilitet är betydligt högre än för liknande koppar- och silverkyanidligander.
(3) Beredningsmetoder
① Kemisk metod
a. Lös upp guld: Placera rent guld i utspädd kungsvatten (förhållandet mellan vattenvolym och kungsvatten är 1:4) och värm tills det löses upp → När guldblocket är helt upplöst, sänk temperaturen på lämpligt sätt → Tillsätt upprepade gånger saltsyra droppvis tills ingen brun kvävedioxid produceras → Koncentrera långsamt tills lösningen blir djupt rödbrun, med ett litet rullande glänsande reducerat guldpulver som syns.
b. Neutralisationsreaktion: Kyl lösningen till cirka 25 ℃. Under omrörning → tillsätt droppvis mättad natriumhydroxidlösning → tills den bildar ett brunrött halvfast ämne → tillsätt kaliumcyanid tills lösningen blir färglös och transparent (med en liten mängd aggregerade guldpulverpartiklar som utfälls).
c. Försurning (beredning av guldcyanid): Kyl lösningen till cirka 25 ℃ → Tillsätt saltsyra droppvis under omrörning → tills en ljus gul-gyllene cyanidfällning bildas → Rör om och låt stå vid låg temperatur → Låt den stå för skiktning, kyl den naturligt till rumstemperatur, avlägsna den övre avfallsvätskan, filtrera den och tvätta den gula fällningen med varmt vatten.
d. Syntes av kaliumguldcyanid: Placera guldcyanid i en liten mängd vatten → Tillsätt en uppmätt mängd mättad kaliumcyanidlösning under omrörning → tills lösningen blir färglös och transparent → Filtrera för att avlägsna guldpulver → Koncentrera → Kyl för att kristallisera → Avlägsna moderluten → Torka den vita kristallina kaliumguldcyaniden vid 80 ℃ → Förslut och förpacka.
Med denna metod för att framställa kaliumguldcyanid är produktionsutrustningen enkel och kan effektivt separera spårföroreningar i guld för att framställa kaliumguldcyanid med högre renhet.
② Membranelektrolys: Metod Sovjetunionen var först med att använda mikroporös keramisk membranelektrolys för att producera olika metaller och metallföreningar. Inhemska och utländska företag använder vanligtvis organisk membranelektrolys för att producera kaliumguldcyanid. Denna elektrolysmetod har dock problemet att organiska membran korroderas av alkaliska elektrolyter, och korrosionsprodukterna orsakar betydande skador på högkvalitativa integrerade kretsar, högdensitetskretskort och guldpläteringsskikt på kontakter (Suzhou University Special Chemical Reagent Industrial Company har framgångsrikt utvecklat en praktisk tillämpning).
1.2 Kaliumtiocyanat (III), K[Au(CN4)]·H2O
(1) Relativ molekylmassa: 358.15.
(2) Egenskaper: Färglösa kristaller, lättlösliga i vatten, blir vid upphettning över 200 ℃ ett vattenfritt salt, smälter vid röd värme och sönderfaller vid högre temperaturer.
(3) Beredningsmetoder:
① Värm kaliumguldcyanid i kaliumcyanidlösning;
② Lös upp guldtriklorid i K3[Fe(CN)6];
③ Lös upp guld(III)dicyanid i K3[Fe(CN)6];
④ Behandla kaliumguldcyanid med brom, och den resulterande K[Au(CN)2Br2] reagerar med kaliumcyanid i metanol för att framställa produkten.
1.3 Guldklorid
(1) Guld(I)klorid, AuCl
① Relativ molekylmassa: 232,46.
② Egenskaper: Ljusgula, icke-hygroskopiska kristaller börjar långsamt sönderfalla vid uppvärmning över 150 ℃. Sönderfaller i vatten och etanol och löses upp i kloralkalilösning för att bilda gulddiklorat.
③ Beredningsmetod: Guldklorat (HAuCl4, III) placeras under högvakuum och upphettas till 156 ℃ för att sönderdela och erhålla produkten.
(2) Guldklorid (III), HAuCl4
① Relativ molekylmassa: 303,37.
② Egenskaper: Röda nålliknande kristaller, smältpunkt 229 ℃, kokpunkt 254 (sönderdelning), hygroskopisk, vattenlösningen är rödbrun, bildar H2[AuCl3O] i sur lösning. Sönderfaller långsamt i en neutral vattenlösning, varvid guld utfälls. Indunstning av vattenlösningen ger ett orange kristallint dihydratsalt, lösligt i etanol och eter.
③ Beredningsmetod: Vid en temperatur mellan 225 och 250 ℃ leds klorgas genom ett guldpulver på 120-127 kPa (900-950 mmHg) för att framställas. Alternativt kan du lösa upp guld i kungsvatten, tillsätta upprepade gånger saltsyra för att avlägsna salpetersyra, sedan värma långsamt vid låg temperatur för att avlägsna överskott av saltsyra, koncentrera, kyla och kristallisera för att erhålla produkten.
1.4 Guld(III)oxid, Au2O3
(1) Relativ molekylmassa: 441,93.
(2) Egenskaper: Svart (brunt) pulver eller kristallin polymerstruktur, en guldförening omgiven av syreatomer som bildar ett plant tetrakoordinatkomplex. Den sönderfaller långsamt i solljus, börjar frigöra syre vid uppvärmning till 110 ℃, blir guld(I)oxid vid 160 ℃ och förlorar allt syre vid 250 ℃, och blir en amfotär oxid som är olöslig i vatten men löslig i saltsyra och alkaliska vattenlösningar.
(3) Beredningsmetod: Lös upp guld i kungsvatten, tillsätt upprepade gånger saltsyra och värm (5 gånger) för att avlägsna salpetersyra, tillsätt natriumkarbonat tills det är alkaliskt för att producera en fällning, tvätta med vatten, centrifugera, utför elektrodialys i 2 veckor, torka sedan vid 140~150 ℃ för att erhålla produkten.
Avsnitt II Tunn guldplätering
Elektroplätering av tunn guldlösning, eller penselplätering av guldlösning, skiljer sig från flashplätering (strikeplätering) av guldlösning. Penselplätering av guldlösning baseras vanligtvis på alkaliska cyanidvätskor, med många typer som sträcker sig från rent guld till legeringar, såsom kaliumguldcyanidpläteringslösningar med olika ligandsystem. Vissa företag använder också sina egna specialutvecklade pläteringslösningar. Flashpläteringsguldlösningar är mestadels sura och kan fungera som baspläteringsskikt för tjocka guldskikt, med högre strömtätheter på kort tid för att plätera ett tunt guldskikt för att förbättra spridningen och vidhäftningen av det övre tjocka guldpläteringsskiktet.
Tabell 1-3 visar sammansättningen och driftsförhållandena för några representativa penselpläteringslösningar för tunn guldplätering. Bland dessa fungerar fosfat som en buffert och även som ett konduktivitetsmedel. Från den nyframställda pläteringslösningen kan man uppnå en bra beläggning, men föroreningar bildas snabbt i pläteringslösningen efter elektrifiering, vilket gör att pläteringsskiktet lätt utvecklar färgskillnader. Den främsta anledningen är att när temperaturen på pläteringslösningen stiger genomgår cyanid en sönderdelningsreaktion. Därför måste pläteringslösningen behandlas efter en tids användning, vanligtvis genom filtrering med aktivt kol.
Tabell 1-3 Olika representativa lösningar för tunn guldplätering med borstplätering
| Komponenter | Ren guldpläteringslösning | Hamiltons färg | Vit 1 | Vit 2 | Grönaktigt guld | Rött guld | ||
|---|---|---|---|---|---|---|---|---|
| Gul | Rosa | Grön | ||||||
| KAu (CN)2/(g/L) | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 0.41 | 0.33 | 2 | 0.82 |
| Fritt KCN/(g/L) | 7.5 | 7.5 | 2.0 | 2.0 | 15 | 15 | 7.5 | 4 |
| K2HPO4/(g/L) | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
| K2Ni(CN)4/(g/L) | - | 0.26 | 0.26 | 0.26 | 1.1 | - | - | 0.21 |
| K2Cu(CN)3/(g/L) | - | 0.13 | 1.1 | - | - | - | - | 2.64 |
| K2Ag(CN)2/(g/L) | - | - | - | 0.05 | - | - | 0.26 | - |
| K2Sn(OH)6/(g/L) | - | - | - | - | - | 2.11 | - | - |
| Pläteringslösningens temperatur / ℃ | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 65 ~ 70 | 65 ~ 70 | 55 ~ 70 | 55 ~ 70 |
| Strömtäthet/(A/dm²2) | 1 ~ 4 | 1 ~ 3.5 | 2 ~ 5 | 1 ~ 4 | 3 ~ 6 | 3 ~ 5 | 1 ~ 3 | 3 ~ 4 |
Vid elektroplätering av rent guld påverkar andra metaller än guld i pläteringslösningen pläteringsskiktets färg avsevärt. Koppar gör pläteringsskiktet märkbart rött, nickel och zink gör pläteringsskiktet vitt, och bly gör att svarta, fläckiga, grova, gråbruna ämnen lätt fäster på ytan av pläteringsskiktet. Därför kan färgen på guldlegeringar i pläteringsskikt erhållas genom att tillsätta olika metaller. Det är dock inte lätt att uppnå den ideala färgtonseffekten i faktiska elektropläteringsprocesser.
Anoden i guldpläteringslösningen använder vanligtvis olösliga anodmaterial, såsom rostfritt stål och svarta platina-titannätplattor, och beroende på pläteringslösningen kan även kolplattor användas. Efter att en viss ström har förbrukat pläteringslösningen bör den analyseras regelbundet för att fylla på koncentrationen av guldjoner, ligander och andra aktiva komponenter. En amperetimmätare kan användas för automatisk beräkning och tillägg till det dagliga arbetet. Det sker också en hel del uttag av elektropläteringslösning under den tunna guldpläteringsprocessen, vilket måste förberäknas före plätering för att fylla på förbrukningen och tidsförlusten. Processflödet för tunn guldplätering visas i figur 1-1.

I processflödet är koncentrationen av flash-förgyllningslösningen ungefär 1/5~1/3 av koncentrationen av den huvudsakliga pläteringslösningen (ytskiktet eller det övre guldskiktet). Efter att ytan på den pläterade delen är helt täckt med ett extremt tunt guldskikt, placeras den sedan i den huvudsakliga pläteringslösningen för att plätera guldskiktet med önskad färgton.
Resterande cyanid på ytan av guldpläteringsskiktet kan bilda vattenfläckar, vilket påverkar pläteringens utseende och elektriska prestanda. Därför måste pläterade delar rengöras och torkas noggrant efter guldplätering. Förutom uppvärmning för torkning kan specialprodukter använda organiska lösningsmedel för uttorkningsbehandling. Till exempel kommer uttorkning och torkning med vattenfri etanol inte att påverka guldpläteringsskiktets färg, och torkhastigheten är också snabb.
Penselförgyllningsskiktet är mycket tunt och kontrolleras generellt under 0,1 μm. Olika organiska skyddsfilmer appliceras oftast på det tunna guldskiktet när det används som ett ytbeläggningsskikt för att förhindra lätt slitage och missfärgning. Det vanligaste organiska skyddet är akrylmelaminserieharts, med en filmhårdhet som är ungefär motsvarande hårdheten hos en 3H~4H-penna och en tjocklek på 10~15 μm. Elektroforetisk beläggning använder ofta anjoniskt akrylmelaminharts.
Eftersom det tunna guldpläteringsskiktets yta snabbt avger en enhetlig och jämn färg på kort tid, använder pläteringsprocessen vanligtvis katodrörelse eller jetrörning av pläteringslösningen. Genom att kontrollera temperaturen på pläteringslösningen, koncentrationen av guldjoner och strömtätheten regleras förhållandena för att undertrycka färgskillnader i pläteringsskiktet.
Avsnitt III Tjock guldplätering
Tabell 1-4 Sammansättning och driftsförhållanden för pläteringslösningen och pläteringsskiktets egenskaper
| Guldförening | Typer av elektroplätering | Ledande salter | Legeringsmetall pH | Sammansättning | Fällningsstruktur | Egenskaper |
|---|---|---|---|---|---|---|
| Kaliumguldklorid | Svag syra | Citronsyra, oregano, fosforsyra, aminosulfonsyra, vinsyra, oxalsyra | Rent guld, kobolt, nickel, järn, indium, tenn 3,0 ~ 5,0 | Citronsyra + natriumcitrat 80~100 g/L Kaliumguldcyanid 8 g/L Nickelsulfamat 3,0 g/L Zinkacetat 0,5 g/L | Skiktstruktur, med eutektisk organisk polymer mellan lagren | Den kan ge ljusa och hårda utfällningar; pläteringslösningen är lätt att justera och lågtemperaturplätering är möjlig. |
| Neutral | Fosforsyra, svavelsyra, borsyra, organiska syror | Rent guld, fällning, kristallmodifierare: titan, selen 5,0 ~ 8,0 | Kaliumguldcyanid 2 ~16 g/L Kaliumcitrat 120 ~150 g/L Kaliumfosfat 10~50 g/L Ammoniumsulfat 20~150 g/L En av Ti, Ce, Te, Bi 0,01~40 mg | Kolumnära eller nålliknande kristaller, mindre utfällning av föroreningar | Rent guldpläteringsskikt 99.99%; utfällt praktiskt mjukt, halvblankt eller matt tjockt pläteringsskikt; ansamling av föroreningar påverkar pläteringslösningens livslängd. | |
| Alkalisk | Cyanid, karbonat, pyroforsyra | Rent guld, silver, kadmium, zink, antimon 8,5 〜 13,0 | Rent guld, silver, kadmium, zink, antimon 8,5 〜 13,0 | Korngränser med utfällning av cyanidpolymerer | Ett mycket jämnt tjockt guldlager på cirka 300 μm kan erhållas; ett pläteringslager från rent guld till 9K-legering kan erhållas; okänsligt för föroreningar, enkel hantering av pläteringslösningen |
(1) Polyetylenimins roll – högmolekylära polyaminorganiska föreningar: Organiska föreningar adsorberas selektivt i Helmholtz dubbelelektriska lager, vilket förstärker polarisationseffekten. Under elektroavsättningsprocessen adsorberas organiska ämnen kontinuerligt på aktiva tillväxtpunkter, vilket hämmar avsättningen och rörelsen av guld över katodytan, vilket resulterar i en jämn och blank yta. Emellertid påverkar en viss mängd organiskt material som samavsätts i gittret hos de avsatta kristallerna allvarligt negativt pläteringsskiktets fysikaliska egenskaper, särskilt dess slitstyrka. Generellt sett förbättras detta genom att tillsätta andra metaller för att producera samavsättning för att förbättra de negativa effekterna av organiska ämnen.
(2) Andra halvmetallers roll, såsom arsenik, tallium, selen och bly: Tillsats av halvmetaller ger inte bara ett bra, blankt guldpläteringsskikt från cyanid-guldpläteringslösningen, utan uppnår också ett mycket blankt guldpläteringsskikt från sulfitpläteringslösningen. Generellt sett är en ytterligare mängd under 10-6 kan ge en mycket tydlig karakteristisk effekt.
Principen för ljusning av halvmetaller: halvmetalliska ämnen adsorberar jämnt på katodytan, katalyserar, främjar kärnbildning av guldkristaller, genererar fler tillväxtpunkter och främjar jämn kristallisering och avsättning.
(3) Eutektikens roll för övergångsmetallerna kobolt, nickel, järn etc.: Det blankförgyllda lagret legerat med kobolt och nickel innehåller en viss mängd kol. Om kolhalten är under 0,1% kan ett blankförgyllt lager inte erhållas även om kobolt genomgår eutektik.
Isotop 14C-experiment har bevisat att kolet härstammar från kobolt-cyanidkomplexliganden. Genom att lösa upp guldpläteringsskiktet som innehåller kobolt- och nickelsyrapläteringslösning med kungsvatten kan ämnen som innehåller kol separeras. Under mikroskopet liknar det kungsvattenbehandlade materialet utseendet plast. Denna membranliknande polymer bildar ett stort kontaktmotstånd på ytan av pläteringsskiktet.

1. Alkalisk guldplätering
Bland alla guldpläteringslösningar är alkalisk cyanid-guldpläteringslösning den äldsta elektrolytiska guldpläteringslösningen. Alkalisk cyanid-guldpläteringslösning används ofta för plätering av rent guld, guldlegeringar och dekorativ guldplätering och kan även användas för funktionell elektronisk guldplätering. Pläteringslösningen består vanligtvis av kaliumguldcyanid, fri cyanid, kaliumkarbonat etc. Olika metallsalter kan tillsättas enligt olika behov vid plätering av guldlegeringar.
Förgyllning med en alkalisk cyanid-förgyllningslösning resulterar i god beläggningsjämnhet och vätbarhet, och den är mycket lämplig för att plätera guldlegeringar med låg guldhalt. Den kan plätera guldlager från låga K-värden till höga K-värden. Pläteringslösningen har en hög halt av fri cyanid, vilket gör den mindre känslig för föroreningar. Fri cyanid kan lösa upp guld, så de pläterade föremålen måste rengöras omedelbart efter att de tagits ur pläteringsbadet; annars kommer kvarvarande pläteringslösning på ytan att orsaka defekter som ett vågigt utseende.
Cyanidfria guldpläteringsskikt används huvudsakligen för wafers, drivkretsar för flytande kristallskärmar, guldsvetsplattor för förpackningar samt kretsledningar, terminaler och andra kontaktpunkter för substrat. På ledningar för wafers med ljuskänsliga resistfilmer är hörnhöjden på guldsvetsplattorna flera tiotals mikrometer och tjockleken 15~20 μm. Den producerade CN- i cyanidguldpläteringslösningen kan korrodera den ljuskänsliga resistfilmen och skyddsfilmen runt substratet; därför används oftast cyanidfria och svagt sura pläteringslösningar.
Alkaliska guldpläteringslösningar är huvudsakligen cyanidförguldpläteringslösningar, med tillsatta metaller från binära till kvartära; praktiska guldlegeringspläteringsskikt är binära eller ternära guldlegeringar. Representativa sammansättningar och driftsförhållanden för alkaliska guldlegeringspläteringslösningar visas i tabell 1-5.
Tabell 1-5 Sammansättning och driftsförhållanden för alkalisk guldlegeringspläteringslösning
| Typer av legeringar | Sammansättning och driftsförhållanden | |
|---|---|---|
| Binära legeringar | Guld-kopparlegering |
Kaliumguldcyanid 12 g/L Kaliumkopparcyanid 7 g/L Kaliumtiocyanid 10 g/L 2-pyridinkarboxylsyra 8 g/L pH 8 (justerat med KOH) 70℃, 0,4A/dm²2 |
| Guld-silverlegering |
Kaliumguldcyanid 15 g/L Kaliumsilverkyanid 3 g/L Kaliumnickelcyanid 20 g/L Kaliumkoboltcyanid 10 g/L Kaliumcyanid 80 g/L Ammoniumhydroxid 20 g/L 15℃, 0,6A/dm²2 |
|
| Guld-tennlegering |
Kaliumguldcyanid 30 g/L Tennnitrat 7 g/L Kaliumpyrofosfat 100 g/L Rumstemperatur, 1A/dm2 |
|
| Ternära legeringar | Guld-koppar-kadmiumlegering |
Kaliumguldcyanid 15 g/L Kaliumkopparcyanid 200 g/L Kaliumkadmiumcyanid 5 g/L L-glutaminsyra 50 g/L 70℃, 1A/dm2 pH 8 (justerat med KOH) Au:Cu:Cd=70:15:15 |
1.1 Plätering av guld-silverlegering
Tabell 1-6 Sammansättning av guld-silverlegeringspläteringslösning
| Sammansättning och driftsförhållanden | Parametrar | Sammansättning och driftsförhållanden | Parametrar |
|---|---|---|---|
| Kaliumguldklorid (beräknat som Au)/(g/L) | 8 | Tensid | Liten mängd |
| Kaliumsilverklorid (beräknat som Ag)/(g/L) | 2.5 | Temperatur /℃ | 27 |
| Fritt kaliumtiocyanat/(g/L) | 100 | Strömtäthet /(A/dm²2) | 1 |
| Aminsalt/(g/L) | 5 |

Koncentrationen av fri kaliumcyanid bör inte vara lägre än 90 g/L, generellt över 100 g/L, vilket är mer lämpligt. Över 120 g/L ökar polarisationen, hämmar silveravsättning, ökar guldavsättningshastigheten och bildar ett högkvalitativt guldlager.
Guldhalten justeras enligt guldlegeringens K-värde genom att reglera koncentrationerna av guld och silver i pläteringslösningen. Till exempel, när silverkoncentrationen är 2,5 g/L i legeringens pläteringsskikt, måste guldkoncentrationen kontrolleras inom intervallet 7~10 g/L för att erhålla 18K guld.
Inverkan av silverkoncentration: När silverkoncentrationen är låg är ljusstyrkan för pläteringsskiktet brett och guldhalten hög.
Inverkan av aminkoncentration: När mängden amin tillsätts till 30 g/L förändras inte guldavsättningshastigheten, men jämfört med ingen tillsats ökar det pläteringsskiktets ljusstyrka. När mängden tillsatt amin ökar till 50 g/L ökar guldavsättningshastigheten, vilket orsakar ett "brinnande" fenomen i områden med hög strömtäthet. Huvudsyftet med att tillsätta amin är att minska spänningen i tjocka guldpläteringsskikt. Att tillsätta ligander som trietylentetramin (10~30 g/L) till ljusa guld-silverlegeringspläteringslösningar kan ge bättre resultat.
Figur 1-4 visar sambandet mellan temperaturen hos pläteringslösningen, strömtätheten och guldavsättningshastigheten. Hårdheten hos det avsatta guldskiktet är Hv25170~210. Yt- och tvärsnittsförhållandena för guldpläteringsskiktet: efter direkt plätering av guld med en tjocklek av 4 μm på nickelpläteringsskiktet observerades det avskalade guldskiktet under ett elektronskanningsmikroskop. Resultaten visas i figur 1-5 och 1-6, vilket indikerar att ytan och tvärsnittet av pläteringsskiktet inte har några porer och är tätt. Kristalliniteten hos guldpläteringsskiktet testades med röntgendiffraktion efter direkt plätering av cirka 10 μm guld på en kopparplatta. Toppen av baskopparskiktet detekterades inte; endast topparna av guld-silverlegeringspläteringsskiktet mättes, och kristallisationen växte i (111)-planet.
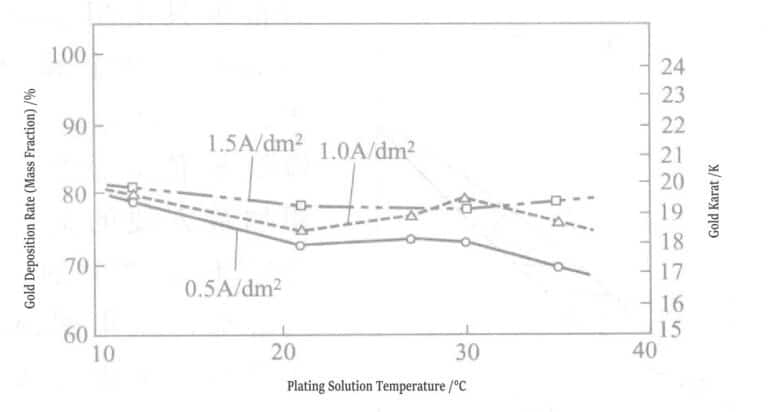

Figur 1-5 Ytbeläggning av guld-silverlegering

Figur 1-6 Organisationsstruktur för beläggningar av guld-silverlegeringar
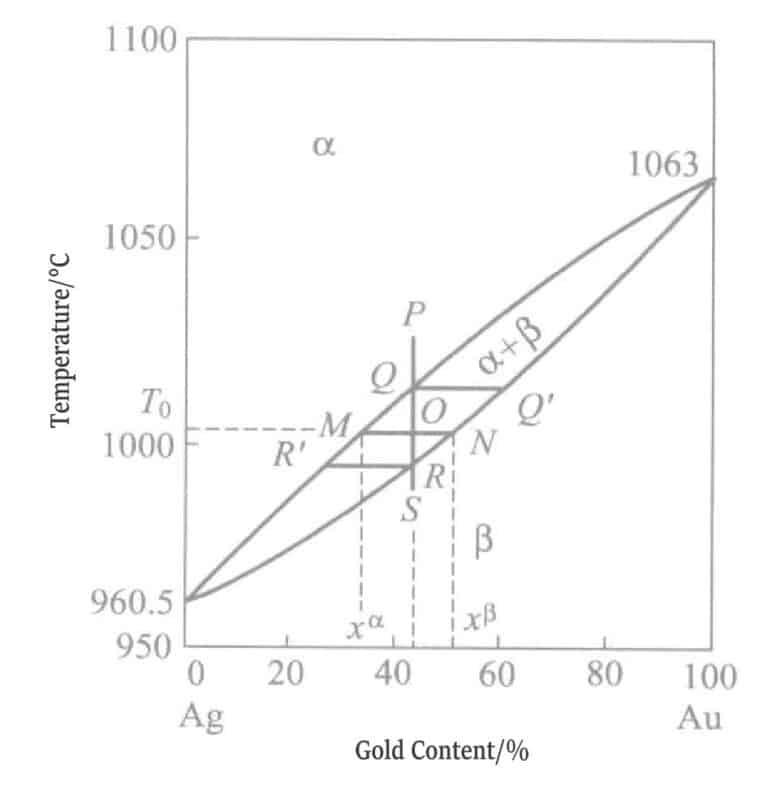
Tillståndet för legeringarna i guld-silverserien visas i figur 1-7, tillhörande en fast lösning med fullförhållande, och både guld och silver har en fcc-struktur (face-centred cubic), med atomradier på båda 1,44 Å (1 Å = 10-10m). Därför deformeras inte gittret.
E. Raub utförde även röntgendiffraktionsstudier på guldpläteringsskikt, vilket bekräftade att guld-silver-legeringarna endast bildar en typ av fast lösning och har utmärkt korrosionsbeständighet.
EA Parker rapporterade att denna serie av guld-silverlegeringar har utmärkt korrosionsbeständighet och konduktivitet, är mycket värdefull för tillverkning av kommunikationsutrustningsdelar, och dess unika guldgröna ton och korrosionsbeständighet gör den lämplig som ett basskikt för tjock guldplätering.
1.2 Förgylld kopparlegering
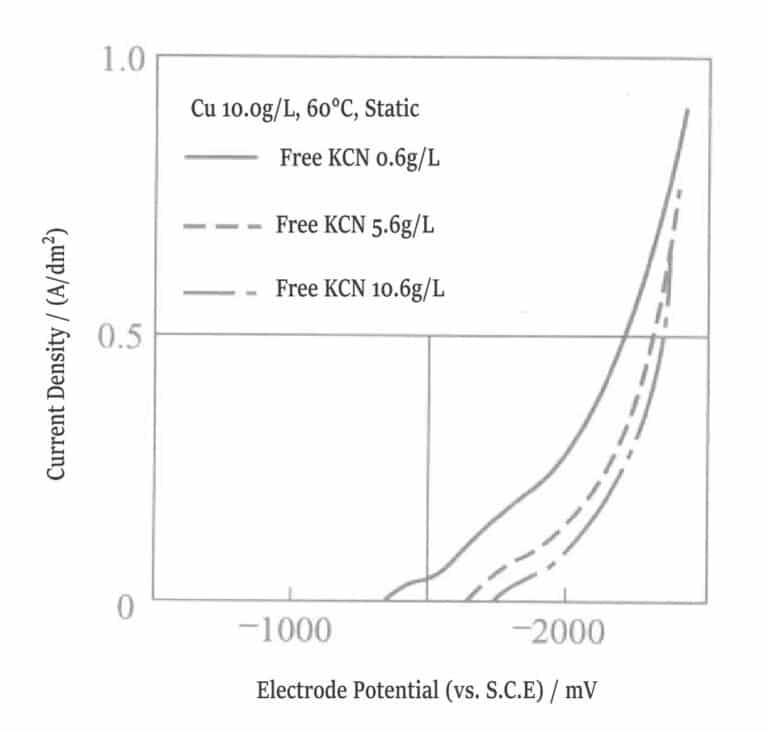
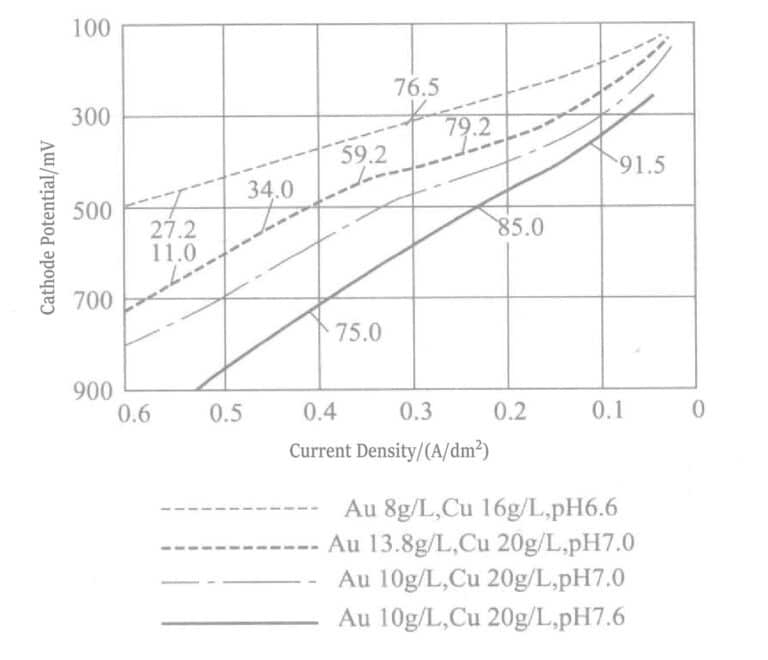
Figur 1-8 Polarisationskurva för kopparpläteringslösning
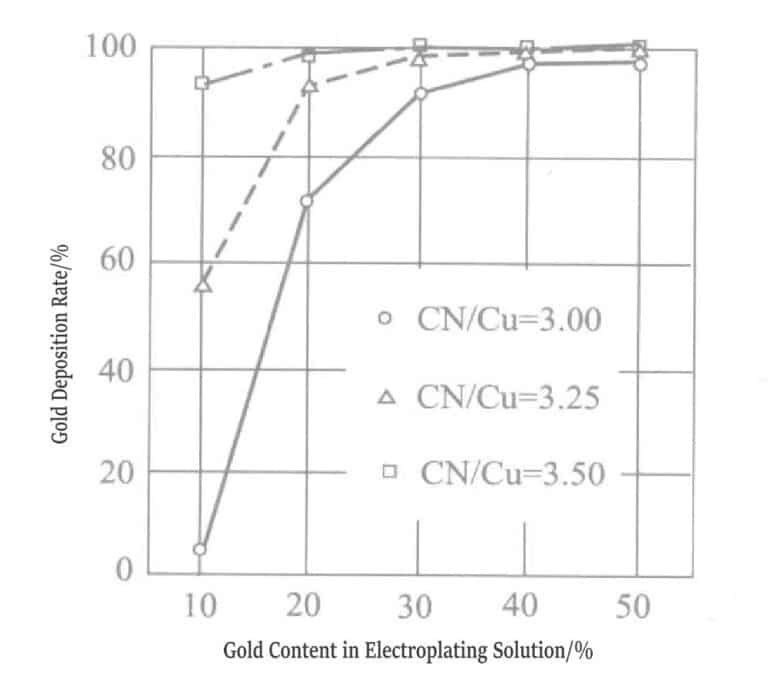
Figur 1-9 Variation av utfällda komponenter i guld-silverlegeringpläteringsskikt
Tabell 1-7 Sammansättning och driftsförhållanden för legeringspläteringslösning
| Sammansättning och driftsförhållanden | Parametrar | Sammansättning och driftsförhållanden | Parametrar |
|---|---|---|---|
| KAu(CN)2/(g/L) | 7.5 ~ 9.0 | Na2SEO4/(g/L) | 0.5 |
| K2Cu(CN)2/(g/L) | 130 | Elektrolyttemperatur/℃ | 60 |
| K2Cd(CN)4/(g/L) | 0.4 ~ 2 | Strömtäthet/(A/dm²2) | 0.75 |
| KCN/(g/L) | 15 |
Att tillsätta nickelsalter till guld-kopparlegeringens pläteringslösning ökar pläteringsskiktets hårdhet. När pläteringslösningens pH-värde är nära surt ökar mängden nickelavsättning. Det kadmiumhaltiga pläteringsskiktet har en färg som liknar roséguld och uppvisar en mycket ädel dekorativ ton.
Det 18K kadmiuminnehållande guldpläteringsskiktet är en fast lösning med hög hårdhet, sträckgräns, draghållfasthet och utmärkt korrosionsbeständighet. Tyvärr, på grund av miljöskyddsproblem, är användningen av metaller som kadmium begränsad av Internationella miljöskyddsorganisationens konventioner och måste strikt kontrolleras inom de tillåtna spårmängderna. Kadmium blir alltmer reglerat och används generellt endast i mycket speciella färgjusteringar, legeringsplätering och elektroformning av 200~300 μm ihåligt guld, där det endast används vid 18K guld-koppar-kadmiumlegeringplätering.
2. Sur guldplätering
Den sura guldpläteringslösningen är stabil inom ett pH-intervall på cirka 3 och kan avsätta nickel eller kobolt som inte genomgår elektrolys i alkaliska guldpläteringslösningar, vilket bildar beläggningar av guld-nickel eller guld-koboltlegeringar. Beläggningens fina kristaller varken deformeras eller lossnar och har inga hålrum, vilket möjliggör långsiktig stabil tillväxt.
Beläggningen som avsätts från sur pläteringslösning har ett ljust utseende och kallas en ljus pläteringslösning. Beläggningen från en sur pläteringslösning har hög hårdhet och är även känd som en hård guldpläteringslösning (tabell 1-8). Olika metaller som tillsätts till organiska syrapläteringslösningar kallas metallvitmedel.
Tabell 1-8 Huvudkomponenter och variationer av sur guldpläteringslösning
| Sammansättning och driftsförhållanden | Referensparametrar | Platinglösningsvillkor |
|---|---|---|
| KAu(CN)2 (g/L) | 4 ~ 6 (beräknat som Au) | Hög koncentration (cirka 16 g/L), lämplig för höghastighetsförgyllning |
| Citronsyrahydrat (g/L) | 50 〜 100 | Tillsätt citronsyra som ligand för borren och som buffert för pläteringslösningen, eller tillsätt andra koboltligander |
| CoSO44 • 7H2O/(g/L) | 0,1 〜 3,0 (beräknat som Co) | Generellt sett, tillsätt kobolt och plätering. Tillsätt svavelsyra (beräknat som Co) vid legering av Au-Ni. |
| pH-värde | 3,5 〜 4,5 | Strömeffektiviteten är hög vid högt pH-värde, men dimma bildas lätt |
| Temperatur/℃ | 30 〜 40 | Hög vätsketemperatur genererar lätt dimma |
Tabell 1-9 Egenskaper hos sur guldpläteringslösning
| Effekt av pH-värde | Egenskaper för pläteringslösning | Tillämpning | |
|---|---|---|---|
| pH 3 | pH 3 ~ 5 | ||
|
① Guld-kobolt, guld-nickellegeringar ② Kobolt och nickel är mycket aktiva och utfälls mer; överpotentialen för väteutveckling är låg, strömeffektiviteten ökar och pläteringseffektiviteten är låg. |
① Eutektisk blank, hård legering; väteutvecklingsöverpotentialen är hög, strömeffektiviteten är låg, pläteringseffektiviteten är hög ② Ingen fri cyanid finns i pläteringslösningen ③ Under utfällningen av guld från KAu(CN)2, en del av KN- bildar HCN, som diffunderar i luften och påverkar miljön |
① Ingen fri cyanid närvarande, under utfällningen av guld från KAu(CN)2, KN- bildar HCN ②Med ökande elektropläteringstid, på grund av ackumulering av K+, ökning av pH i pläteringslösningen ③ Pläteringslösningen är sur; på Pt/Ti-anoden är överpotentialen för vätgasutveckling hög, och organiska karboxylsyror som citronsyra genomgår Kolbe-reaktion för att bilda viskösa polymerer, så en anodplatta med stor yta krävs för att undertrycka denna reaktion. |
① Dekorativ galvanisering ② Förutom att ta bort kobolt och nickel kan indium, zink och järn även tillsättas för färgjustering |
När ingen fri cyanid finns i pläteringslösningen, avsätter kaliumguldcyanid guld och cyanidkomplexjoner (CN – ) bildar HCN, som kommer ut i atmosfären och diffunderar.
I elektropläteringstanken används sällan guldplattor som anoder; generellt används plattor av rostfritt stål eller Pt/Ti-plattor. I sura pläteringslösningar är syreutvecklingsöverpotentialen vid anoden hög, och karboxylsyror som citronsyra tenderar att genomgå Kolbe-reaktioner vid anoden. Metoder som att öka anodarean kan förhindra bildandet av klibbiga polymeravlagringar.
Samavsättningen av nickel och kobolt ökar hårdheten hos det cyanidbaserade hårdförgyllningsskiktet. Efter omlödningslödning vid 260 ℃ ökar kontaktresistansen kraftigt. Tillsats av alifatiska föreningar som etanol till pläteringslösningen kan hämma förändringar i kontaktresistansen efter omlödningslödning och avsevärt öka strömtäthetsintervallet för pläteringslösningen. Till exempel, vid plätering av guld på flexibla kretskort (koppar), kan tillsats av merkaptoföreningar hämma upplösning av kopparrör och stabilt plätera tjockt guld under lång tid.2.1 Plätering av guld-koboltlegering
Sur guldplätering använder vanligtvis organiska syralösningar för guldplätering från citronsyra- och citratserien. Liganden kaliumguldcyanid i den vattenhaltiga organiska syralösningen dissocierar för att producera fri cyanid, vilket gör lösningen till ett elektropläteringsbad med ett pH på cirka 3. Olika komponenter, såsom andra ligander än citronsyra, tillsätts vid behov, inklusive EDTA. pH-justeraren som används är natriumbisulfat. Ledande salter inkluderar kaliumvätefosfat, divätefosfat, ammoniumvätefosfat, natriumpyrofosfat, etc. Buffertar som används inkluderar kaliumsulfat, natriumsulfat, etc. Elektropläteringsförhållanden: guldkoncentration på 1~8 g/L, strömtäthet på 0,3~10 A/dm2, pläteringslösningens temperatur på 25~40 ℃. Generellt sett uppstår inga negativa fenomen, såsom dimning, vid plätering av ett tjockt guldlager. Vitmedlet i pläteringslösningen behöver bara tillsätta en liten mängd övergångsmetaller eller metalloider. Kobolt och nickel är representativa metalliska vitmedel.
R. Duva et al. föreslog guldpläteringslösningen i tabell 1-10 i ett patent och ansökte framgångsrikt om många andra patent för sur guldplätering.
Tabell 1-10 Sammansättning av representativa sura guldpläteringslösningar
| Sammansättning och driftsförhållanden | 1 | 2 |
|---|---|---|
| Citronsyra + Natriumcitrat /(g/L) | 80 | 80 |
| Guld (kaliumguldcyanid) /(g/L) | 8 | 8 |
| Nickel (nickelsulfat) /(g/L) | 3 | |
| Zink (zinkacetat) /(g/L) | 0.5 | |
| Indium (sulfat) /(g/L) | 5 | |
| Kobolt (sulfat) /(g/L) | 3 | |
| pH-värde | 4〜5 | 3〜4 |
| Temperatur /℃ | 21 | 21 |
| Strömtäthet /(A/dm²1) | 1 | 1 |
| K① värde | 23 | 21 |
① Nationell standard GB 11887-89 anger att guldhalten i 1K är 4,166% (”K” är en förkortning av det engelska ordet carat och det tyska ordet karat).
21K = 21×4. 166% = 87. 486% (875‰)
24K guld kallas ofta felaktigt för rent guld eller märks som "1000‰" med en faktisk guldhalt på 99 99%, motsvarande 23,988K (internationella organisationer har förbjudit märkning som "rent guld", "9999 guld" och "24K guld").
Det finns många åsikter om kobolts roll i pläteringslösningar. Eisenmann analyserade innehållet av kalium, kobolt, kol, kväve och andra element i guldpläteringsskiktet och fann att förhållandet mellan dessa element motsvarar förhållandet KCo[Au(CN)2]3 molekyler. Därför drogs slutsatsen att den fungerar som ett vitmedel i pläteringslösningen, snarare än att kobolt ensamt ger vitgörande effekten. I pläteringslösningen bildas den inom Helmholtz-dubbelskiktet och genomgår endast minimal upplösning under typiska pläteringsförhållanden. Efter ligandbildning uppvisar den ett elektrokemiskt beteende som liknar organiska vitmedel och adsorberas katodiskt. Denna övergångsmetall uppvisar vitgörande effekter över ett brett pH-område, vilket överensstämmer med kobolt och andra övergångsmetaller som endast uppvisar vitgörande effekter i sura pläteringslösningar.
Teoretiskt sett måste förhållandet kalium, kobolt, kol och kväve i pläteringsskiktet vara 1:1:6:6, men dessa förhållanden varierar kraftigt. Förhållandet kalium-kobolt varierar från (1,0:0,4) till (1,0:5,5) beroende på pläteringslösningens tillstånd och driftsparametrar; förhållandet kobolt-kol varierar mellan (1:3) till (1:10), medan förhållandet kol-kalium i princip förblir stabilt vid 3:1.
Ovanstående resultat motsäger inte det faktum att KCo[Au(CN)2]3 är det huvudsakliga vitmedlet i guldpläteringslösningen och rapporter om kobolt, CoOOH eller koboltcyanid har också detekterats samtidigt i guldpläteringslösningen. Bildningen av KCo[Au(CN)2]3 kan också förklaras av många egenskaper hos den sura guldpläteringslösningen, såsom att betrakta denna förening endast som en enkel mellanprodukt i elektropläteringsprocessen, med andra reaktioner som representerar vitgöringsprocessen. Sammanfattningsvis tros det att faktorer som reduktion av kalium och kobolt, cyanidligandsalter och bildandet av polymerer bidrar till vitgörandet av guldpläteringsskiktet.
Sammansättningen av representativa blanka, lågspännings- och slitstarka guldpläteringslösningar visas i tabell 1-11. De teoretiska antagandena är ganska förenliga med guldpläteringslösningen i den starka koordinationskraften hos kobolts koordinationsgrupp från liganden KCo[Au(CN)2]3 liganddissociation av koboltjoner, vilket leder till generering av KCo[Au(CN)2]3, genereringen av uppkomsten av vitgörande medels roll. När det tillsätts i form av koboltsalt av EDTA, den totala koboltmängden KCo[Au(CN)2]3 var 6 g/L.
Tabell 1-11 Sammansättning av representativa blanka, lågspännings- och slitstarka guldpläteringslösningar
| Element | Massförhållande/% | Atomförhållande /% | Element | Massförhållande/% | Atomförhållande /% |
|---|---|---|---|---|---|
| K | 0. 26 | 1.3 | Co | 0.24 | 0.80 |
| C | 0.24 | 3.94 | Total | 1.00 | 9.70 |
| N | 0.26 | 3.66 |
Alla guldpläteringselektrolyter innehåller starkt koordinerande cyanidligander (förutom guldsulfitsaltsystemet). Cyanokoboltjonen [Co(CN)6–] är ett av de mest stabila koordinationssaltkomplexen som är kända bland ligander, och cyanidsaltet koordinerat med Co(III) är nästan giftfritt.
Om fri cyanid finns i den sura guldpläteringslösningen kommer HCN att produceras, så koncentrationen av fri cyanid måste vara mycket låg. Om pH-värdet ökar ökar dock koncentrationen av fri cyanid i pläteringslösningen. Vid analys av kobolt i pläteringslösningen är det nödvändigt att skilja mellan "inaktiv kobolt" och "aktiv kobolt", där den förra är Co(III) och den senare Co(II).
Vid ändring av driftsförhållandena för pläteringslösningen bör följande aspekter noteras.
(1) pH har många effekter på pläteringslösningen.
Vid ett högt pH-värde på 5,0 ökar koncentrationen av fri cyanid, vilket främjar bildandet av cyanokobolt(III)-koordinationssalt och ökar lösligheten av KCo[Au(CN)2]3, vilket minskar pläteringsskiktets ljusstyrka. Tillförseln av kobolt i Helmholtz dubbelelektriska lager (Figur 1-3) påverkas av ligandernas koordinationsförmåga, vilken beror på pläteringslösningens pH. Eftersom pläteringslösningens pH kontinuerligt stiger kräver sura pläteringslösningar kontinuerlig tillsats av buffertmedel.
Vid lågt pH urladdas vätejoner företrädesvis, vilket resulterar i lägre strömeffektivitet hos pläteringslösningen.
(2) Pläteringslösningens temperatur: När temperaturen på pläteringslösningen stiger, minskar lösligheten av KCo[Au(CN)2]3 ökar och pläteringsskiktets ljusstyrka minskar.
Temperaturen påverkar också koordinationsstyrkan. När temperaturen i pläteringslösningen ökar kan en ökning av koncentrationerna av guld- och koboltsalter effektivt minska denna effekt.
(3) Höghastighetsplätering: Höghastighetspläteringslösningar kräver regelbundna justeringar. För att förhindra lokal koncentrationsminskning vid katoden (koncentrationspolarisering) bör koncentrationerna av guld och kobolt hållas under den övre gränsen. Av samma anledning bör omrörning utföras med högkoncentrerade lösningar, och jetflödesomrörning används vid högströmstäthetsplätering. Höga temperaturer kan förstärka omrörningseffekten. Huvudkarakteristiken för höghastighetsplätering är hög strömtäthet vid både anod och katod. Övergångsmetallvitmedel kan uppnå optimal prestanda under hög strömtäthet vid båda elektroderna. Följande situationer måste dock beaktas:
① Plateringslösningens pH-värde stiger snabbt.
② Co3+ genereras snabbt.
③ Kobolt(III)cyanidkoordinationssalter bildas lätt.
④ Organiska ligander främjar oxidationen av pläteringslösningen.
Under årens lopp har många pläteringslösningar som innehåller organiska tillsatser utvecklats för att öka strömdensitetsintervallet för pläteringslösningar av kobolt-guld- och nickel-guld-legeringar, vilket uppnår höghastighetsplätering vid lägre koncentrationer.
(4) Nuvarande effektivitet: Strömeffektiviteten är förhållandet (%) mellan den ström som förbrukas i själva guldpläteringsprocessen och den totala ström som används. Andra reduktionsreaktioner förbrukar den återstående strömmen.
Användning av Co3+ + e– =Co2+, ur ett perspektiv av nuvarande förbrukning, kan det förstås att genereringen och adsorptionen av KCo[Au(CN)2]3 ökade polarisationseffekter, vilket resulterar i främjad vätgasurladdning.
Viktiga förhållanden som bidrar till genereringen av KCo[Au(CN)2]3, såsom lågt pH-värde, hög koncentration av fritt Co2+, och låg temperatur hos pläteringslösningen, minskar strömeffektiviteten.
Användning av lämpliga ligander kan reglera den effektiva koboltkoncentrationen och genereringen av KCo[Au(CN)2]3, vilket resulterar i ett blankt pläteringsskikt och optimal strömeffektivitet.
(5) Tillsats av metaller, det vill säga metallvitgörande medel, hindrar genereringen av KCo[Au(CN)2]3Till exempel hindrar bly bildandet av vitmedel genom adsorption, vilket minskar strömeffektiviteten.
(6) Omrörning: Jämfört med pläteringslösningar av andra metaller, på grund av lagret av guldråvaror, pris och andra kostnadsfaktorer, och det faktum att det mesta av strömmen i pläteringsprocessen förbrukas genom elektronöverföring i ledande salter med hög koncentration, använder pläteringslösningar generellt lägsta möjliga koncentration.
Au(CN)2– attraheras inte av katoden vid elektrofores och tillförs Helmholtz-dubbelskiktet (Figur 1-3) genom diffusion; därför är omrörning ett viktigt villkor för att tillföra guldkoordinationssalt och vitmedel till katoden.
Omrörning kan förbättra strömeffektiviteten, men samtidigt kommer det ytterligare att öka strömeffektiviteten i områden med hög strömtäthet, vilket försämrar pläteringsskiktets enhetlighet.
Med utvecklingen av lokal pläteringsteknik har problemet med dålig spridning av pläteringsskiktet gradvis minskat. För närvarande används tillsatser ofta för att utöka strömtäthetsområdet för att förbättra pläteringsuniformiteten.
Copywrite @ Sobling.smycken - Anpassad smyckestillverkare, OEM och ODM smyckesfabrik
2.2 Guld-nickellegeringplätering

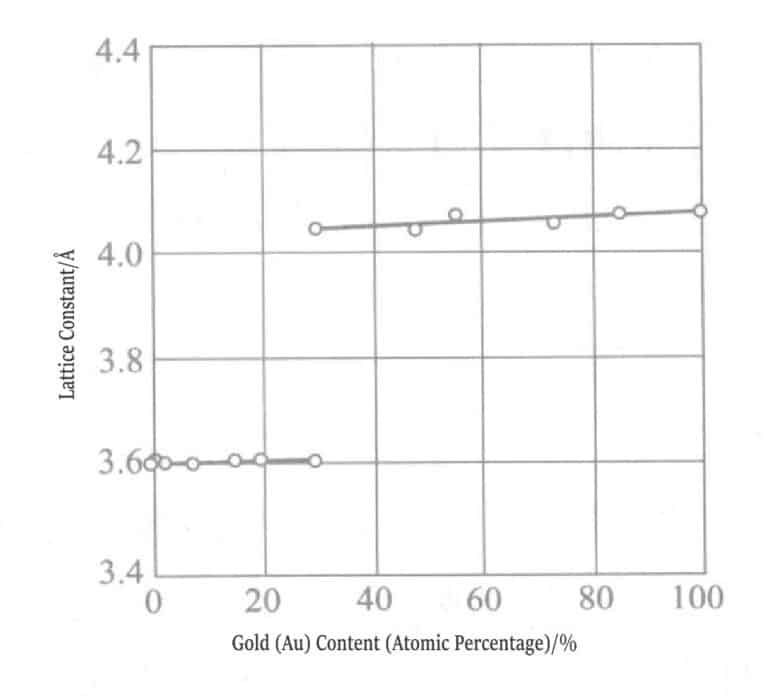
Figur 1-11 Nickelhalt och gitterkonstant för beläggning av guld-nickellegering

Figur 1-12 Nickelhalt och gitterkonstant för beläggning av guld-nickellegering
Sambandet mellan nickelhalt och gitterkonstant i alkaliska och sura pläteringslösningar för elektropläterade skikt av guld-nickellegering mättes. Nickel bildar en fast lösning med guld vid en maximal halt av 5%, och när halten överstiger 5% fälls nickel ut som en enkel blandning.
Jämförande tester utfördes också på pläteringsskikt av guld-nickellegeringar och guld-koboltlegeringar, och resultaten visade att egenskaperna hos de två guldlegeringarna skiljer sig avsevärt. Figurerna 1-13 och 1-14 visar att kol-, kobolt- och nickelhalten i guldlegeringar med samma sammansättning förändras med temperaturen i pläteringslösningen. Kobolt minskar när pläteringslösningens temperatur stiger, och kurvorna för kol och kobolt är parallella, så molförhållandet mellan kol och kobolt är ungefär fixerat vid 4.
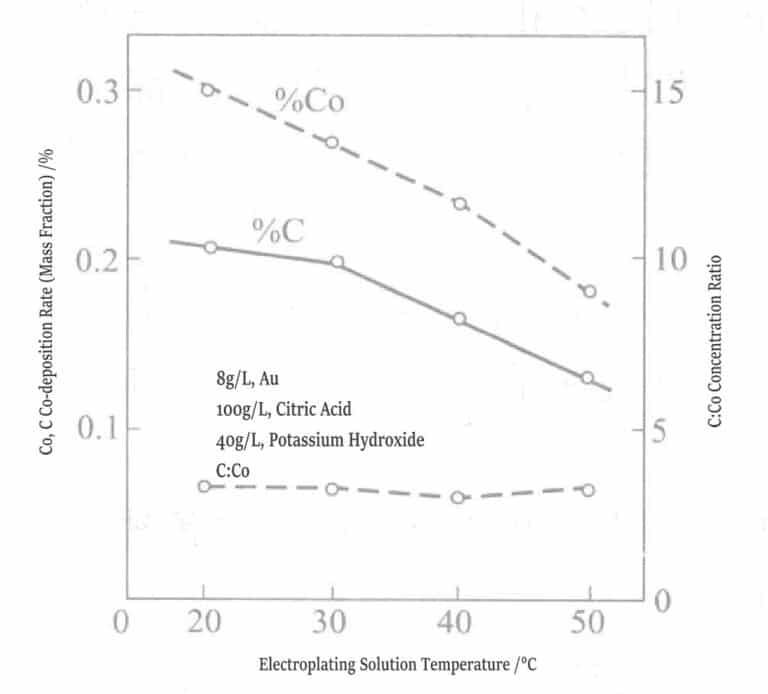
Figur 1-13 Samband mellan pläteringslösningens temperatur och kobolt- och kolavsättningshastighet
(0,5 g/L, pH 3,5, 1 A/dm²)2 )
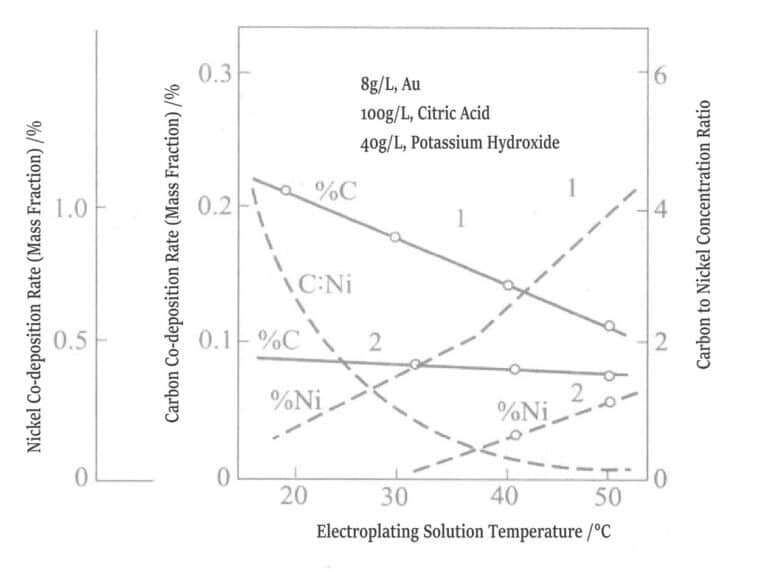
Figur 1-14 Samband mellan pläteringslösningens temperatur och samavsättning av nickel och kol
1–0,5 g/L, pH 3,5, 1 A/dm²2 2–0,5 g/L, Ni, pH 4,5, 1 A/dm2
Figur 1-15 visar effekten av pH på nickel-samavsättning. När pH kontrolleras över 4,5 är samavsättningen av nickel i pläteringsskiktet noll, medan pläteringsskiktet är blankt under pH 4,5.
När andra föroreningar blandas in i förgyllningsskiktet ökar dragspänningen i pläteringsskiktet. Figur 1-16 visar förhållandet mellan temperaturen hos guld-nickellegeringens pläteringslösning och spänningsvärdet i pläteringsskiktet.
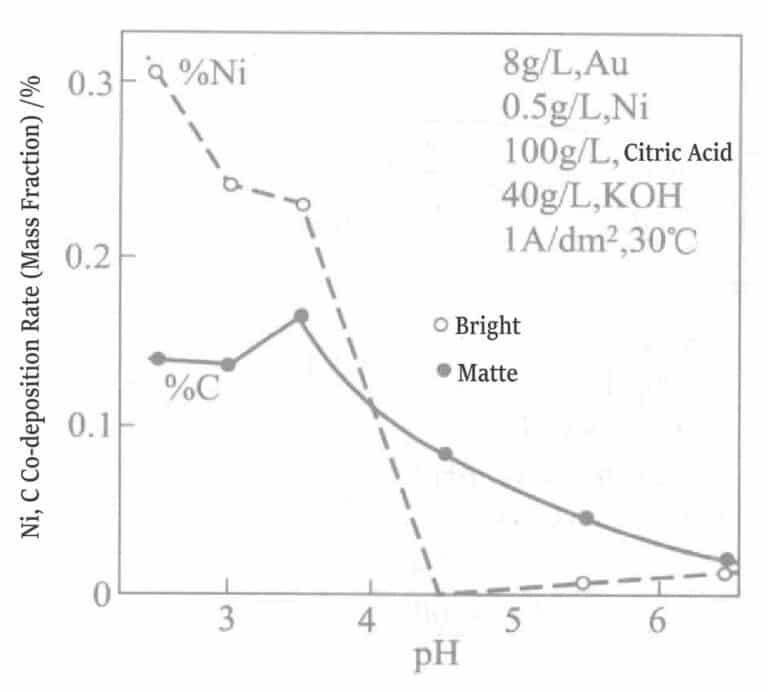
Figur 1-15 Effekt av pH på samavsättningshastigheten för nickel och kol
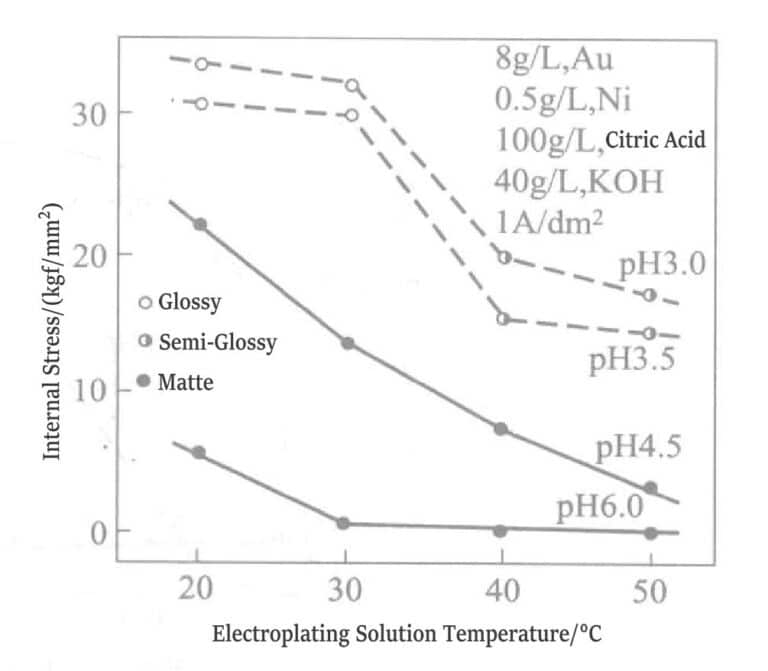
Figur 1-16 Samband mellan internt spänningsvärde, pH och pläteringslösningens temperatur (1 kgf/mm2 =980,665 Pa)
Allt eftersom tjockleken på dessa guldpläteringsskikt ökar, uppstår det lätt sprickor. Draghållfastheten hos guld-nickellegeringens pläteringsskikt visas i figur 1-17. Draghållfastheten påverkas i hög grad av tjockleken, och ett bra pläteringsskikt utan sprickor kan bara pläteras till en tjocklek av 2~3 μm.
När pH-värdet är under 5 kan pläteringslösningen generera ligander. För närvarande är bindningskraften mellan citrat och nickel (Ni2+ ) är starkare än cyanid. Figurerna 1-18 visar de olika förhållandena för pläteringslösningen. Om nickel tillsätts i form av K2Ni(CN)4, kolhalten i pläteringsskiktet ökar kraftigt. Nickelhalten i pläteringsskiktet stiger från en koncentration högre än 0,3 g/L i pläteringslösningen. När nickelkoncentrationen i pläteringslösningen är under 0,3 g/L är pläteringsskiktet matt; över 0,3 g/L blir det blankt. Om nickel tillsätts som nickelsulfat till pläteringslösningen kan en blank effekt uppnås även när nickelkoncentrationen är under 0,3 g/L. Anledningen är att nickel redan har genomgått samavsättning vid en viss koncentrationsnivå.

Figur 1-17 förhållandet mellan guldpläteringens tjocklek och draghållfasthet.
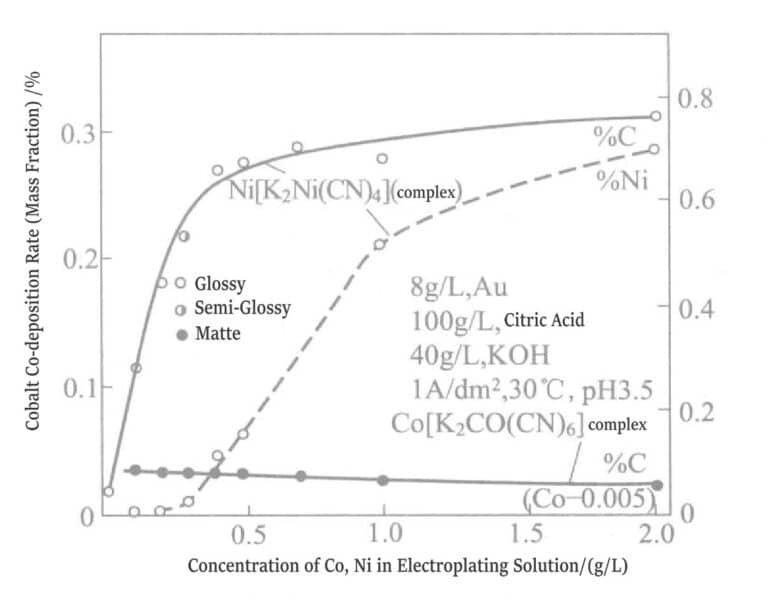
Figur 1-18 Effekt av komplexa joner på koncentrationerna av kobolt och nickel i pläteringslösningen och samavsättningshastigheterna för kobolt, nickel och kol.
(1) Pläteringslösningens sammansättning och driftsförhållanden: Färgen på pläteringsskiktet är nyckeln till dekorativ guldplätering. I sura organiska syrapläteringslösningar är de huvudsakliga komponenterna som används följande: guldsalter, organiska syror, nickelsalter, vitmedel och stressavlastare. Guldsalter, såsom kaliumguldcyanid. Organiska syror inkluderar citronsyra, hydroxibutandisyra och vinsyra. Nickelsalter inkluderar nickelsalter av amidosulfonsyra, citronsyra, svavelsyra, glukonsyra, myrsyra, borsyra, fosforsyra etc. Vitmedel (metaller) inkluderar indium, kobolt, zink, kadmium, antimon etc.
Stresslindrande medel inkluderar magnesium, kalcium, α-bipyridin, natriumalkylbensensulfonat, trietylentetramin, hydrazinsulfat, amidosulfonsyra, etc.
(2) Faktorer som påverkar färgen på guld-nickellegeringarnas pläteringsskikt: Tabell 1-12 listar två typer av pläteringslösningar: pläteringsskiktens färger, pläteringslösningens stabilitet, fysikaliska egenskaper etc.
① Effekt av nickelcitrat: Koncentrationen av nickelcitrat beräknad som nickel i pläteringslösningen varierar med 15 g/L, 20 g/L, 25 g/L, 30 g/L, vilket justerar färgen på guldpläteringsskiktet. När koncentrationen av nickelcitrat är 15 g/L är pläteringsskiktet ljust gyllengult; när den är 20~30 g/L ändras inte färgen. När 1 g/L kobolt tillsätts som koboltsulfat ändras inte färgen, men det gör pläteringsskiktets ljusstyrka. Efter separat ändring av pläteringslösningens temperatur på 35 ℃, 40 ℃, 45 ℃, 55 ℃ ändras pläteringsskiktets färg fortfarande inte.
Tabell 1-12 Sammansättning och driftsförhållanden för två guld-nickelpläteringslösningar
| Sammansättning och driftsförhållanden | Nickelpläteringslösning med citronsyra | Nickelsulfamatpläteringslösning |
|---|---|---|
| Citronsyra /(g/L) | 150 | 150 |
| Kaliumcitrat /(g/L) | 100 | 100 |
| Nickelsulfamat (som Ni)/(g/L) | 15 | |
| Citronsyra nickel (som Ni)/(g/L) | 25 | |
| Koboltsulfat (som Co)/(g/L) | 1 | 0.5 |
| Kaliumguldcyanid (som Au) /(g/L) | 2 | 2 |
| Kaliumcyanid KCN/(g/L) | 1 | 1 |
| pH-värde | 4.2 | 4.2 |
| Temperatur /℃ | 40 | 40 |
② Effekt av nickelaminosulfonat: I pläteringslösningen är koncentrationen av nickelaminosulfonat 5 g/L, 10 g/L, 15 g/L, 20 g/L, beräknat som nickel; med tillsats av 0,5 g/L kobolt (koboltsulfat), 2,5 g/L guld (kaliumguldcyanid) förändras färgen på pläteringsskiktet avsevärt. När nickelkoncentrationen är 5 g/L är pläteringsskiktet ljust gyllengult; när den är 10 g/L är det ljust gyllengult. Jämförs pläteringsskikten som deponerats med två nickelsalter, visar pläteringsskiktet från nickelcitratlösningen en ljus gyllengul färg. Däremot är pläteringsskiktet från nickelaminosulfonatlösningen något svartaktigt.
③ Effekt av nickelsulfat: Efter en viss period producerar nickelsulfatpläteringslösningen nickelhydroxidfällning och är olämplig för användning.
④ Strömeffektivitet: Sambandet mellan strömtäthet och strömeffektivitet för de två pläteringslösningarna visas i figur 1-19. När strömtätheten är 0,5 A/dm²2, 1,0 A/dm²2, 1,5 A/dm2, det finns ingen skillnad mellan citrat-nickelpläteringslösningen och aminosulfonsyra-nickelpläteringslösningen, och båda strömeffektiviteten är 22%~23%.
⑤ Guldavsättningsförhållande: Guldhalten i pläteringsskiktet i citratnickelpläteringslösningen är högre än i pläteringsskiktet i aminosulfonsyranickelpläteringslösningen med 1%~3% (massfraktion) (Figur 1-20).
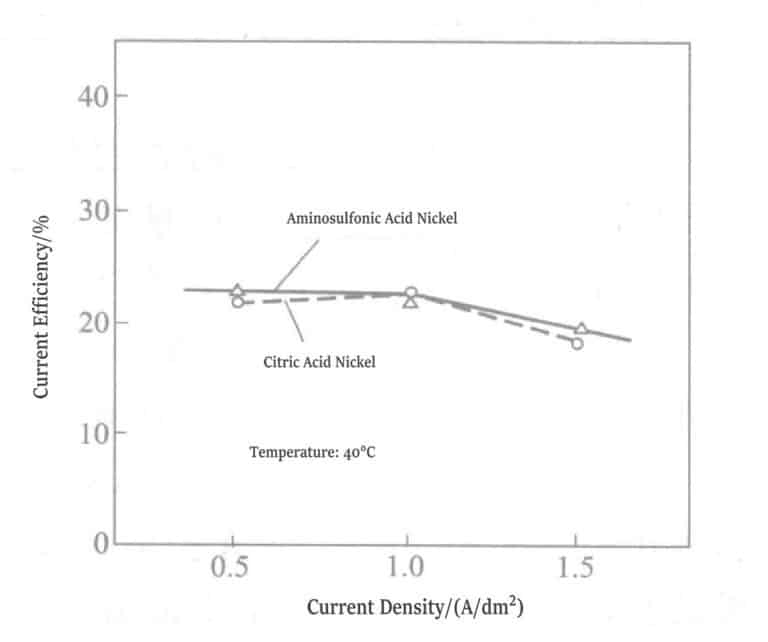
Figur 1-19 Samband mellan strömtäthet och strömeffektivitet
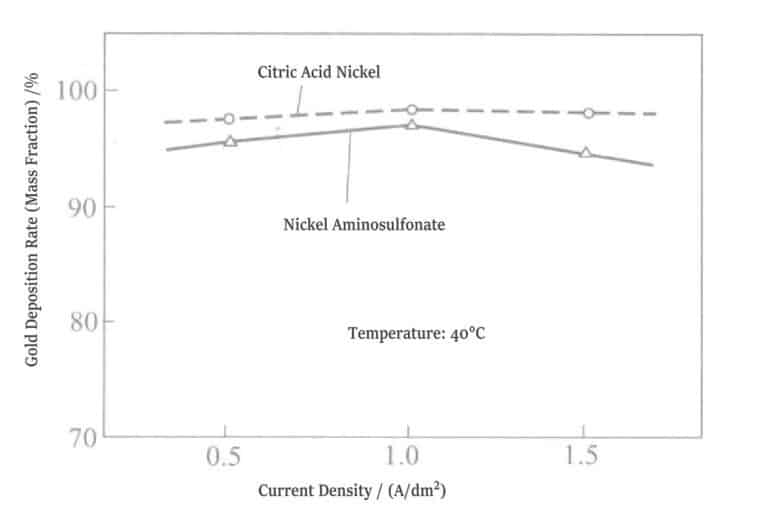
Figur 1-20 Samband mellan nickelsalt och guldavsättningsförhållande
Tabell 1-13 Hårdhet hos tvärsnitt av två typer av pläteringslager
| Typ | Last/gf① | Hårdhet Hv |
|---|---|---|
| Nickelcitratpläteringslösning | 25,50 | 280 ~ 310 |
| Nickelsulfaminsyrapläteringslösning | 25,50 | 210 ~ 240 |
| ① lgf=9.80665×10-3N. | ||
Ytbeskaffenheten hos två pläteringsskikt med en tjocklek på 50 μm är sprickfri, slät och halvblank. När nickelhalten (massfraktionen) i pläteringsskiktet av guld-nickellegering är cirka 5% är hårdheten vanligtvis runt Hv 200. På grund av pläteringsskiktets stora tjocklek genereras inre spänningar, så det uppmätta resultatet överstiger Hv 200. Hårdheten hos pläteringsskiktet från aminosulfonatpläteringslösningen är låg, vilket inte bara påverkas av pläteringsskiktets tjocklek utan också av den spänningsreducerande effekten av själva aminosulfonatet.
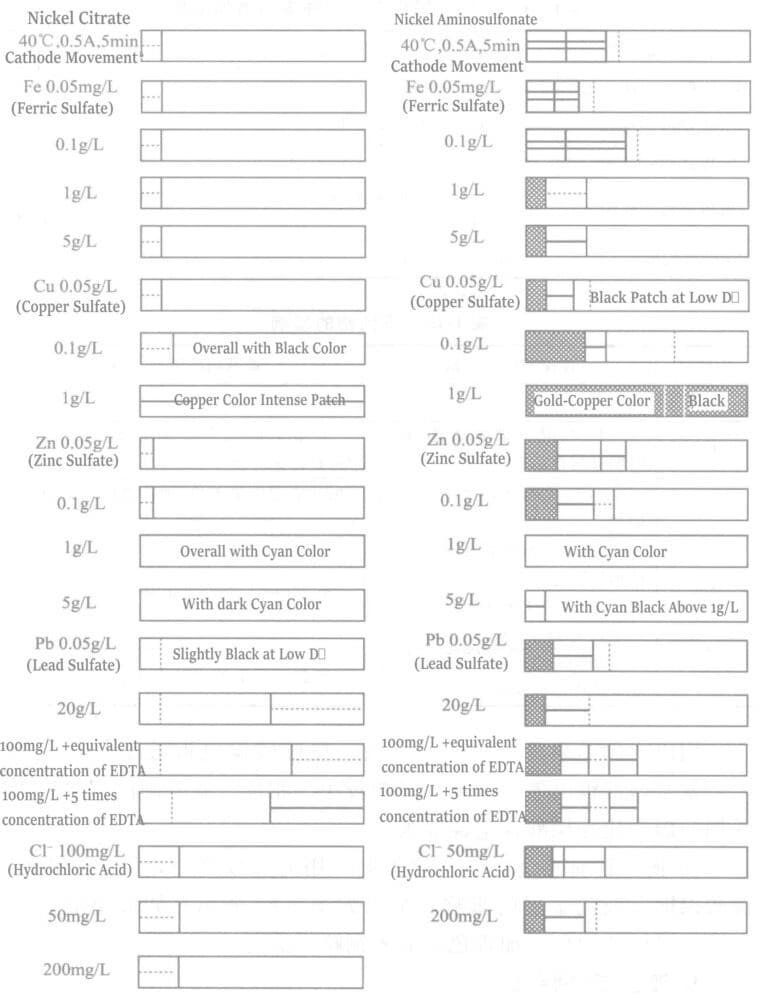
⑦ Effekt av föroreningar: Den experimentella pläteringslösningen och driftsförhållandena för effekten av orena metaller på pläteringsskiktets utseende visas i tabell 1-14. Blank nickel pläterades i en tunnfilmsbatteritesttank för att utföra tunnfilmsbatteriplatttester. Resultaten från de två pläteringslösningarna visas i figur 1-21, och sammanfattningen av resultaten visas i tabell 1-15.
Tabell 1-14 Typer och additionskoncentrationer av orena metallföreningar
| Orena föreningar | Tilläggsbelopp |
|---|---|
| Fe i form av järnsulfat | 0,05 g/L, 0,1 g/L, 1 g/L, 5 g/L |
| Cu i form av kopparsulfat | 0,05 g/L, 0,1 g/L, 1 g/L |
| Zn i form av zinksulfat | 0,05 g/L, 0,1 g/L, 1 g/L, 5 g/L |
| Pb i form av blysulfat | 100 mg+ gånger (molförhållande) EDTA 5 mg/L, 20 mg/L, 100 mg+ ekvivalent mol EDTA |
| Cl i form av saltsyra | 50 mg/L, 200 mg/L |
Tabell 1-15 Effekter av föroreningar
| Föroreningar | Nickelcitratpläteringslösning | Aminosulfonsyra-nickelpläteringslösning |
|---|---|---|
| Fe | Ingen effekt upp till 5 g/L | |
| Cu | Vid 0,1 g/L: Hela ytan ser svart ut; vid 1 g/L: Tydlig kopparaktig utfällning blir uppenbar. | Vid 0,5 g/L: Svartning sker i områden med låg strömtäthet; vid 1 g/L: Ytan blir glanslös. |
| Zn | Upp till 0,1 g/L: Ingen observerbar effekt; Över 0,1 g/L: Blåaktigt gyllengult framträder, med en blåaktig nyans som intensifieras proportionellt med ökande koncentration. | |
| Pb | Runt 5 mg/L: Lätt svärtning manifesteras i områden med låg strömtäthet. Vid cirka 20 mg/L: Disigt utseende uppstår när EDTA-2Na tillförs. | Upp till 20 mg/L: Ingen signifikant påverkan observerad. |
| Cl | Vid 200 mg/L: Marginal disförstärkning begränsad till områden med hög strömtäthet. | Runt 200 mg/L: I princip ingen märkbar påverkan. |
Om man jämför ovanstående resultat för de två typerna av pläteringslösningar, påverkas citronsyra-nickelpläteringslösningen kraftigt av bly. Däremot påverkar bly aminosulfonsyra-nickelpläteringslösningen mindre. Omvänt påverkar koppar aminosulfonsyra-nickelpläteringslösningen mer än citronsyra-nickelpläteringslösningen.
⑧ Koppar och zink påverkar färgen på guldpläteringsskiktet: En glansmätare användes för att mäta effekten av koppar och zink på guldpläteringsskiktet i citronsyra-nickel-guldpläteringslösningen, och resultaten visas i figur 1-22. Om zink blandas i guldpläteringslösningen ökar färgen på pläteringsskiktet i cyan; om koppar blandas i visar det en svagt svart nyans.

2.3 Plätering av guld-nickel-indiumlegering
Tabell 1-16 Sammansättning och driftsförhållanden för guld-nickel-indiumlegeringspläteringslösning
| Sammansättning och driftsförhållanden | Parametrar | Sammansättning och driftsförhållanden | Parametrar |
|---|---|---|---|
| Kaliumguldcyanid/(g/L) | 11.7 | Indium (indiumsulfat)/(g/L) | 5 |
| Citronsyra/(g/L) | 85 | pH-värde | 3.8 |
| Kaliumcitrat /(g/L) | 140 | Elektropläteringslösningens temperatur / ℃ | 38 |
| Nickel (nickelcitrat) / (g/L) | 4.5 | Strömtäthet /(A/dm²2) | 1 |
2,4 pläterad hypoallergen guldlegering
Under lång tid har metaller som nickel och kobolt använts för att justera hårdhet, slitstyrka, korrosionsbeständighet och färg på guldpläteringsskikt. Nickel och kobolt orsakar allergiska reaktioner i människokroppen, och länder i Europa och Amerika har redan infört restriktiva regler för användning av nickel och kobolt. Därför har allergifria guldpläteringslösningar utvecklats.
Att tillsätta järnsalter och titansalter till guldlegeringspläteringslösningar kan uppnå samma ljusa effekt som nickelsalter och koboltsalter. Att tillsätta ledande salter, svaga organiska syror som vinsyra och citronsyra, basmetallsalter, osmiumsalter etc. kan lösa problemet med metallallergi. Dessa guldlegeringspläteringslösningar orsakar inte allergier hos människokroppen. Det är dock svårt att uppnå samma jämnhet som vanliga pläteringslager, och sprickor uppstår när tjockleken överstiger 3 μm. Att justera gula och vita toner är också relativt svårt.
Genom att ersätta nickel och kobolt, som har allergiproblem, med järn, tillsätta indiumledande salter och använda pH-buffertar, har guldlegeringsbeläggningen samma ljusstyrka, vidhäftning och stabilitet, samt samma tjocklek och tonegenskaper som guld-nickel- eller guld-koboltlegeringsbeläggningar.
Guldjonkällan är kaliumguld(I)cyanid eller kaliumguld(III)cyanid. Om koncentrationen är för låg blir strömeffektiviteten låg, pläteringsskiktet ser dimmigt ut och sprickor är benägna att uppstå; om den är för hög ökar viskositeten hos guldpläteringslösningen och guldpläteringsskiktet är benäget att bränna.
Om koncentrationen av järn- eller järnjoner är för låg kan guld inte stabilt avsättas, och guldpläteringsskiktet tenderar att få en dimmig röd färg. Om den är för hög är det lätt att uppstå stora sprickor, vilket gör det svårt att få ett tjockt pläteringsskikt.
Att endast tillsätta järn orsakar överdriven inre spänning i guldpläteringsskiktet, vilket gör att det blir sprickor och förhindrar bildandet av ett slätt legeringspläteringsskikt. Tillsats av indium kan lindra spänningen i guldpläteringsskiktet, vilket möjliggör en tjock guldplätering, och kan också användas för att justera tonen i rent guld.
Om indiumjonkoncentrationen är för låg är det troligt att sprickor uppstår; om den är för hög minskar strömeffektiviteten och guldlagrets avsättning blir instabil.
Oorganiska eller organiska syror kan väljas från fosforsyra, pyrofosforsyra, borsyra, volframsyra, oxalsyra, vinsyra, citronsyra, äppelsyra, mjölksyra, bärnstenssyra, hydroxiättiksyra och glukonsyra.
Om koncentrationen av ledande salter och pH-buffertar är för låg, är konduktiviteten dålig och pH-buffringen otillräcklig, vilket gör att guldpläteringsskiktet avsätts instabilt; om den är för hög ökar viskositeten hos pläteringslösningen, vilket gör sprickbildning mer sannolikt.
pH 1,5 till 7,0. Under 1,5 är strömeffektiviteten låg och avsättningen instabil. Över 7,0 bildas lätt järn- och indiumutfällningar, vilket orsakar onormal avsättning av guldlager.
Att ändra koncentrationen av ovanstående komponenter, tillsätta tensider, andra hjälpämnen etc. kan förbättra det avsatta guldpläteringsskiktets färg, korrosionsbeständighet och slitstyrka. Följande exempel illustrerar detta:
Efter konventionell förbehandling av kopparplattan, använd pläteringslösningen i tabell 1-17, pH 4, temperatur 40 ℃ och strömtäthet 2 A/dm².2 att plätera guldlegeringen.
Tabell 1-17 Lösning för guldlegering och pläteringslager för guldlegering
| Sammansättning och resultat | Kemikalier som används | Nr 1 | Nr 2 | Nr 3 | Nr 4 | Nr 5 | Nr 6 | Nr 7 | Nr 8 |
|---|---|---|---|---|---|---|---|---|---|
| Guld/(g/L) | Kaliumguldcyanid | 5 | 5 | 5 | 5 | 5 | |||
| Kaliumguld(III)cyanid | 5 | 5 | 5 | 5 | |||||
| Järn /(g/L) | Järnjon | 5 | 5 | 5 | 5 | 5 | |||
| Järnjon | 5 | 5 | 5 | 5 | 5 | ||||
| Indium /(g/L) | 5 | 5 | 5 | 5 | 5 (titan) | ||||
| Ledande salt och pH-buffert /(g/L) | Oxalsyra | 100 | 20 | 100 | 10 | 100 | |||
| vinsyra | 100 | 20 | 10 | ||||||
| Citronsyra | 100 | 20 | |||||||
| Borsyra | 20 | ||||||||
| Volframsyra | 20 | 10 | 10 | ||||||
| Fosforsyra | 20 | ||||||||
| Resultat | Ljusstyrka/μm | Över 5 | <1 | <1 | <1 | <1 | |||
| Sedimentationshastighet / (μm/min) | 0. 15 ~ 0. 25 | Kan inte avgöra | |||||||
| Egenskaper | Ljus galvanisering | Sprickor och onormal nederbörd | |||||||
I lösningen med guld-järnlegering kan tillsats av indium, ledande salter och pH-buffertar uppnå ett tjockt pläteringsskikt av ljus guldlegering med en ljusstyrka över 5 μm, och tonen kan justeras från gult till vitt.
Nr 5 ~ Nr 8 är resultatet utan tillsatt indium. Pläteringshastigheten är instabil, pläteringsskiktet producerar många sprickor, ytan är onormal (bränd, dimmig) och det är omöjligt att få ett ljust guldpläteringsskikt över 1 μm. Att använda tallium istället för indium orsakar också sprickor i guldpläteringsskiktet och onormal avsättning. Sådana pläteringslösningar är inte praktiskt användbara. Tabell 1-17 visar egenskaperna hos guldlegeringspläteringslösningar och guldpläteringsskikt.
På grund av nickels och kobolts allergenicitet och försäljnings- eller exportrestriktioner används järn och indium för att ersätta nickel och kobolt i guldlegeringar. Egenskaperna hos pläteringsskikten är desamma, vilket eliminerar de allergiframkallande problemen med metaller som nickel och kobolt. Avsättningen av pläteringsskiktet i pläteringslösningen är stabil och den praktiska färgtonen kan justeras.
3. Neutral guldplätering
Neutral guldplätering kallas mjuk guldplätering eller ren guldplätering, med hög renhet i det avsatta guldskiktet, ingen glans och låg hårdhet, används huvudsakligen för guldpläteringsskikt i IC-kapsling. Pläteringslösningen består av guldsalt, kaliumguldcyanid, buffertmedel med neutralt pH-område såsom citrat, fosfat och blandningar av dessa salter. Dessutom tjänar dessa salter också till att öka pläteringslösningens konduktivitet.
Egenskaper hos neutral pläteringslösning: Tillsats av en spårmängd kristallisationsmodifierare kan förändra pläteringsskiktets utfällningsstruktur, vilket resulterar i en citrongul färgton. När tillsatsen är otillräcklig är utseendet rödbrunt eller bränt; när tillsatsen är för stor sker samutfällning, vilket minskar pläteringsskiktets renhet.
3.1 Dekorativ guldplätering
Tabell 1-18 Sammansättning och driftsförhållanden för guld-kopparlegeringspläteringslösning (I)
| Sammansättning och driftsförhållanden | Parametrar | Sammansättning och driftsförhållanden | Parametrar |
|---|---|---|---|
| Kaliumguldcyanid/(g/L) | 7 | pH-värde | 6. 8〜75 |
| Na2HPO4 (Dinatriumvätefosfat)/(g/L) | 28 | Elektropläteringslösningens temperatur/℃ | 65 〜75 |
| Cu[Na2Cu(CN)3]/(g/L) | 7 | Strömtäthet/(A/dm²2) | 0,5〜1 |
| Fe(järncyanid)/(g/L) | 3 |
Tabell 1-19 Sammansättning och driftsförhållanden för guld-kopparlegeringspläteringslösning (II)
| Sammansättning och driftsförhållanden | Parametrar | Sammansättning och driftsförhållanden | Parametrar |
|---|---|---|---|
| Kaliumguldcyanid/(g/L) | 0. 7~1. 5 | pH-värde | 8.5 |
| Cu(EDTA-kopparsalt)/(g/L) | 8 | Elektropläteringslösningens temperatur/℃ | 53 〜 57 |
| Na2EDTA (fri) (g/L) | 16 | Strömtäthet/(A/dm²2) | 1 ~ 1. 5 |
Dessa är guldlegeringslösningar som vanligtvis används i Europa. Pläteringsskiktet är en helt fast lösning som innehåller en avsevärd mängd koppar men är inte benägen att missfärgas. Salpetersyraluftningstestet visar utmärkt korrosionsbeständighet.
EDTA-pläteringslösningens guld-kopparlegeringsskikt värmebehandlas vid 300~400 ℃ för att erhålla Au-Cu3 intermetallisk förening, som har mycket hög hårdhet. Figur 1-23 visar polarisationskurvan för pläteringslösningen i tabell 1-4.
3.2 Funktionell guldplätering
Tabell 1-20 Sammansättning och driftsförhållanden för neutral guldpläteringslösning med hög renhet
| Sammansättning och driftsförhållanden | Nr 1 | Nr 2 | Nr 3 | Nr 4 | Nr 5 |
|---|---|---|---|---|---|
| Kaliumguldcyanid/(g/L) | 10 〜 31 | 10 〜 20 | 7〜18 | 6 | 8.2 |
| Natriumdivätefosfat/(g/L) | 60 | - | 82 | - | - |
| Kaliumpyrofosfat/(g/L) | - | - | - | - | 150 |
| Citrat/(g/L) | 60 | 60 〜 125 | 50 〜 75 | 90 | - |
| Kaliumcitrat | Kaliumcitrat | Ammoniumcitrat | Lösligt salt av syra | ||
| Natriumtiosulfatpentahydrat/(g/L) | 5 〜 10 | - | - | - | - |
| Trietylfosfat/(g/L) | - | 30 〜 60 | - | - | - |
| Aminotrimetylfosfat/(g/L) | - | - | - | 80 | - |
| Bensylalkohol (massfraktion)/% | - | - | - | - | 0. 05 |
| pH-värde | 5,5 〜 8,0 | 6 〜 8 | 5 ~ 6. 5 | 6.0 | 7 ~ 8 |
| Temperatur /℃ | 60 | 60 | 45 〜 100 | 65 | 60 |
| Strömtäthet /(A/dm²2) | 0,1〜 1,5 | 0. 1 ~ 0. 3 | 0. 1 ~ 0. 4 | 0. 1 ~ 0. 5 | 0. 1 |
4. Sulfitförgyllning
Sedan 1970 har guldplätering med guldsulfitsalter varit praktiskt. Sulfitguld(I)komplexsalter genomgår [Au(SO3)2]3-⇌Au++2SO32- dissociation.
Stabiliteten hos denna typ av komplexjon är mycket lägre än hos cyanidkomplex, med en stabilitetskonstant på cirka 1010, så stabiliteten är 1028 gånger sämre än [Au(CN)2–] .
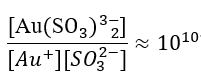
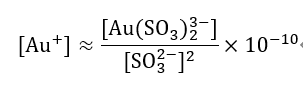
Am är aminogruppen i en alifatisk amin.
Anjonen dissocierar enligt följande formel:
[Au(Am)]2(SO3)2]3- ⇌[Au(Am)2]+ + 2(SO3)2- (1-2)
Och även [Au(Am)]2]+ ⇌Au+ + 02:00 (1-3)
Tabell 1-21 Sammansättning av guldsulfitelektropläteringslösning
| Sammansättning | Parametrar |
|---|---|
| Guld [iminokoordinerat salt av natriumguld(I)sulfit]/(g/L) | 12 |
| Natriumsulfit (fritt)/(g/L) | 50 |
| Natriumcitrat/(g/L) | 50 |
| Natriumtetraborat/(g/L) | 10 |
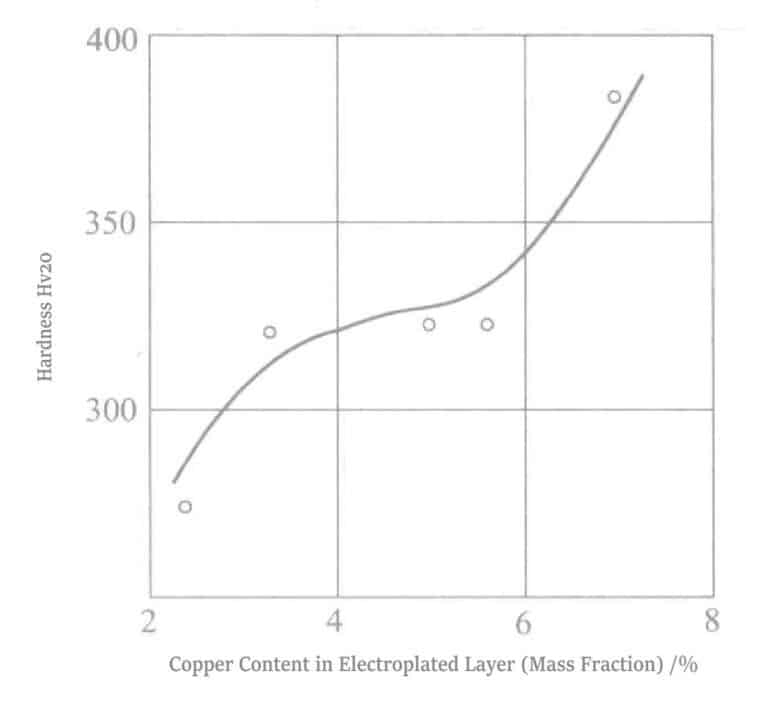
Guldsulfitsalt används vanligtvis för att plätera Au-Pd-Cu ternära guldlegeringar under galvanisering av guldlegeringar. Dess fördelar är: ① pläteringsskiktet ser rosa ut; ② hårdheten når upp till Hv 400; ③ utmärkt slitstyrka; ④ utmärkt korrosionsbeständighet. Nackdelarna är: ① förhållandet mellan legeringsavsättning varierar ojämnt med strömtäthet och temperatur; ② anoden genomgår reduktion och avsättning under långvarig plätering.
Yoshimura et al. använde förhållandena i tabell 1-22, med varierande kopparkoncentration på 0,0021~0,0211 mol/L, pläteringslösningens temperatur på 25℃, 50℃ och strömtäthet på 0,230 A/dm².2 för plätering. Utseende, hårdhet, slitstyrka och andra värden för den avsatta beläggningen visas i tabell 1-23. Jämfört med kornstorleken 337 Å för pläteringsskiktet av guld-palladiumlegering är kornstorleken 161~231 Å för pläteringsskiktet av guld-palladium-kopparlegering mindre, med en pläteringshårdhet på 400 Hv och god slitstyrka. Det finns ett relaterat patent för pläteringsskiktet av guld-palladium-kopparlegering.
Tabell 1-22 Sammansättning av Au-Pd-Cu-legeringselektropläteringslösning Enhet: mol/L
| Sammansättning | Parameter | Sammansättning | Parameter |
|---|---|---|---|
| Au(SO3 )2 3- | 0.0204 | Na2SO3 | 0.1983 |
| Pd(en)2 2+ | 0.0236 | NaAsO2 | 0.0115 |
| EDTA-2Na | 0.2109 | CuSO44 | 0,0021 〜 0,0211 |
Tabell 1-23 Jämförelse av hårdhet och slitstyrka mellan beläggning av Au-Pd-Cu-legering och beläggning av Au-Ni-legering
| Elektropläteringslösningens sammansättning, avsättningsförhållande/% | Hårdhet VHN | Slitstyrka |
|---|---|---|
| Au: Ni | ||
| 92 : 8 | 237 | 20 |
| Au: Pd: Cu | ||
| 87: 3: 10 | 362 | 26 |
| 80: 5: 15 | 437 | 33 |
| 79: 8: 13 | 383 | 28 |
| 75: 9: 16 | 400 | 28 |