لماذا تتعدد ألوان الأحجار الكريمة؟
أسرار تكوين الألوان وطرق قياسها
إن ألوان الأحجار الكريمة غنية ومتنوعة، وتمتلك سحرًا فريدًا لطالما أحبها الناس. تعتمد جودة الأحجار الكريمة إلى حد كبير على لونها. ويُعد لون الأحجار الكريمة مؤشراً مهماً في تقييم الأحجار الكريمة، وتتضمن معظم علاجات تحسين الأحجار الكريمة تغيير لونها أو تحسينه. لذلك، يُعد فهم أسباب تلوين الأحجار الكريمة شرطاً أساسياً حاسماً في معالجة تحسين الأحجار الكريمة. ولا يمكن للمرء تحديد ما إذا كان يمكن تحسين لون الأحجار الكريمة أو لا يمكن تحسين لونها إلا من خلال إتقان كيفية اكتساب الأحجار الكريمة للونها، ومخطط التحسين الذي يجب اعتماده، والخطة التجريبية التي يجب وضعها. هناك خمس نظريات شائعة لتلوين الأحجار الكريمة: نظرية علم المعادن الكلاسيكية، ونظرية المجال البلوري، ونظرية المدار الجزيئي، ونظرية نطاق الطاقة، والتأثيرات البصرية الفيزيائية. وتشكّل هذه النظريات نظريات تلوين الأحجار الكريمة الطبيعية الشائعة، وفيما يلي مقدمة موجزة لنظريات التلوين الخمس هذه.

مخطط تخطيطي للعناصر الثلاثة للون
جدول المحتويات
القسم الأول اللون وقياس لون الأحجار الكريمة
تتسم ألوان الأحجار الكريمة بالثراء والتنوع، ويُعد تحديد أنواع ألوان الأحجار الكريمة أمراً بالغ الأهمية لتقييم قيمتها. كما تؤثر درجات الألوان المختلفة أيضاً على قيمة الأحجار الكريمة؛ ولذلك، فإن تقييم ألوان الأحجار الكريمة المختلفة بدقة هو شرط أساسي لتحديد قيمتها. عند تقييم الأحجار الكريمة الملونة، يكون اللون هو العامل الأكثر أهمية. وبصفة عامة، كلما كان لون الحجر الكريم أكثر جاذبية كلما زادت قيمته. وعادةً ما تكون الألوان الزاهية والغنية والكثيفة أكثر جاذبية من الألوان الداكنة جداً أو الفاتحة جداً. وبالطبع، هناك استثناءات، مثل الألماس، حيث كلما زاد بياض لون الألماس، زادت قيمته.
1. أهمية ألوان الأحجار الكريمة
منذ القدم، أحب الناس منذ القدم الأحجار الكريمة لسحرها الفريد، وخاصةً الألوان الغنية والملونة للأحجار الكريمة، مثل الياقوت الأحمر بلون دم الحمام والزمرد الأخضر الزاهي واليشم، وكلها تترك انطباعاً يدوم طويلاً. ويُعدّ اللون مؤشراً مهماً لتقييم جودة الأحجار الكريمة ويؤدي دوراً حاسماً في تحديد جودتها، وتتجلى أهميته بشكل أساسي في الجوانب الثلاثة التالية
(1) يعد لون معادن الأحجار الكريمة أساسًا مهمًا لتقييم الأحجار الكريمة
لون الحجر الكريم أساسي في تقييمه ويحدد قيمته. على سبيل المثال، في الماس، يمكن أن يؤدي اختلاف درجة واحدة في اللون إلى فرق في السعر يبلغ حوالي 51 تيرابايت 3 تيرابايت. فكلما زاد البياض، زادت درجة بياض الألماس؛ وعلى العكس من ذلك، فإن الألماس الذي يميل لونه إلى اللون الأصفر أو البني تكون درجاته أقل، وتنخفض أسعاره. تتفاوت أسعار الألماس الملون، وتختلف أسعار الألماس الملون باختلاف درجاته. ومع ذلك، وبصفة عامة، يمكن أن تتضاعف أسعار الألماس الملون النادر. تُصنَّف الأحجار الكريمة الملونة الأخرى، مثل الياقوت والياقوت الأزرق والزمرد، أيضاً إلى درجات مختلفة بناءً على اللون، ويمكن أن تتفاوت قيمة الأحجار الكريمة بدرجاتها المختلفة تفاوتاً كبيراً.
(2) غالبًا ما تنطوي المعالجة المثلى للأحجار الكريمة على تحسين لونها
عادةً ما تتضمن طرق المعالجة التحسينية للأحجار الكريمة تغيير أو تحسين لون الأحجار الكريمة، لذلك يمكن الإشارة إلى تحسين الأحجار الكريمة أيضاً باسم تغيير لون الأحجار الكريمة. ومع تحسن لون الأحجار الكريمة، تتغير الشفافية أيضًا وفقًا لذلك. وذلك لأن الشفافية هي خاصية مرتبطة باللون. على سبيل المثال، يظهر الياقوت الأزرق بألوان سوداء معتمة كثيرة للعين المجردة، ولكن يمكن رؤية اللون الأزرق الشفاف عند تقطيعه إلى شرائح رقيقة. وغالباً ما يصاحب التحسن في الشفافية التحسن في اللون. لذلك، لا يمكن التأكد من طرق تحسين لون الحجر الكريم إلا من خلال تحديد سبب لون الحجر الكريم. إن فهم سبب اللون شرط أساسي لدراسة علاجات تحسين الأحجار الكريمة.
(3) توفر دراسة أسباب لون الأحجار الكريمة أساسًا نظريًا للأحجار الكريمة الاصطناعية وتحسين الأحجار الكريمة.
ترجع ألوان الأحجار الكريمة مثل العقيق والمالكيت والأوليفين إلى مكوناتها المتأصلة، ولا يمكن تغيير ألوان هذه الأحجار الكريمة باستخدام طرق المعالجة التقليدية للتحسين. وتعود معظم ألوان الأحجار الكريمة إلى الشوائب الناجمة عن أيونات الشوائب، كما هو الحال في الياقوت والياقوت والزمرد واليشم والعقيق. واستنادًا إلى أسباب لون الأحجار الكريمة، يمكن تغيير محتوى وحالة تكافؤ بعض أيونات الشوائب المسببة للألوان أثناء التحسين، لتغيير لون الحجر الكريم أو تحسينه، وبالتالي تحسين جودة الحجر الكريم المحسّن. لذلك، فإن دراسة أسباب لون الأحجار الكريمة هي الأساس النظري لتحسين الأحجار الكريمة.
2. فيزياء اللون
(1) موجات الألوان والضوء
تحمل الفوتونات طاقة الضوء، وعندما تصل الفوتونات إلى العين البشرية، فإنها تخلق الإحساس بالألوان. اللون هو إدراك العينين والجهاز العصبي للضوء؛ فالاستجابة الناتجة عن الإشارات المتكونة على شبكية العين تحفز القشرة الدماغية. تتكون عملية تكوين إدراك اللون من ثلاثة مكونات رئيسية: مصدر الضوء والجسم والعين البشرية. يؤدي تغيير واحد أو أكثر من هذه العناصر الثلاثة إلى تغيير إدراك اللون. تتفاعل الأحجار الكريمة مع الضوء، وتؤدي ظواهر مثل الانعكاس والانكسار والإرسال والتداخل والحيود التي تحدث على سطح الجوهرة إلى ألوان مختلفة.
إن نطاق الطاقة في طيف الإشعاع الكهرومغناطيسي كبير جدًّا، حيث يتراوح بين فوتونات الموجات الراديوية الطويلة جدًّا وفوتونات الأشعة القصيرة جدًّا، ويتراوح نطاق الطاقة من أقل من جزء من مليار من الإلكترون فولت إلى أكثر من مائة مليون إلكترون فولت.
والضوء المرئي الذي يمكن للعين البشرية أن تقبله وتدركه هو جزء صغير جدًا من الطيف الكهرومغناطيسي، حيث يتراوح نطاق الطول الموجي بين 400-700 نانومتر وطاقة تبلغ حوالي 1.7-3.1eV. إذا كانت ظروف الرصد جيدة بما فيه الكفاية، يمكن تمديد النطاق إلى 380-760 نانومتر (الشكل 3-1). ويشمل الضوء المرئي الألوان التي نراها، وهي الأحمر والبرتقالي والأصفر والأخضر والسماوي والأزرق والأرجواني وألوان أخرى مختلفة. وتنتج الأطوال الموجية المختلفة للضوء المرئي ألوانًا مختلفة؛ فلون الضوء المرئي ذو الطول الموجي الأطول والأقل طاقة هو اللون الأحمر، ويتراوح طوله الموجي بين 647-760 نانومتر، أما الضوء المرئي ذو الطول الموجي الأقصر والأعلى طاقة فهو اللون الأرجواني، ويتراوح طوله الموجي بين 400-425 نانومتر. تقع ألوان الضوء المرئي الأخرى بين 425 و647 نانومتر. الأطوال الموجية لمختلف ألوان الضوء المرئي والألوان المكملة لها موضحة في الجدول 3-1.
الجدول 3-1 الأطوال الموجية لمختلف ألوان الضوء المرئي والألوان المكملة لها
| الطول الموجي/نانومتر | اللون الطيفي | مكمّل |
|---|---|---|
| 400 ~ 425 | أرجواني | أصفر-أخضر |
| 425 ~ 455 | أزرق | أصفر |
| 455 ~ 490 | أخضر-أزرق | برتقالي |
| 490 ~ 500 | أزرق-أخضر | أحمر |
| 500 ~ 560 | أخضر | أرجواني |
| 560 ~ 580 | أصفر-أخضر | أرجواني |
| 580 ~ 595 | أصفر | أزرق |
| 595 ~ 647 | برتقالي | أخضر-أزرق (سماوي) |
| 647 ~ 760 | أحمر | أخضر |
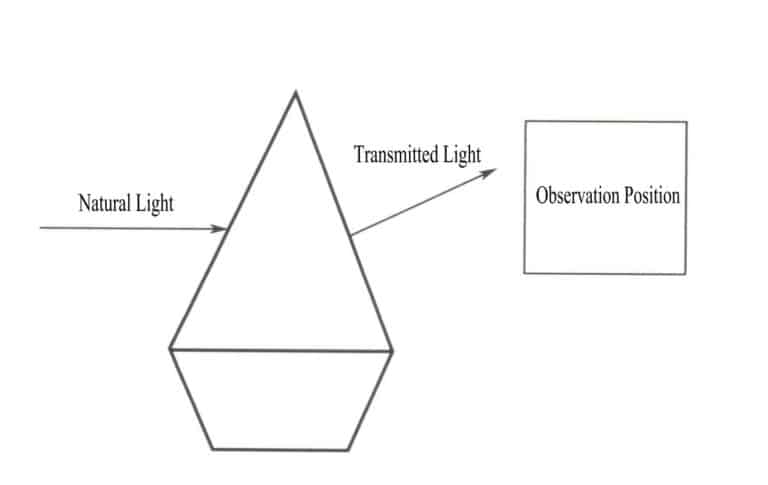
إن جوهر لون الجسم هو نتيجة امتصاص الجسم الانتقائي لأطوال موجية مختلفة من الضوء المرئي. يتمثل جوهر الامتصاص الانتقائي لجسم ما للأطوال الموجية المختلفة للضوء المرئي في امتصاص فوتونات الضوء المرئي ذات الطاقات المختلفة. عندما يسطع الضوء الطبيعي على حجر كريم، يمتص الحجر الكريم جزءاً من الضوء وينقل جزءاً منه أيضاً. واللون الذي يقدّمه الحجر الكريم هو اللون المكمّل للضوء الممتصّ، بما يتوافق مع لون الضوء المنقول (الشكل 3-2). على سبيل المثال، في حالة الياقوت، عندما يمر الضوء الأبيض عبر الياقوت، تكتسب أيونات الكروم الموجودة في الياقوت الطاقة عن طريق امتصاص جميع الفوتونات البنفسجية والخضراء وكذلك معظم الفوتونات الزرقاء، بينما تمر فوتونات الألوان الأخرى، ومعظمها أحمر، عبر الياقوت، مما يجعل الحجر الكريم يبدو أحمر اللون.
الطول الموجي الواحد للضوء لا ينتج عنه اللون الذي يشكله الجسم؛ بل إن إشعاع الجسم عبارة عن مزيج من الفوتونات ذات الطاقات المختلفة، حيث يحدد نطاق الطاقة ذو النسبة الأكبر لون الجسم. ويشكل مزيج منتظم من ألوان مختلفة من الضوء الضوء الضوء الأبيض. وينتج توليد ألوان الأحجار الكريمة من الامتصاص الانتقائي لفوتونات الأطوال الموجية المختلفة للضوء المرئي. عندما يمر الضوء الأبيض من خلال حجر كريم، يكون الضوء الذي يمتصه الحجر الكريم وينقله مزيجاً من الضوء، ويعتمد اللون الذي يقدمه الحجر الكريم على اللون الذي يحتوي على أكبر نسبة من الضوء المنقول. على سبيل المثال، في حالة الياقوت، عندما يضيء الضوء الأبيض على الياقوت، يكون الضوء الذي يمرّ عبره أحمر في الغالب مع كمية صغيرة من اللون الأرجواني المائل إلى الزرقة. وبالتالي، غالباً ما تظهر الياقوتة حمراء مع لون أرجواني مزرق.
(2) أنواع مصادر الضوء وخصائصها
يتسم لون الأحجار الكريمة ببعض الذاتية التي ترتبط بالبيئة المحيطة بالراصد وتتأثر أكثر بمصدر الضوء. يمكن أن تُظهر ملاحظة لون الأحجار الكريمة تحت مصادر الضوء المختلفة اختلافات؛ على سبيل المثال، يظهر حجر ألكسندريت باللون الأخضر في ضوء الشمس ولكنه يظهر باللون الأحمر تحت الضوء المتوهج. وعموماً، يعتبر الناس أن اللون الذي يظهر في ضوء الشمس الطبيعي هو المعيار، ويشار إليه عادةً بالضوء الأبيض.
كانت العمليات الأولية لسوق الأحجار الكريمة تتم في أوقات محددة للحصول على لون دقيق نسبياً للأحجار الكريمة. فعلى سبيل المثال، كانت متاجر الأحجار الكريمة في راتنابورا في سريلانكا تعمل لسنوات عديدة من الساعة 10 صباحًا إلى 12 ظهرًا، حيث أن مصدر الضوء خلال هذا الوقت هو الأقرب إلى الضوء الأبيض. إن ضوء الشمس وضوء النهار ليسا مصدرين ضوئيين متساويين في الخواص الإشعاعية، ويمكن أن تكون الاختلافات النسبية في كميات الإشعاع النسبية في الأطوال الموجية المختلفة بين مصادر الضوء المختلفة كبيرة جداً بسبب اختلاف ظروف المراقبة. ويسرد الشكل 3-3 منحنيات توزيع الطاقة لخمسة مصادر ضوئية شائعة، والاختلافات في الطاقة بين هذه المصادر الضوئية كبيرة جداً.
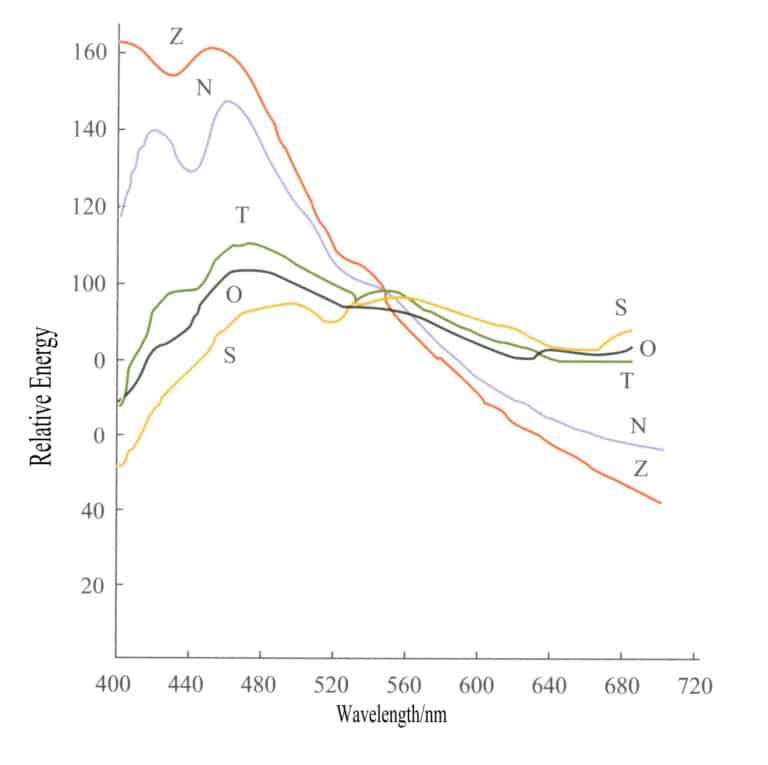
S - ضوء الشمس المباشر؛ O - إضاءة ضوء السماء الملبدة بالغيوم على المستوى الأفقي؛ T - إضاءة ضوء الشمس والسماء الصافية على المستوى الأفقي؛ N - الضوء الصادر من السماء الشمالية الصافية؛ Z - ضوء الزينيوم;
غالبًا ما يتم التعبير عن الخصائص اللونية لضوء الشمس المباشر من حيث درجة حرارة اللون (تقاس بوحدة K). تشير درجة حرارة اللون نفسها إلى الألوان المتشابهة لمصادر الضوء. درجات حرارة الألوان المعترف بها حاليًا في ضوء النهار هي D6500 كلفن و D5500 كلفن و D7500 كلفن. يتم تعيين ثلاثة مصابيح دوليًا كمصادر إضاءة قياسية لأعمال قياس الألوان. SA يمثل متوسط الإضاءة الاصطناعية لمصباح تنجستن متوهج بدرجة حرارة لونية 2854 كلفن؛ حيث تبلغ درجة حرارة اللون 2854 كلفن؛B يمثل ضوء الشمس المتوسط، بدرجة حرارة لونية 4900 كلفن; SC يمثل متوسط ضوء النهار، بدرجة حرارة لونية 6700 كلفن. في اختبار الأحجار الكريمة، يُستخدم مصدر ضوء Sc كمصدر إضاءة قياسي.
(3) حساسية للضوء وتأثيرات الألوان
تُعتبر ملاحظة ألوان الأحجار الكريمة ذاتية؛ فبالإضافة إلى الظروف الموضوعية، يرتبط لون الأحجار الكريمة أيضاً بالإدراك الحسي للمراقب. وتحت نفس مصدر الضوء، تختلف حساسية العين البشرية للألوان المختلفة باختلاف مصدر الضوء، كما تختلف حساسية الأشخاص المختلفين للألوان. إن ملاحظة اللون أمر ذاتي؛ ولتحقيق الموضوعية قدر الإمكان، يجب توصيف الألوان والتعبير عنها بموضوعية نسبياً.
① التأثير الاستقبالي الضوئي:
في ظل الظروف العادية، يتراوح نطاق الطول الموجي لمصادر الضوء المرئي الذي يمكن للعين البشرية ملاحظته في الظروف العادية بين 400-700 نانومتر. يمكن توسيع نطاق الحساسية من خلال تحسين ظروف المراقبة إلى 380-780 نانومتر. للعين البشرية حساسيات مختلفة للموجات الضوئية ذات الأطوال الموجية المختلفة. بالنسبة للرؤية النهارية، تكون العين أكثر حساسية للضوء الأخضر بطول موجي 555 نانومتر، بينما يتحول الطول الموجي الأكثر حساسية للرؤية في الشفق إلى 507 نانومتر. تم تصميم إشارات المرور على الطريق بناءً على الألوان التي تكون العين البشرية أكثر حساسية لها.
② الإحساس بالألوان:
اللون هو الإحساس الناتج عن المكونات الطيفية المختلفة لطاقة الإشعاع ضمن نطاق الضوء المرئي. يمكن لرؤية الشخص العادي تمييز أكثر من 150 درجة من الألوان الطيفية النقية. وعلى الرغم من وجود تطابق واحد لواحد بين موجات الضوء والألوان، إلا أن التطابق بين الألوان وموجات الضوء ليس وحيدًا؛ فغالبًا ما يمكن تشكيل لون واحد من الضوء من خلال الجمع بين لونين أو أكثر من ألوان الضوء الأخرى. والألوان الثلاثة الأساسية المستقلة هي الأحمر والأخضر والأزرق، والمعروفة باسم الألوان الأساسية. تتشكل الألوان الأخرى عن طريق مزج لونين أو أكثر من الألوان الأساسية بنسب مختلفة، والعين البشرية حساسة جدًا للألوان، وقادرة على تمييز العديد من الألوان المختلفة.
3. ثلاثة عناصر تمثل اللون
وينتج اللون من الامتصاص الانتقائي للضوء بواسطة الأحجار الكريمة، وتُظهر الأحجار الكريمة المختلفة ألواناً مختلفة. تشير نظرية الألوان الحالية إلى أن خصائص الألوان تعتمد على السطوع والتدرج والتشبع (الشكل 3-4). يمكن تحديد أنواع ألوان الأحجار الكريمة من خلال وصف العناصر الثلاثة للألوان المختلفة.

(1) السطوع
السطوع هو درجة السطوع التي يسببها الضوء المؤثر على العين البشرية، ويشير إلى درجة الألوان الفاتحة والداكنة، ويمكن أن يطلق عليه أيضاً اسم الإنارة. ويعتمد السطوع إلى حد كبير على إدراك العين لمستويات الضوء والظلام لمصدر الضوء وسطح الجسم، ويتحدد ذلك بشكل أساسي من خلال شدة الضوء. يعتمد السطوع على مستوى إضاءة الجسم وانعكاسية سطح الجسم.
يمكن فهم السطوع على أنه سطوع لون ما؛ فالألوان المختلفة لها مستويات سطوع مختلفة، وأي لون يُظهر اختلافات في الضوء والظلام. للسطوع خاصيتان: يمكن أن يُظهر نفس الجسم تغيرات في السطوع بسبب اختلاف الإضاءة، كما يمكن أن يكون للأضواء الملونة المختلفة بنفس الشدة مستويات سطوع مختلفة.
في حالة عدم وجود لون، يكون اللون ذو السطوع الأعلى هو الأبيض، واللون ذو السطوع الأقل هو الأسود، مع وجود تدرج رمادي بين الفاتح والداكن. في اللون، أي درجة نقاء لها خصائص سطوع خاصة بها. على سبيل المثال، اللون الأصفر هو الأعلى سطوعًا، بينما اللون الأرجواني هو الأقل سطوعًا. أما الأخضر والأحمر والأزرق والأزرق والبرتقالي فلها مستويات سطوع متشابهة، وهي تمثل درجة سطوع متوسطة. بالإضافة إلى ذلك، داخل نفس درجة اللون، هناك اختلافات في السطوع من الفاتح إلى الداكن، مثل الأخضر الفاتح والأخضر الباهت والأخضر الزمردي في الطيف الأخضر.
(2) هوى
يشير التدرج اللوني إلى الاختلافات بين الألوان المختلفة وهو أبرز خصائص اللون. يتم تحديد تدرج الألوان من خلال المكونات الطيفية للضوء التي تمر عبر جسم ما وتصل إلى عين الإنسان بعد سقوطها عليه، وذلك اعتمادًا على الطول الموجي للضوء المنقول. يتم تحديد تدرج لون جسم ما من خلال طيف مصدر الضوء الساقط والضوء المنعكس أو المنقول من الجسم نفسه.
يشير ما يسمى بالتدرج اللوني إلى الاسم الذي يمكن أن يمثل بشكل أكثر دقة فئة لونية معينة، مثل الأحمر الوردي والبرتقالي الأصفر والأصفر الليموني والأزرق الكوبالت والأحمر الأرجواني والأخضر الزمردي وما إلى ذلك. من من منظور علم البصريات الفيزيائي، يتم تحديد درجات الألوان المختلفة من خلال المكونات الطيفية للضوء الذي يدخل العين البشرية. بالنسبة للضوء أحادي اللون، تعتمد أنواع التدرجات اللونية بشكل كامل على الطول الموجي لذلك الضوء؛ أما بالنسبة للضوء المختلط اللون، فيعتمد على الكميات النسبية لمختلف الأطوال الموجية للضوء. يتم تحديد لون جسم ما من خلال المكونات الطيفية لمصدر الضوء وخصائص الضوء المنعكس (أو المنقول) من سطح الجسم. ويرتبط ذلك بالطول الموجي للضوء. على سبيل المثال، اللون الذي يبلغ طوله الموجي السائد 470 نانومتر يسمى أزرق بطول موجي 470 نانومتر، وهو ما يُعرف عادةً باللون الأزرق للصفير.
(3) التشبع
يشير تشبع اللون إلى درجة نقاء اللون وحيويته، مما يشير إلى نسبة المكونات اللونية الموجودة في اللون. وكلما زادت نسبة المكونات اللونية زادت نسبة نقاء اللون، وكلما قلت نسبة المكونات اللونية قلت نسبة نقاء اللون. يتغير التشبع عند مزج لون ما مع الأسود أو الأبيض أو ألوان أخرى. عندما تصل نسبة اللون الممزوج إلى مستوى كبير، يفقد اللون الأصلي تألقه الأصلي للعين، ويصبح اللون المرئي هو لون اللون الممزوج. بالطبع، هذا لا يعني بالطبع أن اللون الأصلي لم يعد موجودًا، بل يعني أن اللون الأصلي قد تم امتصاصه بسبب الألوان الأخرى الكثيرة الممزوجة به، مما يجعله غير ملحوظ للعين البشرية.
وتتمتع الأضواء أحادية اللون في الطيف المرئي بأعلى تشبع وهي الأكثر حيوية. عادةً ما يُعتبر الضوء الأحادي اللون 100/100 = 1، وكلما خفت اللون، تنخفض القيمة تدريجيًا، حيث يكون تشبع اللون الأبيض النقي صفرًا. إذا أخذنا الحبر الأزرق النقي كمثال، فإن تشبع الحبر الأزرق النقي يساوي 1، وعندما يتلاشى تدريجياً إلى عديم اللون تماماً، يصبح التشبع صفراً.
4. قياس لون الأحجار الكريمة
يُطلق على النظام الذي يمثل اللون كمياً اسم نظام الألوان. هناك نوعان شائعان من أنظمة الألوان: أحدهما نظام ألوان يعتمد على عينات لونية قياسية للمقارنة، والآخر هو مجموعة من الأنظمة اللونية القياسية التي يتم قياسها باستخدام أدوات قياس الألوان الحديثة.
(1) نظام الألوان لعينات الألوان القياسية
يتكون نظام الألوان هذا من "بطاقات ألوان" مختلفة مصنوعة من الورق وهي عبارة عن عينات ألوان قياسية مجمعة في كتاب. تتم مقارنتها مع عينات من الأحجار الكريمة لاختيار "بطاقة الألوان" التي تطابق لون الحجر الكريم.
① نظام ألوان مونسيل
نظام ألوان مونسيل هو أحد أقدم أنظمة تمثيل الألوان وأكثرها كلاسيكية. ولا تزال بعض المنظمات تستخدمه حتى اليوم. تم تأسيسه في عام 1905 على يد المربي الأمريكي ومنظّر الألوان ألبرت مونسيل الذي سُمي مباشرة باسمه. وهي طريقة لتمثيل الألوان من خلال نموذج الألوان الصلبة. يتضمن "أطلس ألوان مونسيل"، الذي نشرته الجمعية البصرية الأمريكية (OSA)، إصدارات لامعة وغير لامعة.
يتضمن الإصدار اللامع 1,450 عينة لونية مصحوبة بمجموعة من 37 عينة لونية؛ بينما يتضمن الإصدار غير اللامع 1,150 عينة لونية و32 عينة لونية.
في أطلس مونسيل، يتم تمثيل كل لون بمجموعة من الرموز. توفر الرموز مؤشرات متساوية البُعد للعناصر الثلاثة لتمثيل الألوان: التدرج اللوني والقيمة واللون، ممثلة بـ HV/C = قيمة التدرج اللوني/اللونية.
تنقسم درجات الألوان إلى خمس نغمات أساسية: الأحمر (R)، والأصفر-الأحمر (YR)، والأصفر (Y)، والأخضر-الأصفر (GY)، والأخضر (G)، والأزرق-الأخضر (BG)، والأزرق (B)، والأرجواني-الأزرق (PB)، والأرجواني (P)، والأحمر-الأرجواني (RP)، بالإضافة إلى خمس درجات لونية وسيطة. كما تنقسم كل درجة لونية إلى عشرة مستويات (من 1 إلى 10)، والمستوى الخامس هو اللون الوسيط لتلك الدرجة اللونية (الشكل 3-5).
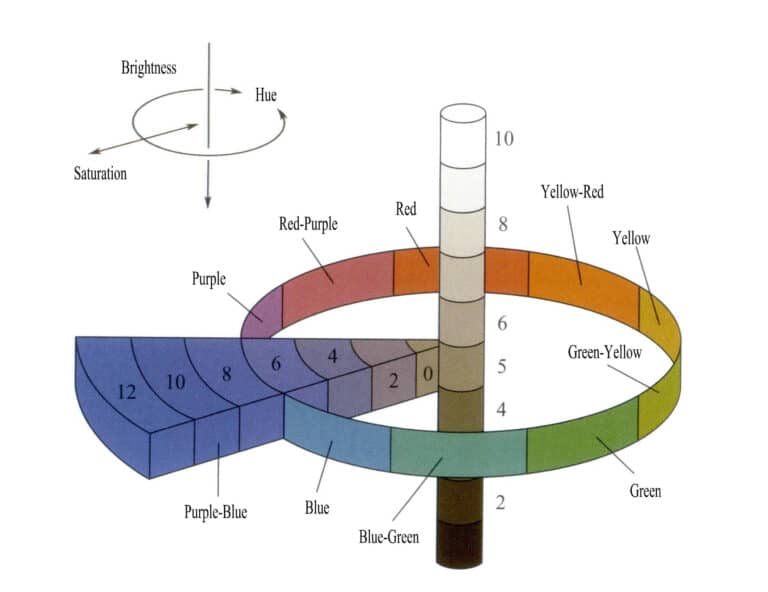
تنقسم القيمة إلى 11 مستوى، حيث تشير القيم الأعلى إلى إضاءة أعلى؛ القيمة الدنيا هي 0 (أسود)، والقيمة القصوى هي 10 (أبيض). ينقسم الكروما إلى 12 مستوى. يتضمن أطلس الألوان بأكمله 40 نوعًا من عينات تدرج الألوان. على سبيل المثال، يمثل اللون 5GY 8/7 لونًا أصفر-أخضر بقيمة 8 وتشبع 7. اصطلاح التسمية لسلسلة الألوان غير اللونية (الأسود والأبيض والرمادي) هو NV/= قيمة إضاءة محايدة؛ على سبيل المثال، يشير اللون المسمى N5/ إلى لون رمادي بقيمة إضاءة 5.
نظام الألوان DIN 6164 DIN 6164
يُعدّ دليل DIN 6164 الألماني أيضاً نظام ألوان مهم. يستخدم العديد من علماء الأحجار الكريمة في أوروبا والمملكة المتحدة هذا النظام. تم تطوير نظام الألوان هذا استناداً إلى نظام مونسيل.
تحتوي بطاقة الألوان DIN 6164 على 24 لونًا، مع تمييز ظهر كل لون بالترميز اللوني المقابل لـ Munsell. يتم التمثيل بتنسيق تدرج اللون: التشبع: الإضاءة. على سبيل المثال، 6:6:2 يمثل تدرج اللون 6 (أحمر)، والتشبع 6 (زاهٍ)، والإضاءة 2 (فاتح) من بطاقة الألوان القياسية.
③ نظام الألوان ISCC-NBS
تأسس مجلس الألوان المشترك بين المجتمعات (ISCC) في عام 1931 كجمعية ألوان محلية في الولايات المتحدة، ويهدف نظام الألوان الخاص به إلى تطوير نظام تسمية الألوان. وهو يجمع 18 تدرجًا لونيًا في نفس مواضع التدرج اللوني والإضاءة في Munsell وDIN 6164.
يحتوي النظام المعياري الوطني الأمريكي ISCC-NBS (المكتب الوطني للمعايير) على عدد قليل جدًا من عينات الألوان في النظام المعياري الوطني الأمريكي ولكنه جمع بعض العينات غير الشائعة. ومن الناحية الهيكلية، فإنه يختلف أيضًا عن نظام Munsell، حيث لا يتم ترتيب الألوان وفقًا لمقاييس متساوية البعد الإدراكي. أهم مساهمة لنظام ISCC-NBS في علم الألوان هو أنه يحدد أسماء الألوان.
④ معيار الألوان OSA
أعدت OSA (الجمعية البصرية الأمريكية) مجموعة عملية من بطاقات الألوان اللامعة المصنوعة من الأكريليك تتضمن 558 لونًا، منها 424 لونًا تشكل مجموعة تعرف باسم معيار الألوان OSA. ويتمثل عيب معيار ألوان OSA في أن بطاقات الألوان مصنوعة من الورق أو البلاستيك، الذي يختلف في الملمس عن الأحجار الكريمة، كما أن لمعان سطح بطاقات الألوان يختلف عن الضوء الذي تعكسه الأحجار الكريمة ذات الأوجه، مما يتطلب استخدامًا دقيقًا. وبسبب البهتان، فإن معظم البطاقات الملونة لها فترة استخدام تتراوح من 4 إلى 5 سنوات.
(2) الإحداثيات اللونية والمخطط اللوني
① نظام فضاء الألوان CIE-XYZ لعام 1931
يعتمد نظام مساحة الألوان هذا على نظام RGB ويستخدم طرقًا رياضية لتحديد ثلاثة ألوان أساسية مثالية لتحل محل الألوان الأساسية الفعلية. وباستخدام الألوان الأساسية الافتراضية كمحاور، فإنه يعرض أطوال موجية مختلفة للضوء المرئي. وتسمى قيم الألوان الأساسية بقيم ثلاثية الألوان. يتطلب هذا النظام أن تكون قيم التريستيمولوس الثلاثية غير سالبة وأن تساوي y التدفق الضوئي. وباستخدام المحور x كمحور أفقي والمحور y كمحور رأسي، فإنه يشكل إحداثيات لونية بإسقاط قيم الإحداثيات اللونية لكل ضوء أحادي اللون للحصول على المخطط اللوني. والشكل 3-6 هو المخطط اللوني القياسي لنظام (XYZ) الذي تم تأسيسه دولياً في عام 1931.
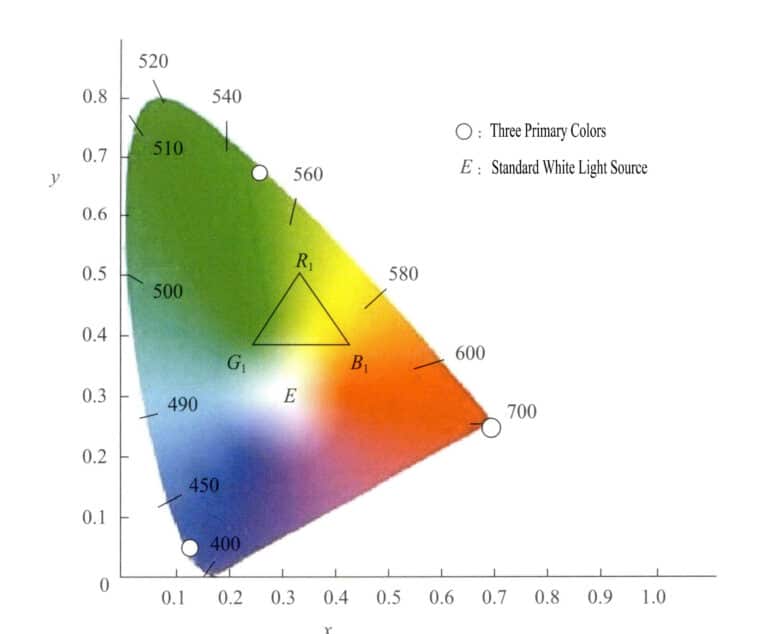
يتميز المخطط اللوني بالخصائص التالية:
- تكون قيم التريستيمولوس الثلاثية للألوان الأساسية لهذا النظام افتراضية.
- تقع جميع النقاط التي تمثل الألوان الطيفية على منحنى على شكل لسان يسمى اللون الطيفي. وبربط طرفي المنحنى بخطوط مستقيمة، تقع جميع الألوان الفعلية داخل المنطقة التي يحيط بها المنحنى على شكل لسان والخطوط المستقيمة.
- تمثل القيمة الإحداثية للنقطة E عند x=0.333، y=0.333 اللون الأبيض النظري. تحتوي مصادر الضوء الأبيض المختلفة على مكونات طيفية مختلفة قليلاً. ينقسم الضوء الأبيض الشائع الاستخدام إلى SA, SB, SC, SEوما إلى ذلك.
- تكون الإحداثيات اللونية للألوان أعلى في التشبع كلما كانت أقرب إلى مسار اللون الطيفي. النقاط الموجودة على مسار اللون الطيفي لها أعلى درجة تشبع، والنقطة البيضاء لها أقل درجة تشبع. يحتوي الخط المرسوم من النقطة البيضاء إلى الإحداثيات اللونية للون ما، والممتد ليتقاطع مع مسار اللون الطيفي، على نقاط على طول هذا الخط تشترك في نفس درجة اللون.
- يمكن استخدام طريقة بيانية لاشتقاق اللون المركب لأي لونين. من خلال إدخال الإحداثيات اللونية للونين في المخطط اللوني، يجب أن يقع اللون المركب على الخط الواصل بين نقطتي إحداثيات اللونين. وترتبط المسافة المسقطة لنقطتي اللونين بكثافة اللونين، والتي يحددها قانون التوزيع المركزي.
- لا تمثل النقاط الموجودة على الخط المستقيم بين نقطتي نهاية منحنى اللون الطيفي ألوانًا طيفية بل تمثل ألوانًا مختلطة متنوعة تم الحصول عليها عن طريق مزج اللون الأرجواني عند 380 نانومتر والأحمر عند 780 نانومتر بنسب مختلفة.
- حدد أي ثلاث نقاط ضمن مسار ألوان الطيف لإنشاء لون. على سبيل المثال، إذا اخترت R1, G1, B1 على أنها الألوان الثلاثة للمطابقة، فإن جميع الألوان المختلفة التي تشكلها هذه الألوان الثلاثة موجودة داخل المثلث الذي تقع رءوسه عند النقاط الثلاث R1, G1, B1.
② تمثيل الطول الموجي السائد والتشبع
في المخطط اللوني، يمكن تمثيل الألوان ليس فقط بالإحداثيات اللونية (س، ص). هناك طريقة أخرى اقترحها هيلمهولتز وهي تمثيلها باستخدام الطول الموجي السائد λd والتشبع (نقاء المثير) Pe. λd و فe هي قيم محددة مشتقة من الإحداثيات اللونية في الرسم البياني (الشكل 3-7). يمثل الطول الموجي السائد تقريباً الإحساس اللوني الذي تدركه العين البشرية.
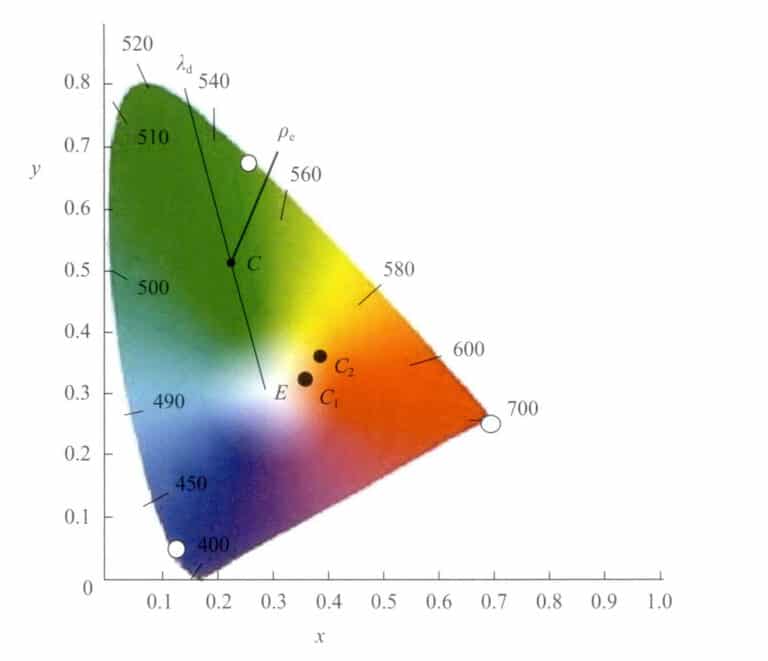
افترض أن موضع هذه النقطة في المخطط اللوني هو ج(س، ص). وصِّل النقطة c مع الأبيض E ومدها لتتقاطع مع مسار الطيف عند λd . بعد ذلك، فإن عدد الطول الموجي للنقطة λd على مسار الطيف هو الطول الموجي السائد لهذا الضوء الملون.
تقع النقطة C على الخط المستقيم الواصل بين النقطتين W و λd التي تمثل تشبع هذا اللون. النقطة W هي الأبيض النقي (E) أو مصدر ضوء أبيض محدد. عندما تتحرك الإحداثيات اللونية للون معين تدريجيًا على طول اتجاه نحو المسار الطيفي من النقطة W البيضاء، يزداد تشبع اللون تدريجيًا حتى يصل إلى المسار الطيفي، بحد أقصى للتشبع يبلغ 1.
يتم تمثيل الألوان باستخدام الطول الموجي السائد والتشبع، مما يسهل مقارنة اختلافات الألوان. الاختلافات اللونية الطفيفة، التي تمثلها التغيرات العددية في λd و ρeيمكن عرضها.
للونين، ج1, C2والإحداثيات اللونية والطول الموجي السائد والتشبع تحت نفس الإضاءة موضحة في الجدول 3-2. يمكن ملاحظة أن الطول الموجي السائد للون C1, C2 يختلف بمقدار 0.052 نانومتر، ويختلف التشبع بمقدار 7%.
الجدول 3-2 مقارنة بيانات الألوان بين C1 و C2
| نقطة الإسقاط اللوني | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. أدوات قياس لون الأحجار الكريمة
(1) مقياس الطيف الضوئي
مبدأ العمل: نظرًا لأن توزيع الطاقة الطيفية لمصدر الضوء القياسي داخل الجهاز معروف، يمكن الحصول على قيم التريستيمولوس الثلاثي لجسم ما من خلال قياس الانعكاس الطيفي له.
(2) مقياس الألوان ثلاثي القيمة اللونية
وهو عبارة عن أداة تكاملية كهروضوئية تقيس مباشرةً قيم المحفزات الثلاثة للون الجسم. وهي تحاكي بشكل أساسي استجابات الراصد القياسية الثلاثة للألوان من خلال مجموعة مناسبة من المرشحات والمحولات الكهروضوئية.
في الوقت الحالي، يعتمد الحكم على لون الأحجار الكريمة بشكل أساسي على ملاحظة العين البشرية. على سبيل المثال، يتأثر الزمرد والياقوت والماس بالعوامل البيئية، مما يؤدي إلى انخفاض الدقة في قياسات الأدوات؛ ولذلك، فإن تطبيق قياس اللون بالأدوات في تحديد لون الأحجار الكريمة نادر نسبياً.
القسم الثاني الأصول النظرية للون الأحجار الكريمة المعدنية
تأتي معادن الأحجار الكريمة بألوان مختلفة، ولكن تختلف أسباب تلوينها أيضاً. ووفقاً لنظرية علم المعادن الكلاسيكية، يمكن تصنيف أصول ألوان معادن الأحجار الكريمة إلى اللون اللوني المجهول واللون اللوني الشامل واللون الزائف.
1. تصنيف نظرية الأصل اللوني لعلم المعادن الكلاسيكية
تُعد النظرية الكلاسيكية لعلم المعادن النظرية الأساسية لدراسة ألوان المعادن الكريمة. ووفقًا لما إذا كان لون المعدن يرجع إلى المعدن نفسه، يمكن تقسيمه إلى ثلاث فئات: اللون اللوني المجهول اللون، واللون اللوني الشامل، واللون الزائف.
(1) أحادي اللون - ملون
يتشكل لون الجوهرة من المكونات الكيميائية المتأصلة في المعدن الذي تتكون منه، والمعروف باسم الأحجار الكريمة ذات اللون اللوني الأحادي. وتُسمّى هذه الأحجار الكريمة أحجاراً كريمة ذات لون ثنائي اللون. وتتسبب المكونات المتأصلة فيها في اللون الذي تنتجه الأحجار الكريمة ذات اللون اللوني الأحادي؛ وبالتالي، فهي تتمتع بثبات لوني جيد ولا يسهل تغيير لونها. على سبيل المثال، التركيب الكيميائي للفيروز هوCuAl6(ص4)4(أوه)8-5H2O، ويحدث اللون الأزرق أو الأزرق المائل إلى الأخضر بسبب النحاس2+؛التركيب الكيميائي للأزوريت هو 2CuCO3 - النحاس(OH)2و Cu2+ يتسبب أيضًا في لونه الأزرق"؛ وينتج اللون الأخضر للأوليفين عن أيونات الحديد في تركيبه الكيميائي (الشكل 3-8).

لا توجد أنواع كثيرة من الأحجار الكريمة ذاتية اللون في معادن الأحجار الكريمة الطبيعية، والأصناف الرئيسية هي الفيروز والمالكيت والأزوريت والأوليفين والعقيق والرودوكروسيت. وترد في الجدول 3-3 الألوان الشائعة وعناصر التلوين والتركيبات الكيميائية للأحجار الكريمة ذاتية اللون.
الجدول 3-3 عناصر التلوين الشائعة والتركيب الكيميائي وألوان الأحجار الكريمة الملونة
| عناصر التلوين | اسم الحجر الكريم | التركيب الكيميائي | اللون |
|---|---|---|---|
| حديد | أوليفين | (المغنيسيوم، الحديد)2 (SiO4) | أخضر |
| المندين | في3آل2 (SiO4)3 | أحمر | |
| الكروم | يوفاروفيت | كاليفورنيا3كر2 (SiO4)3 | أخضر |
| كيبروم | الملكيت | النحاس2شركة3(أوه)2 | أخضر |
| الكريسوكولا | (CuAl)2H2سي2O5(أوه)4 - ن هـ2O | أخضر - أزرق | |
| تركواز | CUAl6(ص4)4(أوه)8.5H2O | أزرق سماوي - أخضر | |
| أزوريت | 2CuCO3 - النحاس(OH)2 | أزرق | |
| المنجنيز | سبيسارتين-غارنيه | من3آل2(SiO4)3 | برتقالي |
| رودوكروسيت | منكو3 | وردي - أحمر | |
| الرودونيت | (المنغنيز والكالسيوم والحديد) - 5(سيليكون5O15) | وردي - أحمر |
نسخ الكتابة على مجوهرات سوبلينج - مصنع مجوهرات حسب الطلب، مصنع مجوهرات OEM و ODM
يمكن أن يتغير لون بعض الأحجار الكريمة الملونة تحت ظروف معينة. على سبيل المثال، يمكن أن يتغير لون الفيروز والمالكيت عند تعرضهما لدرجات حرارة عالية بسبب تبخر جزيئات الماء في تركيبهما؛ ويمكن أن يتحلل الرودوكروسيت، وهو حجر كريم كربوني، عندما يواجه الأحماض (مثل حمض الهيدروكلوريك أو حمض الكبريتيك)، ويتغير لونه أيضاً وفقاً لذلك.
(2) جميع الألوان-الألوانإد
ينجم لون الحجر الكريم عن عناصر شوائب ضئيلة أو طفيفة خارجة عن التركيب الكيميائي المتأصل للمعادن المكوّنة له، وهو ما يُعرف باسم اللون اللوني الشامل. ويُشار إلى هذه الأحجار الكريمة باسم الأحجار الكريمة ذات الألوان اللونية الشاملة.
في معادن الأحجار الكريمة، هناك العديد من أنواع الأحجار الكريمة ذات الألوان المختلفة. عندما لا يكون هناك شوائب في التركيب الكيميائي للأحجار الكريمة، فإنها تكون عديمة اللون وشفافة؛ وعندما تحتوي على شوائب عناصر تلوين مختلفة، يمكن أن تنتج ألواناً مختلفة.
عندما يكون الكوراندوم النقي عديم اللون، يتحول إلى ياقوت عندما يحتوي على كمية صغيرة من أيونات الكروم؛ وعندما يحتوي على كمية صغيرة من الحديد والتيتانيوم، يتحول إلى أحجار كريمة زرقاء أو خضراء. وتشمل الأحجار الكريمة المماثلة الزمرد والإسبنيل والتورمالين والجاديت والعقيق الأبيض والنفريت وغيرها. وترد في الجدول 3-4 العناصر الملونة الشائعة والتركيبات الكيميائية والأحجار الكريمة الملونة بالألوان المختلفة.
الجدول 3-4 عناصر التلوين الشائعة، والتركيب الكيميائي، والأحجار الكريمة الملونة بالألوان المختلفة
| عناصر التلوين | اسم الحجر الكريم | التركيب الكيميائي | اللون |
|---|---|---|---|
| الكروم | روبي | آل2O3 | أحمر |
| الزمرد | كن3آل2(سي6O18) | أخضر | |
| ألكسندريت | BeAl2O4 | أحمر-أخضر | |
| الإسبنيل | المغنيسيوم2O4 | أحمر | |
| العقيق الأبيض | SiO2 | أخضر | |
| حديد | الزبرجد | كن3آل2سي6O18 | أزرق |
| التورمالين | (Na، K، Ca) (Al، Fe، F3+كر)، كر)6(BO3)3سي6O18(أوه)4 | أخضر-بني | |
| الإسبنيل | المغنيسيوم2O4 | أصفر | |
| نيفريت | كاليفورنيا2(المغنيسيوم، الحديد2+) 5 (سي4O11) 2 (أوه)2 | أخضر | |
| الفاناديوم | تنزانيت | كاليفورنيا2آل3(SiO4)3(أوه) | أزرق بنفسجي-أزرق |
| البريل الأخضر | كن3آل2سي6O18 | أخضر | |
| تيتانيوم | بينيتويت | باتيزي BaTiSi3O9 | أزرق |
| الياقوت | آل2O3 | أزرق | |
| المنجنيز | البريل الأحمر | كن3آل2سي6O18 | أحمر |
| رودوكروسيت | منكو3 | وردي | |
| كوبالت | الإسبنيل الطبيعي | المغنيسيوم2O4 | أزرق |
| الإسبنيل الاصطناعي | المغنيسيوم2O4 | أزرق | |
| نيكل | عقيق أخضر | SiO2 | أخضر |
(3) زائف-الألوانإد
لا ترتبط الألوان الناتجة عن الألوان الزائفة بالتركيب الكيميائي لمعادن الأحجار الكريمة. ومع ذلك، فهي ناتجة عن تغيرات هيكلية وتركيبية ناتجة عن الخلائط الميكانيكية أو تكوين المعادن. والألوان الزائفة ليست ألوان المعادن نفسها، بل هي ألوان ناتجة عن تراكيب خاصة تشكلت بفعل مؤثرات خارجية. على سبيل المثال، الألوان المتداخلة الجميلة الناتجة عن تداخل الضوء المنعكس والساقط، مثل تأثير التفلور في اللابرادوريت وتأثير تلاعب الألوان في الأوبال. يندرج التلوين الناجم عن الشوائب أيضاً تحت الألوان الزائفة، مثل الألماس الأسود، بسبب العديد من شوائب الجرافيت السوداء المعتمة داخل الألماس.
2. الأيونات المسببة للألوان في المعادن الثمينة
يمكن أن تكون العناصر الكيميائية التي تنتج ألوان الأحجار الكريمة هي المكونات الرئيسية أو الثانوية. وغالباً ما يُشار إلى العناصر الفلزية الانتقالية، خاصةً المعادن الانتقالية من الفترة الرابعة وهي التيتانيوم والفاناديوم والكروم والمنغنيز والحديد والكوبالت والنيكل والنحاس، باسم الأيونات الملونة أو الأيونات الملونة. تشغل هذه العناصر الثمانية مواضع متتالية في الجدول الدوري، وتتراوح أعدادها الذرية من 22 (Ti) إلى 29 (Cu). الخواص الأساسية لهذه العناصر موضحة في الجدول 3-5.
الجدول 3-5 الخصائص الأساسية لثمانية عناصر انتقالية
| اسم العنصر | تيتانيوم | الفاناديوم | الكروم | المنجنيز | حديد | كوبالت | نيكل | النحاس |
|---|---|---|---|---|---|---|---|---|
| رمز العنصر | تي | V | كر | من | في | شركة | ني | النحاس |
| العدد الذري | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| حالات الأكسدة الرئيسية | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| تكوين إلكترونات التكافؤ | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
تتميز هذه العناصر الفلزية الانتقالية الثمانية بالخصائص التالية:
① تمتلئ إلكترونات التكافؤ في مدارات d في الغلاف قبل الأخير في التسلسل، والصيغة العامة لتوزيع إلكترونات التكافؤ لذرات العناصر الانتقالية هي (n-1)d1-10ن س1-2لذلك تسمى هذه العناصر أيضًا عناصر الكتلة d.
② في الفلزات الانتقالية، نظرًا لأن المدارات d في الغلاف قبل الأخير متصلة بمدارات s الخارجية، ولأن المدارات d لم تصل بعد إلى بنية مستقرة، يمكن أن تشارك كل من إلكترونات s وإلكترونات d في الترابط جزئيًا أو كليًا، مما ينتج عنه سلسلة من حالات التأكسد المتغيرة للفلزات الانتقالية، حيث تقدم الأكاسيد المختلفة ألوانًا مختلفة في الأحجار الكريمة.
③ تُظهر الأيونات لونًا بشكل عام بسبب وجود إلكترونات أحادية غير متزاوجة في المدارات d، وتكون مستويات طاقة هذه الإلكترونات في الحالتين المثارة والأرضية متقاربة نسبيًا، مما يسمح لطاقة الضوء المرئي بإثارتها. وقد تتسبب ظروف الإثارة المختلفة أيضًا في أن تُظهر الأحجار الكريمة ألوانًا مختلفة.
إذا كانت جميع إلكترونات الدوران في الأيون مقترنة، مثل الأيونات ذات التوزيع الإلكتروني للتكافؤ d0, d10, d10s2فإن الإلكترونات تكون في حالة مستقرة ولا يتم إثارتها بسهولة، مما يؤدي إلى عدم وجود لون للأيون؛ ومن ثَمَّ، فإن C+، كر6+ والبعض الآخر ليس له لون ولا يمكنه إنتاج لون في الأحجار الكريمة.
وتشكّل هذه العناصر المعدنية الانتقالية الثمانية تشكيل الألوان في الأحجار الكريمة الشائعة ذات الألوان الطبيعية. وتنتج الكروموفورات المختلفة ألواناً مختلفة في الأحجار الكريمة المختلفة، وقد ينتج نفس الكروموفور ألواناً مختلفة أيضاً. ويوضح الجدول 3-6 الأحجار الكريمة الطبيعية الشائعة والكروموفور في الجدول 3-6.
الجدول 3-6 الألوان التي تعرضها أيونات الفلزات الانتقالية في الأحجار الكريمة الطبيعية الشائعة وأصناف الأحجار الكريمة
| الكروموفور | الألوان الشائعة | أصناف الأحجار الكريمة |
|---|---|---|
| أيون التيتانيوم (Ti) | أزرق | الياقوت، البينيتويت، التوباز |
| أيون الفاناديوم (V) | أخضر | الكوراندوم الاصطناعي المتغير اللون، الإيسونيت، الزمرد |
| أيون الكروم (Cr) | أحمر، أخضر | الياقوت، والياقوت، والكوراندوم، والزمرد، والبيروب، واليشم |
| أيون المنجنيز (Mn) | وردي، أحمر | السبيسارتين، الرودوليت، البريل الأحمر |
| أيون الحديد (Fe) | أزرق، أخضر، أصفر | الياقوت، الزبرجد الزيتوني، الزبرجد الزبرجد، التورمالين، الإسبنيل |
| أيون الكوبالت (Co) | أزرق | إسبنيل اصطناعي، ستولوليت بلون الكوبالت |
| أيون النيكل (نيكل) | أخضر | عقيق أخضر |
| أيون النحاس (النحاس) | أزرق، أزرق-أخضر-أزرق-أخضر | الملكيت، الفيروز، اللازورد، اللازورد |
وتنتج أيونات الكروموفور المختلفة ألواناً مختلفة في الأحجار الكريمة، مما يؤدي إلى أطياف امتصاص ذات خصائص مميزة. بالنسبة لأيونات الكروموفور الشائعة، يكون لأطياف الامتصاص أهمية نموذجية في تحديد الهوية.
(1) طيف امتصاص أيونات الكروم
يتميز طيف الامتصاص لأيونات الكروم بشكل أساسي بالعديد من خطوط الامتصاص الضيقة في المنطقة الحمراء، حيث يقع أقوى خطين في المنطقة الحمراء العميقة وخطين آخرين في المنطقة البرتقالية. تحتوي المنطقة الصفراء الخضراء على نطاق امتصاص واسع، ويرتبط عرض المنطقة الصفراء الخضراء وموضعها وشدتها بعمق لون الجوهرة. يمكن أن يكون هناك عدة نطاقات ضيقة في المنطقة الزرقاء، بينما المنطقة الأرجوانية ممتصة بالكامل. تُنتج أيونات الكروم بشكل أساسي اللونين الأحمر والأخضر، واللذين يختلفان باختلاف الأحجار الكريمة، وتُظهر أطياف الامتصاص بعض الاختلافات. فعلى سبيل المثال، تحتوي أحجار الياقوت على ثلاثة خطوط امتصاص في المنطقة الحمراء، ونطاق امتصاص عريض في المنطقة الصفراء الخضراء، وثلاثة خطوط امتصاص في المنطقة الزرقاء، وامتصاص كامل في المنطقة البنفسجية؛ أما الزمرد فيحتوي على خطوط امتصاص في المنطقة الحمراء، ونطاق امتصاص ضعيف في المنطقة البرتقالية الصفراء، وخطوط امتصاص ضعيفة في المنطقة الزرقاء، وامتصاص كامل في المنطقة البنفسجية؛ ويحتوي حجر الكسندريت على خطوط امتصاص في المنطقة الحمراء، ونطاق امتصاص في المنطقة الصفراء الخضراء، وخط امتصاص واحد في المنطقة الزرقاء، وامتصاص كامل في المنطقة البنفسجية. ويوضح الشكل 3-9 أطياف الامتصاص لهذه الأحجار الكريمة الثلاثة.

(2) خصائص طيف امتصاص أيون الحديد
تُنتج أيونات الحديد ألواناً مختلفة في الأحجار الكريمة المختلفة ولها تأثير تلوين قوي، لكن طيف امتصاص أيونات الحديد يختلف بشكل كبير. فعندما تكون الأحجار الكريمة خضراء، تنتج امتصاصاً في المنطقة الحمراء، وعندما تكون حمراء، تنتج خاصية امتصاص تهيمن عليها المنطقة الزرقاء، مع وجود خط الامتصاص المميز الرئيسي في المنطقتين الخضراء والزرقاء. على سبيل المثال، تظهر أيونات الحديد في الزبرجد الزيتوني باللون الأخضر الزيتوني، حيث يظهر طيف الامتصاص بشكل أساسي ثلاثة نطاقات امتصاص ضيقة في المنطقة الزرقاء عند 453 نانومتر و473 نانومتر و493 نانومتر؛ أما الألمندين الأحمر فيتميز بطيف امتصاص نموذجي للحديد، مع ثلاثة نطاقات امتصاص ضيقة قوية عند 504 نانومتر و520 نانومتر و573 نانومتر في المنطقة الصفراء الخضراء، والتي يشار إليها عادةً في الصناعة باسم "نافذة الحديد". وبالإضافة إلى ذلك، هناك نطاقات امتصاص ضيقة ضعيفة عند 423 نانومتر، و460 نانومتر، و610 نانومتر، و680 إلى 690 نانومتر؛ ويحتوي طيف الامتصاص في الياقوت الأصفر على ثلاثة نطاقات امتصاص ضيقة في المنطقة الزرقاء عند 450 نانومتر، و460 نانومتر، و470 نانومتر (الشكل 3-10).
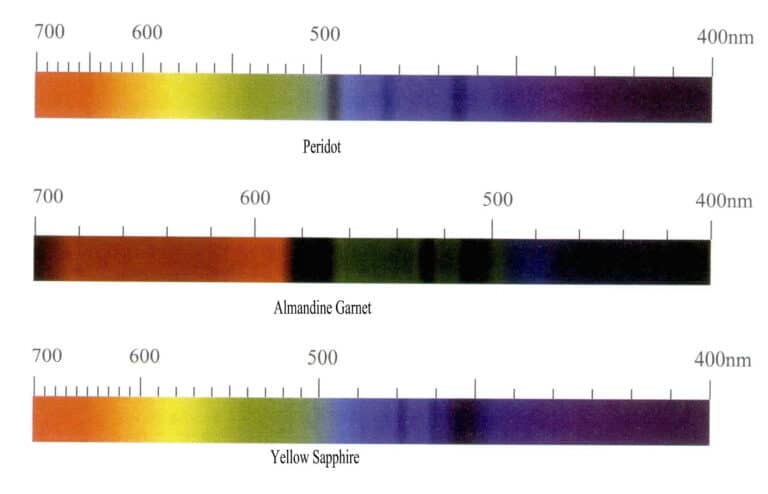
(3) خصائص طيف الامتصاص لأيونات المنجنيز
تتشكل أيونات المنجنيز بشكل أساسي باللون الوردي والبرتقالي والأحمر في الأحجار الكريمة، ويظهر طيف الامتصاص بشكل أساسي امتصاصًا قويًا في المنطقة البنفسجية، ويمتد إلى المنطقة فوق البنفسجية، وبعض الامتصاص في المنطقة الزرقاء. على سبيل المثال، تحتوي خصائص طيف الامتصاص في الرودوكروسيت الوردي على ثلاثة نطاقات امتصاص عند 410 نانومتر و450 نانومتر و540 نانومتر؛ وتحتوي خطوط طيف الامتصاص في السسبسارتين بشكل أساسي على ثلاثة نطاقات امتصاص عند 410 نانومتر و420 نانومتر و430 نانومتر وخطوط امتصاص عند 460 نانومتر و480 نانومتر و520 نانومتر. في بعض الأحيان، قد يكون هناك خطي امتصاص عند 504 نانومتر، 573 نانومتر، 573 نانومتر (الشكل 3-11).

(4) خصائص طيف الامتصاص لأيونات الكوبالت
تتمتع أيونات الكوبالت بتأثير تلوين قوي، وعادةً ما تظهر بلون أزرق فاتح في الأحجار الكريمة، حيث يُظهر طيف الامتصاص بشكل أساسي ثلاثة نطاقات امتصاص قوية وواسعة في المنطقة الصفراء-الخضراء. ونظرًا لانخفاض وفرة الكوبالت في القشرة الأرضية، يوجد عدد قليل جدًا من الأحجار الكريمة الطبيعية الملونة بأيونات الكوبالت. يشير طيف امتصاص أيونات الكوبالت أيضًا إلى الأحجار الكريمة الاصطناعية، مثل الإسبنيل الأزرق الاصطناعي وزجاج الكوبالت. ويحتوي الإسبنيل الأزرق الاصطناعي على ثلاثة نطاقات امتصاص قوية في المنطقتين الصفراء-الخضراء والبرتقالية-الصفراء، مع كون نطاق الامتصاص في المنطقة الخضراء هو الأضيق؛ وتحتوي خطوط امتصاص زجاج الكوبالت بشكل أساسي على ثلاثة نطاقات امتصاص قوية في المنطقتين الصفراء-الخضراء والبرتقالية-الصفراء، مع كون نطاق الامتصاص في المنطقة الصفراء هو الأضيق (الشكل 3-12).

3. تلوين العناصر الأرضية النادرة
تزداد الأبحاث حول تأثير العناصر الأرضية النادرة النادرة على لون الأحجار الكريمة تعمقاً. فألوان العناصر الأرضية النادرة أكثر حيوية، كما أن خواصها الفيزيائية الكيميائية مستقرة للغاية. كما يمكن للعناصر الأرضية النادرة مثل الأباتيت والفلوريت تلوين الأحجار الكريمة الطبيعية. يمكن إضافة عناصر ترابية نادرة مختلفة إلى الأحجار الكريمة الاصطناعية والمعالجة على النحو الأمثل للحصول على أحجار كريمة ملونة مختلفة، مثل الأصفر من السيريوم والأزرق من النيوديميوم.
والعناصر الأرضية النادرة التي تلوّن الأحجار الكريمة هي عناصر اللانثانيد والأكتينيد في الجدول الدوري للعناصر الكيميائية والألوان التي يمكن أن تنتجها موضحة في الجدول 3-7.
الجدول 3-7 العناصر الأرضية النادرة وألوانها في الأحجار الكريمة الشائعة
| رمز العنصر | لا | ج | ن د | ص | داي | سم | إيه | ت م | U |
|---|---|---|---|---|---|---|---|---|---|
| الاسم الكامل | لانثانوم | السيريوم | النيوديميوم | براسيوديميوم | ديسبروسيوم | السماريوم | الإربيوم | ثوليوم | اليورانيوم |
| اللون | عديم اللون | أصفر | أزرق | أخضر | أصفر فاتح | أصفر فاتح | وردي | أخضر فاتح | فضي-أبيض |
العناصر الأرضية النادرة لها أطياف امتصاص مميزة، وغالبًا ما تشكل خطوطًا دقيقة فريدة من نوعها. على سبيل المثال، غالبًا ما يحتوي الأباتيت الأصفر على العنصر الترابي النادر Ce، مع خطوط امتصاص دقيقة مميزة في المنطقة الصفراء. ومع ذلك، لا يُنتج اليورانيوم لونًا أصفر ساطعًا؛ إذ يمكن أن يولد خطوط امتصاص طيفية مميزة. على سبيل المثال، يمكن أن تظهر أكثر من عشرة خطوط امتصاص في الزركون الأخضر في مناطق لونية مختلفة (الشكل 3-13).

القسم الثالث الألوان الناتجة عن العيوب البلورية ومراكز الألوان
في الطبيعة، تنقسم المعادن في الطبيعة إلى بلورات وغير بلورات بناءً على درجات مختلفة من التبلور. فمعظم الأحجار الكريمة، مثل الياقوت والياقوت الأزرق والماس والزمرد والكوارتز، هي أحجار بلورية؛ وبعض الأحجار الكريمة العضوية، مثل الكهرمان والمرجان، غير بلورية. تتميز الهياكل البلورية ببنية شبيهة بالشبيكة، حيث يتم ترتيب جزيئاتها الداخلية (الذرات أو الأيونات أو الجزيئات) في نمط دوري منتظم في فضاء ثلاثي الأبعاد، ويمكن أن تشكل البلورات أشكالاً متعددة الأوجه تلقائياً؛ أما الأجسام غير البلورية فهي أجسام غير متبلورة ذات هياكل غير شبكية لا يمكنها تشكيل أشكال متعددة الأوجه مثل الزجاج والصنوبري والراتنج.
المثال الأكثر شيوعًا للفرق بين البلورات والمواد الصلبة غير المتبلورة هو الكوارتز والزجاج. يتكون الكوارتز الطبيعي من المادة المنصهرة SiO2 في الصهارة التي تبرد في تجاويف داخل القشرة الأرضية. والطبقة الخارجية لكرات الكوارتز الشائعة هي العقيق الذي لا يظهر الشكل البلوري، بينما تقدم الطبقة الداخلية الشكل البلوري للكوارتز. والمكونات الكيميائية الرئيسية لكل من الزجاج والكوارتز هي SiO2؛ الكوارتز عبارة عن بلورة تحتوي على أيونات السيليكون والأكسجين مرتبة بطريقة منظمة، في حين أن الزجاج مادة صلبة غير متبلورة تحتوي على أيونات السيليكون والأكسجين مرتبة بشكل فوضوي يفتقر إلى الانتظام، كما هو موضح في الشكل 3-14.
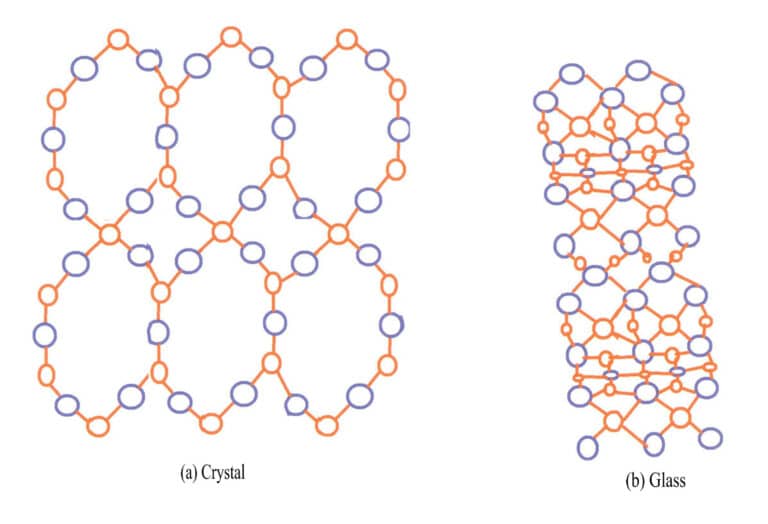
تتلون معظم بلورات الأحجار الكريمة بسبب أيونات الشوائب، مثل الياقوت والزمرد والتورمالين. كما أن بعض الأحجار الكريمة، على الرغم من افتقارها إلى أيونات الكروموفور، تكون ملونة بسبب عيوب في بنيتها البلورية. يمكن أن يتغير لون الأحجار الكريمة الطبيعية المنتجة في الطبيعة بسبب ظروف خارجية، مثل التشعيع والتأين، والتي تغير البنية البلورية. المثال الأكثر شيوعًا هو الكوارتز الدخاني الذي يتطور لونه بسبب تكوين مراكز لونية من الفراغات الناجمة عن الإشعاع. يتميز الكوارتز الدخاني المشعع اصطناعيًا بمبدأ تكوين مماثل للكوارتز الدخاني الطبيعي، باستثناء أن الإشعاع الاصطناعي يخلق اللون بسرعة.
1. عيوب البلورة وأنواعها
وتُسمّى الظاهرة التي ينحرف فيها ترتيب الجسيمات عن قواعد البنية الشبكية (تخضع الجسيمات لتكرار انتقالي دوري في فضاء ثلاثي الأبعاد) ضمن نطاق محلي من البنية البلورية للأحجار الكريمة بعيب شبكي. وترتبط الأسباب بالاهتزازات الحرارية للجسيمات داخل بلورة الأحجار الكريمة، والإجهاد الخارجي، وارتفاع درجة الحرارة والضغط، والإشعاع، والانتشار، وزرع الأيونات، وغيرها من الظروف.
على سبيل المثال، يتبلور الماس في بيئة عالية الحرارة والضغط في الوشاح العلوي عندما تحمله الصهارة المضيفة (الكمبرلايت أو اللمبروايت) بسرعة إلى قرب سطح الأرض، ويمكن أن يؤدي التغير السريع في ظروف الحرارة والضغط والاصطدامات المتبادلة بين البلورات والصخور المحيطة بها بسهولة إلى تغييرات موضعية في بنية بلورات الماس المتطفلة، مما يؤدي إلى عيوب شبكية تغير لون الماس عديم اللون في الأصل، مكونةً ماساً أصفر مائل إلى البني والأصفر والبني والوردي.
إن وجود العيوب البلورية له تأثير كبير على خصائص البلورات. في الواقع، تحتوي البلورات على عيوب أكثر أو أقل. يمكن لكمية معتدلة من بعض العيوب النقطية أن تعزز بشكل كبير من توصيلية المواد شبه الموصلة وإضاءة المواد المضيئة، مما يؤدي دورًا مفيدًا. وفي المقابل، يمكن أن تؤدي العيوب مثل الخلع إلى جعل المواد عرضة للكسر، مما يقلل من قوة الشد للبلورات التي لا تحتوي على عيوب شبكية تقريبًا إلى جزء بسيط منها.
في البلورة المثالية المثالية، تكون الذرات مرتبة بدقة في شبكة منتظمة ودورية في نقاط محددة في الفراغ. ومع ذلك، أثناء النمو والتكوين الفعلي للبلورات، وبسبب تأثير بيئات النمو مثل درجة الحرارة والضغط وتركيز المكوّنات الوسطية، قد ينحرف شكل البلورة بعد النمو أحيانًا عن البنية البلورية المثالية. ويمكن تسمية أي انحراف عن التركيب البلوري المثالي بالعيب البلوري. وتؤثر العيوب البلورية بشكل كبير على الخواص الفيزيائية والكيميائية للبلورات، وترتبط العديد من التخصصات بالعيوب البلورية، مثل المنشطات الأيونية في علم المواد. ويرتبط لون الأحجار الكريمة إلى حد كبير بالعيوب البلورية الموجودة داخلها. وهذا أحد أسباب اللون في الأحجار الكريمة - مراكز الألوان.
هناك العديد من أنواع عيوب البنية البلورية، والتي يمكن تصنيفها إلى أربع فئات بناءً على مدى توزعها في الفضاء ثلاثي الأبعاد: العيوب النقطية، والعيوب الخطية، والعيوب السطحية، وعيوب الحجم.
(1) العيوب النقطية
وتحل ذرات أخرى محل بعض الذرات في البلورة المثالية، أو يتم تخدير بعض الذرات، أو يتم إنشاء فراغات. تُستبدل بعض الذرات في البلورة أو تُفقد بعض الذرات بسبب ذرات خارجية، وتؤدي هذه التغييرات إلى تعطيل الترتيب الدوري للشبكة المنتظمة للبلورة، مما يسبب تغيرات في المجال الكامن للجسيمات وينتج عنه عدم اكتمال البنية البلورية، ويقتصر على مواضع معينة، مما يؤثر على عدد قليل من الذرات القريبة فقط. ويكون تأثير العيوب النقطية على البلورة ضئيلاً، وتشمل الأنواع الشائعة من العيوب النقطية عيوب موضع الشبكة الشبكية والعيوب التركيبية وعيوب الشحنة (الشكل 3-15).
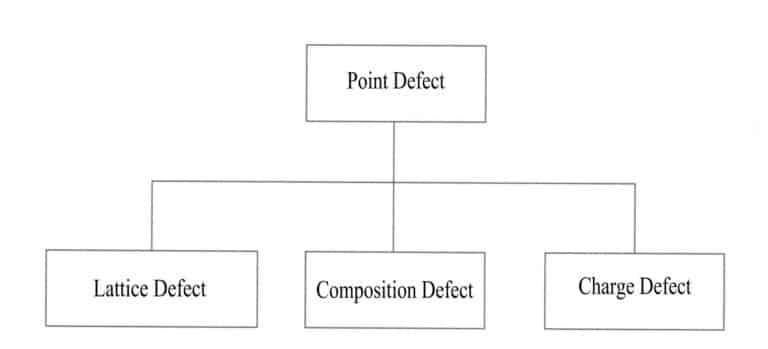
(2) عيوب الخط (2)
تكون العيوب الخطية صغيرة جداً في حجمها في اتجاهين وتمتد بشكل أساسي لفترة أطول في اتجاه آخر. وتُعرف أيضًا باسم العيوب أحادية البعد وتتكون في المقام الأول من خلع مختلف. يمكن النظر إلى الاضطرابات على أنها نتاج انزلاق شبكي محلي على طول مستوى ذري معين. لا يخترق الانزلاق الشبكة بأكملها؛ حيث ينتهي العيب البلوري داخل الشبكة، مما يتسبب في ترتيب غير منظم للجسيمات عند الحد الفاصل بين الأجزاء المنزلقة، وغير المنزلقة، من الشبكة، والمعروف باسم الخلع. ويطلق على هذا الحد الفاصل، وهو خط التقاطع بين المناطق المنزلقة، وغير المنزلقة، اسم خط الخلع. ويوجد نوعان أساسيان من الخلع: عندما تتعرض البلورة لقوى انضغاطية، يشكل مستوى انزلاق الجسيمات خط خلع مع المستوى غير المنزلق، ويكون خط الخلع عموديًا على اتجاه الانزلاق، ويعرف باسم خلع الحافة، ويسمى أيضًا خلع إسفيني؛ وبسبب إجهاد القص، يحدث الانزلاق بين المستويات، وتكون خطوط الخلع المتقاطعة في الجزء المنزلق من البلورة موازية لاتجاه الانزلاق، ويشار إليه باسم الخلع اللولبي (الشكل 16-3).
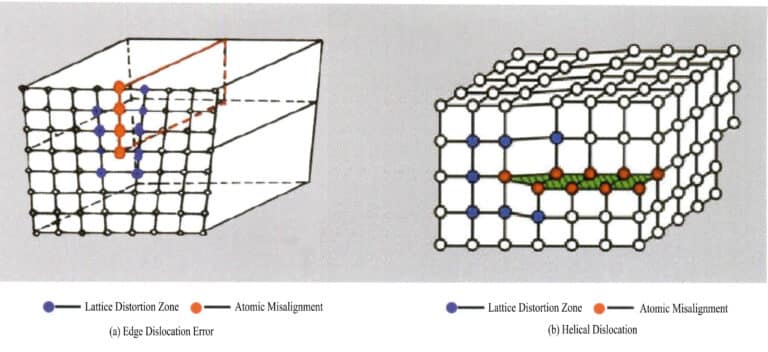
(3) العيوب السطحية
إن أبسط العيوب السطحية هي عيوب التراص التي تنقسم إلى عيوب التراص الجوهرية (حيث تتم إزالة مستوى بلوري) وعيوب التراص الخارجية (حيث يتم إدخال طبقة ذرية في البلورة). تحدث هذه العيوب في نطاق بضع مسافات ذرية على جانبي مستوى معين على طول الشبكة أو بين الحبيبات. وهي تشمل بشكل أساسي عيوب التراص والواجهات البينية داخل البلورات وفيما بينها، مثل حدود الحبيبات ذات الزوايا الصغيرة، وجدران المجال، والحدود التوأمية والبينية.
(4) عيوب الحجم
تشير عيوب الحجم إلى العيوب التي توجد بدرجات متفاوتة في جميع الاتجاهات الثلاثة، وهي عيوب ثلاثية الأبعاد، مثل الشقوق المضمنة والتراكيب الشبكية والتراكيب العائلية والتوائم وشوائب الأحجار الكريمة المختلفة.
2. مراكز الألوان في الأحجار الكريمة
مراكز الألوان هي حالة خاصة من العيوب الشبكية، وتشير بشكل عام إلى العيوب الشبكية في الأحجار الكريمة التي يمكنها امتصاص طاقة الضوء المرئي بشكل انتقائي وإنتاج اللون، وتنتمي إلى أنواع الألوان البنيوية الأكثر شيوعاً. في بعض الحالات، يمكن للإلكترونات غير المزدوجة التي تنتج اللون أن تظهر أيضًا في أيونات العناصر غير الانتقالية أو في العيوب البلورية التي تتشكل بسبب نقص الإلكترونات، وهو ما تمثله المراكز اللونية. يمكن أن تتسبب العيوب النقطية في البلورات الأيونية في امتصاص الضوء المرئي، مما يؤدي إلى ظهور بلورات شفافة في الأصل ملونة؛ وعادة ما يشار إلى هذه الأنواع من العيوب النقطية التي يمكن أن تمتص الضوء المرئي باسم مراكز الألوان. وتنتج أنواع كثيرة من الأحجار الكريمة الطبيعية ألواناً من مراكز الألوان، مثل الفلوريت الأرجواني والكريستال الدخاني والماس الأخضر.
في عملية المعالجة المثلى للأحجار الكريمة، يمكن أن تحتوي بعض الأحجار الكريمة الطبيعية والاصطناعية أيضًا على مراكز لونية ناتجة عن الإشعاع، مثل الماس الأزرق والأصفر والأحمر والأخضر والتوباز الأزرق الذي يتغير لونه بسبب الإشعاع، والتوباز الأزرق، ومن بينها بعض الألوان المستقرة نسبيًا ولا تختفي إلا عند تسخينها؛ وبعض الألوان غير مستقرة وقد تتلاشى حتى في درجة حرارة الغرفة. ويرتبط هذا النوع من المراكز اللونية المسببة للألوان ارتباطاً وثيقاً بالبنية البلورية للأحجار الكريمة، مثل الألماس الأخضر، حيث يكون سبب اللون هو وجود فراغات في البنية البلورية، ولكن يمكن أيضاً إزالة هذا العيب البنيوي عن طريق التشعيع، مما يجعل الألماس عديم اللون. والأنواع الشائعة لمراكز الألوان في الأحجار الكريمة هي "مراكز الألوان الإلكترونية" و"مراكز الألوان الثقبية".
(1) مركز ألوان الإلكترون (مركز F)
مراكز ألوان الإلكترونات هي مراكز لونية تتشكل عندما تتواجد الإلكترونات في شواغر العيوب البلورية الناجمة عن شواغر أنيون في البنية البلورية للأحجار الكريمة. وعندما يكون الأنيون غائباً، تصبح الفجوة مصيدة إلكترونية موجبة الشحنة تحبس الإلكترونات. إذا التقط الفراغ إلكترونًا وربطه بهذا الفراغ، يصبح الإلكترون مثارًا ويمتص بشكل انتقائي طولًا موجيًا معينًا من الطاقة ليصبح ملونًا. ولذلك، يتكون مركز تلوين الإلكترون من فراغ أنيون وإلكترون مرتبط بالمجال الكهربي لهذا الفراغ.
الفلوريت الأرجواني هو لون ينتج عن مراكز الألوان الإلكترونية. الفلوريت (CaF2) تنتمي إلى النظام البلوري المتساوي القياس، حيث ينتمي كلٌّ من Ca2+ متصل باثنين F– [الشكل 3-17 (أ)]. في بعض الحالات، تكون الـ F– في الفلوريت قد يترك موضعه الطبيعي. يظهر فراغ في موضع F الأصلي– الموضع، وللحفاظ على الحياد الكهربي للبلورة، يجب أن يشغل هذا الفراغ كيان سالب الشحنة. ويصبح إلكترون من ذرة معينة في البلورة هو الكيان سالب الشحنة الذي يشغل هذا الفراغ [الشكل 3-17 (ب)]. وهذا يخلق "مركز لوني" يُعرف باسم مركز اللون الإلكتروني. في الفلوريت، تمتص مراكز الألوان الإلكترونية الضوء المرئي، مما ينتج عنه اللون الأرجواني.
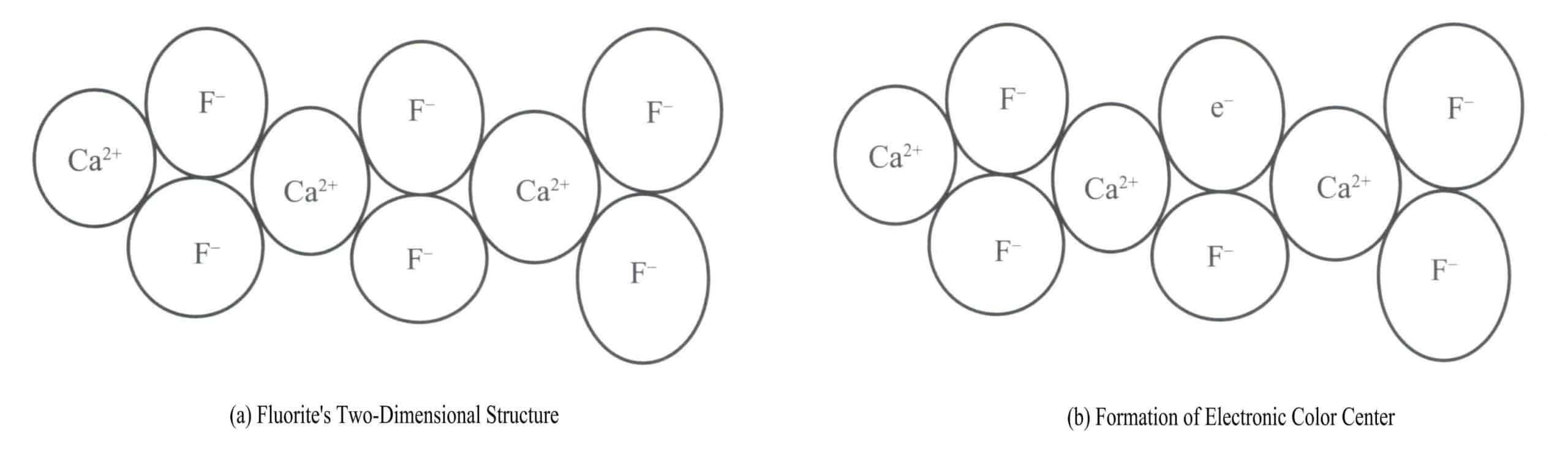
(2) مراكز ألوان الفتحات (مراكز على شكل V)
يتشكل مركز اللون الشاغرة بعوامل خارجية، حيث تخلق الكاتيونات شواغر إلكترونية. ويعني هذا أن الإلكترونات تنفصل عن مواضعها الأصلية، تاركةً وراءها إلكترونًا غير مزاوج. ويرجع سبب اللون إلى أنه عندما تتشكل شواغر الكاتيونات في البلورة، لتحقيق توازن الشحنة، تطلق الأنيونات القريبة من فراغ الكاتيون إلكترونات تحت تأثير الطاقة الخارجية، لتشكل إلكترونات غير مزاوجة تمتص الضوء المرئي وتنتج اللون. على سبيل المثال، في الماس المشععع والتوباز الأزرق، يوفر التشعيع طاقة لتنشيط الإلكترونات، مما يؤدي إلى إزاحة الأيونات أو الذرات في الشبكة، وبالتالي تشكيل عيوب بنيوية ومراكز لونية بسبب التشعيع.
من الأمثلة الكلاسيكية لمركز اللون في البلورة هو تلوين البلورة الدخانية. التركيب البلوري للكوارتز هو رباعي الأكسجين السيليكوني-الأكسجيني، حيث يكون السيليكون في حالة رباعي الإحداثيات، كما هو موضح في المخطط الهيكلي ثنائي الأبعاد في الشكل 3-18 (أ). كل 10000 سيليكون4+ ذرات لها ذرة واحدة مستبدلة بـ3+وعندما يقوم آل3+ بدائل لـ Si4+ في البلورة، آل3+ يجب أن تكون محاطة ببعض الأيونات القلوية (مثل Na+ أو H+) للحفاظ على الحياد الكهربي. ومع ذلك، غالبًا ما تكون هذه الأيونات على مسافة معينة من Al3+.
عندما يتم تشعيع الكوارتز بالأشعة السينية والأشعة γ ومصادر الإشعاع الأخرى، فإن طاقة ذرات الأكسجين المجاورة لـ Al3+ مما يسمح لأحد الإلكترونات الموجودة في الزوج بالانطلاق من موضعه الطبيعي. H+ هذا الإلكترون لتكوين H . يتسبَّب الإشعاع عالي الطاقة في تكوين O2- مع المزيد من إلكترونات التكافؤ لتحرير إلكترون، مكوِّنًا [A1O4]4- مركز اللون الشاغر، و [A1O4]4- يمتص العنقود الذري الضوء المرئي لإنتاج اللون، مكونًا الكوارتز الدخاني.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ الإلكترونات لتصبح H، وهي عديمة اللون ولا تمتص الضوء المرئي. إذا كانت كثافة الإشعاع عالية وكان هناك ما يكفي من Al3+ في البلورة، يمكن تشعيع الكوارتز إلى اللون الأسود. وبما أنه غالبًا ما يكون هناك فراغ في الموضع الذي ينبعث منه الإلكترون، يُشار إلى هذا النوع من مركز اللون باسم "مركز لون الفراغ".
خلال التاريخ الجيولوجي، تتشكل البلورة الدخانية الطبيعية في الغالب من خلال الإشعاع منخفض الجرعة طويل الأجل من المواد المشعة. ويمكن أن يؤدي التسخين إلى إزالة اللون؛ فعندما يتم تسخين هذه البلورة الدخانية إلى حوالي 400 درجة مئوية، تعود الإلكترونات المنبعثة إلى مواضعها الأصلية، وتقترن جميع الإلكترونات وتصبح الكوارتز عديمة اللون مرة أخرى؛ وإذا تم تشعيعها مرة أخرى يمكن أن تتحول إلى بلورة دخانية مرة أخرى [الشكل 3-18 (ب)].
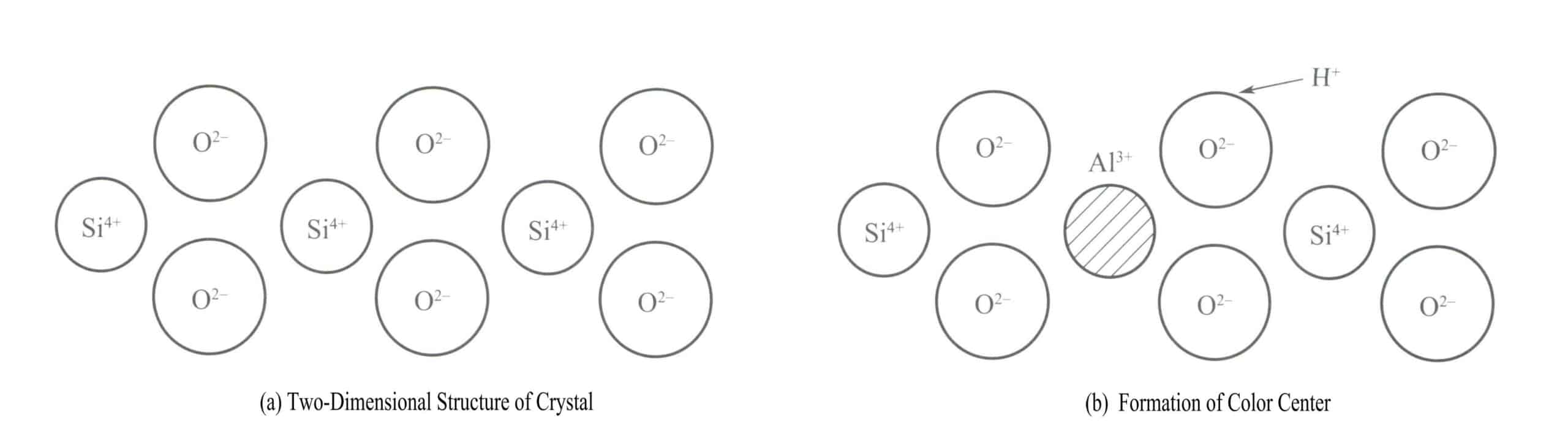
يحتوي الجمشت على نفس مراكز ألوان الفراغ، ولكن شوائبه هي الحديد بدلاً من الألومنيوم. عندما تكون شوائب Fe 3+ يستبدل بـ Si4+ في الكوارتز، تحدث التغيُّرات التالية عند تشعيعه بأشعة عالية الطاقة
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
على غرار مبدأ تكوين الكريستال الدخاني، فإنه ينتج لونًا أرجوانيًا بسبب تكوين [FeO4]4- يتمركز لون الثقب بعد تعرضه للإشعاع. وعندما يتم تسخين هذا الجمشت، يتحول لونه إلى اللون الأصفر، ويتحول إلى السترين، ومع مزيد من التسخين، يتلاشى لونه إلى عديم اللون. وعموماً، تكون درجة حرارة التسخين منخفضة نسبياً، حوالي 400 درجة مئوية. يمكن استعادة اللون الأرجواني للجمشت المعالج بالحرارة عن طريق تشعيع مراكز اللون مرة أخرى. ويتم تصنيع الجمشت الاصطناعي أيضاً استناداً إلى هذا المبدأ.
في بعض الأحجار الكريمة، يمكن أن تشكل بعض مجموعات ذرات الشوائب مراكز لونية وتظهر اللون في بعض الأحجار الكريمة. على سبيل المثال، أثناء نمو البريل وتحت الإشعاع الإشعاعي, يمكن أن يفقد إلكترونًا ليصبح، مكوِّنًا نطاق امتصاص أحمر-أخضر ينتج عنه لون أزرق. هناك العديد من مراكز الألوان في الماس، ومعظمها ناتج عن تكوين فراغات أو خلع في البنية تحت ظروف خارجية، والألوان مستقرة جدًا بشكل عام.
إن صعوبة دراسة اللون المستحث بمركز اللون عالية نسبيًا، مما يتطلب تقنيات مختلفة مثل التحليل الطيفي والرنين المغناطيسي الإلكتروني. تُظهر الأبحاث السابقة أن بعض الخصائص النموذجية للون المستحث بمركز اللون واضحة نسبيًا. يلخص الجدول 38 ألوان وأسباب اللون المستحث بمركز اللون في الأحجار الكريمة الشائعة.
الجدول 3-8 الألوان وأسباب اللون المستحث بالمركز اللوني في الأحجار الكريمة الشائعة
| أنواع الأحجار الكريمة | اللون | السبب |
|---|---|---|
| الماس | أخضر | مركز اللون GR1 الكربوني الشاغر GR1 في الماس |
| أصفر | البنية المفقودة من ركام الماس N3 | |
| برتقالي | Natoms و H3، H4 عيوب مركز الألوان H3 و H4 | |
| الكريستال | لون الدخان | الوظائف الشاغرة الناتجة عن3+ بالاستعاضة عن Si4+ المتعلقة بالإشعاع |
| أصفر | ذات صلة بـ3+، يمكن أن يتولد أيضًا عن طريق الإشعاع | |
| أرجواني | في3+ يحل محل الوظيفة الشاغرة التي أنشأها Si4+ | |
| أحجار الكوراندوم الكريمة | أصفر | اللون غير مستقر، وسبب العيوب الهيكلية غير معروف |
| توباز | أزرق | اللون مستقر، وسبب العيوب الهيكلية غير معروف |
| أصفر | اللون مستقر، وسبب العيوب الهيكلية غير معروف | |
| أحمر مائل إلى البني | اللون غير مستقر، وسبب العيوب الهيكلية غير معروف | |
| التورمالين | أحمر | ذات صلة ب Mn3+ ، يمكن أن يحدث أيضًا بسبب الإشعاع |
| بيريل | أزرق | ذات الصلة بثاني أكسيد الكربون32- ، يمكن أن يحدث أيضًا بسبب الإشعاع |
| الفلوريت | أرجواني | إلكتروني هـ- يحل محل F- لإنتاج |
يُستخدم مبدأ مراكز الألوان أيضاً لتحسين لون الأحجار الكريمة الطبيعية في تحسين الأحجار الكريمة. تستخدم معظم الطرق التشعيع لتغيير لون الأحجار الكريمة. وتتسم بعض مراكز الألوان بالثبات النسبي، بينما تتلاشى بعض أنواع الأحجار الكريمة بسرعة، مما يجعل طريقة التحسين هذه أقل أهمية بالنسبة لتلك الأحجار الكريمة. يسرد الجدول 3-9 بعض الألوان التي تنتجها مراكز الألوان، بما في ذلك مراكز الألوان المستقرة ومراكز الألوان غير المستقرة والألوان التي تنتجها عوامل أخرى محتملة.
الجدول 3-9 الألوان التي تنتجها مراكز الألوان
| مستقر في الأساس في الضوء | الجمشت، الفلوريت (أرجواني-أحمر)، ألماس مشع (أخضر، أصفر، بني، أسود، أزرق، وردي)؛ بعض التوباز الطبيعي أو المشع (أزرق) |
|---|---|
| يتلاشى بسرعة في الضوء | البريل الأخضر الليثيوم السيزيوم السيزيوم (أزرق غامق)؛ بعض التوباز المشع (بني أو أسمر)؛ الياقوت المشع (أصفر)؛ السوداليت الأرجواني المشع بالأشعة فوق البنفسجية (أحمر أرجواني) |
| الألوان الأخرى التي قد تنتجها مراكز الألوان | السيلفين (أزرق)؛ الهاليت (أزرق أو أصفر)؛ الزركون (بني)؛ الكالسيت (أصفر)؛ الباريت والسيليستين (أزرق)؛ الأمازونايت (أزرق إلى أخضر) |















