Πώς να αποτρέψετε το θάμπωμα του ασημιού και να εφαρμόσετε ηλεκτρολυτική επιμετάλλωση αργύρου
Επιμετάλλωση Ασημιού και Λύσεις κατά του Θαμπώματος για Κοσμήματα
Εισαγωγή:
Αυτό το άρθρο εξηγεί πώς να αποτρέψετε το θάμπωμα του ασημιού και των επιπλατινωμένων με ασήμι αντικειμένων, ένα συνηθισμένο πρόβλημα όπου οι επιφάνειες σκουραίνουν λόγω αντιδράσεων με θείο ή φως. Περιγράφει λεπτομερώς διάφορες αντιθαμβωτικές επεξεργασίες, συμπεριλαμβανομένων ανόργανων μεθόδων όπως η ηλεκτρόλυση χρωμικού ή κασσιτέρου, οι εμποτισμοί με οργανικές ενώσεις και οι εφαρμογές επιφανειοδραστικών ουσιών. Το κείμενο καλύπτει επίσης τι είναι η ηλεκτρολυτική επιμετάλλωση ασημιού, εξερευνώντας τόσο την επιμετάλλωση με μετατόπιση για υποστρώματα όπως τα κυκλώματα χαλκού όσο και την επιμετάλλωση με αναγωγή χρησιμοποιώντας παράγοντες όπως φορμαλδεΰδη ή υδραζίνη. Τέλος, περιγράφει γιατί και πώς να αναλύσετε βασικά συστατικά σε διαλύματα επιμετάλλωσης με κυάνιο, όπως ιόντα αργύρου και ελεύθερο κυάνιο.

Πίνακας περιεχομένων
Τμήμα Ι Πρόληψη Θαμπώματος Ασημιού Θεραπεία
Λόγω της υψηλής αντιδραστικότητας της επιφάνειας επιμετάλλωσης Ag, η επιμεταλλωμένη με άργυρο επιφάνεια είναι επιρρεπής σε αποχρωματισμό όταν έρχεται σε επαφή με διαβρωτικά μέσα (όπως H2S, SO2Το φως προσδίδει επίσης περίσσεια ενέργειας στην επιφάνεια επιμετάλλωσης, προωθώντας τον ιονισμό του Ag και την αντίδραση μεταξύ του Ag και του διαβρωτικού μέσου.
Ο Πίνακας 2-28 δείχνει τις επιδράσεις του μήκους κύματος του φωτός και του χρόνου έκθεσης στον αποχρωματισμό του Ag. Ο Πίνακας 2-29 δείχνει τις επιδράσεις του χρόνου έκθεσης στο χρώμα και τη χημική σύνθεση.
Πίνακας 2-28 Επίδραση του μήκους κύματος του φωτός και του χρόνου έκθεσης στην αλλαγή χρώματος του Ag
| Ακτίνα | Χρόνος έκθεσης/ώρα | ||||
|---|---|---|---|---|---|
| 6 | 12 | 18 | 24 | 48 | |
| 2527Å | Καμία αλλαγή στο χρώμα | Κίτρινες κηλίδες | Κιτρινωπό καφέ | Καφέ-μαύρο | Καφέ |
| 3650Å | Καμία αλλαγή στο χρώμα | Καμία αλλαγή στο χρώμα | Καμία αλλαγή στο χρώμα | Κίτρινο | - |
| Ηλιακό φως | Καμία αλλαγή στο χρώμα | Καμία αλλαγή στο χρώμα | Καμία αλλαγή στο χρώμα | Κίτρινες κηλίδες | - |
Πίνακας 2-29 Επίδραση του χρόνου έκθεσης στο χρώμα και τη χημική σύνθεση της επιχρυσωμένης επιφάνειας
| 2537 Å Χρώμα έκθεσης φωτός/ώρα | 6 | 12 | 18 | 24 | 48 |
|---|---|---|---|---|---|
| Χρώμα | Ασημένιο | Κίτρινο | Κιτρινωπό καφέ | Καφέ μαύρο | Μαύρο |
| Κύρια χημική σύνθεση | Ag (μέταλλο) | Ag2Ο+ΑγΟ | Ag2Ο+ΑγΟ | AgO+Ag (Εξαιρετικά λεπτό) | Ag (Εξαιρετικά λεπτό) |
Από αυτά τα αποτελέσματα, μπορεί να φανεί ότι τα προϊόντα αποχρωματισμού είναι σουλφίδια, οξείδια, χλωρίδια ή σωματίδια αργύρου. Το χρώμα της επιμετάλλωσης Ag μετά τον αποχρωματισμό ποικίλλει ανάλογα με τη χημική σύνθεση. Αυτός ο τύπος αλλαγής χρώματος όχι μόνο επηρεάζει την διακοσμητική εμφάνιση της επιμετάλλωσης αργύρου, αλλά αυξάνει και την ηλεκτρική αντίσταση της επιμετάλλωσης Ag, η οποία είναι επιζήμια για τις ηλεκτρικές ιδιότητες της επιμετάλλωσης αργύρου.
Από αυτούς τους μηχανισμούς αποχρωματισμού του στρώματος επιμετάλλωσης Ag, μπορεί να φανεί ότι είναι απαραίτητο μόνο να αποφευχθεί η επαφή μεταξύ της επιφάνειας επιμετάλλωσης και του οξυγόνου, του φωτός και των διαβρωτικών μέσων για να αποφευχθεί ο αποχρωματισμός του στρώματος επιμετάλλωσης αργύρου. Ταυτόχρονα, ο σχηματισμός μιας πυκνής ουσίας (στρώμα μεμβράνης) στην επιφάνεια που μπορεί να απορροφήσει υπεριώδεις ακτίνες θα πρέπει να έχει ανασταλτική επίδραση στον αποχρωματισμό του στρώματος επιμετάλλωσης.
Μεταξύ των παραδοσιακών μεθόδων για την πρόληψη του αποχρωματισμού των στρωμάτων επιμετάλλωσης Ag είναι οι μέθοδοι με ανόργανες ενώσεις, οι μέθοδοι με οργανικές ενώσεις, οι μέθοδοι με επιφανειοδραστικές ουσίες και η συνδυασμένη χρήση αυτών των μεθόδων.
1. Μέθοδος επεξεργασίας ανόργανων ενώσεων
Για να συγκριθούν τα αποτελέσματα διαφορετικών αντιθαμβωτικών επεξεργασιών, τα δοκίμια επιμεταλλώθηκαν με 2~3μm Ag και στη συνέχεια εμβαπτίστηκαν σε διάλυμα πολυθειούχου αμμωνίου [(NH4)2SX] σε συγκέντρωση 0,2% για ένα ορισμένο χρονικό διάστημα. Για την αξιολόγηση χρησιμοποιήθηκε οπτικός έλεγχος. Όταν ο οπτικός έλεγχος ήταν αδύνατος, χρησιμοποιήθηκε ψηφιακός μετρητής στιλπνότητας για τη μέτρηση της κατοπτρικής ανακλαστικότητας και υπολογίστηκε η διαφορά △ πριν και μετά την εμβάπτιση στο διάλυμα πολυθειούχου αμμωνίου. Ταυτόχρονα, για δοκιμές έκθεσης σε εσωτερικούς χώρους, χρησιμοποιήθηκε επίσης μετρητής στιλπνότητας για τη μέτρηση.
Ως αντιθαμβωτική επεξεργασία για τον Ag, δοκιμάστηκαν μεταλλικές μεμβράνες ή μεμβράνες οξειδίων μετάλλων με την ίδια απόχρωση με τον Ag, όπως In, Zn, Cd, Cr, Pd, Rh, Sn, Be, Al, Th και Zr. Μεταξύ αυτών, η ηλεκτρολυτική επεξεργασία χρωμικού άλατος παρουσίασε την πιο εξαιρετική αντιθαμβωτική λειτουργία και εφαρμόστηκε ευρέως. Δεύτερον, το Rh και το Be είναι επίσης μεταξύ των επιλογών.
(1) Επεξεργασία πολύτιμων μετάλλων
Η ηλεκτρολυτική επιμετάλλωση κραμάτων Rh και Pd πραγματοποιήθηκε υπό βέλτιστες συνθήκες, ακολουθούμενη από πειράματα μεταβολών τόνου και αντοχής στον αποχρωματισμό. Τα αποτελέσματα παρουσιάζονται στον Πίνακα 2-30. Η κατοπτρική ανακλαστικότητα του Rh είναι 70%, ενώ η κατοπτρική ανακλαστικότητα του κράματος (Pd80:Ni20) είναι περίπου 57%. Αν και τα πάχη της επιμετάλλωσης διαφέρουν, μπορεί να υπάρχει κάποια συσχέτιση. Το πάχος επιμετάλλωσης του Rh είναι 0,1μm και το πάχος επιμετάλλωσης του Pd-Ni είναι 0,3μm. Όταν το πάχος επιμετάλλωσης άλλων μετάλλων σε Ag αυξάνεται, το ασημί χρώμα του υποκείμενου στρώματος αργύρου εξαφανίζεται. Ωστόσο, συγκρίνοντας οπτικά τον τόνο, τη φωτεινότητα και τις σχετικές τιμές της κατοπτρικής ανακλαστικότητας, διαπιστώθηκε ότι όταν η κατοπτρική ανακλαστικότητα είναι 80%, η διαφορά από το ασημί χρώμα γίνεται εμφανής και το 70% είναι το όριό της. Κάτω από αυτό, το ασημί χρώμα εξαφανίζεται και αλλάζει σε διαφορετικό χρώμα μετάλλου. Επομένως, από την άποψη του τόνου, ένα πάχος επιμετάλλωσης Rh κάτω από 0,1 μm είναι πιο κατάλληλο. Ωστόσο, η αντοχή του στον αποχρωματισμό είναι ανεπαρκής, ενώ το στρώμα επιμετάλλωσης από κράμα Pd-Ni είναι παχύτερο και έχει καλή αντοχή στον αποχρωματισμό. Η χρήση πολύτιμων μετάλλων σημαίνει αυξημένο κόστος, αλλά προσφέρουν καλή αντοχή σε φάρμακα και φθορά. Όσο καλύτερη είναι η αντοχή στον αποχρωματισμό, τόσο περισσότερο εξαφανίζεται το αρχικό ασημένιο χρώμα. Ως εκ τούτου, η βελτίωση της αντοχής στον αποχρωματισμό χωρίς να αλλάξει ο τόνος και η φωτεινότητα της επιμετάλλωσης αργύρου είναι πολύ δύσκολη.
(2) Επεξεργασία κασσιτέρου και κραμάτων κασσιτέρου
Τα κράματα Cu και Sn ονομάζονται κράματα καθρέφτη. Όταν η περιεκτικότητα σε Sn είναι πάνω από 60%, το χρώμα τους είναι ασημί-λευκό και η κατοπτρική ανακλαστικότητα είναι επίσης υψηλή, με καλή αντοχή στη διάβρωση. Ως εκ τούτου, έχουν μελετηθεί από την αρχαιότητα και χρησιμοποιούνται ως επιφάνειες καθρέφτη σε ανακλαστικά τηλεσκόπια. Όταν χρησιμοποιούνται ως επιστρώσεις κατά της θαμπάδας από άργυρο, έχουν αρκετά καλή απόδοση κατά της θαμπάδας για 5~6 ώρες. Ωστόσο, η κατοπτρική ανακλαστικότητα μειώνεται σε περίπου 65%, χάνοντας σαφώς το ασημί χρώμα. Η χρηστικότητα των κραμάτων καθρέφτη εξαρτάται από τον βαθμό απόχρωσης. Αν και φθηνότερα από τα πολύτιμα μέταλλα, όταν το πάχος της μεμβράνης αυξάνεται σε αρκετές χιλιάδες angstrom, προκύπτει μια πιθανή διαφορά μεταξύ του πολύτιμου μετάλλου Ag και του κράματος Cu-Sn, η οποία μπορεί να προκαλέσει προβλήματα αντοχής στη διάβρωση.
Εκτός από την επιμετάλλωση με κράμα Sn, το μέταλλο Sn ή οι ενώσεις Sn που καθιζάνουν με ηλεκτρολυτικές ή εμποτιστικές επεξεργασίες 50~100Å μπορούν επίσης να έχουν αντοχή στο θάμπωμα και βελτιωμένη αντοχή στις καιρικές συνθήκες. Ως επεξεργασία θάμπωσης, μπορεί να διατηρήσει τη σταθερότητα της αντίστασης επαφής των επαφών για μεγάλο χρονικό διάστημα.
Τα πειραματικά αποτελέσματα παρουσιάζονται στον Πίνακα 2-30. Σε σύγκριση με τα αλκαλικά και όξινα διαλύματα, τα μέρη που έχουν υποστεί επεξεργασία με όξινα διαλύματα έχουν ένα ομιχλώδες λευκό ίζημα και δεν μπορούν να χρησιμοποιηθούν για διακοσμητικούς σκοπούς. Αντίθετα, τα μέρη που έχουν υποστεί επεξεργασία με αλκαλικά διαλύματα και ηλεκτρολυτικές επεξεργασίες δεν παρουσιάζουν προβλήματα βραχυπρόθεσμα.
Πίνακας 2-30 Αντοχή ανόργανων ενώσεων στον αποχρωματισμό σε επιπλατινωμένες επιφάνειες
| Σειριακός αριθμός | Σύνθεση διαλύματος | Συνθήκες επεξεργασίας | Προϋπόθεση για την εμφάνιση του εμφανούς χρώματος | Σημείωμα |
|---|---|---|---|---|
| 1 |
PNP (Νισίν Κασέι, Ιαπωνία) Επιμετάλλωση κράματος Pd-Ni |
DK lA/dm2 Θερμοκρασία δωματίου 1 λεπτό
|
Πάνω από 6 ώρες | Απώλεια ασημένιου χρώματος, κακή CN- αντίσταση |
| 2 |
Pewter (Daiya Shokai) Επιμετάλλωση κράματος Cu-Sn
|
3V 55℃ δεκαετία του '40
|
Πάνω από 6 ώρες | Απώλεια ασημί χρώματος |
| 3 |
Na2Cu(CN)3 24g/L Na2SnO3 90g/L Ελεύθερο NaCN 16g/L ΝαΟΗ
|
Dk 2A/dm2 60℃ δεκαετία του '30
|
Πάνω από 6 ώρες | Απώλεια ασημί χρώματος, καλύτερη από το ασημί χρώμα των 1 και 2. |
| 4 |
Na2SnO3 90g/L CH3COONa 0g/L, 5g/L, 10g/L
|
DK 0,5 A/dm2 Θερμοκρασία δωματίου Δεκαετία του 15-90
|
10-20 δευτερόλεπτα | Προσθήκη CH3Το COONa μπορεί να σταθεροποιήσει το διάλυμα και όσο μεγαλύτερος είναι ο χρόνος ηλεκτρόλυσης, τόσο πιο σταθερό είναι, αλλά θα χάσει το ασημί χρώμα του. |
| 5 |
SnCl2 20g/L 0.025NHCl 50mL/L
|
Θερμοκρασία δωματίου 1 λεπτό
|
10 λεπτά | |
| 6 |
SnCl2 20g/L 0,025NHCl 50mL/L
|
DK 0,1 〜 2A/dm2 Θερμοκρασία δωματίου, 10 δευτερόλεπτα
|
10 λεπτά | Λευκό |
|
Θερμοκρασία δωματίου, 1 λεπτό, 10 λεπτά |
Ελαφρώς κιτρινισμένο | |||
| 7 | Φθοροβορικό κασσίτερο 3% |
DK 0,1 ~ 2 A/dm2 Θερμοκρασία δωματίου, 10 δευτερόλεπτα
|
- | Λευκό |
| Θερμοκρασία δωματίου, 1 λεπτό, 10 λεπτά | 10 λεπτά | Ελαφρώς κίτρινο | ||
| 8 |
Θειικός κασσίτερος 20g/L Ιωδικό οξύ 30mL/L
|
DK 0,1 〜 2 A/dm2 Θερμοκρασία δωματίου, 10 δευτερόλεπτα
|
- | Λευκό |
| 9 |
Φθοροβορικός κασσίτερος 20mL/L Φθορικό οξύ 30mL/L Φθοροβορικό οξύ 20g/L
|
Θερμοκρασία δωματίου, 1 λεπτό, 10 λεπτά DK 0,1 〜2 A/dm2 Θερμοκρασία δωματίου, 10 δευτερόλεπτα |
10 λεπτά - |
Ελαφρώς κιτρινωπό Λευκό
|
| Θερμοκρασία δωματίου, 1 λεπτό, 10 λεπτά | 10 λεπτά | Ελαφρώς κίτρινο | ||
| 10 |
BeSO4 , 4Ω2O 2g/L pH = 5,7-5,8
|
DK 0,007 A/dm2 Θερμοκρασία δωματίου 3-10 λεπτά
|
Πάνω από 1 ώρα | |
| 11 |
BeSO4 , 4Ω2O 2g/L pH = 5,8
|
1 〜2. 4V 20 δευτ. ~ 4 λεπτά
|
20 λεπτά | |
| 12 | EverShine S (Tamura Chemical) |
6,5V Θερμοκρασία δωματίου δεκαετία του '90
|
15 λεπτά | |
| 13 |
K2CrO4 15g/L ΝαΟΗ 30g/L
|
2〜6V Θερμοκρασία δωματίου 15-120 δευτερόλεπτα
|
10-30 δευτερόλεπτα | Όσο μεγαλύτερη είναι η διάρκεια της ηλεκτρόλυσης, τόσο το καλύτερο |
| 14 |
K2CrO4 30g/L ΝαΟΗ 40g/L
|
DK 4A/dm2 Θερμοκρασία δωματίου 30-40 δευτερόλεπτα
|
Λευκή ομίχλη Χωρίς ασημί χρώμα
|
|
| 15 |
K2CrO4 30g/L ΝαΟΗ 40g/L Θέρμανση 20 ωρών
|
Λευκή ομίχλη Χωρίς ασημί χρώμα
|
||
| 16 |
Al2(SO4)3 4g/L Οξαλικό αμμώνιο 2g/L pH = 5,8
|
DK 0,06A/dm2 Θερμοκρασία δωματίου 30 δευτερόλεπτα 〜1 λεπτό
|
20-30s | Την ίδια στιγμή όπως και χωρίς θεραπεία |
| 17 | Ανθρακικό νάτριο | |||
| 18 |
Na2SnO3 8,5 g/L CH3COONa 5g/L (Αρ. 4)
|
DK 0,5A/dm2 15-30s Θερμοκρασία δωματίου
|
Πάνω από 6 ώρες | |
|
K2CrO4 15g/L ΚΟΗ 30g/L (Αρ. 13)
|
2〜3V δεκαετία του '30 Θερμοκρασία δωματίου
|
|||
| 19 |
K2CrO4 15g/L ΚΟΗ 30g/L K2CO3 50g/L
|
6V 15-60
|
10 ~ 30 λεπτά |
(3) Επεξεργασία με βηρύλλιο
Η προσκόλληση μιας μεμβράνης οξειδίου του βηρυλλίου σε Au, Cu και ορείχαλκο ως επεξεργασία αλλαγής χρώματος μπορεί να επιτύχει καλό αποτέλεσμα. Η αρχή που χρησιμοποιείται με αυτή τη μέθοδο είναι: το ισοηλεκτρικό σημείο του υδροξειδίου του βηρυλλίου είναι pH=5,8 και μπορεί να συμβεί η ακόλουθη ηλεκτρολυτική αντίδραση:
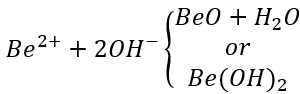
(4) Επεξεργασία αλουμινίου
Υπάρχουν αναφορές για σχηματισμό φιλμ οξειδίου παρόμοιο με το Be. Επιπλέον πειράματα δεν έδειξαν διαφορά μεταξύ επεξεργασμένων και μη επεξεργασμένων δειγμάτων και δεν μπόρεσε να σχηματιστεί φιλμ οξειδίου.
(5) Επεξεργασία χρωμικών αλάτων
Η επιμετάλλωση με ασήμι είναι η πιο συνηθισμένη μέθοδος για την αντιθαμπωτική επεξεργασία της επιμετάλλωσης ορείχαλκου. Υπάρχουν δύο μέθοδοι επεξεργασίας χρωμίου: η καθοδική ηλεκτρόλυση και η εμβάπτιση, αλλά η μέθοδος της καθοδικής ηλεκτρόλυσης είναι πολύ ανώτερη.
Τα πρόσθετα που χρησιμοποιούνται στους ηλεκτρολύτες χρωμίου περιλαμβάνουν: K2CO3, Na2CO3, KCN, NaS2O3, KCNS, NaCl, KI, EDTA, κ.λπ. Μεταξύ αυτών, το K2CO3 Τα πειραματικά αποτελέσματα έδειξαν ότι μπορεί επίσης να λειτουργήσει ως αγώγιμο άλας, μειώνοντας έτσι τον χρόνο επεξεργασίας της ηλεκτρόλυσης σε σύγκριση με την περίπτωση που δεν προστίθεται. Οι επιδράσεις των άλλων προσθέτων δεν έδειξαν σημαντικές διαφορές.
Το μειονέκτημα της επεξεργασίας με χρωμική ηλεκτρόλυση είναι ότι η μεμβράνη έχει χαμηλή αντοχή στην υπεριώδη ακτινοβολία και θα γίνει καφέ μετά από μεγάλο χρονικό διάστημα.
2. Επεξεργασία με Οργανικές Ενώσεις και Επιφανειοδραστικές Ουσίες
Πίνακας 2-31 Πείραμα κατά του αποχρωματισμού οργανικών ενώσεων
| Κατηγοριοποίηση | Σειριακός αριθμός | Οργανικές ενώσεις | Φυσικές ιδιότητες | Διαλυτότητα | Συνθήκες επεξεργασίας | Εμφάνιση | Υδροφοβικότητα | Επίδραση κατά του αποχρωματισμού |
|---|---|---|---|---|---|---|---|---|
| Αλειφατική αμίνη | 1 |
Αιθυλαμίνη (υδατικό διάλυμα 70%) CH3CH2Νιου Χάμσαϊρ2
|
Mw 45. 09 d15 0. 6892 Σημείο τήξης 83,3℃ Σημείο βρασμού 16℃ |
(Υδατικές) αλκοόλες Αιθέρας
|
0,1mol/L (0,65mL/L) 0,01mol/L (6,5mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
pH 10〜11 Άχρωμο Διαφανές O |
X | X |
| 2 |
Δωδεκυλαμίνη CH2(Χ.Ε.)2)11Νιου Χάμσαϊρ2 |
Mw 18. 5 Σημείο τήξης 25℃ Σημείο βρασμού 247℃ |
Ακετόνη (Αιθανόλη) |
0,1 mol/L (18,5 g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές Λεκές νερού |
X | X | |
| 3 |
Τριβουτυλαμίνη (Χ.Ε.)3CH2CH2CH2)3N |
Mw 185 δ 0. 7782 Σημείο βρασμού 216,5℃ |
(Αιθανόλη) Αιθέρας
|
0,1mol/L (24mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
X | X | |
| Αρωματικές αμίνες | 4 | Ο-τολουιδίνη |
Mw 107. 16 d20 0. 9989 Σημείο βρασμού 199,7℃ |
Νερό 1. 5(25) (Αιθανόλη) Αιθέρας |
0,1mol/L (24mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Κοκκινωπό καφέ διαφανές O |
X | X |
| 5 | Διφαινυλαμίνη |
Mw 169.23 δ 1.159 Σημείο βρασμού 302℃ |
(Αιθανόλη) 56 Αιθέρας |
0,1 mol/L (17 g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο διαφανές Λεκές νερού |
X | X | |
| Διαμίνες, Πολυαμίνες | 6 | H2Ν(ΧΗ2)2Νιου Χάμσαϊρ2 |
Mw 45.09 d35 0.892 Σημείο τήξης 8,5℃ Σημείο βρασμού 117℃ |
(νερό) Αιθανόλη |
0,1mol/L (6,7mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 10〜11 O |
X | X |
| Διαμίνη, πολυαμίνη | 7 |
Διαιθυλενοτριαμίνη H2 Ν(ΧΗ2 )2 NH(CH2 )2 Νιου Χάμσαϊρ2 |
Mw 103 Σημείο βρασμού 208℃ |
(νερό) Αιθανόλη |
0,1mol/L (10mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 10〜11 O |
X | X |
| 8 |
Τριαιθυλενοτετραμίνη H2 Ν(ΧΗ2 )2 NH(CH2 )2 Νιου Χάμσαϊρ2 (Χ.Ε.)2 )2 Νιου Χάμσαϊρ2 |
Mw 146 Σημείο τήξης 208℃ Σημείο βρασμού 174℃ |
(νερό) |
0,1mol/L (15mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 10〜11 O |
X | X | |
| Αμινοαλκοόλες | 9 |
Τριαιθυλενοτετραμίνη H2Ν(ΧΗ2)2NH(CH2)2 NH(CH2)2Νιου Χάμσαϊρ2 |
Mw 189 | (νερό) |
0,1mol/L (19mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 10〜11 O |
X | X |
| 10 |
Αιθανολαμίνη HO(CH2)2Νιου Χάμσαϊρ2 |
Mw 61.09 d27 1.0111 Σημείο βρασμού 171℃ |
(νερό) Αιθανόλη |
0,01mol/L (0,61mL/L) 0,1mol/L (6,1mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9-10 O |
X | X | |
| 11 |
Διαιθανολαμίνη (HOCH2CH2)2Νιου Χάμσαϊρ |
Mw 105.14 d20 1.0916 Σημείο τήξης 28℃ Σημείο βρασμού 268℃ |
(νερό) Αιθανόλη |
0,01mol/L (0,96mL/L) 0,1mol/L (9,6mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9-10 O |
O | X | |
| 12 |
Τριαιθανολαμίνη (HOCH2CH2)3Νιου Χάμσαϊρ |
Mw 149.19 d20 1.124 Σημείο τήξης 21,2℃ Σημείο βρασμού 227℃ |
(νερό) Αιθανόλη |
0,01mol/L (1,3mL/L) 0,1mol/L (13mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9-10 O |
O | X | |
| 13 |
2Ν-Διαιθυλαμίνη (Χ.Ε.)2)2NCH2CH2Ω |
Mw 93.1 Σημείο βρασμού 39,5℃ |
(νερό) |
0,1mol/L (0,89mL/L) 0,01mol/L (8,9mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9-10 O |
O | X | |
| 14 | 2-Αμινο-2-αιθυλο-1,3-προπανοδιόλη | Mw 105 | (νερό) |
0,01mol/L (1,1g/L) 0,1mol/L (11g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9-10 O |
O | X | |
| Αμίδιο | 15 | Ακεταμίδιο |
Mw 59.07 δ 1.159 Σημείο τήξης 52,62℃ Σημείο βρασμού 221℃
|
(νερό) Αιθανόλη |
0,1mol/L(5,1mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
△ | X |
| 16 | Ακρυλαμίδιο |
Mw 71.1 δ 1.122 Σημείο τήξης 85℃ |
(νερό) Αιθανόλη Αιθέρας Τριχλωρομεθάνιο
|
0,1mol/L(7,1mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
△ | X | |
| 17 | Βενζυλαμίνη |
Mw 121.14 δ 1.341 Σημείο τήξης 128℃ Σημείο βρασμού 290℃ |
(νερό) Αιθανόλη
|
0,1 mol/L (12 g/L) 30℃ Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
O | X | |
| Οξίμη | 18 | Οξίμη βουτανοδιόνης |
Mw116.12 Σημείο τήξης 240℃ |
(Αιθανόλη) Αιθέρας (Νερό) |
0,01mol/L (0,12g/L) 0,001mol/L (1,2gmL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
X | X |
| 19 | Οξίμη βενζοϋδρίνης |
Mw227 Σημείο τήξης 154℃ |
(Αιθανόλη) (Αμμωνία)
|
0,01mol/L (0,23g/L) 0,001mol/L (2,3g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές △ |
X | X | |
| Πυριδίνη | 20 | Πυριδίνη |
Mw 79.10 d20 0.977 Σημείο βρασμού 115,5℃ |
(νερό) Αιθανόλη |
0,001mol/L (0,1mL/L) 0,1mol/L (8mL/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές O |
X | X |
| Κινολίνη | 21 | Κινολίνη |
Mw 127.16 d20 0.938 Σημείο τήξης -15℃ Σημείο βρασμού 238℃ |
Ζεστό νερό, αραιό οξύ, αιθανόλη, αιθέρας, διθειάνθρακας (6mol/L HCl) 2~20mol/L |
0,1% (1g/L) 1% (10g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 2~4 O |
O | X |
| 22 | Καρβοξυκινολίνη |
Mw 145 Σημείο τήξης 75~76℃ |
Αιθανόλη, ακετόνη, τριχλωρομεθάνιο, βενζόλιο (6mol/L HCl) 2~20mol/L |
0,1% (1g/L) 1% (10g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Κίτρινο Διαφανές pH 2~4 O |
X | X | |
| Κινολίνη | 23 | Οξίμη βουτανοδιόνης | Mw 256 |
Ανόργανο οξύ (6mol/L HCl) 40mol/L Αιθανόλη |
0,1% (1g/L) 1% (10g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Κίτρινο Διαφανές pH 10~11 O |
X | X |
| Διαζο ενώσεις | 24 | p-Αιθοξυ-2,4-διαμινοαζωβενζόλιο | Mw 256 |
Ανόργανο οξύ (6mol/L HCl) 40mol/L Αιθανόλη |
0,1% (1g/L) 1% (10g/L) Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Κόκκινο Διαφανές O |
O | X |
| Υδροξυκαρβοξυλικό οξύ | 25 | Δεψικό οξύ | Κιτρινωπό λευκό, ανοιχτό χρώμα, σκόνη |
(νερό) Αιθανόλη Ακετόνη |
0.1% 0.1% 5% |
Άχρωμο Διαφανές pH 6 Κίτρινο διαφανές pH 4 Κιτρινωπό καφέ διαφανές pH 2 |
X | X |
| Θειουρία | 26 | 1-ακετυλο-2-θειουρία |
Mw 118.16 Σημείο τήξης 165℃ |
(νερό) Αλκοόλ |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 7 O |
O | X |
| Θειουρία | 27 | Αμινοθειουρίες |
Mw 95.6 Σημείο τήξης 81~183℃ |
(6mol/L HCl) 50mL/L |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 1 O |
X | X |
| 28 | Διθιζόνη | Mw 256 |
(Τριχλωρομεθάνιο) Τετραχλωριούχος άνθρακας |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Μπλε λεκές νερού Γίνεται κίτρινο |
O | X | |
| Μονοσακχαρίτης | 29 | Ασκορβικό οξύ (βιταμίνη C) |
Mw 176 Σημείο τήξης 190~192℃ |
(νερό) |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 1 O |
X | X |
| Ιμιδαζόλες | 30 | 1-ακετυλο-2-θειουρία |
Mw 155 Αποσύνθεση 287~288℃ |
Μεθανόλη Νερό 45mL
|
1g/L, 10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 1 O |
X | X |
| 31 | 2-Επταδεκυλιμιδαζόλη |
Μεθανόλη 55mL Νερό 45mL Διάλυση Αλκοόλη, οξύ |
1g/L, 10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Λευκή ανάρτηση Ανώμαλο Λευκή προσκόλληση |
O | O | ||
| Βενζιμιδαζόλες | 32 | 2-μερκαπτοπυριδίνη |
Mw 150 Σημείο τήξης 301~302℃ |
Μεθανόλη 15mL Νερό 45mL Ζεστό νερό Αιθανόλη ΝαΟΗ |
1g/L, 10g/L Θερμοκρασία δωματίου, 60℃ 20 λεπτά, 60 λεπτά |
Άχρωμο διαφανές O |
O | X |
| Τριαζόλες | 33 | 3-Αμινο-1,2,3-τριαζόλη |
Mw 159 Σημείο τήξης 159℃ |
(νερό) Αιθανόλη Τριχλωρομεθάνιο |
Θερμοκρασία δωματίου, 60℃ 1 λεπτό, 10 λεπτά, 60 λεπτά |
O | - | X |
| Βενζοτριαζόλη | 34 | Βενζοτριαζόλη |
Mw 119.13 Σημείο τήξης 99℃ |
Ζεστό νερό Αλκοόλ |
12g/L, pH 6 60℃ 1 λεπτό, 3 λεπτά, 10 λεπτά
|
Άχρωμο Διαφανές O |
- | X |
| Τριαζίνη | 35 | Τριαιθυλενοδιαμίνη |
Mw 140 Εξάχνωση πάνω από 230°C |
(νερό) Ενυδρο (ΣΟ2)2N Τριχλωρομεθάνιο Αλκοόλ |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 8 O |
X | X |
| Οξαζόλη | 36 | 2-οξοβενζαζόλη |
Mw 1151 Σημείο τήξης 143,2℃ |
Αμμωνία 6mol/L αμμωνία 200mL/L Οξικό οξύ Αιθέρας |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 10 O |
O | X |
| (Οξο)ζίνζ | 37 | Μορφολίνη |
Mw 87.12 d13 1.0007 Σημείο βρασμού 128℃ |
(νερό) Αλκοόλ Αιθέρας |
10g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Άχρωμο Διαφανές pH 9~10 O |
X | X |
| Θειαζόλη | 38 | Ορτανίν |
Mw 264 Σημείο τήξης 200~246℃ (Αποσύνθεση) Κόκκινοι κρύσταλλοι που μοιάζουν με βελόνες
|
Ισχυρά οξέα Πυκνός Τριχλωρομεθάνιο Αιθέρας Βενζόλιο (ακετόνη)
|
1g/L Θερμοκρασία δωματίου, 20 λεπτά, 60 λεπτά |
Κόκκινο διαφανές (Κόκκινο ίζημα) Καφέ λεκές νερού |
O | X |
| Βενζοθειαζόλη | 39 | Βενζοθειαζόλη |
Mw 135.39 d12 1.2349 Σημείο βρασμού 231℃ |
(Αιθανόλη) Αιθυλαιθέρας |
1g/L Θερμοκρασία δωματίου, 3 λεπτά, 60 λεπτά |
Κοκκινωπό καφέ Διαφανής O |
△ | X |
| 40 | 2-υδρόφοβη βενζοθειαζόλη |
Mw 167 Σημείο τήξης 177℃ |
Αιθανόλη Αιθυλαιθέρας Βενζόλιο Οξικό οξύ Ανθρακικό κάλιο Υδροξείδιο του καλίου Υδροξείδιο του νατρίου 2g/L |
1g/L Θερμοκρασία δωματίου, 3 λεπτά, 60 λεπτά |
Λευκό θολό pH 10 O |
X | O | |
| Ναφθαλίνες | 41 | παράγοντας εξοικονόμησης ναφθαλίνης |
Mw 217 Σημείο τήξης 109,5℃ |
Νερό (20℃) 0,01 g/L |
0,2 g/L (Κατανέμιση) Θερμοκρασία δωματίου, 2 λεπτά, 10 λεπτά, 30 λεπτά |
O | - | X |
| Ισοακετόνη |
10g/L Θερμοκρασία δωματίου, 10 λεπτά, 60 λεπτά |
Κίτρινο διαφανές Λεκές νερού
|
O | O | ||||
|
Ισοακετόνη 50% Νερό 50% |
5g/L Θερμοκρασία δωματίου, 10 λεπτά, 60 λεπτά |
Κίτρινο διαφανές Λεκές νερού
|
O | O |
Πίνακας 2-32 Πείραμα κατά του αποχρωματισμού επιφανειοδραστικών ουσιών
| Σειριακός αριθμός | Όνομα (όνομα εταιρείας) | Κατάσταση | Συγκέντρωση | Συνθήκες επεξεργασίας | Εμφάνιση | Υδροφοβικότητα | Επίδραση αναστολής | Παρατηρήσεις |
|---|---|---|---|---|---|---|---|---|
| 1 | Αντισκωριακός παράγοντας MC- 501 (Ιαπωνικό γράσο λιονταριού) |
Ανοιχτό κόκκινο διαφανές, d 1,06 pH 8,0-8,5 |
2%,10% | Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά | O | O | Ag: x | |
| 2% | Θερμοκρασία δωματίου 15 δευτερόλεπτα, 10 λεπτά | O | O | Cu: Βύθιση σε νερό βρύσης X, δοκιμή έκθεσης △ | 15 δευτερόλεπτα καλύτερα | |||
| 2 | Enajiko-ru CNS (Ιαπωνικό Λιοντάρι Γράσο) |
Αμφοτερικός pH 8-9 |
1% | Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά (Ag) 15 δευτερόλεπτα, 10 λεπτά (Cu) | O | O | Ag:x Cu:Βύθιση σε νερό βρύσης X, δοκιμή έκθεσης: | 1% 15s καλό |
|
15% Βενζοσουλφονικό νάτριο 15% (Ουδέτερο)
|
Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά (Ag) 15 δευτερόλεπτα, 10 λεπτά (Cu) | Καφέ, λευκή πρόσφυση ιζήματος | O | |||||
|
10% Πυροφωσφορικό κάλιο 5% (Αλκαλικό) |
Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά (Ag) 15 δευτερόλεπτα, 10 λεπτά (Cu) |
Λευκή θολότητα O |
O | |||||
| 3 | Ripa-ru OH- 104P (γράσο Japan Lion) | 0.1% | Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά |
Άχρωμο και διαφανές O Κιτρινωπό-λευκό θολό O
|
O △
|
Ag: x | ||
| 1% | ||||||||
| 10% | ||||||||
| 4 | Dyuomin CD (Japan Lion Grease) | 0.1% | Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά |
Λευκό θολό O Κίτρινες λασπώδεις ραβδώσεις O
|
O | Ag: x | ||
| 1% | ||||||||
| 10% | ||||||||
| 5 | Dyuomin CDA-50 (Lion Grease, Ιαπωνία) | 0.1% | Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά |
Άχρωμο και διαφανές O
|
△ O
|
Ag: x | Ελαφρώς καλύτερα στα 60 λεπτά | |
| 1% | ||||||||
| 10% |
Θολό κίτρινο O |
|||||||
| 6 | FC-98 (Kanto Chemical, Ιαπωνία) | Ανιονική λευκή σκόνη που περιέχει φθόριο |
0.1% 1%
|
Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά |
Άχρωμο και διαφανές pH 5~7 Στικτά σημάδια
|
O | ×(Ag) | |
| 7 | FC-134 (Kanto Chemical, Ιαπωνία) | Σκόνη τσαγιού-καφέ με ιόντα οξυγόνου που περιέχει φθόριο |
0.1% 1% (Αιθανόλη) |
Θερμοκρασία δωματίου 20 λεπτά, 60 λεπτά 5 λεπτά, 30 δευτερόλεπτα |
Κίτρινο διαφανές, Διαφανές κιτρινωπό-καφέ pH 6 Στικτά σημάδια
|
O | ○(Αγ) | Τα σημάδια εξαφανίζονται όταν η θερμοκρασία μειωθεί |
| 8 | Soft-data-jento W (γράσο Japan Lion) | Κατιονική λευκή σκόνη | 1% | Θερμοκρασία δωματίου 20 λεπτά |
Λευκό θολό pH 7 O
|
X | X |
Ω RCH2CH(CH2)nSO3Na (ΜΕΙΓΜΑ) α-αλλυλοσουλφονικό
|
| 9 | Ripomin COH (Ιαπωνικό γράσο λιονταριού) | Αμφοτερικό υγρό | 1% | Θερμοκρασία δωματίου 20 λεπτά |
Λευκό θολό pH 8 O
|
O | X | Ιμιδαζολύλιο |
| 10 | Perettex TR (Κάο, Ιαπωνία) |
Κατιονικό Άχρωμο διαφανές
|
1% | Θερμοκρασία δωματίου 20 λεπτά |
Λευκό θολό pH 10 O
|
O | X |
RODC—CH—SO3N4R—OOC—CH3 Διπροπυλοσουλφοηλεκτρικό νάτριο
|
| 11 | Ema-ru 20C (Κάο, Ιαπωνία) |
Κατιονικό Ανοιχτό κίτρινο υγρό
|
1% | Θερμοκρασία δωματίου 20 λεπτά |
Άχρωμη θολότητα pH 7 O
|
X | X |
R—O(CH2 Ω)nSO3Na Πολυοξυαιθυλενοαλκυλικά οξέα
|
| 12 | Κουταμίν 24P (Κάο, Ιαπωνία) |
Ανιονικό Λευκό στερεό
|
1% |
Άχρωμο και διαφανές pH 7 O
|
O | X | Τριμεθυλαμίνη | |
| 13 | Perettex # 1222 (Kao, Ιαπωνία) | Μη ιονικό | 1% | Θερμοκρασία δωματίου 20 λεπτά |
Λευκό θολό O
|
O | X | |
| 14 | Perettex # 1265 (Kao, Ιαπωνία) | Μη ιονικό | 1% | Θερμοκρασία δωματίου 20 λεπτά |
Άχρωμο και διαφανές O
|
O | X | |
| 15 | Soft-kurin QA-1 (Miyoshi, Ιαπωνία) |
Αμφοτερικός Λευκό στερεό
|
1% | Θερμοκρασία δωματίου 20 λεπτά |
Άχρωμη θολότητα pH 7 O
|
O | X | τύπου β-αλανίνης |
| 16 | Soft-kurin MA-3-70 (Miyoshi, Ιαπωνία) | Αμφοτερικός | 1% | Θερμοκρασία δωματίου 20 λεπτά |
Άχρωμο και διαφανές pH 8 O
|
O | X | |
| 17 | Marusenokku AgT (Ιαπωνία Ma-ruseru) | Αντιθαμβωτικός παράγοντας ασημιού |
3mL/L 30mL/L
|
Θερμοκρασία δωματίου 30 δευτερόλεπτα, 60 λεπτά |
Λευκό θολό pH 8 Προσκόλληση
|
O | △ | Ανατρέξτε στο εγχειρίδιο οδηγιών |
| 18 | Dainshiruba-SS (Yamato Kasei, Ιαπωνία) | Αντιθαμβωτικός παράγοντας ασημιού |
10% ισοπροπυλ Κετόνη 50% Νερό 10%
|
25~30℃ 4 λεπτά, 20 λεπτά, 60 λεπτά
|
Άχρωμο και διαφανές pH 8 O
|
O | X | Ανατρέξτε στο εγχειρίδιο οδηγιών |
| 19 | T611 (Uemura Kogyo, Ιαπωνία) | Αντιθαμβωτικός παράγοντας ασημιού |
Υγρό 10% 90%
|
Θερμοκρασία δωματίου 30 δευτερόλεπτα, 2 λεπτά, 10 λεπτά, 60 λεπτά | Άχρωμες διαφανείς κηλίδες | O | O | Ανατρέξτε στο εγχειρίδιο οδηγιών |
| 20 | Roukorinsu-eido (Αικορούκο, Ιαπωνία) | Αντιθαμβωτικός παράγοντας ασημιού | 1% | Θερμοκρασία δωματίου 31 λεπτά, 5 λεπτά, 30 λεπτά |
Λευκό θολό pH 7 O
|
O | X | Για χρήση σε ηλεκτρονικά εργοστάσια |
Μεταξύ των οργανικών ενώσεων, αυτές που έχουν αντι-αγριογονική αποχρωματιστική δράση όταν εμβαπτίζονται σε διάλυμα πολυθειούχου αμμωνίου 0,2% είναι η 2-17-αλκανιμιδαζόλη, η 2-μερκαπτοβενζιμιδαζόλη και οι συμπλεκτικοί παράγοντες.
Οι οργανικές ενώσεις με αυτές τις αντι-αποχρωματιστικές επιδράσεις μοιράζονται τα ακόλουθα χαρακτηριστικά:
① Η επεξεργασία πραγματοποιείται σε αλκαλική περιοχή κοντά στο pH 7.
② Περιέχει υδρόφοβες ομάδες (αλκύλιο μακράς αλυσίδας, φαινύλιο).
③ Περιέχει διμεθυλαμινομάδες ή —SH ομάδες ή περιέχει διπλούς δεσμούς.
④ Αδιάλυτο στο νερό.
⑤ Άχρωμο, σχεδόν στερεό.
Ωστόσο, ορισμένες περιπτώσεις πληρούν τις παραπάνω προϋποθέσεις αλλά δεν έχουν αντι-αποχρωματιστικές επιδράσεις, όπως η 2-μερκαπτοβενζιμιδαζόλη και η 2-θειαζολυλ βενζιμιδαζόλη.
Η αμοιβαία σχέση μεταξύ τους δεν είναι ακόμη πολύ σαφής.
Οι επιδράσεις των FC-134 και T611 έχουν επιβεβαιωθεί όσον αφορά την αντι-αποχρωματιστική δράση των επιφανειοδραστικών ουσιών. Ταυτόχρονα, διεξήχθησαν πειράματα σχετικά με τη συνδυασμένη δράση οργανικών ενώσεων και επιφανειοδραστικών ουσιών (FC-134) και δεν βρέθηκε σημαντική επίδραση (Πίνακας 2-33). Η αντοχή στον αποχρωματισμό του διαλύματος πολυσουλφιδικού αμμωνίου 0,2% διαρκεί μόνο περίπου 10 λεπτά το πολύ. Εν τω μεταξύ, η αντοχή στον διαλύτη (αραιωτικό) είναι επίσης σχετικά ασθενής. Για την αντοχή στον αποχρωματισμό διακοσμητικών αντικειμένων λόγω της παρουσίας λεκέδων, λαμβάνοντας υπόψη αυτά τα ζητήματα συνολικά, η μόνη δυνατή χρήση είναι η 2-μερκαπτοβενζιμιδαζόλη με FC-134 (βλ. Πίνακα 2-34).
Πίνακας 2-33 Συνδυασμένες επιδράσεις οργανικών ενώσεων και επιφανειοδραστικών ουσιών στην αντι-αποχρωματισμό επιμεταλλωμένων με άργυρο στρωμάτων
| Σειριακός αριθμός | Σύνθεση | Συνθήκες επεξεργασίας | Εμφάνιση | Υδροφοβικότητα | Ιδιότητα κατά της αλλαγής χρώματος | Παρατηρήσεις |
|---|---|---|---|---|---|---|
| 1 |
2-δεκαεπταμιδαζόλη 1g/L FC-134 1g/L EtOH: H2Ο = 1:1 |
Θερμοκρασία δωματίου 1 λεπτό, 60 λεπτά |
Λευκό ίζημα pH7 Πρόσφυση | O |
O Λιγότερο αποτελεσματικό από ό,τι όταν χρησιμοποιείται μόνο του
|
|
| 2 |
2-Μερκαπτοβενζιμιδαζόλη 1g/L FC-134 1g/L NaOH 2 g/L
|
Θερμοκρασία δωματίου 1 λεπτό, 60 λεπτά |
O | X |
O Καλύτερο από όταν χρησιμοποιείται μόνο του |
Μειωμένη ισχύς αφρισμού, όσο περισσότερο τόσο το καλύτερο |
| 3 |
Μερκαπτόνη 5g/L FC-134 0,5 g/L Ισοακετόνη: H2Ο = 1:1 |
Θερμοκρασία δωματίου 1 λεπτό, 60 λεπτά |
O |
O Καλύτερο από όταν χρησιμοποιείται μόνο του
|
Μειωμένη ισχύς αφρισμού, όσο περισσότερο τόσο το καλύτερο |
Πίνακας 2-34 Επίδραση των διαλυτών στην μεμβράνη κατά του αποχρωματισμού
| Οργανικές ενώσεις | Συνθήκες επεξεργασίας | Διαλυτικό μέσο | Εμφάνιση | Επίδραση κατά του αποχρωματισμού |
|---|---|---|---|---|
| 2-δεκαεπταμιδαζόλη |
1g/L (ΝΤΟ2H5ΟΗ: ΗΟ = 1: 1) 20 λεπτά
|
Λεκέδες | O | |
|
Αραιωτικό (5 λεπτά)
|
Ο λεκές εξαφανίζεται O
|
X | ||
|
Αλκοόλ (5 λεπτά)
|
Ο λεκές εξαφανίζεται O
|
X | ||
| Χονδρό ψεκασμό | Γρατσουνιά |
O Μόνο το γρατσουνισμένο μέρος έχει αποχρωματιστεί
|
||
| 2-Μερκαπτοβενζιμιδαζόλη |
10g/L NaOH 2 g/L Θερμοκρασία δωματίου 20 λεπτά
|
O | O | |
|
Λεπτότερος (5 λεπτά)
|
O | X | ||
|
Αλκοόλ (5 λεπτά)
|
O | △ | ||
| Χονδρό ψεκασμό | Γρατσουνιά |
O Μόνο το γρατσουνισμένο μέρος έχει αποχρωματιστεί
|
Τα παραπάνω πειραματικά αποτελέσματα συνοψίζονται ως εξής.
① Είναι δύσκολο να διασφαλιστεί ότι ο μοναδικός τόνος και η λάμψη του Ag δεν θα υποστούν ζημιά κατά την εφαρμογή άλλων πολύτιμων μετάλλων σε Ag για αντιθαμβωτική επεξεργασία.
② Χρησιμοποιώντας μεθόδους Sn ή κράματος Sn, όταν το πάχος του Sn είναι 50~10Å, μπορεί να επιτευχθεί το αντι-θαμπωτικό αποτέλεσμα, αλλά το αποτέλεσμα αυτής της μεθόδου από μόνο του είναι περιορισμένο.
③ Οι θεραπείες με Be και Al έχουν μικρή επίδραση.
④ Οι κλασικές επεξεργασίες όπως οι επεξεργασίες με χρωμικό έχουν σχετικά καλά αποτελέσματα. Ωστόσο, το μεγαλύτερο μειονέκτημά τους είναι ότι η επεξεργασμένη μεμβράνη έχει ασθενή αντοχή στην υπεριώδη ακτινοβολία και μπορεί να γίνει καφέ κατά τη διάρκεια μακροχρόνιας προστασίας.
⑤ Μεταξύ των οργανικών ενώσεων, αυτές με ιδιότητες κατά του αποχρωματισμού περιλαμβάνουν το 2-επταδεκυλιμιδαζόλιο, το 2-αλκυλοβενζιμιδαζόλιο και τους παράγοντες μερκαπτοναφθαλίνης. Ωστόσο, άλλες οργανικές ενώσεις με την ίδια δομή δεν έχουν απαραίτητα την ίδια ικανότητα κατά του αποχρωματισμού.
⑥ Η αποτελεσματικότητα του FC-134 στις επιφανειοδραστικές ουσίες που πωλούνται στην αγορά έχει επιβεβαιωθεί.
3. Επίδραση κατά του αποχρωματισμού της συνδυασμένης επεξεργασίας με ηλεκτρόλυση κασσιτέρου και ηλεκτρόλυση χρωμικού οξέος
(1) Δοκιμή Προώθησης Αποχρωματισμού και η Μέθοδος Μέτρησης Αποχρωματισμού της
Οι συνθήκες για τη δοκιμή προώθησης αποχρωματισμού παρουσιάζονται στον Πίνακα 2-35.
Πίνακας 2-35 Συνθήκες για τη δοκιμή ενίσχυσης κατά του αποχρωματισμού
| Διάλυμα |
Διάλυμα θειούχου αμμωνίου (κίτρινο) (Showa Chemical) (Νιου Χάμσαϊρ4)2Sx(2%) |
| Θερμοκρασία | 20℃ |
| Χρόνος μούλιασμα | 2 ώρες |
△(%) = L1 – Λ2 (2-1)
Στον τύπο,
L1— ανακλαστικότητα πριν από τη δοκιμή αλλαγής χρώματος, %·
L2— ανακλαστικότητα πριν από τη δοκιμή αλλαγής χρώματος, %.
(2) Ηλεκτρολύτης κασσιτέρου
Μέσω πειραμάτων σχετικά με τις επιδράσεις των συνθηκών επεξεργασίας του ηλεκτρολύτη κασσιτέρου, προσδιορίστηκε ότι η συγκέντρωση του κασσιτερικού νατρίου, ο χρόνος ηλεκτρόλυσης, η πυκνότητα ρεύματος και η θερμοκρασία επεξεργασίας μπορούσαν να αγνοηθούν όσον αφορά την επίδρασή τους στα χαρακτηριστικά αντοχής στον αποχρωματισμό. Ταυτόχρονα, προστέθηκε οξικό νάτριο ως σταθεροποιητής στην αλκαλική επιμετάλλωση Sn. Η σύνθεση και οι βέλτιστες συνθήκες για την ηλεκτρόλυση Sn παρουσιάζονται στον Πίνακα 2-36.
Πίνακας 2-36 Σύνθεση και βέλτιστες συνθήκες για την ηλεκτρόλυση Sn
| Σύνθεση διαλύματος επιμετάλλωσης |
NaSnO3 • 3Η20 8,5 g/L CH3COONa ・ 3H20,5 g/L |
| Συνθήκες θεραπείας |
Πυκνότητα ρεύματος 0,5A/dm2 Χρόνος ηλεκτρόλυσης 15s (10~30s) Θερμοκρασία 20℃ (7〜30℃) Υλικό ανόδου Πλάκα από ανοξείδωτο χάλυβα |
(3) Σχέση μεταξύ Εκπομπικής Ικανότητας και Χρόνου Ηλεκτρολύσης
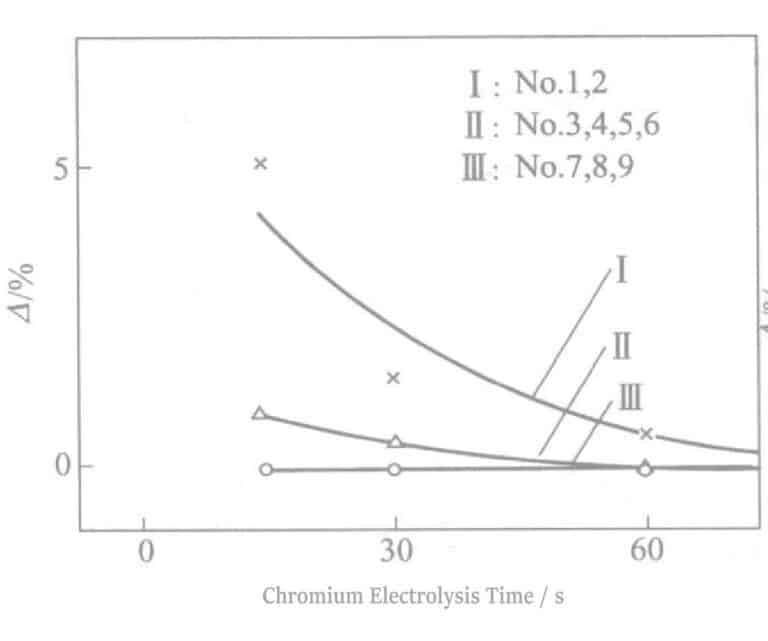
Η σχέση μεταξύ ανακλαστικότητας και χρόνου ηλεκτρόλυσης φαίνεται στο Σχήμα 2-8. Καθώς αυξάνεται ο χρόνος ηλεκτρόλυσης, η ανακλαστικότητα μειώνεται απότομα, γεγονός που μειώνει την απόχρωση του Ag. Ένας χρόνος ηλεκτρόλυσης περίπου 90 δευτερολέπτων θα δείξει ένα χρώμα σαν κασσίτερο-λευκό, και σε περίπου 180 δευτερόλεπτα ηλεκτρόλυσης, εμφανίζονται ανοιχτόχρωμες καφέ ραβδώσεις στην επιφάνεια. Ταυτόχρονα, όταν ο χρόνος ηλεκτρόλυσης υπερβαίνει τα 60 δευτερόλεπτα, οι ηλεκτρικές ιδιότητες επιδεινώνονται επίσης. Τα πειραματικά αποτελέσματα που ελήφθησαν σύμφωνα με την εξίσωση (2-1) φαίνονται στο Σχήμα 2-9. Καθώς αυξάνεται ο χρόνος ηλεκτρόλυσης, η τιμή △ μειώνεται.
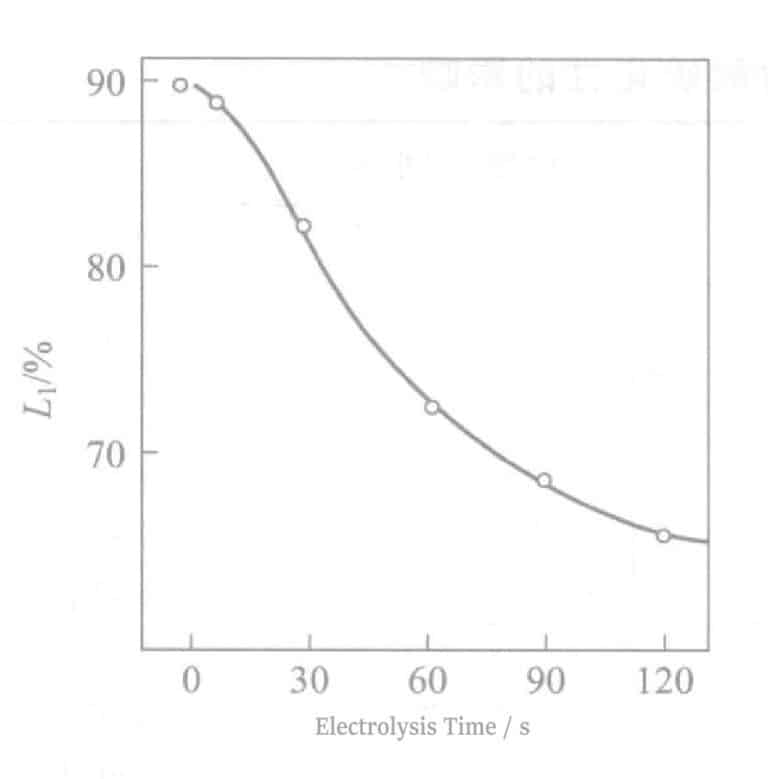
Σχήμα 2-8 Σχέση μεταξύ ανακλαστικότητας και χρόνου ηλεκτρόλυσης
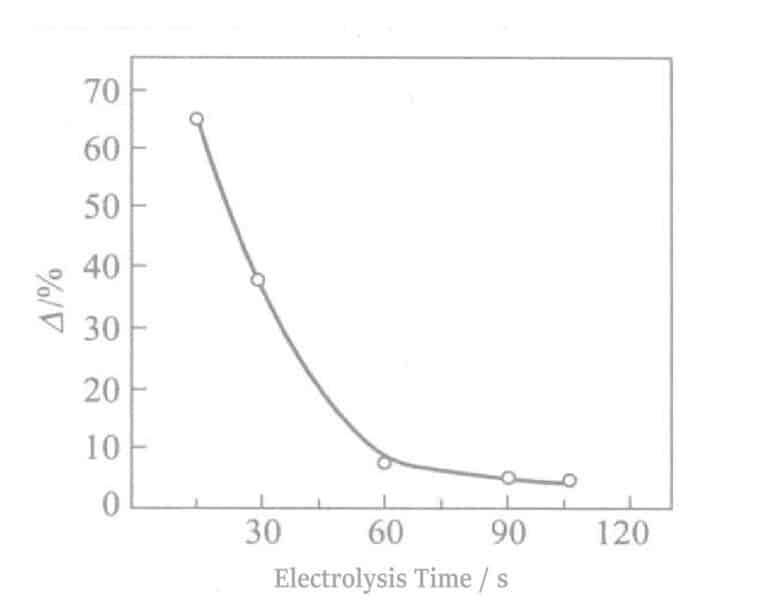
Σχήμα 2-9 Χρόνος ηλεκτρόλυσης και αντίσταση στον αποχρωματισμό
(4) Πάχος ηλεκτρολυτικής μεμβράνης κασσίτερου και ηλεκτρόλυση
Λαμβάνοντας υπόψη την απόδοση ρεύματος καθόδου σύμφωνα με τον νόμο του Faraday, η σχέση μεταξύ του χρόνου ηλεκτρόλυσης και του πάχους της μεμβράνης φαίνεται στο Σχήμα 2-10. Το πάχος του κασσιτέρου είναι περίπου αρκετές δεκάδες angstrom.
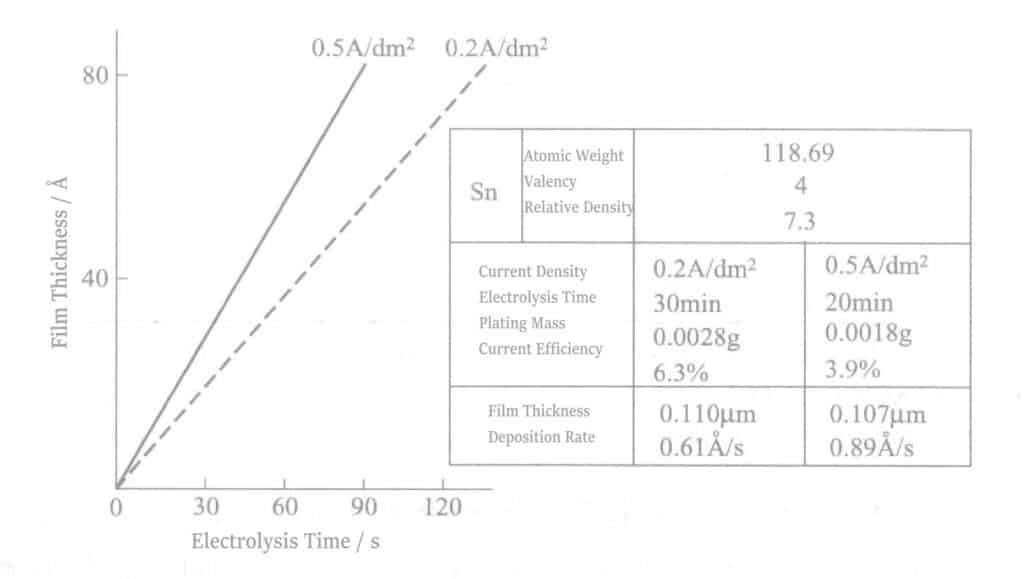
(5) Η επίδραση των ακαθαρσιών
Οι επιδράσεις πιθανών ακαθαρσιών (CN, Ag, Cu, Ni, κ.λπ.) που ενδέχεται να αναμειχθούν στον ηλεκτρολύτη στον Πίνακα 2-36 στην εμφάνιση και την αντοχή της ηλεκτρολυτικής μεμβράνης στα σουλφίδια επιβεβαιώθηκαν μέσω πειραμάτων. Τα αποτελέσματα παρουσιάζονται στον Πίνακα 2-37.
Πίνακας 2-37 Επίδραση των προσμίξεων στην αντοχή στο θείο
| Ακαθαρσίες | Συγκέντρωση/×10-6 | Χρόνος ηλεκτρόλυσης /s | ||
|---|---|---|---|---|
| 30 | 60 | 120 | ||
| Κανένα | 0 | O | O | △(λευκό) |
| ΣΟ |
20 200 2000 20000 |
O O O △, λευκό |
O △, λευκό △, λευκό △, λευκό |
△, λευκό △, λευκό △, λευκό △, λευκό |
| Ag |
20 50 100 150 200 400 |
O O △ X X X |
O △, κόκκινο X, κόκκινο-μαύρο Χ, κόκκινο-μαύρο Χ, κόκκινο-μαύρο Χ, μαύρο |
△, κόκκινο △, κόκκινο-μαύρο X, κόκκινο-μαύρο X, κόκκινο-μαύρο Χ, μαύρο Χ, μαύρο |
| Cu |
20 200 300 400 500 600 1000 |
O O O △, κόκκινο △, κόκκινο x, κόκκινο x, κόκκινο |
O O △, λευκό △, κόκκινο Χ, κόκκινο Χ, κόκκινο Χ, κόκκινο |
△, λευκό △, λευκό △, κόκκινο △, κόκκινο Χ, κόκκινο Χ, κόκκινο Χ, κόκκινο |
| Ni |
20 200 1000 |
O O O |
O O O |
O O O |
|
Σημείωση: 1. Χρησιμοποιούμενες ενώσεις: CN—NaCN;Ag—KAg(CN)2Cu—KCu(CN)2; Ni—Ni (CN)2 • 2KCN - 2H2O. 2. Βαθμός αλλαγής χρώματος: ○ καμία αλλαγή στην εμφάνιση· △ ελαφρά αλλαγή χρώματος· × αλλαγή χρώματος.
|
||||
(6) Ηλεκτρόλυση χρωμικών αλάτων
Εκτός από το χρωμικό, ανόργανα άλατα στον ηλεκτρολύτη, όπως (Na2CO2, KCN, KI, Na2S2O3, κ.λπ.), χρησιμοποιούνται ως πρόσθετα. Αυτά τα υδατικά διαλύματα έχουν αναφερθεί εδώ και καιρό ως παράγοντες κατά της θαμπάδας για το ασήμι. Η βασική σύνθεση του ηλεκτρολύτη φαίνεται στον Πίνακα 2-38.
Πίνακας 2-38 Συνθήκες ηλεκτρολυτικής διεργασίας Cr
| Σύνθεση ηλεκτρολυτών |
K2 CrO4 15g/L ΝαΟΗ 30g/L |
| Χρησιμοποιείται μετά από 30 ώρες θέρμανσης και ωρίμανσης | |
| Συνθήκες θεραπείας |
Τάση 6V (2 〜 6V) Χρόνος ηλεκτρόλυσης 15 δευτερόλεπτα (60 δευτερόλεπτα) Θερμοκρασία 20℃ Υλικό ανόδου Πλάκα από ανοξείδωτο χάλυβα |
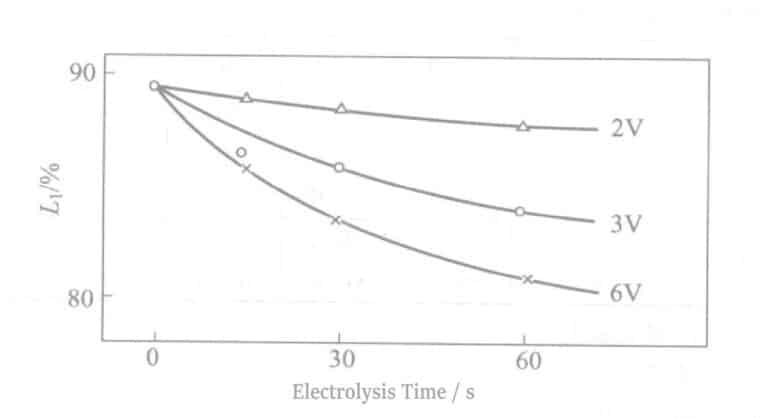
(7) Η σχέση μεταξύ ανακλαστικότητας και χρόνου ηλεκτρόλυσης
Η σχέση μεταξύ της ανακλαστικότητας σε τάση 2~6V και του χρόνου ηλεκτρόλυσης φαίνεται στο Σχήμα 2-11. Καθώς αυξάνεται η τάση, το πάχος της μεμβράνης Cr αυξάνεται ενώ η ανακλαστικότητα μειώνεται. Σε αντίθεση με τον ηλεκτρολύτη Sn, υπό τις ίδιες συνθήκες τάσης, η αύξηση του χρόνου ηλεκτρόλυσης δεν επηρεάζει την ανακλαστικότητα.
7. Η σχέση μεταξύ ανακλαστικότητας και χρόνου ηλεκτρόλυσης
Η σχέση μεταξύ της ανακλαστικότητας σε τάση 2~6V και του χρόνου ηλεκτρόλυσης φαίνεται στο Σχήμα 2-11. Καθώς αυξάνεται η τάση, το πάχος της μεμβράνης Cr αυξάνεται ενώ η ανακλαστικότητα μειώνεται. Σε αντίθεση με τον ηλεκτρολύτη Sn, υπό τις ίδιες συνθήκες τάσης, η αύξηση του χρόνου ηλεκτρόλυσης δεν επηρεάζει την ανακλαστικότητα.
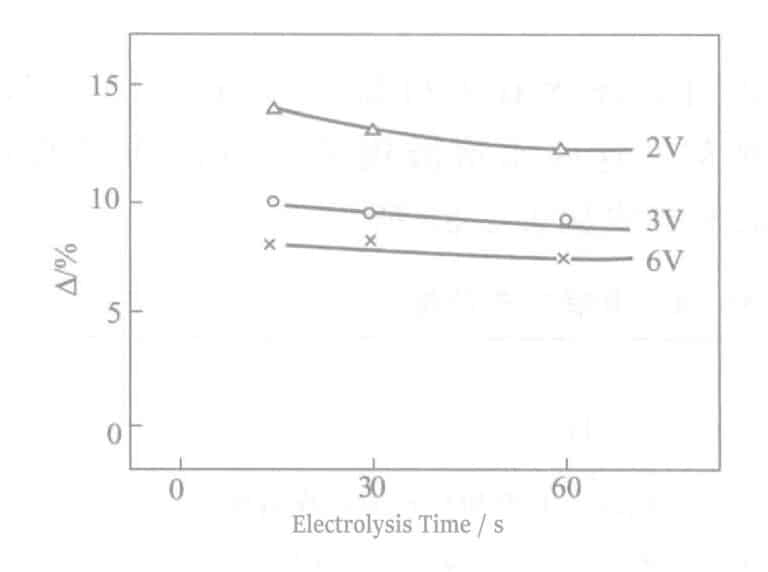
(8) Αντίσταση στα σουλφίδια
Η σύγκριση △ προκύπτει υπό την προϋπόθεση εμποτισμού σε 0,2% (NH4)2Sx διάλυμα για 2 ώρες φαίνονται στο Σχήμα 2-12. Όσο υψηλότερη είναι η τάση, τόσο καλύτερη είναι η αντίσταση στο θείο, κυρίως λόγω της πάχυνσης της μεμβράνης οξειδίου του χρωμίου. Εάν ο χρόνος ηλεκτρόλυσης παραταθεί χωρίς βελτίωση, αυτό συμβαίνει επειδή υπάρχουν πάρα πολλές οπές στην ηλεκτρολυτική μεμβράνη, με αποτέλεσμα την αύξηση του χρωμικού οξέος που αναμιγνύεται στις οπές.
(9) Αποχρωματισμός που προκαλείται από υπεριώδες φως
Τα αποτελέσματα αποχρωματισμού και αντοχής στο θείο των ηλεκτρολυτικά επιμεταλλωμένων μεμβρανών Cr που προκαλούνται από υπεριώδη ακτινοβολία παρουσιάζονται στον Πίνακα 2-39 (συνθήκες ηλεκτρολυτικής επιμετάλλωσης Cr: 6V, 30s). Μετά την υπεριώδη ακτινοβολία, η ηλεκτρολυτικά επιμεταλλωμένη με Cr μεμβράνη καταστρέφεται πλήρως, μετατρέπεται σε κοκκινωπό-μωβ και μπλε-μωβ. Ταυτόχρονα, η αντοχή στο θείο μειώνεται επίσης απότομα, πέφτοντας στο ίδιο επίπεδο όπως χωρίς την επεξεργασία κατά του αποχρωματισμού. Υπάρχει μικρή διαφορά μεταξύ των δειγμάτων που έχουν υποστεί επεξεργασία κατά του αποχρωματισμού και εκείνων που εκτίθενται στο ηλιακό φως λόγω της διαφοράς στην ένταση της υπεριώδους ακτινοβολίας σε σύγκριση με τα γενικά πειράματα υπεριώδους ακτινοβολίας.
Πίνακας 2-39 Αλλαγή χρώματος που προκαλείται από υπεριώδη ακτινοβολία
| Σειριακός αριθμός | Υπεριώδης | L1/% | L2/% | L3/% | △1/% | △2/% | Παρατηρήσεις | |
|---|---|---|---|---|---|---|---|---|
| 1 | - | - | 86. 3 | - | 84. 8 | 0 | 1.5 | (Γίνεται κίτρινο) |
|
2 3 4 |
υπεριώδης ακτινοβολία① |
0.5 1 3 |
86. 0 86. 2 86. 5 |
86. 0 83. 2 58〜65 |
67 53 — |
0 3 21-28 |
19 33 — |
Μπλε - Βιολέτα |
|
5 6 |
Ηλιακό φως② |
3 6 |
86.6 86.4 |
86.6 86.4 |
85.6 85.5 |
0 0 |
0.8 0.9 |
(Γίνεται κίτρινο) - |
|
① Ο φωτοηλεκτρικός μετρητής στιλπνότητας χρησιμοποιεί έναν σωλήνα εκκένωσης υδρογόνου. ② Έκθεση σε εξωτερικούς χώρους κατά τη διάρκεια της ημέρας: L1 —— Ανακλαστικότητα πριν από την ακτινοβολία. L2 —— Ανακλαστικότητα μετά την ακτινοβολία. L3 —— Ανακλαστικότητα μετά από εμβάπτιση σε 0,2% (NH4 )2 Sx για 30 λεπτά μετά την ακτινοβόληση. △1 =Λ1 - Λ2 △2 =Λ1 - Λ3
|
||||||||
Copywrite @ Sobling.Jewelry - Κατασκευαστής προσαρμοσμένων κοσμημάτων, εργοστάσιο κοσμημάτων OEM και ODM
(10) Η επίδραση των ακαθαρσιών
Τα αποτελέσματα των δοκιμών για τις επιπτώσεις των προσμίξεων στη βασική σύνθεση παρουσιάζονται στον Πίνακα 2-40.
Πίνακας 2-40 Επιδράσεις των προσμείξεων
| Ακαθαρσίες | Συγκέντρωση /×10-6 | Εμφάνιση |
|---|---|---|
| ΣΟ |
200 400 600 800 1000
|
O O O O O |
| Ag |
10 20 30 40 50 |
O O O X (μαύρο) X (μαύρο) |
| Sn |
200 400 600 800 1000
|
O O O O O |
(11) Επεξεργασία ηλεκτρόλυσης Sn συν αντοχή σε θείο Cr κατά την ηλεκτρολυτική επεξεργασία
Οι μέθοδοι που παρουσιάζονται παραπάνω έχουν πλεονεκτήματα και μειονεκτήματα και δεν μπορούν να θεωρηθούν πλήρεις μέθοδοι κατά του αποχρωματισμού. Επομένως, εξετάζεται η ακόλουθη προσέγγιση: άμεση εκτέλεση ηλεκτρολυτικής επεξεργασίας με Sn μετά την επιμετάλλωση με Ag, ακολουθούμενη από ηλεκτρολυτική επεξεργασία με Cr.
Υπό συνθήκες σταθερού ρεύματος (DK = 0,5A/dm2 ), ο χρόνος ηλεκτρόλυσης του Sn άλλαξε και κατά την επακόλουθη επεξεργασία ηλεκτρόλυσης Cr, η τάση και ο χρόνος ηλεκτρόλυσης μεταβλήθηκαν. Τα αποτελέσματα φαίνονται στο Σχήμα 2-13. Η μείωση της ανακλαστικότητας υπό κάθε συνθήκη προκαλείται από αλλαγές στον χρόνο ηλεκτρόλυσης Sn. Ο χρόνος ηλεκτρόλυσης πρέπει να διατηρείται εντός 30 δευτερολέπτων για να διατηρηθεί ο ασημί τόνος.
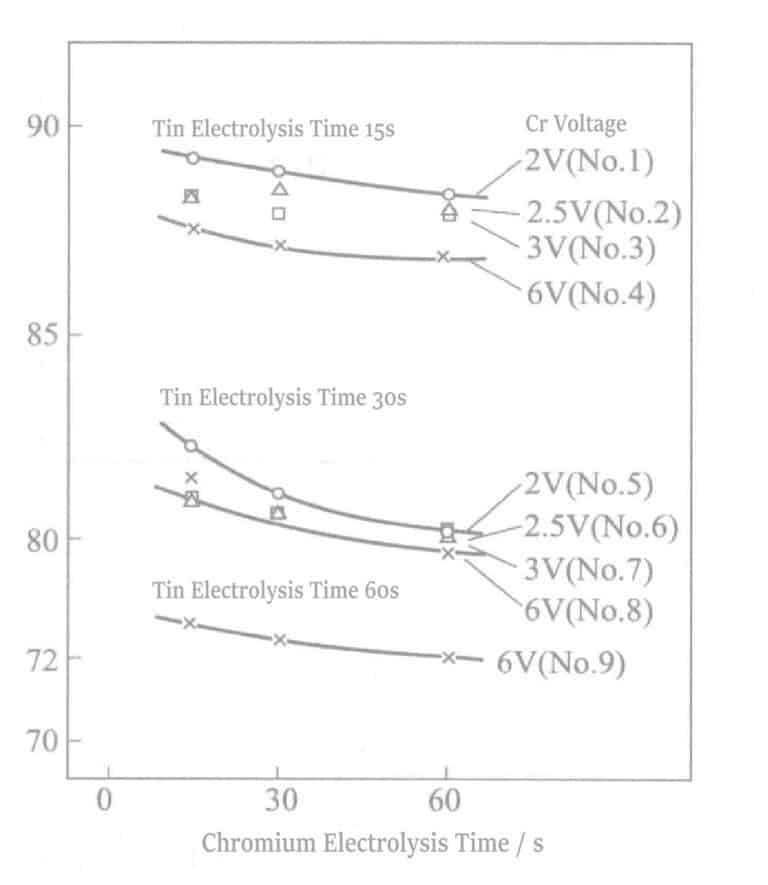
Όταν βρίσκεστε στην ίδια χρονική κατάσταση επεξεργασίας ηλεκτρόλυσης Sn, η παράταση του χρόνου ηλεκτρόλυσης Cr προκαλεί την εμφάνιση του χρώματος του υποκείμενου Sn Cr, με αποτέλεσμα μια λευκή ή γκρι ανομοιόμορφη κατάσταση. Ταυτόχρονα, όταν η ηλεκτρόλυση Cr γίνεται σε υψηλή τάση (6V), αυτό το φαινόμενο εμφανίζεται νωρίτερα. Στα 6V, μπορεί να παρατηρηθεί σε 5 δευτερόλεπτα, ενώ στα 2V, μπορεί να διαρκέσει περισσότερο από 60 δευτερόλεπτα. Η παράταση του χρόνου ηλεκτρόλυσης Sn δείχνει την ίδια τάση. Όσο μεγαλύτερος είναι ο χρόνος ηλεκτρόλυσης, τόσο πιο πιθανό είναι να συμβεί λεύκανση.
Αυτό το φαινόμενο εμφανίζεται όταν το φορτίο που διέρχεται κατά την επεξεργασία με Cr ενός συγκεκριμένου στρώματος ηλεκτρολυτικής επιμετάλλωσης Sn φτάσει σε μια ορισμένη τιμή. Η οξειδοαναγωγική αντίδραση κατά την ηλεκτρολυτική επιμετάλλωση με Cr παίζει έναν συγκεκριμένο ρόλο στο στρώμα ηλεκτρολυτικής επιμετάλλωσης με Sn, προκαλώντας αλλαγές στη μορφολογία κρυστάλλωσης του Sn ή προκαλώντας αλλαγές στην αντίθεση μεταξύ του στρώματος ηλεκτρολυτικής επιμετάλλωσης με Sn και του στρώματος ηλεκτρολυτικής επιμετάλλωσης με Cr.
Όταν δεν παρατηρείται αλλαγή χρώματος, αυτό σχετίζεται με την παράταση του χρόνου ηλεκτρόλυσης Sn. Ο χρόνος ηλεκτρόλυσης είναι 15~30s+ χρόνος ηλεκτρόλυσης σε διάστημα 30 δευτερολέπτων, ειδικά έχει καλή αντοχή στο θείο, αλλά θα υπάρξουν προβλήματα εμφάνισης. Ο συνδυασμός ηλεκτρόλυσης Sn στα 0,5A/dm2 για 15~30s, συν ηλεκτρόλυση Cr στα 2~3V για 30s ήταν η βέλτιστη συνθήκη.
Τα αποτελέσματα της δοκιμής έκθεσης σε εσωτερικούς χώρους παρουσιάζονται στο Σχήμα 2-15. Κιτρίνισμα μετά από 1~2 ημέρες για μη επεξεργασμένη επεξεργασία και 7~10 ημέρες για ηλεκτρολυτική επεξεργασία Cr. Αντίθετα, τα μέρη που υποβλήθηκαν σε επεξεργασία με ηλεκτρόλυση Sn ακολουθούμενη από ηλεκτρόλυση Cr άρχισαν να γίνονται γκρίζα μόνο εν μέρει μετά από 60~100 ημέρες, δείχνοντας καλή αποτελεσματικότητα. Η εμβάπτιση πραγματοποιήθηκε χρησιμοποιώντας 0,2% (NH3).4)2Sx διάλυμα ισοδύναμο με ένα μήνα δοκιμών έκθεσης σε εσωτερικούς χώρους. Η επεξεργασία ηλεκτρόλυσης Sn ακολουθούμενη από την επεξεργασία με Cr αναφέρεται συντομογραφικά ως SGP (διαδικασία προστασίας αργύρου).
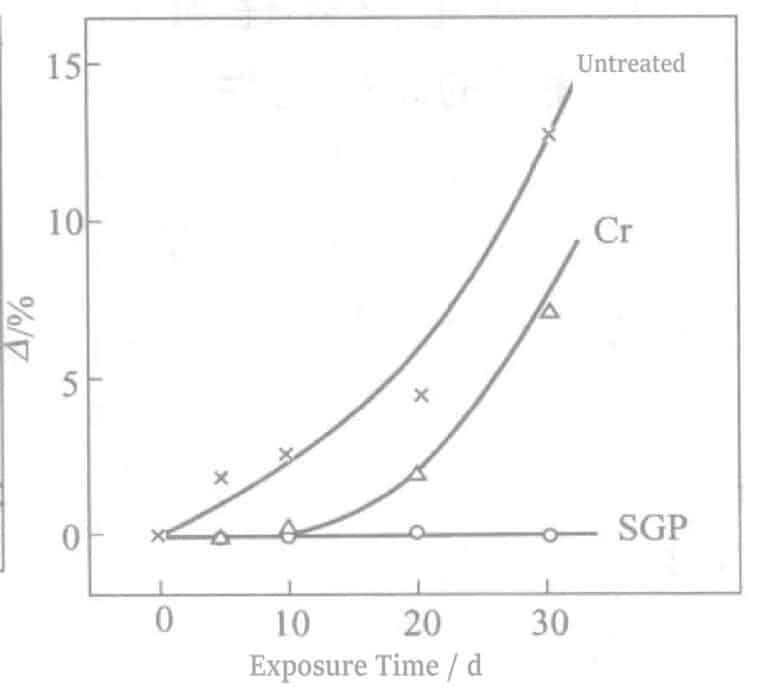
① Η επίδραση διαφόρων αλάτων κασσιτέρου στην αντοχή στο θείο
Τα αποτελέσματα των δοκιμών των επιδράσεων διαφόρων επιφανειακών ενεργοποιητών αλάτων κασσιτέρου στη μέθοδο SGP παρουσιάζονται στον Πίνακα 2-41 και στο Σχήμα 2-16.
Πίνακας 2-41 Σύγκριση των επιδράσεων διαφόρων αλάτων κασσιτέρου
| Σειριακός αριθμός | Σύνθεση και οι συνθήκες επεξεργασίας της | Χρόνος ηλεκτρόλυσης Sn /s | Χρόνος/δευτερόλεπτα ηλεκτρόλυσης Cr | L1/% | △/% | Παρατηρήσεις |
|---|---|---|---|---|---|---|
| 1 |
SnCl2 4g/L HCl 0,025mol/L (βύθιση) |
13 30 60 |
15 |
90. 2 89. 8 89. 2 |
5. 4 4. 8 5. 8 |
Κιτρίνισμα Κιτρίνισμα Κιτρίνισμα |
| 2 |
Na2SnO3 ·3Η20 8,5 g/L CH3COONa·3H20,5 g/L 3. 5V (0.1A/dm2) |
15 30 60 |
15 |
89. 7 87. 3 85. 2 |
0. 7 0. 1 0
|
Μερικό κιτρίνισμα - Χρώμα κασσίτερου |
| 3 |
Νο 2 συν Peretekkusu# 1232① 0,1 g/L 3. 5V (0. 15A/dm2) |
15 30 60 |
15 |
87. 4 85.0 76. 6
|
0 0. 1 0 |
- - Χρώμα κασσίτερου |
| 4 |
K2SnO3·3Η20 8,5 g/L CH3COONa·3H20,5 g/L 3. 5V (0. 1A/dm2) |
15 30 60 |
15 |
89. 6 88. 9 85. 4 |
0. 9 0 0 |
Μερικό κιτρίνισμα - Χρώμα κασσίτερου |
|
① Peretekkusu# Το 1232 είναι προϊόν της Miyoshi Oil & Fat στην Ιαπωνία. Σημείωση: Ηλεκτρολύτης χρωμίου 3 V.
|
||||||
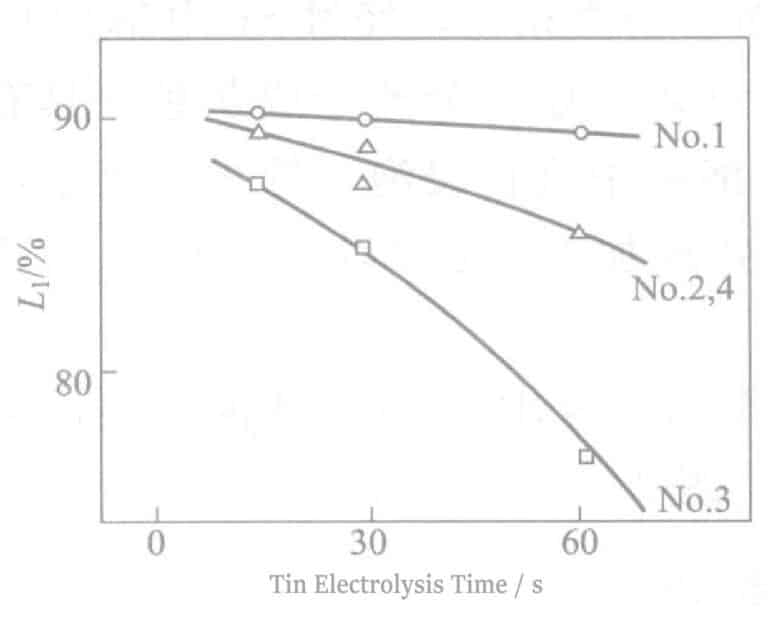
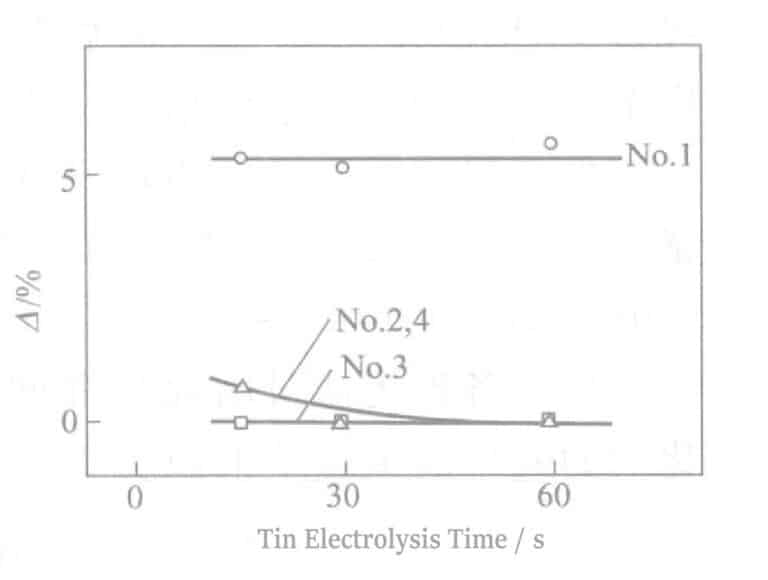
Η προσθήκη ενός μη ιονικού επιφανειοδραστικού (Νο. 3) στον ηλεκτρολύτη κασσιτερικού νατρίου βελτιώνει σημαντικά την απόδοση ρεύματος, επιταχύνει τον ρυθμό ηλεκτρόλυσης (Νο. 2), μειώνει την ανακλαστικότητα και ενισχύει την αντίσταση στο θείο.
Αν και τα αποτελέσματα του ηλεκτρολύτη κασσιτερικού καλίου (Αρ. 4) είναι τα ίδια με αυτά του ηλεκτρολύτη κασσιτερικού νατρίου, υπάρχουν ορισμένες διαφορές μεταξύ των επιδράσεων των αλάτων νατρίου και των αλάτων καλίου σε αλκαλικά διαλύματα επικασσιτερώσεως.
② Η επίδραση του ηλεκτρολύτη χρωμίου στην αντίσταση στο θείο μελετήθηκε κυρίως από πτυχές όπως η συγκέντρωση ηλεκτρολυτών, η επίδραση των επιφανειοδραστικών ουσιών και η επίδραση της πυκνότητας ρεύματος στην εμφάνιση μετά την επεξεργασία.
Πίνακας 2-42 Επίδραση της συγκέντρωσης στην αντοχή στο θείο
| Συγκέντρωση /(g/L) | Χρόνος ηλεκτρόλυσης /s | Τιμή ρεύματος σε σταθερή τάση (6V)/A | ||
|---|---|---|---|---|
| 5 | 15 | 30 | ||
|
K2CrO4 15 ΝαΟΗ 30 |
X | X | X |
4. 0 (40A/dm2) |
|
K2CrO4 7.5 ΝαΟΗ 15 |
O | X | X |
2.4 (24A/dm2) |
|
K2CrO4 1.5 ΝαΟΗ 3.0 |
O | O | X |
0.6 (6A/dm2) |
|
Σημείωση: Το O υποδηλώνει ότι δεν υπάρχει αλλαγή στην εμφάνιση. Το × υποδηλώνει αλλαγή στην εμφάνιση (λεύκανση).
|
||||
- Επίδραση της συγκέντρωσης: Το πρότυπο διάλυμα αραιώθηκε στο 1/2, 1/10 και διερευνήθηκε ο χρόνος ηλεκτρόλυσης στον οποίο εμφανίστηκε χρώμα κασσιτέρου κατά την ηλεκτρόλυση στα 6 V. Τα αποτελέσματα παρουσιάζονται στον Πίνακα 2-42.
- Επίδραση των επιφανειοδραστικών ουσιών: Σε πρότυπα διαλύματα επιφανειοδραστικής ουσίας (Perettekusu#1265, προϊόν της Miyo-shi Oils and Fats Co., Ltd., Ιαπωνία) προστέθηκαν ιοντικά επιφανειοδραστικά σε συγκεντρώσεις 1/1 και 1/2, και ο χρόνος ηλεκτρόλυσης διερευνήθηκε τη στιγμή που άρχισε να εμφανίζει χρώμα κασσίτερου. Τα αποτελέσματα παρουσιάζονται στον Πίνακα 2-43. Σε σύγκριση με την έλλειψη προσθήκης, το αποτέλεσμα ήταν καλύτερο σε υψηλή πυκνότητα ρεύματος όταν προστέθηκαν επιφανειοδραστικά. Σε χαμηλή πυκνότητα ρεύματος, υπήρχε μικρή διαφορά από την περίπτωση χωρίς προσθήκη, αλλά το αέριο εμπόδισε την πρόοδο της ηλεκτρόλυσης. Όταν υπήρχαν επιφανειοδραστικά, η συγκέντρωσή τους και η πυκνότητα ρεύματος επηρέασαν τον χρόνο έναρξης της λεύκανσης, αυξάνοντας τις δυσκολίες διαχείρισης. Ταυτόχρονα, δημιουργήθηκαν φυσαλίδες λόγω της μεγάλης ποσότητας παραγωγής υδρογόνου. Ήταν ευκολότερη η διαχείριση χωρίς προσθήκη.
Πίνακας 2-43 Επιδράσεις των επιφανειοδραστικών ουσιών
| Συγκέντρωση/(g/L) | Perettekusu# 1265/(mL/L) | Τάση/V | DK/(A/dm2 | Χρόνος/δευτ. ηλεκτρόλυσης | ||
|---|---|---|---|---|---|---|
| 5 | 10 | 15 | ||||
|
K2CrO4 15 ΝαΟΗ 30
|
0 |
6 5 6 3 |
40 29 19 7 |
X X X X |
X X X X |
X X X X |
| 0.01 |
6 5 6 3 |
40 29 19 7 |
O O O O |
X X O O |
X X X X |
|
| 0.1 |
6 5 6 3 |
40 29 19 7 |
O O O O |
O O O X |
X X X X |
|
| 1 | 6 | 40 | O | X | X | |
|
K2CrO4 7.5 ΝαΟΗ 15
|
0 |
6 5 6 3 |
24 17 10 3 |
X X X O |
X X X O |
X X X X |
| 0.01 |
6 5 6 3 |
24 17 10 3 |
O O O O |
O O X X |
X X X X |
|
- Επίδραση του ρεύματος: Πυκνότητα Ο χρόνος που εμφανίζεται για πρώτη φορά το χρώμα κασσίτερου σε διάφορες πυκνότητες ρεύματος κατά την ηλεκτρόλυση φαίνεται στο Σχήμα 2-18. Ταυτόχρονα, η καμπύλη EI φαίνεται στο Σχήμα 2-19. Η πυκνότητα ρεύματος είναι πιο κατάλληλη όταν ο χρόνος ηλεκτρόλυσης είναι 0,5A/dm2 περίπου 30 δευτερόλεπτα. Εν τω μεταξύ, ο χρόνος χωρίς την εμφάνιση χρώματος κασσίτερου επηρεάζεται επίσης από τη συγκέντρωση ηλεκτρολύτη, την πυκνότητα ρεύματος ανόδου, την απόσταση ηλεκτροδίων και άλλους παράγοντες. Η διαχείριση της συγκέντρωσης γίνεται υπολογίζοντας το μέγεθος της δεξαμενής και είναι δυνατό να εξαχθεί η εγγενής ισχύς της δεξαμενής που δεν εμφανίζεται στο χρώμα του κασσίτερου σε μια συγκεκριμένη τάση, για ευκολία διαχείρισης.
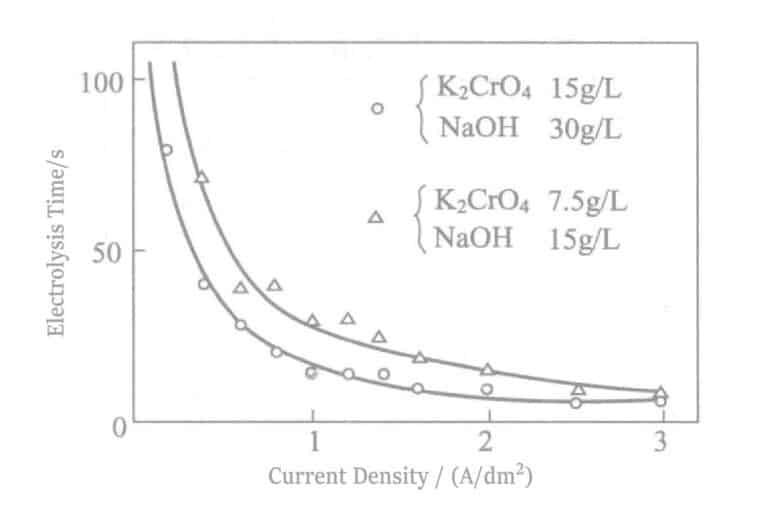
Σχήμα 2-18 Σχέση μεταξύ πυκνότητας ρεύματος και χρόνου ηλεκτρόλυσης
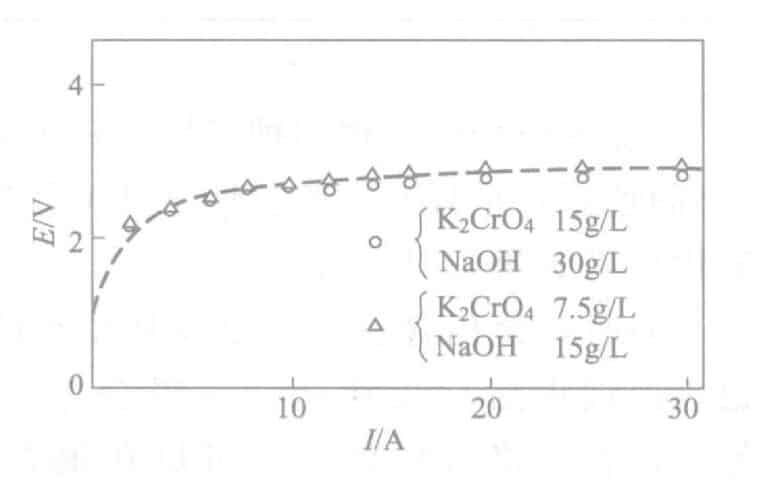
Σχήμα 2-19 Καμπύλη EI του διαλύματος ηλεκτρολύτη
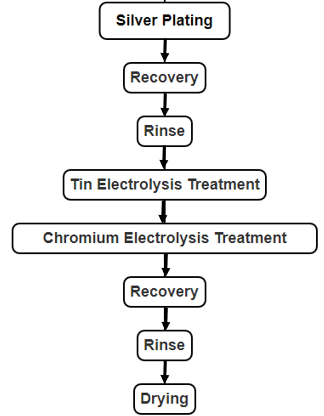
Σχήμα 2-20 Διαδικασία επεξεργασίας ηλεκτρολυτών χρωμίου

Σχήμα 2-21 Σύγκριση της αντοχής στο θείο διαφόρων μεθόδων επεξεργασίας
Ταυτόχρονα, η χρήση απορρυπαντικών (επιφανειοδραστικών ουσιών) που περιέχουν α-δικετόνη και τα άλατά της για το πλύσιμο ή το μούλιασμα του ασημιού (ή των επιπλατινωμένων αντικειμένων) και των κραμάτων του (κράμα κασσιτέρου, κράμα ψευδαργύρου, κράμα ινδίου, κράμα παλλαδίου κ.λπ.) μπορεί να αναστείλει σημαντικά τον αποχρωματισμό ή τη διάβρωση της επιφάνειας.
Η βασική δομή του προσθέτου του φαίνεται στο Σχήμα 2-22.
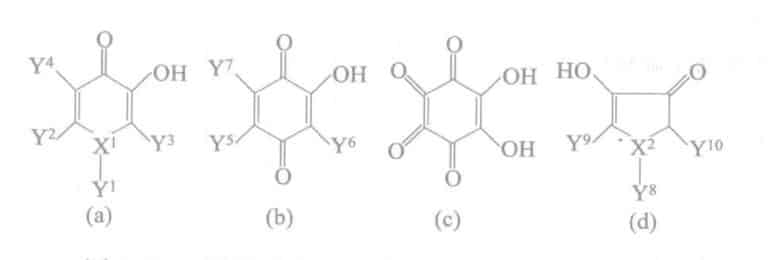
Πίνακας 2-44 Παραδείγματα σκευασμάτων δικετο επιφανειοδραστικών για την πρόληψη της θαμπάδας του αργύρου
| Σύνθεση | Νο. 1 | Αρ. 2 | Αρ. 3 | Αρ. 4 | Αρ. 5 | Αρ. 6 | Αρ. 7 | Αρ. 8 |
|---|---|---|---|---|---|---|---|---|
| Χλωροβανιλικό οξύ | 10 | |||||||
| Πολυοξυαιθυλενοαλκυλαιθέρας | 0.5 | |||||||
| Δισόξινο φωσφορικό νάτριο | 5 | |||||||
| Πολυαιθυλενογλυκόλη | 1 | |||||||
| Τρετινοΐνη | 5 | |||||||
| Χλωριούχο πυραζόλιο | 5 | |||||||
| Διττανθρακικό νάτριο | 5 | |||||||
| Πρωτεάση | 1 | |||||||
| Ιωδιούχο κάλιο | 0.05 | |||||||
| Τετραϋδροξυ-1,4-βενζοκινόνη | 0.5 | |||||||
| 2-αλκυλ-Ν-καρβοξυμεθυλ-Ν-υδροξυμεθυλιμιδαζολίνη | 10 | |||||||
| Θειουρία | 0.5 | |||||||
| Γλυκερόλη | 1 | |||||||
| 3-αιθυλο-2-υδροξυ-2-κυκλοπενταν-1-καρβοξυλικό νάτριο | 0.05 | |||||||
| αλκυλοσουλφονικό κάλιο | 5 | |||||||
| Ισοκυανουρονικό άλας | 5 | |||||||
| Ν-ακυλιωμένες αμίνες | 1 | |||||||
| 3-υδροξυ-2-μεθυλο-4-πυρόνη | 20 | |||||||
| Κιτρικό οξύ | 5 | |||||||
| Βενζοϊκό νάτριο | 5 | |||||||
| Μινθόλη | 0.1 | |||||||
| Ασβέστιο ροσμαρινικό οξύ | 2 | |||||||
| 3-μεθυλο-1,2-κυκλοπενταναμίνιο | 20 | |||||||
| Καστορέλαιο πολυοξυαιθυλενίου | 5 | |||||||
| Στεροειδή γλυκοσίδια | 1 | |||||||
| 3-υδροξυ-1,2-διμεθυλο-4(1H)-πυριδίνη | 6 | |||||||
| Μερκαπτοαλανίνη | 2 | |||||||
| Γλυκοαμυλάση | 5 | |||||||
| Σορβιτόλη | 1 | |||||||
| 2,5-διυδροξυ-1,4-βενζοκινόνη | 10 | |||||||
| Χλωριούχο αλκυλοβενζυλοαμμώνιο | 30 | |||||||
| Τρυγικό κάλιο-νάτριο | 5 | |||||||
| Παπαΐνη | 1 |
Τμήμα II Ηλεκτρολυτική επιμετάλλωση αργύρου
Επειδή το ασήμι έχει χαμηλή ειδική αντίσταση και είναι πολύ φθηνότερο από άλλα πολύτιμα μέταλλα, η επιμετάλλωση με άργυρο χρησιμοποιείται ευρέως στον τομέα της ηλεκτρονικής.
Ως πολύτιμο μέταλλο, το ασήμι έχει πιο θετικό δυναμικό οξειδοαναγωγής από άλλα μέταλλα, επιτρέποντάς του να μετατοπίζεται και να εναποτίθεται σε μέταλλα όπως ο χαλκός, ο σίδηρος και ο ψευδάργυρος, σχηματίζοντας ένα στρώμα επιμετάλλωσης αργύρου σε αυτά τα μέταλλα. Θα αναφερθεί αργότερα ότι αυτός ο τύπος αντίδρασης χρησιμοποιείται σε πλακέτες τυπωμένων κυκλωμάτων για την αντικατάσταση του χαλκού με ασήμι, έτσι ώστε το μοτίβο του χαλκού να καλύπτεται από ένα στρώμα αργύρου, αυξάνοντας έτσι τη συγκολλησιμότητα και μειώνοντας την αντίσταση επαφής. Ωστόσο, αυτή η εναπόθεση μετατόπισης γενικά οδηγεί σε ένα σχετικά λεπτό στρώμα επιμετάλλωσης, περίπου 2 μm ή λιγότερο. Αντίθετα, το στρώμα επιμετάλλωσης που λαμβάνεται μέσω μιας αντίδρασης αναγωγής μπορεί να είναι κάπως παχύτερο.
Στην εφαρμογή της επιμετάλλωσης με άργυρο, η πιο διάσημη θα πρέπει να είναι η αντίδραση του ασημένιου κατόπτρου. Η αντίδραση του ασημένιου κατόπτρου αναπτύχθηκε από τον Drayton το 1830 και εφαρμόστηκε στη βιομηχανία κατασκευής κατόπτρων. Επιπλέον, η χημική επιμετάλλωση με άργυρο (ειδικά η επιμετάλλωση με αναγωγή) χρησιμοποιείται ευρέως στην ηλεκτρονική, επεκτείνοντας έτσι τις βιομηχανικές εφαρμογές της επιμετάλλωσης με άργυρο. Η χημική επιμετάλλωση με άργυρο μπορεί να εφαρμοστεί όχι μόνο σε μέταλλα αλλά και σε μη μέταλλα.
1. Μετατόπιση της επιμετάλλωσης αργύρου και οι εφαρμογές της
Η επιμετάλλωση με άργυρο μετατόπισης χρησιμοποιεί τη διαφορά δυναμικού μεταξύ του βασικού μετάλλου και του αργύρου.
Τα μοτίβα αγωγών στις πλακέτες τυπωμένων κυκλωμάτων είναι συνήθως κατασκευασμένα από χαλκό, αλλά κατά την αποθήκευση, πριν από την τοποθέτηση των εξαρτημάτων, σχηματίζεται μια μεμβράνη οξειδίου στην επιφάνεια του χαλκού. Αυτή η μεμβράνη οξειδίου επηρεάζει την ικανότητα συγκόλλησης της πλακέτας κυκλώματος. Τα προϊόντα υψηλής τεχνολογίας ή ακόμα και η επιμετάλλωση Ni/Au, Ni/Pd, Ni/Pa/Au χρησιμοποιούνται γενικά για την ενίσχυση της ικανότητας συγκόλλησης των κυκλωμάτων χαλκού, γεγονός που φυσικά αυξάνει το κόστος. Ωστόσο, η επιμετάλλωση με Sn δεν έχει επαρκή αντοχή στη σκουριά. Η επιμετάλλωση με ασήμι έχει παρόμοια τιμή με την επιμετάλλωση με Sn και όχι μόνο αποτρέπει τη σκουριά και είναι κατάλληλη για συγκόλληση, αλλά μπορεί επίσης να χρησιμοποιηθεί για συνδέσεις μεταλλικών συρμάτων, πράγμα που σημαίνει ότι το ασήμι μπορεί να επιμεταλλωθεί με μετατόπιση σε κυκλώματα χαλκού. Ωστόσο, το πάχος πρέπει να αυξηθεί για να αντισταθμιστεί εάν το ασήμι επιμεταλλωθεί απευθείας στον χαλκό λόγω ανομοιόμορφης επιμετάλλωσης. Αυτό κάνει την επιμετάλλωση να αποτυγχάνει στη δοκιμή ταινίας, με την επιμετάλλωση να ξεφλουδίζει εύκολα, ειδικά μετά την αποθήκευση. Ωστόσο, αυτό το πρόβλημα μπορεί να λυθεί με επιμετάλλωση δύο σταδίων. Η μέθοδος είναι πρώτα να επιμεταλλωθεί ένα στρώμα μετάλλου, το οποίο είναι πιο ακριβό από τον χαλκό, στον χαλκό και στη συνέχεια να επιμεταλλωθεί μια πλάκα μετατόπισης με ασήμι. Το πρώτο μεταλλικό στρώμα μπορεί να είναι Pd ή Ag. Το πάχος είναι τόσο λεπτό, της τάξης των νανομέτρων (δηλαδή, πάχος αρκετών νανομέτρων), που η παρουσία της επιμετάλλωσης δεν μπορεί να αναγνωριστεί με γυμνό μάτι. Η αντίδραση μετατόπισης είναι:
Το διάλυμα εκτόπισης αργύρου πρέπει επίσης να περιέχει έναν συμπλεκτικό παράγοντα για μονοσθενή χαλκό για τη σταθεροποίηση των εκτοπισμένων ιόντων χαλκού. Όταν η πρώτη επίστρωση είναι άργυρος εκτόπισης, ο ρυθμός εκτόπισής της πρέπει να είναι πολύ πιο αργός από αυτόν του δεύτερου στρώματος επιμετάλλωσης Ag, ισοδύναμος με λιγότερο από 15% της ταχύτητάς της. Εάν είναι πολύ γρήγορος, είναι εύκολο να προκληθεί μείωση της πρόσφυσης της επίστρωσης, με αποτέλεσμα το ξεφλούδισμα της επίστρωσης κατά τη διάρκεια της δοκιμής της ταινίας. Το ακόλουθο είναι ένα παράδειγμα επιμετάλλωσης αργύρου.
Όταν το πρώτο στρώμα επιμετάλλωσης είναι Pd, το διάλυμα επιμετάλλωσης Pd είναι
PdSO44 50mg/L (λογαριασμένο ως Pd)
H2SO4 5%
Θερμοκρασία Θερμοκρασία δωματίου
Χρόνος περίπου 30 δευτερόλεπτα
Πίνακας 2-45 Σύνθεση και διαδικασία εκτόπισης επιμετάλλωσης με άργυρο (πρώτο στρώμα επιμετάλλωσης)
| Σύνθεση και συνθήκες διεργασίας | Σύνθεση και συστατικό | Σύνθεση και συνθήκες διεργασίας | Σύνθεση και συστατικό |
|---|---|---|---|
| Μεθανοσουλφονικό άργυρο (ως Ag) | 1g/L | Lurotex A25 | 20mg/L |
| NaBr | 320g/L | pH | 5.5 |
| Διαιθυλενοτριαμινοπεντυλενοφωσφονικό οξύ | 30mL/L | Θερμοκρασία | 50℃ |
| Πολυαιθυλενογλυκόλη 400 | 80mL/L | Φορά | 5 λεπτά |
| 2,2'-διπυριδίνη | 90mg/L |
Μετά την επιμετάλλωση, τα επιμεταλλωμένα μέρη υποβάλλονται σε θερμική επεξεργασία στους 150℃ για 4 ώρες, ακολουθούμενη από δοκιμή διαβρεξιμότητας, η οποία είναι κατάλληλη.
Όταν το πρώτο στρώμα επιμετάλλωσης είναι Ag, το διάλυμα επιμετάλλωσης και η διαδικασία του παρουσιάζονται στον Πίνακα 2-46.
Πίνακας 2-46 Σύνθεση και διαδικασία επιμετάλλωσης με άργυρο μετατόπισης (Δεύτερη επίστρωση)
| Σύνθεση και συνθήκες διεργασίας | Σύνθεση και συστατικό | Σύνθεση και συνθήκες διεργασίας | Σύνθεση και συστατικό |
|---|---|---|---|
| Μεθανοσουλφονικό άργυρο (ως Ag) | 1g/L | Πολυαιθυλενογλυκόλη 400 | 80mL/L |
| NaBr | 320g/L | 2,2'-διπυριδίνη | 90mg/L |
| Διαιθυλενοτριαμινοπεντυλενοφωσφονικό οξύ | 30mL/L | pH | 5.5 |
Το διάλυμα επιμετάλλωσης για το πρώτο και το δεύτερο στρώμα επιμετάλλωσης μπορεί να έχει την ίδια σύνθεση, αλλά η θερμοκρασία και ο χρόνος εμβάπτισης διαφέρουν. Οι συνθήκες για το πρώτο στρώμα επιμετάλλωσης είναι οι εξής: 25℃, 30s. Οι συνθήκες για το δεύτερο στρώμα επιμετάλλωσης είναι οι εξής: 50℃, 6 λεπτά. Τα προκύπτοντα στρώματα επιμετάλλωσης είναι ομοιόμορφα, ασημένια λαμπερά και έχουν καλή συγκολλησιμότητα με συγκόλληση.
Οι Hutchinson et al. πρότειναν μια μέθοδο διαλύματος επιμετάλλωσης χρησιμοποιώντας αιθέρα αλκυλοπολυαιθυλενογλυκόλης ως λαμπρυντικό, αιθυλενοδιαμίνη και 1-υδροξυαιθυλενο-1,1-διφωσφονικό οξύ ως παράγοντες συμπλοκοποίησης χαλκού, και το ληφθέν στρώμα επιμετάλλωσης μπορεί να ικανοποιήσει τις συνθήκες συγκόλλησης των πλακετών τυπωμένων κυκλωμάτων.
Το ITO (ένα διαφανές οξείδιο ινδίου-κασσιτέρου) χρησιμοποιείται ευρέως σε οθόνες υγρών κρυστάλλων και πλάσματος. Καθώς το μέγεθος των οθονών υγρών κρυστάλλων και των οθονών πλάσματος έχει αυξηθεί τα τελευταία χρόνια, η αντίσταση του ίδιου του ITO έχει γίνει σχετικά υψηλή. Για την επίλυση αυτού του προβλήματος, μπορεί να προστεθεί στο ITO ένα στρώμα αργύρου με χαμηλότερη αγωγιμότητα. Αυτό δεν μπορεί να εφαρμοστεί με απευθείας ηλεκτρολυτική επιμετάλλωση αργύρου, επειδή είναι δύσκολο να εναποτεθούν άμεσα καταλυτικά ενεργά μέταλλα στο ITO. Επομένως, πρώτα εναποτίθεται ένα στρώμα κασσιτέρου στο ITO, ακολουθούμενο από μια καταλυτικά ενεργή εναπόθεση μετάλλου και τέλος, επιμετάλλωση αργύρου. Η σύνθεση του διαλύματος επιμετάλλωσης και οι συνθήκες διεργασίας για την επιμετάλλωση αργύρου σε ITO φαίνονται στον Πίνακα 2-47.
Πίνακας 2-47 Σύνθεση του διαλύματος επιμετάλλωσης και συνθήκες διεργασίας για επιμετάλλωση με άργυρο σε ITO
| Υγρό κασσίτερου εμβάπτισης |
SnCl2 HCl
|
70g/L 230mL/L |
| Ρευστό ενεργοποίησης | AgNO3 | 10g/L |
| Λύση επιμετάλλωσης με άργυρο |
AgNO3 Νιου Χάμσαϊρ4Ω (NH4)2SO4 Co(SO4)2 Mg(OH)2 Πάχος Ag Ειδική αντίσταση Ειδική αντίσταση (250℃, 30 λεπτά μετά την επεξεργασία) |
0,03〜0,08mol/L 7〜10mol/L 0,3 〜0,8mol/L 0,1 〜0,2mol/L 0,01〜0,05mol/L 2900-3200 Å 3〜3.5μΩ• cm 1, 6〜2, 5μΩ• cm |
2. Μείωση της επιμετάλλωσης αργύρου και οι εφαρμογές της
Η σύνθεση του διαλύματος αναγωγής αργύρου επιμετάλλωσης είναι παρόμοια με αυτή της γενικής χημικής επιμετάλλωσης, με τα κύρια συστατικά να είναι: άλας αργύρου, συμπλεκτικός παράγοντας, αναγωγικός παράγοντας, ρυθμιστής pH, σταθεροποιητής κ.λπ. Οι αναγωγικοί παράγοντες για το άργυρο περιλαμβάνουν γλυκόζη, σακχαρίνη, γλυοξάλη, ασκορβικό οξύ, γλυκονικό οξύ, σορβιτόλη, υδραζίνη, HCHO, KBH4, NaBH4, DMAB και άλλοι.
Οι αντιδράσεις ορισμένων αντιπροσωπευτικών αναγωγικών παραγόντων αργύρου είναι οι εξής.
(1) HCHO (όταν χρησιμοποιείται διάλυμα αμμωνίας ως συμπλεκτικός παράγοντας)
2AgNO3 + 2ΝΜ4OH → Ag2Ο + 2ΝΗ4ΟΧΙ3 + Η2O
Ag2Ο + 4ΝΗ4ΟΗ → 2[Ag(NH3)2]OH + 3H2O
2[Ag(NH3)2]OH + HCHO → 2Ag + 4NH3 + HCOOH + H2O
4AgNO3 + 4ΝΧ3 + Γ4H4O6NaK + H2O → 4Ag + 4NH4ΟΧΙ3 + Γ3H2O6NaK + CO2
4[Ag(NH3)3)2]ΟΧΙ3 + N2H4 → 4Ag + 4NH4ΟΧΙ3 + 4ΝΧ3 + N2
N2H4ΒΗ3 + 3Ag+ + 4OH– → 3Ag + Ν2H4 + Β(ΟΗ)4–+ 3/2 ώρες2
Πίνακας 2-48 Σκευάσματα που χρησιμοποιούν οργανικούς διαλύτες για επιμετάλλωση με άργυρο χωρίς ηλεκτρόλυση
| Συστατικά και οι συνθήκες επεξεργασίας τους | Νο. 1 | Αρ. 2 |
|---|---|---|
|
Διμεθυλοσουλφοξείδιο/mL Αιθυλενογλυκόλη/ml Αιθανόλη/mL d-(+)Γλυκόζη/mL Τριαιθυλαμίνη/mL Θερμοκρασία/°C Χρόνος/λεπτό Υλικό επιμετάλλωσης |
300 200 - - 15 70 20 Al2O3 σκόνη |
200 - 300 5 γρ. 2. 5mL/λεπτό 60 10 Νάιλον ύφασμα
|
Μεταξύ αυτών, οι διόλες και η γλυκόζη χρησιμοποιούνται ως αναγωγικά μέσα. Ταυτόχρονα, επειδή το διμεθυλοσουλφοξείδιο έχει ελαφρά αναγωγική ικανότητα, το διάλυμα επιμετάλλωσης δεν απαιτεί επεξεργασία γήρανσης. Τα επιμεταλλωμένα μέρη που προκύπτουν έχουν μεταλλική λάμψη που μοιάζει με άργυρο.
Οργανικές ενώσεις που περιέχουν δύο μονοθειολικές ομάδες χρησιμοποιούνται ως συμπλεκτικοί παράγοντες, με τον ακόλουθο δομικό τύπο:
Στον τύπο, το R1 και Ρ2 είναι αλκυλενικές ομάδες που περιέχουν 1~5 άτομα άνθρακα· R3 είναι μια αλκυλενική ομάδα που περιέχει 2~8 άτομα άνθρακα. Τα Χ και Υ μπορούν να είναι καρβοξυλικές, σουλφονικές, αμινομάδες, αλκυλομάδες, κ.λπ.
Οι αναγωγικοί παράγοντες περιλαμβάνουν αλδεΰδες, υδραζίνες, ενώσεις βοροϋδριδίου, ασκορβικό οξύ, κ.λπ. Ο Πίνακας 2-49 δείχνει παραδείγματα χρήσης αυτής της σειράς.
Πίνακας 2-49 Συνθήκες διεργασίας διαλύματος αναγωγής αργύρου με χρήση δύο οργανικών ενώσεων μονοθειόλης ως συμπλεκτικών παραγόντων
| Σύνθεση και οι συνθήκες επεξεργασίας της | Νο. 1 | Αρ. 2 | Αρ. 3 |
|---|---|---|---|
|
Νιτρικό άργυρο/(g/L) 1,2-Δις(2-καρβοξυαιθυλθειο)αιθάνιο/(g/L) 1,4-δις(2-καρβοξυαιθυλθειο)βουτάνιο/(g/L) 1,2,2'-(αιθυλθειο)διαιθυλομερκαπτάνη/(g/L) Ένυδρη υδραζίνη/(g/L) Φορμαλίνη/(g/L) Υποφωσφορώδες νάτριο/(g/L) pH (ρυθμισμένο με NaOH) Θερμοκρασία/°C |
0. 17 10 - - 8 - - 10 35 |
0. 31 - 15 - - 4 - 11 50 |
0. 34 - - 20 - - 10 10. 5 50 |
Τμήμα III Ανάλυση διαλύματος επιμετάλλωσης με κυανιούχο άργυρο
1. Ανάλυση Ασημιού
Πίνακας 2-50 Μέθοδος ανάλυσης ιόντων αργύρου για διάλυμα επιμετάλλωσης αργύρου
| Ακολουθία λειτουργίας | Σημειώσεις και οδηγίες |
|---|---|
|
(1) Πάρτε 5 ml διαλύματος επιμετάλλωσης σε ποτήρι ζέσεως 300 κυβικών εκατοστών, προσθέστε 20 ml θειικού οξέος και 5 ml νιτρικού οξέος ενώ παρατηρείτε. (2) Θερμάνετε μέχρι να παραχθεί λευκός καπνός (3) Προσθέστε 100 mL νερού και 3 mL θειικού σιδήρου αμμωνίου 10%. (4) Ογκομετρήστε με 0,1mol/L θειοκυανικό κάλιο. Τύπος υπολογισμού: Ag(g/L) = mL × 2,158× f AgCN(g/L) = Ag(g/L) ×1,2402 Στον τύπο, mL——0,1mol/L τίτλου θειοκυανικού καλίου. Συντελεστής διαλύματος θειοκυανικού καλίου f——0,1mol/L |
Λόγω της παραγωγής τοξικού αερίου υδροκυανίου, είναι απαραίτητο να λειτουργείτε σε περιοχή τοπικού αερισμού. Αλλαγή από καφέ καπνό σε λευκό καπνό Τελικό σημείο τιτλοδότησης: ανοιχτό κόκκινο χρώμα 0,1mol/L KCNS 1mL = 0,01079g Ag |
2. Μέθοδοι ανάλυσης ελεύθερου κυανίου
Πίνακας 2-51 Αναλυτικές Μέθοδοι για Ελεύθερο Κυάνιο
| Ακολουθία λειτουργίας | Σημειώσεις και οδηγίες |
|---|---|
|
(1) Πάρτε 5 ml διαλύματος επιμετάλλωσης σε ποτήρι ζέσεως 300 ml, προσθέστε 50 ml νερό (2) Προσθέστε διάλυμα ιωδιούχου καλίου 10% 1~2mL (3) Ογκομετρήστε με διάλυμα νιτρικού αργύρου 0,1mol/1 Τύπος υπολογισμού. Ελεύθερο KCN (g/L) = mL×2,60×f Ελεύθερο NaCN (g/L) = mL×1,96× f Στον τύπο, f - συντελεστής διαλύματος νιτρικού αργύρου 0,1mol/L |
Τελικό σημείο τιτλοδότησης: ανοιχτό κόκκινο χρώμα 0,1mol/L AgNO3 1mL = 0,0130g KCN = 0,0098g NaCN |