Как предотвратить потускнение серебра и нанести покрытие из безэлектролитного серебра
Покрытие серебром и антипокрытие для ювелирных изделий
Введение:
В этой статье рассказывается о том, как предотвратить потускнение серебряных и посеребренных изделий - распространенную проблему, когда поверхность темнеет из-за реакции с серой или светом. В ней подробно описаны различные способы борьбы с потускнением, включая неорганические методы, такие как электролиз хромата или олова, пропитка органическими соединениями и применение поверхностно-активных веществ. В тексте также рассказывается о том, что такое электролитическое серебрение, изучаются как вытесняющее покрытие для таких подложек, как медные цепи, так и восстановительное покрытие с использованием таких агентов, как формальдегид или гидразин. Наконец, в книге описано, зачем и как анализировать ключевые компоненты в растворах цианистого серебрения, такие как ионы серебра и свободный цианид.

Оглавление
Раздел I Профилактика потускнения серебра
Из-за высокой реакционной способности поверхности покрытия Ag, посеребренная поверхность склонна к обесцвечиванию при контакте с коррозионными средами (такими как H2S, SO2). Свет также передает избыточную энергию поверхности покрытия, способствуя ионизации Ag и реакции между Ag и коррозионной средой.
В таблице 2-28 показано влияние длины волны света и времени экспозиции на обесцвечивание Ag. В табл. 2-29 показано влияние времени экспозиции на цвет и химический состав.
Таблица 2-28 Влияние длины волны света и времени экспозиции на изменение цвета Ag
| Рэй | Время экспозиции/ч | ||||
|---|---|---|---|---|---|
| 6 | 12 | 18 | 24 | 48 | |
| 2527Å | Без изменения цвета | Желтые пятна | Желтовато-коричневый | Коричневато-черный | Коричневый |
| 3650Å | Без изменения цвета | Без изменения цвета | Без изменения цвета | Желтый | - |
| Солнечный свет | Без изменения цвета | Без изменения цвета | Без изменения цвета | Желтые пятна | - |
Таблица 2-29 Влияние времени экспозиции на цвет и химический состав поверхности с серебряным напылением
| 2537Å Цвет экспозиции света/ч | 6 | 12 | 18 | 24 | 48 |
|---|---|---|---|---|---|
| Цвет | Серебро | Желтый | Желтовато-коричневый | Коричневато-черный | Черный |
| Основной химический состав | Аг(металл) | Ag2O+AgO | Ag2O+AgO | AgO+Ag (Superfine) | Ag(Superfine) |
Из этих результатов видно, что продукты обесцвечивания представляют собой сульфиды, оксиды, хлориды или частицы серебра. Цвет Ag-покрытия после обесцвечивания варьируется в зависимости от химического состава. Такое изменение цвета не только влияет на декоративный вид серебряного покрытия, но и увеличивает электрическое сопротивление Ag-покрытия, что негативно сказывается на электрических свойствах серебряного покрытия.
Из этих механизмов обесцвечивания слоя Ag видно, что для предотвращения обесцвечивания слоя серебряного покрытия необходимо избегать контакта поверхности покрытия с кислородом, светом и агрессивными средами. В то же время формирование на поверхности плотного вещества (пленочного слоя), способного поглощать ультрафиолетовые лучи, должно оказывать ингибирующее воздействие на обесцвечивание гальванического слоя.
Среди традиционных методов предотвращения обесцвечивания слоев покрытия Ag - методы с использованием неорганических соединений, методы с использованием органических соединений, методы с использованием поверхностно-активных веществ, а также комбинированное использование этих методов.
1. Метод обработки неорганических соединений
Чтобы сравнить эффект от различных способов защиты от потускнения, на образцы наносилось покрытие Ag толщиной 2~3 мкм, а затем они замачивались в 0,2% растворе полисульфида аммония [(NH4)2SX] на определенное время. Для оценки использовался визуальный осмотр. Если визуальный осмотр был невозможен, использовался цифровой блескомер для измерения зеркального отражения, и рассчитывалась разница △ до и после вымачивания в растворе полисульфида аммония. В то же время при проведении испытаний в закрытых помещениях для измерения также использовался измеритель блеска.
В качестве средства против потускнения Ag были протестированы металлические пленки или пленки оксидов металлов с тем же тоном, что и Ag, таких как In, Zn, Cd, Cr, Pd, Rh, Sn, Be, Al, Th и Zr. Среди них электролитическая обработка хроматом показала наиболее выдающуюся функцию защиты от потускнения и получила широкое применение. Во-вторых, Rh и Be также являются одними из самых популярных.
(1) Обработка драгоценных металлов
Гальваническое покрытие сплавов Rh и Pd проводилось в оптимальных условиях, после чего были проведены эксперименты по изменению их тона и устойчивости к обесцвечиванию. Результаты приведены в таблице 2-30. Спекулярное отражение Rh составляет 70%, в то время как спекулярное отражение сплава (Pd80:Ni20) составляет около 57%. Несмотря на то, что толщина покрытия различна, может существовать некоторая корреляция. Толщина покрытия Rh составляет 0,1 мкм, а толщина покрытия Pd-Ni - 0,3 мкм. При увеличении толщины покрытия других металлов на Ag серебристый цвет нижележащего серебряного слоя исчезает. Однако при визуальном сравнении тона, яркости и относительных значений спекулярного отражения было обнаружено, что когда спекулярное отражение составляет 80%, отличие от серебряного цвета становится очевидным, а 70% является его пределом. Ниже этого значения серебряный цвет исчезает и переходит в цвет другого металла. Поэтому с точки зрения тона толщина Rh-покрытия менее 0,1 мкм является более подходящей. Однако его устойчивость к обесцвечиванию недостаточна, в то время как слой покрытия из сплава Pd-Ni толще и обладает хорошей устойчивостью к обесцвечиванию. Использование драгоценных металлов означает увеличение стоимости, но они обеспечивают хорошую лекарственную и износостойкую устойчивость. Чем выше устойчивость к обесцвечиванию, тем больше исчезает первоначальный цвет серебра. Поэтому повысить устойчивость к обесцвечиванию без изменения тона и яркости серебряного покрытия очень сложно.
(2) Обработка олова и оловянных сплавов
Сплавы Cu и Sn называются зеркальными сплавами. При содержании Sn выше 60% их цвет становится серебристо-белым, а зеркальное отражение - высоким, с хорошей коррозионной стойкостью. Поэтому их изучают с древних времен и используют в качестве зеркальных поверхностей в отражающих телескопах. При использовании в качестве серебряных антипотускневших покрытий они достаточно хорошо противостоят потускнению в течение 5~6 часов. Однако спекулярное отражение падает примерно до 65%, явно теряя серебряный цвет. Пригодность зеркальных сплавов зависит от степени тонировки. Хотя они дешевле драгоценных металлов, при увеличении толщины пленки до нескольких тысяч ангстрем возникает разность потенциалов между драгоценным металлом Ag и сплавом Cu-Sn, что может вызвать проблемы с коррозионной стойкостью.
Кроме покрытия из сплава Sn, металл Sn или соединения Sn, осажденные электролитическим способом или вымачиванием при температуре 50~100Å, также могут обладать устойчивостью к потускнению и повышенной погодоустойчивостью. Как средство против потускнения, оно может поддерживать стабильность контактного сопротивления контактов в течение длительного времени.
Результаты эксперимента приведены в таблице 2-30. По сравнению со щелочными и кислотными растворами, детали, обработанные кислотными растворами, имеют туманный белый осадок и не могут быть использованы для декоративных целей. В отличие от этого, детали, обработанные щелочными растворами и электролитическим способом, не вызывают никаких проблем в краткосрочной перспективе.
Таблица 2-30 Устойчивость неорганических соединений к обесцвечиванию на поверхностях с серебряным напылением
| Серийный номер | Состав раствора | Условия обработки | Условие возникновения видимого цвета | Примечание |
|---|---|---|---|---|
| 1 |
PNP (Nissin Kasei, Япония) Покрытие из сплава Pd-Ni |
DK lA/dm2 Комнатная температура 1мин
|
Выше 6 часов | Потеря серебристого цвета, плохой CN- сопротивление |
| 2 |
Оловянный (Daiya Shokai) Покрытие из сплава Cu-Sn
|
3V 55℃ 40s
|
Выше 6 часов | Потеря серебряного цвета |
| 3 |
Na2Cu(CN)3 24 г/л Na2SnO3 90 г/л Свободный NaCN 16 г/л NaOH
|
Dk 2A/дм2 60℃ 30s
|
Выше 6 часов | Потеря серебристого цвета, лучше, чем серебристый цвет 1 и 2. |
| 4 |
Na2SnO3 90 г/л CH3COONa 0 г/л, 5 г/л, 10 г/л
|
DK 0. 5 А/дм2 Комнатная температура 15〜90s
|
10 〜20s | Добавление CH3COONa может стабилизировать раствор, и чем дольше длится электролиз, тем он стабильнее, но при этом теряет свой серебристый цвет. |
| 5 |
SnCl2 20 г/л 0. 025NHCl 50мл/л
|
Комнатная температура 1мин
|
10 мин | |
| 6 |
SnCl2 20 г/л 0,025NHCl 50мл/л
|
DK 0. 1 〜 2A/dm2 Комнатная температура, 10 с
|
10 мин | Белый |
|
Комнатная температура, 1 мин, 10 мин |
Слегка пожелтевшие | |||
| 7 | Фтороборат олова 3% |
DK 0. 1 ~ 2 А/дм2 Комнатная температура, 10 с
|
- | Белый |
| Комнатная температура, 1 мин, 10 мин | 10 мин | Слегка желтый | ||
| 8 |
Сульфат калия 20 г/л Йодная кислота 30 мл/л
|
DK 0. 1 〜 2 A/dm2 Комнатная температура ,10 с
|
- | Белый |
| 9 |
Фтороборат натрия 20 мл/л Плавиковая кислота 30 мл/л Фторборная кислота 20 г/л
|
Комнатная температура ,1мин, 10мин DK 0. 1 〜2 A/dm2 Комнатная температура ,10 с |
10 мин - |
Слегка желтоватый Белый
|
| Комнатная температура, 1 мин, 10 мин | 10 мин | Слегка желтый | ||
| 10 |
BeSO4 , 4H2O 2 г/л pH = 5. 7〜5. 8
|
DK 0. 007 A/дм2 Комнатная температура 3〜10 мин
|
Более 1 ч | |
| 11 |
BeSO4 , 4H2O 2 г/л pH = 5. 8
|
1 〜2. 4V 20с~4мин
|
20мин | |
| 12 | EverShine S (Tamura Chemical) |
6.5V Комнатная температура 90s
|
15мин | |
| 13 |
K2CrO4 15 г/л NaOH 30 г/л
|
2〜6V Комнатная температура 15〜120s
|
10 〜30s | Чем дольше электролиз, тем лучше. |
| 14 |
K2CrO4 30 г/л NaOH 40 г/л
|
DK 4A/дм2 Комнатная температура 30〜40s
|
Белое запотевание Нет серебряного цвета
|
|
| 15 |
K2CrO4 30 г/л NaOH 40 г/л Отопление 20 ч
|
Белое запотевание Нет серебряного цвета
|
||
| 16 |
Эл2(SO4)3 4 г/л Оксалат аммония 2 г/л pH = 5. 8
|
DK 0,06 А/дм2 Комнатная температура 30с〜1мин
|
20 〜30s | То же время, что и без лечения |
| 17 | Карбонат натрия | |||
| 18 |
Na2SnO3 8. 5 г/л CH3COONa 5 г/л (№ 4)
|
DK 0. 5A/дм2 15 〜30s Комнатная температура
|
Выше 6 часов | |
|
K2CrO4 15 г/л KOH 30 г/л (№ 13)
|
2〜3V 30s Комнатная температура
|
|||
| 19 |
K2CrO4 15 г/л KOH 30 г/л K2CO3 50 г/л
|
6V 15 〜60s
|
10 〜30мин |
(3) Обработка бериллия
Нанесение пленки оксида бериллия на Au, Cu и латунь в качестве обработки, изменяющей цвет, позволяет добиться хорошего эффекта. Принцип, используемый в этом методе, таков: изоэлектрическая точка гидроксида бериллия составляет pH=5,8, и может произойти следующая электролитическая реакция:
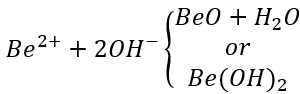
(4) Обработка алюминия
Имеются сообщения об образовании оксидной пленки, подобной Be; дополнительные эксперименты не выявили разницы между обработанными и необработанными образцами, и оксидная пленка не могла образоваться.
(5) Обработка хроматом
Серебрение - наиболее распространенный метод антитусклой обработки латунных покрытий. Существует два метода обработки хроматом: катодный электролиз и вымачивание, но метод катодного электролиза намного лучше.
Добавки, используемые в хроматных электролитах, включают: K2CO3, Na2CO3, KCN, NaS2O3, KCNS, NaCl, KI, EDTA и др. Среди них K2CO3 Результаты экспериментов показали, что он также может выступать в качестве проводящей соли, тем самым сокращая время электролиза по сравнению с тем, когда он не добавлен. Влияние других добавок не показало существенных различий.
Недостатком электролизной обработки хроматом является то, что пленка плохо переносит ультрафиолетовое излучение и становится коричневой после длительного пребывания в помещении.
2. Обработка органическими соединениями и поверхностно-активными веществами
Таблица 2-31 Эксперимент по борьбе с обесцвечиванием органических соединений
| Категоризация | Серийный номер | Органические соединения | Физические свойства | Растворимость | Условия обработки | Внешний вид | Гидрофобность | Антидисколоритный эффект |
|---|---|---|---|---|---|---|---|---|
| Алифатический амин | 1 |
Этиламин (водный раствор 70%) CH3CH2NH2
|
Mw 45. 09 d15 0. 6892 Температура плавления 83,3℃ Температура кипения 16℃ |
(Водные) спирты Эфир
|
0. 1моль/л (0. 65мл/л) 0. 01моль/л (6. 5мл/л) Комнатная температура, 20 мин, 60 мин |
pH 10〜11 Бесцветный Прозрачный O |
X | X |
| 2 |
Додециламин CH2(CH2)11NH2 |
Mw 18. 5 Температура плавления 25℃ Температура кипения 247℃ |
Ацетон (Этанол) |
0. 1моль/л (18. 5г/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный Пятно от воды |
X | X | |
| 3 |
Трибутиламин (CH3CH2CH2CH2)3N |
Mw 185 d 0. 7782 Температура кипения 216,5℃ |
(Этанол) Эфир
|
0. 1моль/л (24мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
X | X | |
| Ароматические амины | 4 | О-Толуидин |
Mw 107. 16 d20 0. 9989 Температура кипения 199. 7℃ |
Вода 1. 5(25) (Этанол) Эфир |
0. 1моль/л (24мл/л) Комнатная температура, 20 мин, 60 мин |
Красновато-коричневый прозрачный O |
X | X |
| 5 | Дифениламин |
Mw 169.23 d 1.159 Температура кипения 302℃ |
(Этанол) 56 Эфир |
0. 1 ммоль/л (17 г/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный прозрачный Пятно от воды |
X | X | |
| Диамины, полиамины | 6 | H2N(CH2)2NH2 |
Mw 45.09 d35 0.892 Температура плавления 8,5℃ Температура кипения 117℃ |
(вода) Этанол |
0,1 ммоль/л (6. 7 ммоль/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 10〜11 O |
X | X |
| Диамин, полиамин | 7 |
Диэтилентриамин H2 N(CH2 )2 NH(CH2 )2 NH2 |
Mw 103 Температура кипения 208℃ |
(вода) Этанол |
0. 1моль/л (10мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 10〜11 O |
X | X |
| 8 |
Триэтилентетрамин H2 N(CH2 )2 NH(CH2 )2 NH2 (CH2 )2 NH2 |
Mw 146 Температура плавления 208℃ Температура кипения 174℃ |
(вода) |
0,1моль/л (15мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 10〜11 O |
X | X | |
| Аминоспирты | 9 |
Триэтилентетрамин H2N(CH2)2NH(CH2)2 NH(CH2)2NH2 |
Mw 189 | (вода) |
0. 1моль/л (19мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 10〜11 O |
X | X |
| 10 |
Этаноламин HO(CH2)2NH2 |
Mw 61.09 d27 1.0111 Температура кипения 171℃ |
(вода) Этанол |
0. 01моль/л (0,61мл/л) 0,1 ммоль/л (6,1 ммоль/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9〜10 O |
X | X | |
| 11 |
Диэтаноламин (HOCH2CH2)2NH |
Mw 105.14 d20 1.0916 Температура плавления 28℃ Температура кипения 268℃ |
(вода) Этанол |
0. 01моль/л (0,96мл/л) 0,1 ммоль/л (9,6 ммоль/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9〜10 O |
O | X | |
| 12 |
Триэтаноламин (HOCH2CH2)3NH |
Mw 149.19 d20 1.124 Температура плавления 21,2℃ Температура кипения 227℃ |
(вода) Этанол |
0. 01моль/л (1,3мл/л) 0,1 ммоль/л (13 мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9〜10 O |
O | X | |
| 13 |
2N-диэтиламин (CH2)2NCH2CH2OH |
Mw 93.1 Температура кипения 39,5℃ |
(вода) |
0. 1моль/л (0,89мл/л) 0. 01моль/л (8,9мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9〜10 O |
O | X | |
| 14 | 2-Amino-2-ethyl-1,3-propanediol | Mw 105 | (вода) |
0,01 ммоль/л (1,1 г/л) 0. 1 ммоль/л (11 г/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9〜10 O |
O | X | |
| Амид | 15 | Ацетамид |
Mw 59.07 d 1.159 Температура плавления 52,62℃ Температура кипения 221℃
|
(вода) Этанол |
0. 1моль/л (5,1мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
△ | X |
| 16 | Акриламид |
Mw 71.1 d 1.122 Температура плавления 85℃ |
(вода) Этанол Эфир Трихлорметан
|
0. 1моль/л (7,1мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
△ | X | |
| 17 | Бензиламин |
Mw 121.14 d 1.341 Температура плавления 128℃ Температура кипения 290℃ |
(вода) Этанол
|
0. 1моль/л (12г/л) 30℃ Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
O | X | |
| Оксим | 18 | Бутандиоксим |
Mw116.12 Температура плавления 240℃ |
(Этанол) Эфир (Вода) |
0. 01моль/л (0,12 г/л) 0. 001моль/л (1,2 гмоль/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
X | X |
| 19 | Бензогидрин оксим |
Mw227 Температура плавления 154℃ |
(Этанол) (Аммиак)
|
0,01 ммоль/л (0,23 г/л) 0. 001моль/л (2,3 г/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный △ |
X | X | |
| Пиридин | 20 | Пиридин |
Mw 79.10 d20 0.977 Температура кипения 115,5℃ |
(вода) Этанол |
0. 001моль/л (0,1мл/л) 0,1 ммоль/л (8 мл/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный O |
X | X |
| Хинолин | 21 | Хинолин |
Mw 127.16 d20 0.938 Температура плавления -15℃ Температура кипения 238℃ |
Горячая вода, разбавленная кислота, этанол, эфир, дисульфид углерода (6 ммоль/л HCl) 2~20моль/л |
0,1% (1 г/л) 1% (10 г/л) Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 2~4 O |
O | X |
| 22 | Карбоксихинолин |
Mw 145 Температура плавления 75~76℃ |
Этанол, ацетон, трихлорметан, бензол (6 ммоль/л HCl) 2~20моль/л |
0,1% (1 г/л) 1% (10 г/л) Комнатная температура, 20 мин, 60 мин |
Желтый прозрачный pH 2~4 O |
X | X | |
| Хинолин | 23 | Бутандиоксим | Mw 256 |
Неорганическая кислота (6 ммоль/л HCl) 40 ммоль/л Этанол |
0,1% (1 г/л) 1% (10 г/л) Комнатная температура, 20 мин, 60 мин |
Желтый прозрачный pH 10~11 O |
X | X |
| Диазосоединения | 24 | п-Этокси-2,4-диаминоазобензол | Mw 256 |
Неорганическая кислота (6 ммоль/л HCl) 40 ммоль/л Этанол |
0,1% (1 г/л) 1% (10 г/л) Комнатная температура, 20 мин, 60 мин |
Красный Прозрачный O |
O | X |
| Гидроксикарбоновая кислота | 25 | Дубильная кислота | Желтовато-белый, светлый цвет, порошок |
(вода) Этанол Ацетон |
0.1% 0.1% 5% |
Бесцветный прозрачный pH 6 Желтый прозрачный pH 4 Желтовато-коричневый прозрачный pH 2 |
X | X |
| Тиомочевина | 26 | 1-Ацетил-2-тиомочевина |
Mw 118.16 Температура плавления 165℃ |
(вода) Алкоголь |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 7 O |
O | X |
| Тиомочевина | 27 | Aminothioureas |
Mw 95.6 Температура плавления 81 ~ 183℃ |
(6 ммоль/л HCl) 50 мл/л |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 1 O |
X | X |
| 28 | Дитизон | Mw 256 |
(Трихлорметан) Тетрахлорид углерода |
10 г/л Комнатная температура, 20 мин, 60 мин |
Синее пятно от воды Становится желтым |
O | X | |
| Моносахарид | 29 | Аскорбиновая кислота (витамин C) |
Mw 176 Температура плавления 190~192℃ |
(вода) |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 1 O |
X | X |
| Имидазолы | 30 | 1-Ацетил-2-тиомочевина |
Mw 155 Разложение 287~288℃ |
Метанол Вода 45 мл
|
1 г/л, 10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 1 O |
X | X |
| 31 | 2-Гептадецилимидазол |
Метанол 55 мл Вода 45 мл Растворение Спирт, кислота |
1 г/л, 10 г/л Комнатная температура, 20 мин, 60 мин |
Белая подвеска Неровный Приверженность белым |
O | O | ||
| Бензимидазолы | 32 | 2-меркаптопиридин |
Mw 150 Температура плавления 301~302℃ |
Метанол 15 мл Вода 45 мл Горячая вода Этанол NaOH |
1 г/л, 10 г/л Комнатная температура, 60℃ 20 мин, 60 мин |
Бесцветный прозрачный O |
O | X |
| Триазолы | 33 | 3-Amino-1,2,3-triazole |
Mw 159 Температура плавления 159℃ |
(вода) Этанол Трихлорметан |
Комнатная температура, 60℃ 1 мин, 10 мин, 60 мин |
O | - | X |
| Бензотриазол | 34 | Бензотриазол |
Mw 119.13 Температура плавления 99℃ |
Горячая вода Алкоголь |
12 г/л, pH 6 60℃ 1 мин, 3 мин, 10 мин
|
Бесцветный Прозрачный O |
- | X |
| Триазин | 35 | Триэтилендиамин |
Mw 140 Сублимация при температуре выше 230°C |
(вода) Гидрат (CN2)2N Трихлорметан Алкоголь |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 8 O |
X | X |
| Оксазол | 36 | 2-Оксобензазол |
Mw 1151 Температура плавления 143,2℃ |
Аммиак 6 ммоль/л аммиака 200 мл/л Уксусная кислота Эфир |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 10 O |
O | X |
| (Оксо)зины | 37 | Морфолин |
Mw 87.12 d13 1.0007 Температура кипения 128℃ |
(вода) Алкоголь Эфир |
10 г/л Комнатная температура, 20 мин, 60 мин |
Бесцветный Прозрачный pH 9~10 O |
X | X |
| Тиазол | 38 | Ортанин |
Mw 264 Температура плавления 200~246℃ (Разложение) Красные игольчатые кристаллы
|
Сильные кислоты Плотный Трихлорметан Эфир Бензол (ацетон)
|
1 г/л Комнатная температура, 20 мин, 60 мин |
Красный прозрачный (Красный осадок) Коричневое пятно от воды |
O | X |
| Бензотиазол | 39 | Бензотиазол |
Mw 135.39 d12 1.2349 Температура кипения 231℃ |
(Этанол) Этиловый эфир |
1 г/л Комнатная температура, 3 мин, 60 мин |
Красновато-коричневый Прозрачный O |
△ | X |
| 40 | 2-Гидрофобный бензотиазол |
Mw 167 Температура плавления 177℃ |
Этанол Этиловый эфир Бензол Уксусная кислота Карбонат калия Гидроксид калия Гидроксид натрия 2 г/л |
1 г/л Комнатная температура, 3 мин, 60 мин |
Белый мутный pH 10 O |
X | O | |
| Нафталины | 41 | Разбавитель нафталина |
Mw 217 Температура плавления 109,5℃ |
Вода (20℃) 0,01 г/л |
0,2 г/л (осадки) Комнатная температура, 2 мин, 10 мин, 30 мин |
O | - | X |
| Изоацетон |
10 г/л Комнатная температура, 10 мин, 60 мин |
Желтый прозрачный Пятно от воды
|
O | O | ||||
|
Изоацетон 50% Вода 50% |
5 г/л Комнатная температура, 10 мин, 60 мин |
Желтый прозрачный Пятно от воды
|
O | O |
Таблица 2-32 Эксперимент по борьбе с обесцвечиванием с помощью поверхностно-активных веществ
| Серийный номер | Имя (название компании) | Статус | Концентрация | Условия обработки | Внешний вид | Гидрофобность | Эффект ингибирования | Примечания |
|---|---|---|---|---|---|---|---|---|
| 1 | Средство для предотвращения ржавчины MC- 501 (Japan Lion Grease) |
Светло-красный прозрачный, d 1.06 pH 8. 0〜8. 5 |
2%,10% | Комнатная температура 20 мин, 60 мин | O | O | Ag:x | |
| 2% | Комнатная температура 15с, 10мин | O | O | Cu:Погружение в воду X, испытание на воздействие △. | 15s better | |||
| 2 | Enajiko-ru CNS (Японская львиная смазка) |
Амфотерный pH 8〜9 |
1% | Комнатная температура 20 мин, 60 мин (Ag)15 с, 10 мин (Cu) | O | O | Ag:x Cu:Погружение в воду X, испытание на экспозицию:. | 1% 15s хорошо |
|
15% Бензолсульфонат натрия 15% (нейтральный)
|
Комнатная температура 20мин, 60мин (Ag)15с, 10мин (Cu) | Коричневый, белый осадок | O | |||||
|
10% Пирофосфат калия 5% (щелочной) |
Комнатная температура 20мин, 60мин (Ag) 15с, 10мин (Cu) |
Белая мутность O |
O | |||||
| 3 | Ripa-ru OH- 104P (Японская львиная смазка) | 0.1% | Комнатная температура 20 мин, 60 мин |
Бесцветный и прозрачный O Желтовато-белый мутный O
|
O △
|
Ag:x | ||
| 1% | ||||||||
| 10% | ||||||||
| 4 | Dyuomin CD (Japan Lion Grease) | 0.1% | Комнатная температура 20 мин, 60 мин |
Белое облако O Желтые мутные полосы O
|
O | Ag:x | ||
| 1% | ||||||||
| 10% | ||||||||
| 5 | Dyuomin CDA-50 (Lion Grease, Япония) | 0.1% | Комнатная температура 20 мин, 60 мин |
Бесцветный и прозрачный O
|
△ O
|
Ag:x | Немного лучше в течение 60 минут | |
| 1% | ||||||||
| 10% |
Мутно-желтый O |
|||||||
| 6 | FC-98 (Kanto Chemical, Япония) | Анионный белый порошок, содержащий фтор |
0.1% 1%
|
Комнатная температура 20 мин, 60 мин |
Бесцветный и прозрачный pH 5~7 Крапчатые знаки
|
O | ×(Ag) | |
| 7 | FC-134 (Kanto Chemical, Япония) | Фторсодержащий ион кислорода чайно-коричневый порошок |
0.1% 1% (Этанол) |
Комнатная температура 20 мин, 60 мин 5 минут, 30 секунд |
Желтый прозрачный, Прозрачный желтовато-коричневый pH 6 Крапчатые знаки
|
O | ○(Ag) | Маркировка исчезает при понижении температуры |
| 8 | Мягкая дата-дженто W (смазка для японских львов) | Катионный Белый порошок | 1% | Комнатная температура 20 мин |
Белый мутный pH 7 O
|
X | X |
OH RCH2CH(CH2)nSO3Na (MIX) α-Аллилсульфонат
|
| 9 | Рипомин COH (Японская львиная смазка) | Амфотерная жидкость | 1% | Комнатная температура 20 мин |
Белый мутный pH 8 O
|
O | X | Имидазолил |
| 10 | Perettex TR (Kao, Япония) |
Катионный Бесцветный прозрачный
|
1% | Комнатная температура 20 мин |
Белый мутный pH 10 O
|
O | X |
RODC-CH-SO3N4R-OOC-CH3 Дипропилсульфосукцинат натрия
|
| 11 | Ema-ru 20C (Kao, Япония) |
Катионный Светло-желтая жидкость
|
1% | Комнатная температура 20 мин |
Бесцветная мутность pH 7 O
|
X | X |
R-O(CH2 OH)nSO3Na Полиоксиэтиленалкиловые кислоты
|
| 12 | Koutamin 24P (Као, Япония) |
Анионный Белый твердый
|
1% |
Бесцветный и прозрачный pH 7 O
|
O | X | Триметиламин | |
| 13 | Perettex # 1222 (Kao, Япония) | Неионные | 1% | Комнатная температура 20 мин |
Белое облако O
|
O | X | |
| 14 | Perettex # 1265 (Kao, Япония) | Неионные | 1% | Комнатная температура 20 мин |
Бесцветный и прозрачный O
|
O | X | |
| 15 | Soft-kurin QA-1 (Миёси, Япония) |
Амфотерный Белый твердый
|
1% | Комнатная температура 20 мин |
Бесцветная мутность pH 7 O
|
O | X | β-аланиновый тип |
| 16 | Soft-kurin MA-3-70 (Миёси, Япония) | Амфотерный | 1% | Комнатная температура 20 мин |
Бесцветный и прозрачный pH 8 O
|
O | X | |
| 17 | Марусенокку Агт (Япония Ма-русеру) | Средство против потускнения серебра |
3 мл/л 30 мл/л
|
Комнатная температура 30 с, 60 мин |
Белое облако pH 8 Адгезия
|
O | △ | Обратитесь к руководству по эксплуатации |
| 18 | Dainshiruba-SS (Yamato Kasei, Япония) | Средство против потускнения серебра |
10% Изопропил Кетон 50% Вода 10%
|
25~30℃ 4 мин, 20 мин, 60 мин
|
Бесцветный и прозрачный pH 8 O
|
O | X | Обратитесь к руководству по эксплуатации |
| 19 | T611 (Uemura Kogyo, Япония) | Средство против потускнения серебра |
Жидкость 10% 90%
|
Комнатная температура 30 с, 2 мин, 10 мин, 60 мин | Бесцветные прозрачные пятна | O | O | Обратитесь к руководству по эксплуатации |
| 20 | Рукоринсу-эйдо (Айкоруко, Япония) | Средство против потускнения серебра | 1% | Комнатная температура 31 мин, 5 мин, 30 мин |
Белое облако pH 7 O
|
O | X | Для использования на электронных заводах |
Среди органических соединений, обладающих противоаггравным эффектом при замачивании в 0,2% растворе полисульфида аммония, можно выделить 2-17 алканимидазол, 2-меркаптобензимидазол и комплексообразователи.
Органические соединения, обладающие такими антиобесцвечивающими свойствами, имеют следующие характеристики:
① Обработка проводится в щелочной области, близкой к pH 7.
② Содержит гидрофобные группы (длинноцепочечные алкилы, фенилы).
③ Содержит диметиламиновые группы или группы -SH, или содержит двойные связи.
④ Нерастворим в воде.
⑤ Бесцветное, близкое к твердому вещество.
Однако некоторые случаи удовлетворяют вышеуказанным условиям, но не обладают антидисколорирующим действием, например, 2-меркапто бензимидазол и 2-тиазолил бензимидазол.
Взаимоотношения между ними до сих пор не очень понятны.
Эффекты FC-134 и T611 были подтверждены в отношении антидисколорирующего действия поверхностно-активных веществ. В то же время были проведены эксперименты по совместному действию органических соединений и ПАВ (ФК-134), и значительного эффекта обнаружено не было (табл. 2-33). Стойкость к обесцвечиванию 0,2% раствора полисульфида аммония длится не более 10 минут. При этом устойчивость к растворителям (разбавителям) также относительно слабая. Для устойчивости декоративных изделий к обесцвечиванию из-за наличия пятен, учитывая все эти проблемы, единственным возможным вариантом является использование 2-меркаптобензимидазола с FC-134 (см. табл. 2-34).
Таблица 2-33 Комбинированное воздействие органических соединений и поверхностно-активных веществ на антидисколоризацию слоев с серебряным напылением
| Серийный номер | Состав | Условия обработки | Внешний вид | Гидрофобность | Свойство анти-изменения цвета | Примечания |
|---|---|---|---|---|---|---|
| 1 |
2-Гептадекамидазол лг/л FC-134 1 г/л EtOH : H2O = 1 :1 |
Комнатная температура 1 мин, 60 мин |
Белый осадок pH7 Адгезия | O |
O Менее эффективен, чем при самостоятельном использовании
|
|
| 2 |
2-Меркаптобензимидазол 1 г/л FC-134 1 г/л NaOH 2 г/л
|
Комнатная температура 1 мин, 60 мин |
O | X |
O Лучше, чем при самостоятельном использовании |
Снижение пенообразующей способности, чем дольше, тем лучше |
| 3 |
Меркаптон 5 г/л FC-134 0. 5 г/л Изоацетон:H2O = 1 :1 |
Комнатная температура 1 мин, 60 мин |
O |
O Лучше, чем при самостоятельном использовании
|
Снижение пенообразующей способности, чем дольше, тем лучше |
Таблица 2-34 Влияние растворителей на антидисколяционную пленку
| Органические соединения | Условия обработки | Растворитель | Внешний вид | Антидисколоритный эффект |
|---|---|---|---|---|
| 2-Гептадекамидазол |
1 г/л (C2H5OH : HO = 1 : 1) 20мин
|
Пятна | O | |
|
Разбавитель (5 мин.)
|
Пятна исчезают O
|
X | ||
|
Алкоголь (5 мин)
|
Пятна исчезают O
|
X | ||
| Крупнодисперсное распыление | Царапина |
O Только поцарапанная часть обесцвечивается
|
||
| 2-Меркаптобензимидазол |
10 г/л NaOH 2 г/л Комнатная температура 20мин
|
O | O | |
|
Разбавитель (5 мин.)
|
O | X | ||
|
Алкоголь (5 мин.)
|
O | △ | ||
| Крупнодисперсное распыление | Царапина |
O Только поцарапанная часть обесцвечивается
|
Приведенные выше экспериментальные результаты обобщены следующим образом.
① Трудно гарантировать, что уникальный тон и блеск Ag не будут повреждены при нанесении других драгоценных металлов на Ag для антитускневой обработки.
② При использовании сплавов Sn или Sn, когда толщина Sn составляет 50~10Å, может быть достигнут эффект антипокрытия, но эффект от этого метода ограничен.
③ Обработка Be и Al не оказывает существенного влияния.
④ Классические методы обработки, такие как обработка хроматами, дают относительно хороший эффект. Однако их главный недостаток заключается в том, что обработанная пленка обладает слабой устойчивостью к УФ-излучению и может стать коричневой при длительной защите.
⑤ Среди органических соединений, обладающих антидисколорирующими свойствами, можно назвать 2-гептадецилимидазол, 2-алкилбензимидазол и меркаптонафталиновые агенты. Однако другие органические соединения с такой же структурой не обязательно обладают такой же способностью к обесцвечиванию.
⑥ Эффективность FC-134 в поверхностно-активных веществах, продаваемых на рынке, была подтверждена.
3. Антидисколорирующий эффект комбинированной обработки электролизом олова и электролизом хромовой кислоты
(1) Испытание на устойчивость к обесцвечиванию и метод измерения обесцвечивания
Условия проведения теста на обесцвечивание приведены в таблице 2-35.
Таблица 2-35 Условия для проведения испытания на устойчивость к обесцвечиванию
| Решение |
Раствор сульфида аммония (желтый) (Showa Chemical) (NH4)2Sx(2%) |
| Температура | 20℃ |
| Время выдержки | 2h |
△(%) = L1 - L2 (2-1)
В формуле,
L1- отражательная способность перед тестом на изменение цвета, %;
L2- отражательная способность перед тестом на изменение цвета, %.
(2) Оловянный электролит
В ходе экспериментов по изучению влияния условий обработки оловянного электролита было установлено, что концентрацией станната натрия, временем электролиза, плотностью тока и температурой обработки можно пренебречь в отношении их влияния на характеристики устойчивости к обесцвечиванию. В то же время ацетат натрия был добавлен в качестве стабилизатора при щелочном осаждении Sn. Состав и оптимальные условия для электролиза Sn приведены в таблице 2-36.
Таблица 2-36 Состав и оптимальные условия для электролиза Sn
| Состав гальванического раствора |
NaSnO3 - 3H2O 8. 5 г/л CH3COONa ・ 3H2O 5 г/л |
| Условия лечения |
Плотность тока 0. 5A/дм2 Время электролиза 15 с (10〜30 с) Температура 20℃ (7〜30℃) Материал анода Пластина из нержавеющей стали |
(3) Взаимосвязь между излучательной способностью и временем электролиза
Зависимость между отражательной способностью и временем электролиза показана на рис. 2-8. По мере увеличения времени электролиза отражательная способность резко снижается, что ухудшает оттенок Ag. При времени электролиза около 90 секунд Ag приобретает оловянно-белый цвет, а при времени электролиза около 180 секунд на поверхности появляются светло-коричневые полосы. В то же время, когда время электролиза превышает 60 секунд, электрические свойства также ухудшаются. Экспериментальные результаты, полученные в соответствии с уравнением (2-1), показаны на рис. 2-9. С увеличением времени электролиза значение △ уменьшается.
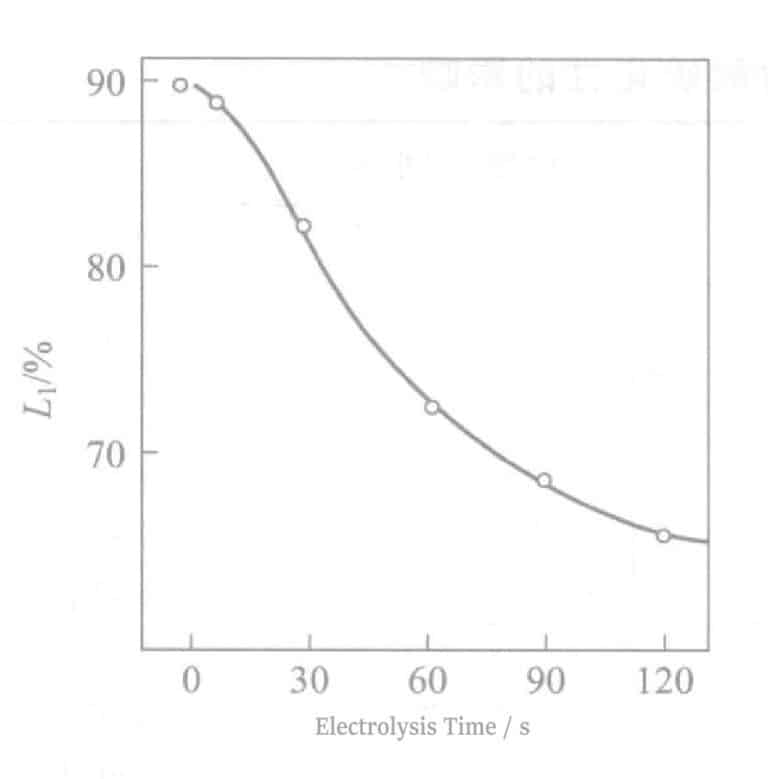
Рисунок 2-8 Зависимость между отражательной способностью и временем электролиза
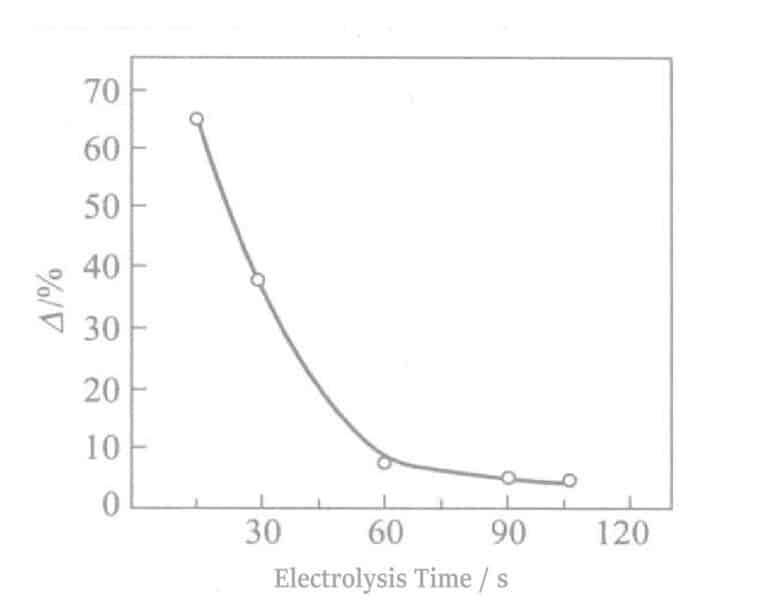
Рисунок 2-9 Время электролиза и устойчивость к обесцвечиванию
(4) Толщина пленки электролитического олова и электролиз
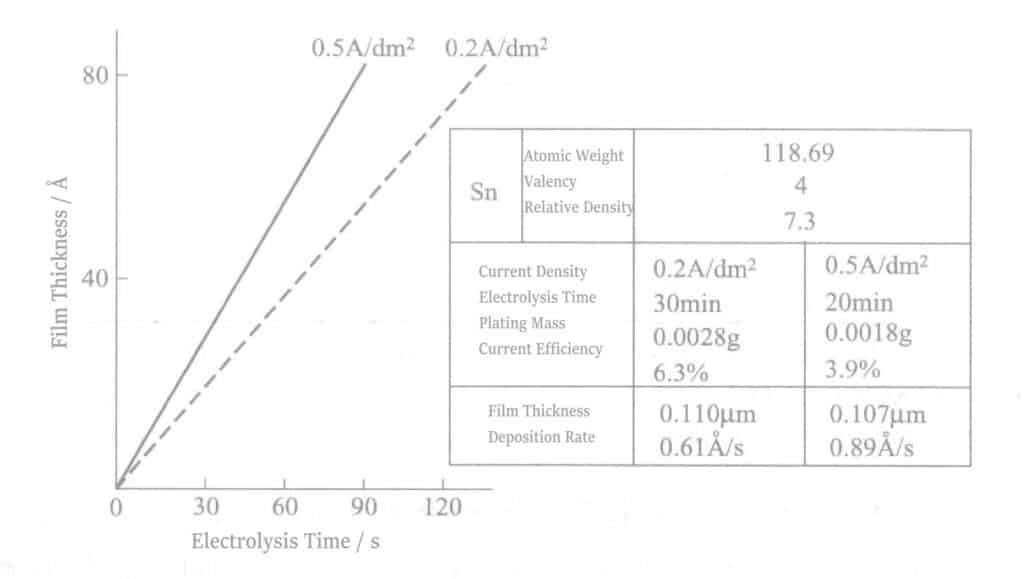
Учитывая эффективность катодного тока в соответствии с законом Фарадея, зависимость между временем электролиза и толщиной пленки показана на рис. 2-10. Толщина олова составляет около нескольких десятков ангстрем.
(5) Влияние примесей
Влияние возможных примесей (CN, Ag, Cu, Ni и т.д.), которые могут быть подмешаны в электролит, указанный в таблице 2-36, на внешний вид и сульфидостойкость электролитической мембраны было подтверждено экспериментально. Результаты приведены в таблице 2-37.
Таблица 2-37 Влияние примесей на стойкость серы
| Примеси | Концентрация/×10-6 | Время электролиза /с | ||
|---|---|---|---|---|
| 30 | 60 | 120 | ||
| Нет | 0 | O | O | △ (белый) |
| CN |
20 200 2000 20000 |
O O O △,белый |
O △,белый △,белый △,белый |
△,белый △,белый △,белый △,белый |
| Ag |
20 50 100 150 200 400 |
O O △ X X X |
O △,красный X, красно-черный X, красно-черный X, красно-черный X, черный |
△,красный △, красно-черный X, красно-черный X, красно-черный X, черный X, черный |
| Cu |
20 200 300 400 500 600 1000 |
O O O △,красный △,красный красный красный |
O O △,белый △,красный Красный Красный Красный |
△,белый △,белый △,красный △,красный Красный Красный Красный |
| Ni |
20 200 1000 |
O O O |
O O O |
O O O |
|
Примечание: 1. Используемые соединения: CN-NaCN;Ag-KAg(CN)2;Cu-KCu(CN)2; Ni-Ni (CN)2 - 2KCN - 2H2O. 2. Степень изменения цвета: ○ без изменения внешнего вида; △ незначительное изменение цвета; × изменение цвета.
|
||||
(6) Электролиз хромата
Кроме хромата, в электролите могут присутствовать неорганические соли, такие как (Na2CO2, KCN, KI, Na2S2O3, и т.д.), используются в качестве добавок. Эти водные растворы давно известны как средства против потускнения серебра. Основной состав электролита приведен в табл. 2-38.
Таблица 2-38 Условия электролитического процесса Cr
| Состав электролита |
K2 CrO4 15 г/л NaOH 30 г/л |
| Используется после 30-часового процесса нагревания и созревания | |
| Условия лечения |
Напряжение 6 В (2 〜 6 В) Время электролиза 15 с (60 с) Температура 20℃ Материал анода Пластина из нержавеющей стали |
(7) Взаимосвязь между отражательной способностью и временем электролиза
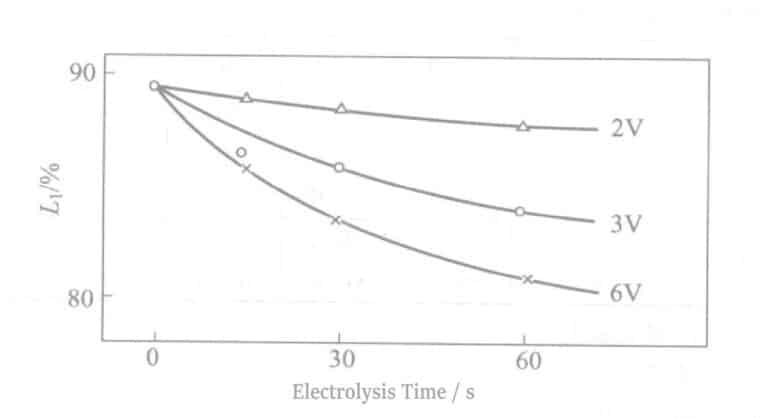
Зависимость между отражательной способностью при напряжении 2~6 В и временем электролиза показана на рис. 2-11. При увеличении напряжения толщина пленки Cr увеличивается, а отражательная способность уменьшается. В отличие от случая с электролитом Sn, при тех же условиях напряжения увеличение времени электролиза не влияет на отражательную способность.
7. Взаимосвязь между отражательной способностью и временем электролиза
Зависимость между отражательной способностью при напряжении 2~6 В и временем электролиза показана на рис. 2-11. При увеличении напряжения толщина пленки Cr увеличивается, а отражательная способность уменьшается. В отличие от случая с электролитом Sn, при тех же условиях напряжения увеличение времени электролиза не влияет на отражательную способность.
(8) Устойчивость к сульфидам
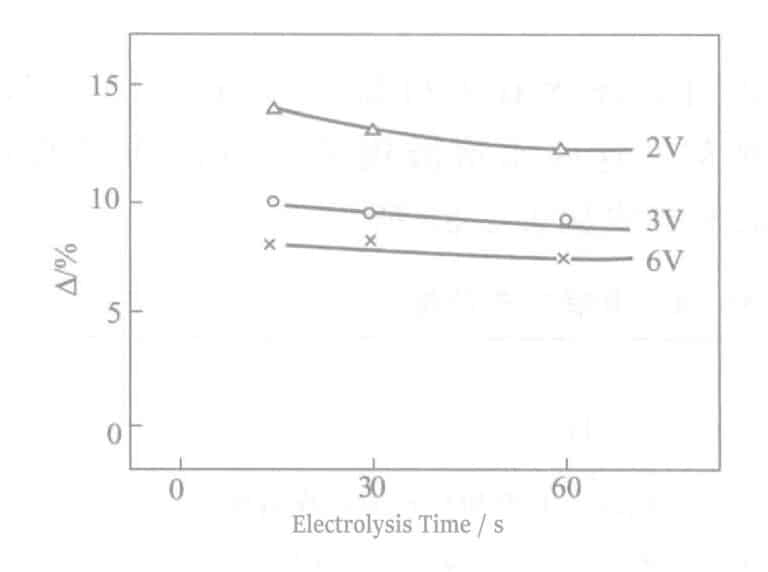
Сравнение △ результатов в условиях замачивания в 0,2% (NH4)2Sx раствора в течение 2 часов показаны на рис. 2-12. Чем выше напряжение, тем лучше устойчивость к сере, в основном за счет утолщения пленки оксида хрома. Если время электролиза увеличивается без улучшения, это связано с тем, что в электролитической пленке слишком много проколов, что приводит к увеличению количества хромовой кислоты, попавшей в проколы.
(9) Обесцвечивание, вызванное ультрафиолетовым излучением
Результаты обесцвечивания и серостойкости гальванических пленок Cr под воздействием ультрафиолетового облучения приведены в таблице 2-39 (условия гальванического покрытия Cr: 6 В, 30 с). После ультрафиолетового облучения гальваническая пленка Cr полностью повреждается, становясь красновато-фиолетовой и синевато-фиолетовой. Одновременно с этим резко снижается устойчивость к сере, опустившись до того же уровня, что и без обработки против обесцвечивания. Разница между образцами, обработанными антидисколоритом, и образцами, подвергшимися воздействию солнечного света, незначительна из-за разницы в интенсивности ультрафиолетового излучения по сравнению с общими экспериментами по ультрафиолетовому облучению.
Таблица 2-39 Изменение цвета, вызванное ультрафиолетовым облучением
| Серийный номер | Ультрафиолет | L1/% | L2/% | L3/% | △1/% | △2/% | Примечания | |
|---|---|---|---|---|---|---|---|---|
| 1 | - | - | 86. 3 | - | 84. 8 | 0 | 1.5 | (Становится желтым) |
|
2 3 4 |
УФ① |
0.5 1 3 |
86. 0 86. 2 86. 5 |
86. 0 83. 2 58〜65 |
67 53 - |
0 3 21〜28 |
19 33 - |
Голубой - Виолетта |
|
5 6 |
Солнечный свет② |
3 6 |
86.6 86.4 |
86.6 86.4 |
85.6 85.5 |
0 0 |
0.8 0.9 |
(Становится желтым) - |
|
① В фотоэлектрическом блескомере используется водородная разрядная трубка. ② Нахождение на открытом воздухе в дневное время: L1 -- Отражение до облучения; L2 -- Отражение после облучения; L3 -- Отражение после замачивания в 0. 2% (NH4 )2 Sx в течение 30 минут после облучения. △1 =L1 - L2 △2 =L1 - L3
|
||||||||
Копирайт @ Sobling.Jewelry - Пользовательские ювелирные изделия производителя, OEM и ODM ювелирный завод
(10) Влияние примесей
Результаты тестирования влияния примесей в базовом составе приведены в таблице 2-40.
Таблица 2-40 Влияние примесей
| Примеси | Концентрация /×10-6 | Внешний вид |
|---|---|---|
| CN |
200 400 600 800 1000
|
O O O O O |
| Ag |
10 20 30 40 50 |
O O O X(черный) X(черный) |
| Sn |
200 400 600 800 1000
|
O O O O O |
(11) Обработка электролизом Sn плюс устойчивость к воздействию серы Cr во время электролитической обработки
Все вышеперечисленные методы имеют свои плюсы и минусы и не могут считаться полноценными методами защиты от обесцвечивания. Поэтому рассматривается следующий подход: после нанесения покрытия Ag сразу выполняется электролитическая обработка Sn, а затем электролитическая обработка Cr.
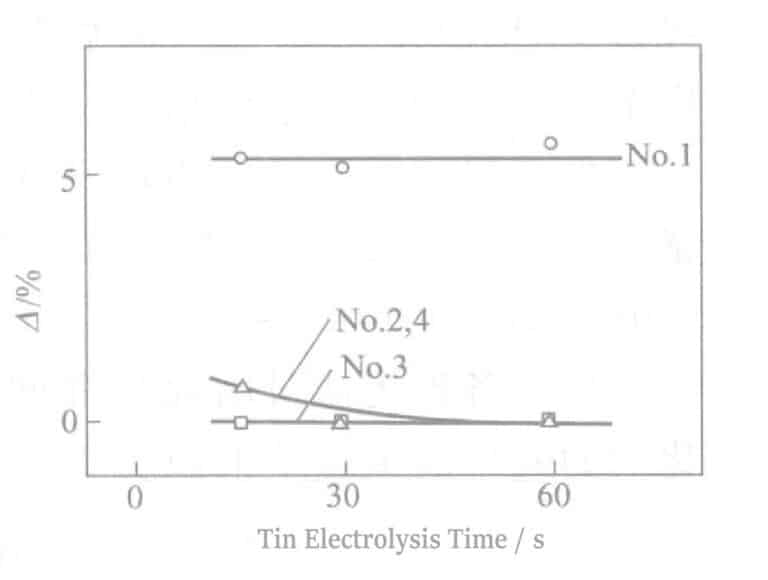
В условиях постоянного тока (DK = 0. 5A/дм2 ), изменялось время электролиза Sn, а при последующей обработке электролизом Cr изменялись напряжение и время электролиза. Результаты показаны на рис. 2-13. Уменьшение отражательной способности при каждом из условий вызвано изменением времени электролиза Sn. Время электролиза должно поддерживаться в пределах 30 секунд для сохранения серебряного тона.
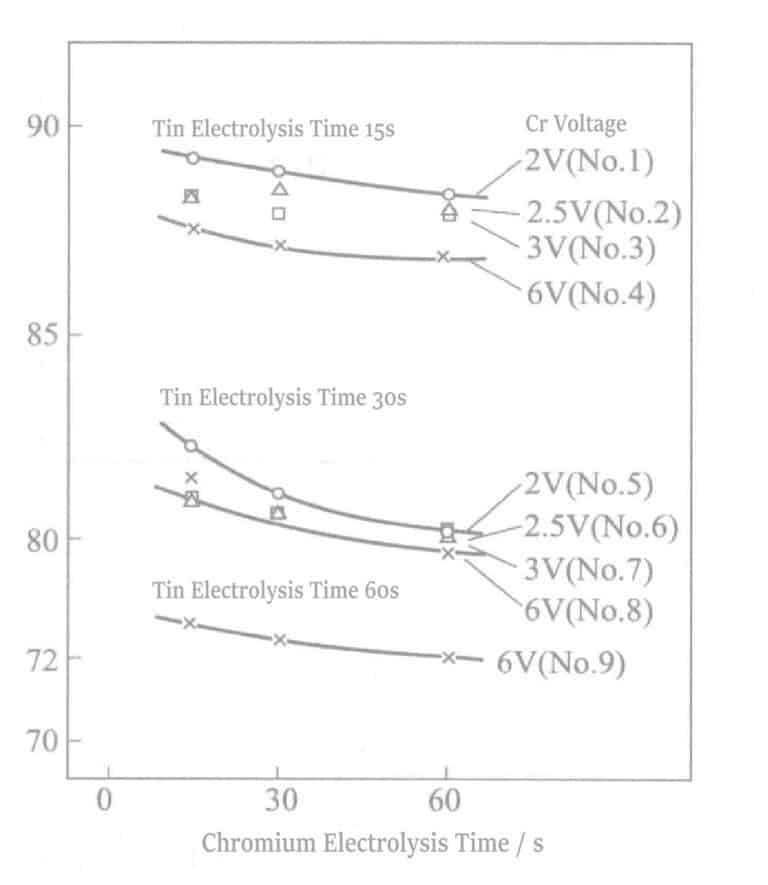
При одинаковом состоянии времени обработки Sn электролизом увеличение времени электролиза Cr приводит к тому, что цвет Cr, лежащий в основе Sn, проявляется, в результате чего образуется белое или серое неравномерное состояние. В то же время, когда электролиз Cr проводится при высоком напряжении (6 В), это явление проявляется раньше; при 6 В его можно заметить через 5 секунд, тогда как при 2 В оно может длиться более 60 секунд. Увеличение времени электролиза Sn демонстрирует ту же тенденцию. Чем дольше время электролиза, тем больше вероятность отбеливания.
Это явление возникает, когда заряд, прошедший во время обработки Cr определенного гальванического слоя Sn, достигает определенного значения. Окислительно-восстановительная реакция во время гальванизации Cr играет определенную роль на гальваническом слое Sn, вызывая изменения в морфологии кристаллизации Sn или вызывая изменения в контрасте между гальваническим слоем Sn и гальваническим слоем Cr.
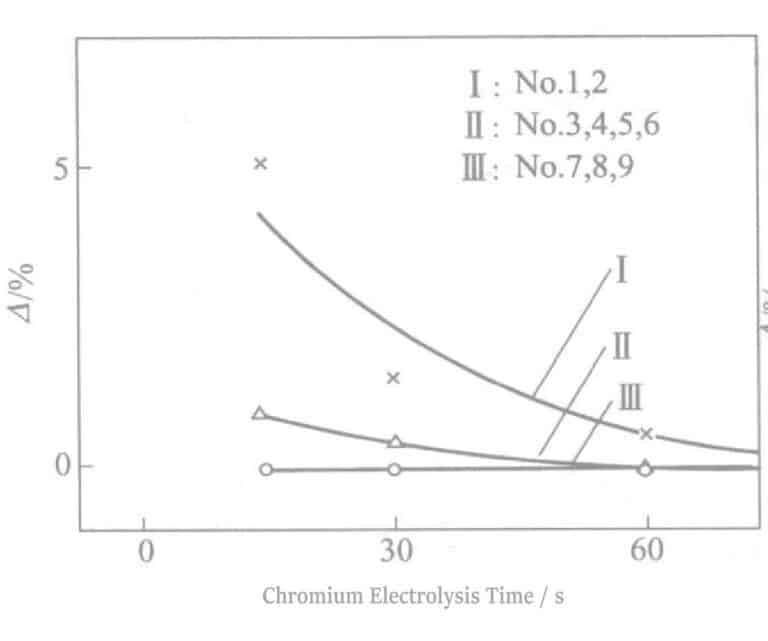
Если изменения цвета не происходит, это связано с увеличением времени электролиза Sn. Время электролиза составляет 15~30 с + время электролиза более 30 секунд особенно хорошо влияет на устойчивость к сере, но при этом возникают проблемы с внешним видом. Сочетание электролиза Sn при 0,5 А/дм2 в течение 15~30 с, плюс электролиз Cr при 2~3 В в течение 30 с - оптимальные условия.
Результаты испытания на воздействие в помещении показаны на рис. 2-15. Пожелтение произошло через 1~2 дня для необработанных деталей и через 7~10 дней для электролитической обработки Cr. В отличие от этого, детали, обработанные электролизом Sn с последующим электролизом Cr, начали частично сереть только через 60~100 дней, что свидетельствует о хорошей эффективности. Замачивание проводилось с использованием 0,2% (NH4)2Sx раствора, что эквивалентно одному месяцу испытаний в помещении. Обработка электролизом Sn с последующей обработкой Cr сокращенно называется SGP (silver guard process).
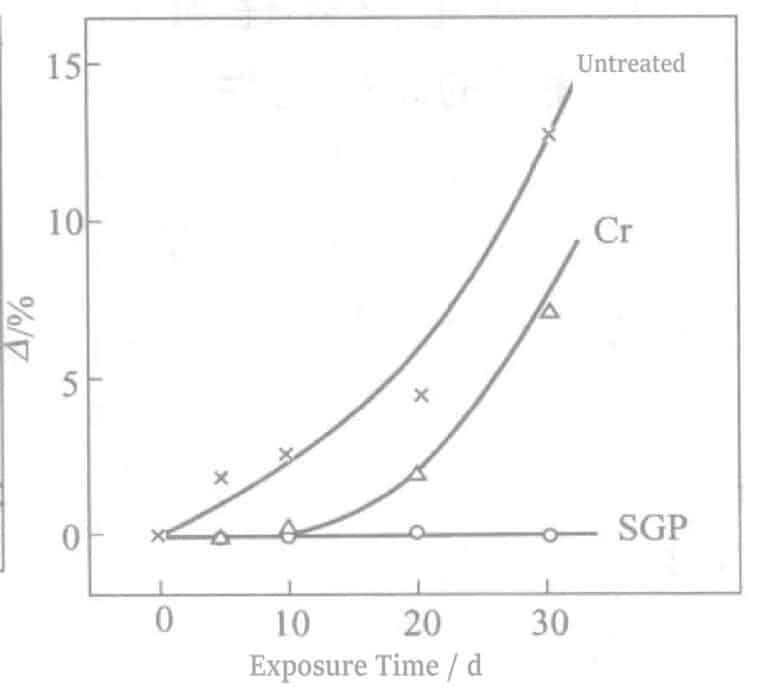
① Влияние различных солей олова на стойкость серы
Результаты испытаний влияния различных активаторов поверхности солей олова в методе SGP приведены в таблице 2-41 и на рисунке 2-16.
Таблица 2-41 Сравнение эффектов различных солей олова
| Серийный номер | Состав и условия его применения | Время электролиза Sn /с | Cr Время электролиза/с | L1/% | △/% | Примечания |
|---|---|---|---|---|---|---|
| 1 |
SnCl2 4 г/л HCl 0,025моль/л (погружение) |
13 30 60 |
15 |
90. 2 89. 8 89. 2 |
5. 4 4. 8 5. 8 |
Пожелтение Пожелтение Пожелтение |
| 2 |
Na2SnO3 -3H2O 8. 5 г/л CH3COONa-3H2O 5 г/л 3. 5В(0. 1А/дм2) |
15 30 60 |
15 |
89. 7 87. 3 85. 2 |
0. 7 0. 1 0
|
Частичное пожелтение - Цвет олова |
| 3 |
№ 2 плюс Перетеккусу# 1232① 0. 1 г/л 3. 5 В (0. 15 А/дм2) |
15 30 60 |
15 |
87. 4 85.0 76. 6
|
0 0. 1 0 |
- - Цвет олова |
| 4 |
K2SnO3-3H2O 8. 5 г/л CH3COONa-3H2O 5 г/л 3. 5 В (0. 1A/дм2) |
15 30 60 |
15 |
89. 6 88. 9 85. 4 |
0. 9 0 0 |
Частичное пожелтение - Цвет олова |
|
① Перетеккусу# 1232 - это продукт японской компании Miyoshi Oil & Fat. Примечание: электролит Cr 3 В.
|
||||||
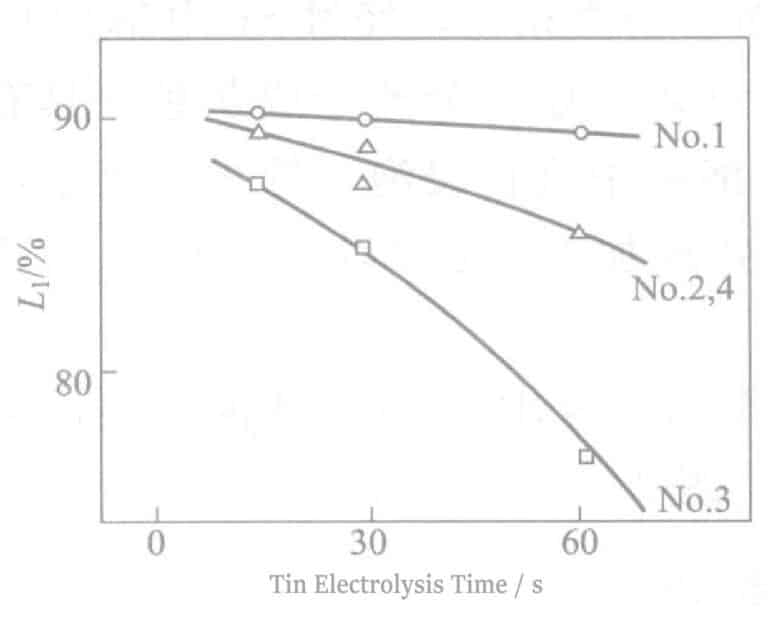
Добавление неионогенного ПАВ (№ 3) в электролит со станнатом натрия значительно повышает эффективность тока, ускоряет скорость электролиза (№ 2), снижает отражательную способность и повышает серостойкость.
Хотя результаты применения электролита со станнатом калия (№ 4) такие же, как и электролита со станнатом натрия, существуют определенные различия между действием солей натрия и калия в щелочных растворах для оловянных покрытий.
② Влияние хромового электролита на стойкость серы В основном изучались такие аспекты, как концентрация электролита, влияние поверхностно-активных веществ и плотность тока на внешний вид после обработки.
Таблица 2-42 Влияние концентрации на устойчивость к сере
| Концентрация /(г/л) | Время электролиза /с | Значение тока при постоянном напряжении (6 В)/А | ||
|---|---|---|---|---|
| 5 | 15 | 30 | ||
|
K2CrO4 15 NaOH 30 |
X | X | X |
4. 0 (40 А/дм2) |
|
K2CrO4 7.5 NaOH 15 |
O | X | X |
2.4 (24A/дм2) |
|
K2CrO4 1.5 NaOH 3,0 |
O | O | X |
0.6 (6A/dm2) |
|
Примечание: O означает отсутствие изменений во внешнем виде; × указывает на изменение внешнего вида (отбеливание).
|
||||
- Влияние концентрации: Стандартный раствор разбавляли до 1/2, 1/10 и исследовали время электролиза, при котором появляется оловянная окраска при электролизе при напряжении 6 В. Результаты приведены в таблице 2-42.
- Влияние поверхностно-активных веществ: Стандартные растворы ПАВ (Perettekusu#1265, продукт компании Miyo-shi Oils and Fats Co., Ltd., Япония) добавляли к ионному ПАВ в концентрациях 1/1 и 1/2, и время электролиза исследовали по моменту, когда оно начинало проявлять оловянный цвет. Результаты приведены в таблице 2-43. По сравнению с отсутствием добавления, при добавлении ПАВ эффект был лучше при высокой плотности тока. При низкой плотности тока эффект мало отличался от случая без добавления, но газ препятствовал ходу электролиза. При наличии поверхностно-активных веществ их концентрация и плотность тока влияли на время начала отбеливания, что увеличивало трудности управления. В то же время из-за большого количества выделяющегося водорода образовывались пузырьки. Без добавок было проще управлять процессом.
Таблица 2-43 Действие поверхностно-активных веществ
| Концентрация/(г/л) | Perettekusu# 1265/(мл/л) | Напряжение/В | DK/(A/dm2 | Время электролиза/с | ||
|---|---|---|---|---|---|---|
| 5 | 10 | 15 | ||||
|
K2CrO4 15 NaOH 30
|
0 |
6 5 6 3 |
40 29 19 7 |
X X X X |
X X X X |
X X X X |
| 0.01 |
6 5 6 3 |
40 29 19 7 |
O O O O |
X X O O |
X X X X |
|
| 0.1 |
6 5 6 3 |
40 29 19 7 |
O O O O |
O O O X |
X X X X |
|
| 1 | 6 | 40 | O | X | X | |
|
K2CrO4 7.5 NaOH 15
|
0 |
6 5 6 3 |
24 17 10 3 |
X X X O |
X X X O |
X X X X |
| 0.01 |
6 5 6 3 |
24 17 10 3 |
O O O O |
O O X X |
X X X X |
|
- Влияние тока: Плотность Время появления цвета олова при различных плотностях тока во время электролиза показано на рис. 2-18. В то же время кривая E-I показана на рисунке 2-19. Плотность тока более подходящая, когда время электролиза составляет 0,5 А/дм2 около 30 секунд. Между тем, время без появления цвета олова также зависит от концентрации электролита, плотности анодного тока, расстояния между электродами и других факторов. Управление концентрацией осуществляется путем расчета размера резервуара, и для удобства управления можно вывести собственную мощность резервуара, при которой не появляется цвет олова при определенном напряжении.
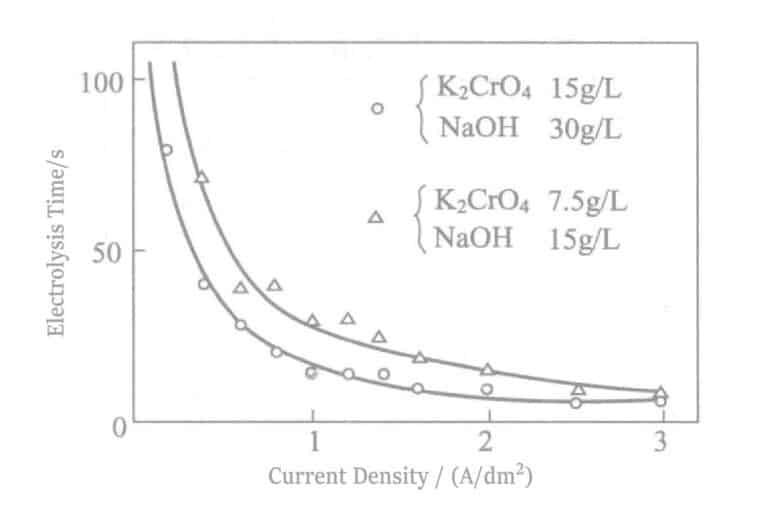
Рисунок 2-18 Зависимость между плотностью тока и временем электролиза
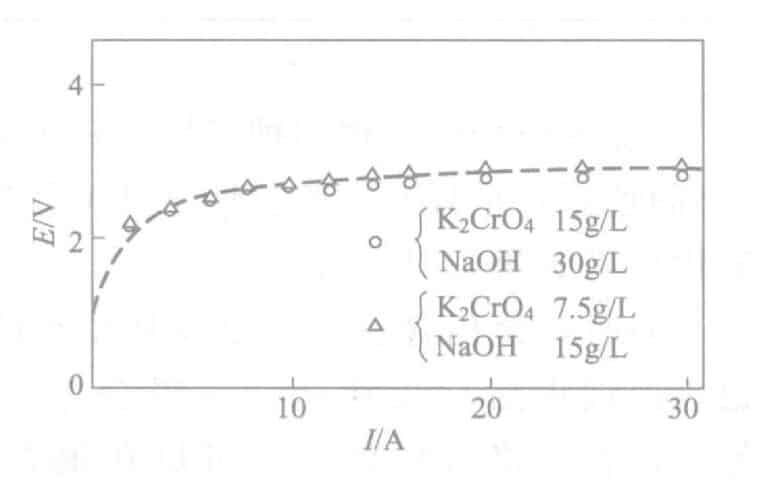
Рисунок 2-19 Кривая E-I раствора электролита
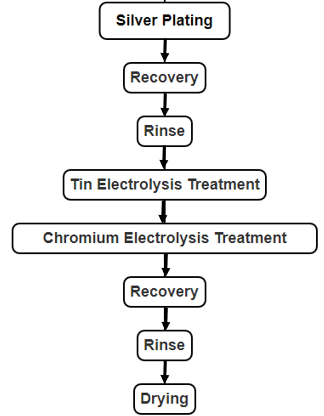
Рисунок 2-20 Процесс обработки хромового электролита

Рисунок 2-21 Сравнение серостойкости различных методов обработки
В то же время, использование моющих средств (ПАВ), содержащих α-дикетон и его соли, для мытья или замачивания серебра (или посеребренных изделий) и его сплавов (сплав олова, сплав цинка, сплав индия, сплав палладия и т.д.) может значительно замедлить обесцвечивание поверхности или коррозию.
Основная структура его добавки показана на рисунке 2-22.
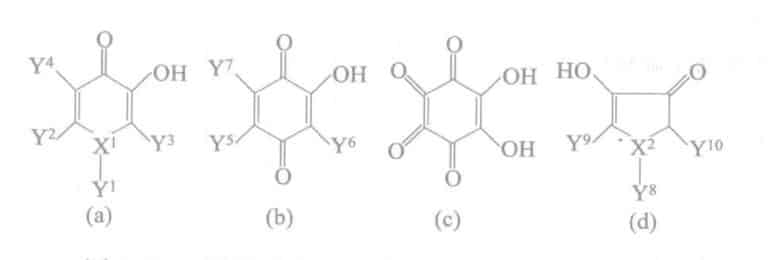
Таблица 2-44 Примеры рецептур дикетосодержащих поверхностно-активных веществ для предотвращения потускнения серебра
| Состав | No. 1 | No. 2 | No. 3 | No. 4 | No. 5 | No. 6 | No. 7 | No. 8 |
|---|---|---|---|---|---|---|---|---|
| Хлорванилловая кислота | 10 | |||||||
| Полиоксиэтиленалкиловый эфир | 0.5 | |||||||
| Дигидрогенфосфат натрия | 5 | |||||||
| Полиэтиленгликоль | 1 | |||||||
| Третиноин | 5 | |||||||
| Пиразол хлорид | 5 | |||||||
| Бикарбонат натрия | 5 | |||||||
| Протеаза | 1 | |||||||
| Йодид калия | 0.05 | |||||||
| Тетрагидрокси-1,4-бензохинон | 0.5 | |||||||
| 2-Алкил-N-карбоксиметил-N-гидроксиметилимидазолин | 10 | |||||||
| Тиомочевина | 0.5 | |||||||
| Глицерин | 1 | |||||||
| Натрия 3-этил-2-гидрокси-2-циклопентан-1-карбоксилат | 0.05 | |||||||
| Алкилсульфонат калия | 5 | |||||||
| Соль изоцианурона | 5 | |||||||
| N-ацилированные амины | 1 | |||||||
| 3-Hydroxy-2-methyl-4-pyrone | 20 | |||||||
| Лимонная кислота | 5 | |||||||
| Бензоат натрия | 5 | |||||||
| Ментол | 0.1 | |||||||
| Кальций розмариновый | 2 | |||||||
| 3-Метил-1,2-циклопентанамин | 20 | |||||||
| Полиоксиэтиленовое касторовое масло | 5 | |||||||
| Стероидные гликозиды | 1 | |||||||
| 3-Гидрокси-1,2-диметил-4(1H)-пиридин | 6 | |||||||
| Меркаптоаланин | 2 | |||||||
| Глюкоамилаза | 5 | |||||||
| Сорбит | 1 | |||||||
| 2,5-Дигидрокси-1,4-бензохинон | 10 | |||||||
| Алкилбензил аммоний хлорид | 30 | |||||||
| Тартрат калия-натрия | 5 | |||||||
| Папаин | 1 |
Раздел II Покрытие безэлектродным серебром
Поскольку серебро обладает низким удельным сопротивлением и стоит гораздо дешевле других драгоценных металлов, серебряное покрытие широко используется в электронике.
Будучи драгоценным металлом, серебро имеет более положительный окислительно-восстановительный потенциал, чем другие металлы, что позволяет ему смещаться и осаждаться на таких металлах, как медь, железо и цинк, образуя на них слой серебряного покрытия. Позже будет упомянуто, что этот тип реакции используется на печатных платах для замены меди на серебро, так что медный рисунок покрывается слоем серебра, тем самым увеличивая паяемость и уменьшая контактное сопротивление. Однако такое вытесняющее осаждение обычно приводит к получению относительно тонкого слоя покрытия, около 2 мкм или менее. В отличие от этого, слой покрытия, полученный в результате реакции восстановления, может быть несколько толще.
В области нанесения серебряных покрытий наиболее известной является реакция серебряного зеркала. Реакция серебряного зеркала была разработана Дрейтоном в 1830 году и была применена в производстве зеркал. Кроме того, химическое серебрение (особенно восстановительное) широко используется в электронике, что расширяет сферу промышленного применения серебра. Химическое серебрение может применяться не только к металлам, но и к неметаллам.
1. Вытеснение серебряного покрытия и его применение
При смещенном серебрении используется разность потенциалов между основным металлом и серебром.
Проводники на печатных платах обычно изготавливаются из меди, но во время хранения, перед монтажом компонентов, на поверхности меди образуется оксидная пленка. Эта оксидная пленка влияет на паяемость печатной платы. Для повышения способности медных схем к пайке обычно используются высококачественные продукты или даже покрытие Ni/Au, Ni/Pd, Ni/Pa/Au, что, естественно, увеличивает стоимость. Однако покрытие Sn не обладает достаточной устойчивостью к ржавчине. Серебряное покрытие близко по цене к Sn и не только предотвращает ржавчину и подходит для пайки, но и может использоваться для соединения металлических проводов, то есть серебро может быть вытеснено медными цепями. Однако при нанесении серебра непосредственно на медь необходимо увеличить толщину ленты, чтобы компенсировать неравномерность покрытия. В этом случае покрытие не выдерживает испытания лентой: покрытие легко отслаивается, особенно после хранения. Однако эту проблему можно решить с помощью двухэтапного нанесения покрытия. Метод заключается в том, что сначала на медь наносится слой металла, более дорогого, чем медь, а затем со смещением наносится слой серебра. Первым металлическим слоем может быть Pd или Ag. Его толщина настолько мала, порядка нанометров (т.е. несколько нанометров), что наличие покрытия невозможно определить невооруженным глазом. Реакция вытеснения происходит следующим образом:
Раствор для вытеснения серебра должен также содержать комплексообразователь моновалентной меди для стабилизации вытесняемых ионов меди. Когда первым покрытием является вытесняющее серебро, скорость его вытеснения должна быть намного медленнее, чем скорость вытеснения второго слоя Ag, эквивалентная менее 15% его скорости. Если скорость слишком велика, легко вызвать снижение адгезии покрытия, что приведет к отслаиванию покрытия во время испытания ленты. Ниже приведен пример нанесения серебряного покрытия.
Когда первый слой покрытия представляет собой Pd, раствор для нанесения покрытия Pd представляет собой
PdSO4 50 мг/л (учитывается как Pd)
H2SO4 5%
Температура Комнатная температура
Время около 30-х годов
Таблица 2-45 Состав и процесс вытесняющего серебряного покрытия (первый слой покрытия)
| Состав и условия процесса | Состав и компоненты | Состав и условия процесса | Состав и компоненты |
|---|---|---|---|
| Метансульфонат серебра (в виде Ag) | 1 г/л | Lurotex A25 | 20 мг/л |
| NaBr | 320 г/л | pH | 5.5 |
| Диэтилентриамин пентиленфосфоновая кислота | 30 мл/л | Температура | 50℃ |
| Полиэтиленгликоль 400 | 80 мл/л | Время | 5 мин |
| 2,2'-Бипиридин | 90 мг/л |
После нанесения покрытия детали проходят термообработку при 150℃ в течение 4 часов, затем тест на смачиваемость, после чего получают квалификацию.
Когда первым слоем покрытия является Ag, раствор для нанесения покрытия и его процесс показаны в таблице 2-46.
Таблица 2-46 Состав и процесс вытесняющего серебряного покрытия (второе покрытие)
| Состав и условия процесса | Состав и компоненты | Состав и условия процесса | Состав и компоненты |
|---|---|---|---|
| Метансульфонат серебра (в виде Ag) | 1 г/л | Полиэтиленгликоль 400 | 80 мл/л |
| NaBr | 320 г/л | 2,2'-Бипиридин | 90 мг/л |
| Диэтилентриамин пентиленфосфоновая кислота | 30 мл/л | pH | 5.5 |
Раствор для нанесения первого и второго слоев может иметь одинаковый состав, но температура и время погружения могут быть разными. Условия для первого слоя покрытия следующие: 25℃, 30s. Условия для второго слоя покрытия следующие: 50℃, 6мин. Полученные слои покрытия являются однородными, серебристо-яркими и обладают хорошей свариваемостью при пайке.
Хатчинсон и др. предложили метод нанесения покрытия с использованием алкилового эфира полиэтиленгликоля в качестве отбеливателя, этилендиамина и 1-гидроксиэтилен-1,1-дифосфоновой кислоты в качестве комплексообразователей меди, и полученный слой покрытия может удовлетворять условиям пайки печатных плат.
ITO (прозрачный оксид индия-олова) широко используется в жидкокристаллических и плазменных дисплеях. Поскольку размеры жидкокристаллических и плазменных дисплеев в последние годы увеличились, сопротивление самого ITO стало относительно высоким. Чтобы решить эту проблему, на ITO можно добавить слой серебра с более низкой проводимостью. Это не может быть реализовано путем прямого гальванического нанесения серебра, поскольку на ITO трудно напрямую наносить каталитически активные металлы. Поэтому сначала на ITO осаждается слой олова, затем каталитически активный металл и, наконец, серебро. Состав раствора для нанесения покрытия и условия процесса нанесения серебряного покрытия на ITO приведены в таблице 2-47.
Таблица 2-47 Состав раствора для нанесения покрытия и условия процесса для нанесения серебряного покрытия на ITO
| Погружная жидкость для олова |
SnCl2 HCl
|
70 г/л 230 мл/л |
| Активирующая жидкость | AgNO3 | 10 г/л |
| Раствор для нанесения серебряного покрытия |
AgNO3 NH4OH (NH4)2SO4 Co(SO4)2 Mg(OH)2 Толщина Ag Специфическое сопротивление Удельное сопротивление (250℃, через 30 минут после обработки) |
0. 03〜0. 08моль/л 7〜10моль/л 0. 3〜0. 8моль/л 0. 1〜0. 2моль/л 0. 01〜0. 05моль/л 2900〜3200Å 3〜3. 5μΩ- см 1. 6〜2. 5μΩ- см |
2. Восстановление серебряного покрытия и его применение
Состав раствора для восстановительного серебрения аналогичен составу раствора для общего химического покрытия, основными компонентами которого являются: соль Ag, комплексообразователь, восстановитель, pH-корректор, стабилизатор и т.д. Восстанавливающие агенты для серебра включают глюкозу, сахарин, глиоксаль, аскорбиновую кислоту, глюконовую кислоту, сорбит, гидразин, HCHO, KBH4, NaBH4, DMAB и другие.
Реакции некоторых репрезентативных восстановителей серебра выглядят следующим образом.
(1) HCHO (при использовании раствора аммиака в качестве комплексообразующего агента)
2AgNO3 + 2NH4OH → Ag2O + 2NH4НЕТ3 + H2O
Ag2O + 4NH4OH → 2[Ag(NH3)2]OH + 3H2O
2[Ag(NH3)2]OH + HCHO → 2Ag + 4NH3 + HCOOH + H2O
4AgNO3 + 4NH3 + C4H4O6NaK + H2O → 4Ag + 4NH4НЕТ3 + C3H2O6NaK + CO2
4[Ag(NH3)2]NO3 + N2H4 → 4Ag + 4NH4НЕТ3 + 4NH3 + N2
N2H4BH3 + 3Ag+ + 4OH– → 3Ag + N2H4 + B(OH)4–+ 3/2H2
Таблица 2-48 Составы с использованием органических растворителей для электролитического серебрения
| Ингредиенты и условия их обработки | No. 1 | No. 2 |
|---|---|---|
|
Диметилсульфоксид/мл Этиленгликоль/мл Этанол/мл d-(+)глюкоза/мл Триэтиламин/мл Температура/°C Время/мин Материалы для нанесения покрытий |
300 200 - - 15 70 20 Эл2O3 порошок |
200 - 300 5g 2. 5 мл/мин 60 10 Нейлоновая ткань
|
Среди них в качестве восстановителей используются диолы и глюкоза. В то же время, поскольку диметилсульфоксид обладает небольшой восстановительной способностью, раствор для нанесения покрытия не требует обработки старением. Полученные в результате гальванического покрытия детали имеют металлический блеск, напоминающий серебро.
В качестве комплексообразователей используются органические соединения, содержащие две монотиоловые группы, со следующей структурной формулой:
В формуле R1 и Р2 представляют собой алкиленовые группы, содержащие 1~5 атомов углерода; R3 представляют собой алкиленовую группу, содержащую 2~8 атомов углерода X и Y могут быть карбоксильными, сульфокислотными, аминогруппами, алкильными группами и т.д.
Восстанавливающие агенты включают альдегиды, гидразины, борогидридные соединения, аскорбиновую кислоту и т.д. В таблице 2-49 приведены примеры использования этой серии.
Таблица 2-49 Условия процесса нанесения раствора для восстановительного серебрения с использованием двух монотиоловых органических соединений в качестве комплексообразователей
| Состав и условия его применения | No. 1 | No. 2 | No. 3 |
|---|---|---|---|
|
Нитрат серебра/(г/л) 1,2-бис(2-карбоксиэтилтио)этан/(г/л) 1,4-бис(2-карбоксиэтилтио)бутан/(г/л) 1,2,2'-(этилтио)диэтилмеркаптан/(г/л) Гидразин гидрат/(г/л) Формалин/(г/л) Гипофосфит натрия/(г/л) pH (корректируется с помощью NaOH) Температура/°C |
0. 17 10 - - 8 - - 10 35 |
0. 31 - 15 - - 4 - 11 50 |
0. 34 - - 20 - - 10 10. 5 50 |
Раздел III Анализ цианистого раствора для серебрения
1. Анализ серебра
Таблица 2-50 Метод анализа ионов серебра для раствора серебряного покрытия
| Последовательность операций | Примечания и инструкции |
|---|---|
|
(1) Возьмите 5 мл раствора для осаждения в стакан 300, добавьте 20 мл серной кислоты и 5 мл азотной кислоты, наблюдая за процессом. (2) Нагревайте до появления белого дыма (3) Добавьте 100 мл воды и 3 мл сульфата железа аммония 10%. (4) Титруйте тиоцианатом калия 0,1 моль/л. Формула расчета: Ag (г/л) = мл × 2. 158 × f AgCN (г/л) = Ag (г/л) ×1. 2402 В формуле, мл - 0. 1моль/л титра тиоцианата калия; f--0. 1моль/л раствора тиоцианата калия коэффициент |
В связи с выделением токсичного газа цианистого водорода необходимо работать в зоне местной вентиляции. Смените коричневый дым на белый Конечная точка титрования: светло-красный цвет 0. 1моль/л KCNS 1мл = 0. 01079г Ag |
2. Методы анализа свободного цианида
Таблица 2-51 Аналитические методы для свободного цианида
| Последовательность операций | Примечания и инструкции |
|---|---|
|
(1) Возьмите 5 мл раствора для осаждения в стакан объемом 300 м, добавьте воды 50 мл (2) Добавьте 10% раствор йодида калия 1~2 мл (3) Титруйте раствором нитрата серебра 0,1 моль/1 Формула расчета. Свободный KCN (г/л) = мл×2,60×f Свободный NaCN (г/л) = мл × 1,96 × f В формуле f - коэффициент 0,1 ммоль/л раствора нитрата серебра |
Конечная точка титрования: светло-красный цвет 0. 1моль/л AgNO3 1 мл = 0. 0130 г KCN = 0. 0098 г NaCN |