Почему драгоценные камни имеют несколько цветов?
Секреты формирования цветов и методы измерения
Цвета драгоценных камней богаты и разнообразны, они обладают неповторимым очарованием, которое всегда нравилось людям. Качество драгоценных камней во многом зависит от их цвета. Цвет камня - важный показатель при оценке драгоценных камней, и большинство оптимизационных процедур с драгоценными камнями связаны с изменением или улучшением их цвета. Поэтому понимание причин окраски драгоценных камней - важнейшее условие их оптимизации. Только зная, как драгоценные камни приобретают свой цвет, можно определить, можно ли оптимизировать драгоценный камень, какую схему оптимизации принять и какой экспериментальный план разработать. Существует пять общих теорий окраски драгоценных камней: классическая теория минералогии, теория кристаллического поля, теория молекулярных орбиталей, теория энергетических полос и физические оптические эффекты. Эти теории составляют теории окраски распространенных природных драгоценных камней, и ниже приводится краткое введение в эти пять теорий окраски.

Схематическая диаграмма трех элементов цвета
Оглавление
Раздел I Цвет и измерение цвета драгоценных камней
Цвета драгоценных камней богаты и разнообразны, и определение типов цветов драгоценных камней имеет решающее значение для оценки их стоимости. Различные цветовые категории также влияют на стоимость драгоценных камней, поэтому точная оценка цвета различных драгоценных камней является основополагающей предпосылкой для определения их стоимости. При оценке цветных драгоценных камней цвет является наиболее важным фактором. Как правило, чем привлекательнее цвет драгоценного камня, тем выше его стоимость. Яркие, насыщенные и интенсивные цвета обычно более привлекательны, чем слишком темные или слишком светлые. Конечно, есть и исключения, например бриллианты, где чем белее цвет бриллианта, тем выше его стоимость.
1. Значение цвета драгоценных камней
С древних времен люди любили драгоценные камни за их неповторимое очарование, особенно богатые и красочные оттенки, такие как красный рубин, яркий зеленый изумруд и нефрит, которые оставляют неизгладимое впечатление. Цвет является важным показателем для оценки качества драгоценных камней и играет решающую роль в определении их качества, причем его значение в основном отражается в следующих трех аспектах.
(1) Цвет минералов драгоценных камней является важной основой для оценки драгоценных камней
Цвет драгоценного камня является основополагающим фактором для его оценки и определяет его стоимость. Например, в бриллиантах разница в цвете на один класс может привести к разнице в цене примерно в 5%. Чем выше белизна, тем выше класс бриллианта; и наоборот, бриллианты с желтыми или коричневыми оттенками имеют более низкий класс, и их цена резко падает. Цены на цветные бриллианты варьируются, и разные цветные бриллианты имеют разную стоимость. Однако в целом цены на редкие цветные бриллианты могут возрастать в несколько раз. Другие цветные драгоценные камни, такие как рубины, сапфиры и изумруды, также делятся на различные классы в зависимости от цвета, и стоимость камней разных классов может значительно отличаться.
(2) Оптимизация обработки драгоценных камней часто включает в себя улучшение их цвета
Методы оптимизации обработки драгоценных камней обычно связаны с изменением или улучшением их цвета, поэтому улучшение цвета драгоценных камней также можно назвать изменением цвета драгоценных камней. При улучшении цвета драгоценного камня соответственно меняется и его прозрачность. Это происходит потому, что прозрачность - свойство, связанное с цветом. Например, синие сапфиры невооруженным глазом кажутся непрозрачными, но при разрезании на тонкие кусочки можно увидеть прозрачный синий цвет. Улучшение прозрачности часто сопровождается улучшением цвета. Поэтому, только определив причину цвета драгоценного камня, можно определить методы его улучшения. Понимание причины цвета - необходимое условие для изучения методов оптимизации драгоценных камней.
(3) Изучение причин цвета драгоценных камней создает теоретическую основу для синтетических драгоценных камней и совершенствования драгоценных камней.
Цвет таких драгоценных камней, как гранат, малахит и оливин, обусловлен их внутренними компонентами, и эти камни не могут изменить свой цвет с помощью обычных методов оптимизационной обработки. Большинство цветов драгоценных камней обусловлено примесями, вызванными ионами примесей, как, например, в рубинах, сапфирах, изумрудах, нефритах и агатах. Исходя из причин цвета драгоценных камней, в процессе улучшения содержание и валентное состояние определенных ионов примесей, вызывающих цвет, может быть изменено, чтобы изменить или улучшить цвет драгоценного камня, тем самым повышая качество улучшенного драгоценного камня. Таким образом, изучение причин цвета драгоценных камней является теоретической основой для улучшения драгоценных камней.
2. Физика цвета
(1) Цвет и световые волны
Фотоны несут в себе энергию света, и когда фотоны достигают человеческого глаза, они создают ощущение цвета. Цвет - это восприятие света глазами и нервной системой; реакция, вызванная сигналами, формирующимися на сетчатке глаза, стимулирует кору головного мозга. В формировании цветового восприятия участвуют три основных компонента: источник света, объект и человеческий глаз. Изменение одного или нескольких из этих трех компонентов приведет к изменению восприятия цвета. Драгоценные камни взаимодействуют со светом, и такие явления, как отражение, преломление, передача, интерференция и дифракция, происходящие на поверхности драгоценного камня, приводят к появлению различных цветов.
Энергетический диапазон спектра электромагнитного излучения довольно велик: от очень длинных радиоволн до очень коротких лучевых фотонов, с энергией от менее одной миллиардной доли электронвольта до более ста миллионов электронвольт.
Видимый свет, который может воспринимать человеческий глаз, - это очень маленькая часть электромагнитного спектра, с диапазоном длин волн 400-700 нм и энергией около 1,7-3,1 эВ. Если условия наблюдения достаточно хороши, диапазон может быть расширен до 380-760 нм (рис. 3-1). Видимый свет включает в себя цвета, которые мы видим, а именно: красный, оранжевый, желтый, зеленый, голубой, синий, фиолетовый и различные другие цвета. Различные длины волн видимого света создают различные цвета; цвет видимого света с самой длинной длиной волны и самой низкой энергией - красный, с диапазоном длин волн 647-760 нм; видимый свет с самой короткой длиной волны и самой высокой энергией - фиолетовый, с диапазоном длин волн 400-425 нм. Другие цвета видимого света лежат в диапазоне от 425 до 647 нм. Длины волн различных цветов видимого света и дополняющих их цветов приведены в таблице 3-1.
Таблица 3-1 Длины волн различных цветов видимого света и дополняющих их цветов
| Длина волны/нм | Спектральный цвет | Дополнение |
|---|---|---|
| 400 ~ 425 | Фиолетовый | Желто-зеленый |
| 425 ~ 455 | Голубой | Желтый |
| 455 ~ 490 | Зелено-голубой | Оранжевый |
| 490 ~ 500 | Сине-зеленый | Красный |
| 500 ~ 560 | Зеленый | Пурпурный |
| 560 ~ 580 | Желто-зеленый | Фиолетовый |
| 580 ~ 595 | Желтый | Голубой |
| 595 ~ 647 | Оранжевый | Зелено-голубой (голубой) |
| 647 ~ 760 | Красный | Зеленый |
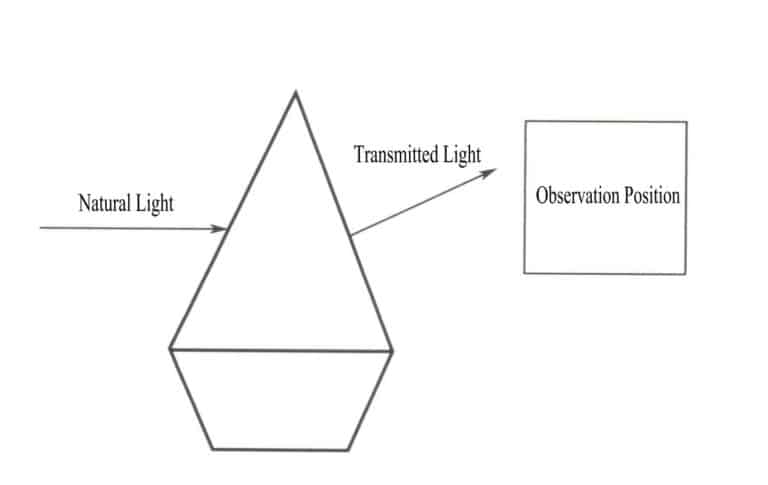
Суть цвета объекта - это результат избирательного поглощения объектом различных длин волн видимого света. Суть избирательного поглощения объектом различных длин волн видимого света заключается в поглощении фотонов видимого света с различной энергией. Когда на драгоценный камень падает естественный свет, он поглощает часть света и пропускает часть. Цвет драгоценного камня дополняет цвет поглощенного света и соответствует цвету пропущенного света (рис. 3-2). Например, в случае рубина, когда белый свет проходит через рубин, ионы хрома, содержащиеся в рубине, получают энергию, поглощая все фиолетовые и зеленые фотоны, а также большую часть синих фотонов, в то время как фотоны других цветов, преимущественно красные, проходят через рубин, в результате чего камень кажется красным.
Одна длина волны света не создает цвет, формируемый объектом; скорее, излучение объекта представляет собой смесь фотонов с различными энергиями, где энергетическая полоса с наибольшей долей определяет цвет объекта. Равномерная смесь различных цветов света образует белый свет. Цвет драгоценных камней образуется в результате избирательного поглощения фотонов различных длин волн видимого света. Когда белый свет проходит через драгоценный камень, поглощенный и пропущенный им свет представляет собой смесь, и цвет драгоценного камня зависит от того, какой из них имеет наибольшую долю в пропущенном свете. Например, в случае с рубином, когда на него светит белый свет, проходящий через него свет преимущественно красный с небольшим количеством голубовато-фиолетового. Поэтому рубины часто кажутся красными с синевато-фиолетовым оттенком.
(2) Типы и свойства источников света
Цвет драгоценных камней обладает определенной субъективностью, которая связана с окружением наблюдателя и в наибольшей степени зависит от источника света. Наблюдение за цветом драгоценных камней под разными источниками света может показать различия; например, александрит кажется зеленым при солнечном свете, но красным при свете ламп накаливания. Обычно стандартным считается цвет, наблюдаемый при естественном солнечном свете, который принято называть белым светом.
Первоначальные операции на рынке драгоценных камней проводились в определенное время, чтобы получить относительно точный цвет драгоценных камней. Например, магазины драгоценных камней в Ратнапуре (Шри-Ланка) в течение многих лет работали с 10 утра до 12 дня, поскольку в это время источник света наиболее близок к белому. Солнечный и дневной свет не являются изотропными источниками света, и относительные различия в относительных количествах излучения в разных длинах волн для разных источников света могут быть очень большими из-за разных условий наблюдения. На рисунке 3-3 приведены кривые распределения энергии пяти распространенных источников света, и различия в энергии между этими источниками света очень велики.
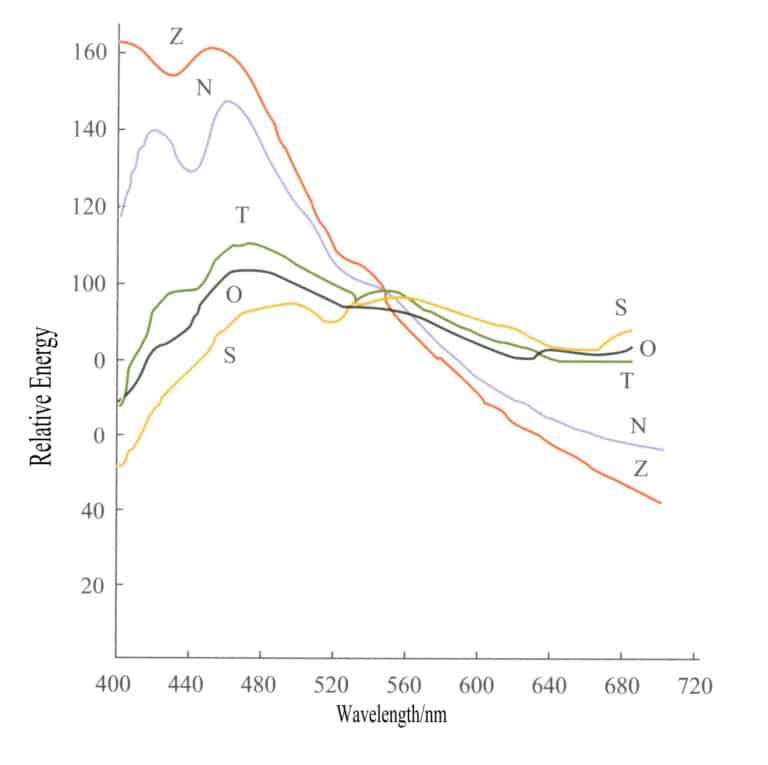
S - Прямой солнечный свет; O - Освещение пасмурного неба на горизонтальной плоскости; T - Освещение солнечного света и ясного неба на горизонтальной плоскости; N - Свет от ясного северного неба; Z - Свет зенита;
Цветовые характеристики прямого солнечного света часто выражаются в терминах цветовой температуры (измеряется в К). Одинаковая цветовая температура указывает на схожие цвета источников света. В настоящее время признаны следующие цветовые температуры дневного света: D6500K, D5500K и D7500K. Три лампы имеют международное обозначение как стандартные источники света для работ по измерению цвета. SA представляет собой среднюю искусственную освещенность вольфрамовой лампы накаливания с цветовой температурой 2854K;SB Представляет собой средний солнечный свет с цветовой температурой 4900K; SC представляет собой средний дневной свет с цветовой температурой 6700K. При тестировании драгоценных камней источник света Sc используется в качестве стандартного источника света.
(3) Чувствительность к свету и цветовым эффектам
Наблюдение за цветом драгоценных камней субъективно; помимо объективных условий, цвет драгоценного камня также связан с сенсорным восприятием наблюдателя. При одном и том же источнике света человеческие глаза по-разному воспринимают разные цвета, а у разных людей чувствительность к цветам неодинакова. Наблюдение за цветом субъективно; чтобы добиться максимальной объективности, цвета должны быть охарактеризованы и выражены относительно объективно.
① Фоторецептивный эффект:
В нормальных условиях диапазон длин волн видимых источников света, которые может наблюдать человеческий глаз, составляет 400-700 нм. При улучшении условий наблюдения диапазон чувствительности может быть расширен до 380-780 нм. Человеческий глаз обладает различной чувствительностью к световым волнам разной длины. Для дневного зрения глаз наиболее чувствителен к зеленому свету с длиной волны 555 нм, в то время как для сумеречного зрения наиболее чувствительная длина волны смещается к 507 нм. Светофоры на дорогах проектируются с учетом цветов, к которым наиболее чувствителен человеческий глаз.
② Сенсация цвета:
Цвет - это ощущение, вызываемое различными спектральными компонентами энергии излучения в диапазоне видимого света. Зрение нормального человека способно различать более 150 оттенков чистых спектральных цветов. Хотя между световыми волнами и цветами существует соответствие один-к-одному, соответствие между цветами и световыми волнами не является единственным; часто один цвет света может быть образован комбинацией двух или более других цветов света. Три основных независимых цвета - красный, зеленый и синий - известны как основные цвета. Другие цвета образуются при смешивании двух или более основных цветов в различных пропорциях, а человеческий глаз очень чувствителен к цветам и способен различать множество различных цветов.
3. Три элемента, представляющие цвет
Цвет возникает в результате избирательного поглощения света драгоценными камнями, и разные драгоценные камни имеют разные цвета. Согласно современной теории цвета, его характеристики зависят от яркости, оттенка и насыщенности (рис. 3-4). Типы цветов драгоценных камней можно определить, описав три элемента различных цветов.

(1) Яркость
Яркость - это степень яркости, вызванная воздействием света на человеческий глаз, относящаяся к степени светлых и темных цветов, и может также называться яркостью. Яркость во многом зависит от восприятия глазом светлого и темного уровней источника света и поверхности объекта, в первую очередь определяемых интенсивностью света. Яркость зависит от уровня освещенности объекта и отражательной способности его поверхности.
Яркость можно понимать как яркость цвета; разные цвета имеют разные уровни яркости, и любой цвет демонстрирует изменения в светлых и темных тонах. Яркость имеет две характеристики: один и тот же объект может иметь изменения в яркости из-за разного освещения, а разные цветные лампы одинаковой интенсивности также могут иметь разные уровни яркости.
В отсутствие цвета цвет с наибольшей яркостью - белый, а цвет с наименьшей яркостью - черный, с градацией серого между светлым и темным. В цвете любая степень чистоты имеет свои характеристики яркости. Например, желтый цвет имеет самую высокую яркость, а фиолетовый - самую низкую. Зеленый, красный, синий и оранжевый имеют схожие уровни яркости, представляя собой среднюю яркость. Кроме того, в пределах одного и того же оттенка существуют вариации яркости от светлого к темному, например, светло-зеленый, бледно-зеленый и изумрудно-зеленый в зеленом спектре.
(2) Hue
Оттенок относится к различиям между разными цветами и является наиболее заметной характеристикой цвета. Оттенок определяется спектральными компонентами света, которые проходят через объект и достигают человеческого глаза после попадания на него, в зависимости от длины волны проходящего света. Оттенок объекта определяется спектром падающего источника света и светом, отраженным или пропущенным самим объектом.
Так называемый оттенок - это название, которое может более точно передать определенную цветовую категорию, например, розово-красный, оранжево-желтый, лимонно-желтый, кобальтово-синий, пурпурно-красный, изумрудно-зеленый и т.д. С точки зрения физической оптики, различные оттенки определяются спектральными составляющими света, попадающего в человеческий глаз. Для монохроматического света тип оттенка полностью зависит от длины волны этого света; для смешанного цвета - от относительного количества различных длин волн света. Цвет объекта определяется спектральными компонентами источника света и характеристиками света, отраженного (или пропущенного) поверхностью объекта. Он связан с длиной волны света. Например, цвет с доминирующей длиной волны 470 нм называется синим цветом с длиной волны 470 нм, который часто встречается в виде синего цвета сапфиров.
(3) Насыщение
Насыщенность цвета относится к чистоте и яркости цвета, указывая на долю хроматических компонентов, содержащихся в цвете. Чем больше доля хроматических компонентов, тем выше чистота цвета; чем меньше доля хроматических компонентов, тем ниже чистота цвета. Насыщенность меняется, когда цвет смешивается с черным, белым или другими цветами. Когда доля смешанного цвета достигает значительного уровня, исходный цвет теряет свой первоначальный блеск для глаза, и видимый цвет становится цветом смешанного цвета. Конечно, это не означает, что оригинальный цвет больше не существует, скорее, он был ассимилирован из-за множества других цветов, смешанных с ним, что делает его незаметным для человеческого глаза.
Монохроматический свет в видимом спектре имеет самую высокую насыщенность и является самым ярким. Монохроматический свет обычно рассматривается как 100/100 = 1, и по мере выцветания цвета значение постепенно уменьшается, а чисто белый цвет имеет нулевую насыщенность. Если взять в качестве примера чистые синие чернила, то их насыщенность равна 1, а по мере того, как они постепенно разбавляются до совершенно бесцветных, насыщенность становится нулевой.
4. Измерение цвета драгоценных камней
Система, количественно отражающая цвет, называется цветовой системой. Существует два широко используемых типа цветовых систем: одна - цветовая система, основанная на стандартных цветовых образцах для сравнения, а другая - набор цветовых стандартных систем, измеренных с помощью современных приборов для измерения цвета.
(1) Цветовая система стандартных образцов цвета
Эта цветовая система состоит из различных "цветовых карт", сделанных из бумаги, которые представляют собой стандартные образцы цветов, собранные в книгу. Их сравнивают с образцами драгоценных камней, чтобы выбрать "цветовую карту", соответствующую цвету драгоценного камня.
① Система цветов Munsell
Цветовая система Munsell - одна из самых ранних и классических систем представления цвета. Она до сих пор используется некоторыми организациями. Она была создана в 1905 году американским педагогом и теоретиком цвета Альбертом Манселлом и названа непосредственно в его честь. Это способ представления цветов с помощью цветосолидной модели. Цветовой атлас Munsell", издаваемый Оптическим обществом Америки (OSA), включает в себя глянцевую и матовую версии.
Глянцевая версия включает 1450 образцов цветов и 37 ахроматических образцов; матовая версия включает 1150 образцов цветов и 32 ахроматических образца.
В атласе Munsell каждый цвет представлен набором символов. Символы представляют собой равноудаленные индикаторы для трех элементов цветового представления: оттенка, значения и цветности, представленные как HV/C = значение оттенка/цветность.
Оттенки делятся на пять основных тонов: красный (R), желто-красный (YR), желтый (Y), зелено-желтый (GY), зеленый (G), сине-зеленый (BG), синий (B), пурпурно-синий (PB), фиолетовый (P) и красно-пурпурный (RP), а также пять промежуточных тонов. Каждый тон делится на десять уровней (от 1 до 10), пятый из которых является промежуточным цветом данного тона (рис. 3-5).
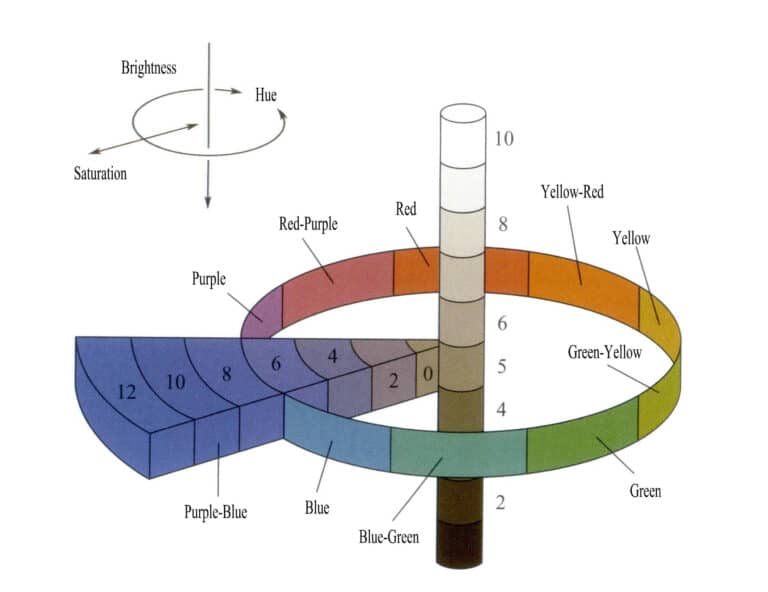
Значение Value делится на 11 уровней, причем более высокие значения означают большую светлоту; минимальное значение - 0 (черный), максимальное - 10 (белый). Цветность делится на 12 уровней. Весь цветовой атлас включает 40 типов образцов оттенков. Например, 5GY 8/7 обозначает желто-зеленый цвет со значением 8 и насыщенностью 7. Для нецветных (черных, белых, серых) серий принято обозначение NV/= нейтральное значение светлоты; например, цвет, обозначенный N5/, обозначает серый цвет со значением светлоты 5.
② Система цветов DIN 6164
Немецкий справочник DIN 6164 также является важной цветовой системой. Многие геммологи в Европе и Великобритании используют эту систему. Эта цветовая система была разработана на основе системы Munsell.
Цветовая карта DIN 6164 имеет 24 цвета, на обратной стороне каждого цвета нанесена соответствующая цветовая нотация Munsell. Они представлены в формате оттенок: насыщенность: светлота. Например, 6:6:2 означает оттенок 6 (красный), насыщенность 6 (яркий) и светлоту 2 (светлый) стандартной цветовой карты.
③ Цветовая система ISCC-NBS
ISCC (Inter-Society Colour Council) был основан в 1931 году как внутренняя цветовая ассоциация в США, и его цветовая система направлена на разработку системы наименования цветов. В ней собраны 18 оттенков, занимающих одинаковые позиции по оттенку и светлоте в стандартах Munsell и DIN 6164.
В системе ISCC-NBS (Национальное бюро стандартов) очень мало образцов цветов, соответствующих американской национальной системе стандартов, но собраны некоторые необычные образцы. Структурно она также отличается от системы Munsell, поскольку цвета в ней расположены не в соответствии с метрикой эквидистантности восприятия. Наиболее важным вкладом системы ISCC-NBS в науку о цвете является то, что она определяет названия цветов.
④ Стандарт цвета OSA
OSA (Оптическое общество Америки) подготовило практичный набор цветовых карт с акриловым блеском, включающий 558 цветов, из которых 424 цвета составляют набор, известный как цветовой стандарт OSA. Недостатком цветового стандарта OSA является то, что цветовые карты изготовлены из бумаги или пластика, которые отличаются по текстуре от драгоценных камней, а блеск поверхности цветовых карт отличается от света, отражаемого ограненными драгоценными камнями, что требует осторожного использования. Из-за выцветания срок службы большинства цветных карт составляет 4-5 лет.
(2) Хроматические координаты и хроматическая диаграмма
① Система цветового пространства CIE-XYZ 1931 года
Эта система цветового пространства основана на системе RGB и использует математические методы для выбора трех идеальных основных цветов вместо реальных основных цветов. Используя виртуальные основные цвета в качестве осей, она проецирует различные длины волн видимого света. Значения основных цветов называются значениями тристимула. Эта система требует, чтобы значения тристимула не были отрицательными и чтобы y равнялся световому потоку. Используя x в качестве горизонтальной оси и y в качестве вертикальной оси, она формирует хроматические координаты, проецируя значения хроматических координат каждого монохроматического света, чтобы получить хроматическую диаграмму. Рисунок 3-6 представляет собой стандартную хроматическую диаграмму системы (XYZ), установленную на международном уровне в 1931 году.
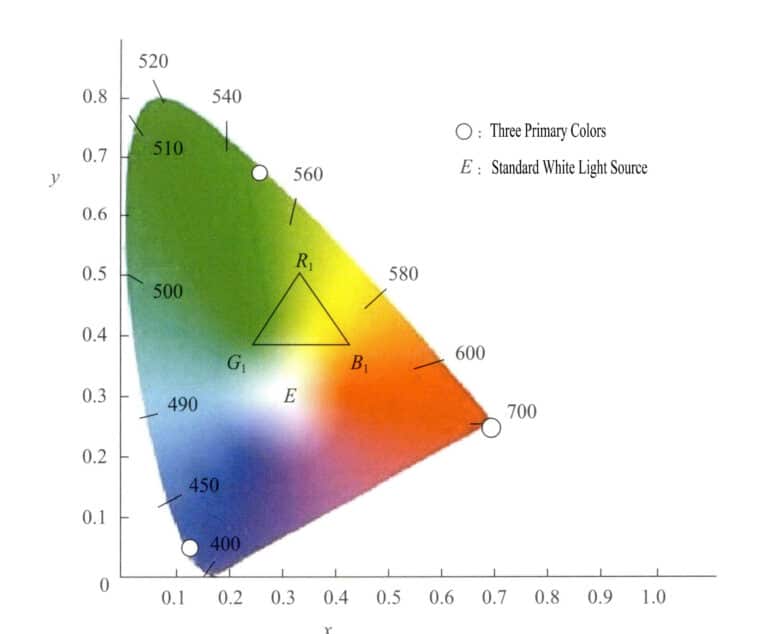
Хроматическая диаграмма имеет следующие характеристики:
- Значения тристимула основных цветов этой системы виртуальны.
- Все точки, представляющие спектральные цвета, попадают на кривую в форме языка, называемую спектральным цветом. Если соединить концы кривой прямыми линиями, то все реальные цвета будут находиться в области, окруженной кривой в форме языка и прямыми линиями.
- Значение координат точки E при x=0.333, y=0.333 представляет собой теоретический белый цвет. Различные источники белого света имеют немного разные спектральные компоненты. Обычно используемый белый свет делится на SA, SB, SC, SEи так далее.
- Хроматические координаты цветов тем насыщеннее, чем ближе они к спектральной цветовой траектории. Точки на траектории спектрального цвета имеют наибольшую насыщенность; белая точка имеет наименьшую насыщенность. Линия, проведенная от белой точки к хроматическим координатам цвета и продолженная до пересечения со спектральной траекторией цвета, имеет точки вдоль этой линии, имеющие одинаковый оттенок.
- Для получения составного цвета из любых двух цветов можно использовать графический метод. Если ввести хроматические координаты двух цветов в хроматическую диаграмму, то составной цвет должен лежать на линии, соединяющей две точки цветовых координат. Расстояние, проецируемое на две цветовые точки, связано с интенсивностью двух цветов, определяемой по закону центроидного распределения.
- Точки на прямой линии между конечными точками спектральной цветовой кривой представляют собой не спектральные цвета, а различные смешанные цвета, полученные путем смешивания пурпурного при 380 нм и красного при 780 нм в различных пропорциях.
- Выберите любые три точки в траектории цвета спектра, чтобы создать цвет. Например, если вы выберете R1, G1, B1 как три цвета для сопоставления, то все различные цвета, образованные этими тремя оттенками, содержатся в треугольнике с вершинами в трех точках R1, G1, B1.
② Представление доминирующей длины волны и насыщенности
На хроматической диаграмме цвета могут быть представлены не только хроматическими координатами (x, y). Другой метод, предложенный Гельмгольцем, заключается в том, чтобы представлять их с помощью доминирующей длины волны λd и насыщенность (чистота стимула) Pe. λd и Pe являются конкретными значениями, полученными из хроматических координат на диаграмме (рис. 3-7). Доминирующая длина волны примерно соответствует цветовому ощущению, воспринимаемому человеческим глазом.
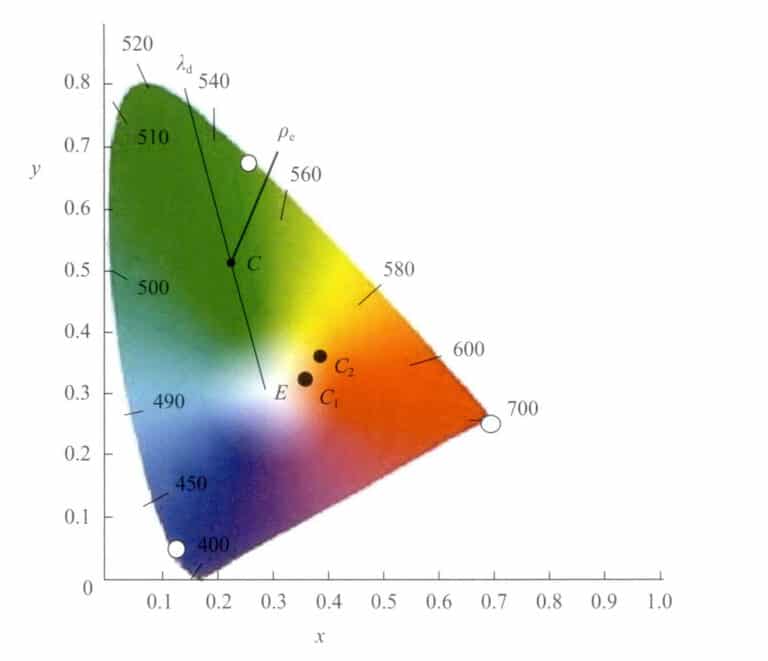
Пусть положение этой точки на хроматической диаграмме будет c(x, y). Соединим точку c с белой точкой E и продлим ее до пересечения с траекторией спектра в точке λd . Тогда волновое число точки λd на траектории спектра - доминирующая длина волны света этого цвета.
Точка C расположена на прямой, соединяющей точки W и λd , отражающая насыщенность этого цвета. Точка W - это чистый белый цвет (E) или определенный источник белого света. Когда хроматические координаты определенного цвета постепенно перемещаются по направлению к спектральной траектории от белой точки W, насыщенность цвета постепенно увеличивается до достижения спектральной траектории с максимальной насыщенностью, равной 1.
Цвета представлены с помощью доминирующей длины волны и насыщенности, что облегчает сравнение цветовых различий. Небольшие цветовые различия, представленные численными изменениями λd и ρeМожно вывести на экран.
Для двух цветов C1, C2Хроматические координаты, доминирующая длина волны и насыщенность при одинаковом освещении приведены в таблице 3-2. Видно, что доминирующая длина волны цвета C1, C2 отличается на 0,052 нм, а насыщенность - на 7%.
Таблица 3-2 Сравнение цветовых данных между C1 и С2
| Точка проекции цвета | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. Приборы для измерения цвета драгоценных камней
(1) Спектрофотометр
Принцип работы: Поскольку спектральное распределение энергии стандартного источника света в приборе известно, тристимульные значения объекта могут быть получены путем измерения его спектрального отражения.
(2) Колориметр для определения величины тристимула
Это фотоэлектрический интегративный прибор, который непосредственно измеряет три значения стимула цвета объекта. В основном он имитирует три реакции стандартного наблюдателя на цвет с помощью соответствующей комбинации фильтров и фотоэлектрических преобразователей.
В настоящее время определение цвета драгоценных камней в основном основывается на наблюдении глазами человека. Например, изумруды, рубины и бриллианты подвержены влиянию факторов окружающей среды, что приводит к низкой точности инструментальных измерений, поэтому применение инструментального измерения цвета в идентификации драгоценных камней относительно редко.
Раздел II Теоретическое происхождение цвета минералов драгоценных камней
Минералы драгоценных камней бывают разных цветов, но причины их окраски также различны. Согласно классической теории минералогии, по происхождению цвета минералы драгоценных камней можно разделить на идиохроматические, аллохроматические и псевдоцветные.
1. Классификация классической минералогии Теория происхождения цвета
Классическая теория минералогии является наиболее фундаментальной для изучения цвета драгоценных минералов. В зависимости от того, обусловлен ли цвет минерала самим минералом, его можно разделить на три категории: идиохроматически окрашенный, аллохроматически окрашенный и псевдоокрашенный.
(1) Идиохроматический цвет
Цвет драгоценного камня обусловлен химическими компонентами, присущими минералу, из которого он состоит, и называется идиохроматическим цветом. Такие драгоценные камни называются идиохроматически окрашенными. Присущие им компоненты обусловливают цвет драгоценных камней идиохроматической окраски, поэтому они обладают хорошей стабильностью цвета и не поддаются изменениям. Например, химический состав бирюзы -CuAl6(PO4)4(OH)8-5H2O, а синяя или сине-зеленая окраска вызвана Cu2+; химический состав азурита - 2CuCO3 - Cu(OH)2, и Cu2+ также является причиной его синего цвета"; зеленый цвет оливина обусловлен ионами железа в его химическом составе (рис. 3-8).

В природных минералах самоцветов не так много, основные разновидности - бирюза, малахит, азурит, оливин, гранат и родохрозит. Распространенные цвета, красящие элементы и химические составы самоцветов приведены в таблице 3-3.
Таблица 3-3 Общие красящие элементы, химический состав и цвета цветных драгоценных камней
| Элементы раскраски | Название драгоценного камня | Химический состав | Цвет |
|---|---|---|---|
| Железо | Оливин | (Mg, Fe)2 (SiO4) | Зеленый |
| Альмандин | Fe3Эл2 (SiO4)3 | Красный | |
| Хром | Уваровит | Ca3Cr2 (SiO4)3 | Зеленый |
| Cuprum | Малахит | Cu2Co3(OH)2 | Зеленый |
| Хризоколла | (CuAl)2H2Si2O5(OH)4 - nH2O | Зеленый - Синий | |
| Бирюза | CUAl6(PO4)4(OH)8.5H2O | Небесно-голубой - Зеленый | |
| Азурит | 2CuCO3 - Cu(OH)2 | Голубой | |
| Марганцовка | Спессартин-Гарне | Mn3Эл2(SiO4)3 | Оранжевый |
| Родохрозит | MnCO3 | Розовый - Красный | |
| Родонит | (Mn, Ca, Fe) - 5(Si5O15) | Розовый - Красный |
Копирайт @ Sobling.Jewelry - Пользовательские ювелирные изделия производителя, OEM и ODM ювелирный завод
Некоторые цветные драгоценные камни могут менять цвет при определенных условиях. Например, бирюза и малахит могут менять цвет под воздействием высоких температур из-за испарения молекул воды, входящих в их состав; родохрозит, карбонатный драгоценный камень, может разлагаться при контакте с кислотами (например, соляной или серной), и его цвет также изменится соответственно.
(2) Аллохроматический-цветред
Цвет драгоценного камня обусловлен незначительными примесями элементов, не входящих в химический состав минералов, входящих в его состав, и называется аллохроматическим цветом. Такие камни называются аллохроматически окрашенными.
В минералах драгоценных камней существует множество разновидностей с различными цветами. Когда в химическом составе драгоценного камня нет примесей, он бесцветен и прозрачен; когда в нем присутствуют примеси различных красящих элементов, он может иметь разные цвета.
Если чистый корунд бесцветен, то при содержании небольшого количества ионов хрома он становится рубином, а при содержании небольшого количества железа и титана - синим или зеленым драгоценным камнем. К подобным драгоценным камням относятся изумруд, шпинель, турмалин, жадеит, халцедон, нефрит и др. Распространенные красящие элементы, химические составы и драгоценные камни аллохроматического цвета приведены в таблице 3-4.
Таблица 3-4 Общие элементы окраски, химический состав и драгоценные камни аллохроматической окраски
| Элементы раскраски | Название драгоценного камня | Химический состав | Цвет |
|---|---|---|---|
| Хром | Руби | Эл2O3 | Красный |
| Изумруд | Будьте3Эл2(Si6O18) | Зеленый | |
| Александрит | BeAl2O4 | Красно-зеленый | |
| Шпинель | MgAl2O4 | Красный | |
| Халцедон | SiO2 | Зеленый | |
| Железо | Аквамарин | Будьте3Эл2Si6O18 | Голубой |
| Турмалин | (Na, K, Ca) (Al, Fe3+, Cr)6(BO3)3Si6O18(OH)4 | Зелено-коричневый | |
| Шпинель | MgAl2O4 | Желтый | |
| Нефрит | Ca2(Mg, Fe2+) 5 (Si4O11) 2 (OH)2 | Зеленый | |
| Ванадий | Танзанит | Ca2Эл3(SiO4)3(OH) | Пурпурно-голубой |
| Зеленый берилл | Будьте3Эл2Si6O18 | Зеленый | |
| Титан | Бенитоит | BaTiSi3O9 | Голубой |
| Сапфир | Эл2O3 | Голубой | |
| Марганцовка | Красный берилл | Будьте3Эл2Si6O18 | Красный |
| Родохрозит | MnCO3 | Розовый | |
| Кобальт | Натуральная шпинель | MgAl2O4 | Голубой |
| Синтетическая шпинель | MgAl2O4 | Голубой | |
| Никель | Зеленый халцедон | SiO2 | Зеленый |
(3) Псевдо-цветред
Цвета, создаваемые псевдоцветами, не связаны с химическим составом минералов драгоценных камней. Тем не менее, они обусловлены структурными и композиционными изменениями, происходящими в результате механического смешения или образования минералов. Псевдоцвета - это не цвета самих минералов, а цвета, вызванные особыми структурами, образовавшимися в результате внешних воздействий. Например, красивые интерференционные цвета, возникающие в результате интерференции отраженного и падающего света, такие как эффект флюоресценции лабрадорита и эффект игры цвета опала. Окраска, вызванная включениями, также относится к псевдоцветам, как, например, черные бриллианты из-за множества черных непрозрачных графитовых включений внутри бриллианта.
2. Ионы, вызывающие окраску, в драгоценных минералах
Химические элементы, создающие цвета драгоценных камней, могут быть основными или второстепенными компонентами. Элементы переходных металлов, особенно переходные металлы четвертого периода - титан, ванадий, хром, марганец, железо, кобальт, никель и медь, - часто называют хромофорами или красящими ионами. Эти восемь элементов занимают последовательные позиции в периодической таблице, их атомные номера варьируются от 22 (Ti) до 29 (Cu). Основные свойства этих элементов приведены в таблице 3-5.
Таблица 3-5 Основные свойства восьми переходных элементов
| Имя элемента | Титан | Ванадий | Хром | Марганцовка | Железо | Кобальт | Никель | Медь |
|---|---|---|---|---|---|---|---|---|
| Символ элемента | Ti | V | Cr | Mn | Fe | Co | Ni | Cu |
| Атомный номер | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| Основные состояния окисления | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| Конфигурация валентного электрона | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
Эти восемь переходных металлических элементов обладают следующими характеристиками:
① Валентные электроны заполняют d-орбитали предпоследней по порядку оболочки, и общая формула для конфигурации валентных электронов атомов переходных элементов имеет вид (n-1)d1-10nS1-2поэтому эти элементы также называются d-блочными.
② В переходных металлах, поскольку d-орбитали предпоследней оболочки связаны с крайними s-орбиталями, а d-орбитали еще не достигли стабильной структуры, как s-электроны, так и d-электроны могут частично или полностью участвовать в связи, что приводит к ряду переменных состояний окисления для переходных металлов, причем разные оксиды имеют разные цвета в драгоценных камнях.
③ Ионы обычно проявляют цвет, потому что на d-орбиталях находятся неспаренные одиночные электроны, а энергетические уровни этих электронов в возбужденном и основном состояниях относительно близки, что позволяет возбуждать их энергией видимого света. Различные условия возбуждения также могут вызывать различные цвета драгоценных камней.
Если все спиновые электроны в ионе спарены, например, ионы с валентной электронной конфигурацией d0, d10, d10s2электроны находятся в стабильном состоянии и не могут быть легко возбуждены, в результате чего ион не имеет цвета; таким образом, C+, Cr6+ и другие не имеют цвета и не могут создавать цвет в драгоценных камнях.
Эти восемь элементов переходных металлов образуют цвет в обычных драгоценных камнях естественного цвета. Различные хромофоры дают разные цвета в разных драгоценных камнях, и один и тот же хромофор может также давать разные цвета. Распространенные природные драгоценные камни и хромофоры приведены в таблице 3-6.
Таблица 3-6 Цвета, представленные ионами переходных металлов в распространенных природных драгоценных камнях и разновидностях драгоценных камней
| Хромофор | Обычные цвета | Сорта драгоценных камней |
|---|---|---|
| Ион титана (Ti) | Голубой | Сапфир, бенитоит, топаз |
| Ион ванадия (V) | Зеленый | Синтетический корунд с изменением цвета, эссонит, изумруд |
| Ион хрома (Cr) | Красный, зеленый | Рубин, корунд, изумруд, пироп, нефрит |
| Ион марганца (Mn) | Розовый, красный | Спессартин, родолит, красный берилл |
| Ион железа (Fe) | Синий, зеленый, желтый | Сапфир, оливин, аквамарин, турмалин, шпинель |
| Ион кобальта (Co) | Голубой | Синтетическая шпинель, ставролит кобальтового цвета |
| Ион никеля (Ni) | Зеленый | Зеленый халцедон |
| Ион меди (Cu) | Синий, сине-зеленый | Малахит, бирюза, азурит |
Различные хромофорные ионы придают драгоценным камням разные цвета, что приводит к появлению спектров поглощения с различными характеристиками. Для распространенных хромофорных ионов спектры поглощения имеют типичное идентификационное значение.
(1) Спектр поглощения ионов хрома
Спектр поглощения ионов хрома характеризуется множеством узких линий поглощения в красной области, причем две самые сильные расположены в глубокой красной области, а еще две - в оранжевой. В желто-зеленой области имеется широкая полоса поглощения, ширина, положение и интенсивность которой зависят от глубины цвета драгоценного камня. В синей области может быть несколько узких полос, а фиолетовая область полностью поглощена. Ионы хрома в основном дают красный и зеленый цвета, которые в разных драгоценных камнях отличаются, и спектры поглощения имеют некоторые различия. Например, рубин имеет три линии поглощения в красной области, широкую полосу поглощения в желто-зеленой области, три линии поглощения в синей области и полное поглощение в фиолетовой области; изумруд имеет линии поглощения в красной области, слабую полосу поглощения в оранжево-желтой области, слабые линии поглощения в синей области и полное поглощение в фиолетовой области; а александрит имеет линии поглощения в красной области, полосу поглощения в желто-зеленой области, одну линию поглощения в синей области и полное поглощение в фиолетовой области. Спектры поглощения этих трех драгоценных камней показаны на рисунке 3-9.

(2) Характеристики спектра поглощения ионов железа
Ионы железа создают различные цвета в разных драгоценных камнях и обладают сильным окрашивающим эффектом, но спектр поглощения ионов железа сильно варьируется. Когда драгоценный камень зеленый, он дает поглощение в красной зоне, а когда он красный, в нем преобладает поглощение в синей зоне, а главная характерная линия поглощения расположена в зеленой и синей зонах. Например, ионы железа в оливине выглядят оливково-зелеными, а в спектре поглощения в основном наблюдаются три узкие полосы поглощения в синей области при 453, 473 и 493 нм; красный альмандин имеет типичный спектр поглощения железа, с тремя сильными узкими полосами поглощения при 504, 520 и 573 нм в желто-зеленой области, обычно называемой в промышленности "железным окном". Кроме того, имеются слабые узкие полосы поглощения при 423 нм, 460 нм, 610 нм и 680~690 нм; спектр поглощения желтого сапфира имеет три узкие полосы поглощения в синей области при 450 нм, 460 нм, 470 нм. (Рисунок 3-10).
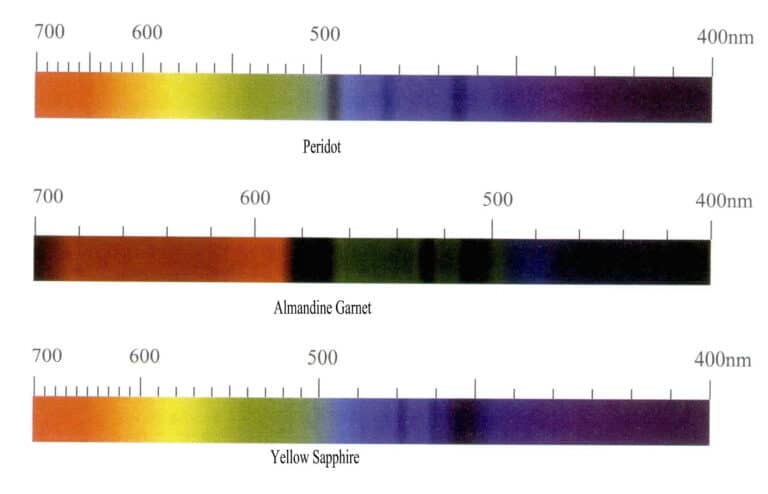
(3) Характеристики спектра поглощения ионов марганца
Ионы марганца в основном образуют в драгоценных камнях розовый, оранжевый и красный цвета, а спектр поглощения в основном показывает сильное поглощение в фиолетовой области, простирающееся в ультрафиолетовую область, и некоторое поглощение в синей области. Например, характеристики спектра поглощения розового родохрозита имеют три полосы поглощения при 410 нм, 450 нм, 540 нм; линии спектра поглощения спессартина в основном имеют 410 нм, 420 нм, 430 нм три полосы поглощения и линии поглощения при 460 нм, 480 нм и 520 нм. Иногда могут присутствовать две линии поглощения 504 нм, 573 нм (рис. 3-11).

(4) Характеристики спектра поглощения ионов кобальта
Ионы кобальта оказывают сильное окрашивающее действие, обычно проявляясь в драгоценных камнях ярко-синим цветом, а в спектре поглощения наблюдаются три сильные и широкие полосы поглощения в желто-зеленой области. Из-за низкого содержания кобальта в земной коре существует очень мало природных драгоценных камней, окрашенных ионами кобальта. Спектр поглощения ионов кобальта также указывают синтетические драгоценные камни, такие как синтетическая голубая шпинель и кобальтовое стекло. Синтетическая голубая шпинель имеет три сильные полосы поглощения в желто-зеленой и оранжево-желтой областях, причем полоса поглощения в зеленой области является самой узкой; линии поглощения кобальтового стекла в основном имеют три сильные полосы поглощения в желто-зеленой и оранжево-желтой областях, причем полоса поглощения в желтой области является самой узкой (рис. 3-12).

3. Раскраска с редкоземельными элементами
Исследования влияния редкоземельных элементов на цвет драгоценных камней становятся все более глубокими. Цвета редкоземельных элементов более яркие, а их физико-химические свойства также очень стабильны. Редкоземельные элементы, такие как апатит и флюорит, также могут окрашивать природные драгоценные камни. Различные редкоземельные элементы могут быть добавлены в синтетические и оптимально обработанные драгоценные камни, чтобы получить различные цветные камни, например, желтый от церия и синий от неодима.
Редкоземельные элементы, окрашивающие драгоценные камни, в основном относятся к лантаноидам и актинидам в периодической таблице химических элементов, а цвета, которые они могут создавать, показаны в таблице 3-7.
Таблица 3-7 Редкоземельные элементы и их цвета в распространенных драгоценных камнях
| Символ элемента | La | Ce | Nd | Pr | Dy | Sm | Er | Tm | U |
|---|---|---|---|---|---|---|---|---|---|
| Полное имя | Лантан | Церий | Неодим | Празеодим | Диспрозий | Самарий | Эрбий | Тулий | Уран |
| Цвет | Бесцветный | Желтый | Голубой | Зеленый | Светло-желтый | Светло-желтый | Розовый | Светло-зеленый | Серебристо-белый |
Редкоземельные элементы имеют характерные спектры поглощения, часто образующие уникальные тонкие линии. Например, желтый апатит часто содержит редкоземельный элемент Ce с характерными тонкими линиями поглощения в желтой области. Однако уран не дает ярко-желтого цвета; он может генерировать отчетливые спектральные линии поглощения. Например, в зеленом цирконе в различных цветовых зонах может наблюдаться более десяти линий поглощения (рис. 3-13).

Раздел III Цвета, создаваемые дефектами кристаллов и центрами окраски
В природе минералы делятся на кристаллы и некристаллы в зависимости от степени кристаллизации. Большинство драгоценных камней, таких как рубины, сапфиры, алмазы, изумруды и кварц, представляют собой кристаллы; некоторые органические драгоценные камни, такие как янтарь и кораллы, являются некристаллическими. Кристаллические структуры имеют решетчатую структуру, где их внутренние частицы (атомы, ионы или молекулы) расположены в регулярном периодическом порядке в трехмерном пространстве, и кристаллы могут спонтанно образовывать многогранные формы; некристаллические - это аморфные тела с нерешетчатой структурой, которые не могут образовывать многогранные формы, такие как стекло, канифоль и смола.
Наиболее типичный пример различия между кристаллами и аморфными твердыми телами - кварц и стекло. Природный кварц образуется из расплавленного материала SiO2 в магме, остывающей в полостях земной коры. Внешний слой обычных кварцевых шаров - это агат, который не имеет кристаллической формы, в то время как внутренний слой представляет кристаллическую форму кварца. Основными химическими компонентами как стекла, так и кварца являются SiO2Кварц - это кристалл, в котором ионы кремния и кислорода расположены упорядоченно, а стекло - это аморфное твердое вещество, в котором ионы кремния и кислорода расположены хаотично, без закономерности, как показано на рисунке 3-14.
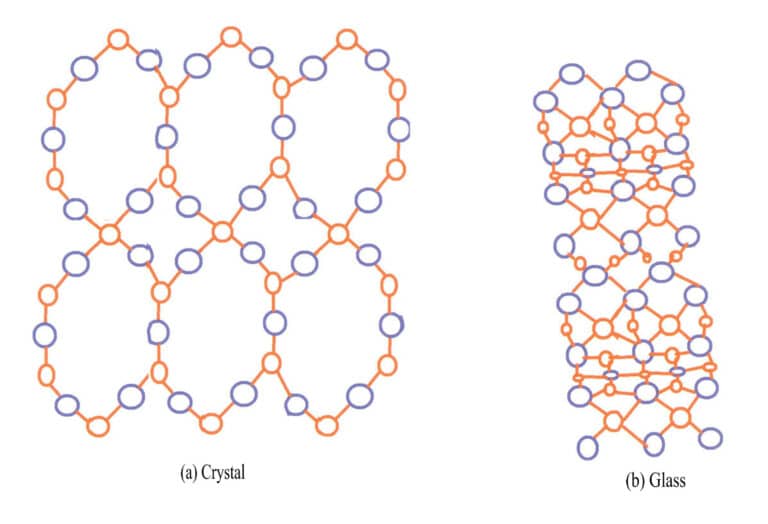
Большинство кристаллов драгоценных камней окрашены за счет ионов примесей, например рубины, изумруды и турмалины. Некоторые драгоценные камни, хотя и не содержат ионов-хромофоров, окрашены из-за дефектов в кристаллической структуре. Натуральные драгоценные камни, добытые в природе, могут менять цвет под воздействием внешних условий, таких как облучение и ионизация, которые изменяют кристаллическую структуру. Наиболее распространенным примером является дымчатый кварц, цвет которого формируется за счет образования центров окраски из радиационно-индуцированных вакансий. Искусственно облученный дымчатый кварц имеет схожий с природным дымчатым кварцем принцип образования, за исключением того, что искусственное излучение быстро создает цвет.
1. Дефекты кристаллов и их типы
Явление, при котором расположение частиц отклоняется от правил строения решетки (частицы совершают периодические трансляционные повторения в трехмерном пространстве) в локальном диапазоне кристаллической структуры драгоценного камня, называется дефектом решетки. Причины возникновения связаны с тепловыми колебаниями частиц внутри кристалла драгоценного камня, внешним напряжением, высокой температурой и давлением, облучением, диффузией, ионной имплантацией и другими условиями.
Например, алмазы, кристаллизовавшиеся в высокотемпературной и высоконапорной среде верхней мантии, быстро выносятся к поверхности Земли вмещающей магмой (кимберлитом или лампроитом), быстрое изменение температуры и давления и взаимные столкновения между кристаллами и окружающими породами могут легко привести к локальным изменениям в структуре интрузивных кристаллов алмаза, в результате чего возникают дефекты решетки, изменяющие цвет изначально бесцветных алмазов, образуя коричневато-желтые, коричневые и розовые алмазы.
Наличие дефектов в кристаллах оказывает существенное влияние на их свойства. В действительности кристаллы имеют большее или меньшее количество дефектов. Умеренное количество определенных точечных дефектов может значительно повысить проводимость полупроводниковых материалов и люминесценцию люминесцентных материалов, играя благоприятную роль. Напротив, такие дефекты, как дислокации, могут сделать материалы склонными к разрушению, снижая прочность на разрыв кристаллов, в которых почти нет дефектов решетки, до незначительной величины.
В идеально совершенном кристалле атомы расположены строго в регулярной, периодической решетке в определенных точках пространства. Однако в процессе роста и формирования кристаллов под влиянием таких условий роста, как температура, давление и концентрация компонентов среды, морфология кристалла после роста может иногда отклоняться от идеальной кристаллической структуры. Любое отклонение от идеальной кристаллической структуры можно назвать дефектом кристалла. Дефекты кристаллов существенно влияют на физические и химические свойства кристаллов, и многие дисциплины связаны с дефектами кристаллов, например, ионное легирование в материаловедении. Цвет драгоценных камней во многом связан с наличием в них кристаллических дефектов. Это одна из причин возникновения цвета в драгоценных камнях - цветовые центры.
Существует множество типов дефектов кристаллической структуры, которые можно разделить на четыре категории по степени их распределения в трехмерном пространстве: точечные дефекты, линейные дефекты, поверхностные дефекты и объемные дефекты.
(1) Точечные дефекты
Другие атомы замещают некоторые атомы в идеальном кристалле, некоторые легируются, или образуются вакансии. Некоторые атомы в кристалле заменяются или отсутствуют из-за воздействия внешних атомов, и эти изменения нарушают периодическое расположение регулярной решетки кристалла, вызывая изменения в потенциальном поле частиц и приводя к неполноте кристаллической структуры, ограниченной определенными позициями и затрагивающей лишь несколько близлежащих атомов. Влияние точечных дефектов на кристалл минимально, и распространенные типы точечных дефектов включают дефекты положения решетки, композиционные дефекты и дефекты заряда (рис. 3-15).
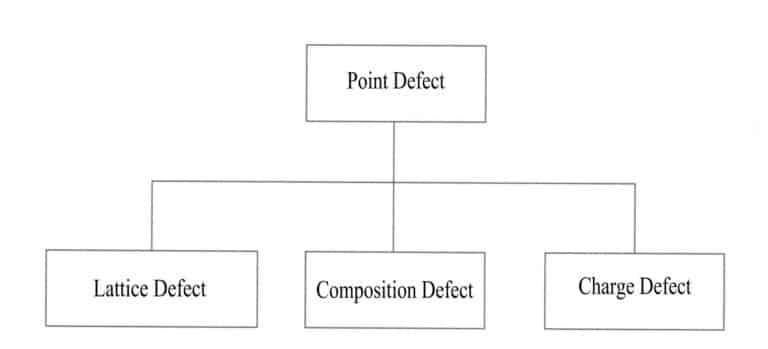
(2) Дефекты линии
Линейные дефекты очень малы по размеру в двух направлениях и в основном имеют большую протяженность в другом направлении. Они также известны как одномерные дефекты и состоят в основном из различных дислокаций. Дислокации можно рассматривать как продукт локального проскальзывания решетки вдоль определенной атомной плоскости. Проскальзывание не пронизывает всю решетку; дефект кристалла заканчивается внутри решетки, вызывая неупорядоченное расположение частиц на границе между проскользнувшей и непроскользнувшей частями решетки, известное как дислокация. Эта граница, линия пересечения между проскользнувшими и непроскользнувшими участками, называется дислокационной линией. Существует два основных типа дислокаций: когда кристалл подвергается сжимающим усилиям, плоскость скольжения частиц образует дислокационную линию с плоскостью скольжения, и дислокационная линия перпендикулярна направлению скольжения, что называется краевой дислокацией, также называемой клиновой дислокацией; под действием сдвигающего напряжения происходит скольжение между плоскостями, и пересекающиеся дислокационные линии в скользкой части кристалла параллельны направлению скольжения, что называется винтовой дислокацией (рис. 3-16).
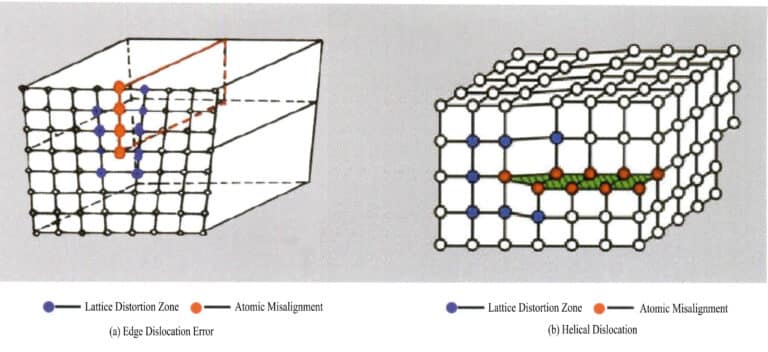
(3) Дефекты поверхности
Простейшим поверхностным дефектом является дефект стэкинга, который подразделяется на внутренний дефект стэкинга (когда кристаллическая плоскость удаляется) и внешний дефект стэкинга (когда атомный слой вставляется в кристалл). Эти дефекты возникают в диапазоне нескольких межатомных расстояний по обе стороны от определенной плоскости решетки или между зернами. В основном они включают дефекты укладки и интерфейсы внутри и между кристаллами, такие как малоугловые границы зерен, доменные стенки, двойниковые и межзеренные границы.
(4) Дефекты объема
Объемные дефекты - это дефекты, которые в той или иной степени существуют во всех трех направлениях, это трехмерные дефекты, такие как вкрапленные трещины, сетчатые структуры, семейные структуры, двойники и различные включения в драгоценных камнях.
2. Цветовые центры в драгоценных камнях
Цветовые центры - это особый случай дефектов решетки, в целом относящийся к дефектам решетки в драгоценных камнях, которые могут избирательно поглощать видимую световую энергию и создавать цвет, относясь к наиболее типичным структурным цветовым типам. В некоторых случаях неспаренные электроны, создающие цвет, могут также появляться в ионах непереходных элементов или в дефектах кристалла, образующихся из-за недостатка электронов, что и является центрами цвета. Точечные дефекты в ионных кристаллах могут вызывать поглощение видимого света, в результате чего изначально прозрачные кристаллы становятся цветными; такие точечные дефекты, способные поглощать видимый свет, обычно называют центрами цвета. Многие виды природных драгоценных камней приобретают цвет благодаря цветовым центрам, например фиолетовый флюорит, дымчатый кристалл и зеленые бриллианты.
В процессе оптимизации обработки драгоценных камней некоторые природные и искусственные камни также могут иметь цветовые центры, генерируемые излучением, такие как синие, желтые, красные, зеленые бриллианты и голубые топазы, которые меняют цвет под воздействием излучения, и голубые топазы, среди которых некоторые цвета относительно стабильны и исчезают только при нагревании; некоторые цвета нестабильны и могут потускнеть даже при комнатной температуре. Этот тип цветового центра тесно связан с кристаллической структурой драгоценного камня, как, например, зеленые бриллианты, где причиной цвета является наличие вакансий в кристаллической структуре, но этот структурный дефект также может быть удален облучением, превращая бриллиант в бесцветный. Распространенными типами центров окраски в драгоценных камнях являются "центры окраски электронов" и "центры окраски дырок".
(1) Центр цвета электронов (F-центр)
Электронные центры цвета - это центры цвета, образующиеся при наличии электронов в вакансиях кристаллических дефектов, вызванных анионными вакансиями в кристаллической структуре драгоценного камня. Когда анион отсутствует, вакансия становится положительно заряженной электронной ловушкой, которая задерживает электроны. Если вакансия захватывает электрон и связывает его с этой вакансией, электрон становится возбужденным и избирательно поглощает энергию определенной длины волны, приобретая окраску. Таким образом, электронный центр окраски состоит из анионной вакансии и электрона, связанного электрическим полем этой вакансии.
Фиолетовый флюорит - цвет, создаваемый электронными центрами цвета. Флюорит (CaF2) принадлежит к изометрической кристаллической системе, причем каждый Ca2+ подключен к двум F– [Рисунок 3-17 (a)]. В некоторых случаях F– в флюорите может покинуть свое нормальное положение. В исходном месте F появляется вакансия.– Чтобы сохранить электрическую нейтральность кристалла, эту вакансию должен занять отрицательно заряженный объект. Отрицательно заряженной сущностью, занимающей эту вакансию, становится электрон из определенного атома в кристалле [Рисунок 3-17 (b)]. Таким образом, образуется "центр цвета", известный как электронный центр цвета. Во флюорите электронные цветовые центры поглощают видимый свет, создавая фиолетовый цвет.
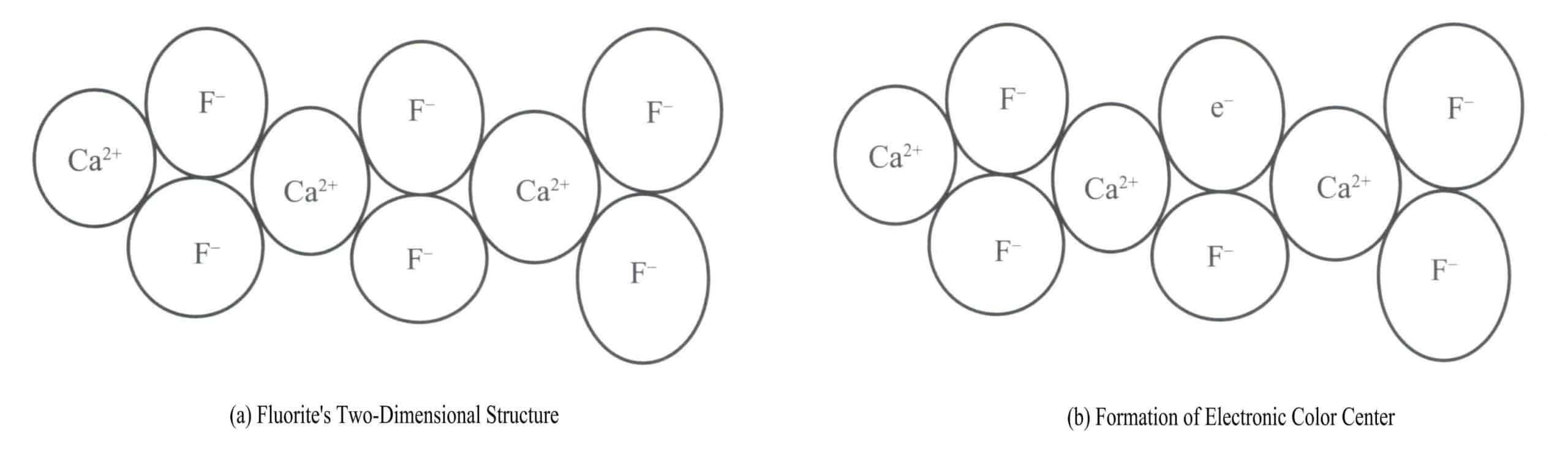
(2) Центры цвета отверстий (V-центры)
Вакантный цветовой центр образуется под воздействием внешних факторов, когда катионы создают электронные вакансии. Это означает, что электроны выбрасываются из своих исходных позиций, оставляя после себя неспаренный электрон. Причина появления цвета заключается в том, что когда в кристалле образуются вакансии катионов, для достижения зарядового баланса анионы вблизи вакансии катиона под воздействием внешней энергии высвобождают электроны, образуя неспаренные электроны, которые поглощают видимый свет и создают цвет. Например, в облученных бриллиантах и голубых топазах облучение дает энергию для активации электронов, заставляя ионы или атомы в решетке смещаться, образуя структурные дефекты и центры цвета, обусловленные облучением.
Классическим примером цветового центра в кристалле является окраска дымчатого кристалла. Кристаллическая структура кварца представляет собой кремниево-кислородный тетраэдр, в котором кремний находится в четырехкоординатном состоянии, как показано на двумерной структурной схеме на рисунке 3-18(a). Каждые 10 000 Si4+ атомы заменены на Al3+, и когда Al3+ заменяет Si4+ в кристалле, Al3+ должны быть окружены некоторыми ионами щелочи (например, Na+ или H+) для поддержания электрической нейтральности. Тем не менее, эти ионы часто находятся на определенном расстоянии от Al3+.
При облучении кварца рентгеновскими, γ-лучами и другими источниками излучения энергия соседних атомов кислорода с Al3+ увеличивается, что позволяет одному из электронов в его паре быть выброшенным из своего обычного положения. H+ захватит этот электрон и образует H . Под действием высокоэнергетического излучения O2- с большим количеством валентных электронов, чтобы освободить электрон, образуя [A1O4]4- центр окраски вакансий, и [A1O4]4- Атомный кластер поглощает видимый свет, придавая ему цвет, образуя дымчатый кварц.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ захватывает электроны и превращается в H, который бесцветен и не поглощает видимый свет. Если интенсивность облучения высока и имеется достаточное количество Al3+ в кристалле, кварц может быть облучен до черного цвета. Поскольку в месте вылета электрона часто имеется вакансия, этот тип цветового центра называют "вакансионным цветовым центром".
В ходе геологической истории природный дымчатый кристалл в основном образуется в результате длительного низкодозового облучения радиоактивными материалами. Нагревание может устранить цвет; когда дымчатый кристалл нагревается примерно до 400℃, выброшенные электроны возвращаются в исходное положение, все электроны объединяются в пары, и кварц снова становится бесцветным; если его снова облучить, он может снова стать дымчатым [рис. 3-18 (b)].
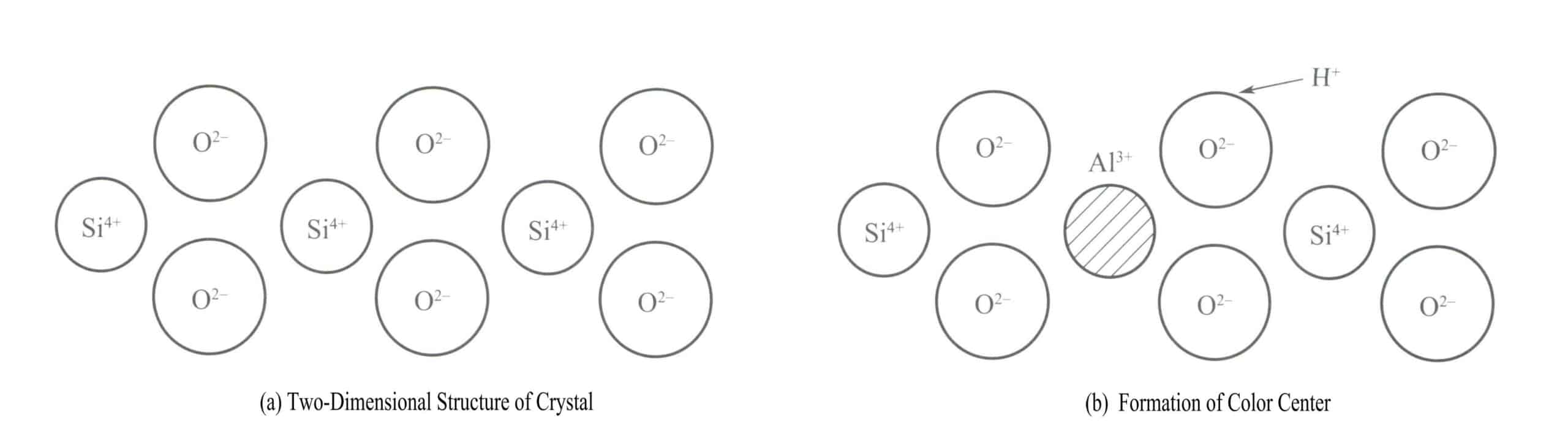
Аметист имеет те же цветовые центры вакансий, но его примесью является железо, а не алюминий. Когда примесь Fe 3+ заменяет Si4+ в кварце при облучении высокоэнергетическими лучами происходят следующие изменения:
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
Подобно принципу образования дымчатого кристалла, он дает фиолетовый цвет за счет образования [FeO4]4- центры цвета дыры после облучения. При нагревании аметист желтеет, превращаясь в цитрин, а при дальнейшем нагревании тускнеет до бесцветного. Как правило, температура нагрева относительно низкая, около 400℃. Пурпурный цвет термообработанного аметиста можно восстановить, снова облучив центры окраски. По такому принципу синтезируется и синтетический аметист.
В некоторых драгоценных камнях несколько кластеров примесных атомов также могут образовывать цветовые центры и проявлять цвет. Например, во время роста берилла и при радиоактивном облучении, может потерять электрон и стать , образуя красно-зеленую полосу поглощения, которая дает синий цвет. В алмазах существует множество цветовых центров, большинство из которых обусловлено образованием вакансий или дислокаций в структуре под воздействием внешних условий, и цвета, как правило, очень стабильны.
Сложность изучения цвета, индуцированного цветовым центром, относительно высока и требует применения различных методов, таких как спектроскопия и электронный парамагнитный резонанс. Предыдущие исследования показывают, что некоторые типичные характеристики цвета, индуцированного центром окраски, относительно ясны. В таблице 38 приведены цвета и причины индуцированной окраски центра цвета в распространенных драгоценных камнях.
Таблица 3-8 Цвета и причины возникновения цвета, индуцированного центром, в распространенных драгоценных камнях
| Виды драгоценных камней | Цвет | Причина |
|---|---|---|
| Алмаз | Зеленый | Углеродная вакансия Центр цвета GR1 в бриллианте |
| Желтый | Недостающая структура алмазных агрегатов N3 | |
| Оранжевый | Натомы и дефекты цветовых центров H3, H4 | |
| Кристалл | Цвет дыма | Вакансии, созданные компанией Al3+ заменяя Si4+ , связанные с радиацией |
| Желтый | Связанные с Элом3+Но она также может генерироваться излучением | |
| Фиолетовый | Fe3+ замещает вакансию, образованную Si4+ | |
| Драгоценный камень корунд | Желтый | Цвет нестабильный, причина структурных дефектов неизвестна |
| Топаз | Голубой | Цвет стабильный, причина структурных дефектов неизвестна |
| Желтый | Цвет стабильный, причина структурных дефектов неизвестна | |
| Коричневато-красный | Цвет нестабильный, причина структурных дефектов неизвестна | |
| Турмалин | Красный | Связанные с Мн3+ может быть вызвано радиацией |
| Берил | Голубой | Связано с CO32- может быть вызвано облучением |
| Флюорит | Фиолетовый | Электронное е- заменяет F-, чтобы произвести |
Принцип цветовых центров также используется для улучшения цвета натуральных драгоценных камней при их облагораживании. Большинство методов используют облучение для изменения цвета драгоценных камней. Некоторые цветовые центры относительно стабильны, в то время как некоторые разновидности драгоценных камней быстро тускнеют, что делает этот метод улучшения менее значимым для этих камней. В таблице 3-9 перечислены некоторые цвета, создаваемые цветовыми центрами, включая стабильные цветовые центры, нестабильные цветовые центры и цвета, создаваемые другими возможными факторами.
Таблица 3-9 Цвета, производимые цветовыми центрами
| Устойчив на свету | Аметист, флюорит (фиолетово-красный), облученные алмазы (зеленый, желтый, коричневый, черный, голубой, розовый); несколько природных или облученных топазов (голубой) |
|---|---|
| Быстро выцветает на свету | Зеленый берилл с цезием лития (темно-синий); некоторые облученные топазы (коричневые или загорелые); облученный сапфир (желтый); облученный ультрафиолетом фиолетовый содалит (пурпурно-красный). |
| Другие цвета, которые могут производить цветовые центры | Сильвин (синий); галит (синий или желтый); циркон (коричневый); кальцит (желтый); барит, целестин (синий); амазонит (от синего до зеленого) |
















