Dlaczego kamienie szlachetne mają wiele kolorów?
Sekrety tworzenia kolorów i metody pomiaru
Kolory kamieni szlachetnych są bogate i zróżnicowane, posiadając unikalny urok, który ludzie zawsze kochali. Jakość kamieni szlachetnych w dużej mierze zależy od ich koloru. Kolor kamienia szlachetnego jest ważnym wskaźnikiem w ocenie kamieni szlachetnych, a większość zabiegów optymalizacyjnych dla kamieni szlachetnych obejmuje zmianę lub poprawę ich koloru. Dlatego też zrozumienie przyczyn zabarwienia kamieni szlachetnych jest kluczowym warunkiem wstępnym dla ich optymalizacji. Tylko poprzez opanowanie tego, w jaki sposób kamienie szlachetne uzyskują swój kolor, można określić, czy kamień szlachetny można zoptymalizować, jaki schemat optymalizacji przyjąć i jaki plan eksperymentalny ustalić. Istnieje pięć powszechnych teorii zabarwienia kamieni szlachetnych: klasyczna teoria mineralogii, teoria pola krystalicznego, teoria orbitali molekularnych, teoria pasm energetycznych i fizyczne efekty optyczne. Teorie te stanowią teorie zabarwienia powszechnych naturalnych kamieni szlachetnych, a poniżej znajduje się krótkie wprowadzenie do tych pięciu teorii zabarwienia.

Schematyczny diagram trzech elementów koloru
Spis treści
Sekcja I Kolor i pomiar koloru kamieni szlachetnych
Kolory kamieni szlachetnych są bogate i zróżnicowane, a określenie rodzajów kolorów kamieni szlachetnych ma kluczowe znaczenie dla oceny ich wartości. Różne klasy kolorów również wpływają na wartość kamieni szlachetnych; dlatego dokładna ocena kolorów różnych kamieni szlachetnych jest podstawowym warunkiem wstępnym do określenia ich wartości. Przy ocenie kolorowych kamieni szlachetnych, kolor jest najważniejszym czynnikiem. Ogólnie rzecz biorąc, im bardziej atrakcyjny kolor kamienia szlachetnego, tym wyższa jego wartość. Jasne, bogate i intensywne kolory są zazwyczaj bardziej atrakcyjne niż te zbyt ciemne lub zbyt jasne. Oczywiście istnieją wyjątki, takie jak diamenty, gdzie im wyższa biel koloru diamentu, tym wyższa jego wartość.
1. Znaczenie kolorów kamieni szlachetnych
Od czasów starożytnych ludzie kochali kamienie szlachetne ze względu na ich wyjątkowy urok, zwłaszcza bogate i kolorowe odcienie kamieni szlachetnych, takie jak rubin w kolorze gołębiej krwi, żywy zielony szmaragd i jadeit, z których wszystkie pozostawiają trwałe wrażenie. Kolor jest ważnym wskaźnikiem oceny jakości kamieni szlachetnych i odgrywa kluczową rolę w określaniu ich jakości, a jego znaczenie znajduje odzwierciedlenie głównie w następujących trzech aspektach.
(1) Kolor minerałów kamieni szlachetnych jest ważną podstawą do oceny kamieni szlachetnych
Kolor kamienia szlachetnego ma fundamentalne znaczenie dla jego oceny i określa jego wartość. Na przykład w przypadku diamentów, różnica w kolorze o jeden stopień może prowadzić do różnicy w cenie wynoszącej około 5%. Im wyższa biel, tym wyższa ocena diamentu; odwrotnie, diamenty o żółtych lub brązowych odcieniach mają niższe oceny, a ich ceny gwałtownie spadają. Ceny kolorowych diamentów są różne, a różne kolorowe diamenty mają różne ceny. Jednak ogólnie rzecz biorąc, ceny rzadkich kolorowych diamentów mogą się zwielokrotnić. Inne kolorowe kamienie szlachetne, takie jak rubiny, szafiry i szmaragdy, są również klasyfikowane w różnych klasach na podstawie koloru, a wartość kamieni szlachetnych w różnych klasach może się znacznie różnić.
(2) Optymalizacja obróbki kamieni szlachetnych często obejmuje poprawę ich koloru
Metody optymalizacji obróbki kamieni szlachetnych zwykle obejmują zmianę lub poprawę koloru kamieni szlachetnych, więc poprawa kamieni szlachetnych może być również określana jako zmiana koloru kamieni szlachetnych. Wraz z poprawą koloru kamienia szlachetnego zmienia się również jego przezroczystość. Wynika to z faktu, że przezroczystość jest właściwością związaną z kolorem. Na przykład niebieskie szafiry wydają się mieć wiele nieprzezroczystych czarnych kolorów gołym okiem, ale przezroczysty niebieski można zobaczyć po pocięciu na cienkie plasterki. Poprawa przezroczystości często towarzyszy poprawie koloru. Dlatego tylko poprzez określenie przyczyny koloru kamienia szlachetnego można ustalić metody jego poprawy. Zrozumienie przyczyny koloru jest warunkiem wstępnym do studiowania metod optymalizacji kamieni szlachetnych.
(3) Badanie przyczyn koloru kamieni szlachetnych stanowi teoretyczną podstawę dla syntetycznych kamieni szlachetnych i ich ulepszania.
Kolory kamieni szlachetnych, takich jak granat, malachit i oliwin, wynikają z ich nieodłącznych składników i nie można zmienić ich kolorów za pomocą konwencjonalnych metod optymalizacji. Większość kolorów kamieni szlachetnych wynika z zanieczyszczeń spowodowanych jonami zanieczyszczeń, takimi jak rubiny, szafiry, szmaragdy, jadeit i agat. W oparciu o przyczyny koloru kamieni szlachetnych, podczas ulepszania, zawartość i stan walencyjny niektórych jonów zanieczyszczeń powodujących kolor można zmienić, aby zmienić lub poprawić kolor kamienia szlachetnego, poprawiając w ten sposób jakość ulepszonego kamienia szlachetnego. Dlatego też badanie przyczyn koloru kamieni szlachetnych jest teoretyczną podstawą do ich ulepszania.
2. Fizyka koloru
(1) Kolor i fale świetlne
Fotony przenoszą energię światła, a gdy docierają do ludzkiego oka, wywołują wrażenie koloru. Kolor to percepcja światła przez oczy i układ nerwowy; reakcja generowana przez sygnały powstające na siatkówce oka stymuluje korę mózgową. Postrzeganie kolorów składa się z trzech głównych elementów: źródła światła, obiektu i ludzkiego oka. Zmiana jednego lub więcej z tych trzech elementów zmieni postrzeganie koloru. Klejnoty oddziałują ze światłem, a zjawiska takie jak odbicie, załamanie, transmisja, interferencja i dyfrakcja zachodzące na powierzchni klejnotu skutkują różnymi kolorami.
Zakres energii widma promieniowania elektromagnetycznego jest dość duży, od bardzo długich fotonów fal radiowych do bardzo krótkich fotonów promieniowania, z zakresem energii od mniej niż jednej miliardowej elektronowolta do ponad stu milionów elektronowoltów.
Światło widzialne, które ludzkie oko może zaakceptować i postrzegać, jest bardzo małą częścią widma elektromagnetycznego, o zakresie długości fali 400-700nm i energii około 1,7-3,1eV. Jeśli warunki obserwacji są wystarczająco dobre, zakres ten można rozszerzyć do 380-760nm (Rysunek 3-1). Światło widzialne obejmuje kolory, które widzimy, a mianowicie czerwony, pomarańczowy, żółty, zielony, cyjan, niebieski, fioletowy i różne inne kolory. Różne długości fal światła widzialnego wytwarzają różne kolory; kolor światła widzialnego o najdłuższej długości fali i najniższej energii to czerwony, o zakresie długości fali 647-760nm; światło widzialne o najkrótszej długości fali i najwyższej energii to fioletowy, o zakresie długości fali 400-425nm. Inne kolory światła widzialnego mieszczą się w zakresie od 425 do 647nm. Długości fal różnych kolorów światła widzialnego i ich kolorów uzupełniających przedstawiono w tabeli 3-1.
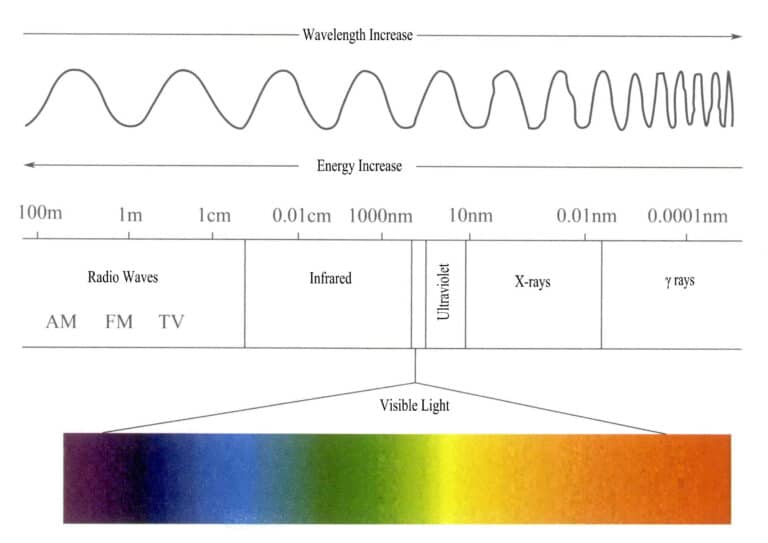
Tabela 3-1 Długości fal różnych kolorów światła widzialnego i ich kolorów dopełniających
| Długość fali/nm | Kolor widmowy | Uzupełniające |
|---|---|---|
| 400 ~ 425 | Fioletowy | Żółto-zielony |
| 425 ~ 455 | Niebieski | Żółty |
| 455 ~ 490 | Zielono-niebieski | Pomarańczowy |
| 490 ~ 500 | Niebiesko-zielony | Czerwony |
| 500 ~ 560 | Zielony | Magenta |
| 560 ~ 580 | Żółto-zielony | Fioletowy |
| 580 ~ 595 | Żółty | Niebieski |
| 595 ~ 647 | Pomarańczowy | Zielono-niebieski (cyjan) |
| 647 ~ 760 | Czerwony | Zielony |
Istotą koloru obiektu jest wynik selektywnej absorpcji przez obiekt różnych długości fal światła widzialnego. Istotą selektywnej absorpcji przez obiekt różnych długości fal światła widzialnego jest absorpcja fotonów światła widzialnego o różnych energiach. Gdy naturalne światło pada na kamień szlachetny, pochłania on część światła, a część przepuszcza. Kolor prezentowany przez kamień szlachetny jest kolorem komplementarnym pochłoniętego światła, zgodnym z kolorem przepuszczanego światła (rysunek 3-2). Na przykład w przypadku rubinu, gdy białe światło przechodzi przez rubin, jony chromu zawarte w rubinie zyskują energię, pochłaniając wszystkie fioletowe i zielone fotony, a także większość niebieskich fotonów, podczas gdy inne kolorowe fotony, głównie czerwone, przechodzą przez rubin, powodując, że kamień szlachetny wydaje się czerwony.
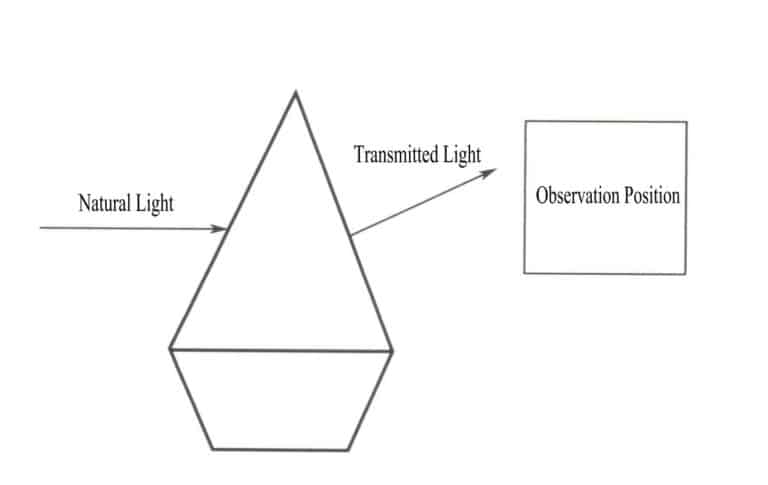
Pojedyncza długość fali światła nie generuje koloru tworzonego przez obiekt; promieniowanie obiektu jest raczej mieszaniną fotonów o różnych energiach, gdzie pasmo energii o największej proporcji określa kolor obiektu. Jednolita mieszanina różnych kolorów światła tworzy światło białe. Generowanie kolorów kamieni szlachetnych wynika z selektywnej absorpcji fotonów o różnych długościach fal światła widzialnego. Gdy białe światło przechodzi przez kamień szlachetny, światło pochłaniane i przepuszczane przez kamień szlachetny jest mieszaniną, a kolor prezentowany przez kamień szlachetny zależy od tego, który ma największy udział w przepuszczanym świetle. Na przykład w przypadku rubinu, gdy białe światło świeci na rubin, światło, które przechodzi, jest głównie czerwone z niewielką ilością niebiesko-fioletowego. Dlatego rubiny często wydają się czerwone z niebiesko-fioletowym odcieniem.
(2) Rodzaje i właściwości źródeł światła
Kolor kamieni szlachetnych cechuje się pewną subiektywnością, która jest związana z otoczeniem obserwatora i na którą największy wpływ ma źródło światła. Obserwacja koloru kamieni szlachetnych w różnych źródłach światła może wykazać różnice; na przykład aleksandryt wydaje się zielony w świetle słonecznym, ale czerwony w świetle żarowym. Ogólnie rzecz biorąc, ludzie uważają kolor widziany w naturalnym świetle słonecznym za standard, powszechnie określany jako białe światło.
Początkowe operacje na rynku kamieni szlachetnych były prowadzone w określonych godzinach, aby uzyskać stosunkowo dokładny kolor kamieni szlachetnych. Na przykład sklepy z kamieniami szlachetnymi w Ratnapura na Sri Lance działały przez wiele lat od 10 rano do 12 po południu, ponieważ źródło światła w tym czasie jest najbardziej zbliżone do światła białego. Światło słoneczne i dzienne nie są izotropowymi źródłami światła, a względne różnice we względnych ilościach promieniowania o różnych długościach fal między różnymi źródłami światła mogą być bardzo duże ze względu na różne warunki obserwacji. Rysunek 3-3 przedstawia krzywe rozkładu energii pięciu popularnych źródeł światła, a różnice energii między tymi źródłami światła są bardzo duże.
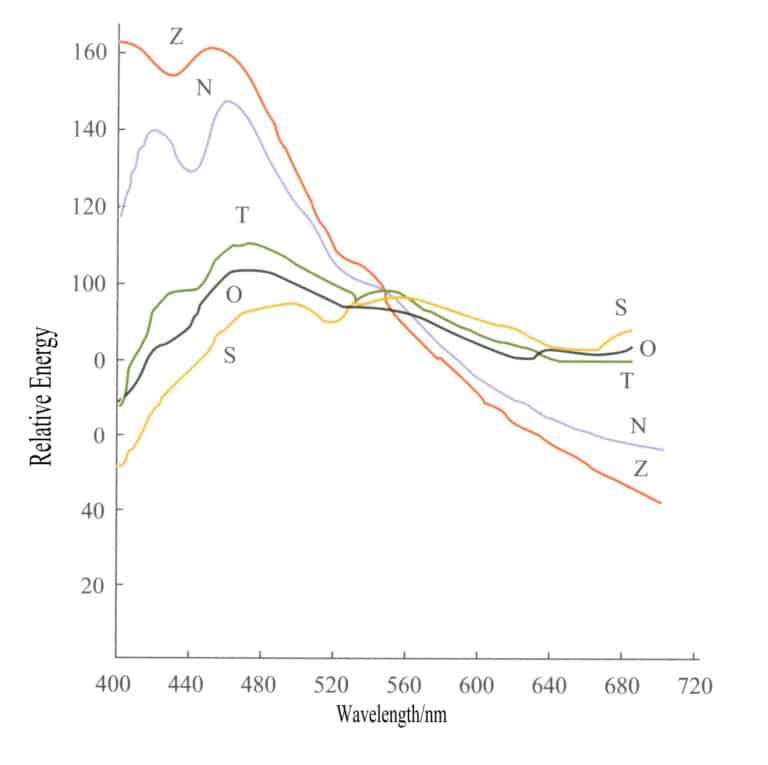
S - Bezpośrednie światło słoneczne; O - Oświetlenie pochmurnego nieba na płaszczyźnie poziomej; T - Oświetlenie światła słonecznego i czystego nieba na płaszczyźnie poziomej; N - Światło z czystego północnego nieba; Z - Światło zenitu;
Charakterystyka kolorystyczna bezpośredniego światła słonecznego jest często wyrażana za pomocą temperatury barwowej (mierzonej w K). Ta sama temperatura barwowa oznacza podobne kolory źródeł światła. Obecnie uznawane temperatury barwowe światła dziennego to D6500K, D5500K i D7500K. Trzy lampy są międzynarodowo określane jako standardowe źródła światła do pomiarów kolorów. SA reprezentuje średnie sztuczne oświetlenie żarowej lampy wolframowej o temperaturze barwowej 2854 K;SB reprezentuje przeciętne światło słoneczne o temperaturze barwowej 4900 K; SC reprezentuje średnie światło dzienne o temperaturze barwowej 6700K. W testach klejnotów źródło światła Sc jest używane jako standardowe źródło światła.
(3) Wrażliwość na światło i efekty kolorystyczne
Obserwacja kolorów klejnotów jest subiektywna; oprócz obiektywnych warunków, kolor klejnotu jest również związany z percepcją zmysłową obserwatora. Przy tym samym źródle światła ludzkie oczy mają różną wrażliwość na różne kolory, a różni ludzie mają różną wrażliwość na kolory. Obserwacja koloru jest subiektywna; aby osiągnąć obiektywizm w jak największym stopniu, kolory muszą być scharakteryzowane i wyrażone stosunkowo obiektywnie.
Efekt fotorecepcji:
W normalnych warunkach zakres długości fal źródeł światła widzialnego, które może obserwować ludzkie oko, wynosi 400-700nm. Zakres czułości można rozszerzyć poprzez poprawę warunków obserwacji do 380-780nm. Ludzkie oko ma różną wrażliwość na fale świetlne o różnych długościach fal. W przypadku widzenia dziennego, oko jest najbardziej wrażliwe na zielone światło o długości fali 555nm, podczas gdy najbardziej wrażliwa długość fali dla widzenia zmierzchowego przesuwa się do 507nm. Światła drogowe są projektowane w oparciu o kolory, na które ludzkie oko jest najbardziej wrażliwe.
② Color Sensation:
Kolor to wrażenie wywoływane przez różne składowe widmowe energii promieniowania w zakresie światła widzialnego. Wzrok normalnej osoby może rozróżnić ponad 150 odcieni czystych kolorów widmowych. Mimo że między falami świetlnymi a kolorami istnieje relacja jeden-do-jednego, relacja między kolorami a falami świetlnymi nie jest pojedyncza; często jeden kolor światła może być utworzony przez połączenie dwóch lub więcej innych kolorów światła. Trzy podstawowe niezależne kolory to czerwony, zielony i niebieski, znane jako kolory podstawowe. Inne kolory są tworzone przez zmieszanie dwóch lub więcej kolorów podstawowych w różnych proporcjach, a ludzkie oko jest bardzo wrażliwe na kolory, zdolne do rozróżnienia wielu różnych kolorów.
3. Trzy elementy reprezentujące kolor
Kolor wynika z selektywnej absorpcji światła przez kamienie szlachetne, a różne kamienie szlachetne wykazują różne kolory. Aktualna teoria koloru sugeruje, że charakterystyka koloru zależy od jasności, odcienia i nasycenia (rysunek 3-4). Rodzaje kolorów kamieni szlachetnych można określić, opisując trzy elementy różnych kolorów.

(1) Jasność
Jasność to stopień jasności spowodowany działaniem światła na ludzkie oko, odnoszący się do stopnia jasnych i ciemnych kolorów i może być również nazywany luminancją. Jasność w dużej mierze zależy od postrzegania przez oko jasnych i ciemnych poziomów źródła światła i powierzchni obiektu, głównie określanych przez intensywność światła. Jasność zależy od poziomu oświetlenia obiektu i współczynnika odbicia powierzchni obiektu.
Jasność może być rozumiana jako jasność koloru; różne kolory mają różne poziomy jasności, a każdy kolor wykazuje różnice w jasności i ciemności. Jasność ma dwie cechy: ten sam obiekt może wykazywać zmiany jasności ze względu na różne oświetlenie, a różne kolorowe światła o tej samej intensywności mogą również mieć różne poziomy jasności.
W przypadku braku koloru, kolorem o najwyższej jasności jest biały, a kolorem o najniższej jasności jest czarny, ze skalą szarości pomiędzy jasnym i ciemnym. W kolorze każdy stopień czystości ma swoją charakterystykę jasności. Na przykład żółty ma najwyższą jasność, a fioletowy najniższą. Zielony, czerwony, niebieski i pomarańczowy mają podobne poziomy jasności, reprezentując średnią jasność. Dodatkowo, w ramach tego samego odcienia, istnieją różnice w jasności od jasnego do ciemnego, takie jak jasnozielony, bladozielony i szmaragdowozielony w zielonym spektrum.
(2) Hue
Barwa odnosi się do różnic między różnymi kolorami i jest najbardziej widoczną cechą koloru. Barwa jest określana przez składowe widmowe światła, które przechodzą przez obiekt i docierają do ludzkiego oka po padnięciu na niego, w zależności od długości fali przepuszczanego światła. Odcień obiektu zależy od widma padającego źródła światła oraz światła odbitego lub przepuszczonego przez sam obiekt.
Tak zwany odcień odnosi się do nazwy, która może dokładniej reprezentować określoną kategorię kolorów, taką jak różowoczerwony, pomarańczowo-żółty, cytrynowożółty, kobaltowy niebieski, fioletowo-czerwony, szmaragdowozielony itp. Z punktu widzenia optyki fizycznej, różne odcienie są określane przez składowe widmowe światła, które dociera do ludzkiego oka. W przypadku światła monochromatycznego rodzaje odcieni całkowicie zależą od długości fali tego światła; w przypadku światła o mieszanych kolorach zależy to od względnych ilości różnych długości fal światła. Kolor obiektu jest określany przez składowe widmowe źródła światła i charakterystykę światła odbijanego (lub transmitowanego) przez powierzchnię obiektu. Jest to związane z długością fali światła. Na przykład, kolor o dominującej długości fali 470nm nazywany jest niebieskim o długości fali 470nm, powszechnie postrzeganym jako niebieski szafirów.
(3) Nasycenie
Nasycenie koloru odnosi się do czystości i żywości koloru, wskazując proporcję składników chromatycznych zawartych w kolorze. Im większa proporcja składników chromatycznych, tym wyższa czystość koloru; im mniejsza proporcja składników chromatycznych, tym niższa czystość koloru. Nasycenie zmienia się, gdy kolor jest mieszany z czernią, bielą lub innymi kolorami. Gdy proporcja zmieszanego koloru osiągnie znaczący poziom, oryginalny kolor straci swój pierwotny blask dla oka, a widziany kolor stanie się kolorem zmieszanego koloru. Oczywiście nie oznacza to, że oryginalny kolor już nie istnieje, ale raczej, że oryginalny kolor został zasymilowany z powodu wielu innych zmieszanych kolorów, co czyni go niezauważalnym dla ludzkiego oka.
Światła monochromatyczne w widmie widzialnym mają najwyższe nasycenie i są najbardziej żywe. Światło monochromatyczne jest zwykle uważane za 100/100 = 1, a wraz z blaknięciem koloru wartość ta stopniowo maleje, a czysta biel ma zerowe nasycenie. Biorąc za przykład czysty niebieski atrament, nasycenie czystego niebieskiego atramentu wynosi 1, a gdy stopniowo rozcieńcza się do całkowicie bezbarwnego, nasycenie staje się zerowe.
4. Pomiar koloru kamienia szlachetnego
System, który ilościowo reprezentuje kolor, nazywany jest systemem kolorów. Istnieją dwa powszechnie stosowane rodzaje systemów kolorów: jeden to system kolorów oparty na standardowych próbkach kolorów do porównania, a drugi to zestaw standardowych systemów kolorów mierzonych za pomocą nowoczesnych przyrządów do pomiaru kolorów.
(1) System kolorów standardowych próbek kolorów
Ten system kolorów składa się z różnych "kart kolorów" wykonanych z papieru, które są standardowymi próbkami kolorów zebranymi w książce. Są one porównywane z próbkami kamieni szlachetnych, aby wybrać "kartę kolorów", która pasuje do koloru kamienia szlachetnego.
① System kolorów Munsell
System kolorów Munsell jest jednym z najwcześniejszych i najbardziej klasycznych systemów reprezentacji kolorów. Jest on nadal używany przez niektóre organizacje. Został on opracowany w 1905 roku przez amerykańskiego pedagoga i teoretyka kolorów Alberta Munsella, a jego nazwa pochodzi bezpośrednio od jego nazwiska. Jest to sposób przedstawiania kolorów za pomocą modelu kolor-stała. "Munsell Color Atlas", opublikowany przez Optical Society of America (OSA), zawiera wersje błyszczące i matowe.
Wersja błyszcząca zawiera 1450 próbek kolorów wraz z zestawem 37 próbek achromatycznych; wersja matowa zawiera 1150 próbek kolorów i 32 próbki achromatyczne.
W atlasie Munsell każdy kolor jest reprezentowany przez zestaw symboli. Symbole zapewniają jednakowo odległe wskaźniki dla trzech elementów reprezentacji koloru: barwy, wartości i chromy, reprezentowanych jako HV/C = barwa/wartość/chroma.
Odcienie są podzielone na pięć tonów podstawowych: czerwony (R), żółto-czerwony (YR), żółty (Y), zielono-żółty (GY), zielony (G), niebiesko-zielony (BG), niebieski (B), fioletowo-niebieski (PB), fioletowy (P) i czerwono-fioletowy (RP), wraz z pięcioma tonami pośrednimi. Każdy ton jest dalej podzielony na dziesięć poziomów (od 1 do 10), przy czym piąty poziom jest kolorem pośrednim tego tonu (rysunek 3-5).
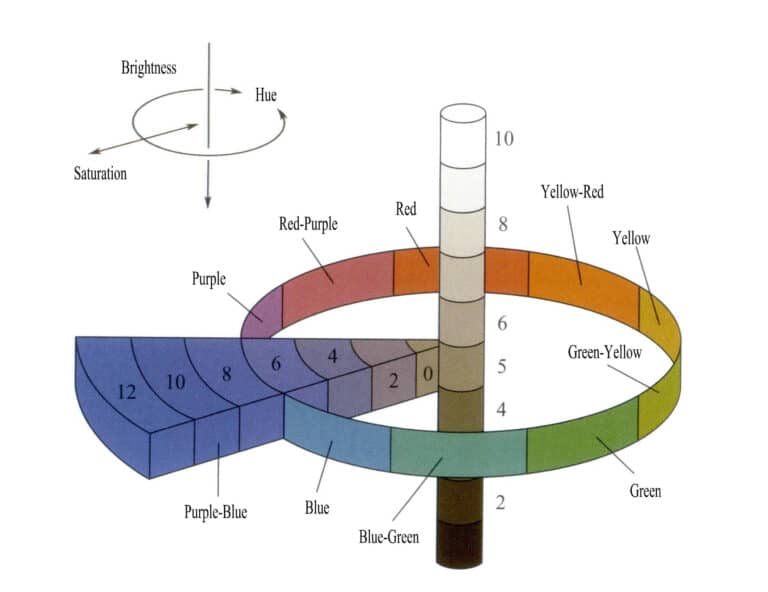
Wartość jest podzielona na 11 poziomów, przy czym wyższe wartości oznaczają większą jasność; minimalna wartość to 0 (czarny), a maksymalna to 10 (biały). Chroma jest podzielona na 12 poziomów. Cały atlas kolorów zawiera 40 rodzajów próbek odcieni. Na przykład 5GY 8/7 reprezentuje żółto-zielony o wartości 8 i nasyceniu 7. Konwencja nazewnictwa dla serii niekolorowych (czarny, biały, szary) to NV/= neutralna wartość jasności; na przykład kolor oznaczony N5/ oznacza szary o wartości jasności 5.
② System kolorów DIN 6164
Niemiecki podręcznik DIN 6164 jest również ważnym systemem kolorów. Wielu gemmologów w Europie i Wielkiej Brytanii używa tego systemu. Ten system kolorów został opracowany na podstawie systemu Munsell.
Karta kolorów DIN 6164 zawiera 24 kolory, z tyłu każdego koloru oznaczonego odpowiednią notacją kolorów Munsell. Reprezentacja jest w formacie odcień: nasycenie: jasność. Na przykład 6:6:2 oznacza odcień 6 (czerwony), nasycenie 6 (żywy) i jasność 2 (jasny) standardowej karty kolorów.
③ System kolorów ISCC-NBS
ISCC (Inter-Society Colour Council) została założona w 1931 roku jako krajowe stowarzyszenie kolorów w Stanach Zjednoczonych, a jej system kolorów ma na celu opracowanie systemu nazewnictwa kolorów. Gromadzi 18 odcieni na tych samych pozycjach odcienia i jasności w Munsell i DIN 6164.
ISCC-NBS (National Bureau of Standards) ma bardzo niewiele próbek kolorów w systemie American National Standard, ale zebrał kilka nietypowych próbek. Strukturalnie różni się on również od systemu Munsell, ponieważ kolory nie są ułożone zgodnie z percepcyjnymi metrykami równych odległości. Najważniejszym wkładem systemu ISCC-NBS w naukę o kolorach jest to, że definiuje on nazwy kolorów.
④ Standard kolorów OSA
OSA (Optical Society of America) przygotowało praktyczny zestaw kart kolorów z połyskiem akrylowym, obejmujący 558 kolorów, z których 424 kolory tworzą zestaw znany jako standard kolorów OSA. Wadą standardu kolorów OSA jest to, że karty kolorów są wykonane z papieru lub plastiku, który różni się fakturą od kamieni szlachetnych, a połysk powierzchni kart kolorów różni się od światła odbijanego przez fasetowane kamienie szlachetne, co wymaga ostrożnego użytkowania. Ze względu na blaknięcie, czas użytkowania większości kart kolorów wynosi od 4 do 5 lat.
(2) Współrzędne chromatyczne i wykres chromatyczny
① System przestrzeni barw CIE-XYZ z 1931 r.
Ten system przestrzeni kolorów jest oparty na systemie RGB i wykorzystuje metody matematyczne do wyboru trzech idealnych kolorów podstawowych, które zastępują rzeczywiste kolory podstawowe. Używając wirtualnych kolorów podstawowych jako osi, wyświetla różne długości fal światła widzialnego. Wartości kolorów podstawowych nazywane są wartościami tristimulus. System ten wymaga, aby wartości tristimulus nie były ujemne, a y równało się strumieniowi świetlnemu. Używając x jako osi poziomej i y jako osi pionowej, tworzy współrzędne chromatyczne, rzutując wartości współrzędnych chromatycznych każdego światła monochromatycznego w celu uzyskania wykresu chromatycznego. Rysunek 3-6 to standardowy diagram chromatyczny systemu (XYZ) ustanowiony na szczeblu międzynarodowym w 1931 roku.
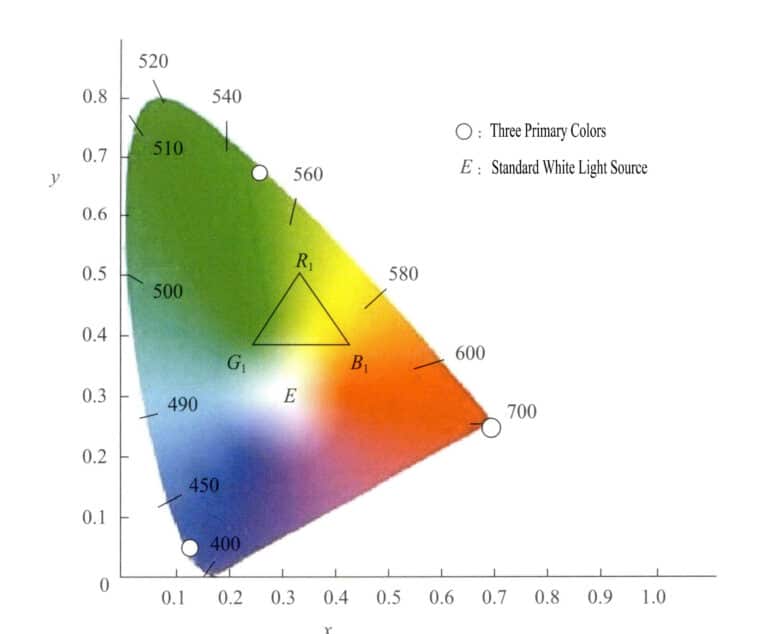
Wykres chromatyczny ma następującą charakterystykę:
- Wartości trójbodźców kolorów podstawowych tego systemu są wirtualne.
- Wszystkie punkty reprezentujące kolory widmowe znajdują się na krzywej w kształcie języka zwanej kolorem widmowym. Łącząc końce krzywej liniami prostymi, wszystkie rzeczywiste kolory są zawarte w obszarze otoczonym krzywą w kształcie języka i liniami prostymi.
- Wartość współrzędnych punktu E przy x=0,333, y=0,333 reprezentuje teoretyczną biel. Różne źródła światła białego mają nieco inne składowe widmowe. Powszechnie stosowane światło białe jest podzielone na SA, SB, SC, SEi tak dalej.
- Współrzędne chromatyczne kolorów mają tym większe nasycenie, im bliżej trajektorii koloru widmowego się znajdują. Punkty na trajektorii koloru widmowego mają najwyższe nasycenie; biały punkt ma najniższe nasycenie. Linia narysowana od białego punktu do współrzędnych chromatycznych koloru, przedłużona do przecięcia trajektorii koloru widmowego, ma punkty wzdłuż tej linii, które mają ten sam odcień.
- Do uzyskania koloru złożonego z dwóch dowolnych kolorów można użyć metody graficznej. Wprowadzając współrzędne chromatyczne dwóch kolorów do diagramu chromatycznego, kolor złożony musi leżeć na linii łączącej dwa punkty współrzędnych koloru. Odległość rzutowana na dwa punkty kolorów jest związana z intensywnością dwóch kolorów, określoną przez prawo rozkładu centroidów.
- Punkty na linii prostej między punktami końcowymi krzywej koloru widmowego nie reprezentują kolorów widmowych, ale raczej różne kolory mieszane uzyskane przez zmieszanie fioletu przy 380nm i czerwieni przy 780nm w różnych proporcjach.
- Wybierz dowolne trzy punkty na trajektorii kolorów widma, aby utworzyć kolor. Na przykład, jeśli wybierzesz R1, G1, B1 jako trzy kolory do dopasowania, wówczas wszystkie różne kolory utworzone przez te trzy odcienie są zawarte w trójkącie o wierzchołkach w trzech punktach R1, G1, B1.
② Reprezentacja dominującej długości fali i nasycenia
Na diagramie chromatycznym kolory mogą być reprezentowane nie tylko przez współrzędne chromatyczne (x, y). Inną metodą zaproponowaną przez Helmholtza jest przedstawienie ich za pomocą dominującej długości fali λd i nasycenie (czystość bodźca) Pe. λd i Pe są konkretnymi wartościami wyprowadzonymi ze współrzędnych chromatycznych na diagramie (Rysunek 3-7). Dominująca długość fali z grubsza reprezentuje wrażenie koloru postrzegane przez ludzkie oko.
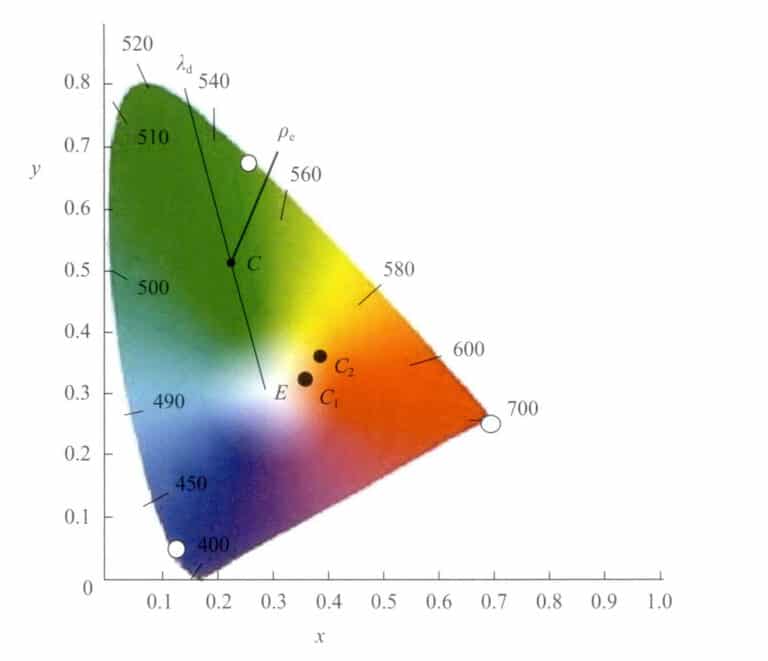
Niech położeniem tego punktu na diagramie chromatycznym będzie c(x, y). Połącz punkt c z białym E i przedłuż go tak, aby przecinał trajektorię widma w punkcie λd . Następnie liczba długości fali punktu λd na trajektorii widma jest dominującą długością fali tego kolorowego światła.
Punkt C leży na prostej łączącej punkty W i λd reprezentujący nasycenie tego koloru. Punkt W to czysta biel (E) lub określone źródło światła białego. Gdy współrzędne chromatyczne określonego koloru stopniowo przesuwają się w kierunku trajektorii widmowej od białego punktu W, nasycenie koloru stopniowo wzrasta, aż osiągnie trajektorię widmową, przy maksymalnym nasyceniu 1.
Kolory są reprezentowane przy użyciu dominującej długości fali i nasycenia, co ułatwia porównywanie różnic kolorów. Niewielkie różnice kolorów, reprezentowane przez zmiany liczbowe w λd i ρemożna wyświetlić.
Dla dwóch kolorów, C1, C2Współrzędne chromatyczne, dominującą długość fali i nasycenie przy tym samym oświetleniu przedstawiono w tabeli 3-2. Można zauważyć, że dominująca długość fali koloru C1, C2 różni się o 0,052 nm, a nasycenie różni się o 7%.
Tabela 3-2 Porównanie danych kolorów pomiędzy C1 i C2
| Punkt projekcji kolorów | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. Przyrządy do pomiaru koloru kamieni szlachetnych
(1) Spektrofotometr
Zasada działania: Ponieważ widmowy rozkład energii standardowego źródła światła wewnątrz urządzenia jest znany, wartości tristimulus obiektu można uzyskać poprzez pomiar jego widmowego współczynnika odbicia.
(2) Kolorymetr wartości tristimulusowej
Jest to fotoelektryczny instrument integracyjny, który bezpośrednio mierzy trzy wartości bodźca koloru obiektu. Symuluje on głównie trzy reakcje standardowego obserwatora na kolor poprzez odpowiednią kombinację filtrów i konwerterów fotoelektrycznych.
Obecnie ocena koloru kamieni szlachetnych opiera się głównie na obserwacji ludzkiego oka. Na przykład na szmaragdy, rubiny i diamenty mają wpływ czynniki środowiskowe, co prowadzi do niskiej dokładności pomiarów przyrządem; dlatego też zastosowanie pomiaru koloru przyrządem w identyfikacji kamieni szlachetnych jest stosunkowo rzadkie.
Sekcja II Teoretyczne pochodzenie kolorów mineralnych kamieni szlachetnych
Minerały kamienne występują w różnych kolorach, ale przyczyny ich zabarwienia również się różnią. Zgodnie z klasyczną teorią mineralogii, pochodzenie koloru minerału kamienia szlachetnego można podzielić na kolor idiochromatyczny, allochromatyczny i pseudokolor.
1. Klasyfikacja klasycznej mineralogii Teoria pochodzenia kolorów
Klasyczna teoria mineralogii jest najbardziej podstawową teorią do badania kolorów minerałów szlachetnych. W zależności od tego, czy kolor minerału wynika z samego minerału, można go podzielić na trzy kategorie: idiochromatyczny, allochromatyczny i pseudokolorowy.
(1) Kolor idiochromatyczny
Kolor klejnotu jest tworzony przez nieodłączne składniki chemiczne minerału, z którego się składa, znanego jako kolor idiochromatyczny. Takie klejnoty nazywane są klejnotami w kolorze idiochromatycznym. Ich nieodłączne składniki powodują kolor wytwarzany przez klejnoty w kolorze idiochromatycznym; dlatego mają dobrą stabilność koloru i nie są łatwo zmieniane. Na przykład, skład chemiczny turkusu to CuAl6(PO4)4(OH)8-5H2O, a niebieski lub niebiesko-zielony kolor jest spowodowany przez Cu2+skład chemiczny azurytu to 2CuCO3 - Cu(OH)2i Cu2+ powoduje również jego niebieski kolor"; zieleń oliwinu jest wytwarzana przez jony żelaza w jego składzie chemicznym (Rysunek 3-8).

W naturalnych minerałach nie ma wielu rodzajów samokolorowych klejnotów, a głównymi odmianami są turkus, malachit, azuryt, oliwin, granat i rodochrozyt. Typowe kolory, pierwiastki barwiące i skład chemiczny samobarwiących się kamieni szlachetnych przedstawiono w tabeli 3-3.
Tabela 3-3 Typowe pierwiastki barwiące, skład chemiczny i kolory kolorowych kamieni szlachetnych
| Elementy do kolorowania | Nazwa kamienia szlachetnego | Skład chemiczny | Kolor |
|---|---|---|---|
| Żelazo | Olivine | (Mg, Fe)2 (SiO4) | Zielony |
| Almandine | Fe3Al2 (SiO4)3 | Czerwony | |
| Chrom | Uvarovite | Ca3Cr2 (SiO4)3 | Zielony |
| Cuprum | Malachit | Cu2Co3(OH)2 | Zielony |
| Chryzokola | (CuAl)2H2Si2O5(OH)4 - nH2O | Zielony - Niebieski | |
| Turkus | CUAl6(PO4)4(OH)8.5H2O | Niebieski - Zielony | |
| Azuryt | 2CuCO3 - Cu(OH)2 | Niebieski | |
| Mangan | Spessartine-Garnet | Mn3Al2(SiO4)3 | Pomarańczowy |
| Rodochrozyt | MnCO3 | Różowy - Czerwony | |
| Rodonit | (Mn, Ca, Fe) - 5(Si5O15) | Różowy - Czerwony |
Copywrite @ Sobling.Jewelry - Producent biżuterii na zamówienie, fabryka biżuterii OEM i ODM
Niektóre kolorowe kamienie szlachetne mogą zmieniać kolor w określonych warunkach. Na przykład turkus i malachit mogą zmienić kolor pod wpływem wysokich temperatur z powodu parowania cząsteczek wody w ich składzie; rodochrozyt, węglanowy kamień szlachetny, może ulec rozkładowi, gdy napotka kwasy (takie jak kwas solny lub kwas siarkowy), a jego kolor również odpowiednio się zmieni.
(2) Allochromatyczny-kolorred
Kolor kamienia szlachetnego jest spowodowany śladowymi lub niewielkimi zanieczyszczeniami poza nieodłącznym składem chemicznym minerałów składowych, znanym jako kolor allochromatyczny. Takie kamienie szlachetne są określane jako kamienie szlachetne o barwie allochromatycznej.
W minerałach kamieni szlachetnych istnieje wiele odmian kamieni szlachetnych o różnych kolorach. Gdy nie ma zanieczyszczeń w składzie chemicznym kamienia szlachetnego, jest on bezbarwny i przezroczysty; gdy zawiera różne zanieczyszczenia elementów barwiących, może wytwarzać różne kolory.
Gdy czysty korund jest bezbarwny, staje się rubinem, gdy zawiera niewielką ilość jonów chromu; gdy zawiera niewielką ilość żelaza i tytanu, zamienia się w niebieskie lub zielone kamienie szlachetne. Podobne kamienie szlachetne obejmują szmaragd, spinel, turmalin, jadeit, chalcedon, nefryt itp. Typowe pierwiastki barwiące, skład chemiczny i kamienie szlachetne o barwie allochromatycznej przedstawiono w tabeli 3-4.
Tabela 3-4 Typowe pierwiastki barwiące, skład chemiczny i kamienie szlachetne o barwie allochromatycznej
| Elementy do kolorowania | Nazwa kamienia szlachetnego | Skład chemiczny | Kolor |
|---|---|---|---|
| Chrom | Ruby | Al2O3 | Czerwony |
| Szmaragd | Być3Al2(Si6O18) | Zielony | |
| Aleksandryt | BeAl2O4 | Czerwono-zielony | |
| Spinel | MgAl2O4 | Czerwony | |
| Chalcedon | SiO2 | Zielony | |
| Żelazo | Akwamaryn | Być3Al2Si6O18 | Niebieski |
| Turmalin | (Na, K, Ca) (Al, Fe3+, Cr)6(BO3)3Si6O18(OH)4 | Zielono-brązowy | |
| Spinel | MgAl2O4 | Żółty | |
| Nefryt | Ca2(Mg, Fe2+) 5 (Si4O11) 2 (OH)2 | Zielony | |
| Wanad | Tanzanit | Ca2Al3(SiO4)3(OH) | Fioletowo-niebieski |
| Zielony beryl | Być3Al2Si6O18 | Zielony | |
| Tytan | Benitoit | BaTiSi3O9 | Niebieski |
| Szafir | Al2O3 | Niebieski | |
| Mangan | Czerwony beryl | Być3Al2Si6O18 | Czerwony |
| Rodochrozyt | MnCO3 | Różowy | |
| Kobalt | Spinel naturalny | MgAl2O4 | Niebieski |
| Syntetyczny spinel | MgAl2O4 | Niebieski | |
| Nikiel | Zielony chalcedon | SiO2 | Zielony |
(3) Pseudo-kolorred
Kolory wytwarzane przez pseudokolory nie są związane ze składem chemicznym minerałów kamieni szlachetnych. Są one jednak spowodowane zmianami strukturalnymi i składowymi wynikającymi z mieszanek mechanicznych lub tworzenia się minerałów. Pseudokolory nie są kolorami samych minerałów, ale raczej kolorami spowodowanymi specjalnymi strukturami utworzonymi przez wpływy zewnętrzne. Na przykład piękne kolory interferencyjne powstałe w wyniku interferencji światła odbitego i padającego, takie jak efekt fluorescencji labradorytu i efekt gry kolorów opalu. Zabarwienie spowodowane inkluzjami również zalicza się do pseudokolorów, takich jak czarne diamenty, ze względu na wiele czarnych, nieprzezroczystych grafitowych inkluzji w diamencie.
2. Jony powodujące kolor w minerałach szlachetnych
Pierwiastki chemiczne, które wytwarzają kolory klejnotów, mogą być głównymi lub drugorzędnymi składnikami. Pierwiastki metali przejściowych, w szczególności metale przejściowe czwartego okresu: tytan, wanad, chrom, mangan, żelazo, kobalt, nikiel i miedź, są często określane jako chromofory lub jony barwiące. Te osiem pierwiastków zajmuje kolejne pozycje w układzie okresowym, z liczbami atomowymi od 22 (Ti) do 29 (Cu). Podstawowe właściwości tych pierwiastków przedstawiono w tabeli 3-5.
Tabela 3-5 Podstawowe właściwości ośmiu elementów przejściowych
| Nazwa elementu | Tytan | Wanad | Chrom | Mangan | Żelazo | Kobalt | Nikiel | Miedź |
|---|---|---|---|---|---|---|---|---|
| Symbol elementu | Ti | V | Cr | Mn | Fe | Co | Ni | Cu |
| Liczba atomowa | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| Główne stopnie utlenienia | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| Konfiguracja elektronów walencyjnych | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
Te osiem pierwiastków metali przejściowych ma następujące właściwości:
① Elektrony walencyjne są zapełniane na orbitalach d przedostatniej powłoki w kolejności, a ogólny wzór na konfigurację elektronów walencyjnych atomów pierwiastków przejściowych to (n-1)d1-10nS1-2, więc elementy te są również nazywane elementami bloku d.
② W metalach przejściowych, ponieważ orbitale d przedostatniej powłoki są połączone z najbardziej zewnętrznymi orbitalami s, a orbitale d nie osiągnęły jeszcze stabilnej struktury, zarówno elektrony s, jak i elektrony d mogą częściowo lub całkowicie uczestniczyć w wiązaniu, co skutkuje szeregiem zmiennych stopni utlenienia dla metali przejściowych, przy czym różne tlenki mają różne kolory w kamieniach szlachetnych.
③ Jony generalnie wykazują kolor, ponieważ na orbitalach d znajdują się niesparowane pojedyncze elektrony, a poziomy energetyczne tych elektronów w stanie wzbudzonym i podstawowym są stosunkowo bliskie, co pozwala na wzbudzenie ich energią światła widzialnego. Różne warunki wzbudzenia mogą również powodować, że kamienie szlachetne wykazują różne kolory.
Jeśli wszystkie elektrony spinowe w jonie są sparowane, jak w przypadku jonów o konfiguracji elektronów walencyjnych d0, d10, d10s2elektrony są w stanie stabilnym i nie są łatwo wzbudzane, co powoduje, że jon nie ma koloru; zatem C+, Cr6+ a inne nie mają koloru i nie mogą wytwarzać koloru w kamieniach szlachetnych.
Te osiem pierwiastków metali przejściowych stanowi formację barwną w typowych kamieniach szlachetnych o naturalnych kolorach. Różne chromofory wytwarzają różne kolory w różnych kamieniach szlachetnych, a ten sam chromofor może również wytwarzać różne kolory. Typowe naturalne kamienie szlachetne i chromofory przedstawiono w tabeli 3-6.
Tabela 3-6 Kolory prezentowane przez jony metali przejściowych w popularnych naturalnych kamieniach szlachetnych i ich odmianach
| Chromofor | Popularne kolory | Odmiany klejnotów |
|---|---|---|
| Jon tytanu (Ti) | Niebieski | Szafir, benitoit, topaz |
| Jon wanadu (V) | Zielony | Syntetyczny korund zmieniający kolor, Essonite, Emerald |
| Jon chromu (Cr) | Czerwony, Zielony | Rubin, korund, szmaragd, pirop, jadeit |
| Jon manganu (Mn) | Różowy, Czerwony | Spessartyn, rodolit, czerwony beryl |
| Jon żelaza (Fe) | Niebieski, zielony, żółty | Szafir, oliwin, akwamaryn, turmalin, spinel |
| Jon kobaltu (Co) | Niebieski | Syntetyczny spinel, staurolit w kolorze kobaltu |
| Jon niklu (Ni) | Zielony | Zielony chalcedon |
| Jon miedzi (Cu) | Niebieski, niebiesko-zielony | Malachit, turkus, azuryt |
Różne jony chromoforowe wytwarzają różne kolory w kamieniach szlachetnych, co skutkuje widmami absorpcji o różnych właściwościach. W przypadku popularnych jonów chromoforowych widma absorpcyjne mają typowe znaczenie identyfikacyjne.
(1) Widmo absorpcyjne jonów chromu
Widmo absorpcyjne jonów chromu charakteryzuje się głównie wieloma wąskimi liniami absorpcyjnymi w regionie czerwonym, z dwoma najsilniejszymi zlokalizowanymi w regionie głębokiej czerwieni i kolejnymi dwoma w regionie pomarańczowym. Żółto-zielony region ma szerokie pasmo absorpcji, a szerokość, położenie i intensywność są związane z głębokością koloru klejnotu. W regionie niebieskim może występować kilka wąskich pasm, podczas gdy region fioletowy jest w pełni pochłaniany. Jony chromu wytwarzają głównie czerwone i zielone kolory, które różnią się w różnych klejnotach, a widma absorpcji wykazują pewne różnice. Na przykład rubiny mają trzy linie absorpcyjne w regionie czerwonym, szerokie pasmo absorpcyjne w regionie żółto-zielonym, trzy linie absorpcyjne w regionie niebieskim i pełną absorpcję w regionie fioletowym; szmaragdy mają linie absorpcyjne w regionie czerwonym, słabe pasmo absorpcyjne w regionie pomarańczowo-żółtym, słabe linie absorpcyjne w regionie niebieskim i pełną absorpcję w regionie fioletowym; a aleksandryt ma linie absorpcyjne w regionie czerwonym, pasmo absorpcyjne w regionie żółto-zielonym, jedną linię absorpcyjną w regionie niebieskim i pełną absorpcję w regionie fioletowym. Widma absorpcyjne tych trzech kamieni szlachetnych pokazano na rysunku 3-9.

(2) Charakterystyka widma absorpcji jonów żelaza
Jony żelaza wytwarzają różne kolory w różnych kamieniach szlachetnych i mają silny efekt barwiący, ale spektrum absorpcji jonów żelaza jest bardzo zróżnicowane. Gdy kamień szlachetny jest zielony, wytwarza absorpcję w strefie czerwonej, a gdy jest czerwony, wytwarza funkcję absorpcji zdominowaną przez strefę niebieską, z główną charakterystyczną linią absorpcji zlokalizowaną w strefach zielonej i niebieskiej. Na przykład jony żelaza w oliwinie mają kolor oliwkowozielony, a widmo absorpcji wykazuje głównie trzy wąskie pasma absorpcji w obszarze niebieskim przy 453 nm, 473 nm i 493 nm; czerwony almandyn ma typowe widmo absorpcji żelaza, z trzema silnymi wąskimi pasmami absorpcji przy 504 nm, 520 nm i 573 nm w obszarze żółto-zielonym, powszechnie określanym w branży jako "okno żelaza". Dodatkowo występują słabe wąskie pasma absorpcji przy 423 nm, 460 nm, 610 nm i 680 ~ 690 nm; widmo absorpcji żółtego szafiru ma trzy wąskie pasma absorpcji w niebieskim regionie przy 450 nm, 460 nm, 470 nm (rysunek 3-10).
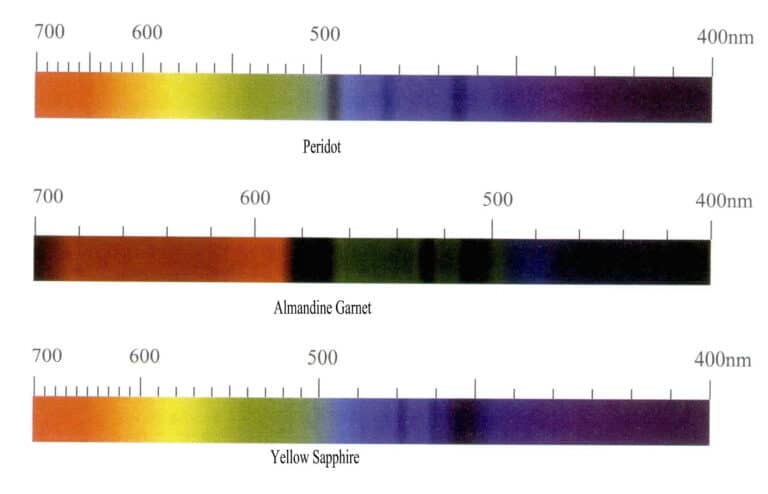
(3) Charakterystyka widma absorpcji jonów manganu
Jony manganu tworzą głównie różowy, pomarańczowy i czerwony kolor w kamieniach szlachetnych, a widmo absorpcji wykazuje przede wszystkim silną absorpcję w obszarze fioletowym, rozciągając się do obszaru ultrafioletowego i pewną absorpcję w obszarze niebieskim. Na przykład charakterystyka widma absorpcji różowego rodochrozytu ma trzy pasma absorpcji przy 410nm, 450nm, 540nm; linie widma absorpcji spessartinu mają głównie 410nm, 420nm, 430nm trzy pasma absorpcji i linie absorpcji przy 460nm, 480nm i 520nm. Czasami mogą występować dwie linie absorpcyjne 504nm, 573nm (Rysunek 3-11).

(4) Charakterystyka widma absorpcji jonów kobaltu
Jony kobaltu mają silny efekt barwiący, zwykle pojawiający się w jasnoniebieskim kolorze w kamieniach szlachetnych, przy czym widmo absorpcji wykazuje głównie trzy silne i szerokie pasma absorpcji w obszarze żółto-zielonym. Ze względu na niską obfitość kobaltu w skorupie ziemskiej, istnieje bardzo niewiele naturalnych kamieni szlachetnych zabarwionych jonami kobaltu. Widmo absorpcyjne jonów kobaltu wskazuje również na syntetyczne kamienie szlachetne, takie jak syntetyczny niebieski spinel i szkło kobaltowe. Syntetyczny niebieski spinel ma trzy silne pasma absorpcji w regionach żółto-zielonym i pomarańczowo-żółtym, przy czym pasmo absorpcji w regionie zielonym jest najwęższe; linie absorpcji szkła kobaltowego mają głównie trzy silne pasma absorpcji w regionach żółto-zielonym i pomarańczowo-żółtym, przy czym pasmo absorpcji w regionie żółtym jest najwęższe (rysunek 3-12).

3. Kolorowanie pierwiastków ziem rzadkich
Badania nad wpływem śladowych pierwiastków ziem rzadkich na kolor kamieni szlachetnych stają się coraz bardziej dogłębne. Kolory pierwiastków ziem rzadkich są bardziej żywe, a ich właściwości fizykochemiczne są również bardzo stabilne. Pierwiastki ziem rzadkich, takie jak apatyt i fluoryt, mogą również barwić naturalne kamienie szlachetne. Różne pierwiastki ziem rzadkich mogą być dodawane do syntetycznych i optymalnie przetworzonych kamieni szlachetnych w celu uzyskania różnych kolorowych kamieni szlachetnych, takich jak żółty z ceru i niebieski z neodymu.
Pierwiastki ziem rzadkich, które barwią kamienie szlachetne, to głównie lantanowce i aktynowce w układzie okresowym pierwiastków chemicznych, a kolory, które mogą wytwarzać, pokazano w tabeli 3-7.
Tabela 3-7 Pierwiastki ziem rzadkich i ich kolory w popularnych kamieniach szlachetnych
| Symbol elementu | La | Ce | Nd | Pr | Dy | Sm | Er | Tm | U |
|---|---|---|---|---|---|---|---|---|---|
| Imię i nazwisko | Lantan | Cer | Neodym | Praseodym | Dysproz | Samar | Erb | Thulium | Uran |
| Kolor | Bezbarwny | Żółty | Niebieski | Zielony | Jasnożółty | Jasnożółty | Różowy | Jasnozielony | Srebrno-biały |
Pierwiastki ziem rzadkich mają charakterystyczne widma absorpcyjne, często tworzące unikalne cienkie linie. Na przykład żółty apatyt często zawiera pierwiastek ziem rzadkich Ce, z charakterystycznymi cienkimi liniami absorpcji w żółtym obszarze. Jednak uran nie wytwarza jasnożółtego koloru; może generować wyraźne absorpcyjne linie widmowe. Na przykład, więcej niż dziesięć linii absorpcyjnych może pojawić się w zielonym cyrkonie w różnych strefach kolorystycznych (Rysunek 3-13).

Sekcja III Kolory wytwarzane przez defekty kryształów i centra kolorów
W naturze minerały dzielą się na kryształy i nie-kryształy w oparciu o różne stopnie krystalizacji. Większość kamieni szlachetnych, takich jak rubiny, szafiry, diamenty, szmaragdy i kwarc, to kryształy; niektóre organiczne kamienie szlachetne, takie jak bursztyn i koral, są niekrystaliczne. Struktury krystaliczne mają strukturę podobną do siatki, w której ich wewnętrzne cząsteczki (atomy, jony lub cząsteczki) są ułożone w regularny okresowy wzór w przestrzeni trójwymiarowej, a kryształy mogą spontanicznie tworzyć kształty wielościenne; nie-kryształy są ciałami amorficznymi o strukturach nie-siatkowych, które nie mogą tworzyć kształtów wielościennych, takich jak szkło, kalafonia i żywica.
Najbardziej typowym przykładem różnicy między kryształami a amorficznymi ciałami stałymi jest kwarc i szkło. Naturalny kwarc powstaje ze stopionego materiału SiO2 w magmie, która stygnie w zagłębieniach skorupy ziemskiej. Zewnętrzna warstwa zwykłych kul kwarcowych to agat, który nie wykazuje kształtu kryształu, podczas gdy wewnętrzna warstwa ma kształt kryształu kwarcu. Głównymi składnikami chemicznymi szkła i kwarcu są SiO2Kwarc jest kryształem z jonami krzemu i tlenu ułożonymi w uporządkowany sposób, podczas gdy szkło jest amorficznym ciałem stałym z jonami krzemu i tlenu ułożonymi chaotycznie, bez regularności, jak pokazano na rysunku 3-14.
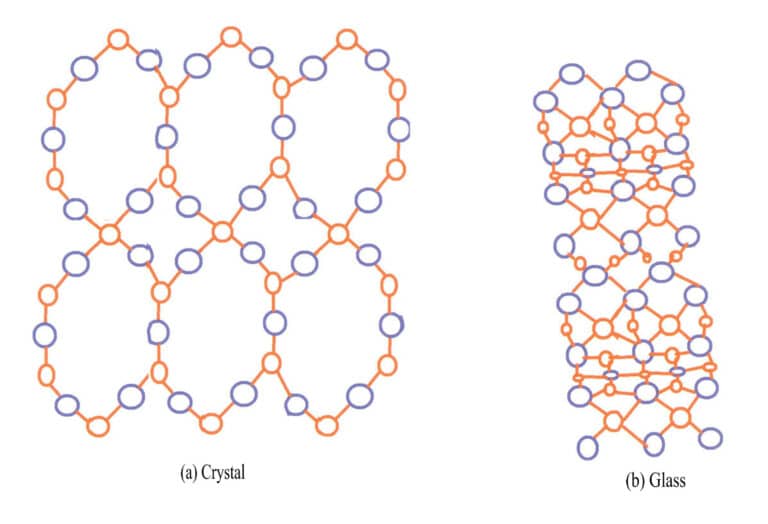
Większość kryształów kamieni szlachetnych jest zabarwiona z powodu jonów zanieczyszczeń, takich jak rubiny, szmaragdy i turmaliny. Niektóre kamienie szlachetne, mimo braku jonów chromoforowych, są zabarwione z powodu defektów w ich strukturze krystalicznej. Naturalne kamienie szlachetne produkowane w przyrodzie mogą zmieniać kolor z powodu warunków zewnętrznych, takich jak napromieniowanie i jonizacja, które zmieniają strukturę kryształu. Najczęstszym przykładem jest kwarc dymny, który uzyskuje kolor w wyniku tworzenia się centrów koloru z wakansów wywołanych promieniowaniem. Sztucznie napromieniowany kwarc dymny ma podobną zasadę formowania do naturalnego kwarcu dymnego, z tym wyjątkiem, że sztuczne promieniowanie szybko tworzy kolor.
1. Wady kryształów i ich rodzaje
Zjawisko, w którym rozmieszczenie cząstek odbiega od zasad struktury sieci (cząstki ulegają okresowym powtórzeniom translacyjnym w przestrzeni trójwymiarowej) w lokalnym zakresie struktury kryształu kamienia szlachetnego, nazywane jest defektem sieci. Przyczyny są związane z drganiami termicznymi cząstek w krysztale kamienia szlachetnego, naprężeniami zewnętrznymi, wysoką temperaturą i ciśnieniem, napromieniowaniem, dyfuzją, implantacją jonów i innymi warunkami.
Na przykład diamenty skrystalizowane w środowisku o wysokiej temperaturze i wysokim ciśnieniu górnego płaszcza, gdy są szybko przenoszone w pobliże powierzchni Ziemi przez magmę macierzystą (kimberlit lub lamproit), szybka zmiana warunków temperatury i ciśnienia oraz wzajemne zderzenia między kryształami a otaczającymi skałami mogą łatwo prowadzić do lokalnych zmian w strukturze natrętnych kryształów diamentu, powodując defekty sieci, które zmieniają kolor pierwotnie bezbarwnych diamentów, tworząc brązowo-żółte, brązowe i różowe diamenty.
Obecność defektów krystalicznych ma znaczący wpływ na właściwości kryształów. W rzeczywistości kryształy mają mniej lub więcej defektów. Umiarkowana ilość niektórych defektów punktowych może znacznie poprawić przewodnictwo materiałów półprzewodnikowych i luminescencję materiałów luminescencyjnych, odgrywając korzystną rolę. Z kolei defekty, takie jak dyslokacje, mogą sprawić, że materiały będą podatne na pękanie, zmniejszając wytrzymałość na rozciąganie kryształów prawie bez defektów sieci do ułamka ich wartości.
W idealnym krysztale atomy są ściśle ułożone w regularną, okresową sieć w określonych punktach w przestrzeni. Jednak podczas rzeczywistego wzrostu i formowania kryształów, ze względu na wpływ środowisk wzrostu, takich jak temperatura, ciśnienie i stężenie składników medium, morfologia kryształu po wzroście może czasami odbiegać od idealnej struktury kryształu. Każde odchylenie od idealnej struktury kryształu można nazwać defektem kryształu. Defekty krystaliczne znacząco wpływają na właściwości fizyczne i chemiczne kryształów, a wiele dyscyplin jest związanych z defektami krystalicznymi, takimi jak domieszkowanie jonowe w materiałoznawstwie. Kolor kamieni szlachetnych jest w dużej mierze związany z występującymi w nich defektami krystalicznymi. Jest to jedna z przyczyn koloru w centrach kolorów kamieni szlachetnych.
Istnieje wiele rodzajów defektów struktury krystalicznej, które można podzielić na cztery kategorie w oparciu o zakres ich rozmieszczenia w przestrzeni trójwymiarowej: defekty punktowe, defekty liniowe, defekty powierzchniowe i defekty objętościowe.
(1) Wady punktowe
Inne atomy zastępują niektóre atomy w idealnym krysztale, niektóre są domieszkowane lub powstają puste przestrzenie. Niektóre atomy w krysztale są zastępowane lub ich brakuje z powodu atomów zewnętrznych, a zmiany te zakłócają okresowy układ regularnej sieci krystalicznej, powodując zmiany w polu potencjalnym cząstek i powodując niekompletność struktury kryształu, ograniczoną do pewnych pozycji, wpływając tylko na kilka pobliskich atomów. Wpływ defektów punktowych na kryształ jest minimalny, a powszechne rodzaje defektów punktowych obejmują defekty położenia sieci, defekty składu i defekty ładunku (Rysunek 3-15).
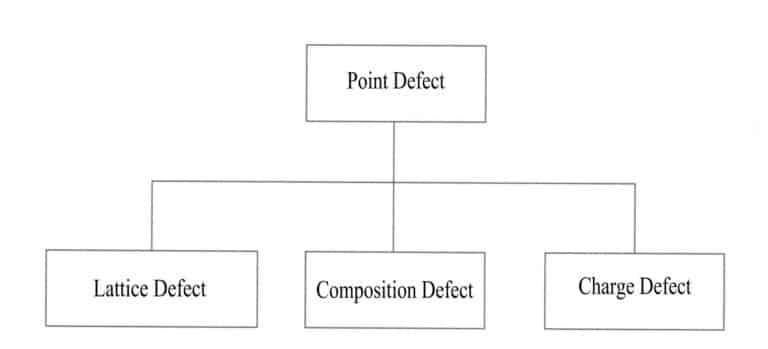
(2) Wady linii
Defekty liniowe są bardzo małe w dwóch kierunkach i rozciągają się głównie w innym kierunku. Znane są również jako defekty jednowymiarowe i składają się głównie z różnych dyslokacji. Dyslokacje mogą być postrzegane jako produkt lokalnego poślizgu sieci wzdłuż określonej płaszczyzny atomowej. Poślizg nie penetruje całej sieci; defekt kryształu kończy się wewnątrz sieci, powodując nieuporządkowany układ cząstek na granicy między poślizgniętymi i nie poślizgniętymi częściami sieci, znany jako dyslokacja. Granica ta, linia przecięcia między obszarami zsuniętymi i niezsuniętymi, nazywana jest linią dyslokacji. Istnieją dwa podstawowe rodzaje dyslokacji: gdy kryształ jest poddawany siłom ściskającym, płaszczyzna poślizgu cząstek tworzy linię dyslokacji z płaszczyzną nieślizgniętą, a linia dyslokacji jest prostopadła do kierunku poślizgu, zwana dyslokacją krawędziową, zwaną również dyslokacją klinową; z powodu naprężeń ścinających poślizg występuje między płaszczyznami, a przecinające się linie dyslokacji w poślizgniętej części kryształu są równoległe do kierunku poślizgu, zwane dyslokacją śrubową (Rysunek 3-16).
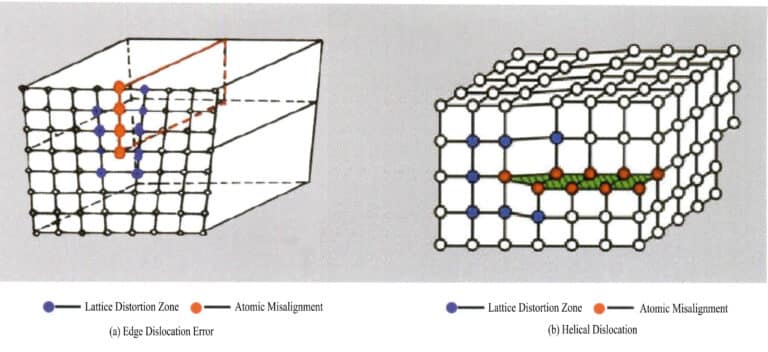
(3) Wady powierzchni
Najprostszym defektem powierzchniowym jest defekt stackingowy, podzielony na wewnętrzne defekty stackingowe (gdzie płaszczyzna kryształu jest usuwana) i zewnętrzne defekty stackingowe (gdzie warstwa atomowa jest wprowadzana do kryształu). Wady te występują w zakresie kilku odstępów atomowych po obu stronach określonej płaszczyzny wzdłuż sieci lub między ziarnami. Obejmują one głównie uskoki ułożenia i interfejsy wewnątrz i między kryształami, takie jak granice ziaren pod małym kątem, ściany domen oraz granice bliźniacze i międzyziarnowe.
(4) Wady objętościowe
Wady objętościowe odnoszą się do wad, które występują w różnym stopniu we wszystkich trzech kierunkach, które są wadami trójwymiarowymi, takimi jak osadzone pęknięcia, struktury siatkowe, struktury rodzinne, bliźniaki i różne wtrącenia kamieni szlachetnych.
2. Centra kolorów w kamieniach szlachetnych
Centra kolorów są szczególnym przypadkiem defektów sieci krystalicznej, ogólnie odnoszących się do defektów sieci krystalicznej w kamieniach szlachetnych, które mogą selektywnie absorbować energię światła widzialnego i wytwarzać kolor, należąc do najbardziej typowych typów kolorów strukturalnych. W niektórych przypadkach niesparowane elektrony, które wytwarzają kolor, mogą również pojawiać się w jonach pierwiastków nieprzejściowych lub w defektach krystalicznych powstałych z powodu braku elektronów, czym są centra kolorów. Defekty punktowe w kryształach jonowych mogą powodować absorpcję światła widzialnego, w wyniku czego pierwotnie przezroczyste kryształy wydają się kolorowe; tego typu defekty punktowe, które mogą absorbować światło widzialne, są zwykle określane jako centra kolorów. Wiele rodzajów naturalnych kamieni szlachetnych wytwarza kolor z centrów koloru, takich jak fioletowy fluoryt, dymny kryształ i zielone diamenty.
W procesie optymalizacji obróbki kamieni szlachetnych niektóre naturalne i sztuczne kamienie szlachetne mogą również mieć centra kolorów generowane przez promieniowanie, takie jak niebieskie, żółte, czerwone, zielone diamenty i niebieski topaz, które zmieniają kolor pod wpływem promieniowania, oraz niebieski topaz, wśród których niektóre kolory są stosunkowo stabilne i znikają dopiero po podgrzaniu; niektóre kolory są niestabilne i mogą blaknąć nawet w temperaturze pokojowej. Ten rodzaj centrum koloru powodującego kolor jest ściśle związany ze strukturą krystaliczną kamienia szlachetnego, takiego jak zielone diamenty, gdzie przyczyną koloru jest obecność wakatów w strukturze krystalicznej, ale ten defekt strukturalny można również usunąć przez napromieniowanie, zmieniając diament w bezbarwny. Typowe rodzaje centrów koloru w kamieniach szlachetnych to "centra koloru elektronów" i "centra koloru dziur".
(1) Centrum koloru elektronów (centrum F)
Centra kolorów elektronowych to centra kolorów powstające, gdy elektrony istnieją w pustych przestrzeniach defektów krystalicznych spowodowanych przez anionowe puste przestrzenie w strukturze krystalicznej kamienia szlachetnego. Gdy anion jest nieobecny, wakans staje się dodatnio naładowaną pułapką elektronową, która wychwytuje elektrony. Jeśli wakans przechwytuje elektron i wiąże go z tym wakansem, elektron zostaje wzbudzony i selektywnie pochłania określoną długość fali energii, aby stać się kolorowym. Dlatego centrum koloru elektronowego składa się z anionowego wakansu i elektronu związanego przez pole elektryczne tego wakansu.
Fioletowy fluoryt to kolor wytwarzany przez elektroniczne centra kolorów. Fluoryt (CaF2) należy do izometrycznego układu krystalicznego, w którym każdy Ca2+ podłączone do dwóch F– [Rysunek 3-17 (a)]. W niektórych przypadkach wartość F– we fluorycie może opuścić swoją normalną pozycję. W pierwotnym miejscu F– Aby utrzymać neutralność elektryczną kryształu, ujemnie naładowana jednostka musi zająć to wolne miejsce. Elektron z pewnego atomu w krysztale staje się ujemnie naładowaną jednostką zajmującą to wolne miejsce [Rysunek 3-17 (b)]. Tworzy to "centrum koloru", znane jako elektroniczne centrum koloru. We fluorycie elektronowe centra barwne absorbują światło widzialne, dając kolor fioletowy.
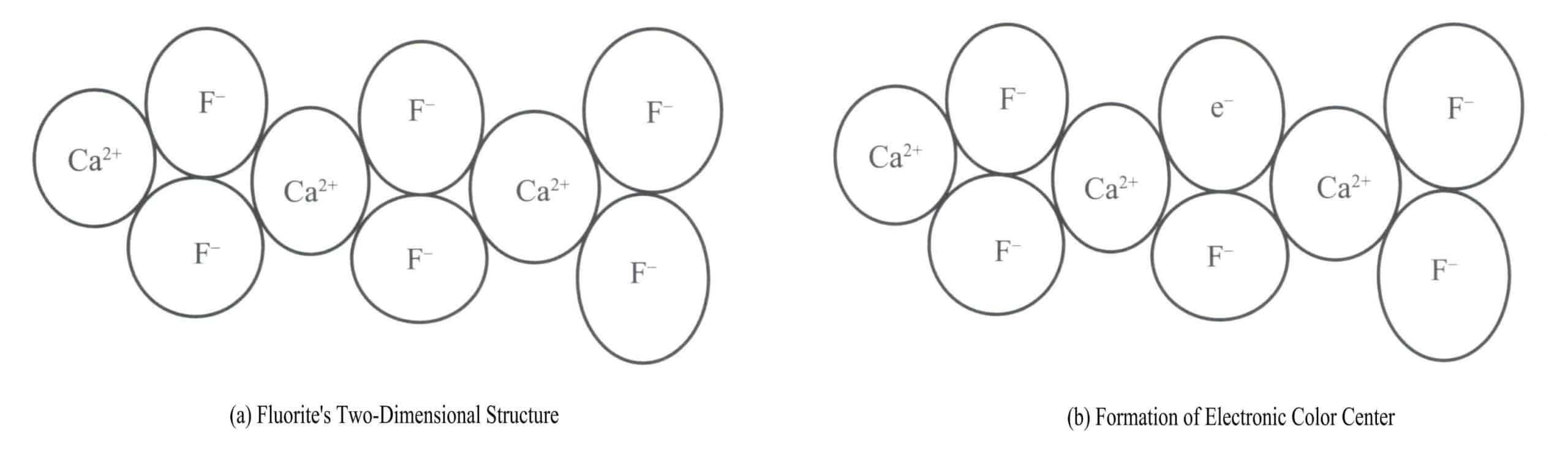
(2) Centra kolorów otworów (centra V)
Centrum koloru wakansu jest tworzone przez czynniki zewnętrzne, gdzie kationy tworzą wakanse elektronowe. Oznacza to, że elektrony są wyrzucane ze swoich pierwotnych pozycji, pozostawiając niesparowany elektron. Przyczyną koloru jest to, że gdy w krysztale tworzą się wakaty kationowe, aby osiągnąć równowagę ładunku, aniony w pobliżu wakatu kationowego uwalniają elektrony pod wpływem energii zewnętrznej, tworząc niesparowane elektrony, które pochłaniają światło widzialne i wytwarzają kolor. Na przykład, w napromieniowanych diamentach i niebieskich topazach, napromieniowanie dostarcza energii do aktywacji elektronów, powodując przemieszczanie się jonów lub atomów w sieci krystalicznej, tworząc w ten sposób defekty strukturalne i centra kolorów spowodowane napromieniowaniem.
Klasycznym przykładem centrum koloru w krysztale jest zabarwienie dymnego kryształu. Struktura krystaliczna kwarcu to czworościan krzemowo-tlenowy, z krzemem w stanie czterokoordynacyjnym, jak pokazano na dwuwymiarowym schemacie strukturalnym na rysunku 3-18(a). Co 10 000 Si4+ mają jeden atom zastąpiony przez Al3+i kiedy Al3+ zastępuje Si4+ w krysztale, Al3+ musi być otoczony jonami alkalicznymi (takimi jak Na+ lub H+), aby utrzymać neutralność elektryczną. Mimo to jony te często znajdują się w pewnej odległości od Al3+.
Gdy kwarc jest napromieniowany promieniami X, γ i innymi źródłami promieniowania, energia sąsiadujących atomów tlenu do Al3+ wzrasta, umożliwiając wyrzucenie jednego z elektronów w parze z jego normalnej pozycji. H+ wychwyci ten elektron, tworząc H . Promieniowanie wysokoenergetyczne powoduje, że O2- z większą liczbą elektronów walencyjnych, aby uwolnić elektron, tworząc [A1O4]4- i [A1O4]4- Klastry atomowe pochłaniają światło widzialne, tworząc kwarc dymny.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ wychwytuje elektrony i przekształca się w H, który jest bezbarwny i nie absorbuje światła widzialnego. Jeśli intensywność naświetlania jest wysoka i jest wystarczająca ilość Al3+ w krysztale, kwarc może być napromieniowany na czarno. Ponieważ w miejscu, w którym elektron jest wyrzucany, często występuje wakat, ten typ centrum koloru jest określany jako "wakatowe centrum koloru".
W historii geologicznej naturalny dymny kryształ powstaje głównie w wyniku długotrwałego promieniowania o niskiej dawce z materiałów radioaktywnych. Ogrzewanie może wyeliminować kolor; gdy ten dymny kryształ zostanie podgrzany do około 400 ℃, wyrzucone elektrony powrócą do swoich pierwotnych pozycji, wszystkie elektrony zostaną sparowane, a kwarc stanie się ponownie bezbarwny; jeśli zostanie ponownie napromieniowany, może ponownie stać się dymny [Rysunek 3-18 (b)].
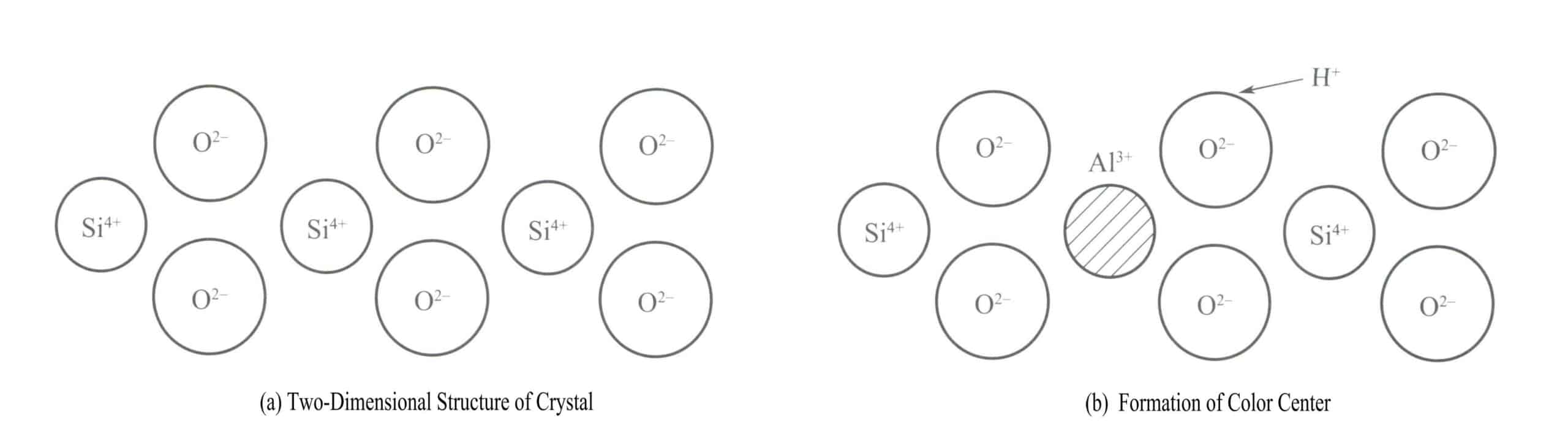
Ametyst ma te same centra kolorów, ale jego zanieczyszczenie to żelazo zamiast aluminium. Gdy zanieczyszczenie Fe 3+ zastępuje Si4+ w kwarcu zachodzą następujące zmiany po napromieniowaniu promieniami o wysokiej energii:
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
Podobnie jak w przypadku kryształu dymu, wytwarza on fioletowy kolor z powodu tworzenia się [FeO4]4- Centra kolorów otworów po napromieniowaniu. Po podgrzaniu ametyst zmienia kolor na żółty, stając się cytrynem, a przy dalszym ogrzewaniu blaknie do bezbarwnego. Ogólnie rzecz biorąc, temperatura ogrzewania jest stosunkowo niska, około 400 ℃. Fioletowy kolor ametystu poddanego obróbce cieplnej można przywrócić poprzez ponowne napromieniowanie centrów kolorów. Syntetyczny ametyst jest również syntetyzowany w oparciu o tę zasadę.
W niektórych kamieniach szlachetnych kilka klastrów atomów zanieczyszczeń może również tworzyć centra kolorów i wykazywać kolor. Na przykład podczas wzrostu berylu i pod wpływem promieniowania radioaktywnego, może stracić elektron, tworząc czerwono-zielone pasmo absorpcyjne, które daje niebieski kolor. Istnieje wiele centrów kolorów w diamentach, z których większość jest spowodowana tworzeniem się wakansów lub dyslokacji w strukturze w warunkach zewnętrznych, a kolory są na ogół bardzo stabilne.
Trudność badania koloru indukowanego przez centrum koloru jest stosunkowo wysoka i wymaga zastosowania różnych technik, takich jak spektroskopia i elektronowy rezonans paramagnetyczny. Wcześniejsze badania wykazały, że niektóre typowe cechy koloru indukowanego przez centrum koloru są stosunkowo jasne. Tabela 38 podsumowuje kolory i przyczyny koloru indukowanego przez centrum koloru w popularnych kamieniach szlachetnych.
Tabela 3-8 Kolory i przyczyny występowania koloru centralnego w popularnych kamieniach szlachetnych
| Rodzaje kamieni szlachetnych | Kolor | Przyczyna |
|---|---|---|
| Diament | Zielony | Środek koloru GR1 z próżnią węglową w diamencie |
| Żółty | Brakująca struktura diamentowych agregatów N3 | |
| Pomarańczowy | Wady centrum kolorów Natoms i H3, H4 | |
| Kryształ | Kolor dymu | Wolne miejsca pracy generowane przez Al3+ zastępując Si4+ związane z promieniowaniem |
| Żółty | Związane z Al3+może być również generowany przez promieniowanie | |
| Fioletowy | Fe3+ zastępuje wakat utworzony przez Si4+ | |
| Kamień szlachetny korund | Żółty | Kolor jest niestabilny, przyczyna wad strukturalnych jest nieznana. |
| Topaz | Niebieski | Kolor jest stabilny, przyczyna wad strukturalnych jest nieznana |
| Żółty | Kolor jest stabilny, przyczyna wad strukturalnych jest nieznana | |
| Brązowo-czerwony | Kolor jest niestabilny, przyczyna wad strukturalnych jest nieznana. | |
| Turmalin | Czerwony | Związane z Mn3+ może być również spowodowane promieniowaniem |
| Beryl | Niebieski | Związane z CO32- może być również spowodowane napromieniowaniem |
| Fluoryt | Fioletowy | Elektroniczny e- zastępuje F-, tworząc |
Zasada centrów kolorów jest również wykorzystywana do poprawy koloru naturalnych kamieni szlachetnych. Większość metod wykorzystuje napromieniowanie do zmiany koloru kamieni szlachetnych. Niektóre centra kolorów są stosunkowo stabilne, podczas gdy niektóre odmiany kamieni szlachetnych szybko blakną, co sprawia, że ta metoda poprawy jest mniej znacząca dla tych kamieni szlachetnych. W tabeli 3-9 wymieniono niektóre kolory wytwarzane przez centra kolorów, w tym stabilne centra kolorów, niestabilne centra kolorów i kolory wytwarzane przez inne możliwe czynniki.
Tabela 3-9 Kolory produkowane przez centra kolorów
| Zasadniczo stabilny w świetle | Ametyst, fluoryt (fioletowo-czerwony), napromieniowane diamenty (zielony, żółty, brązowy, czarny, niebieski, różowy); niektóre naturalne lub napromieniowane topazy (niebieskie). |
|---|---|
| Szybko blaknie pod wpływem światła | zielony beryl litowo-cysowy (ciemnoniebieski); niektóre napromieniowane topazy (brązowe lub brązowe); napromieniowany szafir (żółty); napromieniowany ultrafioletem fioletowy sodalit (fioletowo-czerwony). |
| Inne kolory, które mogą wytwarzać centra kolorów | Sylwin (niebieski); halit (niebieski lub żółty); cyrkonia (brązowy); kalcyt (żółty); baryt, celestyn (niebieski); amazonit (niebieski do zielonego) |
















