Hvorfor har edelstener flere farger?
Hemmelighetene bak fargedannelse og målemetoder
Fargene på edelstener er rike og varierte, og har en unik sjarm som folk alltid har elsket. Kvaliteten på edelstener avhenger i stor grad av fargen. Fargen på en edelsten er en viktig indikator i evalueringen av edelstener, og de fleste optimaliseringsbehandlinger for edelstener innebærer å endre eller forbedre fargen. Derfor er det en avgjørende forutsetning for å kunne optimalisere edelstener å forstå årsakene til fargen. Bare ved å forstå hvordan edelstener får fargen sin, kan man avgjøre om en edelsten kan optimaliseres, hvilket optimaliseringsopplegg som skal brukes, og hvilken eksperimentell plan som skal etableres. Det finnes fem vanlige teorier om farging av edelstener: klassisk mineralogiteori, krystallfeltteori, molekylær orbitalteori, energibåndteori og fysiske optiske effekter. Disse teoriene utgjør fargeleggingsteoriene for vanlige naturlige edelstener, og det følgende er en kort introduksjon til disse fem fargeleggingsteoriene.

Skjematisk diagram over de tre fargeelementene
Innholdsfortegnelse
Del I Farge og måling av edelsteners farge
Fargene på edelstener er rike og varierte, og det er avgjørende å bestemme hvilke typer farger edelstener har for å kunne vurdere verdien av dem. Ulike fargeklasser påvirker også verdien av edelstener, og derfor er en nøyaktig vurdering av fargene til ulike edelstener en grunnleggende forutsetning for å bestemme verdien. Når man vurderer fargede edelstener, er fargen den viktigste faktoren. Generelt sett er det slik at jo mer attraktiv fargen på en edelsten er, desto høyere er dens verdi. Lyse, rike og intense farger er vanligvis mer tiltalende enn de som er for mørke eller for lyse. Det finnes selvfølgelig unntak, for eksempel diamanter, der jo hvitere fargen er, desto høyere verdi har diamanten.
1. Betydningen av edelstenens farger
Siden antikken har folk elsket edelstener på grunn av deres unike sjarm, spesielt de rike og fargerike fargetonene, som den dueblodrøde rubinen, den levende grønne smaragden og jade, som alle etterlater et varig inntrykk. Fargen er en viktig indikator for å evaluere kvaliteten på edelstener og spiller en avgjørende rolle for å bestemme kvaliteten, med betydning som hovedsakelig gjenspeiles i følgende tre aspekter.
(1) Fargen på edelstenmineraler er et viktig grunnlag for å vurdere edelstener
Fargen på en edelsten er grunnleggende for vurderingen av den og bestemmer dens verdi. For eksempel kan en fargeforskjell på én grad føre til en prisforskjell på ca. 5% for diamanter. Jo hvitere diamanten er, desto høyere karakter har den, mens diamanter med gule eller brune fargetoner har lavere karakter, og prisen på dem synker. Prisene på fargede diamanter varierer, og forskjellige fargede diamanter har forskjellige priser. Generelt sett kan imidlertid prisene på sjeldne fargede diamanter mangedobles. Andre fargede edelstener, som rubiner, safirer og smaragder, klassifiseres også i ulike grader basert på farge, og verdien av edelstener i ulike grader kan variere betydelig.
(2) Optimaliseringsbehandlingen av edelstener innebærer ofte å forbedre fargen
Optimaliseringsbehandlingsmetodene for edelstener innebærer vanligvis å endre eller forbedre fargen på edelstenene, så forbedringen av edelstener kan også omtales som fargeendring av edelstener. Når fargen på edelstenen forbedres, endres også gjennomsiktigheten tilsvarende. Dette er fordi gjennomsiktighet er en egenskap relatert til farge. For eksempel ser blå safirer ut til å ha mange ugjennomsiktige svarte farger for det blotte øye, men gjennomsiktig blå kan sees når de kuttes i tynne skiver. Forbedringen i gjennomsiktighet følger ofte med forbedringen i farge. Derfor er det bare ved å finne årsaken til edelstenens farge at man kan finne metoder for å forbedre edelstenens farge. Å forstå årsaken til fargen er en forutsetning for å kunne studere optimaliseringsbehandlinger av edelstener.
(3) Å studere årsakene til edelsteners farge gir et teoretisk grunnlag for syntetiske edelstener og forbedring av edelstener.
Fargene på edelstener som granat, malakitt og olivin skyldes deres iboende komponenter, og disse edelstenene kan ikke få endret fargene sine ved hjelp av konvensjonelle metoder for optimaliseringsbehandling. De fleste edelstensfarger skyldes urenheter forårsaket av urenhetsioner, for eksempel i rubiner, safirer, smaragder, jade og agat. Basert på årsakene til edelstensfarge, under forbedring, kan innholdet og valenstilstanden til visse fargeforårsakende urenhetsioner endres for å endre eller forbedre fargen på edelstenen, og dermed forbedre kvaliteten på den forbedrede edelstenen. Derfor er det å studere årsakene til edelstensfarge det teoretiske grunnlaget for å forbedre edelstener.
2. Fysikken bak farger
(1) Farge og lysbølger
Fotoner bærer energien i lyset, og når fotonene når det menneskelige øyet, skaper de følelsen av farge. Farge er øyets og nervesystemets oppfatning av lys; responsen som genereres av signalene som dannes på øyets netthinne, stimulerer hjernebarken. Det er tre hovedkomponenter som ligger til grunn for fargeoppfatningen: lyskilden, gjenstanden og det menneskelige øyet. Hvis man endrer en eller flere av disse tre, vil fargeoppfatningen endres. Edelstener interagerer med lys, og fenomener som refleksjon, brytning, transmisjon, interferens og diffraksjon som oppstår på overflaten av edelstenen, resulterer i forskjellige farger.
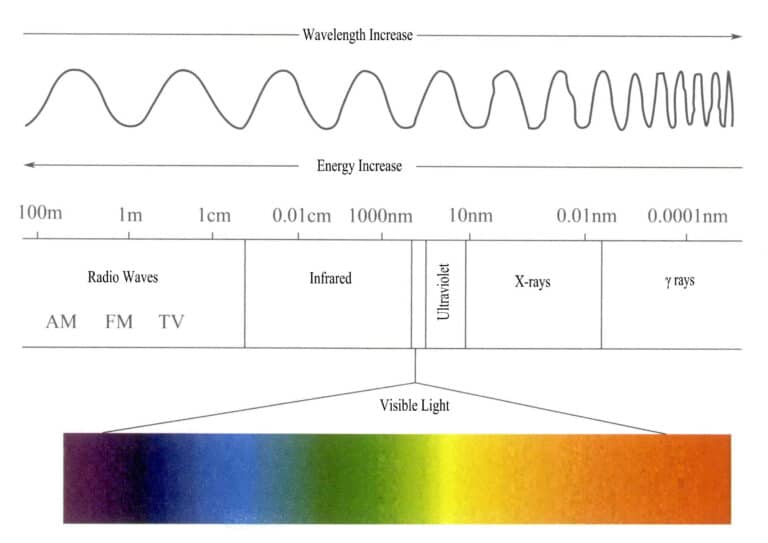
Energispekteret i det elektromagnetiske strålingsspekteret er ganske stort, og varierer fra svært lange radiobølgefotoner til svært korte strålefotoner, med et energiområde fra mindre enn en milliarddel av en elektronvolt til over hundre millioner elektronvolt.
Det synlige lyset som det menneskelige øyet kan akseptere og oppfatte, er en svært liten del av det elektromagnetiske spekteret, med et bølgelengdeområde på 400-700 nm og en energi på ca. 1,7-3,1eV. Hvis observasjonsforholdene er gode nok, kan området utvides til 380-760 nm (figur 3-1). Synlig lys omfatter de fargene vi ser, nemlig rødt, oransje, gult, grønt, cyan, blått, lilla og en rekke andre farger. Forskjellige bølgelengder av synlig lys gir forskjellige farger; den fargen i synlig lys med lengst bølgelengde og lavest energi er rød, med et bølgelengdeområde på 647-760 nm; det synlige lyset med kortest bølgelengde og høyest energi er lilla, med et bølgelengdeområde på 400-425 nm. Andre synlige lysfarger ligger mellom 425 og 647 nm. Bølgelengdene til de ulike fargene i synlig lys og deres komplementærfarger er vist i tabell 3-1.
Tabell 3-1 Bølgelengder for ulike farger av synlig lys og deres komplementære farger
| Bølgelengde/nm | Spektral farge | Utfyllende |
|---|---|---|
| 400 ~ 425 | Lilla | Gulgrønn |
| 425 ~ 455 | Blå | Gul |
| 455 ~ 490 | Grønnblå | Oransje |
| 490 ~ 500 | Blågrønn | Rød |
| 500 ~ 560 | Grønn | Magenta |
| 560 ~ 580 | Gulgrønn | Lilla |
| 580 ~ 595 | Gul | Blå |
| 595 ~ 647 | Oransje | Grønn-blå (cyan) |
| 647 ~ 760 | Rød | Grønn |
Essensen av fargen på et objekt er resultatet av objektets selektive absorpsjon av ulike bølgelengder av synlig lys. Essensen av et objekts selektive absorpsjon av ulike bølgelengder av synlig lys er absorpsjonen av fotoner av synlig lys med ulik energi. Når naturlig lys skinner på en edelsten, absorberer edelstenen en del av lyset og sender også en del av det videre. Fargen på edelstenen er komplementærfargen til det absorberte lyset, i samsvar med fargen på det transmitterte lyset (Figur 3-2). Når for eksempel hvitt lys passerer gjennom en rubin, vil kromionene i rubinen få energi ved å absorbere alle de fiolette og grønne fotonene samt de fleste av de blå fotonene, mens de andre fargefotonene, hovedsakelig røde, passerer gjennom rubinen og får edelstenen til å se rød ut.
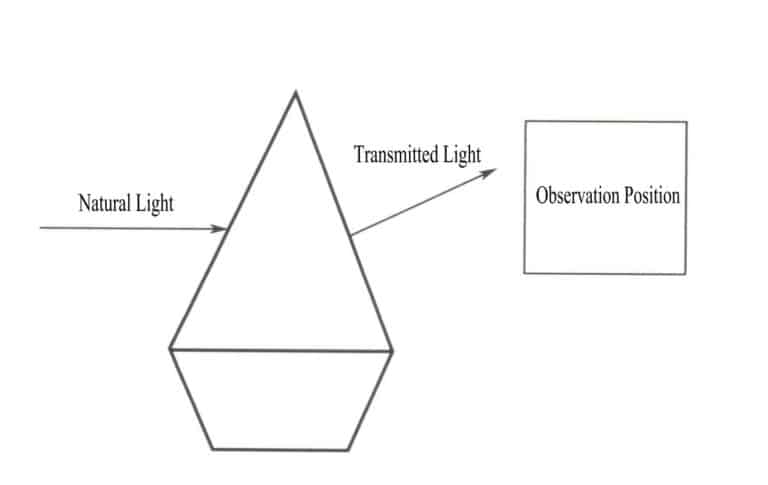
Det er ikke én enkelt bølgelengde som gir fargen på et objekt, men objektets stråling er en blanding av fotoner med ulike energier, der energibåndet med den største andelen bestemmer objektets farge. En jevn blanding av ulike lysfarger danner hvitt lys. Edelsteners farger oppstår ved selektiv absorpsjon av fotoner med ulike bølgelengder av synlig lys. Når hvitt lys passerer gjennom en edelsten, er lyset som absorberes og overføres av edelstenen en blanding, og fargen som presenteres av edelstenen, avhenger av den med den største andelen av det overførte lyset. For eksempel, når hvitt lys skinner på en rubin, er lyset som passerer gjennom rubinen overveiende rødt med en liten mengde blålilla. Derfor ser rubiner ofte røde ut med et blålilla skjær.
(2) Typer og egenskaper til lyskilder
Fargen på edelstener har en viss subjektivitet, som er relatert til observatørens miljø og påvirkes mest av lyskilden. Ved å observere fargen på edelstener under forskjellige lyskilder kan man se forskjeller; for eksempel kan en alexandritt se grønn ut i sollys, men rød under glødelys. Vanligvis anser folk fargen sett i naturlig sollys som standard, ofte referert til som hvitt lys.
De første edelstensmarkedene ble drevet på bestemte tidspunkter for å oppnå en relativt nøyaktig farge på edelstenene. For eksempel har edelstensbutikkene i Ratnapura på Sri Lanka i mange år holdt åpent fra kl. 10.00 til 12.00, ettersom lyskilden i dette tidsrommet er nærmest hvitt lys. Sollys og dagslys er ikke isotrope lyskilder, og de relative forskjellene i strålingsmengde i ulike bølgelengder mellom ulike lyskilder kan være svært store på grunn av ulike observasjonsforhold. Figur 3-3 viser energifordelingskurvene for fem vanlige lyskilder, og energiforskjellene mellom disse lyskildene er svært store.
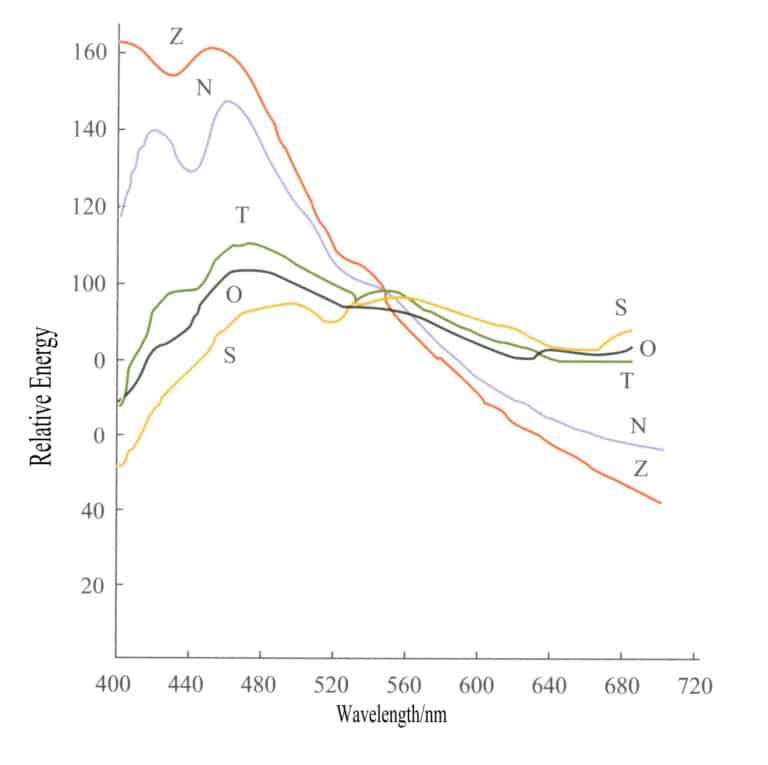
S - Direkte sollys; O - Belysning av overskyet himmellys på horisontalplanet; T - Belysning av sollys og klar himmel på horisontalplanet; N - Lys fra den klare nordhimmelen; Z - Zenitlys;
Fargeegenskapene til direkte sollys uttrykkes ofte i fargetemperatur (målt i K). Samme fargetemperatur indikerer lignende farger på lyskilder. De anerkjente fargetemperaturene for dagslys er D6500K, D5500K og D7500K. Tre lamper er internasjonalt utpekt som standard lyskilder for fargemåling. SA representerer den gjennomsnittlige kunstige belysningen fra en glødelampe med en fargetemperatur på 2854 K ; SB representerer gjennomsnittlig sollys, med en fargetemperatur på 4900K; SC representerer gjennomsnittlig dagslys, med en fargetemperatur på 6700K. I perletesting brukes Sc-lyskilden som standard lyskilde.
(3) Følsomhet for lys- og fargeeffekter
Observasjonen av edelstenens farger er subjektiv; i tillegg til objektive forhold er edelstenens farge også relatert til observatørens sanseoppfatning. Under samme lyskilde har menneskelige øyne ulik følsomhet for forskjellige farger, og forskjellige mennesker har varierende følsomhet for farger. Observasjonen av farger er subjektiv; for å oppnå objektivitet så mye som mulig, må farger karakteriseres og uttrykkes relativt objektivt.
① Fotoreseptiv effekt:
Under normale forhold ligger bølgelengdeområdet for synlige lyskilder som det menneskelige øyet kan observere, på 400-700 nm. Ved å forbedre observasjonsforholdene kan følsomhetsområdet utvides til 380-780 nm. Det menneskelige øyet har ulik følsomhet for lysbølger med forskjellige bølgelengder. På dagtid er øyet mest følsomt for grønt lys med en bølgelengde på 555 nm, mens den mest følsomme bølgelengden for skumringssyn skifter til 507 nm. Trafikklysene på veien er utformet basert på de fargene som det menneskelige øyet er mest følsomt for.
② Fargefølelse:
Farge er den følelsen som forårsakes av de ulike spektrale komponentene av strålingsenergi i det synlige lysområdet. En normal persons syn kan skille mellom mer enn 150 nyanser av rene spektralfarger. Selv om det er en én-til-én-korrespondanse mellom lysbølger og farger, er korrespondansen mellom farger og lysbølger ikke entydig; ofte kan en lysfarge dannes ved å kombinere to eller flere andre lysfarger. De tre grunnleggende, uavhengige fargene er rød, grønn og blå, kjent som primærfargene. Andre farger dannes ved å blande to eller flere primærfarger i forskjellige proporsjoner, og det menneskelige øyet er svært følsomt for farger og kan skille mellom mange forskjellige farger.
3. Tre elementer som representerer farge
Farge er et resultat av selektiv absorpsjon av lys i edelstener, og ulike edelstener har ulike farger. Dagens fargeteori antyder at fargeegenskapene avhenger av lysstyrke, fargetone og metning (Figur 3-4). Hvilke typer edelstensfarger som finnes, kan bestemmes ved å beskrive de tre elementene i ulike farger.

(1) Lysstyrke
Lysstyrke er graden av lysstyrke forårsaket av lys som virker på det menneskelige øyet, og refererer til graden av lyse og mørke farger, og kan også kalles luminans. Lysstyrken avhenger i stor grad av øyets oppfatning av lyskildens og objektets overflates lys- og mørkenivåer, som først og fremst bestemmes av lysets intensitet. Lysstyrken avhenger av objektets belysningsnivå og refleksjonsevnen til objektets overflate.
Lysstyrke kan forstås som lysstyrken til en farge; forskjellige farger har forskjellige lysstyrkenivåer, og alle farger har variasjoner i lys og mørke. Lysstyrke har to egenskaper: Samme objekt kan ha ulik lysstyrke på grunn av forskjellig belysning, og forskjellige fargede lys med samme intensitet kan også ha ulike lysstyrkenivåer.
I fravær av farge er fargen med høyest lysstyrke hvit, og fargen med lavest lysstyrke er svart, med en gråskala mellom lys og mørk. I farger har enhver grad av renhet sine lysstyrkeegenskaper. For eksempel har gult den høyeste lysstyrken, mens lilla har den laveste. Grønn, rød, blå og oransje har lignende lysstyrkenivåer, som representerer middels lysstyrke. I tillegg finnes det variasjoner i lysstyrke fra lys til mørk innenfor samme fargetone, for eksempel lysegrønn, blekgrønn og smaragdgrønn i det grønne spekteret.
(2) Hue
Fargetone refererer til forskjellene mellom ulike farger og er den mest fremtredende egenskapen ved farger. Fargetonen bestemmes av de spektrale komponentene i lyset som passerer gjennom et objekt og når det menneskelige øyet etter å ha truffet det, avhengig av bølgelengden på det transmitterte lyset. Fargetonen til et objekt bestemmes av spekteret til den innfallende lyskilden og lyset som reflekteres eller overføres av selve objektet.
Den såkalte fargetonen refererer til navnet som mer nøyaktig kan representere en bestemt fargekategori, for eksempel rosenrød, oransjegul, sitrongul, koboltblå, purpurrød, smaragdgrønn osv. Fra et fysisk optisk perspektiv bestemmes de ulike fargetonene av spektralkomponentene i lyset som kommer inn i det menneskelige øyet. For monokromatisk lys avhenger fargetonene helt og holdent av lysets bølgelengde, mens de for lys med blandingsfarger avhenger av de relative mengdene av de ulike bølgelengdene. Fargen på et objekt bestemmes av spektralkomponentene i lyskilden og egenskapene til lyset som reflekteres (eller transmitteres) av objektets overflate. Den er relatert til lysets bølgelengde. En farge med en dominerende bølgelengde på 470 nm kalles for eksempel blå med en bølgelengde på 470 nm, som ofte ses som den blå fargen på safirer.
(3) Metning
Metningen av en farge refererer til fargens renhet og livlighet, og indikerer andelen kromatiske komponenter som finnes i fargen. Jo større andel kromatiske komponenter, desto renere er fargen; jo mindre andel kromatiske komponenter, desto mindre ren er fargen. Metningen endres når en farge blandes med svart, hvitt eller andre farger. Når andelen av den blandede fargen når et betydelig nivå, vil den opprinnelige fargen miste sin opprinnelige glans for øyet, og fargen som sees, vil bli den blandede fargen. Dette betyr selvfølgelig ikke at den opprinnelige fargen ikke lenger eksisterer, men snarere at den opprinnelige fargen har blitt assimilert på grunn av de mange andre fargene som er blandet inn, slik at den ikke lenger er merkbar for det menneskelige øyet.
De monokromatiske lysene i det synlige spekteret har høyest metning og er de mest levende. Monokromatisk lys regnes vanligvis som 100/100 = 1, og etter hvert som fargen blekner, synker verdien gradvis, og rent hvitt har null metning. Hvis vi tar rent blått blekk som eksempel, er metningen til rent blått blekk 1, og når det gradvis fortynnes til å bli helt fargeløst, blir metningen null.
4. Måling av edelstenens farge
Systemet som kvantitativt representerer farger, kalles et fargesystem. Det finnes to typer fargesystemer som ofte brukes: Det ene er et fargesystem basert på standard fargeprøver for sammenligning, og det andre er et sett med fargestandardsystemer som måles ved hjelp av moderne fargemålingsinstrumenter.
(1) Fargesystem for standard fargeprøver
Dette fargesystemet består av ulike "fargekort" laget av papir som er standard fargeprøver samlet i en bok. De sammenlignes med edelstensprøver for å velge det "fargekortet" som matcher edelstenens farge.
① Munsell Color System
Munsell Color System er et av de tidligste og mest klassiske fargesystemene. Det brukes fortsatt av enkelte organisasjoner i dag. Det ble etablert i 1905 av den amerikanske pedagogen og fargeteoretikeren Albert Munsell, som ble oppkalt direkte etter ham. Det er en måte å representere farger på gjennom en farge-faststoffmodell. "Munsell Color Atlas", som utgis av Optical Society of America (OSA), finnes i en blank og en matt versjon.
Den blanke versjonen inneholder 1450 fargeprøver, ledsaget av et sett med 37 akromatiske prøver; den matte versjonen inneholder 1150 fargeprøver og 32 akromatiske prøver.
I Munsell Atlas er hver farge representert med et sett med symboler. Symbolene gir ekvidistante indikatorer for de tre elementene i fargegjengivelsen: fargetone, -verdi og -kroma, representert som HV/C = fargetoneverdi/kroma.
Fargene deles inn i fem primærfarger: rød (R), gulrød (YR), gul (Y), grønngul (GY), grønn (G), blågrønn (BG), blå (B), purpurblå (PB), purpur (P) og rødlilla (RP), samt fem mellomtoner. Hver tone er videre delt inn i ti nivåer (1 til 10), der det femte nivået er mellomfargen for den aktuelle tonen (Figur 3-5).
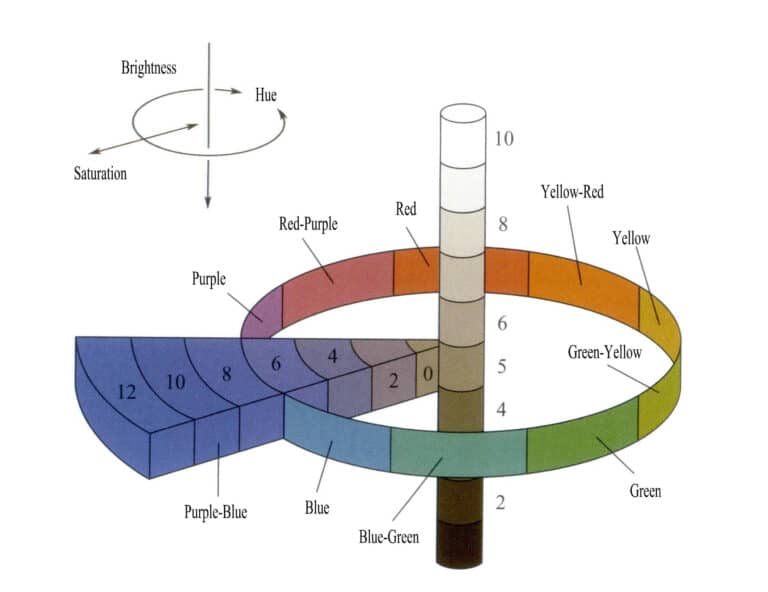
Value er delt inn i 11 nivåer, der høyere verdier indikerer høyere lyshet; minimumsverdien er 0 (svart), og maksimumsverdien er 10 (hvit). Chroma er delt inn i 12 nivåer. Hele fargeatlaset inneholder 40 typer fargetoneprøver. 5GY 8/7 representerer for eksempel en gulgrønn farge med en verdi på 8 og en metning på 7. Navngivningskonvensjonen for ikke-fargeserier (svart, hvitt, grått) er NV/= nøytral lyshetsverdi; en farge merket N5/ indikerer for eksempel en grå farge med en lyshetsverdi på 5.
② DIN 6164 Fargesystem
Tysklands DIN 6164-manual er også et viktig fargesystem. Mange gemmologer i Europa og Storbritannia bruker dette systemet. Dette fargesystemet ble utviklet basert på Munsell-systemet.
DIN 6164-fargekortet har 24 farger, og baksiden av hver farge er merket med den tilsvarende Munsell-fargenotasjonen. Representasjonen er i formatet fargetone: metning: lyshet. For eksempel representerer 6:6:2 fargetone 6 (rød), metning 6 (levende) og lyshet 2 (lys) på standardfargekortet.
ISCC-NBS-fargesystemet ③ ISCC-NBS Color System
ISCC (Inter-Society Colour Council) ble etablert i 1931 som en innenlandsk fargesammenslutning i USA, og deres fargesystem har som mål å utvikle et fargenavnsystem. Det samler 18 fargetoner på samme fargetone- og lyshetsposisjoner i Munsell og DIN 6164.
ISCC-NBS (National Bureau of Standards) har svært få fargeprøver i det amerikanske nasjonale standardsystemet, men har samlet noen uvanlige prøver. Strukturelt sett skiller det seg også fra Munsell-systemet, ettersom fargene ikke er ordnet i henhold til perseptuelle ekvidistanseverdier. ISCC-NBS-systemets viktigste bidrag til fargelæren er at det definerer fargenavn.
④ OSA Color Standard
OSA (Optical Society of America) har utarbeidet et praktisk sett med akrylglansfargekort, inkludert 558 farger, hvorav 424 farger utgjør et sett kjent som OSA-fargestandarden. Ulempen med OSA-fargestandarden er at fargekortene er laget av papir eller plast, som har en annen tekstur enn edelstener, og overflateglansen på fargekortene skiller seg fra lyset som reflekteres av fasetterte edelstener, noe som krever forsiktig bruk. På grunn av falming har de fleste fargekort en brukstid på 4 til 5 år.
(2) Kromatiske koordinater og kromatisk diagram
① 1931 CIE-XYZ-fargeromssystem
Dette fargeromssystemet er basert på RGB-systemet og bruker matematiske metoder for å velge ut tre ideelle primærfarger som skal erstatte de faktiske primærfargene. Ved å bruke virtuelle primærfarger som akser projiserer det ulike bølgelengder av synlig lys. Verdiene til primærfargene kalles tristimulusverdier. Dette systemet krever at tristimulusverdiene ikke er negative, og at y er lik lysstrømmen. Ved å bruke x som horisontal akse og y som vertikal akse danner det kromatiske koordinater, og projiserer de kromatiske koordinatverdiene for hvert monokromatiske lys for å få det kromatiske diagrammet. Figur 3-6 er det kromatiske standarddiagrammet i (XYZ)-systemet som ble etablert internasjonalt i 1931.
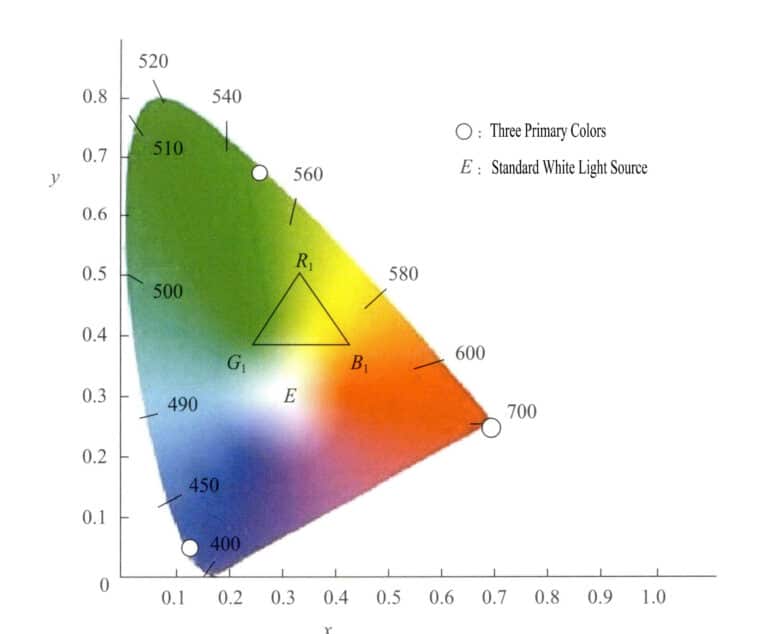
Det kromatiske diagrammet har følgende egenskaper:
- Tristimulusverdiene for primærfargene i dette systemet er virtuelle.
- Alle punkter som representerer spektralfarger, faller på den tungeformede kurven som kalles spektralfargen. Ved å koble endene av kurven sammen med rette linjer, ligger alle de faktiske fargene innenfor området som er omgitt av den tungeformede kurven og de rette linjene.
- Koordinatverdien til punkt E ved x=0,333, y=0,333 representerer teoretisk hvitt. Ulike hvite lyskilder har litt forskjellige spektrale komponenter. Det hvite lyset som vanligvis brukes, deles inn i SA, SB, SC, SEog så videre.
- Fargenes kromatiske koordinater har høyere metning jo nærmere de ligger den spektrale fargebanen. Punkter på den spektrale fargebanen har høyest metning, mens det hvite punktet har lavest metning. En linje som trekkes fra det hvite punktet til de kromatiske koordinatene til en farge, og som forlenges slik at den skjærer den spektrale fargebanen, har punkter langs denne linjen som har samme fargetone.
- En grafisk metode kan brukes til å utlede den sammensatte fargen av to farger. Ved å legge inn de kromatiske koordinatene til de to fargene i det kromatiske diagrammet, må den sammensatte fargen ligge på linjen som forbinder de to fargekoordinatpunktene. Avstanden som projiseres til de to fargepunktene, er relatert til intensiteten til de to fargene, bestemt av loven om tyngdepunktfordeling.
- Punkter på den rette linjen mellom endepunktene på den spektrale fargekurven representerer ikke spektralfarger, men ulike blandingsfarger som oppnås ved å blande lilla ved 380 nm og rødt ved 780 nm i ulike proporsjoner.
- Velg tre punkter innenfor spektrumets fargebane for å opprette en farge. Hvis du for eksempel velger R1, G1, B1 som de tre fargene for matching, så er alle de ulike fargene som dannes av disse tre fargetonene inneholdt i trekanten med hjørner i de tre punktene R1, G1, B1.
② Representasjon av dominerende bølgelengde og metning
I det kromatiske diagrammet kan farger ikke bare representeres ved hjelp av kromatiske koordinater (x, y). En annen metode foreslått av Helmholtz er å representere dem ved hjelp av den dominerende bølgelengden λd og metning (stimulusrenhet) Pe. λd og Pe er spesifikke verdier avledet fra de kromatiske koordinatene i diagrammet (Figur 3-7). Den dominerende bølgelengden representerer omtrent den fargefølelsen som oppfattes av det menneskelige øyet.
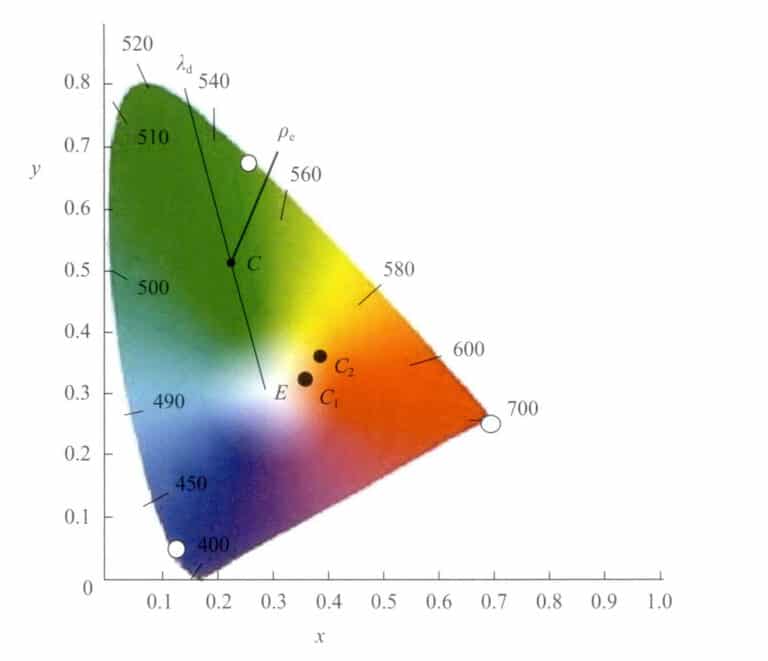
La posisjonen til dette punktet i det kromatiske diagrammet være c(x, y). Forbind punkt c med hvit E og forleng den slik at den skjærer spektrumbanen ved λd . Da vil bølgelengdenummeret til punktet λd på spektrumbanen er den dominerende bølgelengden i dette fargelyset.
Punktet C ligger på linjen som forbinder punktene W og λd , som representerer metningen av denne fargen. Punkt W er ren hvit (E) eller en bestemt hvit lyskilde. Når de kromatiske koordinatene til en bestemt farge gradvis beveger seg i retning av spektralbanen fra det hvite punktet W, øker fargens metning gradvis til den når spektralbanen, med en maksimal metning på 1.
Fargene er representert ved hjelp av dominerende bølgelengde og metning, noe som gjør det enkelt å sammenligne fargeforskjeller. De små fargeforskjellene, representert ved de numeriske endringene i λd og ρekan vises.
For to farger, C1, C2er de kromatiske koordinatene, den dominerende bølgelengden og metningen under samme belysning vist i Tabell 3-2. Det fremgår at den dominerende bølgelengden for fargen C1, C2 avviker med 0,052 nm, og metningen avviker med 7%.
Tabell 3-2 Sammenligning av fargedata mellom C1 og C2
| Fargeprojeksjonspunkt | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. Instrumenter for måling av edelstenens farge
(1) Spektrofotometer
Arbeidsprinsipp: Fordi den spektrale energifordelingen til standardlyskilden inne i instrumentet er kjent, kan tristimulusverdiene til et objekt beregnes ved å måle den spektrale reflektansen.
(2) Tristimulusverdi-kolorimeter
Det er et fotoelektrisk integrativt instrument som direkte måler de tre stimulusverdiene til et objekts farge. Det simulerer hovedsakelig standardobservatørens tre responser på farger ved hjelp av en passende kombinasjon av filtre og fotoelektriske omformere.
For tiden er vurderingen av edelstensfarge hovedsakelig avhengig av observasjon av det menneskelige øye. For eksempel påvirkes smaragder, rubiner og diamanter av miljøfaktorer, noe som fører til lav nøyaktighet i instrumentmålinger; derfor er anvendelsen av instrumentfargemåling i identifikasjon av edelstener relativt sjelden.
Del II Teoretisk opprinnelse til edelsteners mineralfarge
Edelsteinsmineraler kommer i forskjellige farger, men årsakene til fargene deres er også forskjellige. Ifølge klassisk mineralogisk teori kan opprinnelsen til edelstenmineralfarger klassifiseres i idiokromatisk farge, allokromatisk farge og pseudofarge.
1. Klassifisering av klassisk mineralogi Fargeopprinnelsesteori
Den klassiske teorien om mineralogi er den mest grunnleggende teorien for å studere fargene på edelstenmineraler. Avhengig av om mineralets farge skyldes selve mineralet, kan det deles inn i tre kategorier: idiokromatisk farget, allokromatisk farget og pseudofarget.
(1) Idiokromatisk-farget
Fargen på en edelsten dannes av de iboende kjemiske komponentene i mineralet den består av, kjent som idiokromatisk farget. Slike edelstener kalles idiokromatisk fargede edelstener. Det er de iboende bestanddelene som gir den fargen som produseres av idiokromatisk fargede edelstener, og de har derfor god fargestabilitet og er ikke lette å endre. For eksempel er den kjemiske sammensetningen av turkisCuAl6(PO4)4(OH)8-5H2O, og den blå eller blågrønne fargen skyldes Cu2+; den kjemiske sammensetningen av azuritt er 2CuCO3 - Cu(OH)2, og Cu2+ er også årsaken til den blå fargen"; den grønne fargen på olivin skyldes jernioner i den kjemiske sammensetningen (Figur 3-8).

Det finnes ikke mange typer ensfargede edelstener i naturlige smykkemineraler, og de viktigste variantene er turkis, malakitt, azuritt, olivin, granat og rhodokrositt. De vanligste fargene, fargestoffene og kjemiske sammensetningene til selvfargede edelstener er vist i tabell 3-3.
Tabell 3-3 Vanlige fargestoffer, kjemisk sammensetning og farger på fargede edelstener
| Fargelegging av elementer | Navn på edelsten | Kjemisk sammensetning | Farge |
|---|---|---|---|
| Jern | Olivine | (Mg, Fe)2 (SiO4) | Grønn |
| Almandine | Fe3Al2 (SiO4)3 | Rød | |
| Krom | Uvarovitt | Ca3Cr2 (SiO4)3 | Grønn |
| Cuprum | Malakitt | Cu2Co3(OH)2 | Grønn |
| Krysokoll | (CuAl)2H2Si2O5(OH)4 - nH2O | Grønn - Blå | |
| Turkis | CUAl6(PO4)4(OH)8.5H2O | Himmelblå - Grønn | |
| Azuritt | 2CuCO3 - Cu(OH)2 | Blå | |
| Mangan | Spessartine-Garnet | Mn3Al2(SiO4)3 | Oransje |
| Rhodokrositt | MnCO3 | Rosa - Rød | |
| Rhodonitt | (Mn, Ca, Fe) - 5(Si5O15) | Rosa - Rød |
Copywrite @ Sobling.jewelry - Tilpasset smykkeprodusent, OEM og ODM smykkefabrikk
Noen fargede edelstener kan endre farge under visse forhold. For eksempel kan turkis og malakitt endre farge når de utsettes for høye temperaturer på grunn av fordampning av vannmolekyler i sammensetningen. Rhodokrositt, en karbonat-edelsten, kan brytes ned når den møter syrer (som saltsyre eller svovelsyre), og fargen vil også endre seg tilsvarende.
(2) Allokromatisk-fargeed
Fargen på en edelsten er forårsaket av spor eller mindre urenheter som ligger utenfor den iboende kjemiske sammensetningen av de inngående mineralene, kjent som allokromatisk farge. Slike edelstener omtales som allokromatisk fargede edelstener.
I edelstenmineraler finnes det mange varianter av edelstener med forskjellige farger. Når det ikke er urenheter i edelstenens kjemiske sammensetning, er den fargeløs og gjennomsiktig; når den inneholder forskjellige fargestoffer, kan den produsere forskjellige farger.
Når ren korund er fargeløs, blir den til rubin når den inneholder en liten mengde kromioner; når den inneholder en liten mengde jern og titan, blir den til blå eller grønne edelstener. Lignende edelstener inkluderer smaragd, spinell, turmalin, jadeitt, kalcedon, nefrit osv. De vanligste fargestoffene, kjemiske sammensetningene og allokromatisk fargede edelstener er vist i tabell 3-4.
Tabell 3-4 Vanlige fargestoffer, kjemisk sammensetning og allokromatisk fargede edelstener
| Fargelegging av elementer | Navn på edelsten | Kjemisk sammensetning | Farge |
|---|---|---|---|
| Krom | Ruby | Al2O3 | Rød |
| Smaragd | Være3Al2(Si6O18) | Grønn | |
| Alexandritt | BeAl2O4 | Rød-grønn | |
| Spinell | MgAl2O4 | Rød | |
| Kalcedon | SiO2 | Grønn | |
| Jern | Akvamarin | Være3Al2Si6O18 | Blå |
| Turmalin | (Na, K, Ca) (Al, Fe3+, Cr)6(BO3)3Si6O18(OH)4 | Grønn-Brun | |
| Spinell | MgAl2O4 | Gul | |
| Nephrite | Ca2(Mg, Fe2+) 5 (Si4O11) 2 (OH)2 | Grønn | |
| Vanadium | Tanzanitt | Ca2Al3(SiO4)3(OH) | Lilla-blå |
| Grønn beryll | Være3Al2Si6O18 | Grønn | |
| Titan | Benitoitt | BaTiSi3O9 | Blå |
| Safir | Al2O3 | Blå | |
| Mangan | Rød beryll | Være3Al2Si6O18 | Rød |
| Rhodokrositt | MnCO3 | Rosa | |
| Kobolt | Naturlig spinell | MgAl2O4 | Blå |
| Syntetisk spinell | MgAl2O4 | Blå | |
| Nikkel | Grønn kalcedon | SiO2 | Grønn |
(3) Pseudo-fargeed
Fargene som produseres av pseudofarger er ikke relatert til den kjemiske sammensetningen av edelstenmineraler. De er likevel forårsaket av strukturelle og sammensetningsmessige endringer som følge av mekaniske blandinger eller dannelse av mineraler. Pseudofarger er ikke fargene på selve mineralene, men snarere farger forårsaket av spesielle strukturer dannet av ytre påvirkninger. For eksempel vakre interferensfarger som oppstår ved interferens mellom reflektert og innfallende lys, slik som labradorittens fluorescenseffekt og opalens fargespill. Farger forårsaket av inneslutninger faller også inn under pseudofarger, som for eksempel svarte diamanter, som skyldes mange svarte, ugjennomsiktige grafittinneslutninger i diamanten.
2. Fargeskapende ioner i edelstenmineraler
De kjemiske grunnstoffene som gir edelstener farge, kan være hoved- eller underkomponenter. Overgangsmetaller, spesielt overgangsmetallene titan, vanadium, krom, mangan, jern, kobolt, nikkel og kobber fra 4. periode, omtales ofte som kromoforer eller fargeioner. Disse åtte grunnstoffene står på rekke og rad i det periodiske systemet, med atomnummer fra 22 (Ti) til 29 (Cu). De grunnleggende egenskapene til disse grunnstoffene er vist i tabell 3-5.
Tabell 3-5 Grunnleggende egenskaper for åtte overgangselementer
| Elementets navn | Titan | Vanadium | Krom | Mangan | Jern | Kobolt | Nikkel | Kobber |
|---|---|---|---|---|---|---|---|---|
| Elementsymbol | Ti | V | Cr | Mn | Fe | Co | Ni | Cu |
| atomnummer | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| Viktigste oksidasjonstrinn | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| Valenselektronkonfigurasjon | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
Disse åtte overgangsmetallene har følgende egenskaper:
① Valenselektronene fylles i d-orbitalene i det nest siste skallet i rekkefølgen, og den generelle formelen for valenselektronkonfigurasjonen til overgangselementatomer er (n-1)d1-10nS1-2, så disse elementene kalles også d-blokkelementer.
② I overgangsmetaller er d-orbitalene i det nest siste skallet koblet til de ytterste s-orbitalene, og d-orbitalene har ennå ikke nådd en stabil struktur, slik at både s-elektroner og d-elektroner kan delta helt eller delvis i bindingen, noe som resulterer i en rekke varierende oksidasjonstrinn for overgangsmetaller, med forskjellige oksider som gir forskjellige farger i edelstener.
Ioner har vanligvis farge fordi det finnes uparede enkeltelektroner i d-orbitalene, og energinivåene til disse elektronene i eksitert tilstand og grunntilstand ligger relativt nær hverandre, slik at de kan eksiteres av synlig lysenergi. Forskjellige eksitasjonsforhold kan også føre til at edelstener får forskjellige farger.
Hvis alle spinnelektronene i ionet er paret, for eksempel ioner med en valenselektronkonfigurasjon på d0, d10, d10s2er elektronene i en stabil tilstand og blir ikke lett eksitert, noe som resulterer i at ionet ikke har noen farge; dermed er C+, Cr6+ og andre har ingen farge og kan ikke produsere farge i edelstener.
Disse åtte overgangsmetallene utgjør fargedannelsen i vanlige naturfargede edelstener. Ulike kromoforer gir ulike farger i ulike edelstener, og den samme kromoforen kan også gi ulike farger. Vanlige naturlige edelstener og kromoforer er vist i tabell 3-6.
Tabell 3-6 Farger presentert av overgangsmetallioner i vanlige naturlige edelstener og edelstenvarianter
| Kromofor | Vanlige farger | Edelsteinsorter |
|---|---|---|
| Titan (Ti)-ion | Blå | Safir, benitoitt, topas |
| Vanadium (V)-ion | Grønn | Syntetisk fargeskiftende korund, essonitt, smaragd |
| Krom (Cr)-ion | Rød, Grønn | Rubin, korund, smaragd, pyrop, jade |
| Mangan (Mn)-ion | Rosa, Rød | Spessartin, rhodolitt, rød beryll |
| Jern (Fe)-ion | Blå, grønn, gul | Safir, olivin, akvamarin, turmalin, spinell |
| Kobolt (Co)-ion | Blå | Syntetisk spinell, koboltfarget staurolitt |
| Nikkel (Ni)-ion | Grønn | Grønn kalcedon |
| Kobber (Cu)-ion | Blå, blågrønn | Malakitt, turkis, asuritt |
Ulike kromoforioner gir forskjellige farger i edelstener, noe som resulterer i absorpsjonsspektre med distinkte egenskaper. For vanlige kromoforioner har absorpsjonsspektrene typisk identifikasjonsbetydning.
(1) Absorpsjonsspekteret til kromioner
Absorpsjonsspekteret til kromioner er hovedsakelig preget av mange smale absorpsjonslinjer i det røde området, med de to sterkeste i det dyprøde området og to andre i det oransje området. Den gulgrønne regionen har et bredt absorpsjonsbånd, og bredden, posisjonen og intensiteten er relatert til dybden på edelstenens farge. Det kan være flere smale bånd i den blå regionen, mens den lilla regionen er fullstendig absorbert. Kromioner produserer hovedsakelig røde og grønne farger, som varierer i forskjellige edelstener, og absorpsjonsspektrene viser noen forskjeller. For eksempel har rubiner tre absorpsjonslinjer i den røde regionen, et bredt absorpsjonsbånd i den gulgrønne regionen, tre absorpsjonslinjer i den blå regionen og full absorpsjon i den lilla regionen; smaragder har absorpsjonslinjer i den røde regionen, et svakt absorpsjonsbånd i den oransjegule regionen, svake absorpsjonslinjer i den blå regionen og full absorpsjon i den lilla regionen; og alexandritt har absorpsjonslinjer i den røde regionen, et absorpsjonsbånd i den gulgrønne regionen, en absorpsjonslinje i den blå regionen og full absorpsjon i den lilla regionen. Absorpsjonsspektrene til disse tre edelstenene er vist i figur 3-9.

(2) Kjennetegn ved absorpsjonsspekteret for jernioner
Jernioner gir forskjellige farger i forskjellige edelstener og har en sterk fargeeffekt, men absorpsjonsspekteret til jernioner varierer veldig. Når edelstenen er grønn, gir den en absorpsjon i rød sone, og når den er rød, gir den en absorpsjonsfunksjon dominert av den blå sonen, med den viktigste karakteristiske absorpsjonslinjen i de grønne og blå sonene. For eksempel ser jernioner i olivin olivengrønne ut, og absorpsjonsspekteret viser hovedsakelig tre smale absorpsjonsbånd i den blå sonen ved 453 nm, 473 nm og 493 nm. Rød almandin har et typisk jernabsorpsjonsspekter med tre sterke, smale absorpsjonsbånd ved 504 nm, 520 nm og 573 nm i den gulgrønne sonen, som i bransjen ofte kalles "jernvinduet". I tillegg er det svake smale absorpsjonsbånd ved 423 nm, 460 nm, 610 nm og 680 ~ 690 nm; absorpsjonsspekteret til gul safir har tre smale absorpsjonsbånd i den blå regionen ved 450 nm, 460 nm og 470 nm (figur 3-10).
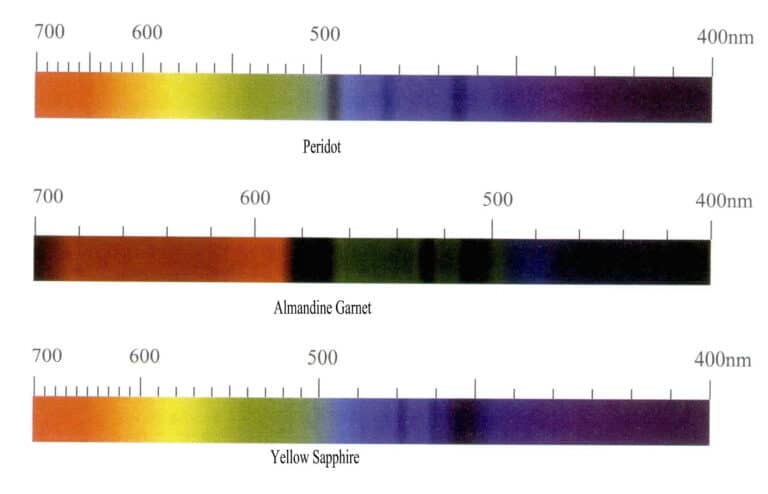
(3) Absorpsjonsspekteregenskaper for manganioner
Manganioner danner hovedsakelig rosa, oransje og rød i edelstener, med absorpsjonsspekteret som primært viser sterk absorpsjon i det fiolette området, som strekker seg inn i det ultrafiolette området, og noe absorpsjon i det blå området. For eksempel har absorpsjonsspekteregenskapene til rosa rhodochrositt tre absorpsjonsbånd ved 410nm, 450nm, 540nm; absorpsjonsspektrumlinjene til spessartin har hovedsakelig 410nm, 420nm, 430nm tre absorpsjonsbånd og absorpsjonslinjer ved 460nm, 480nm og 520nm. Noen ganger kan det være 504nm, 573nm to absorpsjonslinjer (figur 3-11).

(4) Absorpsjonsspekteregenskaper for koboltioner
Koboltioner har en sterk fargeeffekt, og vises vanligvis i en lys blå farge i edelstener, med absorpsjonsspekteret som hovedsakelig viser tre sterke og brede absorpsjonsbånd i det gulgrønne området. På grunn av den lave forekomsten av kobolt i jordskorpen finnes det svært få naturlige edelstener som er farget av koboltioner. Absorpsjonsspekteret til koboltioner indikerer også syntetiske edelstener, som syntetisk blå spinell og koboltglass. Syntetisk blå spinell har tre sterke absorpsjonsbånd i de gulgrønne og oransjegule områdene, med det grønne absorpsjonsbåndet som det smaleste; absorpsjonslinjene til koboltglass har hovedsakelig tre sterke absorpsjonsbånd i de gulgrønne og oransjegule områdene, med det gule absorpsjonsbåndet som det smaleste (figur 3-12).

3. Fargelegging av sjeldne jordarter
Forskning på innflytelsen av spor av sjeldne jordartsmetaller på fargen på edelstener blir stadig mer dyptgående. Fargene på sjeldne jordartsmetaller er mer levende, og deres fysisk-kjemiske egenskaper er også veldig stabile. Sjeldne jordartsmetaller som apatitt og fluoritt kan også farge naturlige edelstener. Ulike sjeldne jordartsmetaller kan tilsettes syntetiske og optimalt behandlede edelstener for å oppnå forskjellige fargede edelstener, for eksempel gul fra cerium og blå fra neodym.
De sjeldne jordartsmetallene som farger edelstener, er hovedsakelig lantanidene og aktinidene i det periodiske system av grunnstoffer, og fargene de kan gi, er vist i tabell 3-7.
Tabell 3-7 Sjeldne jordarter og deres farger i vanlige edelstener
| Elementsymbol | La | Ce | Nd | Pr | Dy | Sm | Er | Tm | U |
|---|---|---|---|---|---|---|---|---|---|
| Fullstendig navn | Lanthanum | Cerium | Neodym | Praseodym | Dysprosium | Samarium | Erbium | Thulium | Uran |
| Farge | Fargeløs | Gul | Blå | Grønn | Lys gul | Lys gul | Rosa | Lysegrønn | Sølvhvit |
Sjeldne jordartsmetaller har karakteristiske absorpsjonsspektre, som ofte danner unike fine linjer. For eksempel inneholder gul apatitt ofte det sjeldne jordartselementet Ce, med karakteristiske fine absorpsjonslinjer i det gule området. Uran gir imidlertid ikke en lysende gul farge, men kan danne distinkte absorpsjonsspektrallinjer. For eksempel kan mer enn ti absorpsjonslinjer forekomme i grønn zirkon i ulike fargesoner (figur 3-13).

Del III Farger produsert av krystalldefekter og fargesentre
I naturen deles mineraler inn i krystaller og ikke-krystaller basert på ulike grader av krystallisering. De fleste edelstener, som rubiner, safirer, diamanter, smaragder og kvarts, er krystaller, mens enkelte organiske edelstener, som rav og koraller, er ikke-krystallinske. Krystallstrukturer har en gitterlignende struktur, der de indre partiklene (atomer, ioner eller molekyler) er ordnet i et regelmessig periodisk mønster i et tredimensjonalt rom, og krystaller kan spontant danne polyedriske former. Ikke-krystaller er amorfe legemer med ikke-gitterlignende strukturer som ikke kan danne polyedriske former, for eksempel glass, kolofonium og harpiks.
Det mest typiske eksempelet på forskjellen mellom krystaller og amorfe faste stoffer er kvarts og glass. Naturlig kvarts er dannet av smeltet materiale SiO2 i magma som avkjøles i hulrom i jordskorpen. Det ytre laget av vanlige kvartskuler er agat, som ikke viser krystallformen, mens det indre laget har krystallformen til kvarts. De viktigste kjemiske bestanddelene i både glass og kvarts er SiO2kvarts er en krystall med silisium- og oksygenioner ordnet på en ordnet måte, mens glass er et amorft fast stoff med silisium- og oksygenioner ordnet kaotisk, uten regelmessighet, som vist i figur 3-14.
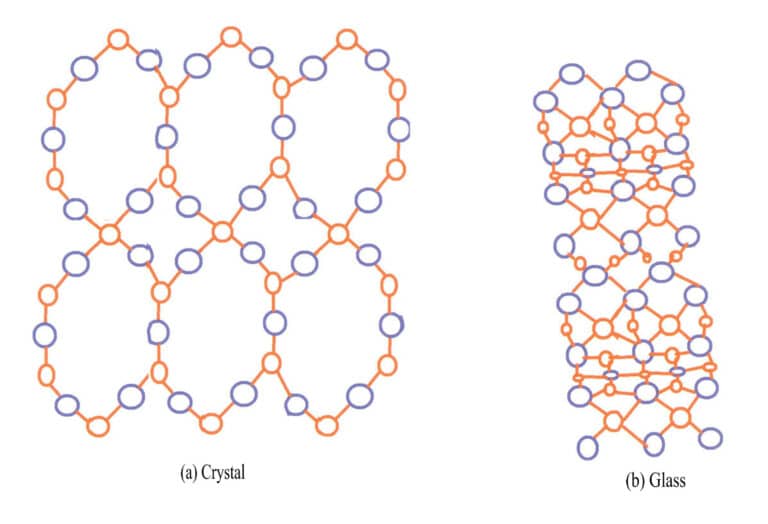
De fleste edelstenskrystaller er farget på grunn av urenhetsioner, for eksempel rubiner, smaragder og turmalin. Noen edelstener, selv om de mangler kromoforioner, er fargede på grunn av defekter i krystallstrukturen. Naturlige edelstener produsert i naturen kan endre farge på grunn av ytre forhold, som bestråling og ionisering, som endrer krystallstrukturen. Det vanligste eksemplet er røykkvarts, som utvikler farge på grunn av dannelsen av fargesentre fra strålingsinduserte vakanser. Kunstig bestrålt røykkvarts har et lignende dannelsesprinsipp som naturlig røykkvarts, bortsett fra at kunstig stråling skaper farge raskt.
1. Krystalldefekter og -typer
Fenomenet der partikkelarrangementet avviker fra gitterstrukturreglene (partikler gjennomgår periodisk translasjonsrepetisjon i tredimensjonalt rom) innenfor et lokalt område av edelstenens krystallstruktur kalles en gitterdefekt. Årsakene er knyttet til termiske vibrasjoner av partikler i edelstenkrystallen, ytre påkjenninger, høy temperatur og høyt trykk, bestråling, diffusjon, ioneimplantasjon og andre forhold.
For eksempel kan diamanter som krystalliseres i høytemperatur- og høytrykksmiljøet i den øvre mantelen når de raskt transporteres til nær jordoverflaten av vertsmagmaet (kimberlitt eller lamproitt), den raske endringen i temperatur- og trykkforhold og de gjensidige kollisjonene mellom krystallene og de omkringliggende bergartene lett føre til lokale endringer i strukturen til de påtrengende diamantkrystallene, noe som resulterer i gitterdefekter som endrer fargen på opprinnelig fargeløse diamanter, og danner brungule, brune og rosa diamanter.
Tilstedeværelsen av krystalldefekter har en betydelig innvirkning på krystallenes egenskaper. I virkeligheten har krystaller mer eller mindre defekter. En moderat mengde av visse punktdefekter kan forbedre halvledermaterialers ledningsevne og selvlysende materialers luminescens, noe som spiller en gunstig rolle. Derimot kan defekter som dislokasjoner gjøre materialene mer utsatt for brudd, noe som reduserer strekkfastheten til krystaller nesten uten gitterdefekter til en brøkdel av den.
I en ideell perfekt krystall er atomene strengt ordnet i et regelmessig, periodisk gitter på bestemte punkter i rommet. Under selve veksten og dannelsen av krystaller kan imidlertid krystallmorfologien etter vekst noen ganger avvike fra den ideelle krystallstrukturen, på grunn av påvirkning fra vekstmiljøer som temperatur, trykk og konsentrasjon av mediumkomponenter. Ethvert avvik fra den ideelle krystallstrukturen kan kalles en krystalldefekt. Krystalldefekter har stor innvirkning på krystallers fysiske og kjemiske egenskaper, og mange fagområder er relatert til krystalldefekter, som for eksempel ionisk doping i materialvitenskap. Fargen på edelstener er i stor grad relatert til krystalldefektene i dem. Dette er en av årsakene til fargen i edelstener - fargesentre.
Det finnes mange typer krystallstrukturdefekter, som kan klassifiseres i fire kategorier basert på omfanget av fordelingen i det tredimensjonale rommet: punktdefekter, linjedefekter, overflatedefekter og volumdefekter.
(1) Punktdefekter
Andre atomer erstatter noen atomer i en ideell krystall, noen dopes inn, eller det oppstår vakanser. Noen atomer i krystallen erstattes eller mangler på grunn av eksterne atomer, og disse endringene forstyrrer det periodiske arrangementet av krystallens regelmessige gitter, forårsaker endringer i partiklenes potensialfelt og resulterer i at krystallstrukturen er ufullstendig, begrenset til visse posisjoner, og påvirker bare noen få atomer i nærheten. Punktdefekter har minimal innvirkning på krystallen, og vanlige typer punktdefekter omfatter gitterposisjonsdefekter, sammensetningsdefekter og ladningsdefekter (figur 3-15).
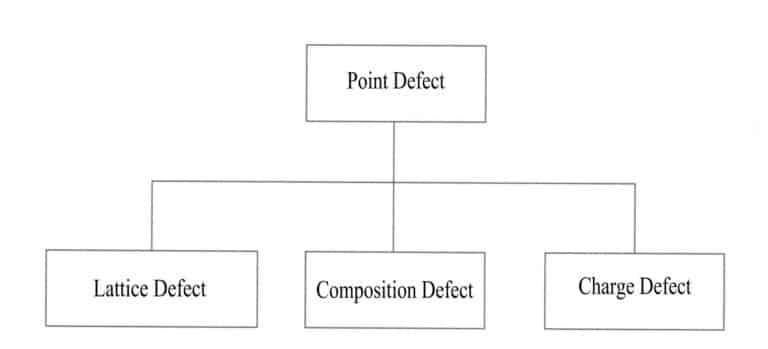
(2) Linjefeil
Linjedefekter er svært små i størrelse i to retninger og strekker seg hovedsakelig lenger i en annen retning. De er også kjent som endimensjonale defekter og består primært av ulike dislokasjoner. Dislokasjoner kan ses på som et produkt av lokal gitterglidning langs et bestemt atomplan. Glidningen trenger ikke gjennom hele gitteret, men krystalldefekten ender opp i gitteret, noe som fører til en uordnet ordning av partikler på grensen mellom den glidede og den uglidede delen av gitteret, kjent som dislokasjon. Denne grensen, skjæringslinjen mellom de glidede og ikke-glidede områdene, kalles dislokasjonslinjen. Det finnes to grunnleggende typer dislokasjoner: Når krystallen utsettes for trykkrefter, danner partikkelens glideplan en dislokasjonslinje med det uslipte planet, og dislokasjonslinjen er vinkelrett på glideretningen, kjent som kantdislokasjon, også kalt kiledislokasjon; på grunn av skjærspenning oppstår det glidning mellom planene, og de kryssende dislokasjonslinjene i den glidede delen av krystallen er parallelle med glideretningen, kjent som skruedislokasjon (figur 3-16).
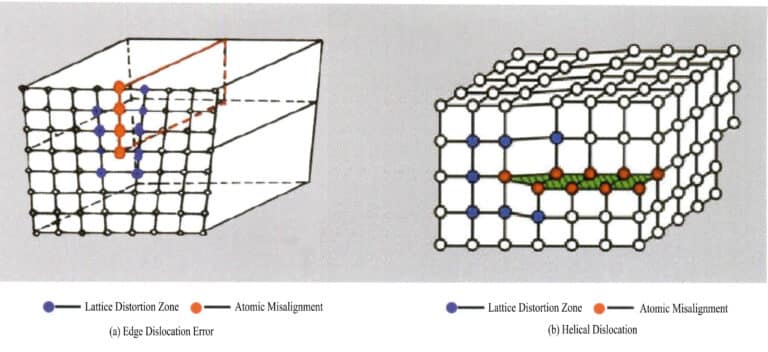
(3) Overflatedefekter
Den enkleste overflatefeilen er stablingsfeilen, som deles inn i indre stablingsfeil (der et krystallplan er fjernet) og ytre stablingsfeil (der et atomlag er satt inn i krystallet). Disse feilene oppstår innenfor et område på noen få atomavstander på hver side av et bestemt plan langs gitteret eller mellom kornene. De omfatter hovedsakelig stablingsfeil og grenseflater i og mellom krystaller, for eksempel korngrenser med små vinkler, domenevegger, tvillinggrenser og intergranulære grenser.
(4) Volumdefekter
Volumdefekter refererer til defekter som i varierende grad finnes i alle tre retninger, og som er tredimensjonale defekter, for eksempel innebygde sprekker, nettstrukturer, familiære strukturer, tvillinger og ulike edelsteninneslutninger.
2. Fargesentre i edelstener
Fargesentre er et spesialtilfelle av gitterdefekter, som vanligvis refererer til gitterdefekter i edelstener som selektivt kan absorbere synlig lysenergi og produsere farge, og som tilhører de mest typiske strukturelle fargetypene. I noen tilfeller kan de uparede elektronene som produserer farge, også forekomme i ioner som ikke er overgangselementer eller i krystalldefekter som dannes på grunn av mangel på elektroner, noe som er det fargesentre er. Punktdefekter i ioniske krystaller kan forårsake absorpsjon av synlig lys, noe som resulterer i at opprinnelig gjennomsiktige krystaller blir fargede. Denne typen punktdefekter som kan absorbere synlig lys, kalles vanligvis fargesentre. Mange typer naturlige edelstener produserer farge fra fargesentre, for eksempel lilla fluoritt, røykkrystall og grønne diamanter.
I optimaliseringsbehandlingsprosessen av edelstener kan noen naturlige og kunstige edelstener også ha fargesentre generert av stråling, for eksempel blå, gule, røde, grønne diamanter og blå topas som endrer farge på grunn av stråling, og blå topas, blant hvilke noen farger er relativt stabile og bare forsvinner når de varmes opp; noen farger er ustabile og kan falme selv ved romtemperatur. Denne typen fargeforårsakende fargesenter er nært knyttet til krystallstrukturen til edelstenen, for eksempel grønne diamanter, der årsaken til farge er tilstedeværelsen av vakanser i krystallstrukturen, men denne strukturelle defekten kan også fjernes ved bestråling, noe som gjør diamanten fargeløs. De vanligste typene fargesentre i edelstener er "elektronfargesentre" og "hullfargesentre".
(1) Elektronfargesenter (F-senter)
Elektronfargesentre er fargesentre som dannes når elektroner eksisterer i vakanser i krystalldefekter forårsaket av anioniske vakanser i edelstenens krystallstruktur. Når anionet er fraværende, blir vakansen en positivt ladet elektronfelle som fanger opp elektroner. Hvis en vakanse fanger opp et elektron og binder det til denne vakansen, blir elektronet eksitert og absorberer selektivt en bestemt bølgelengde energi for å bli farget. Et elektronfargesenter består derfor av en anionisk vakanse og et elektron som er bundet av det elektriske feltet til denne vakansen.
Lilla fluoritt er en farge som produseres av elektroniske fargesentre. Fluoritt (CaF2) tilhører det isometriske krystallsystemet, der hver Ca2+ koblet til to F– [Figur 3-17 (a)]. I noen tilfeller kan F– i fluoritten kan forlate sin normale posisjon. Det oppstår en vakanse ved den opprinnelige F– For å opprettholde krystallens elektriske nøytralitet må en negativt ladet enhet oppta denne ledige plassen. Et elektron fra et bestemt atom i krystallet blir den negativt ladede enheten som opptar denne ledige plassen [Figur 3-17 (b)]. Dette skaper et "fargesenter", kjent som et elektronisk fargesenter. I fluoritt absorberer elektroniske fargesentre synlig lys, noe som gir lilla.
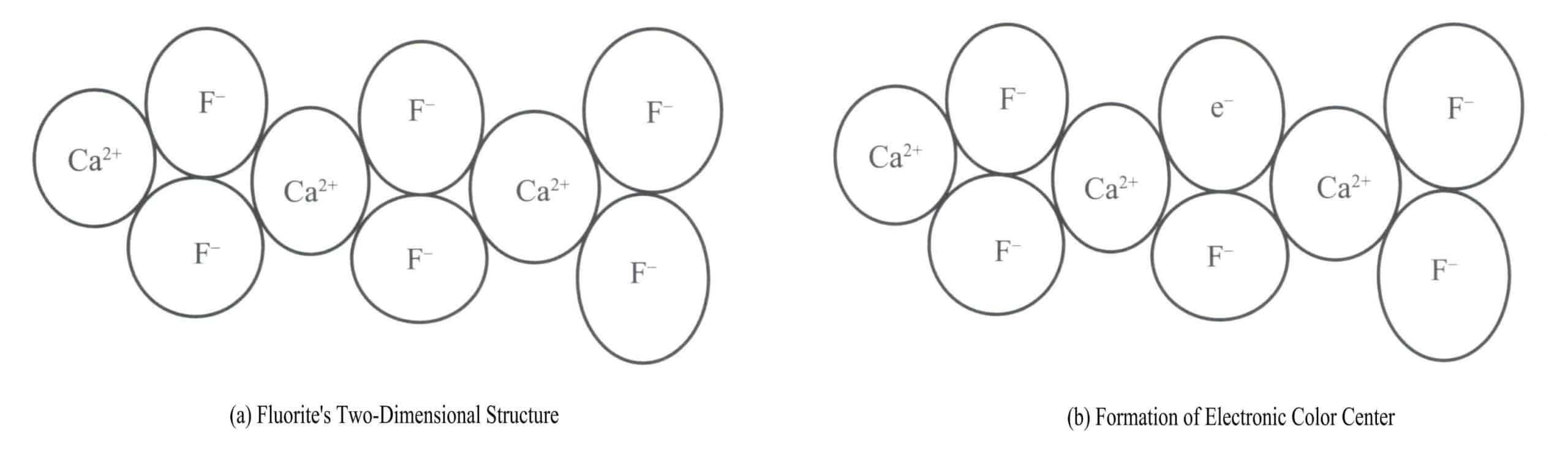
(2) Hullfargesentre (V-sentre)
Vakansefargesenteret dannes av eksterne faktorer, der kationer skaper elektronvakanser. Dette betyr at elektroner blir kastet ut fra sine opprinnelige posisjoner og etterlater seg et uparret elektron. Årsaken til fargen er at når det dannes kationvakanser i krystallen, for å oppnå ladningsbalanse, frigjør anionene i nærheten av kationvakansen elektroner under påvirkning av ekstern energi, og danner uparede elektroner som absorberer synlig lys og produserer farge. I for eksempel bestrålte diamanter og blå topas gir bestråling energi til å aktivere elektroner, noe som fører til at ioner eller atomer i gitteret forskyves, og dermed dannes strukturelle defekter og fargesentre på grunn av bestråling.
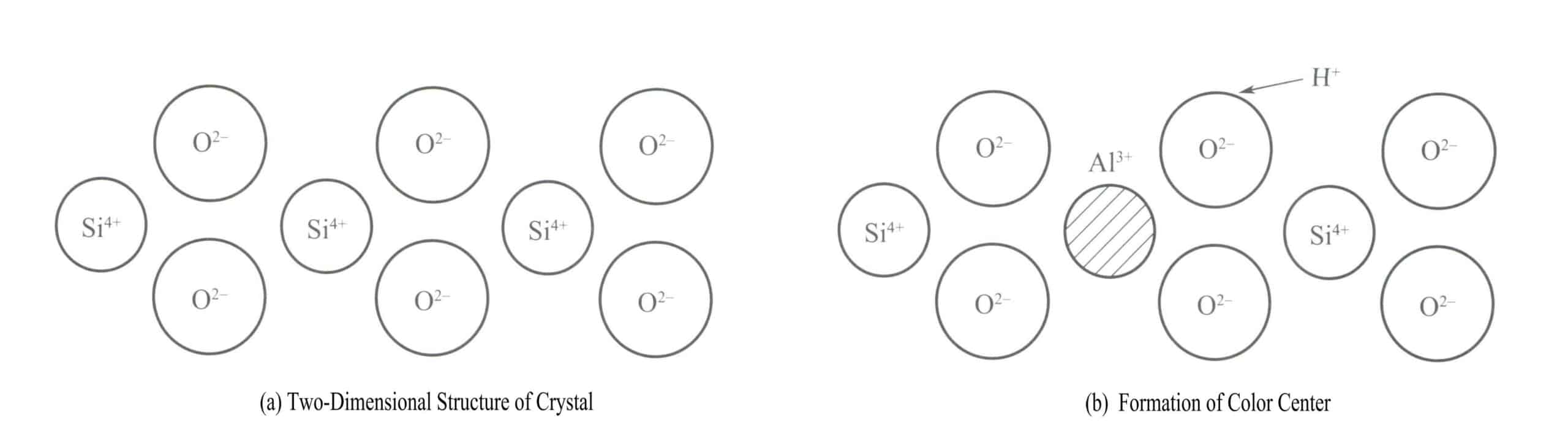
Et klassisk eksempel på et fargesenter i en krystall er fargen på røykkrystall. Krystallstrukturen til kvarts er et silisium-oksygen-tetraeder, med silisium i en firekoordinattilstand, som vist i det todimensjonale strukturdiagrammet i figur 3-18(a). Hver 10 000. Si4+ atomer har ett erstattet av Al3+, og når Al3+ erstatninger for Si4+ i krystallen, Al3+ må være omgitt av noen alkali-ioner (for eksempel Na+ eller H+) for å opprettholde elektrisk nøytralitet. Likevel befinner disse ionene seg ofte i en viss avstand fra Al3+.
Når kvarts bestråles med røntgenstråler, γ-stråler og andre strålekilder, vil energien til de tilstøtende oksygenatomene til Al3+ øker, slik at ett av elektronene i paret kan slynges ut fra sin normale posisjon. H+ vil fange opp dette elektronet og danne H . Høyenergetisk stråling fører til at O2- med flere valenselektroner til å frigjøre et elektron, og danner en [A1O4]4- vakansefargesenter, og [A1O4]4- atomklyngen absorberer synlig lys for å produsere farge, og danner røykkvarts.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ fanger opp elektroner og blir til H, som er fargeløst og ikke absorberer synlig lys. Hvis bestrålingsintensiteten er høy og det er nok Al3+ i krystallen, kan kvartsen bestråles til svart. Siden det ofte er en ledig plass der et elektron kastes ut, kalles denne typen fargesenter for et "vakansfargesenter".
I løpet av geologisk historie dannes naturlig røykfylt krystall for det meste gjennom langvarig lavdosestråling fra radioaktive materialer. Oppvarming kan eliminere fargen; når denne røykfylte krystallen varmes opp til rundt 400 °C, vil de utkastede elektronene gå tilbake til sine opprinnelige posisjoner, alle elektronene vil pares sammen, og kvartsen vil bli fargeløs igjen; hvis den bestråles igjen, kan den bli røykfylt igjen [Figur 3-18 (b)].
Ametyst har samme fargesenter for vakanse, men urenheten er jern i stedet for aluminium. Når urenheten Fe 3+ erstatter Si4+ i kvartsen skjer følgende endringer når den bestråles med høyenergistråler:
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
I likhet med dannelsesprinsippet for røykfylt krystall, gir det en lilla farge på grunn av dannelsen av [FeO4]4- hullfargen sentreres etter bestråling. Når denne ametysten varmes opp, blir den gul og blir sitrin, og ved ytterligere oppvarming blekner den til fargeløs. Generelt er oppvarmingstemperaturen relativt lav, rundt 400 ℃. Den lilla fargen på varmebehandlet ametyst kan gjenopprettes ved å bestråle fargesentrene igjen. Syntetisk ametyst syntetiseres også basert på dette prinsippet.
I noen edelstener kan noen få urenhetsatomklynger også danne fargesentre og utvise farge. For eksempel under veksten av beryll og under radioaktiv bestråling, kan miste et elektron for å bli , danner et rødgrønt absorpsjonsbånd som gir en blå farge. Det er mange fargesentre i diamanter, hvorav de fleste er forårsaket av dannelse av vakanser eller dislokasjoner i strukturen under ytre forhold, og fargene er generelt veldig stabile.
Det er relativt vanskelig å studere fargesenterindusert farge, og det krever ulike teknikker som spektroskopi og elektronparamagnetisk resonans. Tidligere forskning viser at noen typiske kjennetegn ved fargesenterindusert farge er relativt klare. Tabell 38 oppsummerer fargene og årsakene til fargesenterindusert farge i vanlige edelstener.
Tabell 3-8 Farger og årsaker til farge Sentrumsindusert farge i vanlige edelstener
| Typer edelstener | Farge | Årsak |
|---|---|---|
| Diamant | Grønn | Karbonledig GR1-fargesenter i diamant |
| Gul | Manglende struktur i N3-aggregater av diamant | |
| Oransje | Natoms og H3, H4 fargesenterdefekter | |
| Krystall | Røykfarge | Ledige stillinger generert av Al3+ erstatte Si4+ , relatert til stråling |
| Gul | Relatert til Al3+kan den også genereres av stråling | |
| Lilla | Fe3+ erstatter den ledige plassen som ble opprettet av Si4+ | |
| Edelstenen korund | Gul | Fargen er ustabil, årsaken til strukturelle defekter er ukjent |
| Topas | Blå | Fargen er stabil, årsaken til strukturelle defekter er ukjent |
| Gul | Fargen er stabil, årsaken til strukturelle defekter er ukjent | |
| Brunlig-rød | Fargen er ustabil, årsaken til strukturelle defekter er ukjent | |
| Turmalin | Rød | Relatert til Mn3+ kan også være forårsaket av stråling |
| Beryl | Blå | Relatert til CO32- kan også være forårsaket av bestråling |
| Fluoritt | Lilla | Elektronisk e- erstatter F- for å produsere |
Prinsippet med fargesentre brukes også til å forbedre fargen på naturlige edelstener i edelstensforbedring. De fleste metodene bruker bestråling for å endre fargen på edelstenene. Noen fargesentre er relativt stabile, mens noen edelsteinsvarianter blekner raskt, noe som gjør denne forbedringsmetoden mindre viktig for disse edelstenene. Tabell 3-9 viser noen farger som produseres av fargesentre, inkludert stabile fargesentre, ustabile fargesentre og farger som produseres av andre mulige faktorer.
Tabell 3-9 Farger produsert av fargesentre
| I utgangspunktet stabil i lys | Ametyst, fluoritt (purpurrød), bestrålte diamanter (grønn, gul, brun, svart, blå, rosa); noen naturlige eller bestrålte topaser (blå) |
|---|---|
| Falmer raskt i lys | Litium cesiumgrønn beryll (dypblå); noen bestrålte topaser (brun eller brunbrun); bestrålt safir (gul); ultrafiolett bestrålt lilla sodalitt (purpurrød) |
| Andre farger som fargesentre kan produsere | Sylvin (blå); halitt (blå eller gul); zirkon (brun); kalsitt (gul); barytt, celestin (blå); amazonitt (blå til grønn) |