Ce que vous devez savoir sur le plaquage or et les alliages d'or
Le guide ultime des techniques et solutions de plaquage or pour la joaillerie
Introduction :
Quels sont les différents types de solutions de dorure et leurs caractéristiques ? Comment utiliser divers composés d’or pour le plaquage ? Pourquoi choisir une dorure fine ou épaisse pour vos projets ? Ce guide complet aborde tous les aspects, des bases des solutions de dorure (avec ou sans acide, neutre ou sans cyanure) aux procédés détaillés de dorure fine et épaisse. Découvrez l’histoire et les techniques modernes utilisées dans le secteur, un guide idéal pour les bijoutiers, les créateurs et les détaillants souhaitant sublimer leurs produits avec des finitions dorées durables et esthétiques.
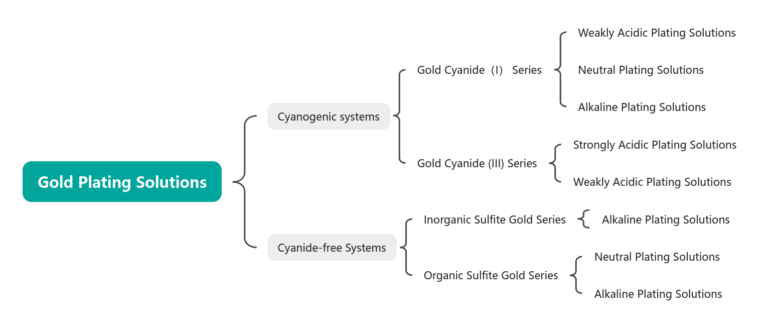
Classification des solutions de plaquage or
Table des matières
Section I Vue d'ensemble
En 1800, le professeur italien Luigi V. Broughatell inventa la technique de la dorure. Pendant plus d'un siècle, le nickelage, le cuivrage et le laiton électrolytiques furent largement répandus en Europe. Seules quelques manufactures réalisaient des dorures sur des montres, des bijoux et de la vaisselle en métal pour répondre aux besoins d'une clientèle fortunée. Aux États-Unis, en revanche, l'activité se concentrait principalement sur la dorure appliquée au traitement des pierres précieuses.
En 1913, Frary a mis au point un système de galvanoplastie à l'or relativement complet, faisant œuvre de pionnier dans le domaine de la galvanoplastie moderne.
En 1950, EC Rinker fut la première entreprise à développer une technologie de dorure brillante en ajoutant des traces d'argent aux solutions de dorure.
Par la suite, des solutions de dorure acides à base d'acides organiques ont été mises au point et largement utilisées.
En 1952, EA Parker a été le pionnier de l'application du cyanure d'or (I) de potassium et a signalé que l'ajout d'acides organiques faibles (tels que l'acide citrique, l'acide tartrique, etc.) aux solutions de placage de cyanure d'or (I) de potassium partiellement neutralisées avec des sels d'ammonium alcalins pouvait maintenir la solution de placage stable à pH=3.
En 1959, EC Rinker a divulgué une technologie de placage à l'or acide dans la gamme de pH 3~5.
Par la suite, la technologie de dépôt électrolytique d'or a fait l'objet de recherches plus approfondies et plus poussées, notamment sur les principes de dépôt et l'analyse des propriétés physico-chimiques.
Face à la demande croissante de production industrielle moderne, de nombreuses technologies de dorure appliquées ont mûri et sont devenues pratiques.
1. Types et caractéristiques des solutions de dorure
Tableau 1-1 Classification des solutions de dorure
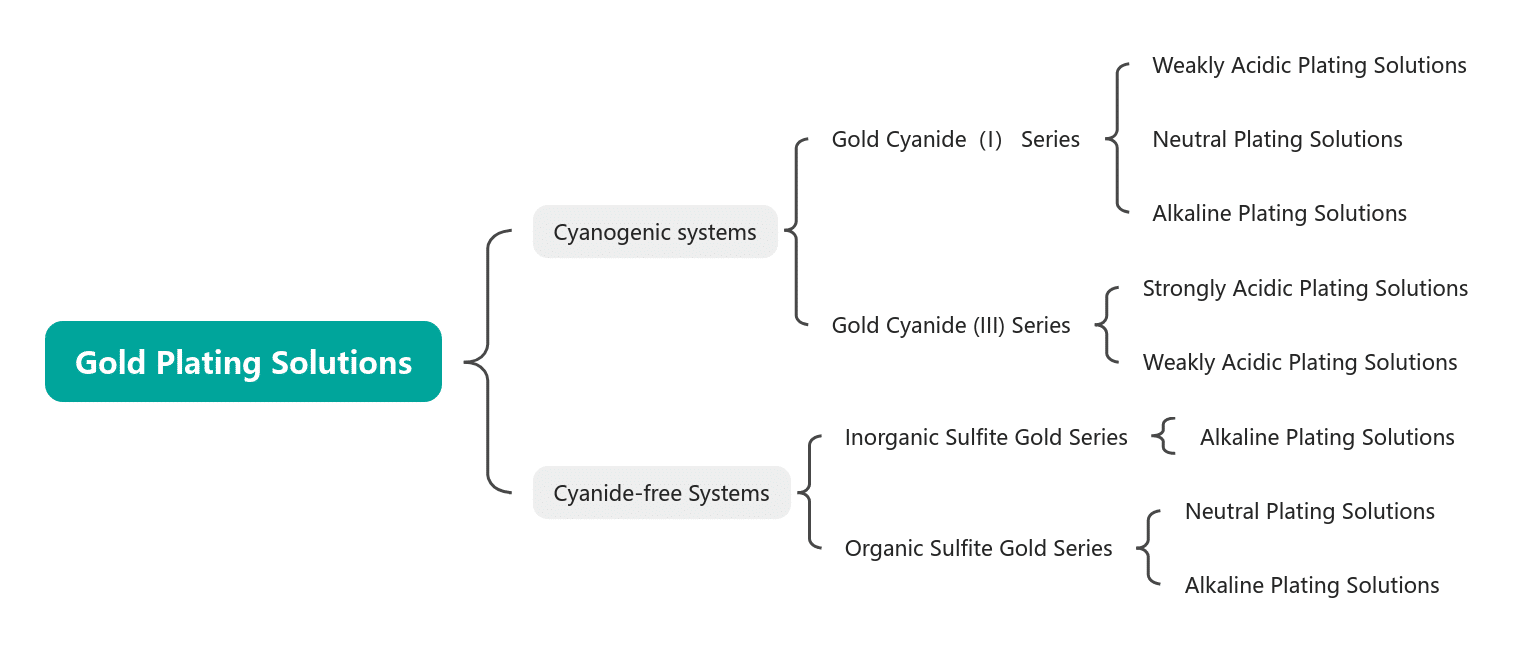
Tableau 1-2 Caractéristiques de différents types de solutions de dorure
| solution de galvanoplastie | Ligand d'or | Acidité et alcalinité | pH | Apparence | Appareil |
|---|---|---|---|---|---|
| Placage à l'or acide Placage à l'or dur | KAu(CN)2 | Faiblement acide | 3~5 | Brillant | Connecteurs, contacts, bornes, pièces décoratives |
| Placage or neutre Placage or doux Placage or pur | KAu(CN)2 | Neutre | 6~9 | Sans brillance | Carte de circuit imprimé, semi-conducteur |
| Placage or au cyanure | KAu(CN)2 | Alcalin | 10~13 | Brillant | parties décoratives |
| Placage or sans cyanure | Na3Au(SO3)2 | Neutre | 6〜8 | Sans brillance | Circuits imprimés dorés, cartes de circuits imprimés |
| Alcalin | 8~12 | Brillant |
2. Composés d'or utilisés pour la dorure
L'or possède de nombreux états de valence. Parmi ceux-ci, les composés à l'état d'oxydation +3 sont les plus stables, suivis des composés à l'état d'oxydation +2, tandis que les composés à l'état d'oxydation +5 se décomposent facilement. En solution aqueuse, l'or(I) présente plusieurs ligands stables, tels que les sels de coordination acides dihalogénoaurate(I), les sels de coordination dicyanoaurate, les sels acides thiosulfate d'or(I), etc. Parmi ces ligands, les cyanures sont particulièrement stables, avec une constante de stabilité K = 4 × 10⁻³.28. Par conséquent, les composés d'or(I) et d'or(III) sont les plus utilisés et les plus courants, tandis que les composés d'or(II) et d'or(V) sont également de plus en plus compris et appliqués.
À ce jour, le cyanure d'or(I) et de potassium est le sel principal le plus couramment utilisé pour la dorure. Ces dernières années, les solutions de placage au cyanure d'or(III) et au sulfite d'or(I) et de sodium sont de plus en plus employées.
1.1 Cyanure d'or(I) de potassium, KAu(CN)2 (ci-après dénommé cyanure d'or et de potassium)
(1) Moléculaire relative masse : 288,10. Les méthodes de préparation comprennent des méthodes chimiques et des méthodes d'électrolyse.
(2) Propriétés : Le cyanure d'or et de potassium ainsi préparé se présente sous forme de cristaux incolores, facilement solubles dans l'eau, légèrement solubles dans l'éthanol et insolubles dans l'acétone et l'hexadécanol. Il se décompose facilement par chauffage en milieu acide, est stable à la lumière à l'air et sa stabilité est nettement supérieure à celle des ligands cyanurés de cuivre et d'argent similaires.
(3) Méthodes de préparation
① Méthode chimique
a. Dissolution de l'or : Placer l'or pur dans de l'eau régale diluée (rapport volumique eau/eau régale de 1:4) et chauffer pour dissoudre → Une fois le bloc d'or complètement dissous, abaisser la température de manière appropriée → Ajouter à plusieurs reprises de l'acide chlorhydrique goutte à goutte jusqu'à ce qu'aucun dioxyde d'azote brun ne soit produit → Concentrer lentement jusqu'à ce que la solution devienne brun rougeâtre foncé, avec l'apparition d'une fine poudre d'or réduit brillante et roulante.
b. Réaction de neutralisation : Refroidir la solution à environ 25 °C. Sous agitation → ajouter goutte à goutte une solution saturée d'hydroxyde de sodium → jusqu'à la formation d'un semi-solide brun-rouge → ajouter du cyanure de potassium jusqu'à ce que la solution devienne incolore et transparente (avec un léger précipité de particules de poudre d'or agrégées).
c. Acidification (préparation du cyanure d'or) : Refroidir la solution à environ 25 °C → Sous agitation, ajouter de l'acide chlorhydrique goutte à goutte → jusqu'à la formation d'un précipité de cyanure d'or jaune vif → Agiter et laisser vieillir à basse température → Laisser reposer pour permettre la séparation des phases, refroidir naturellement à température ambiante, éliminer le liquide résiduel supérieur, le filtrer et laver le précipité jaune à l'eau chaude.
d. Synthèse du cyanure d'or et de potassium : Placer le cyanure d'or dans une petite quantité d'eau → Sous agitation, ajouter une quantité mesurée de solution saturée de cyanure de potassium → jusqu'à ce que la solution devienne incolore et transparente → Filtrer pour éliminer la poudre d'or → Concentrer → Refroidir pour cristalliser → Éliminer la liqueur mère → Sécher le cyanure d'or et de potassium cristallin blanc à 80 °C → Sceller et emballer.
Cette méthode de préparation du cyanure d'or et de potassium nécessite un équipement de production simple qui permet de séparer efficacement les impuretés à l'état de traces dans l'or afin de produire un cyanure d'or et de potassium de plus haute pureté.
② Électrolyse membranaire : Méthode : L’Union soviétique fut la première à utiliser l’électrolyse à membrane céramique microporeuse pour produire divers métaux et composés métalliques. Les entreprises nationales et étrangères utilisent généralement l’électrolyse à membrane organique pour produire du cyanure d’or et de potassium. Cependant, cette méthode d’électrolyse présente l’inconvénient de la corrosion des membranes organiques par les électrolytes alcalins, et les produits de corrosion endommagent considérablement les circuits intégrés de haute qualité, les cartes de circuits imprimés haute densité et les couches de plaquage or sur les contacts (la société Suzhou University Special Chemical Reagent Industrial Company a développé avec succès une application pratique).
1.2 Thiocyanate de potassium (III), K[Au(CN)4)]·H2O
(1) Masse moléculaire relative : 358.15.
(2) Propriétés : Cristaux incolores, facilement solubles dans l'eau, qui, chauffés à plus de 200 °C, deviennent un sel anhydre, fondent à une température incandescente et se décomposent à des températures plus élevées.
(3) Méthodes de préparation :
① Chauffer le cyanure d'or et de potassium dans une solution de cyanure de potassium ;
② Dissoudre le trichlorure d'or dans du K3[Fe(CN)6];
③ Dissoudre le dicyanure d'or(III) dans du K3[Fe(CN)6];
④ Traiter le cyanure d'or et de potassium avec du brome, et le K[Au(CN)] résultant2Br2réagit avec le cyanure de potassium dans le méthanol pour préparer le produit.
1.3 Chlorure d'or
(1) Chlorure d'or(I), AuCl
① Masse moléculaire relative : 232,46.
② Propriétés : cristaux jaune pâle non hygroscopiques qui commencent à se décomposer lentement lorsqu'ils sont chauffés au-dessus de 150 °C. Se décompose dans l'eau et l'éthanol et se dissout dans une solution chloralcaline pour former du dichlorate d'or.
③ Méthode de préparation : Chlorate d'or (HAuCl₄)4, III) est placé sous vide poussé et chauffé à 156℃ pour se décomposer et obtenir le produit.
(2) Chlorure d'or (III), HAuCl4
① Masse moléculaire relative : 303,37.
② Propriétés : Cristaux rouges aciculaires, point de fusion de 229 °C, point d'ébullition de 254 °C (décomposition), hygroscopiques, solution aqueuse brun rougeâtre, forme H2[AuCl3En solution acide, il se décompose lentement en solution aqueuse neutre, précipitant de l'or. L'évaporation de la solution aqueuse donne un sel dihydraté cristallin orange, soluble dans l'éthanol et l'éther.
③ Méthode de préparation : À une température comprise entre 225 et 250 °C, le chlore gazeux est passé à travers une poudre d'or de 120 à 127 kPa (900 à 950 mmHg) à préparer. Autre possibilité : dissoudre l’or dans de l’eau régale, ajouter à plusieurs reprises de l’acide chlorhydrique pour éliminer l’acide nitrique, puis chauffer lentement à basse température pour éliminer l’excès d’acide chlorhydrique, concentrer, refroidir et cristalliser pour obtenir le produit.
1.4 Oxyde d'or(III), Au2O3
(1) Masse moléculaire relative : 441,93.
(2) Propriétés : Poudre noire (brune) ou structure polymère cristalline, composé d’or entouré d’atomes d’oxygène formant un complexe tétracoordonné plan. Il se décompose lentement à la lumière du soleil, commence à libérer de l’oxygène lorsqu’il est chauffé à 110 °C, se transforme en oxyde d’or(I) à 160 °C et perd tout son oxygène à 250 °C, devenant un oxyde amphotère insoluble dans l’eau mais soluble dans l’acide chlorhydrique et les solutions aqueuses alcalines.
(3) Méthode de préparation : Dissoudre l'or dans l'eau régale, ajouter à plusieurs reprises de l'acide chlorhydrique et chauffer (5 fois) pour éliminer l'acide nitrique, ajouter du carbonate de sodium jusqu'à ce que le milieu soit alcalin pour produire un précipité, laver à l'eau, centrifuger, effectuer une électrodialyse pendant 2 semaines, puis sécher à 140~150℃ pour obtenir le produit.
Section II Placage or mince
L'électrodéposition d'une fine couche d'or, ou dépôt d'or par brossage, diffère du dépôt flash (ou dépôt par frappe) d'une couche d'or. La solution de dépôt par brossage est généralement à base de cyanure alcalin, et se décline en de nombreuses formulations, allant de l'or pur aux alliages, comme les solutions de cyanure d'or et de potassium avec différents systèmes de ligands. Certaines entreprises utilisent également leurs propres solutions de dépôt spécialement développées. Les solutions de dépôt flash sont majoritairement acides et peuvent servir de sous-couche pour des couches d'or plus épaisses. Elles utilisent des densités de courant plus élevées sur une courte durée pour déposer une fine couche d'or, améliorant ainsi la dispersion et l'adhérence de la couche d'or supérieure plus épaisse.
Le tableau 1-3 présente la composition et les conditions opératoires de quelques solutions représentatives de placage d'or mince au pinceau. Parmi celles-ci, le phosphate agit comme tampon et comme agent conducteur. Une solution de placage fraîchement préparée permet d'obtenir un bon revêtement, mais des impuretés se forment rapidement après électrification, ce qui provoque facilement des différences de couleur dans la couche plaquée. La principale cause est la décomposition du cyanure lorsque la température de la solution augmente. Par conséquent, la solution de placage doit être traitée après utilisation, généralement par filtration sur charbon actif.
Tableau 1-3 : Diverses solutions représentatives de placage à l’or mince au pinceau
| Composants | solution de plaquage en or pur | Couleur Hamilton | Blanc 1 | Blanc 2 | or verdâtre | Or rouge | ||
|---|---|---|---|---|---|---|---|---|
| Jaune | Rose | Vert | ||||||
| KAu (CN)2/(g/L) | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 1.23 ~ 2.0 | 0.41 | 0.33 | 2 | 0.82 |
| KCN libre/(g/L) | 7.5 | 7.5 | 2.0 | 2.0 | 15 | 15 | 7.5 | 4 |
| K2HPO4/(g/L) | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
| K2Ni(CN)4/(g/L) | - | 0.26 | 0.26 | 0.26 | 1.1 | - | - | 0.21 |
| K2Cu(CN)3/(g/L) | - | 0.13 | 1.1 | - | - | - | - | 2.64 |
| K2Ag(CN)2/(g/L) | - | - | - | 0.05 | - | - | 0.26 | - |
| K2Sn(OH)6/(g/L) | - | - | - | - | - | 2.11 | - | - |
| Température de la solution de placage /℃ | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 60 ~ 70 | 65 ~ 70 | 65 ~ 70 | 55 ~ 70 | 55 ~ 70 |
| Densité de courant (A/dm)2) | 1 ~ 4 | 1 ~ 3.5 | 2 ~ 5 | 1 ~ 4 | 3 ~ 6 | 3 ~ 5 | 1 ~ 3 | 3 ~ 4 |
Lors du dépôt électrolytique d'or pur, la présence d'autres métaux dans la solution de placage influence considérablement la couleur de la couche. Le cuivre confère à la couche une teinte rougeâtre, le nickel et le zinc une couleur blanche, tandis que le plomb favorise l'adhérence de substances noires, tachetées, rugueuses et gris-brun à sa surface. Par conséquent, l'ajout de divers métaux permet d'obtenir la couleur souhaitée pour les placages d'alliages d'or. Cependant, il est difficile d'obtenir la teinte idéale lors des procédés de dépôt électrolytique.
L'anode de la solution de dorure est généralement constituée de matériaux insolubles, tels que l'acier inoxydable et des plaques en treillis de platine-titane noir. Selon la solution de dorure, des plaques de carbone peuvent également être utilisées. Après consommation d'un certain courant, la solution de dorure doit être analysée régulièrement afin de rétablir la concentration en ions or, ligands et autres composants actifs. Un ampèremètre-heure permet d'automatiser les calculs et les ajouts aux opérations quotidiennes. Le procédé de dorure à l'or fin génère d'importantes pertes de solution, qui doivent être calculées au préalable afin de compenser ces pertes. Le déroulement du procédé de dorure à l'or fin est illustré à la figure 1-1.

Dans ce procédé, la concentration de la solution de dorure flash est environ 1/5 à 1/3 de celle de la solution de dorure principale (couche superficielle ou couche d'or supérieure). Une fois la surface de la pièce entièrement recouverte d'une couche d'or extrêmement fine, celle-ci est plongée dans la solution de dorure principale pour obtenir la teinte souhaitée.
Les résidus de cyanure présents à la surface de la couche de dorure peuvent former des taches d'eau, altérant l'aspect et les performances électriques du placage. Il est donc impératif de nettoyer et de sécher soigneusement les pièces après le plaquage or. Outre le séchage à chaud, certains produits spécifiques peuvent utiliser des solvants organiques pour la déshydratation. Par exemple, la déshydratation et le séchage à l'éthanol anhydre préservent la couleur de la couche de dorure et sont rapides.
La couche de dorure appliquée au pinceau est très fine et généralement inférieure à 0,1 µm. Divers films protecteurs organiques sont appliqués sur cette fine couche d'or lorsqu'elle est utilisée comme couche de placage de surface, afin de prévenir l'usure et la décoloration. La protection organique la plus couramment utilisée est une résine acrylique-mélamine, présentant une dureté de film équivalente à celle d'un crayon 3H-4H et une épaisseur de 10 à 15 µm. Le revêtement électrophorétique utilise souvent une résine acrylique-mélamine anionique.
Comme la fine couche de placage or se dépose rapidement et présente une couleur uniforme, le procédé de placage utilise généralement le mouvement de la cathode ou l'agitation par jet d'eau de la solution de placage. En contrôlant la température de la solution, la concentration en ions or et la densité de courant, on obtient des conditions optimales pour limiter les différences de couleur dans la couche de placage.
Section III Placage or épais
Tableau 1-4 Composition et conditions opératoires de la solution de placage et propriétés de la couche de placage
| Composé d'or | Types de galvanoplastie | sels conducteurs | Alliage métallique pH | Composition | Structure précipitée | Caractéristiques |
|---|---|---|---|---|---|---|
| Chlorure d'or de potassium | Acidité faible | Acide citrique, acide phosphorique d'origan, acide aminosulfonique, acide tartrique, acide oxalique | Or pur, cobalt, nickel, fer, indium, étain 3.0~5.0 | Acide citrique + citrate de sodium 80 à 100 g/L, cyanure d'or et de potassium 8 g/L, sulfamate de nickel 3,0 g/L, acétate de zinc 0,5 g/L | Structure en couches, avec un eutectique de polymère organique entre les couches | Il permet d'obtenir des précipités brillants et durs ; la solution de placage est facile à ajuster et le placage à basse température est possible. |
| Neutre | Acide phosphorique, acide sulfurique, acide borique, acides organiques | Or pur, précipité, modificateur de cristallisation : titane, sélénium 5,0 ~ 8,0 | Cyanure d'or et de potassium : 2 à 16 g/L ; citrate de potassium : 120 à 150 g/L ; phosphate de potassium : 10 à 50 g/L ; sulfate d'ammonium : 20 à 150 g/L ; un des éléments suivants : Ti, Ce, Te ou Bi : 0,01 à 40 mg | Cristaux colonnaires ou aciculaires, coprécipitation d'impuretés moins importante | Couche de placage en or pur 99,99% ; couche de placage précipitée, souple, semi-brillante ou mate ; l'accumulation d'impuretés affecte la durée de vie de la solution de placage. | |
| Alcalin | Cyanure, carbonate, acide pyrophorique | Or pur, argent, cadmium, zinc, antimoine 8,5 à 13,0 | Or pur, argent, cadmium, zinc, antimoine 8,5 à 13,0 | Joints de grains avec précipitation de polymères de cyanure | On peut obtenir une couche d'or épaisse et très uniforme d'environ 300 µm ; il est possible d'obtenir un placage d'or pur ou d'alliage 9K ; le procédé est insensible aux impuretés et la solution de placage est facile à manipuler. |
(1) Rôle des composés organiques de type polyéthylèneimine – polyamines de haut poids moléculaire : Les composés organiques sont adsorbés sélectivement au sein de la double couche électrique de Helmholtz, renforçant ainsi l’effet de polarisation. Lors de l’électrodéposition, les substances organiques s’adsorbent continuellement sur les sites de croissance actifs, inhibant le dépôt et la migration de l’or à la surface de la cathode et conférant à cette dernière une finition lisse et brillante. Cependant, la présence d’une certaine quantité de matière organique co-déposée dans le réseau cristallin des dépôts altère considérablement les propriétés physiques de la couche de placage, notamment sa résistance à l’usure. Généralement, l’ajout d’autres métaux permet d’atténuer les effets néfastes des substances organiques.
(2) Rôle d'autres semi-métaux tels que l'arsenic, le thallium, le sélénium et le plomb : L'ajout de semi-métaux permet non seulement d'obtenir une couche de dorure brillante à partir d'une solution de dorure au cyanure, mais aussi une couche de dorure très brillante à partir d'une solution de dorure au sulfite. Généralement, une quantité supplémentaire inférieure à 10-6 peut produire un effet caractéristique très évident.
Principe de brillance des semi-métaux : les substances semi-métalliques s'adsorbent uniformément sur la surface de la cathode, catalysent et favorisent la nucléation des cristaux d'or, génèrent davantage de points de croissance et favorisent une cristallisation et un dépôt uniformes.
(3) Rôle de l'eutectique des métaux de transition cobalt, nickel, fer, etc. : La couche de dorure brillante obtenue par alliage de cobalt et de nickel contient une certaine quantité de carbone. Si la teneur en carbone est inférieure à 0,11 TP3T, il est impossible d'obtenir une couche de dorure brillante, même en cas d'eutectique du cobalt.
Isotope 14Des expériences ont démontré que le carbone provient du ligand complexe cobalt-cyanure. La dissolution de la couche de placage or contenant du cobalt et du nickel dans une solution de placage acide avec de l'eau régale permet de séparer les substances carbonées. Au microscope, le matériau traité à l'eau régale présente un aspect plastique. Ce polymère membranaire induit une forte résistance de contact à la surface de la couche de placage.

1. Placage or alcalin
Parmi toutes les solutions de dorure, la solution de dorure au cyanure alcalin est la plus ancienne. Elle est largement utilisée pour le placage d'or pur, d'alliages d'or et pour la dorure décorative, ainsi que pour la dorure fonctionnelle de composants électroniques. Cette solution est généralement composée de cyanure d'or et de potassium, de cyanure libre, de carbonate de potassium, etc. Différents sels métalliques peuvent être ajoutés selon les besoins, notamment pour le placage d'alliages d'or.
Le placage à l'or par une solution alcaline de cyanure offre une excellente uniformité et mouillabilité du revêtement, et convient parfaitement aux alliages d'or à faible teneur en or. Il permet de déposer des couches d'or de valeurs K faibles à élevées. La solution de placage, riche en cyanure libre, est moins sensible aux impuretés. Le cyanure libre pouvant dissoudre l'or, les pièces plaquées doivent être nettoyées immédiatement après leur retrait du bain ; à défaut, les résidus de solution en surface peuvent engendrer des défauts, comme un aspect ondulé.
Les couches de placage or sans cyanure sont principalement utilisées pour les plaquettes de silicium, les circuits intégrés de commande des écrans à cristaux liquides, les plots de soudure en or pour le conditionnement, ainsi que les pistes de circuits, les bornes et autres points de contact avec le substrat. Sur les plaquettes de silicium recouvertes d'un film photosensible, la hauteur des plots de soudure en or est de plusieurs dizaines de micromètres et leur épaisseur de 15 à 20 µm. Les ions CN⁻ produits par la solution de placage or au cyanure peuvent corroder le film photosensible et le film protecteur autour du substrat ; c'est pourquoi on utilise majoritairement des solutions de placage sans cyanure et faiblement acides.
Les solutions de dorure alcalines sont principalement des solutions de dorure au cyanure, auxquelles s'ajoutent des métaux binaires ou ternaires ; les couches de placage en alliage d'or utilisées en pratique sont des alliages d'or binaires ou ternaires. Les compositions et conditions opératoires typiques des solutions de dorure alcalines sont présentées dans le tableau 1-5.
Tableau 1-5 Composition et conditions de fonctionnement de la solution de placage d'alliage d'or alcalin
| Types d'alliages | Composition et conditions de fonctionnement | |
|---|---|---|
| Alliages binaires | Alliage or-cuivre |
Cyanure d'or et de potassium 12 g/L Cyanure de potassium et de cuivre 7 g/L Thiocyanure de potassium 10 g/L Acide 2-pyridinecarboxylique 8 g/L pH 8 (ajusté avec du KOH) 70 °C, 0,4 A/dm2 |
| Alliage or-argent |
Cyanure d'or et de potassium 15 g/L Cyanure d'argent et de potassium 3 g/L Cyanure de potassium et de nickel 20 g/L Cyanure de cobalt et de potassium 10 g/L Cyanure de potassium 80 g/L Hydroxyde d'ammonium 20 g/L 15 °C, 0,6 A/dm2 |
|
| Alliage d'or et d'étain |
Cyanure d'or et de potassium 30 g/L Nitrate stanneux 7 g/L Pyrophosphate de potassium 100 g/L Température ambiante, 1 A/dm2 |
|
| Alliages ternaires | Alliage or-cuivre-cadmium |
Cyanure d'or et de potassium 15 g/L Cyanure de potassium et de cuivre 200 g/L Cyanure de potassium et de cadmium 5 g/L Acide L-glutamique 50 g/L 70℃, 1 A/dm2 pH 8 (ajusté avec du KOH) Au:Cu:Cd=70:15:15 |
1.1 Placage en alliage or-argent
Tableau 1-6 Composition de la solution de placage en alliage or-argent
| Composition et conditions de fonctionnement | Paramètres | Composition et conditions de fonctionnement | Paramètres |
|---|---|---|---|
| Chlorure d'or et de potassium (calculé en Au)/(g/L) | 8 | tensioactif | petite quantité |
| Chlorure d'argent et de potassium (calculé en Ag)/(g/L) | 2.5 | Température /℃ | 27 |
| Thiocyanate de potassium libre/(g/L) | 100 | Densité de courant (A/dm)2) | 1 |
| sel d'amine/(g/L) | 5 |

La concentration de cyanure de potassium libre ne doit pas être inférieure à 90 g/L ; généralement, une concentration supérieure à 100 g/L est plus appropriée. Au-delà de 120 g/L, la polarisation accrue freine le dépôt d'argent, augmente la vitesse de dépôt d'or et permet la formation d'une couche d'or de haute qualité.
La teneur en or est ajustée en fonction de la valeur K de l'alliage d'or en régulant les concentrations d'or et d'argent dans la solution de placage. Par exemple, lorsque la concentration d'argent est de 2,5 g/L dans la couche de placage, la concentration d'or doit être maintenue entre 7 et 10 g/L pour obtenir un plaqué or 18 carats.
Influence de la concentration en argent : lorsque la concentration en argent est faible, la plage de brillance de la couche de plaquage est large et la teneur en or est élevée.
Influence de la concentration en amine : L’ajout d’amine à une concentration de 30 g/L ne modifie pas la vitesse de dépôt d’or, mais augmente la brillance de la couche de placage par rapport à une solution sans ajout. À une concentration de 50 g/L, la vitesse de dépôt d’or augmente, provoquant un phénomène de « brûlure » dans les zones de forte densité de courant. L’ajout d’amine vise principalement à réduire les contraintes mécaniques dans les couches de placage d’or épaisses. L’ajout de ligands tels que la triéthylènetétramine (10 à 30 g/L) aux solutions de placage d’alliage or-argent brillant permet d’obtenir de meilleurs résultats.
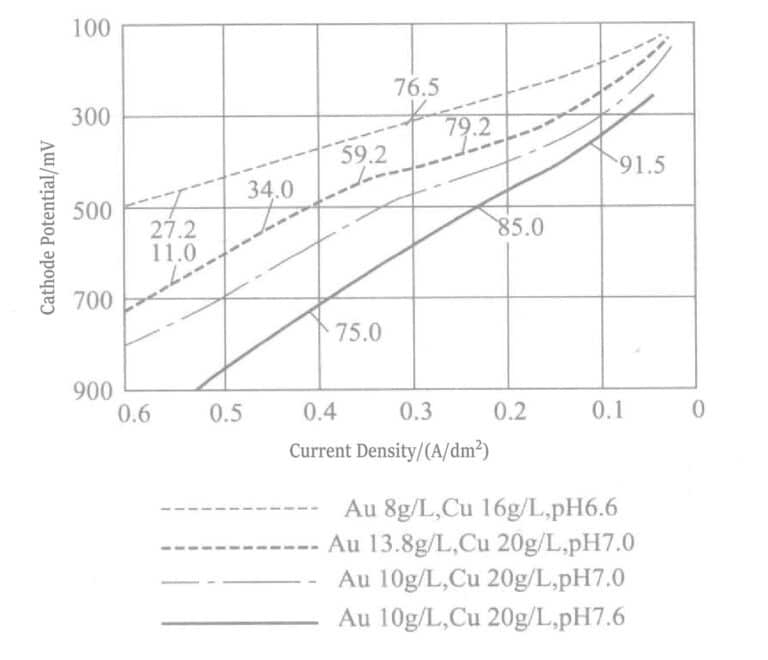
La figure 1-4 illustre la relation entre la température de la solution de placage, la densité de courant et la vitesse de dépôt d'or. La dureté de la couche d'or déposée est Hv.25170-210. État de surface et en coupe de la couche de placage or : après dépôt direct d’une couche d’or de 4 µm d’épaisseur sur la couche de nickel, la couche d’or détachée a été observée au microscope électronique à balayage. Les résultats, présentés dans les figures 1-5 et 1-6, montrent que la surface et la coupe de la couche de placage sont denses et exemptes de porosités. La cristallinité de la couche de placage or a été analysée par diffraction des rayons X après dépôt direct d’environ 10 µm d’or sur une plaque de cuivre. Aucun pic de la couche de cuivre sous-jacente n’a été détecté ; seuls les pics de la couche d’alliage or-argent ont été mesurés, indiquant une cristallisation selon le plan (111).
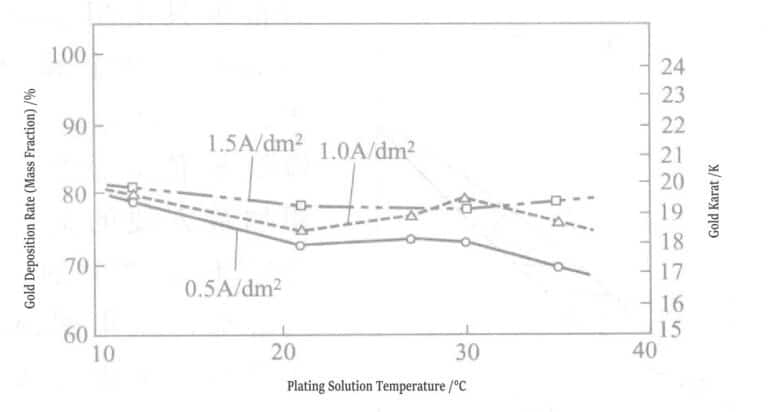

Figure 1-5 État de surface du placage en alliage or-argent

Figure 1-6 Structure organisationnelle des revêtements en alliage or-argent
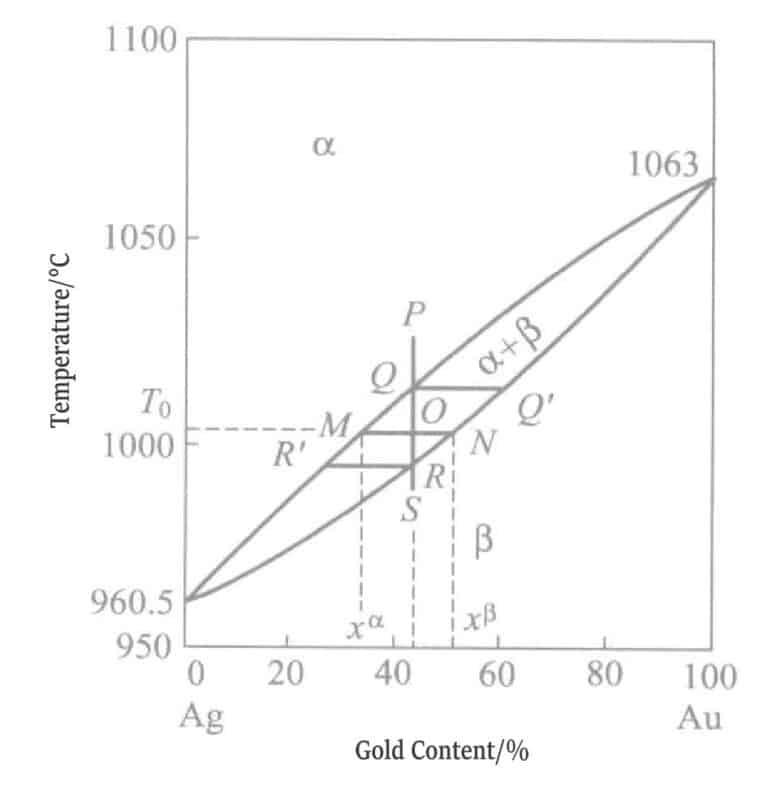
L'état des alliages or-argent est illustré sur la figure 1-7. Ces alliages forment une solution solide à rapport complet, et l'or comme l'argent possèdent une structure cubique à faces centrées (cfc), avec un rayon atomique de 1,44 Å (1 Å = 10⁻¹⁰ m).-10m). Par conséquent, le réseau ne subit aucune distorsion.
E. Raub a également mené des études de diffraction des rayons X sur des couches de plaquage or, confirmant que les alliages de la série or-argent ne forment qu'un seul type de solution solide et possèdent une excellente résistance à la corrosion.
EA Parker a indiqué que cette série d'alliages or-argent possède une excellente résistance à la corrosion et une excellente conductivité, qu'elle est très précieuse pour la fabrication de pièces d'équipements de communication, et que sa teinte or-vert unique et sa résistance à la corrosion la rendent appropriée comme couche de base pour un plaquage or épais.
1.2 Alliage de cuivre plaqué or
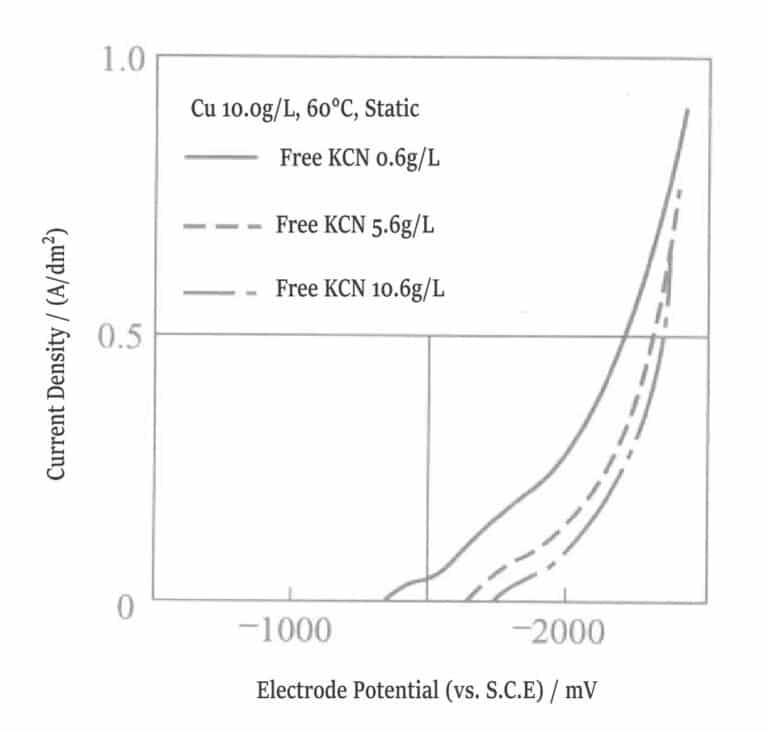
Figure 1-8 Courbe de polarisation de la solution de cuivrage
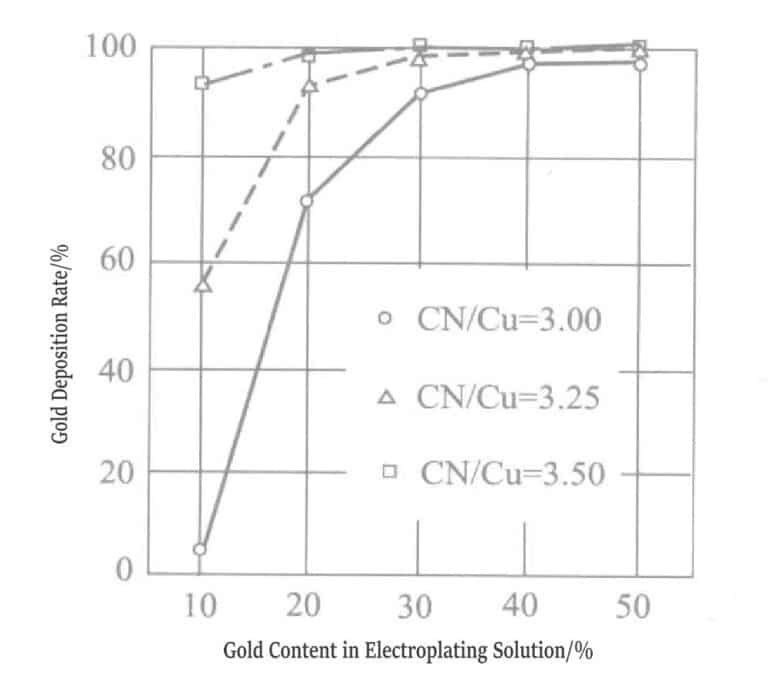
Figure 1-9 Variation des composants précipités dans la couche de placage en alliage or-argent
Tableau 1-7 Composition et conditions de fonctionnement de la solution de placage d'alliage
| Composition et conditions de fonctionnement | Paramètres | Composition et conditions de fonctionnement | Paramètres |
|---|---|---|---|
| KAu(CN)2/(g/L) | 7.5 ~ 9.0 | Na2SeO4/(g/L) | 0.5 |
| K2Cu(CN)2/(g/L) | 130 | Température de l'électrolyte/℃ | 60 |
| K2Cd(CN)4/(g/L) | 0.4 ~ 2 | Densité de courant (A/dm)2) | 0.75 |
| KCN/(g/L) | 15 |
L'ajout de sels de nickel à la solution de placage en alliage or-cuivre accroît la dureté de la couche de placage. Lorsque le pH de la solution est proche de l'acide, la quantité de nickel déposée augmente. La couche de placage contenant du cadmium présente une couleur proche de l'or rose, lui conférant un aspect décoratif très raffiné.
La couche de plaquage or 18 carats contenant du cadmium est une solution solide présentant une dureté, une limite d'élasticité et une résistance à la traction élevées, ainsi qu'une excellente résistance à la corrosion. Malheureusement, pour des raisons environnementales, l'utilisation de métaux tels que le cadmium est restreinte par les conventions de l'Organisation internationale de protection de l'environnement (OIP) et doit être strictement contrôlée afin de ne contenir que des traces. L'utilisation du cadmium est de plus en plus réglementée et se limite généralement à des ajustements de couleur très spécifiques, au plaquage d'alliages et à l'électroformage de couches d'or creuses de 200 à 300 µm, exclusivement lors du plaquage d'alliages or-cuivre-cadmium 18 carats.
2. Placage à l'or acide
La solution de dorure acide est stable à un pH d'environ 3 et permet le dépôt de nickel ou de cobalt qui ne s'électrolyse pas dans les solutions de dorure alcalines, formant ainsi des revêtements en alliage or-nickel ou or-cobalt. Les fins cristaux du revêtement ne se déforment pas, ne se déplacent pas et sont exempts de porosités, assurant une croissance stable à long terme.
Le revêtement déposé à partir d'une solution de placage acide présente un aspect brillant et est appelé solution de placage brillant. Ce revêtement possède une dureté élevée et est également connu sous le nom de solution de placage à l'or dur (Tableau 1-8). Les différents métaux ajoutés aux solutions de placage à base d'acide organique sont appelés agents de polissage des métaux.
Tableau 1-8 : Principaux composants et variations de la solution de placage d'or acide
| Composition et conditions de fonctionnement | Paramètres de référence | Conditions de la solution de placage |
|---|---|---|
| KAu(CN)2 (g/L) | 4 ~ 6 (calculé en Au) | Concentration élevée (environ 16 g/L), adaptée au plaquage or à grande vitesse. |
| Hydrate d'acide citrique (g/L) | 50 à 100 | Ajouter de l'acide citrique comme ligand pour le foret et comme tampon pour la solution de placage, ou ajouter d'autres ligands de cobalt. |
| CoSO4 • 7H2O/(g/L) | 0,1 à 3,0 (calculé comme Co) | Généralement, on ajoute du cobalt et on effectue un placage. On ajoute de l'acide sulfurique (calculé en équivalent Co) lors de l'alliage Au-Ni. |
| pH | 3,5 à 4,5 | L'efficacité du courant est élevée lorsque le pH est élevé, mais du brouillard est facilement généré. |
| Température/℃ | 30 à 40 | Une température élevée du liquide génère facilement de la brume. |
Tableau 1-9 Propriétés de la solution de placage d'or acide
| Effet de la valeur du pH | propriétés de la solution de placage | Application | |
|---|---|---|---|
| pH 3 | pH 3 ~ 5 | ||
|
① Alliages or-cobalt, or-nickel ② Le cobalt et le nickel sont très réactifs et précipitent davantage ; la surtension de dégagement d'hydrogène est faible, le rendement du courant augmente, le rendement du placage est faible |
① Alliage eutectique brillant et dur ; surtension de dégagement d'hydrogène élevée, rendement de courant faible, rendement de placage élevé ② Absence de cyanure libre dans la solution de placage ③ Lors de la précipitation de l'or à partir de KAu(CN)2, une partie de CN- Il se forme du HCN, qui se diffuse dans l'air et affecte l'environnement. |
① Aucun cyanure libre n'est présent lors de la précipitation de l'or à partir de KAu(CN).2, CN- formation de HCN ② Avec l'augmentation de la durée de l'électrodéposition, en raison de l'accumulation de K+, augmentation du pH de la solution de placage ③ La solution de placage est acide ; sur l’anode Pt/Ti, la surtension de dégagement d’hydrogène est élevée et les acides carboxyliques organiques, tels que l’acide citrique, subissent une réaction de Kolbe pour former des polymères visqueux. Par conséquent, une plaque d’anode de grande surface est nécessaire pour limiter cette réaction. |
① Galvanoplastie décorative ② Outre l'élimination du cobalt et du nickel, l'indium, le zinc et le fer peuvent également être ajoutés pour ajuster la couleur. |
En l'absence de cyanure libre dans la solution de placage, le cyanure d'or et de potassium dépose de l'or et des ions complexes de cyanure (CN₆⁻). – ) forme du HCN, qui pénètre dans l'atmosphère et se diffuse.
Dans les bains d'électrolyse, les plaques d'or sont rarement utilisées comme anodes ; on emploie généralement des plaques d'acier inoxydable ou de platine/titane. Dans les solutions de placage acides, la surtension d'oxydation de l'oxygène à l'anode est élevée, et les acides carboxyliques, comme l'acide citrique, ont tendance à subir des réactions de Kolbe à l'anode. Des méthodes telles que l'augmentation de la surface de l'anode permettent de prévenir la formation de dépôts polymères collants.
Le dépôt simultané de nickel et de cobalt accroît la dureté de la couche d'or dur cyanurée. Après brasage par refusion à 260 °C, la résistance de contact augmente fortement. L'ajout de composés aliphatiques, tels que l'éthanol, à la solution de placage permet de limiter les variations de résistance de contact après brasage par refusion et d'augmenter significativement la plage de densité de courant de la solution. Par exemple, lors du placage d'or sur des circuits imprimés flexibles (cuivre), l'ajout de composés mercapto permet d'inhiber la dissolution des nanotubes de cuivre et d'obtenir un placage d'or épais et stable sur le long terme.2.1 Placage en alliage or-cobalt
Le placage à l'or acide utilise généralement des solutions d'or à base d'acides organiques, notamment l'acide citrique et le citrate. Le cyanure d'or et de potassium, ligand présent dans la solution aqueuse d'acide organique, se dissocie pour libérer du cyanure, conférant à la solution un pH d'environ 3, faisant d'elle un bain d'électroplacage. Différents composants, tels que des ligands autres que l'acide citrique, sont ajoutés selon les besoins, notamment l'EDTA. Le bisulfate de sodium est utilisé comme agent d'ajustement du pH. Parmi les sels conducteurs, on trouve le phosphate monopotassique, le phosphate monoammonique, le pyrophosphate de sodium, etc. Les tampons utilisés comprennent le sulfate de potassium, le sulfate de sodium, etc. Conditions d'électroplacage : concentration en or de 1 à 8 g/L, densité de courant de 0,3 à 10 A/dm².2La température de la solution de placage est de 25 à 40 °C. Généralement, aucun phénomène indésirable, tel que le voile, ne se produit lors du dépôt d'une couche d'or épaisse. L'agent de brillance dans la solution de placage ne nécessite que l'ajout d'une petite quantité de métaux de transition ou de métalloïdes. Le cobalt et le nickel sont des exemples d'agents de brillance métalliques.
R. Duva et al. ont proposé la solution de plaquage à l'or du tableau 1-10 dans un brevet et ont déposé avec succès de nombreuses autres demandes de brevets pour le plaquage à l'or acide.
Tableau 1-10 Composition de solutions de dorure acides représentatives
| Composition et conditions de fonctionnement | 1 | 2 |
|---|---|---|
| Acide citrique + citrate de sodium / (g/L) | 80 | 80 |
| Or (cyanure d'or et de potassium) / (g/L) | 8 | 8 |
| Nickel (sulfate de nickel) / (g/L) | 3 | |
| Zinc (acétate de zinc) / (g/L) | 0.5 | |
| Indium (sulfate) / (g/L) | 5 | |
| Cobalt (sulfate) / (g/L) | 3 | |
| pH | 4〜5 | 3 à 4 |
| Température /℃ | 21 | 21 |
| Densité de courant (A/dm)1) | 1 | 1 |
| K① valeur | 23 | 21 |
① La norme nationale GB 11887-89 stipule que la teneur en or de 1K est de 4,166% (« K » est l’abréviation du mot anglais carat et du mot allemand karat).
21K = 21×4. 166% = 87. 486% (875‰)
L'or 24 carats est souvent appelé à tort or pur ou étiqueté « 1000‰ » alors qu'il a une teneur réelle en or de 99,99%, équivalent à 23,988K (les organisations internationales interdisent l'étiquetage « or pur », « or 9999 » et « or 24 carats »).
Il existe de nombreux points de vue sur le rôle du cobalt dans les solutions de placage. Eisenmann a analysé la teneur en potassium, cobalt, carbone, azote et autres éléments dans la couche de placage d'or et a constaté que le rapport de ces éléments correspond au rapport KCo[Au(CN)2]3 Il a donc été conclu que ce métal agit comme agent de blanchiment dans la solution de placage, plutôt que le cobalt seul. Dans cette solution, il se forme au sein de la double couche de Helmholtz et ne subit qu'une dissolution minimale dans les conditions de placage classiques. Après la formation du ligand, il présente un comportement électrochimique similaire à celui des agents de blanchiment organiques et est adsorbé cathodiquement. Ce métal de transition présente des effets de blanchiment sur une large gamme de pH, ce qui concorde avec le fait que le cobalt et d'autres métaux de transition ne présentent ces effets que dans les solutions de placage acides.
En théorie, le rapport potassium/cobalt/carbone/azote dans la couche de placage devrait être de 1:1:6:6, mais ces rapports varient considérablement. Le rapport potassium/cobalt oscille entre 1,0:0,4 et 1,0:5,5 selon les caractéristiques de la solution de placage et les paramètres opératoires ; le rapport cobalt/carbone varie entre 1:3 et 1:10, tandis que le rapport carbone/potassium reste globalement stable à 3:1.
Les résultats ci-dessus ne nient pas le fait que KCo[Au(CN)2]3 Le principal agent de blanchiment dans la solution de dorure est le cobalt, et des cas de cobalt, de CoOOH ou de cyanure de cobalt ont également été détectés simultanément dans cette solution. La formation de KCo[Au(CN)2]3 Ce phénomène peut également s'expliquer par plusieurs caractéristiques de la solution acide de dorure, notamment en considérant ce composé comme un simple intermédiaire du processus d'électrodéposition, d'autres réactions étant responsables du processus de brillance. En résumé, on pense que des facteurs tels que la réduction du potassium et du cobalt, les sels de ligands cyanure et la formation de polymères contribuent à la brillance de la couche d'or.
La composition de solutions de placage à l'or représentatives, brillantes, à faible contrainte et résistantes à l'usure, est présentée dans le tableau 1-11. Les hypothèses théoriques sont tout à fait cohérentes avec le comportement de la solution de placage à l'or, notamment en raison de la forte force de coordination du groupe de coordination du cobalt provenant du ligand KCo[Au(CN)₆].2]3 dissociation du ligand des ions cobalt, induisant la génération de KCo[Au(CN)2]3, la génération de l'apparition du rôle de l'éclaircissement. Lorsqu'il est ajouté sous forme de sel de cobalt d'EDTA, la quantité totale de cobalt de KCo[Au(CN)2]3 était de 6 g/L.
Tableau 1-11 Composition de solutions de plaquage or représentatives : brillantes, peu contraignantes et résistantes à l'usure
| Élément | Rapport massique/% | Rapport atomique /% | Élément | Rapport massique/% | Rapport atomique /% |
|---|---|---|---|---|---|
| K | 0. 26 | 1.3 | Co | 0.24 | 0.80 |
| C | 0.24 | 3.94 | Total | 1.00 | 9.70 |
| N | 0.26 | 3.66 |
Tous les électrolytes de dorure contiennent des ligands cyanure fortement coordinants (à l'exception du système à base de sulfite d'or). L'ion cyanocobalt [Co(CN)6–] est l'un des complexes de sel de coordination les plus stables connus parmi les ligands, et le sel de cyanure coordonné avec Co(III) est presque non toxique.
Si du cyanure libre est présent dans la solution de dorure acide, du HCN sera produit ; la concentration de cyanure libre doit donc être très faible. Cependant, si le pH augmente, la concentration de cyanure libre dans la solution de dorure augmente également. Lors de l’analyse du cobalt dans la solution de dorure, il est nécessaire de distinguer le cobalt inactif du cobalt actif, le premier étant le Co(III) et le second le Co(II).
Lors de la modification des conditions opératoires de la solution de placage, les aspects suivants doivent être pris en compte.
(1) Le pH a de nombreux effets sur la solution de placage.
À un pH élevé de 5,0, la concentration de cyanure libre augmente, favorisant la formation du sel de coordination cyanocobalt(III) et augmentant la solubilité de KCo[Au(CN)2]3Ce qui réduit la brillance de la couche de placage. L'apport de cobalt dans la double couche électrique de Helmholtz (figure 1-3) est influencé par la capacité de coordination des ligands, laquelle dépend du pH de la solution de placage. Lorsque le pH de la solution de placage augmente continuellement, les solutions de placage acides nécessitent l'ajout constant d'agents tampons.
À faible pH, les ions hydrogène se déchargent préférentiellement, ce qui entraîne une diminution du rendement de courant de la solution de placage.
(2) Température de la solution de placage : Lorsque la température de la solution de placage augmente, la solubilité de KCo[Au(CN)2]3 augmente et la brillance de la couche de placage diminue.
La température influe également sur la force de coordination. Lorsque la température de la solution de placage augmente, l'augmentation des concentrations en sels d'or et de cobalt permet de réduire efficacement cet effet.
(3) Placage à grande vitesse : Les solutions de placage à grande vitesse nécessitent des ajustements réguliers. Afin d'éviter une réduction locale de la concentration à la cathode (polarisation de concentration), les concentrations d'or et de cobalt doivent être maintenues en dessous de la limite supérieure. Pour la même raison, une agitation est nécessaire pour les solutions à forte concentration, et une agitation par jet d'air est utilisée lors du placage à haute densité de courant. Les températures élevées peuvent renforcer l'effet d'agitation. La principale caractéristique du placage à grande vitesse est la forte densité de courant à l'anode et à la cathode. Les agents de brillance à base de métaux de transition offrent des performances optimales sous une forte densité de courant aux deux électrodes. Cependant, les situations suivantes doivent être prises en compte :
① Le pH de la solution de placage augmente rapidement.
② Co3+ est généré rapidement.
③ Les sels de coordination du cyanure de cobalt(III) se forment facilement.
④ Les ligands organiques favorisent l'oxydation de la solution de placage.
Au fil des années, de nombreuses solutions de placage contenant des additifs organiques ont été développées pour augmenter la plage de densité de courant des solutions de placage d'alliages cobalt-or et nickel-or, permettant un placage à grande vitesse à des concentrations plus faibles.
(4) Rendement actuel : Le rendement de courant est le rapport (%) entre le courant consommé lors du processus de dorure proprement dit et le courant total utilisé. D'autres réactions de réduction consomment le courant restant.
Utilisation de Co3+ + e– =Co2+Du point de vue de la consommation actuelle, on peut comprendre que la génération et l'adsorption de KCo[Au(CN)2]3 effets de polarisation accrus, favorisant la décharge d'hydrogène.
Conditions importantes qui favorisent la génération de KCo[Au(CN)2]3, comme une faible valeur de pH, une concentration élevée de Co libre2+et la basse température de la solution de placage, réduisent l'efficacité du courant.
L'utilisation de ligands appropriés permet de réguler la concentration effective de cobalt et la génération de KCo[Au(CN)2]3, ce qui permet d'obtenir une couche de placage brillante et une efficacité de courant optimale.
(5) Ajout de métaux, c'est-à-dire les agents de brillance pour métaux, entravent la génération de KCo[Au(CN)2]3; par exemple, le plomb entrave la formation d'azurants optiques par adsorption, réduisant ainsi l'efficacité du courant.
(6) Remuer : Comparativement aux solutions de placage d'autres métaux, en raison des stocks de matières premières en or, du prix et d'autres facteurs de coûts, et du fait que la majeure partie du courant dans le processus de placage est consommée par le transfert d'électrons dans des sels conducteurs à haute concentration, les solutions de placage utilisent généralement la concentration la plus faible possible.
Au(CN)2– n'est pas attiré par la cathode lors de l'électrophorèse et est fourni à la double couche de Helmholtz (Figure 1-3) par diffusion ; par conséquent, l'agitation est une condition importante pour fournir le sel de coordination d'or et les agents de brillance à la cathode.
L'agitation peut améliorer l'efficacité du courant, mais elle augmentera encore davantage cette efficacité dans les zones à forte densité de courant, ce qui détériorera l'uniformité de la couche de placage.
Grâce aux progrès des techniques de dépôt de couches minces, le problème de la mauvaise dispersion de la couche de placage s'est progressivement atténué. Actuellement, l'utilisation d'additifs est courante pour élargir la plage de densité de courant et ainsi améliorer l'uniformité du placage.
Copywrite @ Sobling.Jewelry - Fabricant de bijoux sur mesure, usine de bijoux OEM et ODM
2.2 Placage en alliage or-nickel

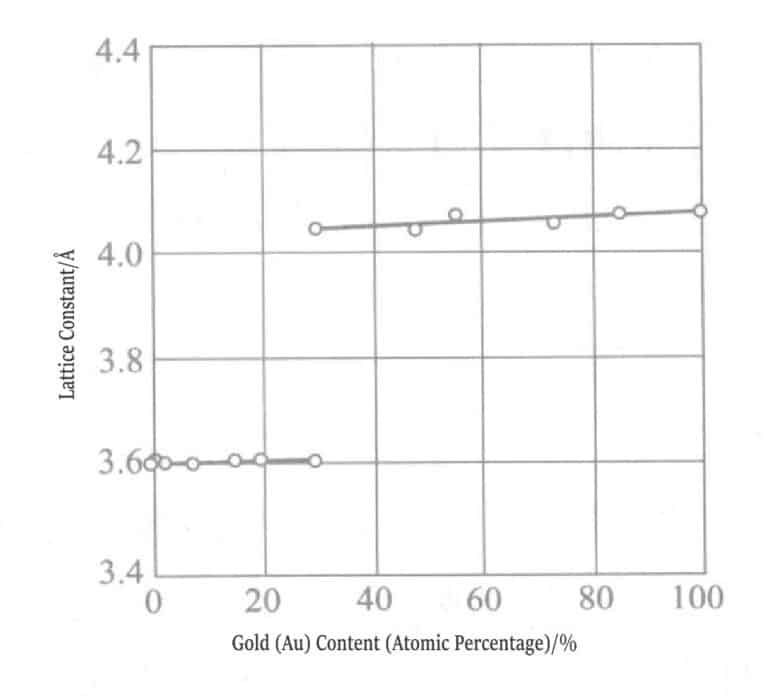
Figure 1-11 Teneur en nickel et constante de réseau du revêtement en alliage or-nickel

Figure 1-12 Teneur en nickel et constante de réseau du revêtement en alliage or-nickel
La relation entre la teneur en nickel et le paramètre de maille dans les solutions de placage alcalines et acides pour les couches électrodéposées d'alliage or-nickel a été mesurée. Le nickel forme une solution solide avec l'or à une teneur maximale de 5%, et au-delà de 5%, il précipite sous forme de mélange simple.
Des tests comparatifs ont également été menés sur des couches de placage en alliage or-nickel et en alliage or-cobalt. Les résultats ont montré que les propriétés des deux alliages d'or diffèrent significativement. Les figures 1-13 et 1-14 illustrent que les teneurs en carbone, cobalt et nickel des alliages d'or de même composition varient en fonction de la température du bain de placage. La teneur en cobalt diminue lorsque la température du bain augmente, et les courbes de carbone et de cobalt sont parallèles ; le rapport molaire carbone/cobalt est donc approximativement constant à 4.
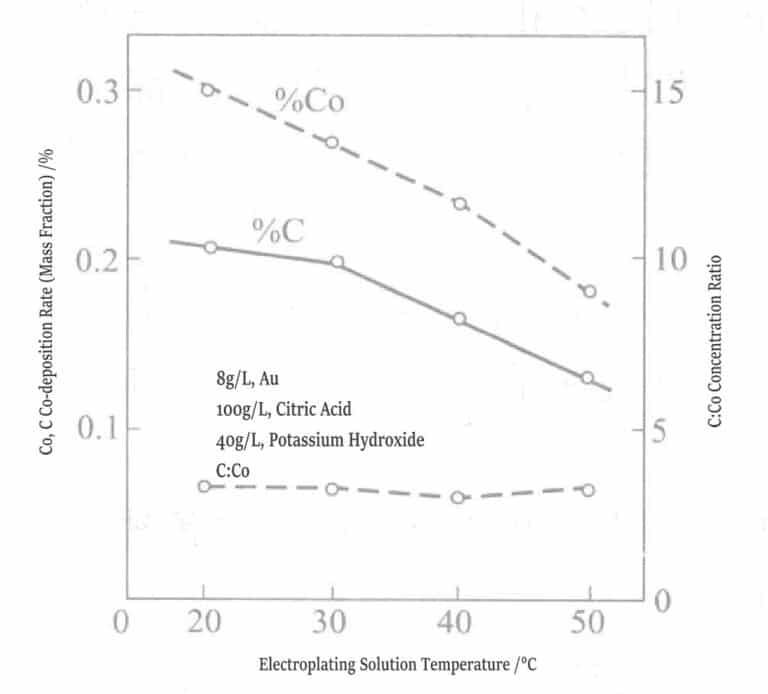
Figure 1-13 Relation entre la température de la solution de placage et le taux de codéposition du cobalt et du carbone
(0,5 g/L, pH 3,5, 1 A/dm³)2 )
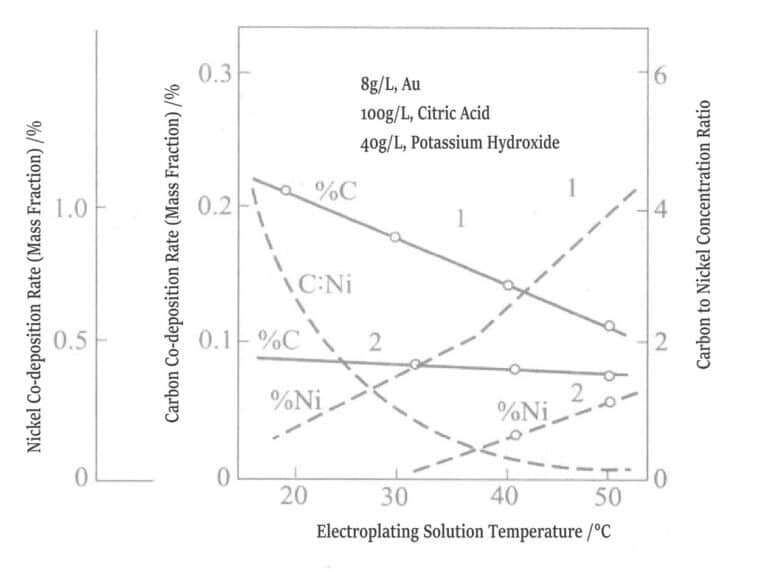
Figure 1-14 Relation entre la température de la solution de placage et la codéposition de nickel et de carbone
1-0,5 g/L, pH 3,5, 1 A/dm³2 ; 2-0,5 g/L, Ni, pH 4,5, 1 A/dm2
La figure 1-15 illustre l'influence du pH sur le co-dépôt de nickel. Lorsque le pH est supérieur à 4,5, le co-dépôt de nickel dans la couche de placage est nul, tandis qu'en dessous de pH 4,5, la couche de placage est brillante.
Lorsque d'autres impuretés sont mélangées à la couche de dorure, la contrainte de traction de cette dernière augmente. La figure 1-16 illustre la relation entre la température de la solution de placage en alliage or-nickel et la valeur de la contrainte au sein de la couche de placage.
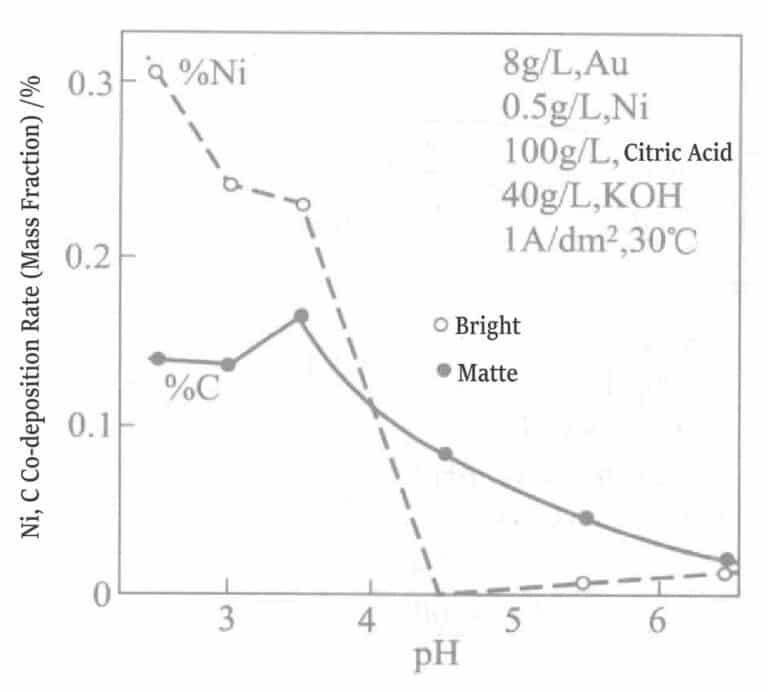
Figure 1-15 Effet du pH sur le taux de codéposition du nickel et du carbone
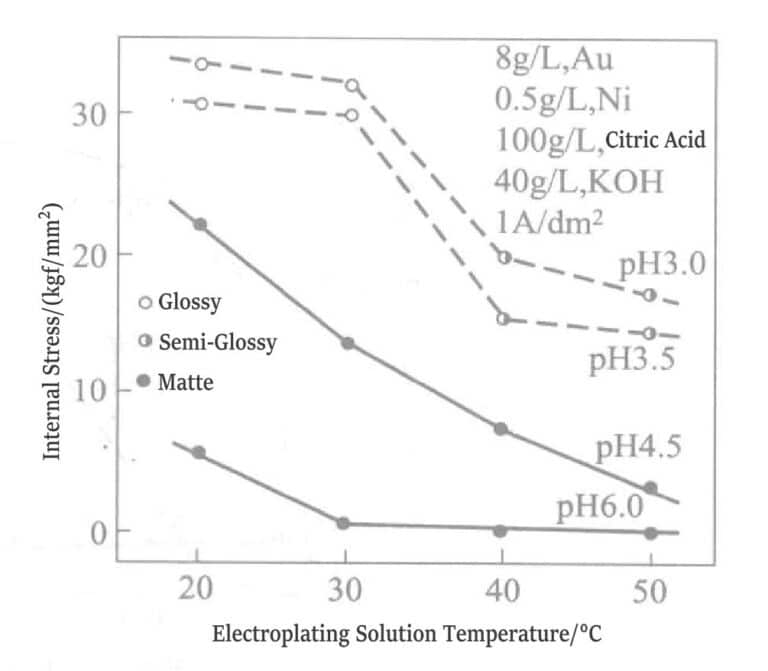
Figure 1-16 Relation entre la contrainte interne, le pH et la température de la solution de placage (1 kgf/mm²)2 =980,665Pa)
L'épaisseur croissante des couches de placage or favorise l'apparition de fissures. La résistance à la traction de la couche de placage en alliage or-nickel est illustrée par la figure 1-17. Cette résistance est fortement influencée par l'épaisseur, et une couche de placage de qualité, exempte de fissures, ne peut être obtenue que jusqu'à une épaisseur de 2 à 3 µm.
Lorsque le pH est inférieur à 5, la solution de placage peut générer des ligands. Actuellement, la force de liaison entre le citrate et le nickel (Ni)2+ ) est plus fort que celui du cyanure. Les figures 1 à 18 illustrent les différentes conditions de la solution de placage. Si le nickel est ajouté sous forme de K2Ni(CN)4La teneur en carbone de la couche de placage augmente fortement. La teneur en nickel de cette couche croît à partir d'une concentration supérieure à 0,3 g/L dans la solution de placage. Lorsque la concentration en nickel est inférieure à 0,3 g/L, la couche de placage est mate ; au-delà de 0,3 g/L, elle devient brillante. Cependant, l'ajout de nickel sous forme de sulfate de nickel à la solution de placage permet d'obtenir un effet brillant même à une concentration inférieure à 0,3 g/L. Ceci s'explique par le fait que le nickel a déjà subi une codéposition à une certaine concentration.

Figure 1-17 la relation entre l'épaisseur du plaquage or et la résistance à la traction.
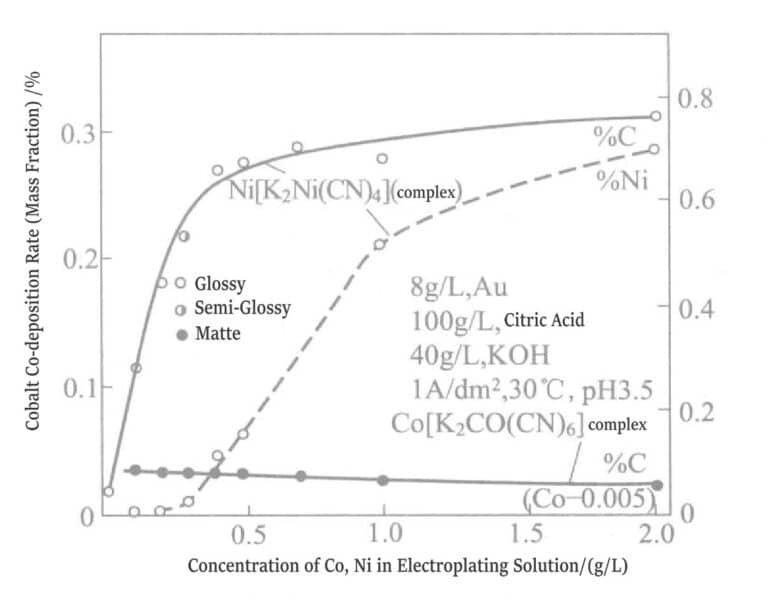
Figure 1-18 Effet des ions complexes sur les concentrations de cobalt et de nickel dans la solution de placage et les taux de codéposition du cobalt, du nickel et du carbone.
(1) Composition et conditions de fonctionnement de la solution de placage : La couleur de la couche de placage est essentielle pour un plaquage or décoratif. Dans les solutions de plaquage à base d'acides organiques, les principaux composants utilisés sont les suivants : sels d'or, acides organiques, sels de nickel, agents de brillance et agents de relaxation des contraintes. Parmi les sels d'or, on trouve le cyanure d'or et de potassium. Les acides organiques comprennent l'acide citrique, l'acide hydroxybutanedioïque et l'acide tartrique. Les sels de nickel incluent les sels de nickel de l'acide amidosulfonique, de l'acide citrique, de l'acide sulfurique, de l'acide gluconique, de l'acide formique, de l'acide borique, de l'acide phosphorique, etc. Les agents de brillance (métaux) comprennent l'indium, le cobalt, le zinc, le cadmium, l'antimoine, etc.
Les substances anti-stress comprennent le magnésium, le calcium, l'α-bipyridine, le sulfonate d'alkylbenzène de sodium, la triéthylènetétramine, le sulfate d'hydrazine, l'acide amidosulfonique, etc.
(2) Facteurs affectant la couleur des couches de placage en alliage or-nickel : Le tableau 1-12 répertorie deux types de solutions de placage : couleurs de la couche de placage, stabilité de la solution de placage, propriétés physiques, etc.
① Effet du citrate de nickel : La concentration de citrate de nickel, exprimée en équivalent nickel dans la solution de placage, varie de 15 g/L à 30 g/L, influençant ainsi la couleur de la couche de placage or. À une concentration de 15 g/L, la couche est d'un jaune doré brillant ; entre 20 et 30 g/L, la couleur reste inchangée. L'ajout de 1 g/L de cobalt sous forme de sulfate de cobalt ne modifie pas la couleur, mais augmente la brillance de la couche. Enfin, la température de la solution de placage est testée à 35 °C, 40 °C, 45 °C et 55 °C, sans modification de la couleur de la couche.
Tableau 1-12 Composition et conditions de fonctionnement de deux solutions de plaquage or-nickel
| Composition et conditions de fonctionnement | Solution de nickelage à l'acide citrique | solution de placage au sulfamate de nickel |
|---|---|---|
| Acide citrique /(g/L) | 150 | 150 |
| Citrate de potassium /(g/L) | 100 | 100 |
| sulfamate de nickel (sous forme de Ni)/(g/L) | 15 | |
| Acide citrique nickel (sous forme de Ni)/(g/L) | 25 | |
| Sulfate de cobalt (sous forme de Co)/(g/L) | 1 | 0.5 |
| Cyanure d'or et de potassium (sous forme d'Au) /(g/L) | 2 | 2 |
| Cyanure de potassium KCN/(g/L) | 1 | 1 |
| pH | 4.2 | 4.2 |
| Température /℃ | 40 | 40 |
2. Effet de l'aminosulfonate de nickel : Dans la solution de placage, la concentration d'aminosulfonate de nickel est de 5 g/L, 10 g/L, 15 g/L et 20 g/L (exprimée en nickel). L'ajout de 0,5 g/L de cobalt (sulfate de cobalt) et de 2,5 g/L d'or (cyanure d'or et de potassium) modifie sensiblement la couleur du dépôt. À une concentration de nickel de 5 g/L, le dépôt est jaune doré vif ; à 10 g/L, il est or clair. En comparant les dépôts obtenus avec les deux sels de nickel, celui obtenu avec la solution de citrate de nickel est d'un jaune doré vif. En revanche, celui obtenu avec la solution d'aminosulfonate de nickel est légèrement noirâtre.
③ Effet du sulfate de nickel : Après une certaine période, la solution de placage au sulfate de nickel produit un précipité d'hydroxyde de nickel et devient impropre à l'utilisation.
④ Rendement du courant : La relation entre la densité de courant et le rendement du courant pour les deux solutions de placage est illustrée à la figure 1-19. Lorsque la densité de courant est de 0,5 A/dm²2, 1,0 A/dm2, 1,5 A/dm2, il n'y a pas de différence entre la solution de nickelage au citrate et la solution de nickelage à l'acide aminosulfonique, et les deux ont une efficacité de courant de 22%~23%.
⑤ Rapport de dépôt d'or : La teneur en or dans la couche de placage de la solution de nickelage au citrate est supérieure à celle de la couche de placage de la solution de nickelage à l'acide aminosulfonique de 1%~3% (fraction massique) (Figure 1-20).
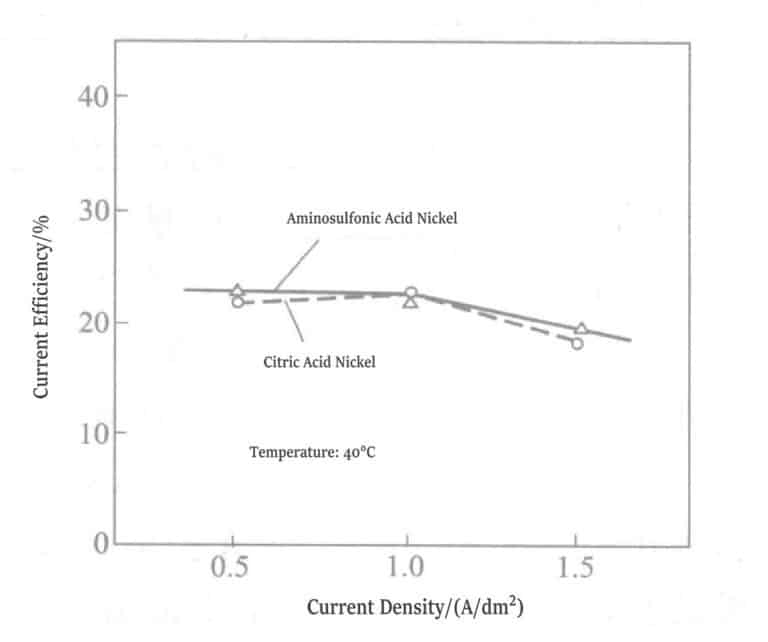
Figure 1-19 Relation entre la densité de courant et le rendement du courant
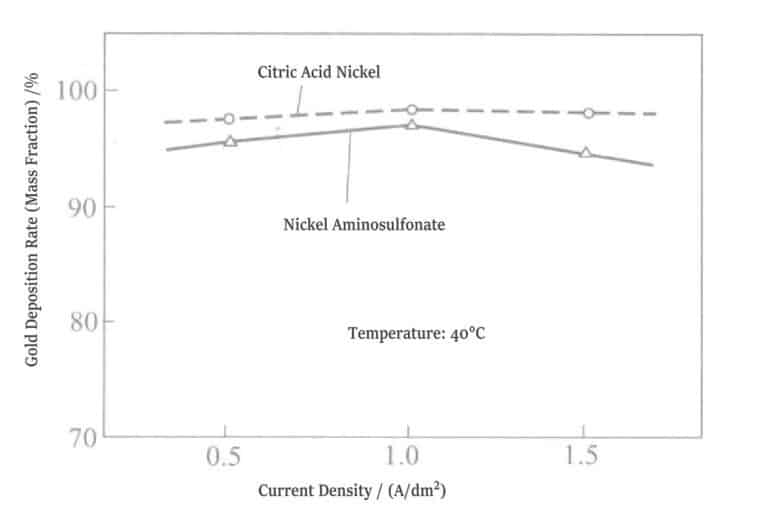
Figure 1-20 Relation entre le sel de nickel et le rapport de dépôt d'or
Tableau 1-13 Dureté des sections transversales de deux types de couches de placage
| Type | Charger/gf① | Dureté Hv |
|---|---|---|
| solution de placage au citrate de nickel | 25,50 | 280 ~ 310 |
| solution de placage à l'acide sulfamique de nickel | 25,50 | 210 ~ 240 |
| ① lgf=9,80665×10-3N。 | ||
L'état de surface de deux couches de placage d'une épaisseur de 50 µm est exempt de fissures, lisse et semi-brillant. Lorsque la teneur en nickel (fraction massique) de la couche de placage en alliage or-nickel est d'environ 5%, la dureté est généralement d'environ 200 HV. En raison de l'épaisseur importante de la couche de placage, des contraintes internes se créent, ce qui explique la valeur de dureté supérieure à 200 HV. La dureté de la couche de placage obtenue par la solution de placage à base d'aminosulfonate est faible, ce qui est dû non seulement à l'épaisseur de la couche, mais aussi à l'effet réducteur de contraintes de l'aminosulfonate lui-même.
⑦ Effet des impuretés : La solution de placage expérimentale et les conditions opératoires relatives à l’effet des métaux impurs sur l’aspect de la couche de placage sont présentées dans le tableau 1-14. Du nickel brillant a été déposé dans une cuve d’essai pour batteries à couches minces afin de réaliser des essais de placage. Les résultats obtenus avec les deux solutions de placage sont illustrés dans la figure 1-21 et résumés dans le tableau 1-15.
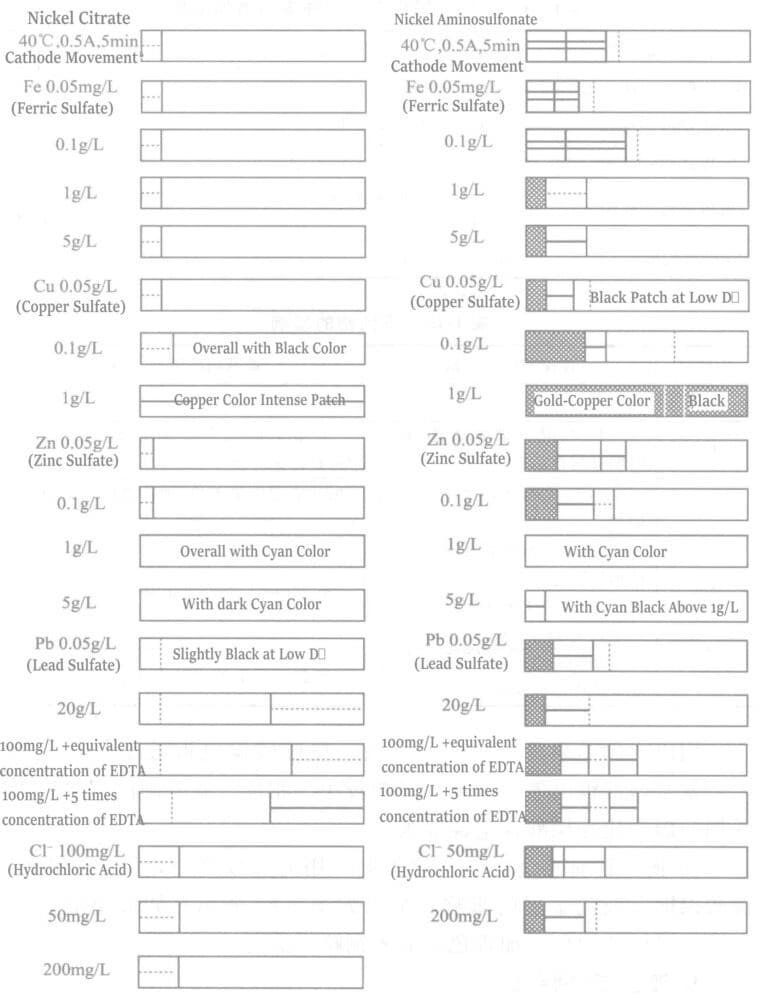
Tableau 1-14 Types et concentrations d'ajout de composés métalliques impurs
| Composés impurs | Montant supplémentaire |
|---|---|
| Le fer sous forme de sulfate ferreux | 0,05 g/L, 0,1 g/L, 1 g/L, 5 g/L |
| Cu sous forme de sulfate de cuivre | 0,05 g/L, 0,1 g/L, 1 g/L |
| Le zinc sous forme de sulfate de zinc | 0,05 g/L, 0,1 g/L, 1 g/L, 5 g/L |
| Le plomb sous forme de sulfate de plomb | 100 mg+ fois (rapport molaire) EDTA 5 mg/L, 20 mg/L, 100 mg+ Mole équivalente d'EDTA |
| Cl sous forme d'acide chlorhydrique | 50 mg/L, 200 mg/L |
Tableau 1-15 Effets des impuretés
| Impuretés | solution de placage au citrate de nickel | solution de nickelage à l'acide aminosulfonique |
|---|---|---|
| Fe | Aucun effet jusqu'à 5 g/L | |
| Cu | À 0,1 g/L : toute la surface apparaît noire ; à 1 g/L : une précipitation cuivrée distincte devient évidente. | À 0,5 g/L : un noircissement apparaît dans les zones à faible densité de courant ; à 1 g/L : la surface devient mate. |
| Zn | Jusqu'à 0,1 g/L : aucun effet observable ; au-delà de 0,1 g/L : une couleur jaune doré bleuâtre apparaît, la teinte bleutée s'intensifiant proportionnellement à l'augmentation de la concentration. | |
| Pb | Aux alentours de 5 mg/L : un léger noircissement apparaît dans les zones de faible densité de courant. À environ 20 mg/L : un aspect trouble se manifeste lors de l’introduction d’EDTA-2Na. | Jusqu'à 20 mg/L : aucun impact significatif n'a été observé. |
| Cl | À 200 mg/L : Augmentation marginale du voile atmosphérique limitée aux régions à forte densité de courant. | Environ 200 mg/L : influence pratiquement indétectable. |
En comparant les résultats obtenus pour les deux types de solutions de nickelage, on constate que la solution de nickelage à l'acide citrique est fortement influencée par le plomb. En revanche, le plomb a moins d'influence sur la solution de nickelage à l'acide aminosulfonique. Inversement, le cuivre affecte davantage la solution de nickelage à l'acide aminosulfonique que la solution de nickelage à l'acide citrique.
⑧ Effet du cuivre et du zinc sur la couleur de la couche de dorure : Un brillancemètre a été utilisé pour mesurer l’effet du cuivre et du zinc sur la couche de dorure de la solution de nickelage à l’acide citrique, et les résultats sont présentés dans la figure 1-22. Si du zinc est ajouté à la solution de dorure, la couleur de la couche de placage augmente en cyan ; si du cuivre est ajouté, elle présente une légère teinte noire.

2.3 Placage en alliage or-nickel-indium
Tableau 1-16 Composition et conditions de fonctionnement de la solution de placage en alliage or-nickel-indium
| Composition et conditions de fonctionnement | Paramètres | Composition et conditions de fonctionnement | Paramètres |
|---|---|---|---|
| Cyanure d'or et de potassium (g/L) | 11.7 | Indium (sulfate d'indium)/(g/L) | 5 |
| Acide citrique (g/L) | 85 | pH | 3.8 |
| Citrate de potassium (g/L) | 140 | Température de la solution d'électroplacage /℃ | 38 |
| Nickel (citrate de nickel)/(g/L) | 4.5 | Densité de courant (A/dm)2) | 1 |
2.4 Alliage d'or hypoallergénique plaqué
Depuis longtemps, des métaux comme le nickel et le cobalt sont couramment utilisés pour ajuster la dureté, la résistance à l'usure et à la corrosion, ainsi que la couleur des couches de dorure. Le nickel et le cobalt provoquent des réactions allergiques chez l'homme, et des pays d'Europe et d'Amérique ont déjà mis en place des réglementations strictes concernant leur utilisation. C'est pourquoi des solutions de dorure hypoallergéniques ont été développées.
L'ajout de sels de fer et de titane aux solutions de placage d'alliage d'or permet d'obtenir un brillant équivalent à celui des sels de nickel et de cobalt. L'ajout de sels conducteurs, d'acides organiques faibles tels que l'acide tartrique et l'acide citrique, de sels de métaux non précieux, de sels d'osmium, etc., permet de résoudre les problèmes d'allergie aux métaux. Ces solutions de placage d'alliage d'or sont hypoallergéniques. Toutefois, l'obtention d'une surface aussi lisse que celle des couches de placage classiques reste difficile, et des fissures apparaissent lorsque l'épaisseur dépasse 3 µm. Le réglage des teintes jaunes et blanches est également relativement complexe.
En remplaçant le nickel et le cobalt, qui posent des problèmes d'allergie, par du fer, en ajoutant des sels conducteurs d'indium et en utilisant des tampons de pH, la couche de placage en alliage d'or présente la même brillance, la même adhérence et la même stabilité, ainsi que les mêmes caractéristiques d'épaisseur et de tonalité que les couches de placage en alliage or-nickel ou or-cobalt.
La source d'ions or est le cyanure d'or(I) ou le cyanure d'or(III) de potassium. Si la concentration est trop faible, le rendement du courant est faible, la couche de placage est opaque et sujette aux fissures ; si elle est trop élevée, la viscosité de la solution de placage à l'or augmente et la couche de placage risque de brûler.
Si la concentration d'ions ferreux ou ferriques est trop faible, l'or ne peut pas être déposé de manière stable et la couche de placage d'or a tendance à présenter un aspect rougeâtre et trouble ; si elle est trop élevée, de larges fissures risquent d'apparaître, rendant difficile l'obtention d'une couche de placage épaisse.
L'ajout de fer seul engendre des contraintes internes excessives dans la couche de placage or, la rendant sujette aux fissures et empêchant la formation d'une couche d'alliage lisse. L'ajout d'indium permet de réduire ces contraintes, autorisant ainsi un placage or épais, et peut également servir à ajuster la teinte de l'or pur.
Si la concentration en ions indium est trop faible, des fissures risquent d'apparaître ; si elle est trop élevée, le rendement du courant diminue et le dépôt de la couche d'or devient instable.
Les acides inorganiques ou organiques peuvent être choisis parmi l'acide phosphorique, l'acide pyrophosphorique, l'acide borique, l'acide tungstique, l'acide oxalique, l'acide tartrique, l'acide citrique, l'acide malique, l'acide lactique, l'acide succinique, l'acide hydroxyacétique et l'acide gluconique.
Si la concentration en sels conducteurs et en tampons de pH est trop faible, la conductivité est médiocre et le tamponnage du pH insuffisant, ce qui entraîne un dépôt instable de la couche de placage d'or ; si elle est trop élevée, la viscosité de la solution de placage augmente, ce qui accroît le risque de fissures.
pH 1,5 à 7,0. En dessous de 1,5, le rendement du courant est faible et le dépôt instable. Au-dessus de 7,0, des précipités de fer et d'indium se forment facilement, entraînant un dépôt anormal de la couche d'or.
En modifiant la concentration des composants mentionnés ci-dessus, en ajoutant des tensioactifs, d'autres auxiliaires, etc., il est possible d'améliorer la couleur, la résistance à la corrosion et la résistance à l'usure de la couche de placage or déposée. Les exemples suivants illustrent ce principe :
Après prétraitement classique de la plaque de cuivre, utiliser la solution de placage du tableau 1-17, à pH 4, à une température de 40 °C et à une densité de courant de 2 A/dm².2 pour plaquer l'alliage d'or.
Tableau 1-17 Solution de placage en alliage d'or et couche de placage en alliage d'or
| Composition et résultats | Produits chimiques utilisés | N° 1 | N° 2 | N° 3 | N° 4 | N° 5 | N° 6 | N° 7 | N° 8 |
|---|---|---|---|---|---|---|---|---|---|
| Or (g/L) | Cyanure d'or et de potassium | 5 | 5 | 5 | 5 | 5 | |||
| Cyanure d'or(III) de potassium | 5 | 5 | 5 | 5 | |||||
| Fer (g/L) | ion ferreux | 5 | 5 | 5 | 5 | 5 | |||
| ion ferreux | 5 | 5 | 5 | 5 | 5 | ||||
| Indium (g/L) | 5 | 5 | 5 | 5 | 5(titane) | ||||
| Sel conducteur et tampon pH /(g/L) | acide oxalique | 100 | 20 | 100 | 10 | 100 | |||
| acide tartrique | 100 | 20 | 10 | ||||||
| Acide citrique | 100 | 20 | |||||||
| acide borique | 20 | ||||||||
| acide tungstique | 20 | 10 | 10 | ||||||
| Acide phosphorique | 20 | ||||||||
| Résultat | Épaisseur de brillance/μm | Au-dessus de 5 | <1 | <1 | <1 | <1 | |||
| Vitesse de sédimentation / (μm/min) | 0. 15 ~ 0. 25 | Impossible de déterminer | |||||||
| Caractéristiques | galvanoplastie brillante | Fissures et précipitations anormales | |||||||
Dans la solution de placage en alliage or-fer, l'ajout d'indium, de sels conducteurs et de tampons de pH permet d'obtenir une couche de placage épaisse en alliage d'or brillant d'une brillance supérieure à 5 μm, et la teinte peut être ajustée du jaune au blanc.
Les résultats n° 5 à 8 correspondent à l'absence d'indium. La vitesse de dépôt est instable, la couche de placage présente de nombreuses fissures, la surface est anormale (brûlée, opaque) et il est impossible d'obtenir une couche d'or brillante d'une épaisseur supérieure à 1 µm. L'utilisation de thallium à la place de l'indium provoque également des fissures dans la couche d'or et un dépôt irrégulier. De telles solutions de placage sont inutilisables. Le tableau 1-17 présente les caractéristiques des solutions de placage d'alliages d'or et des couches d'or obtenues.
En raison du caractère allergène du nickel et du cobalt, et des restrictions à leur vente et à leur exportation, le fer et l'indium remplacent ces métaux dans les solutions de placage d'alliage d'or. Les caractéristiques des couches de placage restent identiques, éliminant ainsi les problèmes d'allergie liés à des métaux comme le nickel et le cobalt. Le dépôt de la couche de placage est stable et la teinte obtenue peut être ajustée selon les besoins.
3. Placage or neutre
Le plaquage à l'or neutre, également appelé plaquage à l'or doux ou plaquage à l'or pur, se caractérise par une grande pureté de la couche d'or déposée, un aspect mat et une faible dureté. Il est principalement utilisé pour le plaquage à l'or des boîtiers de circuits intégrés. La solution de plaquage est composée de sels d'or, de cyanure d'or et de potassium, et d'agents tampons à pH neutre tels que le citrate, le phosphate, ou des mélanges de ces sels. Ces sels contribuent également à améliorer la conductivité de la solution de plaquage.
Caractéristiques de la solution de placage neutre : L’ajout d’une infime quantité de modificateur de cristallisation peut modifier la structure de précipitation de la couche de placage, lui conférant une teinte jaune citron. En cas d’ajout insuffisant, la couche prend une couleur brun rougeâtre ou brûlée ; en cas d’ajout excessif, une coprécipitation se produit, réduisant la pureté de la couche de placage.
3.1 Placage doré décoratif
Tableau 1-18 Composition et conditions de fonctionnement de la solution de placage en alliage or-cuivre (I)
| Composition et conditions de fonctionnement | Paramètres | Composition et conditions de fonctionnement | Paramètres |
|---|---|---|---|
| Cyanure d'or et de potassium (g/L) | 7 | pH | 6. 8〜75 |
| Na2HPO4 (Phosphate disodique)/(g/L) | 28 | Température de la solution d'électroplacage/℃ | 65 à 75 |
| Cu[Na2Cu(CN)3]/(g/L) | 7 | Densité de courant (A/dm)2) | 0,5 à 1 |
| Fe (cyanure ferreux)/(g/L) | 3 |
Tableau 1-19 Composition et conditions de fonctionnement de la solution de placage en alliage or-cuivre (II)
| Composition et conditions de fonctionnement | Paramètres | Composition et conditions de fonctionnement | Paramètres |
|---|---|---|---|
| Cyanure d'or et de potassium (g/L) | 0. 7~1. 5 | pH | 8.5 |
| Cu(EDTA sel de cuivre)/(g/L) | 8 | Température de la solution d'électroplacage/℃ | 53 à 57 |
| Na2EDTA (sans) (g/L) | 16 | Densité de courant (A/dm)2) | 1 ~ 1. 5 |
Il s'agit de solutions de placage en alliage d'or couramment utilisées en Europe. La couche de placage est une solution entièrement solide contenant une quantité importante de cuivre, mais elle ne se décolore pas. Le test d'aération à l'acide nitrique révèle une excellente résistance à la corrosion.
La couche de placage en alliage or-cuivre de la solution de placage EDTA est traitée thermiquement à 300-400 °C pour obtenir Au-Cu3 Composé intermétallique présentant une dureté très élevée. La figure 1-23 illustre la courbe de polarisation de la solution de placage du tableau 1-4.
3.2 Placage or fonctionnel
Tableau 1-20 Composition et conditions de fonctionnement de la solution de placage d'or neutre de haute pureté
| Composition et conditions de fonctionnement | N° 1 | N° 2 | N° 3 | N° 4 | N° 5 |
|---|---|---|---|---|---|
| Cyanure d'or et de potassium (g/L) | 10 à 31 | 10 à 20 | 7 à 18 | 6 | 8.2 |
| Phosphate de dihydrogène de sodium/(g/L) | 60 | - | 82 | - | - |
| Pyrophosphate de potassium (g/L) | - | - | - | - | 150 |
| Citrate (g/L) | 60 | 60 à 125 | 50 à 75 | 90 | - |
| Citrate de potassium | Citrate de potassium | Citrate d'ammonium | Sel soluble d'acide | ||
| thiosulfate de sodium pentahydraté/(g/L) | 5 à 10 | - | - | - | - |
| phosphate de triéthyle/(g/L) | - | 30 à 60 | - | - | - |
| Aminotriméthylphosphate/(g/L) | - | - | - | 80 | - |
| Alcool benzylique (fraction massique)/% | - | - | - | - | 0. 05 |
| pH | 5.5 à 8.0 | 6 〜 8 | 5 ~ 6. 5 | 6.0 | 7 ~ 8 |
| Température /℃ | 60 | 60 | 45 à 100 | 65 | 60 |
| Densité de courant (A/dm)2) | 0,1 à 1,5 | 0. 1 ~ 0. 3 | 0. 1 ~ 0. 4 | 0. 1 ~ 0. 5 | 0. 1 |
4. Placage or au sulfite
Depuis 1970, le plaquage à l'or à l'aide de sulfites d'or est une technique courante. Les complexes de sulfite d'or(I) subissent une réaction [Au(SO₄)₂]²⁻.3)2]3-⇌Au++2SO32- dissociation.
La stabilité de ce type d'ion complexe est bien inférieure à celle des complexes de cyanure, avec une constante de stabilité d'environ 10.10, donc la stabilité est de 1028 fois pire que [Au(CN)2–] .
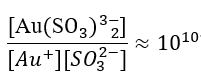
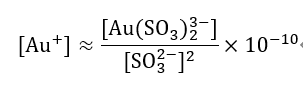
Am représente le groupe amino d'une amine aliphatique.
L'anion se dissocie selon la formule suivante :
[Au(Am)2(SO3)2]3- ⇌[Au(Am)2]+ + 2(SO3)2- (1-2)
Et aussi [Au(Am)2]+ ⇌Au+ + 2h du matin (1-3)
Tableau 1-21 Composition de la solution de galvanoplastie au sulfite d'or
| Composition | Paramètres |
|---|---|
| Or [sel iminocoordonné de sulfite de sodium et d'or(I)]/(g/L) | 12 |
| sulfite de sodium (libre)/(g/L) | 50 |
| Citrate de sodium (g/L) | 50 |
| tétraborate de sodium/(g/L) | 10 |
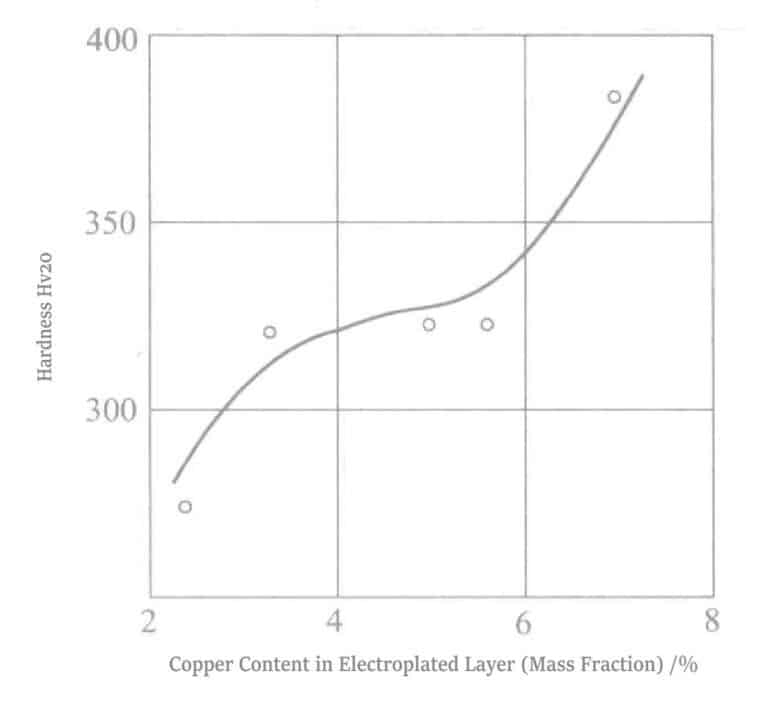
Le sulfite d'or est généralement utilisé pour le dépôt d'alliages ternaires Au-Pd-Cu lors de la galvanoplastie. Ses avantages sont les suivants : ① la couche de dépôt est rose ; ② sa dureté atteint 400 Hv ; ③ elle présente une excellente résistance à l'usure ; ④ elle offre une excellente résistance à la corrosion. Ses inconvénients sont les suivants : ① le taux de dépôt de l'alliage varie de manière irrégulière en fonction de la densité de courant et de la température ; ② l'anode subit une réduction et un dépôt lors des dépôts de longue durée.
Yoshimura et al. ont utilisé les conditions décrites dans le tableau 1-22, en faisant varier la concentration de cuivre de 0,0021 à 0,0211 mol/L, la température de la solution de placage de 25 °C et 50 °C, et la densité de courant de 0,230 A/dm².2 Pour le placage. L'aspect, la dureté, la résistance à l'usure et d'autres caractéristiques du revêtement déposé sont présentés dans le tableau 1-23. Comparée à la taille de grain de 337 Å de la couche de placage en alliage or-palladium, la taille de grain de la couche de placage en alliage or-palladium-cuivre est plus petite (161 à 231 Å), avec une dureté de 400 Hv et une bonne résistance à l'usure. Un brevet existe pour cette couche de placage en alliage or-palladium-cuivre.
Tableau 1-22 Composition de la solution d'électrodéposition d'alliage Au-Pd-Cu Unité : mol/L
| Composition | Paramètres | Composition | Paramètres |
|---|---|---|---|
| Au(SO3 )2 3- | 0.0204 | Na2SO3 | 0.1983 |
| Pd(en)2 2+ | 0.0236 | NaAsO2 | 0.0115 |
| EDTA-2Na | 0.2109 | CuSO4 | 0,0021 à 0,0211 |
Tableau 1-23 : Comparaison de la dureté et de la résistance à l’usure des revêtements en alliage Au-Pd-Cu et en alliage Au-Ni
| Composition de la solution d'électroplacage, rapport de dépôt/% | Dureté VHN | résistance à l'usure |
|---|---|---|
| Au : Ni | ||
| 92 : 8 | 237 | 20 |
| Au : Pd : Cu | ||
| 87 : 3 : 10 | 362 | 26 |
| 80 : 5 : 15 | 437 | 33 |
| 79 : 8 : 13 | 383 | 28 |
| 75 : 9 : 16 | 400 | 28 |