Pourquoi les pierres précieuses ont-elles plusieurs couleurs ?
Secrets de la formation des couleurs et méthodes de mesure
Les couleurs des pierres précieuses sont riches et variées et possèdent un charme unique que les gens ont toujours aimé. La qualité des pierres précieuses dépend en grande partie de leur couleur. La couleur d'une pierre précieuse est un indicateur important dans l'évaluation des pierres précieuses, et la plupart des traitements d'optimisation des pierres précieuses impliquent de changer ou d'améliorer leur couleur. Par conséquent, la compréhension des causes de la coloration des pierres précieuses est une condition préalable essentielle au traitement d'optimisation des pierres précieuses. Ce n'est qu'en maîtrisant la manière dont les pierres précieuses acquièrent leur couleur que l'on peut déterminer si une pierre précieuse peut être optimisée, quel schéma d'optimisation adopter et quel plan expérimental établir. Il existe cinq théories communes de la coloration des pierres précieuses : la théorie minéralogique classique, la théorie du champ cristallin, la théorie de l'orbitale moléculaire, la théorie de la bande d'énergie et les effets optiques physiques. Ces théories constituent les théories de la coloration des pierres précieuses naturelles courantes, et ce qui suit est une brève introduction à ces cinq théories de la coloration.

Schéma des trois éléments de la couleur
Table des matières
Section I Couleur et mesure de la couleur des pierres précieuses
Les couleurs des pierres précieuses sont riches et variées, et il est essentiel de déterminer les types de couleurs des pierres précieuses pour évaluer leur valeur. Les différents degrés de couleur affectent également la valeur des pierres précieuses. Par conséquent, l'évaluation précise des couleurs des différentes pierres précieuses est une condition préalable fondamentale pour déterminer leur valeur. Lors de l'évaluation des pierres précieuses colorées, la couleur est le facteur le plus important. En règle générale, plus la couleur d'une pierre est attrayante, plus sa valeur est élevée. Les couleurs vives, riches et intenses sont généralement plus attrayantes que les couleurs trop sombres ou trop claires. Bien entendu, il existe des exceptions, comme les diamants, dont la valeur est d'autant plus élevée que la couleur est blanche.
1. La signification de la couleur des pierres précieuses
Depuis l'Antiquité, les gens aiment les pierres précieuses pour leur charme unique, en particulier pour leurs teintes riches et colorées, comme le rubis rouge sang de pigeon, l'émeraude vert vif et le jade, qui laissent tous une impression durable. La couleur est un indicateur important pour évaluer la qualité des pierres précieuses et joue un rôle crucial dans la détermination de leur qualité, dont l'importance se reflète principalement dans les trois aspects suivants.
(1) La couleur des minéraux des pierres précieuses est une base importante pour l'évaluation des pierres précieuses.
La couleur d'une pierre précieuse est fondamentale pour son évaluation et détermine sa valeur. Par exemple, pour les diamants, une différence de couleur d'un grade peut entraîner une différence de prix d'environ 5%. Plus la blancheur est importante, plus la qualité du diamant est élevée ; à l'inverse, les diamants de couleur jaune ou brune sont moins bien classés et leur prix s'effondre. Les prix des diamants de couleur varient, et des diamants de couleur différente ont des prix différents. Toutefois, d'une manière générale, les prix des diamants de couleur rare peuvent être multipliés. D'autres pierres précieuses de couleur, telles que les rubis, les saphirs et les émeraudes, sont également classées en différentes catégories en fonction de leur couleur, et la valeur des pierres précieuses de différentes catégories peut varier de manière significative.
(2) Le traitement d'optimisation des pierres précieuses consiste souvent à améliorer leur couleur.
Les méthodes d'optimisation des pierres précieuses impliquent généralement de modifier ou d'améliorer la couleur des pierres, de sorte que l'amélioration des pierres précieuses peut également être appelée altération de la couleur des pierres précieuses. Lorsque la couleur de la pierre précieuse s'améliore, la transparence change également en conséquence. En effet, la transparence est une propriété liée à la couleur. Par exemple, les saphirs bleus semblent avoir de nombreuses couleurs noires opaques à l'œil nu, mais le bleu transparent est visible lorsqu'on les coupe en fines tranches. L'amélioration de la transparence va souvent de pair avec l'amélioration de la couleur. Par conséquent, ce n'est qu'en déterminant la cause de la couleur de la pierre précieuse que l'on peut déterminer les méthodes d'amélioration de la pierre précieuse. Comprendre la cause de la couleur est une condition préalable à l'étude des traitements d'optimisation des pierres précieuses.
(3) L'étude des causes de la couleur des pierres précieuses fournit une base théorique pour les pierres synthétiques et l'amélioration des pierres précieuses.
Les couleurs des pierres précieuses telles que le grenat, la malachite et l'olivine sont dues à leurs composants inhérents, et ces pierres précieuses ne peuvent pas être modifiées par des méthodes de traitement d'optimisation conventionnelles. La plupart des couleurs des pierres précieuses sont dues à des impuretés causées par des ions d'impureté, comme dans les rubis, les saphirs, les émeraudes, le jade et l'agate. Sur la base des causes de la couleur des pierres précieuses, la teneur et l'état de valence de certains ions d'impureté responsables de la couleur peuvent être modifiés au cours de l'amélioration afin de changer ou d'améliorer la couleur de la pierre précieuse, améliorant ainsi la qualité de la pierre précieuse améliorée. Par conséquent, l'étude des causes de la couleur des pierres précieuses constitue la base théorique de l'amélioration des pierres précieuses.
2. La physique de la couleur
(1) Couleur et ondes lumineuses
Les photons transportent l'énergie de la lumière et, lorsqu'ils atteignent l'œil humain, ils créent la sensation de couleur. La couleur est la perception de la lumière par les yeux et le système nerveux ; la réponse générée par les signaux formés sur la rétine de l'œil stimule le cortex cérébral. La formation de la perception de la couleur a trois composantes principales : la source lumineuse, l'objet et l'œil humain. La modification d'une ou plusieurs de ces trois composantes altère la perception de la couleur. Les gemmes interagissent avec la lumière et les phénomènes de réflexion, de réfraction, de transmission, d'interférence et de diffraction qui se produisent à la surface de la gemme donnent lieu à des couleurs différentes.
La gamme d'énergie du spectre de rayonnement électromagnétique est assez large, allant des photons d'ondes radio très longues aux photons de rayons très courts, avec une gamme d'énergie allant de moins d'un milliardième d'électronvolt à plus de cent millions d'électronvolts.
La lumière visible que l'œil humain peut accepter et percevoir est une très petite partie du spectre électromagnétique, avec une gamme de longueurs d'onde de 400-700nm et une énergie d'environ 1,7-3,1eV. Si les conditions d'observation sont suffisamment bonnes, la gamme peut être étendue à 380-760 nm (figure 3-1). La lumière visible comprend les couleurs que nous voyons, à savoir le rouge, l'orange, le jaune, le vert, le cyan, le bleu, le violet et diverses autres couleurs. Les différentes longueurs d'onde de la lumière visible produisent des couleurs différentes ; la couleur de la lumière visible ayant la plus grande longueur d'onde et la plus faible énergie est le rouge, avec une plage de longueurs d'onde de 647-760nm ; la lumière visible ayant la plus petite longueur d'onde et la plus forte énergie est le violet, avec une plage de longueurs d'onde de 400-425nm. Les autres couleurs de la lumière visible se situent entre 425 et 647 nm. Les longueurs d'onde des différentes couleurs de la lumière visible et leurs couleurs complémentaires sont indiquées dans le tableau 3-1.
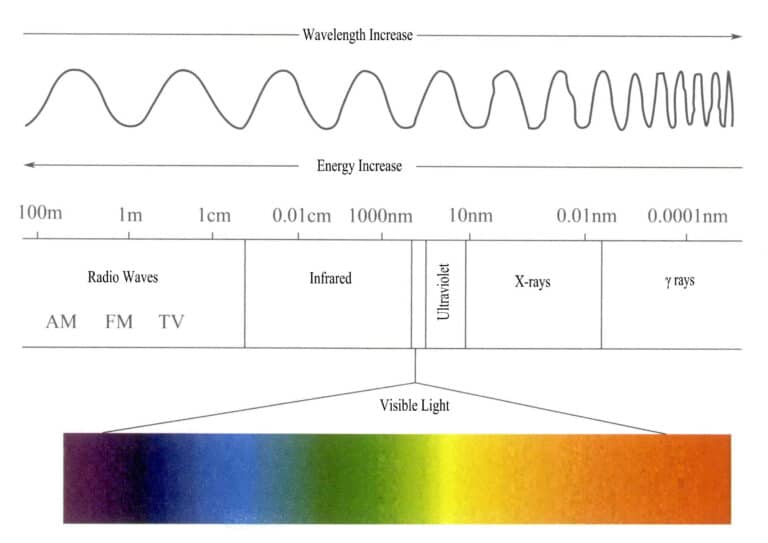
Tableau 3-1 Longueurs d'onde des différentes couleurs de la lumière visible et de leurs couleurs complémentaires
| Longueur d'onde/nm | Couleur spectrale | Complémentaire |
|---|---|---|
| 400 ~ 425 | Pourpre | Jaune-vert |
| 425 ~ 455 | Bleu | Jaune |
| 455 ~ 490 | Vert-bleu | Orange |
| 490 ~ 500 | Bleu-vert | Rouge |
| 500 ~ 560 | Vert | Magenta |
| 560 ~ 580 | Jaune-vert | Pourpre |
| 580 ~ 595 | Jaune | Bleu |
| 595 ~ 647 | Orange | Vert-bleu (cyan) |
| 647 ~ 760 | Rouge | Vert |
L'essence de la couleur d'un objet est le résultat de l'absorption sélective par l'objet de différentes longueurs d'onde de la lumière visible. L'essence de l'absorption sélective par un objet de différentes longueurs d'onde de la lumière visible est l'absorption de photons de lumière visible ayant des énergies différentes. Lorsque la lumière naturelle éclaire une pierre précieuse, celle-ci absorbe une partie de la lumière et en transmet une autre. La couleur présentée par la pierre précieuse est la couleur complémentaire de la lumière absorbée, cohérente avec la couleur de la lumière transmise (figure 3-2). Par exemple, dans le cas du rubis, lorsque la lumière blanche traverse le rubis, les ions de chrome contenus dans le rubis gagnent de l'énergie en absorbant tous les photons violets et verts ainsi que la plupart des photons bleus, tandis que les autres photons de couleur, principalement rouges, traversent le rubis, ce qui fait apparaître la pierre précieuse en rouge.
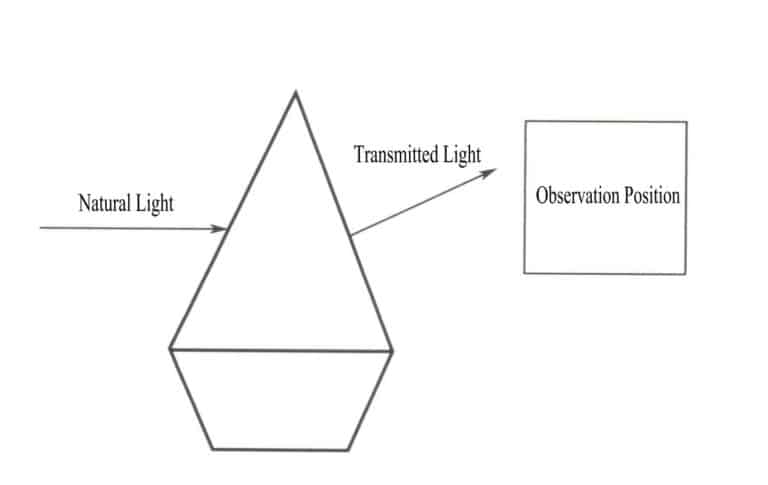
Une seule longueur d'onde de la lumière ne produit pas la couleur d'un objet ; le rayonnement de l'objet est plutôt un mélange de photons de différentes énergies, la bande d'énergie la plus importante déterminant la couleur de l'objet. Un mélange uniforme de différentes couleurs de lumière forme la lumière blanche. La couleur des pierres précieuses résulte de l'absorption sélective de photons de différentes longueurs d'onde de la lumière visible. Lorsque la lumière blanche traverse une pierre précieuse, la lumière absorbée et transmise par la pierre précieuse est un mélange, et la couleur présentée par la pierre précieuse dépend de celle qui a la plus grande proportion de lumière transmise. Par exemple, dans le cas d'un rubis, lorsque la lumière blanche brille sur le rubis, la lumière qui passe est principalement rouge avec une petite quantité de bleu-violet. Ainsi, les rubis apparaissent souvent rouges avec une teinte bleu-violet.
(2) Types et propriétés des sources lumineuses
La couleur des pierres précieuses présente une certaine subjectivité, liée à l'environnement de l'observateur et surtout influencée par la source de lumière. L'observation de la couleur des pierres précieuses sous différentes sources de lumière peut faire apparaître des différences ; par exemple, une alexandrite apparaît verte à la lumière du soleil, mais rouge sous une lumière incandescente. En général, les gens considèrent que la couleur observée à la lumière naturelle du soleil est la norme, communément appelée lumière blanche.
Les premières opérations sur le marché des pierres précieuses ont été menées à des heures précises afin d'obtenir une couleur relativement exacte des pierres précieuses. Par exemple, les magasins de pierres précieuses de Ratnapura, au Sri Lanka, ont fonctionné pendant de nombreuses années de 10 heures à 12 heures, car la source de lumière à ce moment-là est la plus proche de la lumière blanche. La lumière du soleil et la lumière du jour ne sont pas des sources lumineuses isotropes, et les différences relatives entre les quantités de rayonnement dans les différentes longueurs d'onde entre les différentes sources lumineuses peuvent être très importantes en raison des différentes conditions d'observation. La figure 3-3 présente les courbes de distribution de l'énergie de cinq sources lumineuses courantes, et les différences d'énergie entre ces sources lumineuses sont très importantes.
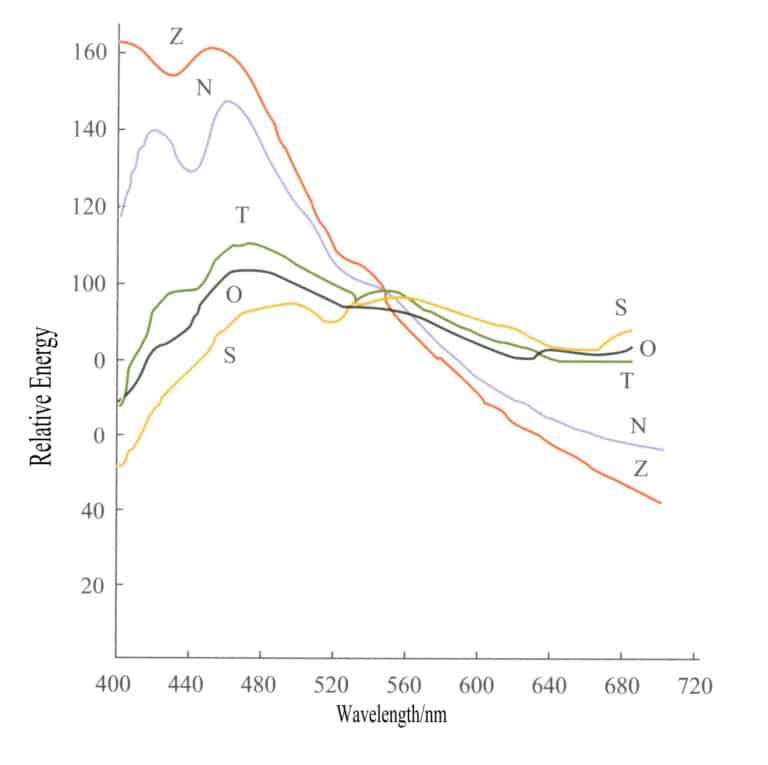
S - Lumière directe du soleil ; O - Illumination de la lumière du ciel couvert sur le plan horizontal ; T - Illumination de la lumière du soleil et du ciel clair sur le plan horizontal ; N - Lumière du ciel clair du nord ; Z - Lumière zénithale ;
Les caractéristiques de couleur de la lumière directe du soleil sont souvent exprimées en termes de température de couleur (mesurée en K). Une même température de couleur indique que les sources lumineuses ont des couleurs similaires. Les températures de couleur de la lumière du jour actuellement reconnues sont D6500K, D5500K et D7500K. Trois lampes sont internationalement désignées comme sources lumineuses standard pour les travaux de mesure de la couleur. SA représente l'éclairage artificiel moyen d'une lampe à incandescence au tungstène, avec une température de couleur de 2854K;SB représente la lumière moyenne du soleil, avec une température de couleur de 4900K ; SC représente la lumière du jour moyenne, avec une température de couleur de 6700K. Dans les tests de gemmologie, la source lumineuse Sc est utilisée comme source lumineuse standard.
(3) Sensibilité aux effets de la lumière et de la couleur
L'observation de la couleur des gemmes est subjective ; outre les conditions objectives, la couleur de la gemme est également liée à la perception sensorielle de l'observateur. Sous la même source de lumière, les yeux humains ont des sensibilités différentes aux différentes couleurs, et les personnes ont des sensibilités différentes aux couleurs. L'observation de la couleur est subjective ; pour atteindre l'objectivité autant que possible, les couleurs doivent être caractérisées et exprimées de manière relativement objective.
① Effet photoréceptif :
Dans des conditions normales, la gamme de longueurs d'onde des sources de lumière visible que l'œil humain peut observer est comprise entre 400 et 700 nm. En améliorant les conditions d'observation, il est possible d'étendre la plage de sensibilité à 380-780 nm. L'œil humain a des sensibilités différentes aux ondes lumineuses de différentes longueurs d'onde. Pour la vision diurne, l'œil est plus sensible à la lumière verte d'une longueur d'onde de 555 nm, tandis que la longueur d'onde la plus sensible pour la vision crépusculaire passe à 507 nm. Les feux de signalisation sont conçus en fonction des couleurs auxquelles l'œil humain est le plus sensible.
② Sensation de couleur :
La couleur est la sensation provoquée par les différentes composantes spectrales de l'énergie de rayonnement dans la gamme de la lumière visible. La vision d'une personne normale permet de distinguer plus de 150 nuances de couleurs spectrales pures. Bien qu'il existe une correspondance biunivoque entre les ondes lumineuses et les couleurs, la correspondance entre les couleurs et les ondes lumineuses n'est pas unique ; souvent, une couleur de lumière peut être formée par la combinaison de deux ou plusieurs autres couleurs de lumière. Les trois couleurs indépendantes de base sont le rouge, le vert et le bleu, appelées couleurs primaires. D'autres couleurs sont formées en mélangeant deux ou plusieurs couleurs primaires dans des proportions différentes. L'œil humain est très sensible aux couleurs et peut en distinguer un grand nombre.
3. Trois éléments représentant la couleur
La couleur résulte de l'absorption sélective de la lumière par les pierres précieuses, et des pierres précieuses différentes présentent des couleurs différentes. La théorie actuelle de la couleur suggère que les caractéristiques de la couleur dépendent de la luminosité, de la teinte et de la saturation (figure 3-4). Les types de couleurs des pierres précieuses peuvent être déterminés en décrivant les trois éléments des différentes couleurs.

(1) Luminosité
La luminosité est le degré d'éclat causé par la lumière agissant sur l'œil humain, se référant au degré de couleurs claires et foncées, et peut également être appelée luminance. La luminosité dépend en grande partie de la perception par l'œil des niveaux de clarté et d'obscurité de la source lumineuse et de la surface de l'objet, principalement déterminée par l'intensité de la lumière. La luminosité dépend du niveau d'éclairage de l'objet et de la réflectivité de sa surface.
La luminosité peut être considérée comme la luminosité d'une couleur ; différentes couleurs ont différents niveaux de luminosité, et toute couleur présente des variations de clarté et d'obscurité. La luminosité présente deux caractéristiques : un même objet peut présenter des variations de luminosité dues à des éclairages différents, et des lumières colorées différentes de même intensité peuvent également présenter des niveaux de luminosité différents.
En l'absence de couleur, la couleur la plus lumineuse est le blanc, et la couleur la moins lumineuse est le noir, avec une échelle de gris entre le clair et le foncé. En couleur, chaque degré de pureté a ses caractéristiques de luminosité. Par exemple, le jaune a la luminosité la plus élevée, tandis que le violet a la luminosité la plus faible. Le vert, le rouge, le bleu et l'orange ont des niveaux de luminosité similaires, ce qui représente une luminosité moyenne. En outre, au sein d'une même teinte, il existe des variations de luminosité du clair au foncé, comme le vert clair, le vert pâle et le vert émeraude dans le spectre vert.
(2) Hue
La teinte fait référence aux différences entre les différentes couleurs et constitue la caractéristique la plus importante de la couleur. La teinte est déterminée par les composantes spectrales de la lumière qui traversent un objet et atteignent l'œil humain après avoir été émises, en fonction de la longueur d'onde de la lumière transmise. La teinte d'un objet est déterminée par le spectre de la source lumineuse incidente et par la lumière réfléchie ou transmise par l'objet lui-même.
La teinte fait référence au nom qui peut représenter plus précisément une certaine catégorie de couleurs, comme le rouge rose, le jaune orangé, le jaune citron, le bleu cobalt, le rouge pourpre, le vert émeraude, etc. Du point de vue de l'optique physique, les différentes teintes sont déterminées par les composantes spectrales de la lumière qui pénètre dans l'œil humain. Pour la lumière monochromatique, les types de teintes dépendent entièrement de la longueur d'onde de cette lumière ; pour la lumière mixte, elles dépendent des quantités relatives des différentes longueurs d'onde de la lumière. La couleur d'un objet est déterminée par les composantes spectrales de la source lumineuse et les caractéristiques de la lumière réfléchie (ou transmise) par la surface de l'objet. Elle est liée à la longueur d'onde de la lumière. Par exemple, une couleur dont la longueur d'onde dominante est de 470 nm est appelée bleu de 470 nm de longueur d'onde, communément appelé le bleu des saphirs.
(3) Saturation
La saturation d'une couleur fait référence à la pureté et à la vivacité de la couleur, en indiquant la proportion de composants chromatiques contenus dans la couleur. Plus la proportion de composants chromatiques est importante, plus la couleur est pure ; plus la proportion de composants chromatiques est faible, moins la couleur est pure. La saturation change lorsqu'une couleur est mélangée avec du noir, du blanc ou d'autres couleurs. Lorsque la proportion de la couleur mélangée atteint un niveau significatif, la couleur d'origine perd son éclat original à l'œil et la couleur observée devient celle de la couleur mélangée. Bien entendu, cela ne signifie pas que la couleur d'origine n'existe plus, mais plutôt qu'elle a été assimilée en raison des nombreuses autres couleurs mélangées, ce qui la rend imperceptible à l'œil humain.
Les lumières monochromatiques du spectre visible ont la saturation la plus élevée et sont les plus vives. La lumière monochromatique est généralement considérée comme 100/100 = 1, et au fur et à mesure que la couleur s'estompe, la valeur diminue progressivement, le blanc pur ayant une saturation nulle. Si l'on prend l'exemple de l'encre bleue pure, sa saturation est de 1. Au fur et à mesure qu'elle se dilue pour devenir totalement incolore, la saturation devient nulle.
4. Mesure de la couleur des pierres précieuses
Le système qui représente quantitativement la couleur est appelé système de couleur. Il existe deux types de systèmes de couleurs couramment utilisés : un système de couleurs basé sur des échantillons de couleurs standard à des fins de comparaison, et un ensemble de systèmes de couleurs standard mesurés à l'aide d'instruments de mesure des couleurs modernes.
(1) Système de couleur des échantillons de couleur standard
Ce système de couleurs consiste en plusieurs "cartes de couleurs" en papier qui sont des échantillons de couleurs standard compilés dans un livre. Elles sont comparées à des échantillons de pierres précieuses afin de sélectionner la "carte de couleur" qui correspond à la couleur de la pierre précieuse.
① Système de couleurs Munsell
Le système de couleurs Munsell est l'un des premiers et des plus classiques systèmes de représentation des couleurs. Il est encore utilisé aujourd'hui par certaines organisations. Il a été établi en 1905 par l'éducateur américain et théoricien de la couleur Albert Munsell, qui a été nommé directement d'après lui. Il s'agit d'une manière de représenter les couleurs par le biais d'un modèle couleur-solide. Le "Munsell Color Atlas", publié par l'Optical Society of America (OSA), comprend des versions brillantes et mates.
La version brillante comprend 1 450 échantillons de couleurs, accompagnés d'un ensemble de 37 échantillons achromatiques ; la version mate comprend 1 150 échantillons de couleurs et 32 échantillons achromatiques.
Dans l'atlas Munsell, chaque couleur est représentée par un ensemble de symboles. Les symboles fournissent des indicateurs équidistants pour les trois éléments de la représentation de la couleur : la teinte, la valeur et la chroma, représentés par HV/C = teinte, valeur et chroma.
Les teintes sont divisées en cinq tons primaires : rouge (R), jaune-rouge (YR), jaune (Y), vert-jaune (GY), vert (G), bleu-vert (BG), bleu (B), violet-bleu (PB), violet (P) et rouge-violet (RP), ainsi qu'en cinq tons intermédiaires. Chaque ton est divisé en dix niveaux (1 à 10), le cinquième niveau étant la couleur intermédiaire de ce ton (figure 3-5).
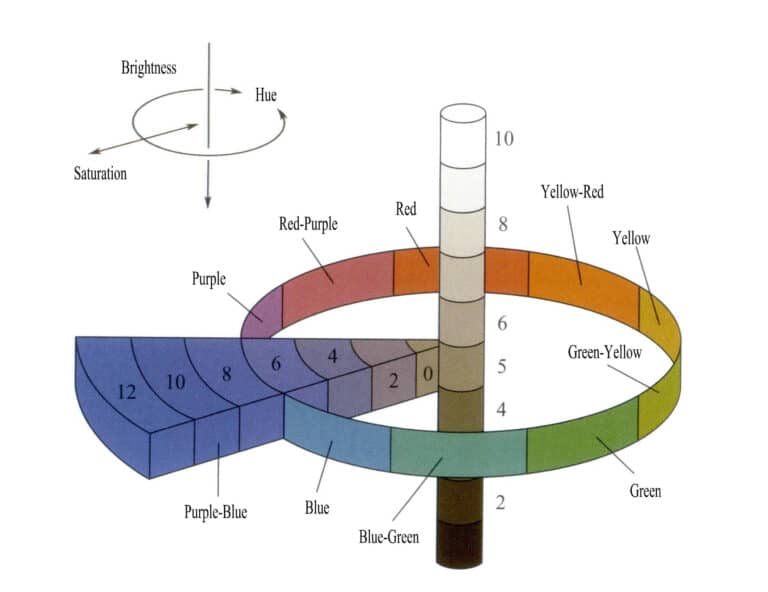
La valeur est divisée en 11 niveaux, les valeurs les plus élevées indiquant une plus grande clarté ; la valeur minimale est de 0 (noir) et la valeur maximale de 10 (blanc). La chroma est divisée en 12 niveaux. L'ensemble de l'atlas des couleurs comprend 40 types d'échantillons de teintes. Par exemple, 5GY 8/7 représente un jaune-vert avec une valeur de 8 et une saturation de 7. La convention de dénomination pour les séries non colorées (noir, blanc, gris) est NV/= valeur de luminosité neutre ; par exemple, une couleur étiquetée N5/ indique un gris avec une valeur de luminosité de 5.
② DIN 6164 Système de couleurs
Le manuel allemand DIN 6164 est également un système de couleurs important. De nombreux gemmologues en Europe et au Royaume-Uni utilisent ce système. Ce système de couleurs a été développé sur la base du système Munsell.
La carte des couleurs DIN 6164 comporte 24 couleurs, le dos de chaque couleur étant marqué de la notation de couleur Munsell correspondante. La représentation se fait sous la forme suivante : teinte : saturation : luminosité. Par exemple, 6:6:2 représente la teinte 6 (rouge), la saturation 6 (vif) et la luminosité 2 (clair) de la carte de couleurs standard.
③ Système de couleurs ISCC-NBS
L'ISCC (Inter-Society Colour Council) a été créé en 1931 en tant qu'association nationale de la couleur aux États-Unis, et son système de couleurs vise à développer un système de dénomination des couleurs. Il rassemble 18 teintes aux mêmes positions de teinte et de luminosité dans les normes Munsell et DIN 6164.
L'ISCC-NBS (National Bureau of Standards) dispose de très peu d'échantillons de couleurs dans le système American National Standard, mais a collecté quelques échantillons peu communs. Sur le plan structurel, il diffère également du système Munsell, car les couleurs ne sont pas classées en fonction de métriques équidistantes perceptives. La contribution la plus importante du système ISCC-NBS à la science des couleurs est qu'il définit les noms des couleurs.
④ Norme de couleur OSA
L'OSA (Optical Society of America) a préparé un ensemble pratique de cartes de couleurs acryliques brillantes, comprenant 558 couleurs, dont 424 couleurs constituent un ensemble connu sous le nom de norme de couleur OSA. L'inconvénient du standard de couleurs de l'OSA est que les cartes de couleurs sont fabriquées en papier ou en plastique, dont la texture diffère de celle des pierres précieuses, et que la brillance de la surface des cartes de couleurs diffère de la lumière réfléchie par les pierres précieuses à facettes, ce qui nécessite une utilisation prudente. En raison de la décoloration, la plupart des cartes de couleurs ont une durée d'utilisation de 4 à 5 ans.
(2) Coordonnées chromatiques et diagramme chromatique
① Système d'espace couleur CIE-XYZ de 1931
Ce système d'espace colorimétrique est basé sur le système RVB et utilise des méthodes mathématiques pour sélectionner trois couleurs primaires idéales afin de remplacer les couleurs primaires réelles. En utilisant les couleurs primaires virtuelles comme axes, il projette différentes longueurs d'onde de la lumière visible. Les valeurs des couleurs primaires sont appelées valeurs tristimulus. Ce système exige que les valeurs tristimulus ne soient pas négatives et que y soit égal au flux lumineux. En utilisant x comme axe horizontal et y comme axe vertical, il forme les coordonnées chromatiques, en projetant les valeurs des coordonnées chromatiques de chaque lumière monochromatique pour obtenir le diagramme chromatique. La figure 3-6 est le diagramme chromatique standard du système (XYZ) établi au niveau international en 1931.
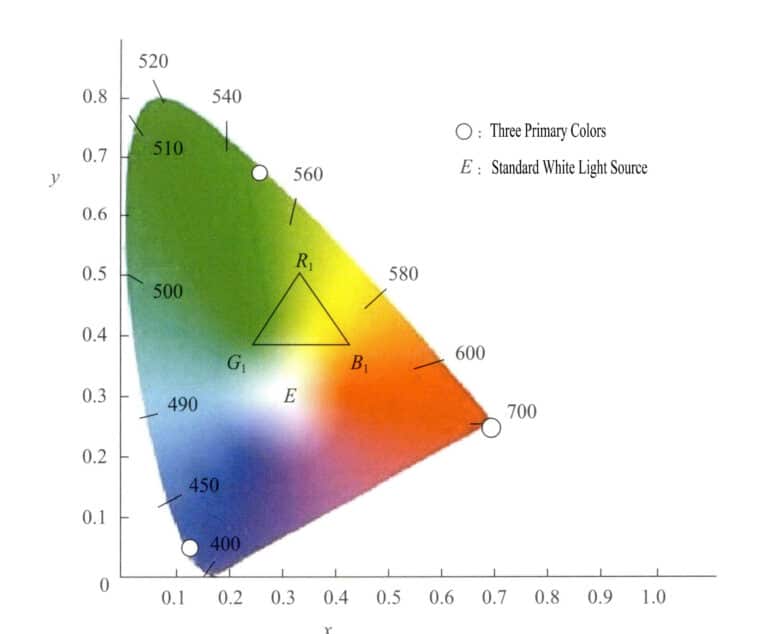
Le diagramme chromatique présente les caractéristiques suivantes :
- Les valeurs tristimulus des couleurs primaires de ce système sont virtuelles.
- Tous les points représentant les couleurs spectrales tombent sur la courbe en forme de langue appelée couleur spectrale. En reliant les extrémités de la courbe par des lignes droites, toutes les couleurs réelles sont contenues dans la zone entourée par la courbe en forme de langue et les lignes droites.
- La valeur des coordonnées du point E à x=0,333, y=0,333 représente le blanc théorique. Les différentes sources de lumière blanche ont des composantes spectrales légèrement différentes. La lumière blanche couramment utilisée est divisée en SA, SB, SC, SEet ainsi de suite.
- Les coordonnées chromatiques des couleurs sont d'autant plus saturées qu'elles sont proches de la trajectoire spectrale des couleurs. Les points situés sur la trajectoire spectrale des couleurs ont la saturation la plus élevée ; le point blanc a la saturation la plus faible. Une ligne reliant le point blanc aux coordonnées chromatiques d'une couleur, prolongée jusqu'à l'intersection avec la trajectoire spectrale de la couleur, comporte des points de même teinte le long de cette ligne.
- Une méthode graphique peut être utilisée pour calculer la couleur composite de deux couleurs quelconques. En introduisant les coordonnées chromatiques des deux couleurs dans le diagramme chromatique, la couleur composite doit se situer sur la ligne reliant les deux points de coordonnées chromatiques. La distance projetée entre les deux points de couleur est liée à l'intensité des deux couleurs, déterminée par la loi de distribution des centroïdes.
- Les points situés sur la ligne droite entre les extrémités de la courbe de couleur spectrale ne représentent pas des couleurs spectrales, mais plutôt diverses couleurs mixtes obtenues en mélangeant du violet à 380nm et du rouge à 780nm dans des proportions différentes.
- Sélectionnez trois points quelconques dans la trajectoire de couleur du spectre pour créer une couleur. Par exemple, si vous choisissez R1, G1, B1 comme étant les trois couleurs pour l'appariement, alors toutes les différentes couleurs formées par ces trois teintes sont contenues dans le triangle dont les sommets sont situés aux trois points R1, G1, B1.
② Représentation de la longueur d'onde dominante et de la saturation
Dans le diagramme chromatique, les couleurs peuvent être représentées non seulement par les coordonnées chromatiques (x, y). Une autre méthode proposée par Helmholtz consiste à les représenter par la longueur d'onde dominante λd et la saturation (pureté du stimulus) Pe. λd et Pe sont des valeurs spécifiques dérivées des coordonnées chromatiques du diagramme (figure 3-7). La longueur d'onde dominante représente approximativement la sensation de couleur perçue par l'œil humain.
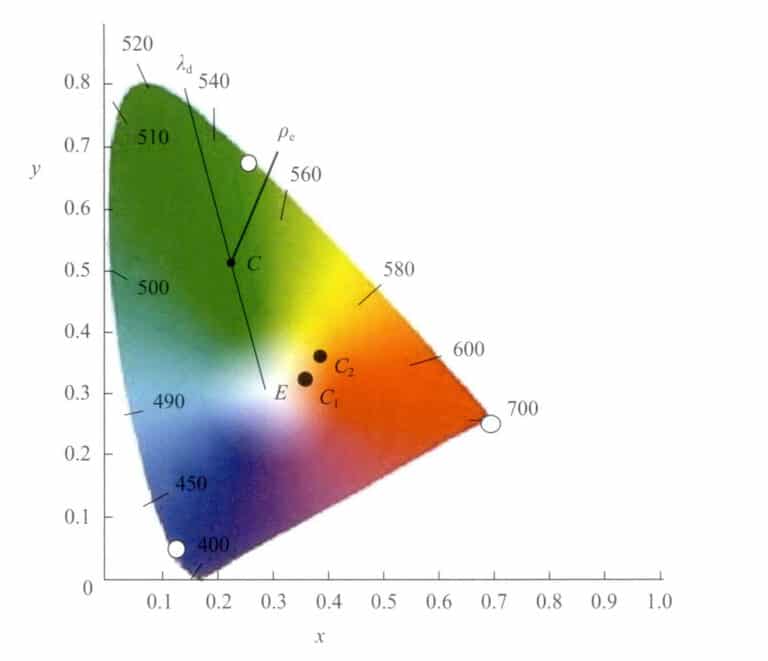
La position de ce point dans le diagramme chromatique est c(x, y). Reliez le point c au blanc E et prolongez-le jusqu'à ce qu'il croise la trajectoire du spectre à λd . Le nombre de longueurs d'onde du point λd sur la trajectoire du spectre est la longueur d'onde dominante de cette couleur de lumière.
Le point C est situé sur la ligne reliant les points W et λd représentant la saturation de cette couleur. Le point W est le blanc pur (E) ou une source de lumière blanche spécifique. Lorsque les coordonnées chromatiques d'une certaine couleur se déplacent progressivement en direction de la trajectoire spectrale à partir du point blanc W, la saturation de la couleur augmente progressivement jusqu'à ce qu'elle atteigne la trajectoire spectrale, avec une saturation maximale de 1.
Les couleurs sont représentées à l'aide de la longueur d'onde dominante et de la saturation, ce qui facilite la comparaison des différences de couleur. Les légères différences de couleur, représentées par les variations numériques de λd et ρepeut être affichée.
Pour deux couleurs, C1, C2les coordonnées chromatiques, la longueur d'onde dominante et la saturation sous le même éclairage sont indiquées dans le tableau 3-2. On constate que la longueur d'onde dominante de la couleur C1, C2 diffère de 0,052nm, et la saturation diffère de 7%.
Tableau 3-2 Comparaison des données colorimétriques entre C1 et C2
| Point de projection des couleurs | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. Instruments de mesure de la couleur des pierres précieuses
(1) Spectrophotomètre
Principe de fonctionnement : la distribution spectrale de l'énergie de la source lumineuse standard à l'intérieur de l'instrument étant connue, les valeurs tristimulus d'un objet peuvent être obtenues en mesurant sa réflectance spectrale.
(2) Colorimètre à valeur tristimulus
Il s'agit d'un instrument d'intégration photoélectrique qui mesure directement les trois valeurs de stimulus de la couleur d'un objet. Il simule principalement les trois réponses de l'observateur standard à la couleur grâce à une combinaison appropriée de filtres et de convertisseurs photoélectriques.
Actuellement, l'évaluation de la couleur des pierres précieuses repose principalement sur l'observation de l'œil humain. Par exemple, les émeraudes, les rubis et les diamants sont affectés par des facteurs environnementaux, ce qui entraîne une faible précision des mesures instrumentales ; par conséquent, l'application de la mesure instrumentale de la couleur à l'identification des pierres précieuses est relativement rare.
Section II Origines théoriques de la couleur minérale des pierres précieuses
Les minéraux des pierres précieuses sont de différentes couleurs, mais les raisons de leur coloration diffèrent également. Selon la théorie minéralogique classique, les origines de la couleur des minéraux des pierres précieuses peuvent être classées en couleurs idiochromatiques, couleurs allochromatiques et pseudo-couleurs.
1. Classification de la minéralogie classique Théorie de l'origine des couleurs
La théorie classique de la minéralogie est la théorie la plus fondamentale pour étudier les couleurs des minéraux précieux. Selon que la couleur du minéral est due au minéral lui-même, elle peut être divisée en trois catégories : idiochromatique, allochromatique et pseudo-colorée.
(1) Couleur idiochromatique
La couleur d'une gemme est formée par les composants chimiques inhérents au minéral dont elle est composée, connu sous le nom de couleur idiochromatique. Ces gemmes sont appelées gemmes de couleur idiochromatique. Leurs composants inhérents sont à l'origine de la couleur produite par les gemmes de couleur idiochromatique ; elles ont donc une bonne stabilité de couleur et ne sont pas facilement modifiables. Par exemple, la composition chimique de la turquoise estCuAl6(PO4)4(OH)8-5H2O, et le bleu ou le bleu-vert qu'il présente est causé par le Cu2+; la composition chimique de l'azurite est 2CuCO3 - Cu(OH)2et Cu2+ est également à l'origine de sa couleur bleue" ; le vert de l'olivine est produit par les ions de fer dans sa composition chimique (figure 3-8).

Il n'y a pas beaucoup de types de gemmes auto-colorées dans les minéraux gemmes naturels, les principales variétés étant la turquoise, la malachite, l'azurite, l'olivine, le grenat et la rhodochrosite. Le tableau 3-3 présente les couleurs, les éléments colorants et les compositions chimiques les plus courants des gemmes colorées.
Tableau 3-3 Éléments colorants communs, composition chimique et couleurs des pierres précieuses colorées
| Éléments de coloriage | Nom de la pierre précieuse | Composition chimique | Couleur |
|---|---|---|---|
| Le fer | Olivine | (Mg, Fe)2 (SiO4) | Vert |
| Almandine | Fe3Al2 (SiO4)3 | Rouge | |
| Chrome | Uvarovite | Ca3Cr2 (SiO4)3 | Vert |
| Cuprum | Malachite | Cu2Co3(OH)2 | Vert |
| Chrysocolle | (CuAl)2H2Si2O5(OH)4 - nH2O | Vert - Bleu | |
| Turquoise | CUAl6(PO4)4(OH)8.5H2O | Bleu ciel - Vert | |
| Azurite | 2CuCO3 - Cu(OH)2 | Bleu | |
| Manganèse | Spessartine-Garnet | Mn3Al2(SiO4)3 | Orange |
| Rhodochrosite | MnCO3 | Rose - Rouge | |
| Rhodonite | (Mn, Ca, Fe) - 5(Si5O15) | Rose - Rouge |
Copywrite @ Sobling.Jewelry - Fabricant de bijoux sur mesure, usine de bijoux OEM et ODM
Certaines pierres précieuses colorées peuvent changer de couleur dans certaines conditions. Par exemple, la turquoise et la malachite peuvent changer de couleur lorsqu'elles sont exposées à des températures élevées en raison de l'évaporation des molécules d'eau dans leur composition ; la rhodochrosite, une pierre précieuse carbonatée, peut se décomposer lorsqu'elle rencontre des acides (tels que l'acide chlorhydrique ou l'acide sulfurique), et sa couleur changera également en conséquence.
(2) Allochromatique-couleured
La couleur d'une pierre précieuse est causée par des traces ou des impuretés mineures en dehors de la composition chimique inhérente des minéraux constitutifs, connue sous le nom de couleur allochromatique. Ces pierres précieuses sont appelées pierres précieuses de couleur allochromatique.
Dans les minéraux des pierres précieuses, il existe de nombreuses variétés de pierres précieuses de différentes couleurs. Lorsqu'il n'y a pas d'impuretés dans la composition chimique de la pierre précieuse, elle est incolore et transparente ; lorsqu'elle contient des impuretés de différents éléments colorants, elle peut produire différentes couleurs.
Lorsque le corindon pur est incolore, il devient rubis lorsqu'il contient une petite quantité d'ions chrome ; lorsqu'il contient une petite quantité de fer et de titane, il se transforme en pierres précieuses bleues ou vertes. Les pierres précieuses similaires sont l'émeraude, le spinelle, la tourmaline, la jadéite, la calcédoine, la néphrite, etc. Les éléments colorants courants, les compositions chimiques et les pierres précieuses de couleur allochromatique sont présentés dans le tableau 3-4.
Tableau 3-4 Éléments colorants communs, composition chimique et pierres précieuses de couleur allochromatique
| Éléments de coloriage | Nom de la pierre précieuse | Composition chimique | Couleur |
|---|---|---|---|
| Chrome | Rubis | Al2O3 | Rouge |
| Émeraude | Être3Al2(Si6O18) | Vert | |
| Alexandrite | BeAl2O4 | Rouge-Vert | |
| Spinelle | MgAl2O4 | Rouge | |
| Calcédoine | SiO2 | Vert | |
| Le fer | Aigue-marine | Être3Al2Si6O18 | Bleu |
| Tourmaline | (Na, K, Ca) (Al, Fe3+, Cr)6(BO3)3Si6O18(OH)4 | Vert-brun | |
| Spinelle | MgAl2O4 | Jaune | |
| Nephrite | Ca2(Mg, Fe2+) 5 (Si4O11) 2 (OH)2 | Vert | |
| Vanadium | Tanzanite | Ca2Al3(SiO4)3(OH) | Bleu violet |
| Béryl vert | Être3Al2Si6O18 | Vert | |
| Titane | Benitoite | BaTiSi3O9 | Bleu |
| Saphir | Al2O3 | Bleu | |
| Manganèse | Béryl rouge | Être3Al2Si6O18 | Rouge |
| Rhodochrosite | MnCO3 | Rose | |
| Cobalt | Spinelle naturelle | MgAl2O4 | Bleu |
| Spinelle synthétique | MgAl2O4 | Bleu | |
| Nickle | Calcédoine verte | SiO2 | Vert |
(3) Pseudo-couleured
Les couleurs produites par les pseudo-couleurs ne sont pas liées à la composition chimique des minéraux des pierres précieuses. Elles sont toutefois dues à des changements structurels et de composition résultant de mélanges mécaniques ou de la formation de minéraux. Les pseudo-couleurs ne sont pas les couleurs des minéraux eux-mêmes, mais plutôt des couleurs causées par des structures spéciales formées par des influences externes. Par exemple, les belles couleurs d'interférence produites par l'interférence de la lumière réfléchie et incidente, comme l'effet de fluorescence de la labradorite et l'effet de jeu de couleurs de l'opale. La coloration causée par des inclusions fait également partie des pseudo-couleurs, comme les diamants noirs, dus à de nombreuses inclusions de graphite noir opaque à l'intérieur du diamant.
2. Ions colorants dans les minéraux précieux
Les éléments chimiques qui produisent les couleurs des pierres précieuses peuvent être les composants principaux ou secondaires. Les éléments métalliques de transition, en particulier les métaux de transition de la quatrième période (titane, vanadium, chrome, manganèse, fer, cobalt, nickel et cuivre), sont souvent appelés chromophores ou ions colorants. Ces huit éléments occupent des positions consécutives dans le tableau périodique, avec des numéros atomiques allant de 22 (Ti) à 29 (Cu). Les propriétés de base de ces éléments sont présentées dans le tableau 3-5.
Tableau 3-5 Propriétés de base des huit éléments de transition
| Nom de l'élément | Titane | Vanadium | Chrome | Manganèse | Le fer | Cobalt | Nickel | Cuivre |
|---|---|---|---|---|---|---|---|---|
| Symbole de l'élément | Ti | V | Cr | Mn | Fe | Co | Ni | Cu |
| Numéro atomique | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| Principaux états d'oxydation | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| Configuration des électrons de Valence | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
Ces huit éléments métalliques de transition présentent les caractéristiques suivantes :
① Les électrons de valence sont placés dans les orbitales d de l'avant-dernière enveloppe, et la formule générale de la configuration des électrons de valence des atomes d'éléments de transition est (n-1)d1-10nS1-2Ces éléments sont donc également appelés éléments du bloc d.
② Dans les métaux de transition, les orbitales d de l'avant-dernière enveloppe étant reliées aux orbitales s les plus externes et les orbitales d n'ayant pas encore atteint une structure stable, les électrons s et les électrons d peuvent participer partiellement ou totalement à la liaison, ce qui entraîne une série d'états d'oxydation variables pour les métaux de transition, les différents oxydes présentant des couleurs différentes dans les pierres précieuses.
③ Les ions présentent généralement une couleur parce qu'ils contiennent des électrons simples non appariés dans les orbitales d et que les niveaux d'énergie de ces électrons à l'état excité et à l'état fondamental sont relativement proches, ce qui permet à l'énergie de la lumière visible de les exciter. Des conditions d'excitation différentes peuvent également être à l'origine de couleurs différentes pour les pierres précieuses.
Si les électrons de spin de l'ion sont tous appariés, comme c'est le cas pour les ions dont la configuration électronique de valence est d0, d10, d10s2les électrons sont dans un état stable et ne sont pas facilement excités, ce qui fait que l'ion n'a pas de couleur ; ainsi, C+, Cr6+ et d'autres n'ont pas de couleur et ne peuvent pas produire de couleur dans les pierres précieuses.
Ces huit éléments métalliques de transition constituent la formation de la couleur dans les pierres précieuses de couleur naturelle courante. Des chromophores différents produisent des couleurs différentes dans des pierres précieuses différentes, et le même chromophore peut également produire des couleurs différentes. Les pierres précieuses naturelles courantes et les chromophores sont présentés dans le tableau 3-6.
Tableau 3-6 Couleurs présentées par les ions de métaux de transition dans les pierres précieuses naturelles courantes et les variétés de pierres précieuses
| Chromophore | Couleurs communes | Variétés de pierres précieuses |
|---|---|---|
| Ion de titane (Ti) | Bleu | Saphir, benitoite, Topaze |
| Ion vanadium (V) | Vert | Changement de couleur synthétique corindon, essonite, émeraude |
| Ion chrome (Cr) | Rouge, vert | Rubis, Corindon, Émeraude, Pyrope, Jade |
| Ion de manganèse (Mn) | Rose, rouge | Spessartine, Rhodolite, Béryl rouge |
| Ion ferreux (Fe) | Bleu, vert, jaune | Saphir, olivine, aigue-marine, tourmaline, spinelle |
| Ion de cobalt (Co) | Bleu | Spinelle synthétique, staurolite couleur cobalt |
| Ion de nickel (Ni) | Vert | Calcédoine verte |
| Ion cuivre (Cu) | Bleu, bleu-vert | Malachite, turquoise, azurite |
Les différents ions chromophores produisent des couleurs différentes dans les pierres précieuses, ce qui se traduit par des spectres d'absorption aux caractéristiques distinctes. Pour les ions chromophores courants, les spectres d'absorption ont une signification d'identification typique.
(1) Le spectre d'absorption des ions chrome
Le spectre d'absorption des ions chrome est principalement caractérisé par de nombreuses lignes d'absorption étroites dans la région rouge, les deux plus fortes étant situées dans la région rouge foncé et deux autres dans la région orange. La région jaune-vert présente une large bande d'absorption, dont la largeur, la position et l'intensité sont liées à la profondeur de la couleur de la gemme. Il peut y avoir plusieurs bandes étroites dans la région bleue, tandis que la région violette est entièrement absorbée. Les ions de chrome produisent principalement des couleurs rouges et vertes, qui varient d'une gemme à l'autre, et les spectres d'absorption présentent certaines différences. Par exemple, les rubis présentent trois lignes d'absorption dans la région rouge, une large bande d'absorption dans la région jaune-vert, trois lignes d'absorption dans la région bleue et une absorption totale dans la région violette ; les émeraudes présentent des lignes d'absorption dans la région rouge, une faible bande d'absorption dans la région orange-jaune, de faibles lignes d'absorption dans la région bleue et une absorption totale dans la région violette ; et l'alexandrite présente des lignes d'absorption dans la région rouge, une bande d'absorption dans la région jaune-vert, une ligne d'absorption dans la région bleue et une absorption totale dans la région violette. Les spectres d'absorption de ces trois gemmes sont illustrés à la figure 3-9.

(2) Caractéristiques du spectre d'absorption de l'ion de fer
Les ions de fer produisent différentes couleurs dans différentes pierres précieuses et ont un fort effet colorant, mais le spectre d'absorption des ions de fer varie considérablement. Lorsque la pierre précieuse est verte, elle produit une absorption dans la zone rouge, et lorsqu'elle est rouge, elle produit une caractéristique d'absorption dominée par la zone bleue, avec la principale ligne d'absorption caractéristique située dans les zones verte et bleue. Par exemple, les ions de fer dans l'olivine apparaissent en vert olive, le spectre d'absorption montrant principalement trois bandes d'absorption étroites dans la région bleue à 453nm, 473nm et 493nm ; l'almandine rouge a un spectre d'absorption du fer typique, avec trois bandes d'absorption étroites et fortes à 504nm, 520nm et 573nm dans la région jaune-vert, communément appelée dans l'industrie la "fenêtre du fer". Le spectre d'absorption du saphir jaune présente trois bandes d'absorption étroites dans la région bleue à 450nm, 460nm et 470nm (figure 3-10).
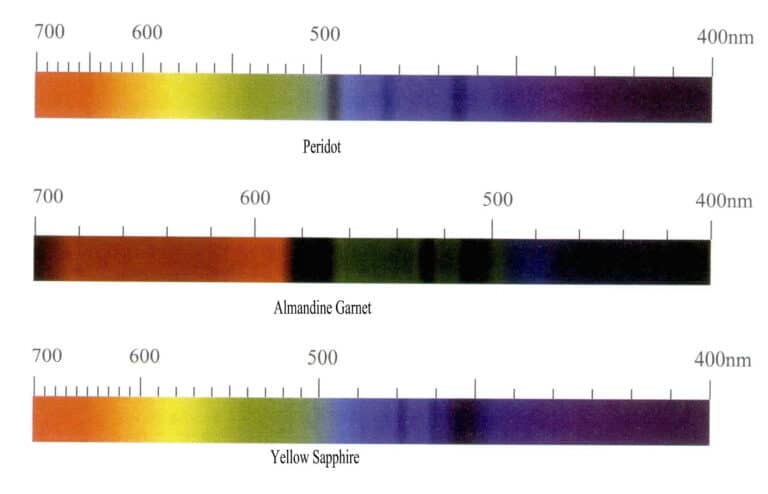
(3) Caractéristiques du spectre d'absorption des ions manganèse
Les ions manganèse forment principalement du rose, de l'orange et du rouge dans les pierres précieuses, le spectre d'absorption montrant principalement une forte absorption dans la région violette, s'étendant à la région ultraviolette, et une certaine absorption dans la région bleue. Par exemple, les caractéristiques du spectre d'absorption de la rhodochrosite rose présentent trois bandes d'absorption à 410nm, 450nm, 540nm ; les lignes du spectre d'absorption de la spessartine présentent principalement trois bandes d'absorption à 410nm, 420nm, 430nm et des lignes d'absorption à 460nm, 480nm, et 520nm. Parfois, il peut y avoir deux lignes d'absorption à 504nm, 573nm (figure 3-11).

(4) Caractéristiques du spectre d'absorption des ions cobalt
Les ions cobalt ont un fort effet colorant, apparaissant généralement en bleu vif dans les pierres précieuses, avec le spectre d'absorption montrant principalement trois bandes d'absorption fortes et larges dans la région jaune-vert. En raison de la faible abondance du cobalt dans la croûte terrestre, il existe très peu de pierres précieuses naturelles colorées par des ions cobalt. Le spectre d'absorption des ions cobalt indique également la présence de pierres précieuses synthétiques, telles que le spinelle bleu synthétique et le verre de cobalt. Le spinelle bleu synthétique présente trois fortes bandes d'absorption dans les régions jaune-vert et orange-jaune, la bande d'absorption de la région verte étant la plus étroite ; les lignes d'absorption du verre de cobalt présentent principalement trois fortes bandes d'absorption dans les régions jaune-vert et orange-jaune, la bande d'absorption de la région jaune étant la plus étroite (figure 3-12).

3. Coloriage des éléments des terres rares
Les recherches sur l'influence des traces de terres rares sur la couleur des pierres précieuses sont de plus en plus approfondies. Les couleurs des éléments des terres rares sont plus vives et leurs propriétés physicochimiques sont également très stables. Les éléments des terres rares comme l'apatite et la fluorine peuvent également colorer les pierres précieuses naturelles. Différents éléments de terres rares peuvent être ajoutés à des pierres synthétiques et traitées de manière optimale afin d'obtenir des pierres de différentes couleurs, comme le jaune du cérium et le bleu du néodyme.
Les éléments de terre rare qui colorent les pierres précieuses sont principalement les lanthanides et les actinides du tableau périodique des éléments chimiques et les couleurs qu'ils peuvent produire sont indiquées dans le tableau 3-7.
Tableau 3-7 Éléments des terres rares et leurs couleurs dans les pierres précieuses courantes
| Symbole de l'élément | La | Ce | Nd | Pr | Dy | Sm | Er | Tm | U |
|---|---|---|---|---|---|---|---|---|---|
| Nom complet | Lanthane | Cérium | Néodyme | Praséodyme | Dysprosium | Samarium | Erbium | Thulium | Uranium |
| Couleur | Incolore | Jaune | Bleu | Vert | Jaune clair | Jaune clair | Rose | Vert clair | Blanc argenté |
Les éléments de terre rare ont des spectres d'absorption caractéristiques, formant souvent des lignes fines uniques. Par exemple, l'apatite jaune contient souvent l'élément de terre rare Ce, avec des lignes fines d'absorption caractéristiques dans la région jaune. Cependant, l'uranium ne produit pas un jaune brillant ; il peut générer des lignes spectrales d'absorption distinctes. Par exemple, plus de dix raies d'absorption peuvent apparaître dans le zircon vert dans différentes zones de couleur (figure 3-13).

Section III Couleurs produites par les défauts du cristal et les centres de couleur
Dans la nature, les minéraux sont divisés en cristaux et non cristaux en fonction de leur degré de cristallisation. La plupart des pierres précieuses, telles que les rubis, les saphirs, les diamants, les émeraudes et les quartz, sont des cristaux ; certaines pierres précieuses organiques, telles que l'ambre et le corail, sont non cristallines. Les structures cristallines ont une structure en treillis, dans laquelle leurs particules internes (atomes, ions ou molécules) sont disposées selon un schéma périodique régulier dans l'espace tridimensionnel, et les cristaux peuvent spontanément prendre des formes polyédriques ; les non-cristaux sont des corps amorphes dont la structure n'est pas en treillis et qui ne peuvent pas prendre de formes polyédriques, comme le verre, la colophane et la résine.
L'exemple le plus typique de la différence entre les cristaux et les solides amorphes est le quartz et le verre. Le quartz naturel est formé à partir d'un matériau fondu SiO2 dans le magma qui se refroidit dans les cavités de la croûte terrestre. La couche externe des sphères de quartz communes est de l'agate, qui ne présente pas la forme cristalline, tandis que la couche interne présente la forme cristalline du quartz. Les principaux composants chimiques du verre et du quartz sont SiO2Le quartz est un cristal dont les ions de silicium et d'oxygène sont disposés de manière ordonnée, tandis que le verre est un solide amorphe dont les ions de silicium et d'oxygène sont disposés de manière chaotique, sans régularité, comme le montre la figure 3-14.
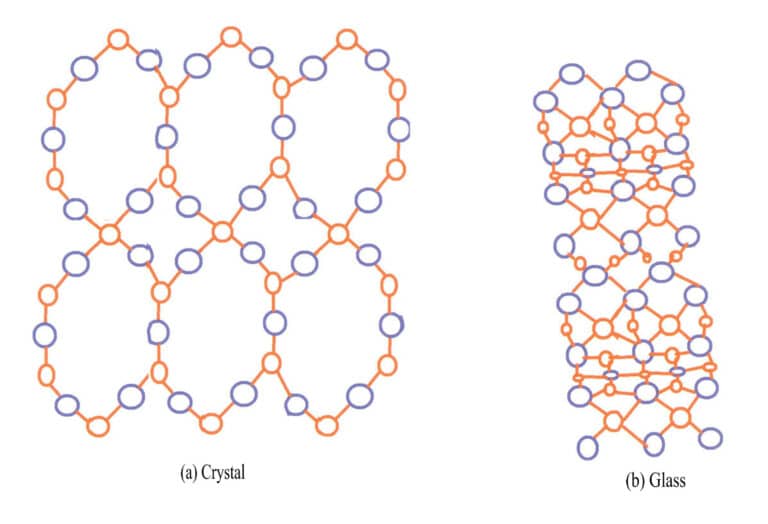
La plupart des cristaux de pierres précieuses sont colorés par des ions impurs, comme les rubis, les émeraudes et les tourmalines. Certaines pierres précieuses, bien que dépourvues d'ions chromophores, sont colorées en raison de défauts dans leur structure cristalline. Les pierres précieuses naturelles produites dans la nature peuvent changer de couleur en raison de conditions externes, telles que l'irradiation et l'ionisation, qui modifient la structure cristalline. L'exemple le plus courant est le quartz fumé, dont la couleur se développe en raison de la formation de centres de couleur à partir de lacunes induites par l'irradiation. Le quartz fumé irradié artificiellement a un principe de formation similaire à celui du quartz fumé naturel, sauf que l'irradiation artificielle crée rapidement de la couleur.
1. Défauts et types de cristaux
Le phénomène par lequel la disposition des particules s'écarte des règles de la structure du réseau (les particules subissent une répétition périodique de translation dans l'espace tridimensionnel) dans une zone locale de la structure cristalline de la pierre précieuse est appelé défaut de réseau. Les causes sont liées aux vibrations thermiques des particules dans le cristal de la pierre précieuse, aux contraintes externes, aux températures et pressions élevées, à l'irradiation, à la diffusion, à l'implantation d'ions et à d'autres conditions.
Par exemple, les diamants cristallisés dans l'environnement à haute température et à haute pression du manteau supérieur lorsqu'ils sont rapidement transportés près de la surface de la Terre par le magma hôte (kimberlite ou lamproïte), le changement rapide des conditions de température et de pression et les collisions mutuelles entre les cristaux et les roches environnantes peuvent facilement entraîner des changements locaux dans la structure des cristaux de diamant intrusifs, entraînant des défauts de réseau qui modifient la couleur des diamants initialement incolores, formant des diamants brun-jaune, bruns et roses.
La présence de défauts cristallins a un impact significatif sur les propriétés des cristaux. En réalité, les cristaux présentent plus ou moins de défauts. Une quantité modérée de certains défauts ponctuels peut améliorer considérablement la conductivité des matériaux semi-conducteurs et la luminescence des matériaux luminescents, jouant ainsi un rôle bénéfique. En revanche, les défauts tels que les dislocations peuvent rendre les matériaux susceptibles de se fracturer, réduisant la résistance à la traction des cristaux ne présentant pratiquement aucun défaut de réseau à une fraction de celle-ci.
Dans un cristal idéalement parfait, les atomes sont strictement disposés dans un réseau régulier et périodique en des points spécifiques de l'espace. Cependant, au cours de la croissance et de la formation des cristaux, en raison de l'influence des environnements de croissance tels que la température, la pression et la concentration des composants du milieu, la morphologie du cristal après la croissance peut parfois s'écarter de la structure cristalline idéale. Tout écart par rapport à la structure cristalline idéale peut être appelé défaut cristallin. Les défauts cristallins ont un impact significatif sur les propriétés physiques et chimiques des cristaux, et de nombreuses disciplines sont liées aux défauts cristallins, comme le dopage ionique dans la science des matériaux. La couleur des pierres précieuses est largement liée aux défauts cristallins qu'elles contiennent. C'est l'une des causes de la couleur des pierres précieuses - les centres de couleur.
Il existe de nombreux types de défauts de structure cristalline, qui peuvent être classés en quatre catégories en fonction de l'étendue de leur distribution dans l'espace tridimensionnel : défauts ponctuels, défauts linéaires, défauts de surface et défauts de volume.
(1) Défauts ponctuels
D'autres atomes remplacent certains atomes dans un cristal idéal, d'autres sont dopés ou des vides sont créés. Certains atomes du cristal sont remplacés ou manquent à cause d'atomes externes, et ces changements perturbent l'arrangement périodique du réseau régulier du cristal, provoquant des changements dans le champ potentiel des particules et entraînant l'incomplétude de la structure cristalline, limitée à certaines positions, n'affectant que quelques atomes proches. L'impact des défauts ponctuels sur le cristal est minime et les types de défauts ponctuels les plus courants sont les défauts de position dans le réseau, les défauts de composition et les défauts de charge (figure 3-15).
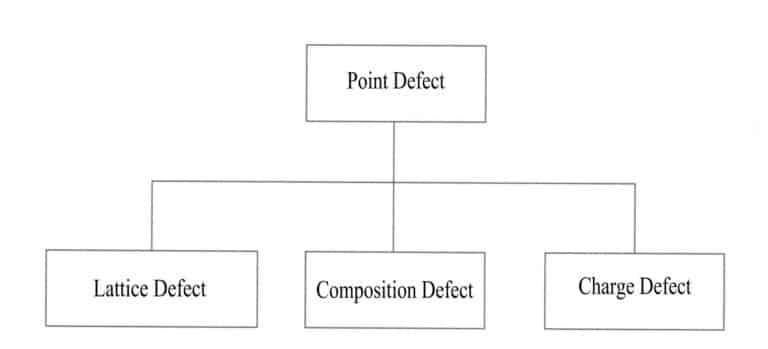
(2) Défauts de ligne
Les défauts linéaires sont de très petite taille dans deux directions et s'étendent principalement plus loin dans une autre direction. Ils sont également connus sous le nom de défauts unidimensionnels et sont principalement constitués de diverses dislocations. Les dislocations peuvent être considérées comme le produit d'un glissement local du réseau le long d'un certain plan atomique. Le glissement ne pénètre pas l'ensemble du réseau ; le défaut cristallin se termine à l'intérieur du réseau, provoquant un arrangement désordonné des particules à la limite entre les parties glissées et non glissées du réseau, connu sous le nom de dislocation. Cette limite, la ligne d'intersection entre les zones glissées et non glissées, est appelée ligne de dislocation. Il existe deux types fondamentaux de dislocations : lorsque le cristal est soumis à des forces de compression, le plan de glissement des particules forme une ligne de dislocation avec le plan non glissé, et la ligne de dislocation est perpendiculaire à la direction de glissement, appelée dislocation d'arête, également appelée dislocation en coin ; sous l'effet d'une contrainte de cisaillement, le glissement se produit entre les plans, et les lignes de dislocation qui se croisent dans la partie glissée du cristal sont parallèles à la direction de glissement, appelée dislocation en vis (figure 3-16).
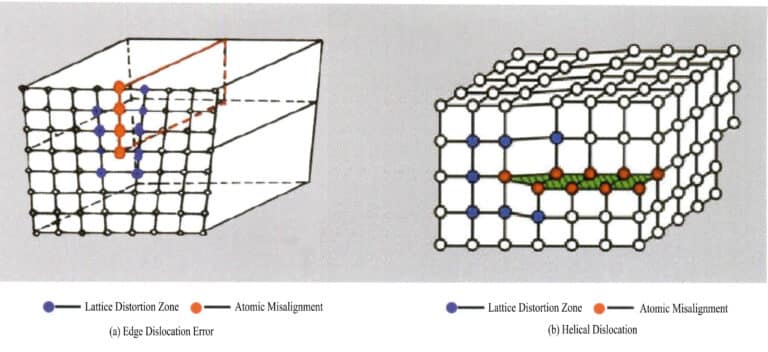
(3) Défauts de surface
Le défaut de surface le plus simple est le défaut d'empilement, divisé en défauts d'empilement intrinsèques (où un plan cristallin est enlevé) et en défauts d'empilement extrinsèques (où une couche atomique est insérée dans le cristal). Ces défauts se produisent dans une fourchette de quelques espacements atomiques de part et d'autre d'un certain plan le long du réseau ou entre les grains. Ils comprennent principalement les défauts d'empilement et les interfaces à l'intérieur et entre les cristaux, tels que les limites de grains à petit angle, les parois de domaine et les limites jumelles et intergranulaires.
(4) Défauts de volume
Les défauts de volume sont des défauts qui existent à des degrés divers dans les trois directions, qui sont des défauts tridimensionnels, tels que les fissures encastrées, les structures maillées, les structures familiales, les jumeaux et diverses inclusions dans les pierres précieuses.
2. Centres de couleur dans les pierres précieuses
Les centres de couleur sont un cas particulier de défauts de réseau, se référant généralement à des défauts de réseau dans les pierres précieuses qui peuvent absorber sélectivement l'énergie de la lumière visible et produire de la couleur, appartenant aux types de couleurs structurelles les plus typiques. Dans certains cas, les électrons non appariés qui produisent de la couleur peuvent également apparaître dans des ions d'éléments non transitionnels ou dans des défauts cristallins formés en raison d'un manque d'électrons, ce que sont les centres de couleur. Les défauts ponctuels dans les cristaux ioniques peuvent provoquer l'absorption de la lumière visible, ce qui fait que des cristaux initialement transparents apparaissent colorés ; ces types de défauts ponctuels qui peuvent absorber la lumière visible sont généralement appelés centres de couleur. De nombreux types de pierres précieuses naturelles produisent de la couleur à partir de centres de couleur, comme la fluorine pourpre, le cristal fumé et les diamants verts.
Dans le processus d'optimisation du traitement des pierres précieuses, certaines pierres précieuses naturelles et artificielles peuvent également avoir des centres de couleur générés par le rayonnement, comme les diamants bleus, jaunes, rouges, verts et les topazes bleues qui changent de couleur sous l'effet du rayonnement, et les topazes bleues, parmi lesquelles certaines couleurs sont relativement stables et ne disparaissent que lorsqu'elles sont chauffées ; d'autres couleurs sont instables et peuvent s'estomper même à la température ambiante. Ce type de centre coloré est étroitement lié à la structure cristalline de la pierre précieuse, comme dans le cas des diamants verts, où la couleur est due à la présence d'espaces vacants dans la structure cristalline, mais ce défaut structurel peut également être éliminé par irradiation, rendant le diamant incolore. Les types courants de centres de couleur dans les pierres précieuses sont les "centres de couleur des électrons" et les "centres de couleur des trous".
(1) Centre de couleur des électrons (centre F)
Les centres de couleur électroniques sont des centres de couleur formés lorsque des électrons se trouvent dans des vides de défauts cristallins causés par des vides anioniques dans la structure cristalline de la pierre précieuse. Lorsque l'anion est absent, la vacance devient un piège à électrons chargé positivement qui retient les électrons. Si une vacance capture un électron et le lie à cette vacance, l'électron devient excité et absorbe sélectivement une certaine longueur d'onde d'énergie pour devenir coloré. Par conséquent, un centre de coloration électronique se compose d'une cavité anionique et d'un électron lié par le champ électrique de cette cavité.
La fluorine pourpre est une couleur produite par les centres de couleurs électroniques. La fluorine (CaF2) appartient au système cristallin isométrique, avec chaque Ca2+ connecté à deux F– [Figure 3-17 (a)]. Dans certains cas, la valeur F– dans la fluorine peut quitter sa position normale. Une vacance apparaît à l'emplacement d'origine de la F– et pour maintenir la neutralité électrique du cristal, une entité chargée négativement doit occuper cette vacance. Un électron d'un certain atome du cristal devient l'entité chargée négativement qui occupe cette place [figure 3-17 (b)]. Cela crée un "centre de couleur", connu sous le nom de centre de couleur électronique. Dans la fluorine, les centres de couleur électroniques absorbent la lumière visible, produisant du violet.
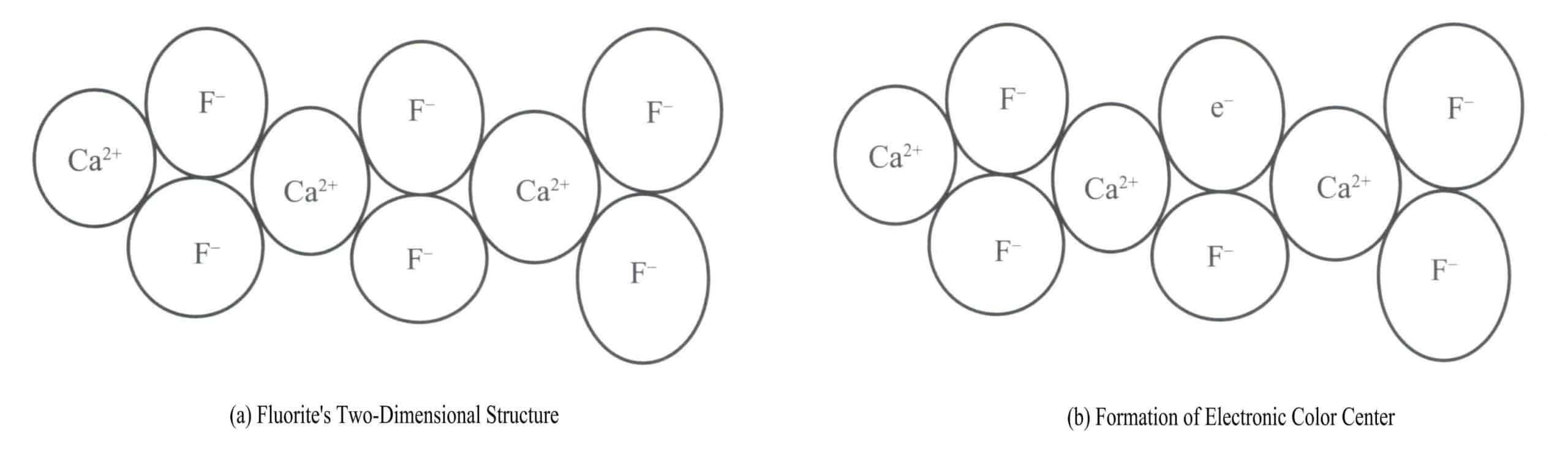
(2) Centres de couleur des trous (centres V)
Le centre de couleur vacant est formé par des facteurs externes, lorsque les cations créent des électrons vacants. Cela signifie que les électrons sont éjectés de leur position d'origine, laissant derrière eux un électron non apparié. La couleur s'explique par le fait que lorsque des cations vacants se forment dans le cristal, les anions proches des cations vacants libèrent des électrons sous l'influence de l'énergie externe, formant des électrons non appariés qui absorbent la lumière visible et produisent de la couleur, afin de parvenir à un équilibre des charges. Par exemple, dans les diamants et les topazes bleues irradiés, l'irradiation fournit de l'énergie pour activer les électrons, provoquant le déplacement des ions ou des atomes dans le réseau, formant ainsi des défauts structurels et des centres de couleur dus à l'irradiation.
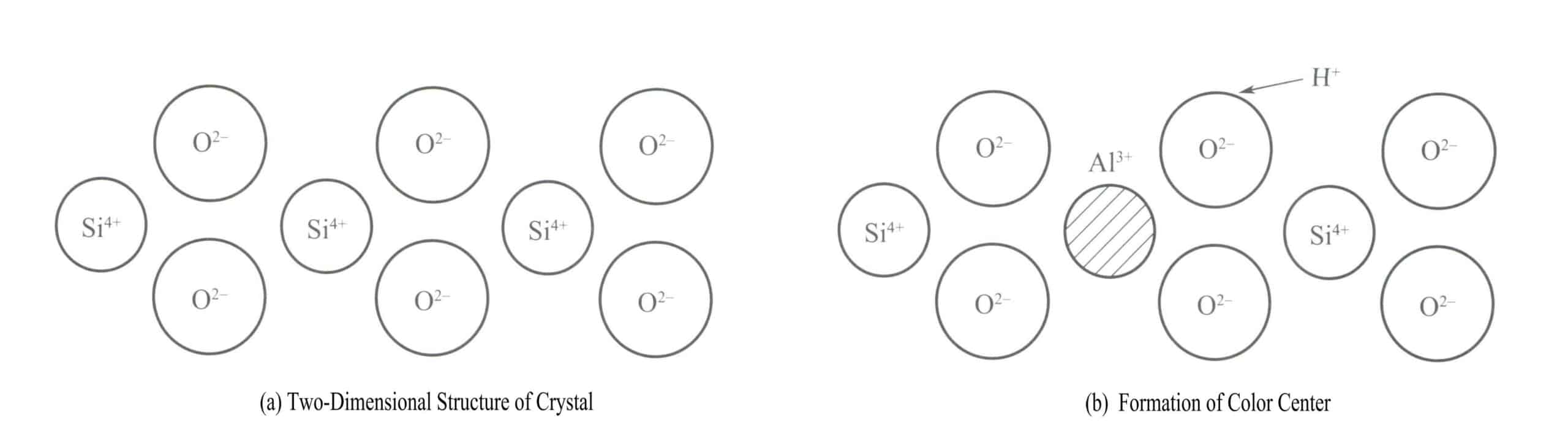
Un exemple classique de centre de couleur dans un cristal est la coloration du cristal fumé. La structure cristalline du quartz est un tétraèdre silicium-oxygène, avec du silicium dans un état à quatre coordinations, comme le montre le diagramme structurel bidimensionnel de la figure 3-18(a). Tous les 10 000 Si4+ ont été remplacés par des atomes d'Al3+et lorsque Al3+ se substitue à Si4+ dans le cristal, Al3+ doit être entouré de quelques ions alcalins (tels que Na+ ou H+) pour maintenir la neutralité électrique. Cependant, ces ions se trouvent souvent à une certaine distance de l'Al3+.
Lorsque le quartz est irradié par des rayons X, des rayons γ et d'autres sources de rayonnement, l'énergie des atomes d'oxygène adjacents à l'Al3+ augmente, ce qui permet à l'un des électrons de sa paire d'être éjecté de sa position normale. H+ capturera cet électron pour former H . Un rayonnement de haute énergie provoque la formation de l'O2- avec plus d'électrons de valence pour libérer un électron, formant un [A1O4]4- et le centre de couleur de la vacance [A1O4]4- L'amas atomique absorbe la lumière visible pour produire la couleur, formant le quartz fumé.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ capture des électrons pour devenir H, qui est incolore et n'absorbe pas la lumière visible. Si l'intensité de l'irradiation est élevée et qu'il y a suffisamment d'Al3+ dans le cristal, le quartz peut être irradié au noir. Comme il y a souvent une vacance à l'endroit où un électron est éjecté, ce type de centre coloré est appelé "centre coloré de vacance".
Au cours de l'histoire géologique, le cristal fumé naturel est principalement formé par un rayonnement à faible dose de longue durée provenant de matériaux radioactifs. Le chauffage peut éliminer la couleur ; lorsque ce cristal fumé est chauffé à environ 400℃, les électrons éjectés retournent à leur position d'origine, tous les électrons s'apparient et le quartz redevient incolore ; s'il est à nouveau irradié, il peut redevenir fumé [Figure 3-18 (b)].
L'améthyste a les mêmes centres de couleur pour la vacance, mais son impureté est le fer au lieu de l'aluminium. Lorsque l'impureté Fe 3+ remplace Si4+ dans le quartz, les changements suivants se produisent lorsqu'il est irradié par des rayons de haute énergie :
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
Similaire au principe de formation du cristal fumé, il produit une couleur pourpre due à la formation de [FeO4]4- L'améthyste est un centre de couleur troué après avoir été irradiée. Lorsque cette améthyste est chauffée, elle devient jaune, devenant citrine, et en continuant à chauffer, elle devient incolore. En général, la température de chauffage est relativement basse, environ 400℃. La couleur pourpre de l'améthyste traitée thermiquement peut être restaurée en irradiant à nouveau les centres de couleur. L'améthyste synthétique est également synthétisée sur la base de ce principe.
Dans certaines pierres précieuses, quelques groupes d'atomes d'impuretés peuvent également former des centres de couleur et présenter de la couleur. Par exemple, pendant la croissance du béryl et sous irradiation radioactive, peut perdre un électron pour devenir , formant une bande d'absorption rouge-vert qui produit une couleur bleue. Il existe de nombreux centres de couleur dans les diamants, dont la plupart sont dus à la formation de lacunes ou de dislocations dans la structure dans des conditions externes, et les couleurs sont généralement très stables.
L'étude de la couleur induite par le centre de la couleur est relativement difficile et nécessite diverses techniques telles que la spectroscopie et la résonance paramagnétique électronique. Des recherches antérieures montrent que certaines caractéristiques typiques de la couleur induite par le centre de la couleur sont relativement claires. Le tableau 38 résume les couleurs et les causes de la couleur induite par le centre de la couleur dans les pierres précieuses courantes.
Tableau 3-8 Couleurs et causes de la couleur Couleur induite par le centre dans les pierres précieuses courantes
| Types de pierres précieuses | Couleur | Cause |
|---|---|---|
| Diamant | Vert | Carbone vacant GR1 centre de couleur dans le diamant |
| Jaune | Structure manquante des agrégats de diamant N3 | |
| Orange | Natoms et défauts de centre de couleur H3, H4 | |
| Cristal | Couleur fumée | Les postes vacants générés par Al3+ en remplaçant Si4+ liées aux radiations |
| Jaune | En rapport avec Al3+il peut également être généré par rayonnement | |
| Pourpre | Fe3+ remplace le poste vacant créé par Si4+ | |
| Pierre précieuse corindon | Jaune | La couleur est instable, la raison des défauts structurels est inconnue. |
| Topaze | Bleu | La couleur est stable, la raison des défauts structurels est inconnue. |
| Jaune | La couleur est stable, la cause des défauts structurels est inconnue. | |
| Rouge brunâtre | La couleur est instable, la cause des défauts structurels est inconnue. | |
| Tourmaline | Rouge | En rapport avec Mn3+ peut également être causée par des radiations |
| Béryl | Bleu | En rapport avec le CO32- peut également être causée par l'irradiation |
| Fluorite | Pourpre | Électronique e- remplace F- pour produire |
Le principe des centres de couleur est également utilisé pour améliorer la couleur des pierres précieuses naturelles dans le cadre de l'amélioration des pierres précieuses. La plupart des méthodes utilisent l'irradiation pour modifier la couleur des pierres précieuses. Certains centres de couleur sont relativement stables, tandis que certaines variétés de pierres précieuses se décolorent rapidement, ce qui rend cette méthode d'amélioration moins significative pour ces pierres précieuses. Le tableau 3-9 énumère certaines couleurs produites par les centres de couleur, y compris les centres de couleur stables, les centres de couleur instables et les couleurs produites par d'autres facteurs possibles.
Tableau 3-9 Couleurs produites par les centres de couleurs
| Essentiellement stable à la lumière | Améthyste, fluorine (violet-rouge), diamants irradiés (vert, jaune, brun, noir, bleu, rose) ; quelques topazes naturelles ou irradiées (bleu) |
|---|---|
| S'estompe rapidement à la lumière | Béryl vert (bleu profond) ; topaze irradiée (brun ou beige) ; saphir irradié (jaune) ; sodalite violette irradiée aux ultraviolets (rouge-violet). |
| Autres couleurs que les centres de couleurs peuvent produire | Sylvine (bleu) ; halite (bleu ou jaune) ; zircon (brun) ; calcite (jaune) ; barytine, célestine (bleu) ; amazonite (bleu à vert) |