Εξερευνήστε τα υλικά από καθαρό ασήμι και κράμα αργύρου που χρησιμοποιούνται για κοσμήματα
Ένας ολοκληρωμένος οδηγός για τις ιδιότητες και τα χαρακτηριστικά του καθαρού αργύρου και των κραμάτων αργύρου
Το ασήμι έχει γοητευτική λευκή λάμψη, υψηλή χημική σταθερότητα και συλλεκτική αισθητική αξία, γεγονός που το καθιστά ιδιαίτερα αγαπητό στους ανθρώπους (ιδίως στις γυναίκες), κερδίζοντας έτσι τον τίτλο του "μετάλλου των γυναικών". Χρησιμοποιείται ευρέως για κοσμήματα, διακοσμητικά αντικείμενα, ασημένια σκεύη, επιτραπέζια σκεύη, συγχαρητήρια δώρα, μετάλλια και αναμνηστικά νομίσματα. Τα ασημένια κοσμήματα έχουν ευρεία αγορά στις αναπτυσσόμενες χώρες και τα ασημένια επιτραπέζια σκεύη είναι δημοφιλή στις οικογένειες. Τα αναμνηστικά ασημένια νομίσματα είναι εξαιρετικά σχεδιασμένα, εκδίδονται σε περιορισμένες ποσότητες και έχουν τη λειτουργία της διατήρησης και της αύξησης της αξίας, γεγονός που τα καθιστά ιδιαίτερα περιζήτητα από τους συλλέκτες νομισμάτων και τους επενδυτές.

Πίνακας περιεχομένων
Ενότητα Ⅰ Βασικές ιδιότητες του αργύρου
1. Φυσικές ιδιότητες του αργύρου
Το ασήμι είναι στοιχείο της ομάδας IB της 5ης περιόδου του περιοδικού πίνακα, με σύμβολο στοιχείου Ag, ατομικό αριθμό 47 και σχετική ατομική μάζα 107,870. Ο άργυρος έχει πολύ υψηλή ανακλαστικότητα για το ορατό φως, που φτάνει τα 92%-96% στην περιοχή μήκους κύματος 380-780 nm, την υψηλότερη μεταξύ όλων των μεταλλικών στοιχείων, σημαντικά υψηλότερη από τα άλλα πολύτιμα μεταλλικά στοιχεία (Σχήμα 4-1). Ως εκ τούτου, ο άργυρος εμφανίζεται φωτεινός
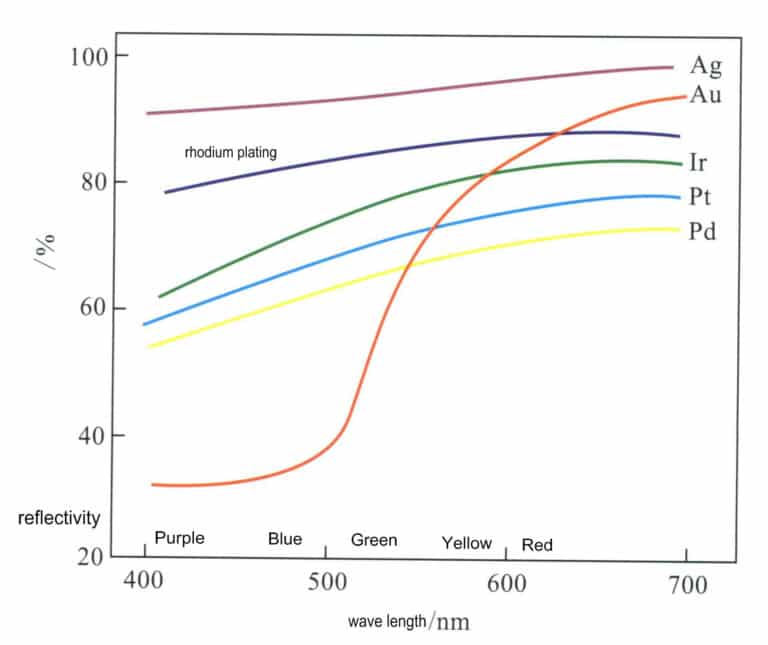
Οι κύριες φυσικές ιδιότητες του αργύρου παρουσιάζονται στον Πίνακα 4-1. Σε θερμοκρασία δωματίου, η πυκνότητα του αργύρου είναι 10,49 g/cm3και καθώς αυξάνεται η θερμοκρασία, η πυκνότητα του αργύρου μειώνεται, πέφτοντας στα 9,35 g/cm3 λίγο πριν λιώσει. Το ασήμι είναι ο καλύτερος αγωγός του ηλεκτρισμού και της θερμότητας μεταξύ όλων των μετάλλων, γεγονός που αυξάνει τη δυσκολία για την τρισδιάστατη εκτύπωση και τη συγκόλληση με λέιζερ, καθώς η θερμότητα που εφαρμόζεται τοπικά μεταφέρεται γρήγορα στο περιβάλλον, καθιστώντας δύσκολη τη συγκέντρωση της θερμότητας.
Πίνακας 4-1 Κύριες φυσικές ιδιότητες και τιμές δεικτών του αργύρου
| Φυσικές ιδιότητες | Τιμές δείκτη | Φυσικές ιδιότητες | Τιμές δείκτη |
|---|---|---|---|
| Συντεταγμένες χρώματος | L* = 95,8, a* =-0,7, b* = 5,3 | Συντελεστής γραμμικής διαστολής (0-100℃) | 19.2 x 10-6/℃ |
| Πυκνότητα (20℃) | 10,49 g/cm3 | Ειδική αντίσταση (25℃) | 1.59 x 10-6Ω⸳cm |
| Σημείο τήξης | 961.78 | Ειδική θερμοχωρητικότητα (25℃) | 25,41 J/(mol⸳K) |
| Σημείο βρασμού | 2177 | Θερμότητα σύντηξης | 11,30 kJ/mol |
| Πίεση ατμών ( τήξη ) | 0,38 Pa | Θερμότητα εξάτμισης | 284,6 kJ/mol |
| Θερμική αγωγιμότητα (25℃) | 433 W/(m⸳K) | Θερμοκρασία Debye ϴd | 215 K |
| Συντελεστής θερμικής διάχυσης (0℃) | 1.75 m2/s | Μαγνητική επιδεκτικότητα | -0.15 x 10-6 cm3/g |
2. Χημικές ιδιότητες του αργύρου
Οι χημικές ιδιότητες του αργύρου δεν είναι αντιδραστικές και η χημική του σταθερότητα είναι καλύτερη από εκείνη των μετάλλων όπως ο σίδηρος και ο χαλκός. Δεν αντιδρά με το οξυγόνο, το υδρογόνο, τα αδρανή αέρια και τα οργανικά αέρια σε θερμοκρασία δωματίου, και ακόμη και σε υψηλές θερμοκρασίες, δεν αντιδρά με το υδρογόνο ή τα αδρανή αέρια, καθιστώντας τον επιρρεπή στη διάβρωση και τον αποχρωματισμό.
Ο άργυρος έχει ισχυρή συγγένεια με το θείο και σε ατμόσφαιρες που περιέχουν επιβλαβείς ουσίες όπως το H2S, SO2, COS (καρβονυλοσουλφίδιο), και σε υδατικά διαλύματα που περιέχουν σουλφίδια, είναι επιρρεπές στη διάβρωση, σχηματίζοντας αδιάλυτο μαύρο Ag2S στην επιφάνειά του και η συμπεριφορά διάβρωσης παρουσιάζει κυρίως ηλεκτροχημικά χαρακτηριστικά. Όταν ο άργυρος αφήνεται στον αέρα, η επιφάνειά του σχηματίζει σταδιακά μαύρο Ag2S, με αποτέλεσμα τα κοσμήματα να γίνονται θαμπά και να αποχρωματίζονται. Αυτή η ιδιότητα του αργύρου επηρεάζει σοβαρά την αξία του ως πολύτιμο μέταλλο. Ag2Το S μπορεί να αποσυντεθεί σε μεταλλικό ασήμι και SO2 όταν θερμαίνεται στον αέρα.
Σε θερμοκρασία δωματίου, ο άργυρος διαλύεται στο νιτρικό οξύ και στο πυκνό θειικό οξύ, αλλά είναι αδιάλυτος στο υδροχλωρικό οξύ και στο αραιό θειικό οξύ. Διαλύεται σε υδροχλωρικό οξύ, θειικό οξύ, νιτρικό οξύ και βασιλικό νερό όταν θερμαίνεται. Όπως και ο χρυσός, ο άργυρος αντιδρά εύκολα με το βασιλικό ύδωρ και τα κορεσμένα χλωριωμένα οξέα- ο άργυρος σχηματίζει ίζημα AgCl, το οποίο μπορεί να χρησιμοποιηθεί για το διαχωρισμό του χρυσού και του αργύρου.
Όπως και ο χρυσός, ο άργυρος έχει καλή αντοχή στη διάβρωση σε αλκαλικά διαλύματα και λιωμένα αλκαλικά μέταλλα, καθιστώντας τον κοινό υλικό χωνευτηρίου για λιωμένο NaOH και KOH.
Ο άργυρος μπορεί να συνδυαστεί αργά με αλογόνα σε θερμοκρασία δωματίου, αλλά υπό συνθήκες θέρμανσης, ο άργυρος μπορεί να αντιδράσει πολύ γρήγορα με αλογόνα σχηματίζοντας αλογονίδια αργύρου. Ο άργυρος διαλύεται σε ορισμένους συμπλοκοποιητές κορεσμένους με αέρα (όπως τα κυανίδια των αλκαλικών μετάλλων της ομάδας ⅠA και τα μέταλλα αλκαλικών γαιών της ομάδας ⅡA, διαλύματα κυανίου που περιέχουν οξυγόνο και όξινα διαλύματα θειουρίας που περιέχουν Fe3+ ), σχηματίζοντας σταθερά σύμπλοκα (Πίνακας 4-2).
Πίνακας 4-2 Συμπεριφορά του αργύρου σε διάφορα διαβρωτικά μέσα
| Διαβρωτικά μέσα | Μεσαία κατάσταση | Θερμοκρασία | Ο βαθμός διάβρωσης του αργύρου | |||
|---|---|---|---|---|---|---|
| Διαβρωτικά μέσα | Μεσαία κατάσταση | Θερμοκρασία | Σχεδόν καμία διάβρωση | Ελαφρά διάβρωση | Μέτρια διάβρωση | Σοβαρή διάβρωση |
| Θειικό οξύ | 98% | 18℃ | Ναι | |||
| Θειικό οξύ | 98% | 100℃ | Ναι | |||
| Νιτρικό οξύ | 0,1 mol/L | Θερμοκρασία δωματίου | Ναι | |||
| Νιτρικό οξύ | 70% | Θερμοκρασία δωματίου | Ναι | |||
| Νιτρικό οξύ | Smoke (>90%) | Θερμοκρασία δωματίου | Ναι | |||
| Υδροχλωρικό οξύ | 36% | 18℃ | Ναι | |||
| Υδροχλωρικό οξύ | 36% | 100℃ | Ναι | |||
| Υδροφθορικό οξύ | 40% | Θερμοκρασία δωματίου | Ναι | |||
| Aqua regia | 75%HCl + 25%HNO3 | Θερμοκρασία δωματίου | Ναι | |||
| Σουλφίδιο του υδρογόνου | Υγρασία | Θερμοκρασία δωματίου | Ναι | |||
| Φωσφορικό οξύ | > 90% | Θερμοκρασία δωματίου-100℃ | Ναι | |||
| Χλώριο | Ξηρό χλώριο | Θερμοκρασία δωματίου | Ναι | |||
| Χλώριο | Υγρό χλώριο | Θερμοκρασία δωματίου | Ναι | |||
| Κιτρικό οξύ | Θερμοκρασία δωματίου-100℃ | Ναι | ||||
| Ερμής | Θερμοκρασία δωματίου | Ναι | ||||
| Διάλυμα χλωριούχου σιδήρου (I II) | Θερμοκρασία δωματίου | Ναι | ||||
| Διάλυμα υδροξειδίου του νατρίου | Θερμοκρασία δωματίου | Ναι | ||||
| Διάλυμα αμμωνίας | Θερμοκρασία δωματίου | Ναι | ||||
| Διάλυμα κυανιούχου καλίου | Θερμοκρασία δωματίου ~ 100℃ | Ναι | ||||
| Λιωμένο υδροξείδιο του νατρίου | 350℃ | Ναι | ||||
| Λιωμένο υπεροξείδιο του νατρίου | 350℃ | Ναι | ||||
| Λιωμένο θειικό νάτριο | 350℃ | Ναι | ||||
Ο άργυρος μπορεί να σχηματίσει ενώσεις με διάφορες ουσίες και υπάρχει με τη μορφή μονοσθενών ιόντων σε αυτές τις ενώσεις, όπως AgNO3, Ag2O, AgCl, AgBr, AgCN, Ag2SO4, κ.λπ. AgNO3 χρησιμοποιείται συνήθως ως το κύριο άλας για την επιμετάλλωση αργύρου χωρίς κυάνιο και αποτελεί πηγή ιόντων αργύρου. Το διάλυμα νιτρικού αργύρου περιέχει μεγάλο αριθμό ιόντων αργύρου, γεγονός που το καθιστά ιδιαίτερα οξειδωτικό, αποσυντίθεται εύκολα στο φως, μπορεί να προκαλέσει πήξη πρωτεϊνών και έχει ορισμένες διαβρωτικές επιδράσεις στο δέρμα, γι' αυτό πρέπει να αποθηκεύεται σε καφέ φιάλες. Ag2O είναι μια μαύρη-καφέ σκόνη με κακή θερμική σταθερότητα, που αποσυντίθεται σε άργυρο και οξυγόνο όταν θερμαίνεται. Το AgCl είναι αδιάλυτο στο νερό αλλά εύκολα διαλυτό σε KCN, NaCN και άλλες ουσίες. Το AgCl που αιωρείται σε αραιό θειικό οξύ μπορεί εύκολα να αναχθεί σε άργυρο από αρνητικά φορτισμένα μέταλλα, όπως ψευδάργυρο, σίδηρο κ.λπ., και αυτή η απλή μέθοδος χρησιμοποιείται ευρέως για τον εξευγενισμό του αργύρου.
Οι ιδιότητες του AgBr είναι παρόμοιες με εκείνες του AgCl, διαλύεται σε άλατα αμμωνίου, θειοθειικά, θειώδη και κυανιούχα διαλύματα και μπορεί εύκολα να αναχθεί σε μεταλλικό άργυρο. Οι φωτοευαίσθητες ιδιότητες των αλογονιδίων του αργύρου είναι τα σημαντικότερα χαρακτηριστικά- υπό την επίδραση του φωτός, διασπώνται σε άργυρο και ελεύθερα αλογόνα. Αυτή η ιδιότητα των αλογονιδίων του αργύρου χρησιμοποιείται για την παραγωγή φωτογραφικού φιλμ, φωτογραφικού χαρτιού και ευαισθητοποιημένων μεμβρανών.
3. Μηχανικές ιδιότητες
Οι κύριες μηχανικές ιδιότητες του καθαρού αργύρου παρουσιάζονται στον πίνακα 4-3. Ο καθαρός άργυρος είναι πολύ μαλακός, με καλή ολκιμότητα και πλαστιμότητα, δεύτερος μετά τον χρυσό σε ολκιμότητα, ικανός να συμπιεστεί σε λεπτά φύλλα και να τραβηχτεί σε λεπτά σύρματα. 1 γραμμάριο αργύρου μπορεί να τραβηχτεί σε σύρμα μήκους 1800m και να τυλιχτεί σε φύλλο με πάχος 10μm. Ωστόσο, όταν ο άργυρος περιέχει μικρές ποσότητες προσμίξεων, όπως Sb, Bi και Pb, γίνεται εύθραυστος και η ολκιμότητα μειώνεται σημαντικά, με την επίδραση του Pb να είναι η πιο έντονη.
Στον πίνακα 4-3 παρουσιάζονται οι κύριες μηχανικές ιδιότητες του ανοπτημένου καθαρού αργύρου.
| Μηχανικές ιδιότητες | Τιμές δείκτη | Μηχανικές ιδιότητες | Τιμές δείκτη |
|---|---|---|---|
| Σκληρότητα Brinell HB/N/mm2 | 25 | Ποσοστό συρρίκνωσης διατομής /% | 80 ~ 95 |
| Αντοχή σε εφελκυσμό /MPa | 140 ~ 160 | Μέτρο ελαστικότητας E/GPa | 82 |
| Αντοχή σε διαρροή /MPa | 20 ~ 25 | Μέτρο διάτμησης G/GPa | 28 |
| Ρυθμός επιμήκυνσης /% | 40 ~ 50 | Μέτρο θλίψης B/GPa | 101.8 |
Το καθαρό ασήμι μπορεί να ενισχυθεί με ψυχρή κατεργασία Σχήμα 4-2. Ο ρυθμός επεξεργασίας επηρεάζει τις μηχανικές ιδιότητες του αργύρου. Ο πρώτος ρυθμός επεξεργασίας του ανοπτημένου καθαρού αργύρου μπορεί να φθάσει τα 99%. Καθώς ο ρυθμός επεξεργασίας αυξάνεται, η σκληρότητα, η αντοχή σε εφελκυσμό και το όριο διαρροής του αργύρου αυξάνονται όλα, ενώ ο ρυθμός επιμήκυνσης μειώνεται γρήγορα και ο ρυθμός σκλήρυνσης με κατεργασία παρουσιάζει ένα μοτίβο αρχικά γρήγορου και στη συνέχεια αργού ρυθμού. Ωστόσο, λόγω της χαμηλής ενέργειας σφάλματος στοίβαξης του καθαρού αργύρου, η επίδραση της σκλήρυνσης λόγω εργασίας δεν είναι σημαντική και η αντοχή και η σκληρότητα μετά την επεξεργασία παραμένουν πολύ χαμηλές, καθιστώντας δύσκολη την ικανοποίηση των απαιτήσεων αντοχής για την τοποθέτηση κοσμημάτων.
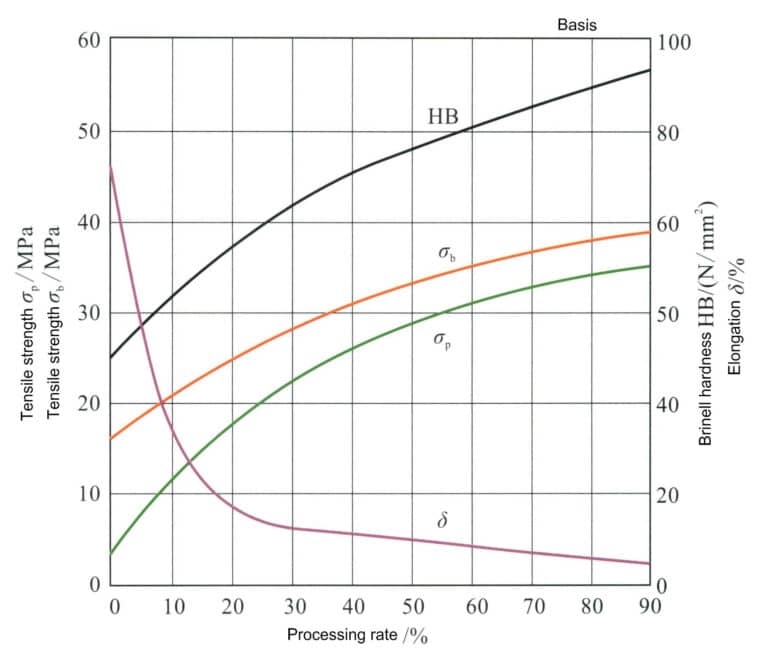
Η χαμηλή ενέργεια σφάλματος στοίβαξης του καθαρού αργύρου σημαίνει ότι η επίδραση της σκλήρυνσης λόγω εργασίας δεν είναι σημαντική και η αντοχή και η σκληρότητα μετά την επεξεργασία παραμένουν πολύ χαμηλές, καθιστώντας δύσκολη την ικανοποίηση των απαιτήσεων αντοχής για την τοποθέτηση κοσμημάτων. Οι μηχανικές ιδιότητες του αργύρου στην κατεργασμένη σκληρυμένη κατάσταση αλλάζουν γρήγορα μετά την επεξεργασία ανόπτησης. Καθώς αυξάνεται η θερμοκρασία ανόπτησης, η σκληρότητα του καθαρού αργύρου μειώνεται σταδιακά σε διαφορετικούς ρυθμούς επεξεργασίας, αλλά ο ρυθμός μείωσης πρέπει να είναι πιο σταθερός. Όταν ο ρυθμός επεξεργασίας είναι κάτω από 50%, η σκληρότητα μειώνεται ταχύτερα σε θερμοκρασία ανόπτησης 200℃- όταν ο ρυθμός επεξεργασίας είναι πάνω από 70%, η σκληρότητα μειώνεται ταχύτερα σε θερμοκρασία ανόπτησης 100℃ (Σχήμα 4-3).
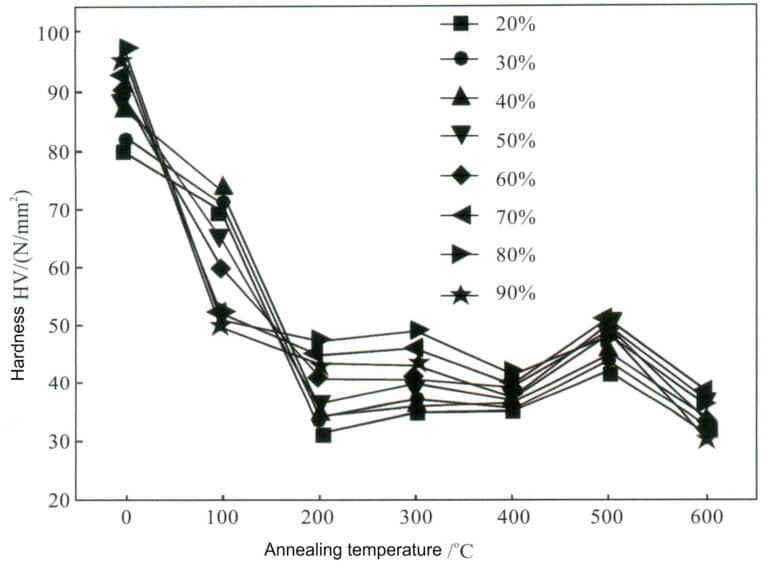
Ένα άλλο χαρακτηριστικό του καθαρού αργύρου σε επεξεργασμένη κατάσταση είναι ότι είναι επιρρεπές σε "φυσική γήρανση", που σημαίνει ότι η αντοχή και η σκληρότητα του επεξεργασμένου προφίλ ή προϊόντος μειώνονται σταδιακά κατά τη διάρκεια της φυσικής τοποθέτησης, γεγονός που είναι δυσμενές για τη χρήση κοσμημάτων. Η μαλάκυνση του καθαρού αργύρου κατά τη φυσική γήρανση προκαλείται στην πραγματικότητα από την ανάκτηση ή ακόμη και το σχηματισμό ανακρυσταλλωμένων δομών. Η έρευνα δείχνει ότι η αλλαγή της αντοχής του καθαρού αργύρου μετά από ψυχρή παραμόρφωση σχετίζεται με την καθαρότητα του υλικού, το ποσό της παραμόρφωσης, τη θερμοκρασία γήρανσης και το χρόνο τοποθέτησης. Ο πολυκρυσταλλικός καθαρός άργυρος μπορεί να εμφανίσει ακόμη και φυσική γήρανση μαλάκυνσης σε θερμοκρασίες κάτω των 20℃- ο ρυθμός μαλάκυνσης εξαρτάται από την παραμόρφωση και την περιεκτικότητα σε προσμίξεις στον καθαρό άργυρο. Το μέγεθος της παραμόρφωσης επεξεργασίας επηρεάζει επίσης σε μεγάλο βαθμό την αποδυνάμωση γήρανσης. Ο άργυρος με καθαρότητα 99,999% αρχίζει να μαλακώνει μετά από παραμόρφωση 99% και διατήρηση για 10 ώρες στους 20℃, ενώ μετά από παραμόρφωση 50%, μπορεί να διατηρηθεί για 100 ώρες στους 20℃ πριν αρχίσει να μαλακώνει.
4. Απόδοση διαδικασίας
Ο άργυρος έχει σχετικά χαμηλό σημείο τήξης και μπορεί να λιώσει χρησιμοποιώντας μεθόδους θέρμανσης με φλόγα, επαγωγική θέρμανση και θέρμανση με αντίσταση. Ωστόσο, κατά τη διάρκεια της τήξης του αργύρου, εμφανίζεται συχνά ένα φαινόμενο γνωστό ως "ασημένια βροχή", το οποίο χαρακτηρίζεται από εκτόξευση μετάλλων, οδηγώντας σε σημαντικές απώλειες. Κατά την τήξη του αργύρου σε περιβάλλον με κακές ατμοσφαιρικές συνθήκες ή συνθήκες κενού, η πτητικότητα του αργύρου είναι σχετικά υψηλή και είναι ακόμη υψηλότερη σε οξειδωτική ατμόσφαιρα από ό,τι σε αναγωγική ατμόσφαιρα.
Ο άργυρος είναι επιρρεπής στο σχηματισμό ατελειών πορώδους κατά τη χύτευση και η αρχή του σχηματισμού τους συνδέεται στενά με τις ιδιότητες του αργύρου. Σύμφωνα με τη θεωρία σχηματισμού χύτευσης, ο κύριος λόγος για τη δημιουργία πορώδους είναι ότι κατά τη διάρκεια της διαδικασίας στερεοποίησης, η διαλυτότητα του αερίου στο λιωμένο μέταλλο μειώνεται με την πτώση της θερμοκρασίας, οδηγώντας σε υπερκορεσμό αερίου, κατακρήμνιση και ανάπτυξη φυσαλίδων, οι οποίες δεν αποβάλλονται εγκαίρως, με αποτέλεσμα τη δημιουργία πόρων. Οι πόροι στα χυτά αργύρου σχετίζονται με το οξυγόνο που απορροφάται από το λιωμένο μέταλλο. Από το διάγραμμα δυαδικών φάσεων Ag-O (Σχήμα 4-4), φαίνεται ότι όταν το κορεσμένο σε οξυγόνο τήγμα αργύρου στερεοποιείται, αρχίζει να στερεοποιείται σε περίπου 951℃ κάτω από το σημείο τήξης του αργύρου (961,78℃) και η στερεοποίηση ολοκληρώνεται σε περίπου 931℃.
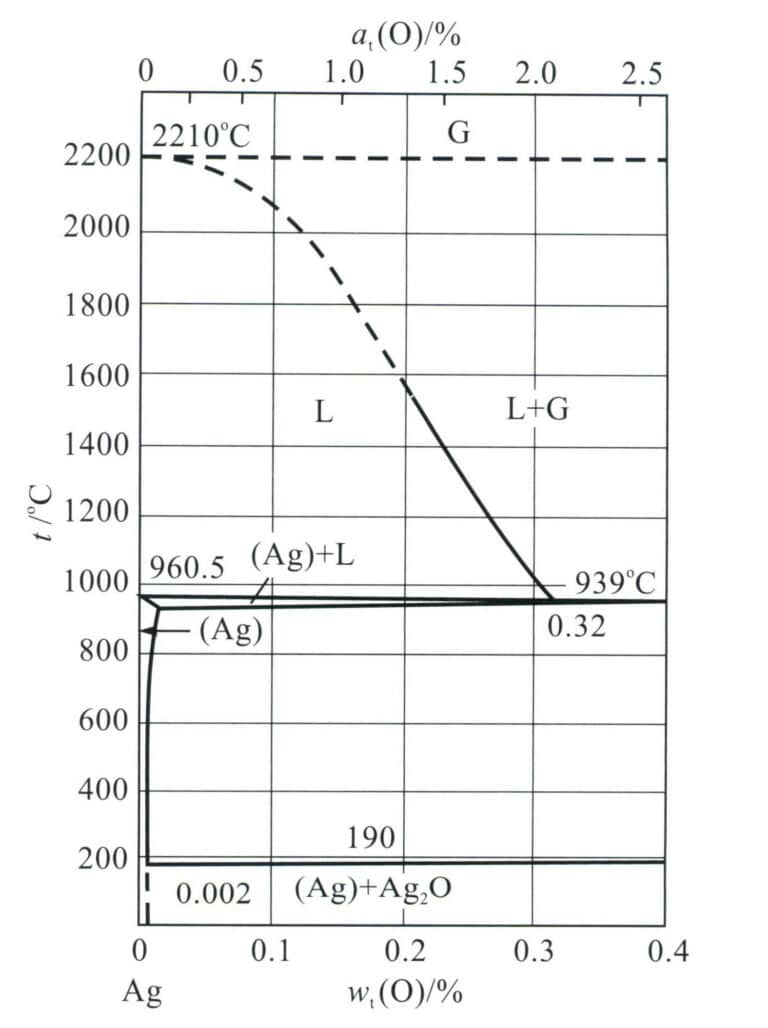
Σημείωση: Το G αντιπροσωπεύει την αέρια φάση- το (Ag) +L αντιπροσωπεύει τη διφασική περιοχή στερεού-υγρού,
όπου το (Ag) αντιπροσωπεύει το στερεό διάλυμα με βάση τον άργυρο και το L αντιπροσωπεύει την υγρή φάση.
Στον πίνακα 4-4 παρουσιάζεται η διαλυτότητα του οξυγόνου διαλυμένου ως άτομα σε άργυρο σε ατμόσφαιρα οξυγόνου σε 1 atm. Η διαλυτότητα του οξυγόνου στο λιωμένο ασήμι λίγο πάνω από το σημείο τήξης είναι η υψηλότερη, περίπου 3200 x 10-6, φτάνοντας τις 21 φορές τον όγκο του. Καθώς αυξάνεται η θερμοκρασία, ο βαθμός υπερθέρμανσης του υγρού αργύρου αυξάνεται και η διαλυτότητα του οξυγόνου μειώνεται.
Όταν το υγρό ασήμι στερεοποιείται, η διαλυτότητα του οξυγόνου στο στερεό ασήμι μειώνεται σημαντικά. Η διαλυτότητα του οξυγόνου σε στερεό άργυρο στους 931℃ φθάνει στο μέγιστο, περίπου 60 x10-6. Καθώς η θερμοκρασία πέφτει, η διαλυτότητα του οξυγόνου στο στερεό ασήμι μειώνεται γρήγορα και σε θερμοκρασία δωματίου το ασήμι δεν μπορεί σχεδόν καθόλου να απορροφήσει οξυγόνο. Η διαλυτότητα του οξυγόνου δεν σχετίζεται μόνο με τη θερμοκρασία αλλά και με τη μερική πίεση του οξυγόνου. Καθώς η μερική πίεση του οξυγόνου αυξάνεται, η διαλυτότητα αυξάνεται και η αντίδραση μεταξύ αργύρου και οξυγόνου επίσης αλλάζει.
Στον πίνακα 4-4 παρουσιάζεται η διαλυτότητα του οξυγόνου στον άργυρο σε ατμόσφαιρα οξυγόνου σε 1 atm.
| Θερμοκρασία /℃ | Θερμοκρασία /℃ | 200 | 400 | 600 | 800 | 973 | 1024 | 1075 | 1125 |
|---|---|---|---|---|---|---|---|---|---|
| Περιεκτικότητα σε οξυγόνο | x10-6 | 0.03 | 1.4 | 10.6 | 38.1 | 3050 | 2950 | 2770 | 2640 |
| Περιεκτικότητα σε οξυγόνο | mm3/g | - | - | - | - | 2135 | 2056 | 1939 | 1849 |
Κατά τη διάρκεια της στερεοποίησης, ουσίες διαλυμένες στο αργυρό υγρό, όπως το Ο, το Ν και το Η, αποβάλλονται στη διεπιφάνεια στερεού-υγρού. Μόλις ξεπεραστεί η διαλυτότητά τους στον κορεσμό, θα απελευθερωθούν. Ο σχηματισμός των αερίων πόρων αποτελείται από δύο στάδια: την πυρηνοποίηση και την ανάπτυξη. Η πυρηνοποίηση πρέπει να ξεπεράσει τις συνδυασμένες επιδράσεις της ατμοσφαιρικής πίεσης, της στατικής πίεσης του μετάλλου και των πρόσθετων πιέσεων από την επιφανειακή τάση. Μόνο όταν η πίεση του αερίου που κατακρημνίζεται υπερβαίνει τη συνολική τιμή των εξωτερικών πιέσεων μπορεί να σχηματιστεί πυρήνας φυσαλίδας. Η φυσαλίδα αναπτύσσεται περαιτέρω και όταν γίνει αρκετά μεγάλη, η άνωση που την επηρεάζει αυξάνεται, με αποτέλεσμα να ανυψώνεται και να αποκολλάται. Όταν η γωνία διαβροχής της φυσαλίδας με την επιφάνεια της στερεάς φάσης είναι ϴ> 90, είναι εύκολο να αποκολληθεί- όταν ϴ< 90, δεν είναι εύκολο να αποκολληθεί. Εάν ο ρυθμός ανάπτυξης δενδριτών κατά τη στερεοποίηση είναι μεγαλύτερος από την ταχύτητα ανόδου, οι αναπτυσσόμενοι δενδρίτες θα περικλείσουν πλήρως τις φυσαλίδες, σχηματίζοντας πόρους αερίου.
Το ασήμι έχει μαλακή υφή, καθιστώντας το κατάλληλο για χειροποίητα κοσμήματα. Στην παραδοσιακή κατασκευή ασημένιων κοσμημάτων, το καθαρό ασήμι χρησιμοποιείται εκτενώς για τη δημιουργία φιλιγκράν και υφαντών κοσμημάτων, χρησιμοποιώντας συχνά τεχνικές όπως το σφυρηλάτηση και η χάραξη για τη δημιουργία διακοσμητικών μοτίβων στην επιφάνεια του κοσμήματος. Στη σύγχρονη παραγωγή κοσμημάτων, οι τεχνικές ψυχρής επεξεργασίας, όπως η έλαση, το τράβηγμα, η σφράγιση και η υδραυλική πρέσα, χρησιμοποιούνται επίσης ευρέως για την επεξεργασία ασημένιων κοσμημάτων, εκμεταλλευόμενοι την εξαιρετική ολκιμότητα του καθαρού αργύρου. Τεχνικές όπως η έλαση, το βαθύ τράβηγμα και η βαθιά σφράγιση χρησιμοποιούνται συχνά για τη δημιουργία ασημένιων μπολ, ασημένιων φλιτζανιών και άλλων χειροτεχνημάτων.
Ενότητα II Η καθαρότητα και η ταξινόμηση των ασημένιων κοσμημάτων
1. Σήμανση καθαρότητας των ασημένιων κοσμημάτων
Για τα ασημένια κοσμήματα, η καθαρότητα δηλώνεται με τον συνδυασμό της χιλιοστής καθαρότητας και του αργύρου, Ag ή S (S είναι η συντομογραφία του αργύρου στα αγγλικά). Για παράδειγμα, τα ασημένια κοσμήματα που περιέχουν 92,5% μπορούν να επισημαίνονται με μια ετικέτα καθαρότητας όπως 925 silver, 925Ag, 925 S ή 925. Για ασημένια κοσμήματα με καθαρότητα όχι μικρότερη από 99%, η ετικέτα καθαρότητας σημειώνεται ως fine silver, 990 silver, 990 Ag, ή S 990. Ο συνήθως αναφερόμενος στην αγορά χιλιοστός άργυρος (με περιεκτικότητα σε άργυρο όχι χαμηλότερη από 99,9% ) φέρει ομοιόμορφη σήμανση ως καθαρός άργυρος.
2. Ταξινόμηση της καθαρότητας των ασημένιων κοσμημάτων
Το ασήμι χρησιμοποιείται ευρέως στην παραγωγή κοσμημάτων, χειροτεχνίας και άλλων διακοσμητικών αντικειμένων. Με βάση την καθαρότητα του αργύρου, μπορεί να διαχωριστεί σε υψηλής καθαρότητας ασημένιο κόσμημα και σε συνηθισμένης καθαρότητας ασημένιο κόσμημα.
2.1 Ασήμι κοσμήματος υψηλής καθαρότητας
Όπως υποδηλώνει και το όνομα, ο άργυρος κοσμήματος υψηλής καθαρότητας αναφέρεται σε ασήμι με υψηλό επίπεδο καθαρότητας, το οποίο μπορεί να υποδιαιρεθεί περαιτέρω σε:
(1) Καθαρό ασήμι.
Θεωρητικά, η περιεκτικότητα σε άργυρο πρέπει να είναι 100%. Ωστόσο, όπως ακριβώς "ο χρυσός δεν είναι απόλυτα καθαρός", έτσι δεν είναι και ο άργυρος. Ακόμη και με το σημερινό επιστημονικό και τεχνολογικό επίπεδο, είναι πολύ δύσκολο να λιώσει κανείς ασήμι με καθαρότητα 100% και μπορεί να πλησιάσει μόνο αυτή την τιμή καθαρότητας. Το καθαρό ασήμι είναι επίσης γνωστό ως "λεπτό ασήμι" και πήρε το όνομά του από τα μοναδικά σχέδια που σχηματίζονται στην επιφάνεια κατά τη διάρκεια των διαδικασιών τήξης, εξευγενισμού και συμπύκνωσης. Όσον αφορά τα υλικά κοσμήματος, η υπερβολική επιδίωξη της καθαρότητας του αργύρου δεν είναι ούτε απαραίτητη ούτε πρακτική. Ως εκ τούτου, ο άργυρος με καθαρότητα όχι μικρότερη από 99,6% στη βιομηχανία χαρακτηρίζεται γενικά ως λεπτό ασήμι. Ο άργυρος με περιεκτικότητα όχι μικρότερη από 99,9% αναφέρεται ως καθαρό ασήμι.
(2) 990 λεπτό ασήμι.
Η περιεκτικότητα σε άργυρο πρέπει να είναι τουλάχιστον 990‰. Ο άργυρος λεπτότητας 990‰ χρησιμοποιούνταν συνήθως στο παρελθόν ως πρότυπο ασήμι για την κυκλοφορία και τις συναλλαγές. Μπορεί να χρησιμοποιηθεί ως εγγύηση για ακίνητα, ως ασημένια κάλυψη εταιρικών κοινοπραξιών και ως μέσο για εμπορικές ανταλλαγές.
Το καθαρό ασήμι και το ασήμι 990 έχουν υψηλότερο βαθμό, που τα καθιστά πιο μαλακά στην υφή. Χρησιμοποιούνται γενικά μόνο για ασημένια κοσμήματα χωρίς διακοσμητικά στοιχεία, με τα παραδοσιακά ασημένια στολίδια να είναι τα πιο συνηθισμένα.
2.2 Ασήμι κοσμήματος συνήθους καθαρότητας
Το συνηθισμένης καθαρότητας ασήμι κοσμήματος με την προσθήκη μικρής ποσότητας άλλων μετάλλων σε καθαρό ασήμι ή ασήμι 925, με αποτέλεσμα να δημιουργείται μια πιο σκληρή υφή του αργύρου. Αυτά τα είδη αργύρου βασίζονται γενικά σε κράματα Ag-Cu, καθώς οι φυσικές και χημικές ιδιότητες του χαλκού είναι παρόμοιες με εκείνες του αργύρου, οι οποίες μπορούν να προσδώσουν στον έγχρωμο άργυρο σκληρότητα και να διατηρήσουν καλή ολκιμότητα. Επιπλέον, ορισμένα στοιχεία κράματος μπορούν να καταστείλουν σε κάποιο βαθμό την επίδραση του αέρα στο θάμπωμα των ασημένιων κοσμημάτων. Ως εκ τούτου, η επιφανειακή λάμψη πολλών χρωματιστών ασημένιων στολιδιών είναι λιγότερο επιρρεπής σε αλλαγές σε σύγκριση με το καθαρό ασήμι και το ασήμι 925. Το ασήμι κοσμήματος συνήθους καθαρότητας περιλαμβάνει κυρίως τις ακόλουθες κατηγορίες:
(1) 980 ασήμι.
Υποδεικνύει περιεκτικότητα σε ασήμι 98%, με σήμα καθαρότητας 980 S. Αυτό το χρωματισμένο ασήμι είναι ελαφρώς σκληρότερο από το καθαρό ασήμι και το ασήμι 925 και χρησιμοποιείται κυρίως για την κατασκευή κοσμημάτων που διατηρούν την αξία τους.
(2) 958 ασημένια.
Έχει περιεκτικότητα σε ασήμι 95,8%, το δεύτερο πρότυπο κράμα αργύρου για κοσμήματα στην Αγγλία του 12ου αιώνα, γνωστό ως ασήμι Britannia. Έχει χαμηλότερη σκληρότητα και δεν είναι κατάλληλο για την τοποθέτηση πολύτιμων λίθων.
(3) ασήμι 925.
Υποδεικνύει περιεκτικότητα σε ασήμι 92,5%, γνωστό ως "ασήμι στερλίνας", όταν χρησιμοποιείται μόνο Cu ως στοιχείο κράματος. Αυτό είναι το πρώτο πρότυπο κράμα αργύρου για κοσμήματα στην Αγγλία του 12ου αιώνα, που χρησιμοποιείται ακόμη και σήμερα, με ιστορία άνω των 800 ετών, και είναι ευρέως αποδεκτό και χρησιμοποιείται σε όλο τον κόσμο. Αυτός ο άργυρος έχει μια ορισμένη σκληρότητα και ανθεκτικότητα, καθιστώντας τον κατάλληλο για την κατασκευή δαχτυλιδιών, περιδέραιων, καρφιτσών, καρφιτσών για τα μαλλιά και άλλων κοσμημάτων, και ευνοεί την τοποθέτηση πολύτιμων λίθων.
(4) 900 ασημένια.
Η περιεκτικότητα σε άργυρο είναι 90%, με καλή αντοχή και σκληρότητα. Αρχικά σχεδιάστηκε κυρίως για την κατασκευή ασημένιων νομισμάτων, είναι επίσης γνωστό ως ασήμι νομισμάτων και αργότερα χρησιμοποιήθηκε για την κατασκευή κοσμημάτων.
(5) 800 ασημένια.
Αυτό το ασήμι έχει υψηλή σκληρότητα και καλή ελαστικότητα, καθιστώντας το κατάλληλο για την κατασκευή κουδουνιών χειρός, κλιπ για κολάρα και άλλων κοσμημάτων.
Υπάρχουν τύποι αργύρου χαμηλότερης καθαρότητας, όπως ο άργυρος 700, ο άργυρος 600 και ο άργυρος 500. Πρέπει να σημειωθεί ότι οι χημικές ιδιότητες του αργύρου δεν είναι τόσο σταθερές όσο του χρυσού, ιδίως όταν εκτίθεται στον αέρα, γεγονός που μπορεί να τον κάνει να αμαυρώσει και να χάσει τη λάμψη του. Ως εκ τούτου, η θέση του στα κοσμήματα από πολύτιμα μέταλλα ήταν ανέκαθεν χαμηλή, κατατασσόμενο στα κοσμήματα από πολύτιμα μέταλλα χαμηλής ποιότητας με αξία χαμηλότερη από την πλατίνα και τον χρυσό.
Ενότητα ΙΙΙ Η κράματωση του καθαρού αργύρου και του αργύρου
1. Διακοσμητικό καθαρό ασήμι
Η κουλτούρα των παραδοσιακών χειροποίητων ασημένιων κοσμημάτων έχει ιστορία χιλιάδων ετών. Τα παραδοσιακά ασημένια κοσμήματα χρησιμοποιούν κυρίως τεχνικές χειροτεχνίας, όπως σφυρηλάτηση, χύτευση, φιλιγκράν και χάραξη, απαιτώντας μαλακά και εύκολα στο σχήμα υλικά. Ως εκ τούτου, το υλικό είναι κυρίως καθαρό ασήμι και τα σχήματα και τα μοτίβα διαθέτουν κυρίως αμπέλια, λουλούδια, ευοίωνα ζώα και ευοίωνους χαρακτήρες. Αυτή η παραδοσιακή βιοτεχνική κουλτούρα έχει περάσει μέχρι σήμερα και εξακολουθεί να έχει μια ορισμένη αγορά (Εικόνα 4-5).

Οι εταιρείες κοσμημάτων αγοράζουν γενικά κόκκους καθαρού αργύρου ή ράβδους καθαρού αργύρου ως πρώτες ύλες για την παραγωγή ασημένιων κοσμημάτων (Εικόνα 4-6. Εικόνα 4-7).


Για να διασφαλιστεί η ποιότητα των προϊόντων καθαρού αργύρου, είναι απαραίτητο να ξεκινήσουμε από την πηγή των βαθμών της πρώτης ύλης. Ο καθαρός άργυρος χωρίζεται σε τρεις ποιότητες με βάση τη χημική σύνθεση: IC-Ag99.99, IC-Ag99.95 και IC-Ag99.90. Το βιομηχανικό πρότυπο "Κόκκοι αργύρου" (YS/T 856-2012) καθορίζει τις απαιτήσεις για τις προδιαγραφές των κόκκων αργύρου, με μέγεθος σωματιδίων 1-15 mm, και η χημική σύνθεση πρέπει να πληροί τις απαιτήσεις του διεθνούς προτύπου για τις ράβδους αργύρου. Το διεθνές πρότυπο "Πλινθώματα αργύρου" καθορίζει σαφώς τη χημική σύνθεση και την περιεκτικότητα σε προσμίξεις αυτών των τριών κατηγοριών καθαρών πλινθωμάτων αργύρου, όπως φαίνεται στον πίνακα 4-5.
Πίνακας 4-5 Απαιτήσεις για τη χημική σύνθεση των ράβδων καθαρού αργύρου
| Βαθμός | wt (Ag) (≥)% | Περιεκτικότητα σε προσμίξεις (wt≤)/% | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Βαθμός | wt (Ag) (≥)% | Cu | Pb | Fe | Sb | Se | Te | Bi | Pd | Συνολικές ακαθαρσίες |
| IC-Ag99.99 | 99.99 | 0.0025 | 0.001 | 0.001 | 0.001 | 0.0005 | 0.0008 | 0.0008 | 0.001 | 0.01 |
| IC-Ag99.95 | 99.95 | 0.0250 | 0.015 | 0.002 | 0.002 | - | - | 0.001 | - | 0.05 |
| IC-Ag99. 90 | 99.90 | 0.0500 | 0.025 | 0.002 | - | - | - | 0.002 | - | 0.10 |
Όπως αναφέρθηκε προηγουμένως, η αντοχή και η σκληρότητα των παραδοσιακών κοσμημάτων από καθαρό ασήμι είναι πολύ χαμηλές. Ακόμη και με ψυχρή επεξεργασία, το επίπεδο σκλήρυνσης της εργασίας θα μπορούσε να είναι υψηλότερο λόγω του ότι ο άργυρος είναι ένα μέταλλο χαμηλής ενέργειας σφάλματος στοίβαξης. Επιπλέον, ο καθαρός άργυρος σε κατάσταση εργαστηριακής σκλήρυνσης είναι επιρρεπής στη φυσική γήρανση και μαλακώνει, με αποτέλεσμα να παραμορφώνεται και να φθείρεται εύκολα κατά την καθημερινή χρήση. Λόγω της χαμηλής αντοχής του, είναι επίσης ακατάλληλο για την τοποθέτηση πολύτιμων λίθων, καθιστώντας δύσκολη τη δημιουργία σχεδίων με τρισδιάστατο αποτέλεσμα. Επιπλέον, το καθαρό ασήμι είναι επιρρεπές στο θάμπωμα και τον αποχρωματισμό στον αέρα.
Για να βελτιωθούν οι ελλείψεις του καθαρού ασημένιου υλικού, είναι απαραίτητο να τροποποιηθεί με τη χρήση κραμάτων ή ειδικών τεχνικών επεξεργασίας, έτσι ώστε το τροποποιημένο υλικό να πληροί τα αντίστοιχα πρότυπα χρώματος κοσμημάτων, ενώ παράλληλα να έχει καλή συνολική απόδοση σε φυσικές, χημικές, μηχανικές και επεξεργαστικές πτυχές.
2. Μικρο-κραματωμένο ασήμι
Η βιομηχανία έχει αναπτύξει υψηλής καθαρότητας ασήμι που αντιστέκεται στη φυσική γήρανση, το μαλάκωμα και τη θαμπάδα μέσω μεθόδων μικροκραμάτωσης ή έχει δημιουργήσει κοσμήματα από ασήμι υψηλής σκληρότητας και καθαρότητας χρησιμοποιώντας ειδικές τεχνικές επεξεργασίας.
2.1 Μικρο-κραματωμένο ασήμι
Η έρευνα έχει διαπιστώσει ότι η προσθήκη ιχνοστοιχείων κραμάτωσης στον καθαρό άργυρο μπορεί να βελτιώσει την αντοχή και τον ρυθμό σκλήρυνσης, να καταστείλει σε κάποιο βαθμό τη διαδικασία ανάκτησης, να αυξήσει τη θερμοκρασία ανακρυστάλλωσης και να βελτιώσει τα χαρακτηριστικά σκλήρυνσης του κράματος και την αντοχή του σε φυσική γήρανση και μαλάκυνση. Για παράδειγμα, η προσθήκη ιχνοστοιχείων σπάνιων γαιών (Y, La, Ce) σε καθαρό άργυρο με καθαρότητα 99,96% σε ποσότητες μικρότερες από 0,11% έχει ως αποτέλεσμα ένα κράμα στερεού διαλύματος συγκόλλησης αργύρου που έχει καλύτερη αντοχή στη διάβρωση και υψηλότερη αντίσταση στην αποδυνάμωση λόγω γήρανσης σε σύγκριση με τον καθαρό άργυρο, καθιστώντας το κατάλληλο για χρήση ως υλικό για ασημένια κοσμήματα (Εικόνα 4-8).
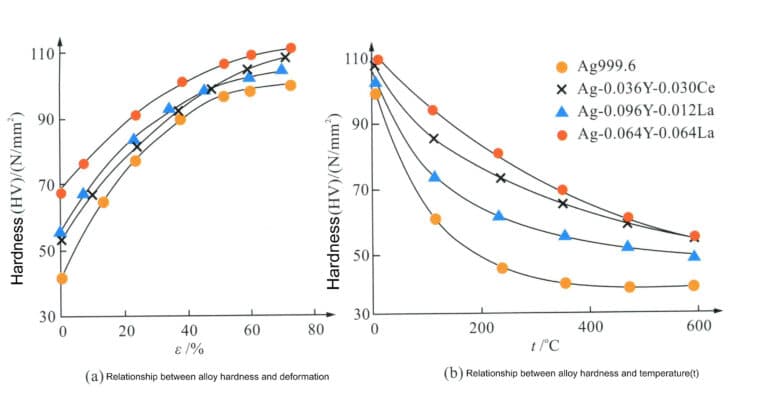
Ομοίως, η προσθήκη 0,01% Mn σε συνηθισμένο καθαρό ασήμι, με ποσοστό επεξεργασίας 97%, οδηγεί σε αντοχή σε εφελκυσμό 340 MPa και σκληρότητα HV103 για τον καθαρό ασήμι με μικρο-κραματώσεις Mn, ο οποίος μπορεί να παραμείνει σταθερός για 365 ημέρες στους 25℃, ενώ ο συνηθισμένος καθαρός άργυρος επανέρχεται στα επίπεδα αντοχής και σκληρότητας πριν από την παραμόρφωση σε λιγότερο από 30 ημέρες, η αντοχή και η σκληρότητά του ουσιαστικά αποκαθίστανται στο επίπεδο πριν από την παραμόρφωση (Σχήμα 4-9). Η προσθήκη Mn μπορεί να βελτιώσει αποτελεσματικά τους κόκκους του αργύρου, να αυξήσει τον αριθμό των ορίων των κόκκων, να ενισχύσει την αντίσταση στην παραμόρφωση και να διαδραματίσει ρόλο στην ενίσχυση και τη σταθεροποίηση των μηχανικών ιδιοτήτων.
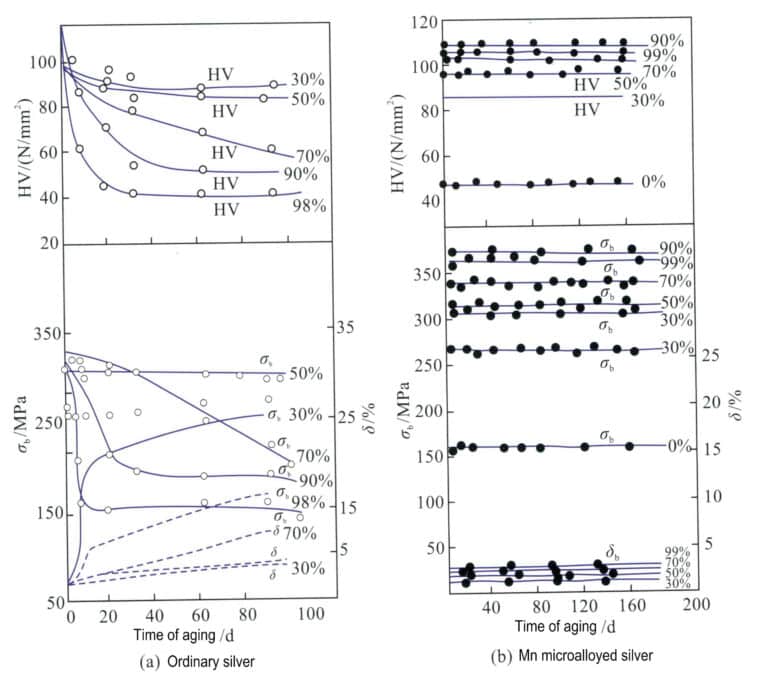
σb. Αντοχή σε εφελκυσμό- δ. Επιμήκυνση- HV. Μικροσκληρότητα Vickers; Συνήθης καθαρός άργυρος; Μικροκραματωμένος καθαρός άργυρος Mn
2.2 Ηλεκτροδιαμορφωμένο σκληρό ασήμι στερλίνας
Η διαδικασία ηλεκτροδιαμόρφωσης σκληρού αργύρου 999 είναι μια τεχνική κατασκευής κοσμημάτων που βασίζεται στην αρχή της ηλεκτροχημικής εναπόθεσης. Βελτιώνοντας τη σύνθεση του διαλύματος ηλεκτρομόρφωσης και παραμέτρους όπως η τιμή του pH, η θερμοκρασία εργασίας, η περιεκτικότητα σε οργανικό λαμπρυντικό και η ταχύτητα ανάδευσης, ενισχύεται η εσωτερική δομή του αργύρου, επιτυγχάνοντας μια πυκνή δομή κοντά σε νανοκρυστάλλους, αυξάνοντας σημαντικά την αντοχή και τη σκληρότητα του αργύρου. Αντιπροσωπεύει μια επανάσταση και καινοτομία στα παραδοσιακά κοσμήματα από ασήμι 925.
Η περιεκτικότητα σε ασήμι του ηλεκτροδιαμορφωμένου σκληρού αργύρου 999 δεν είναι μικρότερη από 99,9%, πληροί το πρότυπο ποιότητας για το ασήμι 999, αλλά η σκληρότητά του είναι περισσότερο από τρεις φορές μεγαλύτερη από εκείνη των συνηθισμένων κοσμημάτων 999 αργύρου. Έχει σκληρότητα συγκρίσιμη με το ασήμι 925, βελτιώνοντας σημαντικά την αντίσταση παραμόρφωσης και φθοράς του καθαρού ασημένιου κοσμήματος και ικανοποιώντας τις απαιτήσεις για ένθετα πολύτιμων λίθων. Επιπλέον, λόγω του κοίλου εσωτερικού του κοσμήματος, ο όγκος του είναι τετραπλάσιος από αυτόν των συνηθισμένων κοσμημάτων από καθαρό ασήμι με το ίδιο βάρος, επιτρέποντας τη δημιουργία τρισδιάστατων και ζωντανών σχημάτων. Το προϊόν έχει καλό τρισδιάστατο αποτέλεσμα και διαθέτει συνδυασμό ποιότητας καθαρού αργύρου, σκληρότητας αργύρου 925 και βάρους 1/3 παραδοσιακού ασημένιου κοσμήματος (Εικόνα 4-10).

3. Συστήματα κράματος αργύρου για κοσμήματα
Η απόδοση αντοχής του μικρο-κραματωμένου αργύρου βασίζεται σε μεγάλο βαθμό στη σκλήρυνση λόγω ψυχρής παραμόρφωσης. Ωστόσο, μόλις τα κοσμήματα υποβληθούν σε θερμότητα κατά τη διάρκεια διεργασιών όπως η συγκόλληση και η στίλβωση, η σκληρότητά τους μειώνεται γρήγορα, καθιστώντας δύσκολη την ικανοποίηση των απαιτήσεων παραγωγής και χρήσης. Ως εκ τούτου, η κατάλληλη μείωση της λεπτότητας του αργύρου μέσω της κραματοποίησης για την απόκτηση ενός κράματος αργύρου με καλή συνολική απόδοση είναι η κύρια προσέγγιση στην αγορά ασημένιων κοσμημάτων, με τα κράματα αργύρου που περιέχουν 92,5% να είναι τα πιο ευρέως χρησιμοποιούμενα. Θεωρητικά, όλα τα στοιχεία που μπορούν να διαλυθούν στον άργυρο μπορούν να παράγουν ένα ενισχυτικό αποτέλεσμα, αλλά ο βαθμός ενίσχυσης ποικίλλει μεταξύ των διαφόρων κραματικών στοιχείων. Επιπλέον, πολλά στοιχεία έχουν σοβαρή τάση να διαχωρίζονται στα όρια των κόκκων στον άργυρο. Κατά τη μικροκραμάτωση για την ενίσχυση του αργύρου, η ποσότητα που προστίθεται είναι πολύ μικρή και μπορεί να χρησιμεύσει ως ευεργετικό στοιχείο κράματος. Ωστόσο, μόλις η περιεκτικότητά τους υπερβεί το όριο διαλυτότητας, μπορεί να οδηγήσει σε ευθραυστότητα του αργύρου. Τα συνήθως χρησιμοποιούμενα στοιχεία κράματος για κράματα αργύρου περιλαμβάνουν κυρίως Cu, Zn, Pd, Pt, Sn, In, Si, Ge και άλλα.
3.1 Κράμα Ag-Cu
Το διάγραμμα φάσεων του δυαδικού κράματος Ag-Cu παρουσιάζεται στο Σχήμα 4-11. Το κράμα Ag-Cu είναι ένα ευτηκτικό κράμα με περιεκτικότητα σε χαλκό σε ευτηκτικό σημείο 28,1%, που εμφανίζεται στους 779℃. Η μέγιστη διαλυτότητα του χαλκού στον άργυρο είναι 8,8%. Εντός αυτού του εύρους, καθώς αυξάνεται η περιεκτικότητα σε χαλκό, το σημείο τήξης του κράματος μειώνεται μέχρι να φθάσει στην ευτηκτική θερμοκρασία του κράματος. Επομένως, η προσθήκη χαλκού στον άργυρο βελτιώνει την απόδοση της χύτευσης. Μετά τη στερεοποίηση, το κράμα Ag-Cu σχηματίζει αναμίξιμα στερεά διαλύματα πλούσια σε άργυρο και πλούσια σε χαλκό, αυξάνοντας σημαντικά την αντοχή του κράματος. Η κατεργασία γήρανσης του κράματος στερεού διαλύματος σε χαμηλές θερμοκρασίες μπορεί να παράγει περαιτέρω ενίσχυση με κατακρήμνιση. Έτσι, ο χαλκός μπορεί να παράγει αξιοσημείωτο αποτέλεσμα ενίσχυσης στον άργυρο και να αυξήσει τη θερμοκρασία ανακρυστάλλωσής του.
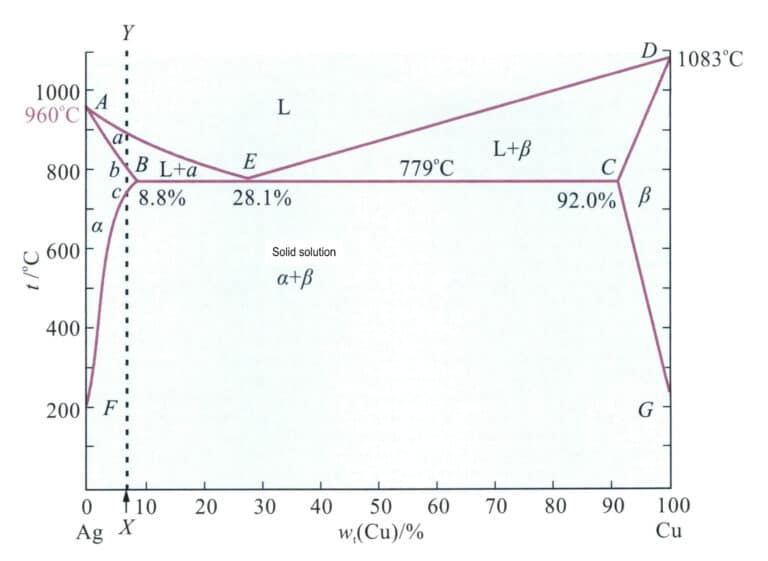
Σημείωση: 960℃ αντιπροσωπεύει το σημείο τήξης του καθαρού αργύρου- 1083℃ αντιπροσωπεύει το σημείο τήξης του καθαρού χαλκού- 8,8% είναι η μέγιστη διαλυτότητα του χαλκού στον άργυρο- 28,1% είναι η περιεκτικότητα σε χαλκό στο ευτηκτικό σημείο- 779℃ είναι η ευτηκτική θερμοκρασία- 92.0% υποδηλώνει ότι η μέγιστη διαλυτότητα του αργύρου στον χαλκό είναι 100%-92,0% = 8,0%- το σημείο Α σημείο Ε αντιπροσωπεύει τη γραμμή liquidus- α είναι το στερεό διάλυμα με βάση τον άργυρο- 0 είναι το στερεό διάλυμα με βάση τον χαλκό- G αντιπροσωπεύει τη θερμοκρασία στην οποία η διαλυτότητα του αργύρου στον χαλκό μειώνεται στο 0 υπό συνθήκες ισορροπίας.
Οι κύριες μηχανικές ιδιότητες του κράματος παρουσιάζονται στον πίνακα 4-6. Καθώς αυξάνεται η περιεκτικότητα σε Cu, η αντοχή και η σκληρότητα του κράματος Ag-Cu βελτιώνονται, ενώ η επιμήκυνση μειώνεται αντίστοιχα.
Στον πίνακα 4-6 παρουσιάζονται οι κύριες μηχανικές ιδιότητες του κράματος Ag-Cu.
| Βαθμός κράματος | Σκληρότητα HB/(N/mm2) | Αντοχή σε εφελκυσμό/MPa | Επιμήκυνση/% | |||
|---|---|---|---|---|---|---|
| Βαθμός κράματος | Annea οδήγησε κατάσταση | Επεξεργασμένη κατάσταση | Ανυψωμένη κατάσταση | Επεξεργασμένη κατάσταση | Annea οδήγησε κατάσταση | Επεξεργασμένη κατάσταση |
| 95%Ag-5%Cu | 50 | 119 | 240 | 450 | 43 | 5 |
| 92,5%Ag-7,5%Cu | 57 | 118 | 260 | 470 | 41 | 4 |
| 90%Ag-10%Cu | 64 | 125 | 270 | 450 | 35 | 4 |
| 87,5%Ag-12,5%Cu | 70 | 127 | 260 | - | 38 | 4 |
| 80%Ag-20%Cu | 79 | 134 | 310 | 500 | 35 | 4 |
| 75%Ag-25%Cu | 82 | 135 | 320 | 540 | 33 | 4 |
Μετά την προσθήκη Cu στον άργυρο, το χρώμα του έχει μια συγκεκριμένη επίδραση. Καθώς αυξάνεται η περιεκτικότητα σε Cu, η ανακλαστικότητα του κράματος Ag-Cu στο ορατό φως μειώνεται σταδιακά (Σχήμα 4-12) και το χρώμα του κράματος μεταβάλλεται σταδιακά από ασημόλευκο σε ανοιχτό ροζ, ροζ και ακόμη και κόκκινο.
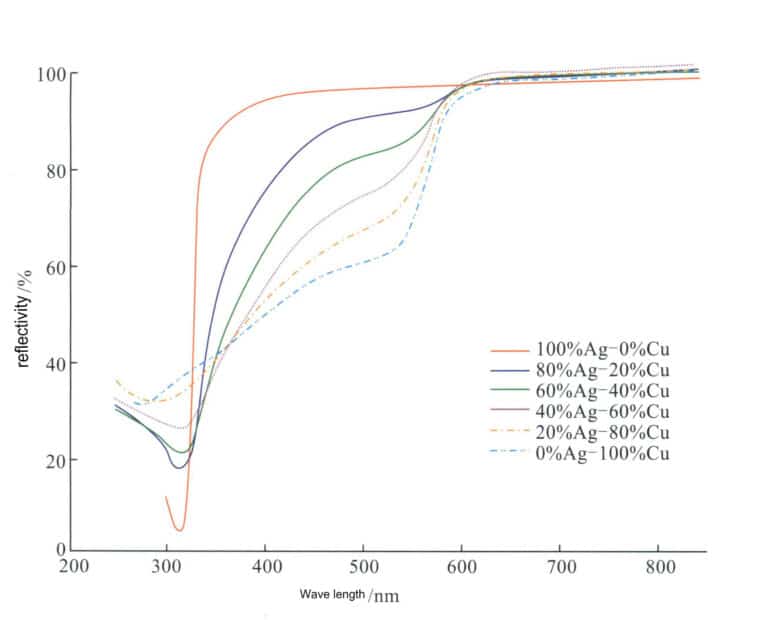
Ο Cu είναι το πιο συχνά χρησιμοποιούμενο στοιχείο κράματος στο Ag, και το παραδοσιακό ασημένιο χρώμα είναι ένα δυαδικό κράμα με Cu ως στοιχείο κράματος, με κύριες ποιότητες που περιλαμβάνουν ασήμι 980, ασήμι 925, ασήμι 900 και ασήμι 800. Τα κράματα αργύρου στην τρέχουσα αγορά είναι επίσης βασικά βασισμένα στο κράμα Ag-Cu ως βασικό κράμα. Αν και ο χαλκός μπορεί να βελτιώσει την αντοχή, τη σκληρότητα και την απόδοση της χύτευσης του αργύρου, δεν βελτιώνει την αντοχή του στο σκούρο χρώμα και τον αποχρωματισμό. Επιπλέον, λόγω της διφασικής δομής του κράματος, υπάρχει ένα φαινόμενο μικρο-μπαταρίας διάβρωσης σε διαβρωτικά περιβάλλοντα, καθιστώντας την αντοχή του στη διάβρωση χειρότερη από εκείνη ενός μονοφασικού στερεού διαλύματος αργύρου.
3.2 Κράμα Ag-Pd
Οι έρευνες δείχνουν ότι η προσθήκη μιας ορισμένης ποσότητας πολύτιμων μετάλλων στο ασήμι βελτιώνει αποτελεσματικά την αντοχή του στο σκούρο χρώμα και τον αποχρωματισμό. Το Pd είναι το προτιμώμενο στοιχείο πολύτιμου μετάλλου για τον άργυρο και στο Σχήμα 4-13 παρουσιάζεται το διάγραμμα φάσεων του δυαδικού κράματος Ag-Pd.
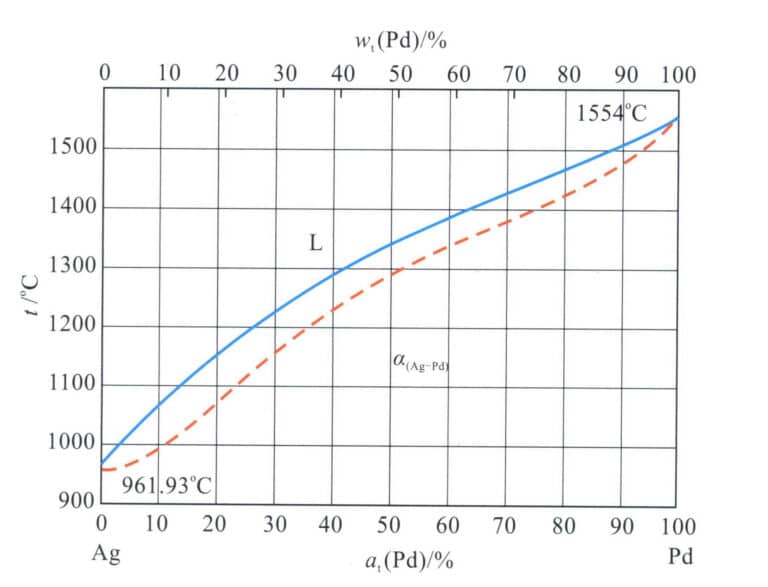
Το κράμα είναι απείρως διαλυτό σε υγρή και στερεή φάση, σχηματίζοντας ένα συνεχές στερεό διάλυμα. Ως εκ τούτου, η ενισχυτική επίδραση του παλλαδίου στον άργυρο είναι γενικά μέτρια, όπως φαίνεται στον πίνακα 4-7. Η ψυχρή παραμόρφωση μπορεί να βελτιώσει την αντοχή και τη σκληρότητα του κράματος σε κάποιο βαθμό. Ωστόσο, εξακολουθεί να μην μπορεί να ικανοποιήσει πλήρως τις απαιτήσεις αντοχής για ενσωματωμένα κοσμήματα, καθιστώντας αναγκαία την προσθήκη άλλων κραματικών στοιχείων για περαιτέρω ενίσχυση.
Πίνακας 4-7 Κύριες ιδιότητες του ανοπτημένου κράματος
| Βαθμός κράματος | Θερμοκρασία τήξης /℃ | Πυκνότητα /(g/cm3) | Σκληρότητα HV/(N/mm)2) | Αντοχή σε εφελκυσμό /MPa | Θερμική αγωγιμότητα /[W/(cm⸳K)] |
|---|---|---|---|---|---|
| 95%Ag - 5%Pd | 980 ~ 1020 | 10.5 | 28 | 170 | 2.20 |
| 90%Ag - 10%Pd | 1000 ~ 1060 | 10.6 | 35 | 210 | 1.42 |
| 80%Ag - 20%Pd | 1070 ~ 1150 | 10.7 | 45 | 260 | 0.92 |
Το παλλάδιο βελτιώνει αποτελεσματικά την αντίσταση του αργύρου στην αμαύρωση από σουλφίδια. Καθώς αυξάνεται η περιεκτικότητα σε παλλάδιο, μειώνεται σημαντικά η τάση του αργύρου να αμαυρώνεται και να αποχρωματίζεται λόγω σουλφιδίου. Ωστόσο, το σημείο τήξης του κράματος αυξάνεται, το διάστημα κρυστάλλωσης επίσης διευρύνεται και το παλλάδιο είναι επιρρεπές στην απορρόφηση αερίων κατά την τήξη, γεγονός που αυξάνει τη δυσκολία τήξης και χύτευσης, απαιτώντας τήξη υπό κενό ή προστασία από αδρανή αέρια.
Λόγω της συνεχούς αύξησης της τιμής του παλλαδίου, η προσθήκη παλλαδίου αυξάνει σημαντικά το κόστος των κραμάτων αργύρου. Ως εκ τούτου, τα τελευταία χρόνια, η εφαρμογή του παλλαδίου στον άργυρο έχει μειωθεί σημαντικά και οι υπάρχουσες χρήσεις βασίζονται κυρίως σε μικρές προσθήκες.
Copywrite @ Sobling.Jewelry - Κατασκευαστής προσαρμοσμένων κοσμημάτων, εργοστάσιο κοσμημάτων OEM και ODM
Ενότητα IV Το ασημένιο ασήμι και οι τροποποιήσεις του
Το Sterling προέρχεται από το όνομα ενός Γερμανού κατασκευαστή νομισμάτων, των Easterlings, τον 12ο αιώνα. Έφερε στην Αγγλία προηγμένες τεχνικές παρασκευής ασημένιων νομισμάτων και κραμάτων αργύρου κατά τη διάρκεια της βασιλείας του Ερρίκου Β', δημιουργώντας ένα κράμα αργύρου που αποτελούνταν από 92,5 % Ag και 7,5 % Cu. Το κράμα αυτό χρησιμοποιήθηκε ευρέως και έγινε το πρώτο εμπορικό σήμα κράματος αργύρου στην Αγγλία του 12ου αιώνα. Προς τιμήν αυτού του νομισματοποιού, το κράμα ονομάστηκε ασήμι στερλίνας. Αρχικά, ο άργυρος sterling αναφερόταν συγκεκριμένα στο κράμα 92,5%Ag-7,5%Cu, αλλά αργότερα, το φάσμα των κραμάτων επεκτάθηκε, και έγινε γενικός όρος για όλο τον άργυρο 925. Από τον 12ο αιώνα, ο ασήμι 925 χρησιμοποιείται ευρέως σε ασημένια σκεύη και ασημένια κοσμήματα, χρησιμεύοντας σταθερά ως κράμα τυποποιημένης ποιότητας, και είναι το παλαιότερο διακοσμητικό κράμα αργύρου στην ιστορία.
1. Χαρακτηριστικά του ασήμι 925
1.1 Μηχανικές ιδιότητες
Σύμφωνα με το Σχήμα 4-11, η σύνθεση του κράματος αργύρου στερλίνας αντιστοιχεί στη διακεκομμένη γραμμή XY και τα σημεία τομής με το όριο φάσης είναι τα A, B, C. Η περιοχή από το σημείο B έως το σημείο C είναι ένα ενιαίο στερεό διάλυμα και μετά από αργή ψύξη κάτω από το σημείο C, μια φάση στερεού διαλύματος πλούσια σε χαλκό θα κατακρημνιστεί από το στερεό διάλυμα. Η θέρμανση του αργύρου στερλίνας στους 800 ℃ για επεξεργασία με στερεό διάλυμα δίνει ένα ενιαίο στερεό διάλυμα, το οποίο μπορεί να δώσει στο κράμα εξαιρετική ολκιμότητα και εργασιμότητα. Ο πίνακας 4-6 δείχνει ότι η αντοχή και η σκληρότητα του στερεού διαλύματος στον στερλίνα είναι σημαντικά υψηλότερες από εκείνες του καθαρού αργύρου. Η ψυχρή κατεργασία του στερεού αργύρου στερεού διαλύματος μπορεί να επιτύχει ένα καλό αποτέλεσμα σκλήρυνσης εργασίας (Εικόνα 4-14).
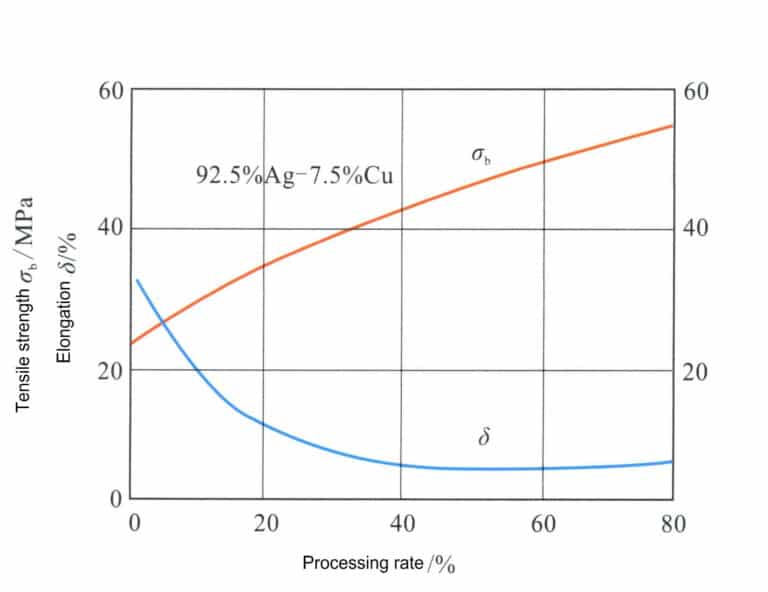
Ένα εξέχον χαρακτηριστικό του κράματος αργύρου είναι τα εξαιρετικά χαρακτηριστικά σκλήρυνσης λόγω γήρανσης, τα οποία μπορούν να μεταβληθούν μέσω της επεξεργασίας γήρανσης (Εικόνα 4-15). Το στερεό διάλυμα του αργύρου στερλίνας υποβάλλεται σε επεξεργασία γήρανσης στους 200-300℃ και όταν η θερμοκρασία γήρανσης είναι 200℃, η υψηλότερη σκληρότητα που επιτυγχάνεται είναι κοντά στην HV160, συγκρίσιμη με εκείνη του κράματος χρυσού 18Κ. ωστόσο, απαιτείται μεγαλύτερος χρόνος γήρανσης για να επιτευχθεί αυτή η μέγιστη τιμή. Καθώς αυξάνεται η θερμοκρασία γήρανσης, ο χρόνος για την επίτευξη της μέγιστης σκληρότητας μειώνεται σημαντικά, αλλά η μέγιστη σκληρότητα μειώνεται επίσης αναλόγως. Όταν η θερμοκρασία γήρανσης φτάσει τους 300℃, η επίδραση της σκλήρυνσης λόγω γήρανσης έχει μειωθεί σημαντικά.
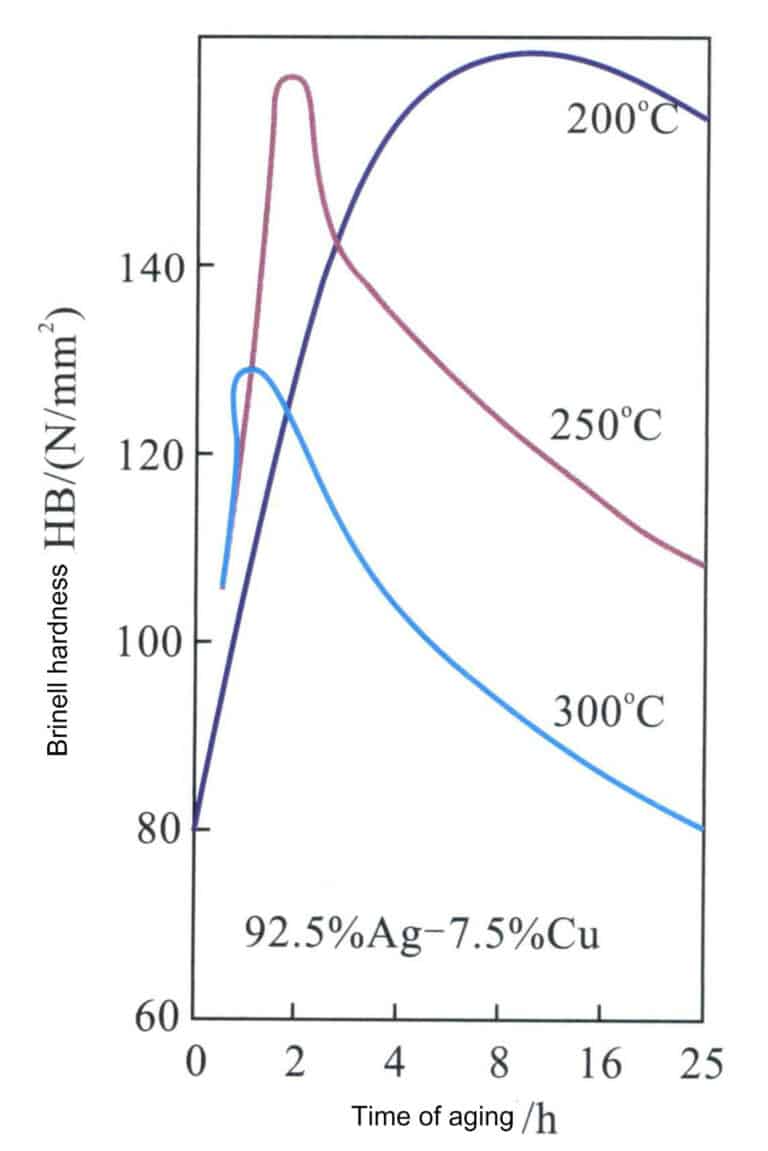
1.2 Casting Characteristics
The liquidus temperature of sterling silver is 898℃, and the alloy has a low melting point, making it suitable for melting in a graphite crucible.
However, sterling silver absorbs a large amount of oxygen in the molten state, which poses problems for smelting and casting. This property makes the alloy prone to volatilization at high temperatures or causes significant loss during the high-temperature cooling process due to splashing. For sterling silver, without sufficient deoxidizers, if protection is not applied during smelting, oxygen can easily accumulate, leading to copper oxidation, and jewelry castings are prone to defects such as porosity and oxidized inclusions. The oxidized copper in the castings can cause two types of problems: (1) the entire casting may have oxidized copper inclusions, which form hard spots when the inclusions are near the surface, protruding on the polished surface; (2) oxidized copper inclusions near shrinkage cavities appear as mottled cloudy spots on the polished surface, which are deep and difficult to clean off. Suppose the sterling silver melt is severely overheated or not protected for a long time. In that case, copper will oxidize severely, forming a viscous liquid surface, reducing the fluidity of the molten metal, leading to incomplete filling in some small areas of the casting, and often resulting in underfilling. The surface near the casting area appears red. In addition, the crystallization interval of sterling silver is relatively large, reaching 90℃, with significant differences between the liquid and solid phase components, tending towards paste-like solidification, with severe dendritic growth, while having lower fluidity, leading to a greater tendency for shrinkage porosity.
To prevent the accumulation of oxygen in the sterling silver melt, it is crucial to avoid contact between the molten metal and the atmosphere as much as possible during the smelting or casting process. Therefore, the following points should be noted.
(1) During electric furnace smelting, vacuum protection is used, or inert gases such as argon or nitrogen are employed for protection, which can eliminate oxygen in the smelting chamber and reduce the oxidation of the molten metal.
(2) When using a fire gun for smelting, the flame should be adjusted to a reducing yellow flame, covering the entire liquid surface to prevent the molten metal from absorbing oxygen. During electric furnace smelting, a reducing flame can sometimes be added at the mouth of the crucible to cover the molten metal.
(3) Sprinkle charcoal or anhydrous boric acid on the surface of the molten metal; they float on the surface of the silver liquid and can protect the silver liquid in two ways: a. forming a barrier between the molten metal and the air; b. reducing copper oxide. This method is unsuitable for centrifugal casting machines but works very well on manually operated vacuum casting machines.
(4) In the above method, it is also important to strengthen the protection of the molten metal during the pouring process. Especially when using a vacuum casting machine for pouring, since it is a manual pouring under vacuum conditions, it is necessary to protect the flow of molten metal. Typically, a reducing flame is used; when the gypsum mold is placed, the flame is ignited, and the flame must cover the pouring gate of the mold, which can eliminate the air inside the mold.
1.3 Polishing "red spot" phenomenon
Sterling silver often forms dark red spots on the surface during polishing, which severely affects the brightness and aesthetics of the polished surface, as well as the adhesion of the electroplated layer. This phenomenon is more pronounced on the surfaces of products that have undergone thermal processing, such as annealing and welding.
After heating the sterling silver block at 700℃ for 1.5 hours, the oxidation condition was observed under a microscope, revealing that the alloy not only formed an oxide layer on the surface but also developed an internal oxidation zone beneath the surface (Figure 4-16).

Sterling silver belongs to the Ag-Cu alloy. When the alloy comes into contact with oxygen in the air at high temperatures, selective oxidation of Cu occurs only after the temperature exceeds 400K. When the sample is immersed in dilute sulfuric acid, the surface layer of copper oxide can be removed. Therefore, after the sample is lightly polished, it can present a silver-white color. However, after further polishing, dark red spots appeared on the polished surface, damaging the reflective properties of the polished silver surface (Figure 4-17), indicating that oxidation products of Cu still exist in that area.

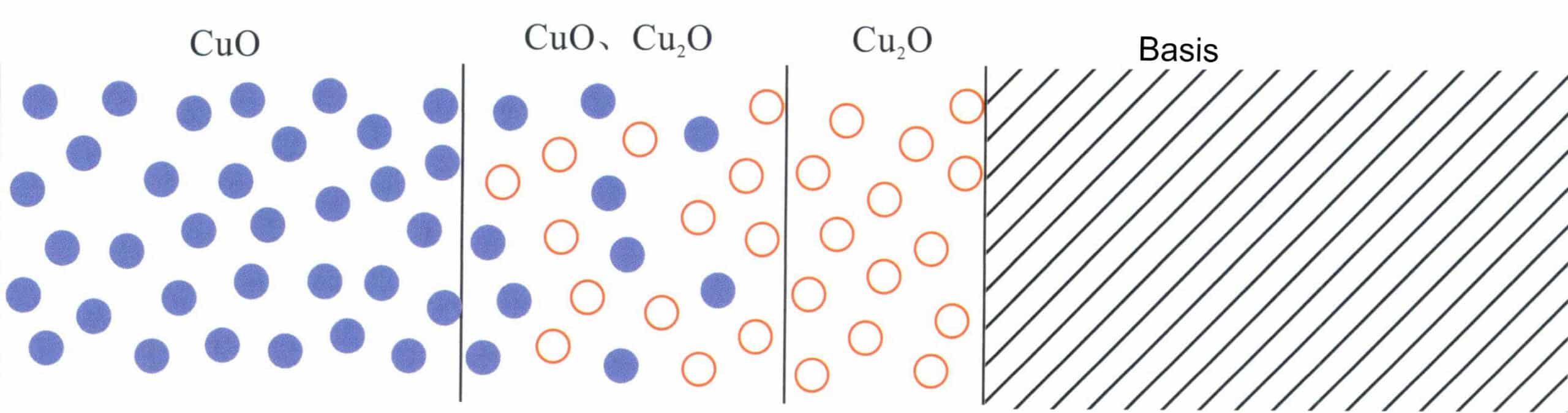
When copper comes into contact with oxygen in the air at high temperatures, such as during hot rolling, annealing, or welding, the surface of the copper workpiece first oxidizes to form red Cu2O and then further oxidizes to become black CuO. The oxidation of copper is not limited to the surface of silver alloys but may penetrate to a certain depth (Figure 4-18). According to the theory of high-temperature oxidation kinetics of alloys, when two diffuses simultaneously with Cu, there must be an accumulation of the Cu2O precipitate phase in the internal oxidation zone, and the alloy that has not undergone internal oxidation at the internal oxidation front will show depletion of Cu. Ag has a strong ability to absorb oxygen and transport oxygen to the interior of the metal at high temperatures. Hence, oxygen diffusion is dominant, and its permeability is much higher than that of Cu. Therefore, oxygen can penetrate the alloy surface’s sublayer, generating internal oxide precipitates. A direct pathway from the oxide to the alloy surface must exist to remove the sublayer’s copper oxide through acid etching. The copper content in sterling silver is only 7.5%, and its structure is a dual-phase solid solution without forming an oxide network, which means there is no direct pathway into the interior during acid immersion, allowing the internal Cu2O to remain intact. As a result, the surface of the oxidized sterling silver sample still exhibits black and irregular patches, known as “red spots.”
Research has found that the severity of the red spots on the surface of sterling silver is closely related to the heating temperature and heating time (Figure 4-19). The higher the heating temperature and the longer the heating time, the thicker the surface oxide film becomes, and the deeper the internal oxide layer penetrates into the substrate, making it difficult to remove through conventional polishing methods.

1.4 Darkening Color Change Phenomenon
Silver itself is prone to darkening and discoloration. The addition of Cu elements in sterling silver does not improve the alloy’s tendency to discolor. Moreover, the sterling silver alloy has a two-phase structure in both the cast and aged states, consisting of a silver-rich solid solution and a copper-rich solid solution, which are two incompatible phases. The potential difference between these two phases forms localized micro-battery reactions, increasing the electrochemical corrosion performance of the sterling silver alloy and reducing its corrosion resistance. Therefore, sterling silver jewelry is prone to corrosion and discoloration, severely affecting the appearance quality of silver ornaments.
2. The Influence of Alloying Elements on Sterling Silver
Due to the tendency of sterling silver to develop polishing red spots and dull discoloration issues, as well as the susceptibility to metallurgical and casting defects during melting, modification treatment is required. This involves alloying to enhance its overall performance while maintaining its good mechanical properties. Common alloying elements include Si, Zn, Sn, Ce, Ge, and others.
2.1 The impact of Silicon(Si) on sterling silver
Traditional sterling silver alloys tend to absorb gas during melting and pouring, making them prone to oxidation and resulting in larger gas pores in the castings. At the top are gas escape channels due to solidification gas absorption, accompanied by oxidized inclusions, and inclusions also exist within the castings. Adding a small amount of silicon to sterling silver can effectively improve its gas absorption tendency and oxidation resistance, resulting in better casting quality, reduced defects of gas pores and inclusions, and improved surface quality after polishing. From a thermodynamic perspective, the Gibbs free energy value for silicon-forming oxides is higher than that for copper oxides. Therefore, after adding an appropriate amount of silicon, the silicon in the molten metal preferentially reacts with oxygen, reducing gas pore defects. Due to the low density and high viscosity of silica, it can be removed from the surface of the molten metal using flux once it floats to the surface. The silicon added to sterling silver also helps improve the alloy’s resistance to oxidation and sulfide discoloration.
As the Si content increases, the grain structure will gradually become coarser, worsening the surface polishing effect and leading to the appearance of an “orange peel” effect on the surface. When the silicon content exceeds a certain value, the brittleness of the alloy significantly increases, making it prone to cracking during processing.
2.2 The Influence of Zinc(Zn) on Sterling Silver
Zn can lower the melting point of sterling silver, increase the fluidity of the melt, reduce shrinkage defects, and make the cast structure denser, but it has no significant effect on grain size. As an oxygen-active element, Zn, when added to sterling silver, preferentially reacts with oxygen in the molten metal, which can help reduce the oxidation of the molten metal due to absorbed oxygen. However, when the zinc content is too high, it can easily increase the amount of oxidized inclusions in the molten metal.
The atomic size difference between Zn and Ag is 7.76%, Cu, and the atomic size difference with Ag is 11.50%, Zn. The strengthening effect of Ag is less strong than that of Cu. When Zn partially replaces Cu in sterling silver, the casting and annealed hardness are reduced. When the Zn content exceeds 3.36%, the casting hardness of sterling silver is only around HV50, making it difficult to meet the jewelry inlay requirements and wear resistance requirements. Zn has an adverse effect on the processing performance of the alloy, reducing its plasticity. Excessive Zn content will cause issues such as delamination, scaling, and cracking during processing.
The electrode potential of Zn is lower than Ag and Cu, and a passivation film will spontaneously form on the Sterling silver surface, slowing down electrochemical corrosion and improving the alloy’s resistance to sulfide discoloration and oxidation. As the Zn content increases, Sterling Silver. The thickness of the oxide film gradually decreases. Still, when the Zn content exceeds 3.5%, Sterling silver is more prone to oxidation inclusions, which is detrimental to its electrochemical corrosion resistance and anti-sulfide discoloration performance.
2.3 The effect of Stannum(Sn) on Sterling silver
Adding Sn to sterling silver can lower the alloy’s melting point, increase the fluidity of the melt, and reduce the alloy’s shrinkage, resulting in a denser cast structure. A small amount of Sn can also refine the alloy’s structure; however, when the Sn content exceeds 2%, the alloy’s structure shows a noticeable coarsening, forming relatively large dendrites and shrinkage and segregation.
In sterling silver alloys, the partial replacement of Cu with Sn generally improves the initial hardness of the alloy in the cast state. As the Sn content increases, the hardness of the alloy first rises and then decreases. When the Sn content approaches 1%, the hardness reaches its maximum value; however, the ductility of the alloy is significantly affected, which may lead to cracking during cold working.
Sn is also an oxygen-active element. A certain amount of Sn can form a dense oxide film on the alloy’s surface, protecting the substrate. Sn can improve the electrochemical corrosion resistance of sterling silver. As the Sn content increases, the alloy’s electrochemical corrosion resistance improves. When the Sn content exceeds 2%, the alloy’s sulfide discoloration and oxidation resistance are significantly enhanced.
2.4 The impact of Cerium (Ce) on sterling silver
The addition of rare earth element Ce to sterling silver significantly impacts its structure. Ce can effectively purify the metal liquid and reduce gas content. When the Ce content is below 0.05%, it can refine the grain structure, mainly because Ce acts as a grain refiner during the solidification process of the metal liquid, reducing the degree of shrinkage porosity and improving density during annealing; Ce can also hinder grain boundary migration, thereby maintaining a fine grain structure.
Trace amounts of Ce can improve the mechanical properties of sterling silver, increasing its strength and hardness, enhancing ductility, and improving the alloy’s work-hardening effect. When the Ce content is further increased, it is prone to segregation at the grain boundaries, worsening the alloy’s processing performance and making it more susceptible to oxidation inclusions.
After adding trace amounts of Ce, the electrochemical corrosion resistance, oxidation spot resistance, and sulfide discoloration resistance of sterling silver can be greatly improved. When the Ce content exceeds 0.075%, the corrosion resistance of sterling silver will decline.
2.5 The impact of Ge on sterling silver
When Ge is added to sterling silver, and its content is between 0.2% and 0.8%, the cast hardness of sterling silver is higher, and its work hardening performance, electrochemical corrosion resistance, and discoloration resistance are all improved compared to sterling silver, reflecting better overall performance. When the Ge content is too low, the performance improvement of sterling silver is not significant; however, when the content is too high, it can easily cause grain coarsening of the alloy, leading to a decline in the overall performance of the alloy.
Section V The Discoloration and Protection of Silver
Silver and its alloy materials are widely used in the jewelry industry, and they have a significant characteristic: they easily undergo tarnishing and discoloration. After silver alloys discolor, the surface gloss greatly decreases, severely affecting the appearance quality of the jewelry and increasing the difficulty of the alloy processing.
1. The reason for silver tarnishing
The chemical potential of pure silver is +0.799 V, which is relatively high compared to the standard potential of hydrogen, classifying it as an inert metal. Under normal conditions, it does not react chemically with acids or bases, only reacting with strong oxidizing concentrated acids (such as concentrated nitric acid and hot concentrated sulfuric acid). However, silver jewelry will gradually tarnish after being worn for some time or even when placed in a storage box for a certain duration, and traditional sterling silver is particularly prone to tarnishing. The reasons for silver tarnishing can be summarized as follows.
1.1 Silver sulfide discoloration
Silver and its alloys are prone to corrosion and discoloration in environments containing H2S, SO2, and COS. Silver is very sensitive to H2S gas, and when the concentration of H2S in the atmosphere reaches 0.2 x 10-9 (volume fraction), it is sufficient to corrode silver, resulting in the formation of black Ag2S, namely:
4Ag + 2 H2S + O2 = 2Ag2S + 2H2O
The rate of silver sulfide discoloration in the atmosphere of H2S follows the Wagner diffusion kinetic mechanism, and when the content of H2S increases or when H2S coexists with other gases such as NO2, O2, the discoloration rate of silver sulfide intensifies. The SO2 in the air can also be converted into S2-to form Ag2S, causing silver discoloration. The sensitivity of SO2 is not as high as that of H2S, but when SO2 coexists with other gases such as NO2 and O2, the rate of sulfide discoloration will also intensify.
Silver is very sensitive to oxygen-containing sulfide solutions. The discoloration occurs slowly when silver is immersed in an oxygen-free Na2S solution. However, if the sample is taken out and the sodium sulfide solution attached to the silver surface comes into contact with oxygen, the silver sample will quickly show obvious discoloration. The longer it is exposed to air, the more severe the discoloration becomes. The sequence of color changes is silver, white → yellow → brown → blue. This is because the standard electrode potential of Ag (0.779 V) is lower than that of O at 1.229 V. Ag is thermodynamically unstable when oxygen is present, first by O2 being oxidized to Ag+ and then combining with Ag+ and S2-to form an insoluble compound Ag2S. The higher the concentration of sulfides, the more severe the discoloration. The chemical reaction of silver in oxygen-containing Na2S aqueous solution is:
4Ag + 2H2O + O2 + 2S2-= 2Ag2S↓+4OH–
Ag-Cu Alloys are more prone to sulfide formation and produce black Cu2 S because Cu is more easily sulfide than Ag; thus, they discolor more easily than pure silver.
1.2 Electrochemical corrosion in humid environments
In humid environments, the unevenness of the silver surface state (uneven alloy composition or physical states such as internal stress, surface smoothness, etc.) can cause different potentials in different areas of the metal surface beneath the water film, creating a potential difference between these areas. Two adjacent areas with different potentials are connected, with the water film acting as an electrolyte to transport ions and the metal serving as a conductor for electron transport, forming an electric cycle. This creates the effect of a short-circuit battery, forming many corrosion micro-batteries on the metal surface. The cast structure of sterling silver generally consists of a two-phase structure made up of silver-rich solid solution and copper-rich solid solution. In humid environments, the copper-rich solid solution phase becomes the anode of the corrosion micro-battery, making the alloy more susceptible to corrosion and discoloration. Higher-quality silver can also undergo electrochemical corrosion due to impurities, and in humid environments containing salt, the silver surface often transforms into silver chloride, a gray-brown adhesive substance resembling soil.
1.3 The effect of ultraviolet light on silver discoloration
Light, as an external energy source, can promote the ionization of metal ions, thereby accelerating the reaction between silver and the corrosive medium, that is accelerating the discoloration reaction of silver. When the surface of the silver-plated layer is irradiated with light of different wavelengths, the results are shown in Table 4-8. It can be seen that the silver-plated layer is prone to discoloration after absorbing ultraviolet light, and the ability of the irradiated light wavelength to cause discoloration increases as the wavelength decreases.
Table 4-8 The effect of irradiated light wavelength and irradiation time on the discoloration of the silver-plated layer
| Irradiated light wavelength/nm | Irradiation time /hours | ||||
|---|---|---|---|---|---|
| Irradiated light wavelength/nm | 6 | 12 | 18 | 24 | 48 |
| 253.7 | Unchanged | Focal Macula | Yellow Brown | Brown-Black | All Black |
| 365.0 | Unchanged | Unchanged | Unchanged | Κίτρινο | - |
| Ηλιακό φως | Unchanged | Unchanged | Unchanged | Localized macular | - |
According to the results of X-ray photoelectron spectroscopy and Auger spectroscopy analysis, the color change of the silver-plated layer under ultraviolet light is mainly composed of Ag2O, AgO, AgCl, and corresponding silver compounds.
2. Ways to prevent silver discoloration
Regarding the discoloration of silver and its alloys, considerable research has been conducted both domestically and internationally on how to improve the discoloration resistance of silver. From the perspective of promoting discoloration resistance, it can be summarized into two main categories: surface modification treatment of silver alloys and the development of discoloration-resistant silver alloys.
2.1 Surface modification technology to prevent silver discoloration
Surface modification involves using chemical or physical methods to form an inert film on the surface of silver jewelry, isolating the silver substrate from corrosive media in the environment, blocking the reactions between light, oxidants, corrosive media, and silver, and preventing the occurrence of discoloration. Depending on the type of film formed, surface modification can be categorized into several major types: electroplating, immersion, chemical passivation, electrochemical passivation, organic adsorption passivation, resin coating, and self-assembled films.
Rhodium plating is the most widely used surface modification method for sterling silver jewelry. By coating a thin film of rhodium on the surface of the jewelry, a bright, mirror-like appearance can be achieved, and the rhodium layer has high hardness and good chemical stability, which can enhance the wear resistance and discoloration resistance of silver jewelry. However, due to production costs and the surface brightness effect, the rhodium layer on jewelry is usually very thin and can easily wear off during use, losing its protective effect.
Chemical passivation or electrochemical passivation methods can form an inorganic passivation film on the surface of silver. Chromate passivation is a commonly used chemical passivation method for silver craft jewelry, which generates a layer of silver oxide and silver chromate in an acidic or alkaline solution containing hexavalent chromium compounds. Electrochemical passivation utilizes the principle of cathodic reduction to generate a film layer composed of silver chromate, chromic acid, basic silver chromate, and basic chromic acid on the surface of silver. These film layers have good passivation effects, can reduce the free energy of the alloy surface, and serve to prevent discoloration while having no significant impact on the appearance of silver crafts. However, issues include the film layer needing to be more non-dense, poor mechanical stability, complex structure, difficulty covering edges, and environmental impact.
The application of methods such as immersion, spraying, and coating to form an organic protective film on the surface of silver can improve its anti-tarnish performance, and considerable research has been conducted in this area both domestically and internationally. Benzotriazole, tetrazolium, and various sulfur-containing compounds can form complexes on silver. Composite films can be formed, and some water-soluble polymers are added to create film agents, but the resulting film layer needs to be more dense, and the anti-tarnish effect could be better. Some protective agents are oil-soluble anti-tarnish agents based on paraffin and long-chain quaternary ammonium salts, which can form a solid lubricating layer on the surface of silver, providing a good anti-tarnish effect. However, their resistance to solution corrosion is poor, and using hot gasoline as a solvent poses significant risks. Additionally, after coating a layer of wax on the surface, the brightness and reflectivity of the alloy will be greatly reduced. Spraying acrylic varnish, polyurethane varnish, and organic silicone transparent varnish on the surface of silver alloys can enhance their anti-tarnish ability. Still, the coating must also have sufficient thickness to provide a certain anti-tarnish effect, which can also affect the appearance of silver craft jewelry.
Traditional protective agents do not perform well in protecting the gaps of silver craft jewelry, while molecular self-assembly systems such as alkyl thiols, organ silanes, and Schiff bases can form protective films on the surface of silver jewelry. These films have characteristics such as dense and uniform structure, unaffected by the shape of the substrate surface, free of metallic impurities, and do not affect the appearance of the substrate, demonstrating excellent anti-tarnish ability for silver, making them one of the promising processes for surface treatment of tarnished silver craft jewelry.
Overall, surface modification processes have characteristics such as low cost, simple and practical processes, and certain anti-tarnish performance. However, due to the thinness of the generated film, the exposed silver substrate will still come into contact with corrosive media and tarnish once it is scratched.
2.2 Anti-tarnish silver alloys through overall alloying
As early as 1927, the National Bureau of Standards in the United States proposed after research that there is no other way to completely prevent the sulfidation reaction of silver unless alloyed with other precious metal elements. To suppress the formation of silver sulfides, it is necessary to form alloys with 40% palladium, 70% gold, or 60% platinum. However, it is undeniable that improving the tarnish resistance of silver alloys through alloying is still a necessary and effective method. Many countries worldwide are still striving to develop new types of tarnish-resistant silver alloys, achieving some research results. The main alloying elements that form tarnish-resistant silver alloys can be classified into three categories.
(1) Alloying with precious metals.
Among all precious metal elements, silver has relatively active chemical properties. Adding precious metal elements with higher chemical potentials, such as Au, Pd, and Pt, can improve the electrode potential of silver alloys and enhance their tarnish resistance. For example, adding 5% Pd to sterling silver significantly improved the tarnish resistance of the silver alloy, which showed no significant discoloration or corrosion after ten days in a chlorine or ammonia atmosphere. The elongation of the alloy is between 15%-26%, and it can be produced using conventional casting and mechanical forming methods. Similarly, in the series of tarnish-resistant silver alloys containing platinum, when the Pt content is 1%, the tarnish resistance is more than three times that of sterling silver; when containing Pt 3.5%, the tarnish resistance is more than six times that of sterling silver; when containing Pt 5%, the tarnish resistance is more than eight times that of sterling silver. Silver alloys containing platinum can significantly refine the grain size while increasing hardness; the alloy also has excellent plasticity; it enhances the brightness of the alloy, approaching the color of platinum, and prevents the appearance of red spots. Alloying with precious metals significantly increases the material cost of tarnish-resistant silver, and its market application is relatively limited.
(2) Alloying with rare earth metals.
Many studies have shown that adding trace amounts of rare earth elements to silver or silver alloys helps improve the alloy’s resistance to sulfidation discoloration. The most widely used rare earth elements include Yttrium(Y), cerium(Ce), lanthanum(La), etc. For example, when rare earth elements are added to pure silver if the rare earth content is below 0.11%, it can exhibit better sulfidation discoloration resistance than pure silver. The addition of rare earth elements refines the grain size of the cold-deformed recrystallization structure, and the dispersed silver-rare earth compound second phase formed through fragmentation and re-aggregation effectively strengthens the silver alloy and improves the thermal stability of the alloy, demonstrating a high resistance to aging softening. Most tarnish-resistant silver developed domestically has chosen rare earth elements as alloying elements.
(3) Alloying with other oxygen-active elements.
Adding oxygen-active elements such as Zn, Si, Sn, In, and Ge to the Ag-Cu alloy can improve the sulfidation and oxidation discoloration resistance of silver alloys. This is currently the most common type of tarnish-resistant silver alloy on the market. Italy, the United States, Germany, and others have developed various tarnish-resistant silver alloy fillers, achieving sulfidation discoloration effects that reach more than five times that of sterling silver. The principle of its tarnish resistance: these elements belong to oxygen-active elements, and their oxides have lower free energy than copper oxides, with a stronger affinity for oxygen, allowing for the formation of more stable oxides. Before forming Ag2S, these oxides form a dense protective film layer, acting as a barrier to protect the silver matrix.
Section VI Performance Evaluation and Common Issues of Tarnish-Resistant Silver
1. Performance Evaluation of Anti-tarnish Silver
Various anti-discoloration silver filling materials have appeared on the market, with performance varying widely. Adopting appropriate methods to evaluate their performance is necessary, providing a basis for selecting suitable filling materials.
1.1 Evaluation Methods for Anti-Discoloration Performance
Anti-discoloration performance is one of silver alloys’ most important performance indicators, mainly including resistance to sulfide discoloration and oxidative red spots, which must be tested through experiments.
1.1.1 Evaluation Method for Resistance to Sulfide Discoloration
According to the conditions and locations used in the experiment, it is divided into outdoor and laboratory testing methods.
(1) Outdoor testing method
The outdoor testing method involves placing silver alloy samples in a real environment to observe the time the samples remain unchanged in color and the specific phenomena of color change that occur to evaluate the alloy’s resistance to color change. This method can more accurately reflect the alloy’s resistance to color change, but it has its own drawbacks: (1) The time to obtain test results is relatively long; for example, in certain environments, alloys with good corrosion resistance may take years to yield results; (2) The reproducibility of the results is low. Due to differences in regions and times, the natural environment will vary to some extent. Therefore, the results of the same alloy tested in different regions will differ significantly; even in the same region at different times, the test results will also vary.
Due to the long testing time in natural environments, accelerated corrosion methods are sometimes used to obtain results more quickly. For example, they are placing the alloy in harsh environments such as near electroplating workshops or boiler flue gas or exposing it to ultraviolet radiation in the atmosphere for testing. However, these methods are easily affected by environmental pollution and other factors, leading to significant differences in the degree of similarity, authenticity, and reproducibility of the test results compared to natural corrosion color change. Therefore, they are not advisable.
(2) Laboratory testing method
According to the corrosive media used in laboratory tests, it can be divided into two methods: liquid phase tests and gas phase tests.
(2.1) Liquid phase test method.
The more commonly used methods are the sulfide solution and artificial sweat immersion methods. The former involves immersing the sample in a solution of sodium sulfide or ammonium sulfide at a certain concentration, using the Tuccillo-Nielsen method, which is quite general. The sample is fixed on a rotating wheel and is periodically immersed in a solution of concentration 0.5% or 2% Na2S solution at a speed of 1r/min. It can effectively detect the discoloration resistance of silver alloys under the action of oxygenated sodium sulfide solution. The latter involves preparing artificial sweat according to relevant standards, immersing the sample in sweat with a certain pH value and temperature, usually around pH 6.5, at a temperature of 30℃ or 37℃. During the immersion test, it is necessary to maintain the stability of the solution temperature, and the sample and the comparison sample should be tested under the same conditions. The color changes of the comparison sample after different immersion times can be accurately measured using a colorimeter to determine the degree of discoloration of the sample.
(2.2) Gas phase test method.
Using gas phase test methods to examine the discoloration resistance of silver alloys and silver coatings has become quite common, forming international and domestic standards. Gas phase tests can be conducted in static or flowing gas. The gas contains substances that can cause discoloration of silver alloy materials, such as H2S, SO2, Cl2, and NO2, which can be a single gas or a mixture of two or more gases; the gas can be introduced or generated through chemical reactions. Common gas phase test methods mainly include:
A. H2S test method. This method uses H2S to conduct accelerated corrosion tests, widely used in the electronics industry for evaluating the discoloration resistance of electronic components and electrical contact materials, with multiple international and national standards. These standards include those using high-concentration H2S atmospheres as well as low-concentration ones. However, there is no specific test standard for discoloration resistance in the jewelry industry, leading to various practices, some referencing electronic industry standards for testing, while others choose their testing conditions. A typical testing method is the Thioacetamide (TAA) method, which is a strict standard for measuring silver jewelry, corresponding to the international standard Metallic Coatings-Thioacetamide corrosion test (TAA test) (BS EN ISO 4538-1995). Due to the high concentration of H2S atmosphere, some silver alloy surfaces are prone to discoloration, and the corrosion film layer may become loose and peel off, which can affect the accuracy and reproducibility of the results to some extent. The discoloration conditions of different types of silver alloys after H2S corrosion for 3 hours are compared as shown in Figure 4-20, where the concentration of H2S is 13 x 10-6, relative humidity is 75%, and temperature is 30℃.

B. SO2 Test method. SO2 Can accelerate the corrosion of silver alloys, typical methods include the “Corrosion Test of Metals and Other Inorganic Coatings under Condensation Conditions of Sulfur Dioxide”, which uses a certain volume, heated closed acrylic test chamber, introducing a certain concentration of SO2 gas, tested over three cycles (non-continuous exposure). Using a single SO2 gas for corrosion testing has a longer test cycle, and assessing the corrosion results between samples is somewhat difficult.
C. Mixed gas test method. The corrosion products of this method are relatively close to actual conditions, and the test results are relatively stable. This method is conducted in a specially designed test environment, with humidity at 75%, the temperature at 25℃, H2S, and concentrations of 0.8mg/L, SO2, and 3mg/L, updated three times per hour. Japan invented a mixed gas accelerated corrosion method for testing the corrosion status of silver alloys in electronic devices, composed of air, H2S, and NO2, where H2S is the main factor causing discoloration, and NO2 acts as a catalyst to accelerate the reaction between silver and H2S, allowing the formation of corrosion products in a shorter time.
1.1.2 Evaluation method for anti-oxidation red spot performance
There are generally two methods to evaluate silver alloys’ anti-oxidation red spot performance. (1) Place the sample in an electric furnace for heating, controlling the atmosphere, heating temperature, and insulation time, then take a cross-section of the sample to observe the oxidation film under a microscope (Figure 4-21). Polish the sample and observe the red spot condition on the polished surface. This method can stably control test conditions, and the test accuracy is relatively good. (2) Heat the sample with a torch to a certain temperature, then stop heating and let the sample cool naturally to room temperature, repeating the above operation several times, taking a cross-section of the sample to observe the oxidation film condition, and polishing to observe the red spot condition on the sample surface; this method has a larger human factor.

1.2 Evaluation of Process Performance
Silver alloys used for making jewelry need to have good resistance to sulfide discoloration and oxidation spots and require good mechanical and process performance, which often presents contradictions in joint development. Some alloying elements are beneficial for discoloration resistance. Still, when their content reaches a certain level, they may negatively impact the alloy’s casting and processing performance, leading to a decline in the overall performance of the alloy; In contrast, some alloying elements can improve the mechanical properties of silver, they may not be favorable for its discoloration resistance. Therefore, when selecting discoloration-resistant silver alloys, it is necessary to evaluate their discoloration resistance while fully considering the performance requirements of the alloy for different processing techniques. For example, the melting method can affect the oxidation resistance of the alloy; the same alloy can yield different results when melted using a torch, induction heating in the atmosphere, or melted in a protective atmosphere or vacuum; similarly, jewelry production may use casting methods, stamping methods, or welding methods, each of which has a different emphasis on the process performance requirements of the alloy, requiring separate evaluations from the perspectives of castability ability, cold working performance, welding performance, etc., and fully consider the process operability of the alloy to avoid operational issues that may arise from a too-narrow process range.
1.3 Evaluation of Safety and Cost-Effectiveness
The silver alloy used for jewelry must meet safety requirements, and the content of toxic and harmful impurity elements must not exceed international standards. Additionally, the silver alloy’s comprehensive performance and material cost should be evaluated in terms of cost-effectiveness.
2. Common issues with anti-tarnish silver for jewelry
The issues with anti-tarnish silver for jewelry in the market mainly include the following aspects.
2.1 Insufficient anti-tarnish performance
When jewelry companies discuss the silver jewelry business, the most direct question from customers is how long the silver jewelry can remain untarnished. Many customers require it to remain untarnished for at least one year, but companies need help guaranteeing this. Besides the influence of usage environment and storage methods, a significant reason is that the anti-tarnish performance of the alloy itself is not outstanding. Silver alloys containing precious metal elements like Pd and Pt have better anti-tarnish performance, but their relatively high prices deter many companies, as customers often need to specify the use of such alloys or pay extra for them. The market is predominantly occupied by anti-tarnish silver alloys that use oxygen-active element alloying. Theoretically, the dense oxide film formed by these elements should prevent the internal metal from further sulfiding and oxidizing, thereby improving the silver alloy’s resistance to sulfide and oxidative discoloration. However, it should be noted that the microstructure of the base alloy, the distribution of alloying elements in the base, and the structure and mechanical properties of the surface oxide film can significantly affect the structure of the oxide film. If the formed alloy oxide film is unevenly distributed, loose and coarse, or has micro-cracks, it will not provide effective protection. In other words, different alloys with different component ratios will yield different anti-tarnish results. Even if the same alloy manufacturer uses the same alloy formula, if the company does not strictly adhere to the specified melting and casting process standards during production, the results may also vary.
2.2 The problem of insufficient hardness
Many companies have reported that the hardness of tarnish-resistant silver alloys is much lower than that of sterling silver, making them relatively easy to deform and unable to meet the requirements for mold making, elastic parts, etc. This is indeed the case. For silver alloys that improve tarnish resistance with Pd, Pt precious metal elements, due to their similar crystal structure to silver and high solubility, the strengthening effect is poor, and the initial hardness is generally low. Zn is commonly used as the main alloying element for tarnish-resistant silver alloys alloyed with other elements, and the strengthening effect could be better. Therefore, most tarnish-resistant silver alloys have low as-cast hardness, usually below HV60, which is insufficient for jewelry products with certain strength requirements. Although alloys can increase hardness through deformation processing, only casting processes can be used for the production of most set jewelry, making deformation methods unsuitable. Of course, some alloys can improve hardness through aging treatment, but they are often not used or misused in actual production because jewelry-making involves a multi-process craft. During the mold-making stage, gemstone setting stage, and even polishing stage, the workpiece may undergo welding or heating, usually done by operators using flame heating, with heating temperature, heating time, and cooling speed being quite arbitrary, making it generally difficult to achieve the effects expected by alloy suppliers. Additionally, once the jewelry has been set with gemstones, it is no longer suitable to use aging treatment methods to increase hardness, as high-temperature quenching can easily damage the gemstones.
Therefore, from a practical application perspective, it is necessary to improve the alloys’ as-cast and annealed hardness. From China’s resource advantages, rare earth elements should be worth considering.
2.3 Issues related to casting
The vast majority of jewelry is formed through casting, and several jewelry companies have established their casting departments. Companies generally only purchase filler from alloy suppliers and then buy pure silver to prepare the required silver alloy. During the casting production process, many companies are often troubled by various casting issues such as porosity, sand holes, shrinkage, inclusions, and cracks, which affect the normal order of production and increase production costs.
Sterling silver, with Cu as the main alloying element, is prone to defects such as porosity and oxidized inclusions if not protected during melting, increasing the molten metal’s viscosity. The oxidized film formed at the front of the molten metal increases surface tension, leading to increased filling resistance and affecting forming performance. The resulting defects, such as porosity and inclusions, significantly increase the difficulty of subsequent polishing.
Silver alloys primarily composed of Pd, Pt, and other precious metal elements have a higher melting point, increasing the likelihood of porosity. This is because jewelry mainly uses gypsum molds, and gypsum has poor thermal stability; the higher the alloy’s melting point, the greater the possibility of thermal decomposition of gypsum, leading to porosity in the castings.
Different anti-tarnish silver alloys contain different types and amounts of oxygen-active elements, exhibiting varying casting performances. Si oxide has a low density and high viscosity, making it easy to float to the surface of the molten metal and be removed with the help of flux, which is beneficial for fluidity and filling performance. However, excessive Si can lead to thermal cracking and polishing issues; removing Zn and Sn oxides is more difficult. For silver alloys containing a large amount of low-melting-point oxygen-active elements (such as Zn, Sn, In ), using a torch for melting can easily produce volatiles and oxidized inclusions, and using induction heating can also lead to similar problems due to overheating. A small amount of rare earth added can improve filling properties. Still, the amount of rare earth increases to a certain extent. In that case, the formed rare earth oxides will increase the viscosity of the molten metal, counteracting the purifying effect of the rare earth and negatively affecting casting performance.
Among the issues above, porosity is one of the most prominent problems. The porosity generation is closely related to the properties of the silver alloy itself. As mentioned earlier, silver has a typical characteristic of absorbing a large amount of oxygen in the molten state, causing the molten metal to splash at high temperatures, resulting in significant losses easily. During the solidification process of casting, the solubility of gas in the molten metal decreases with the drop in temperature, leading to gas supersaturation, precipitation, and enlargement, forming bubbles that fail to be discharged in time, resulting in porosity (Figure 4-22).

From the mechanism of pore formation, it can be seen that there are mainly two approaches to reduce or avoid pore defects: (1) minimize the amount of gas entering the molten metal; (2) take measures to release the gas in the molten metal before pouring.
(1) Reduce the gas entering the molten metal.
First, the quality of the raw materials must be controlled. The raw materials should be dry and clean, not damp or oily. The purchased pure silver materials come in forms such as granules, bars, and plates, with granules being the most common. Since granules are formed by metal droplets rapidly cooling in water, they can sometimes be hollow and even contain water inside, which can introduce a large amount of gas during melting. They must be thoroughly dried or pre-melted into ingots before use. If the surface of the raw materials has oil or other organic impurities, it will also introduce gas, especially when reusing scrap from stamped jewelry, which often adheres to oil. It should be degreased and cleaned thoroughly before use. The ratio of new and reused materials should be reasonably controlled when mixing materials. Each time the raw materials are melted and cast, they will be contaminated, including gas absorption, reaction with gypsum molds, and residual inclusions. Therefore, the amount of reused materials should generally be controlled within 50%.
Secondly, effective protective measures should be taken during melting. Different enterprises have different production conditions, and the melting methods used also vary. Common melting methods include gas-oxygen flame, acetylene oxygen flame, high-frequency induction furnace, and medium-frequency induction furnace. When melting in the open atmosphere, the molten metal will inevitably absorb gas; the larger the liquid surface and the longer the contact time, the greater the tendency to absorb gas, mainly oxygen from the air. When using flame melting, it also includes oxygen brought in by the oxidizing flame. Therefore, protective measures should be taken during the melting process to reduce the amount of gas absorption if silver is melting in the atmosphere; crushed charcoal, graphite sheets, or dehydrated borax can be used as a cover. If flame melting is used, it should be adjusted to an orange-yellow reducing flame, and the melting time should be a manageable length. If conditions permit, priority should be given to vacuum induction melting, which can be done under low vacuum with protective gas. This involves evacuating the melting chamber first, then backfilling it with nitrogen or argon as protective gas, followed by heating and melting. Nitrogen is cheaper, but it has a certain solubility in silver, which poses a risk of causing pores; argon is more expensive but is more stable in silver and should be prioritized.
(2) Promote gas release in the molten metal before pouring.
Under atmospheric conditions, molten silver inevitably absorbs gas. To avoid the formation of gas pores, the molten metal should undergo degassing treatment before pouring, allowing as much gas dissolved in the silver liquid as possible to be released. Two methods can be adopted:
A. Using floating gas bubbles for degassing. By blowing fine, dense argon bubbles into the bottom of the molten metal using a breathable plug, it does not react with the molten metal and becomes floating gas bubbles. The bubbles serve as a vacuum space for the gases dissolved in the molten metal, allowing the dissolved gases to diffuse into the floating bubbles, becoming gaseous molecules that rise with the bubbles. When the floating bubbles rise to the surface of the molten metal, the gas inside the bubbles escapes into the atmosphere, achieving the goal of reducing the gas content in the molten metal.
B. Using condensation method for degassing. The silver liquid is slowly cooled to the solidification temperature, causing most of the dissolved oxygen and other gases to precipitate due to the decrease in solubility with the drop in temperature, thus achieving the purpose of degassing. It is then rapidly heated back to the pouring temperature for casting. For silver liquids with poor raw material quality and high gas content, multiple cycles of condensation and remelting can be performed to improve their quality.
2.4 Issues in cold processing
Issues in cold processing in the production process of silver jewelry, common cold deformation processing techniques include cold volume forging such as cold heading, cold extrusion, stamping, etc., and sheet metal stamping such as stretching, blanking, trimming, punching, etc. Material rolling, such as cold rolling, roll forming, etc., and the following issues are often encountered during processing.
(1) Surface sand holes of profiles.
The surface quality of profiles depends not only on the surface quality of the ingot but is also closely related to the surface quality of the rollers. When the roller surface has scratches or local damage, it will be replicated on the profile surface; when dust or other debris accumulates on the roller surface, it will be pressed into the profile surface, worsening the surface quality of the profile (Figure 4-23). Therefore, during production, the roller surface should be frequently wiped to prevent dust and other impurities from accumulating and scratching the rollers or being pressed into the strip surface. The rollers should be covered when not in use to protect the surface. The diameter of the finished product rollers should be small and highly polished or electroplated to achieve a mirror effect.

(2) Annealing defects.
This includes blistering, abnormal grain growth, and incomplete annealing.
A. Blistering. Blistering on the surface of sheets and strips is caused by gas holes within the ingot or reactions between the ingot and the atmosphere during annealing. The pressure increases when the bubbles are heated, causing the metal surrounding the bubble to expand and form blisters (Figure 4-24). This issue can generally be avoided by controlling the casting or annealing conditions. For example, it enhances deoxidation during the melting process, reduces the dissolved oxygen content and oxidation in the molten metal, controls the annealing temperature, and avoids using hydrogen-rich annealing atmospheres.
B. Abnormal grain growth. Silver will exhibit significant grain growth when the annealing temperature is too high or the annealing time at high temperature is too long (Figure 4-25). Excessively coarse grains affect mechanical properties and severely impact the surface quality of processed jewelry. Therefore, the annealing process should be reasonably formulated based on the size and quality of the profile.
Figure 4-24 Bubbles appearing on the surface of silver profiles after annealing

Figure 4-25 Abnormal grain growth caused by improper annealing of silver
C. Incomplete annealing. Different silver alloy materials have different recrystallization temperatures. If the annealing temperature is too low, the amount loaded into the furnace is too large, or uneven heating is applied with a torch, incomplete annealing may occur. In this case, residual stress will remain within the profile, affecting subsequent processing and leading to defects such as cracks.
2.5 Issues related to polishing
Jewelry has high requirements for surface quality, and most jewelry must undergo polishing to achieve a mirror-like finish. Polishing of anti-tarnish silver alloys often encounters several typical problems, such as orange peel surface, dents, scratches, and comet tails. When the alloy’s grain is coarse, it is prone to forming an orange peel surface; when there are shrinkage or porosity defects in the alloy, it is likely to form polishing dents; when high hardness segregated phases or inclusions appear within the alloy’s grain structure, it is easy to form polishing scratches and comet tails.
To achieve a good surface polishing effect, in addition to correctly executing the polishing operation process, the properties of the alloy itself also have an important impact. Grain refinement and improvement of casting performance are the main ways to enhance polishing performance.