Proč mají drahé kameny více barev?
Tajemství tvorby barev a metody měření
Barvy drahých kamenů jsou bohaté a rozmanité a mají jedinečné kouzlo, které lidé odjakživa milují. Kvalita drahých kamenů do značné míry závisí na jejich barvě. Barva drahého kamene je důležitým ukazatelem při hodnocení drahých kamenů a většina optimalizačních úprav drahých kamenů zahrnuje změnu nebo zlepšení jejich barvy. Proto je pochopení příčin zbarvení drahých kamenů zásadním předpokladem pro optimalizační ošetření drahých kamenů. Pouze na základě znalosti toho, jak drahé kameny získávají svou barvu, lze určit, zda lze drahý kámen optimalizovat, jaké optimalizační schéma přijmout a jaký experimentální plán stanovit. Existuje pět běžných teorií zbarvení drahých kamenů: klasická mineralogická teorie, teorie krystalového pole, teorie molekulových orbitalů, teorie energetických pásů a fyzikální optické efekty. Tyto teorie tvoří teorie zbarvení běžných přírodních drahých kamenů a níže je uveden stručný úvod do těchto pěti teorií zbarvení.

Schéma tří barevných prvků
Obsah
Oddíl I Barva a měření barvy drahých kamenů
Barvy drahých kamenů jsou bohaté a různorodé a určení typů barev drahých kamenů je zásadní pro posouzení jejich hodnoty. Hodnotu drahých kamenů ovlivňují také různé barevné stupně, proto je přesné posouzení barev různých drahých kamenů základním předpokladem pro určení jejich hodnoty. Při hodnocení barevných drahých kamenů je barva nejdůležitějším faktorem. Obecně platí, že čím atraktivnější je barva drahého kamene, tím vyšší je jeho hodnota. Jasné, syté a intenzivní barvy jsou obvykle přitažlivější než barvy příliš tmavé nebo příliš světlé. Samozřejmě existují výjimky, například u diamantů, kde čím vyšší je bělost barvy diamantu, tím vyšší je jeho hodnota.
1. Význam barev drahých kamenů
Již od starověku lidé milují drahé kameny pro jejich jedinečný půvab, zejména pro jejich syté a barevné odstíny, jako je rubín rudý jako holubí krev, zářivě zelený smaragd a nefrit, které zanechávají trvalý dojem. Barva je důležitým ukazatelem pro hodnocení kvality drahých kamenů a hraje zásadní roli při určování jejich kvality, přičemž význam se odráží především v následujících třech aspektech.
(1) Barva minerálů drahých kamenů je důležitým základem pro hodnocení drahých kamenů.
Barva drahého kamene má zásadní význam pro jeho hodnocení a určuje jeho hodnotu. Například u diamantů může rozdíl v barvě o jeden stupeň vést k cenovému rozdílu přibližně 5%. Čím vyšší je bělost, tím vyšší je stupeň diamantu; naopak diamanty se žlutými nebo hnědými odstíny mají nižší stupeň a jejich cena prudce klesá. Ceny barevných diamantů se liší a různé barevné diamanty mají různé ceny. Obecně však platí, že ceny vzácně zbarvených diamantů se mohou násobit. Ostatní barevné drahé kameny, jako jsou rubíny, safíry a smaragdy, se také dělí do různých tříd podle barvy a hodnota drahých kamenů v různých třídách se může výrazně lišit.
(2) Optimalizační úprava drahých kamenů často zahrnuje zlepšení jejich barvy.
Optimalizační metody úpravy drahých kamenů obvykle zahrnují změnu nebo zlepšení barvy drahých kamenů, takže zlepšení drahých kamenů lze také označit jako změnu barvy drahých kamenů. Se zlepšováním barvy drahého kamene se odpovídajícím způsobem mění i jeho průhlednost. Průhlednost je totiž vlastnost související s barvou. Například modré safíry se pouhým okem jeví jako mnoho neprůhledných černých barev, ale při rozřezání na tenké plátky je vidět průhledná modř. Zlepšení průhlednosti často doprovází zlepšení barvy. Proto pouze na základě určení příčiny barvy drahého kamene lze zjistit metody pro jeho zlepšení. Pochopení příčiny barvy je předpokladem pro studium úprav pro optimalizaci drahých kamenů.
(3) Studium příčin barvy drahých kamenů poskytuje teoretický základ pro syntetické drahé kameny a jejich zkvalitňování.
Barvy drahých kamenů, jako je granát, malachit a olivín, jsou dány jejich přirozenými složkami a u těchto drahých kamenů nelze jejich barvu změnit běžnými metodami optimalizace. Většina barev drahých kamenů je způsobena nečistotami způsobenými ionty příměsí, například u rubínů, safírů, smaragdů, nefritů a achátů. Na základě příčin barvy drahých kamenů lze při zušlechťování měnit obsah a valenční stav určitých příměsových iontů způsobujících barvu, aby se změnila nebo zlepšila barva drahého kamene, a tím se zvýšila kvalita zušlechtěného drahého kamene. Studium příčin barvy drahých kamenů je proto teoretickým základem pro zlepšování drahých kamenů.
2. Fyzika barev
(1) Barevné a světelné vlny
Fotony nesou energii světla, a když se dostanou k lidskému oku, vytvářejí vjem barvy. Barva je vnímání světla očima a nervovým systémem; reakce vyvolaná signály vytvořenými na sítnici oka stimuluje mozkovou kůru. Vznik barevného vjemu má tři hlavní složky: zdroj světla, objekt a lidské oko. Změna jedné nebo více z těchto tří složek změní vnímání barev. Drahé kameny interagují se světlem a jevy, jako je odraz, lom, transmise, interference a difrakce, ke kterým dochází na povrchu drahého kamene, mají za následek různé barvy.
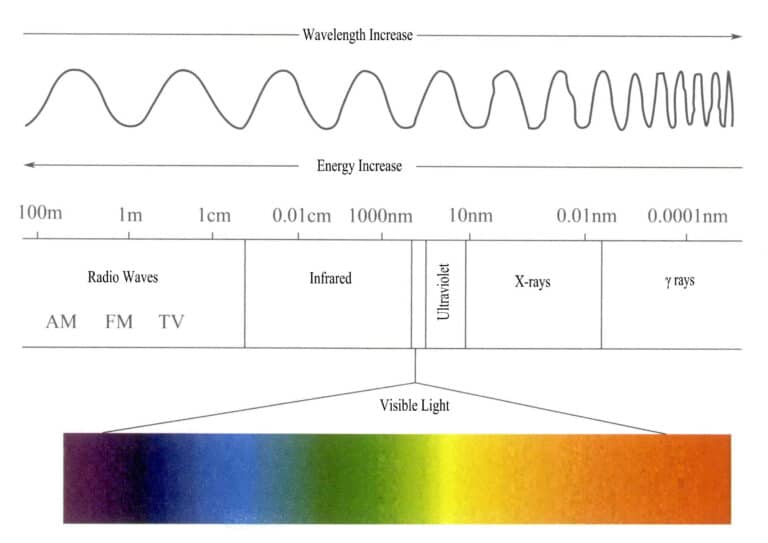
Energetický rozsah spektra elektromagnetického záření je poměrně velký, od velmi dlouhých fotonů rádiových vln po velmi krátké fotony paprsků, s rozsahem energie od méně než jedné miliardtiny elektronvoltu po více než sto milionů elektronvoltů.
Viditelné světlo, které je lidské oko schopno přijímat a vnímat, je velmi malou částí elektromagnetického spektra s vlnovou délkou 400-700 nm a energií přibližně 1,7-3,1 eV. Při dostatečně dobrých pozorovacích podmínkách lze tento rozsah rozšířit na 380-760 nm (obrázek 3-1). Viditelné světlo zahrnuje barvy, které vidíme, a to červenou, oranžovou, žlutou, zelenou, azurovou, modrou, fialovou a různé další barvy. Různé vlnové délky viditelného světla vytvářejí různé barvy; barva viditelného světla s nejdelší vlnovou délkou a nejnižší energií je červená, s rozsahem vlnových délek 647-760 nm; viditelné světlo s nejkratší vlnovou délkou a nejvyšší energií je fialové, s rozsahem vlnových délek 400-425 nm. Ostatní barvy viditelného světla se pohybují v rozmezí 425-647 nm. Vlnové délky různých barev viditelného světla a jejich doplňkové barvy jsou uvedeny v tabulce 3-1.
Tabulka 3-1 Vlnové délky různých barev viditelného světla a jejich doplňkové barvy
| Vlnová délka/nm | Spektrální barva | Doplňkový |
|---|---|---|
| 400 ~ 425 | Fialová | Žlutozelená |
| 425 ~ 455 | Modrá | Žlutý |
| 455 ~ 490 | Zelenomodrá | Orange |
| 490 ~ 500 | Modrozelená | Červená |
| 500 ~ 560 | Zelená | Magenta |
| 560 ~ 580 | Žlutozelená | Fialová |
| 580 ~ 595 | Žlutý | Modrá |
| 595 ~ 647 | Orange | Zelenomodrá (azurová) |
| 647 ~ 760 | Červená | Zelená |
Podstata barvy objektu je výsledkem selektivní absorpce různých vlnových délek viditelného světla. Podstatou selektivní absorpce různých vlnových délek viditelného světla objektem je absorpce fotonů viditelného světla s různými energiemi. Když na drahokam svítí přirozené světlo, drahokam část světla pohlcuje a část světla také propouští. Barva prezentovaná drahým kamenem je komplementární barvou absorbovaného světla, která odpovídá barvě procházejícího světla (obrázek 3-2). Například v případě rubínu, když jím prochází bílé světlo, získávají ionty chromu obsažené v rubínu energii tím, že pohlcují všechny fialové a zelené fotony a většinu modrých fotonů, zatímco ostatní barevné fotony, převážně červené, rubínem procházejí, což způsobuje, že se drahokam jeví jako červený.
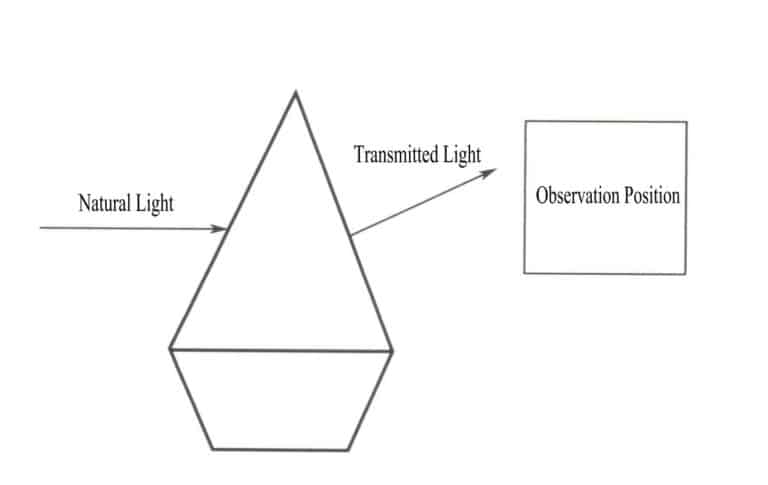
Barvu objektu nevytváří jediná vlnová délka světla; záření objektu je spíše směsí fotonů s různou energií, přičemž barvu objektu určuje pásmo energie s největším podílem. Rovnoměrná směs různých barev světla tvoří bílé světlo. Vznik barev drahých kamenů je výsledkem selektivní absorpce fotonů různých vlnových délek viditelného světla. Když bílé světlo prochází drahým kamenem, světlo pohlcené a prošlé drahým kamenem je směs a barva prezentovaná drahým kamenem závisí na té s největším podílem prošlého světla. Například v případě rubínu, když na něj svítí bílé světlo, je světlo, které jím prochází, převážně červené s malým podílem modrofialové. Rubíny se tedy často jeví jako červené s modrofialovým nádechem.
(2) Typy a vlastnosti zdrojů světla
Barva drahých kamenů má určitou subjektivitu, která souvisí s prostředím pozorovatele a je nejvíce ovlivněna zdrojem světla. Pozorování barvy drahých kamenů pod různými zdroji světla může ukázat rozdíly; například alexandrit se ve slunečním světle jeví jako zelený, ale pod žárovkovým světlem jako červený. Obecně lidé považují za standard barvu viditelnou v přirozeném slunečním světle, běžně označovanou jako bílé světlo.
Počáteční operace na trhu s drahými kameny byly prováděny ve specifických časech, aby bylo možné získat relativně přesnou barvu drahých kamenů. Například obchody s drahými kameny v Ratnapuře na Srí Lance fungovaly po mnoho let od 10 do 12 hodin, protože zdroj světla je v tuto dobu nejblíže bílému světlu. Sluneční a denní světlo nejsou izotropní zdroje světla a relativní rozdíly v množství záření různých vlnových délek mezi různými zdroji světla mohou být vzhledem k různým pozorovacím podmínkám velmi velké. Na obrázku 3-3 jsou uvedeny křivky rozložení energie pěti běžných zdrojů světla a rozdíly v energii mezi těmito zdroji světla jsou velmi velké.
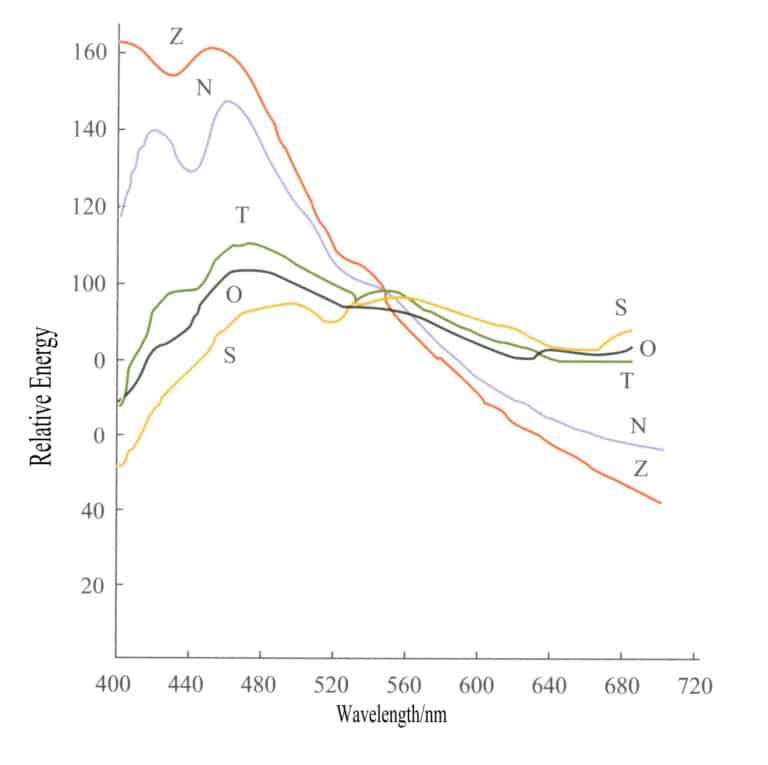
S - Přímé sluneční světlo; O - Osvětlení světlem zatažené oblohy v horizontální rovině; T - Osvětlení slunečním světlem a jasnou oblohou v horizontální rovině; N - Světlo z jasné severní oblohy; Z - Zenitové světlo;
Barevné vlastnosti přímého slunečního světla se často vyjadřují pomocí barevné teploty (měřené v K). Stejná barevná teplota označuje podobné barvy světelných zdrojů. V současné době jsou uznávány tyto teploty barev denního světla: D6500K, D5500K a D7500K. Jako standardní světelné zdroje pro práci s měřením barev jsou mezinárodně označeny tři lampy. SA představuje průměrné umělé osvětlení wolframové žárovky s barevnou teplotou 2854 K;S.B představuje průměrné sluneční světlo s barevnou teplotou 4900 K; SC představuje průměrné denní světlo s barevnou teplotou 6700 K. Při testování drahokamů se jako standardní zdroj světla používá světelný zdroj Sc.
(3) Citlivost na světelné a barevné efekty
Pozorování barev drahokamů je subjektivní; kromě objektivních podmínek souvisí barva drahokamu také se smyslovým vnímáním pozorovatele. Lidské oči jsou pod stejným zdrojem světla různě citlivé na různé barvy a různí lidé mají různou citlivost na barvy. Pozorování barev je subjektivní; aby bylo dosaženo co největší objektivity, je třeba barvy charakterizovat a vyjádřit relativně objektivně.
① Fotorecepční efekt:
Za normálních podmínek je vlnová délka zdrojů viditelného světla, které může lidské oko pozorovat, 400-700 nm. Rozsah citlivosti lze rozšířit zlepšením pozorovacích podmínek na 380-780 nm. Lidské oko má různou citlivost na světelné vlny různých vlnových délek. Pro denní vidění je oko nejcitlivější na zelené světlo o vlnové délce 555 nm, zatímco nejcitlivější vlnová délka pro soumrakové vidění se posouvá na 507 nm. Semafory na silnicích jsou navrženy na základě barev, na které je lidské oko nejcitlivější.
② Color Sensation:
Barva je vjem způsobený různými spektrálními složkami energie záření v oblasti viditelného světla. Normální zrak člověka dokáže rozlišit více než 150 odstínů čistých spektrálních barev. Ačkoli mezi světelnými vlnami a barvami existuje shoda jedna ku jedné, shoda mezi barvami a světelnými vlnami není jednoznačná; často může být jedna barva světla vytvořena kombinací dvou nebo více jiných barev světla. Tři základní nezávislé barvy jsou červená, zelená a modrá, známé jako základní barvy. Další barvy vznikají smícháním dvou nebo více základních barev v různých poměrech a lidské oko je na barvy velmi citlivé a dokáže rozlišit mnoho různých barev.
3. Tři prvky reprezentující barvu
Barva je výsledkem selektivní absorpce světla drahými kameny a různé drahé kameny vykazují různé barvy. Podle současné teorie barev závisí barevné vlastnosti na jasu, odstínu a sytosti (obrázek 3-4). Typy barev drahých kamenů lze určit na základě popisu tří prvků různých barev.

(1) Jas
Jas je stupeň jasu způsobený světlem působícím na lidské oko, který se vztahuje ke stupni světlých a tmavých barev, a může být také nazýván jasem. Jas do značné míry závisí na tom, jak oko vnímá světlé a tmavé úrovně světelného zdroje a povrchu předmětu, které jsou určeny především intenzitou světla. Jas závisí na úrovni osvětlení objektu a odrazivosti povrchu objektu.
Jas lze chápat jako jas barvy; různé barvy mají různé úrovně jasu a každá barva vykazuje rozdíly ve světlosti a tmavosti. Jas má dvě vlastnosti: stejný objekt může vykazovat změny jasu v důsledku různého osvětlení a různá barevná světla stejné intenzity mohou mít také různé úrovně jasu.
Při absenci barvy je barva s nejvyšším jasem bílá a barva s nejnižším jasem je černá, se stupnicí šedi mezi světlou a tmavou. V barvě má jakýkoli stupeň čistoty své jasové charakteristiky. Například žlutá má nejvyšší jas, zatímco fialová nejnižší. Zelená, červená, modrá a oranžová mají podobnou úroveň jasu, což představuje střední jas. Navíc v rámci stejného odstínu existují rozdíly v jasu od světlého po tmavý, například světle zelená, bledě zelená a smaragdově zelená v zeleném spektru.
(2) Hue
Odstín označuje rozdíly mezi různými barvami a je nejvýraznější charakteristikou barvy. Odstín je určen spektrálními složkami světla, které procházejí objektem a po dopadu na něj se dostanou do lidského oka v závislosti na vlnové délce procházejícího světla. Odstín předmětu je určen spektrem dopadajícího světelného zdroje a světlem odraženým nebo prošlým samotným předmětem.
Tzv. odstín označuje název, který může přesněji reprezentovat určitou kategorii barev, jako je růžově červená, oranžově žlutá, citronově žlutá, kobaltově modrá, fialově červená, smaragdově zelená atd. Z hlediska fyzikální optiky jsou různé odstíny určeny spektrálními složkami světla, které vstupuje do lidského oka. U monochromatického světla závisí typy odstínů zcela na vlnové délce tohoto světla; u smíšeného barevného světla závisí na relativním množství různých vlnových délek světla. Barva objektu je určena spektrálními složkami zdroje světla a vlastnostmi světla odraženého (nebo prošlého) povrchem objektu. Souvisí s vlnovou délkou světla. Například barva s dominantní vlnovou délkou 470 nm se nazývá modrá o vlnové délce 470 nm, běžně se vyskytuje jako modrá barva safírů.
(3) Nasycení
Sytost barvy označuje čistotu a živost barvy a udává podíl chromatických složek obsažených v barvě. Čím větší je podíl chromatických složek, tím vyšší je čistota barvy; čím menší je podíl chromatických složek, tím nižší je čistota barvy. Sytost se mění při smíchání barvy s černou, bílou nebo jinými barvami. Když podíl smíšené barvy dosáhne významné úrovně, původní barva ztratí pro oko svůj původní lesk a viděná barva se stane barvou smíšené barvy. To samozřejmě neznamená, že původní barva již neexistuje, ale spíše to, že původní barva byla asimilována díky mnoha dalším přimíchaným barvám, takže je pro lidské oko nepostřehnutelná.
Monochromatická světla ve viditelném spektru mají nejvyšší sytost a jsou nejživější. Monochromatické světlo se obvykle považuje za 100/100 = 1 a s ubývající barvou se hodnota postupně snižuje, přičemž čistě bílá má nulovou sytost. Vezmeme-li jako příklad čistě modrý inkoust, sytost čistě modrého inkoustu je 1, a jak se postupně ředí až na zcela bezbarvý, sytost se stává nulovou.
4. Měření barvy drahých kamenů
Systém, který kvantitativně reprezentuje barvu, se nazývá barevný systém. Existují dva běžně používané typy barevných systémů: jeden je barevný systém založený na standardních barevných vzorcích pro porovnání a druhý je soubor barevných standardních systémů měřených pomocí moderních přístrojů pro měření barev.
(1) Systém barev standardních barevných vzorků
Tento systém barev se skládá z různých "barevných karet" z papíru, které jsou standardními vzorky barev sestavenými do knihy. Ty se porovnávají se vzorky drahých kamenů a vybírá se "barevná karta", která odpovídá barvě drahého kamene.
① Munsellův systém barev
Munsellův systém barev je jedním z prvních a nejklasičtějších systémů znázornění barev. Některé organizace jej používají dodnes. Byl vytvořen v roce 1905 americkým pedagogem a teoretikem barev Albertem Munsellem a byl pojmenován přímo po něm. Jedná se o způsob reprezentace barev prostřednictvím barevně-solidárního modelu. "Munsellův atlas barev", který vydává Optická společnost Ameriky (OSA), obsahuje lesklou a matnou verzi.
Lesklá verze obsahuje 1 450 barevných vzorků a sadu 37 achromatických vzorků; matná verze obsahuje 1 150 barevných vzorků a 32 achromatických vzorků.
V Munsellově atlasu je každá barva reprezentována sadou symbolů. Symboly poskytují rovnocenné ukazatele pro tři prvky reprezentace barev: odstín, hodnotu a chromatičnost, reprezentované jako HV/C = hodnota odstínu/chroma.
Odstíny se dělí na pět základních tónů: červený (R), žlutočervený (YR), žlutý (Y), zelenožlutý (GY), zelený (G), modrozelený (BG), modrý (B), fialovomodrý (PB), fialový (P) a červenofialový (RP) a pět mezitónů. Každý tón je dále rozdělen do deseti úrovní (1 až 10), přičemž pátá úroveň představuje mezibarvu daného tónu (obrázek 3-5).
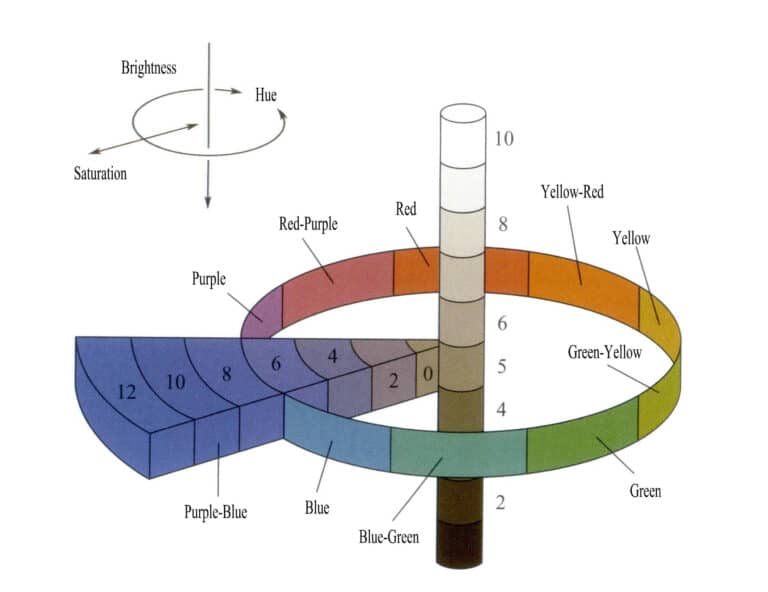
Hodnota je rozdělena do 11 úrovní, přičemž vyšší hodnoty znamenají vyšší světlost; minimální hodnota je 0 (černá) a maximální 10 (bílá). Chroma je rozdělena do 12 úrovní. Celý atlas barev obsahuje 40 typů vzorků odstínů. Například 5GY 8/7 představuje žlutozelenou barvu s hodnotou 8 a sytostí 7. Pojmenovací konvence pro nebarevné řady (černá, bílá, šedá) je NV/= neutrální hodnota světlosti; například barva označená N5/ označuje šedou barvu s hodnotou světlosti 5.
② Barevný systém DIN 6164
Důležitým barevným systémem je také německá příručka DIN 6164. Tento systém používá mnoho gemologů v Evropě a ve Velké Británii. Tento barevný systém byl vyvinut na základě systému Munsell.
Barevná karta DIN 6164 má 24 barev, přičemž zadní strana každé barvy je označena odpovídajícím Munsellovým barevným označením. Zobrazení je ve formátu odstín: sytost: světlost. Například 6:6:2 představuje odstín 6 (červená), sytost 6 (živá) a světlost 2 (světlá) standardní barevné karty.
③ Systém barev ISCC-NBS
ISCC (Inter-Society Colour Council) byla založena v roce 1931 jako domácí asociace barev ve Spojených státech a její systém barev se zaměřuje na vývoj systému pojmenování barev. Shromažďuje 18 odstínů na stejných pozicích odstínu a světlosti podle norem Munsell a DIN 6164.
ISCC-NBS (National Bureau of Standards) má v systému amerických národních norem velmi málo vzorků barev, ale shromáždil některé neobvyklé vzorky. Strukturálně se také liší od systému Munsell, protože barvy nejsou uspořádány podle percepčních ekvidistantních metrik. Nejdůležitějším přínosem systému ISCC-NBS pro vědu o barvách je, že definuje názvy barev.
④ Barevný standard OSA
OSA (Optical Society of America) připravila praktickou sadu akrylových lesklých barevných karet, která obsahuje 558 barev, z nichž 424 barev tvoří sadu známou jako barevný standard OSA. Nevýhodou barevného standardu OSA je, že barevné karty jsou vyrobeny z papíru nebo plastu, který se liší strukturou od drahých kamenů, a povrchový lesk barevných karet se liší od světla odraženého fasetovanými drahými kameny, což vyžaduje opatrné používání. Vzhledem k blednutí má většina barevných karet dobu používání 4 až 5 let.
(2) Chromatické souřadnice a chromatický diagram
① 1931 Systém barevného prostoru CIE-XYZ
Tento systém barevného prostoru je založen na systému RGB a používá matematické metody pro výběr tří ideálních základních barev, které nahrazují skutečné základní barvy. Pomocí virtuálních základních barev jako os promítá různé vlnové délky viditelného světla. Hodnoty základních barev se nazývají tristimulové hodnoty. Tento systém vyžaduje, aby tristimulové hodnoty nebyly záporné a aby se y rovnalo světelnému toku. Pomocí x jako vodorovné osy a y jako svislé osy vytváří chromatické souřadnice, promítá hodnoty chromatických souřadnic každého monochromatického světla a získává chromatický diagram. Na obrázku 3-6 je standardní chromatický diagram systému (XYZ) zavedený na mezinárodní úrovni v roce 1931.
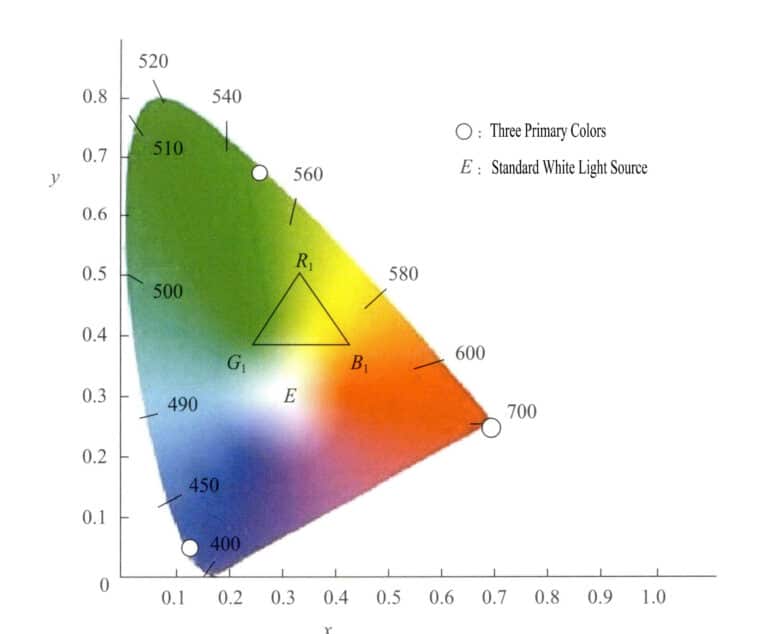
Chromatický diagram má následující charakteristiky:
- Tristimulové hodnoty základních barev tohoto systému jsou virtuální.
- Všechny body reprezentující spektrální barvy spadají na jazykovitou křivku zvanou spektrální barva. Spojíme-li konce křivky přímkami, jsou všechny skutečné barvy obsaženy v oblasti ohraničené jazykovitou křivkou a přímkami.
- Hodnota souřadnice bodu E v bodě x=0,333, y=0,333 představuje teoretickou bílou barvu. Různé zdroje bílého světla mají mírně odlišné spektrální složky. Běžně používané bílé světlo se dělí na SA, SB, SC, SEa tak dále.
- Chromatické souřadnice barev mají tím větší sytost, čím blíže jsou ke spektrální barevné trajektorii. Body na spektrální barevné trajektorii mají nejvyšší sytost; bílý bod má sytost nejnižší. Přímka vedená od bílého bodu k chromatickým souřadnicím barvy, prodloužená tak, aby protínala spektrální barevnou trajektorii, má podél této přímky body, které mají stejný odstín.
- Grafickou metodou lze odvodit složenou barvu libovolných dvou barev. Po zadání chromatických souřadnic obou barev do chromatického diagramu musí složená barva ležet na přímce spojující oba body barevných souřadnic. Vzdálenost promítnutá do obou barevných bodů souvisí s intenzitou obou barev, která je určena zákonem rozdělení centroidů.
- Body na přímce mezi koncovými body spektrální barevné křivky nepředstavují spektrální barvy, ale různé smíšené barvy získané smícháním fialové při 380 nm a červené při 780 nm v různých poměrech.
- Výběrem libovolných tří bodů v rámci trajektorie barevného spektra vytvoříte barvu. Pokud například vyberete R1, G1, B1 jako tři barvy pro porovnání, pak všechny různé barvy tvořené těmito třemi odstíny jsou obsaženy v trojúhelníku s vrcholy ve třech bodech R1, G1, B1.
② Zastoupení dominantní vlnové délky a nasycení
V chromatickém diagramu lze barvy znázornit nejen pomocí chromatických souřadnic (x, y). Další Helmholtzem navrženou metodou je jejich znázornění pomocí dominantní vlnové délky λd a nasycení (čistota podnětu) Pe. λd a Pe jsou konkrétní hodnoty odvozené z chromatických souřadnic v diagramu (obrázek 3-7). Dominantní vlnová délka zhruba představuje barevný vjem vnímaný lidským okem.
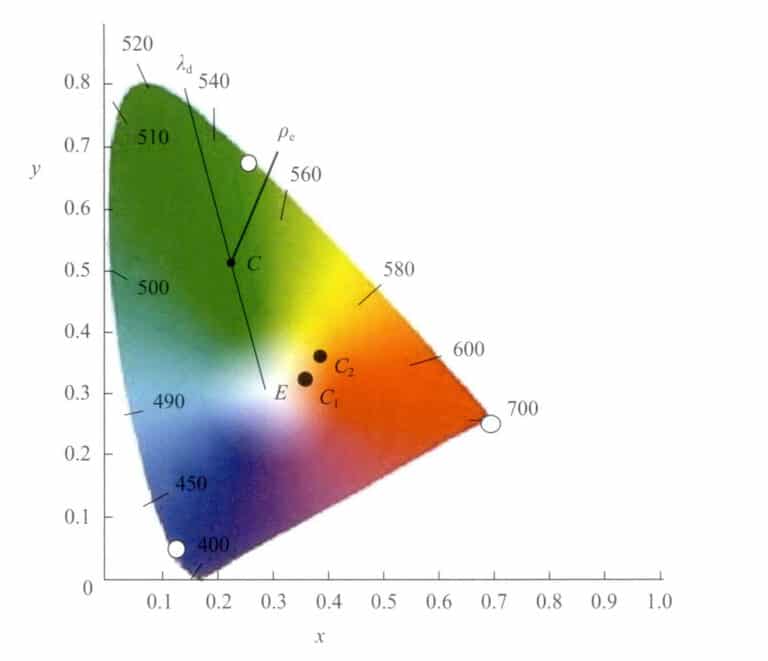
Poloha tohoto bodu v chromatickém diagramu nechť je c(x, y). Bod c spojíme s bílým E a prodloužíme jej tak, aby protínal trajektorii spektra v bodě λd . Pak číslo vlnové délky bodu λd na trajektorii spektra je dominantní vlnová délka tohoto barevného světla.
Bod C leží na přímce spojující body W a λd , což představuje sytost této barvy. Bod W představuje čistě bílou barvu (E) nebo specifický zdroj bílého světla. Když se chromatické souřadnice určité barvy postupně pohybují směrem ke spektrální trajektorii od bílého bodu W, sytost barvy se postupně zvyšuje, dokud nedosáhne spektrální trajektorie, přičemž maximální sytost je 1.
Barvy jsou reprezentovány pomocí dominantní vlnové délky a sytosti, což usnadňuje porovnávání barevných rozdílů. Mírné barevné rozdíly, reprezentované číselnými změnami v λd a ρe, lze zobrazit.
Pro dvě barvy C1, C2, chromatické souřadnice, dominantní vlnová délka a sytost při stejném osvětlení jsou uvedeny v tabulce 3-2. Je vidět, že dominantní vlnová délka barvy C1, C2 se liší o 0,052 nm a nasycení se liší o 7%.
Tabulka 3-2 Srovnání barevných dat mezi C1 a C2
| Barevný projekční bod | X | y | λd | ρe |
|---|---|---|---|---|
| C1 | 0.368 | 0.416 | 0.592 | 0.35 |
| C2 | 0.392 | 0.355 | 0.540 | 0.28 |
5. Přístroje pro měření barvy drahých kamenů
(1) Spektrofotometr
Princip činnosti: Protože je známo spektrální rozložení energie standardního zdroje světla uvnitř přístroje, lze hodnoty tristimulu objektu získat měřením jeho spektrální odrazivosti.
(2) Kolorimetr s tristimulovou hodnotou
Jedná se o fotoelektrický integrační přístroj, který přímo měří tři podnětové hodnoty barvy objektu. Simuluje především tři reakce standardního pozorovatele na barvu prostřednictvím vhodné kombinace filtrů a fotoelektrických převodníků.
V současné době se posuzování barvy drahých kamenů opírá především o pozorování lidským okem. Například smaragdy, rubíny a diamanty jsou ovlivněny faktory prostředí, což vede k nízké přesnosti přístrojových měření; proto je použití přístrojového měření barvy při identifikaci drahých kamenů poměrně vzácné.
Oddíl II Teoretický původ barvy drahých kamenů
Minerály drahých kamenů mají různé barvy, ale liší se i důvody jejich zbarvení. Podle klasické mineralogické teorie lze původ barvy minerálů drahých kamenů rozdělit na idiochromatickou barvu, alochromatickou barvu a pseudobarvu.
1. Klasifikace klasické mineralogie Teorie původu barev
Klasická mineralogická teorie je nejzákladnější teorií pro studium barev drahých minerálů. Podle toho, zda je barva minerálu způsobena samotným minerálem, ji lze rozdělit do tří kategorií: idiochromaticky zbarvená, alochromaticky zbarvená a pseudobarvená.
(1) Idiochromaticky zbarvené
Barva drahokamu je tvořena chemickými složkami minerálu, ze kterého se skládá, tzv. idiochromatickou barvou. Takové drahokamy se nazývají idiochromaticky zbarvené drahokamy. Barvu, kterou idiochromaticky zbarvené drahokamy vytvářejí, způsobují jejich inherentní složky; mají tedy dobrou barevnou stálost a nejsou snadno měnitelné. Například chemické složení tyrkysu jeCuAl6(PO4)4(OH)8-5H2O a modrá nebo modrozelená barva je způsobena Cu2+; chemické složení azuritu je 2CuCO3 - Cu(OH)2a Cu2+ také způsobuje jeho modrou barvu"; zelená barva olivínu je způsobena ionty železa v jeho chemickém složení (obrázek 3-8).

V přírodních drahých minerálech není mnoho typů samobarvících drahokamů, hlavními druhy jsou tyrkys, malachit, azurit, olivín, granát a rodochrozit. Běžné barvy, barvicí prvky a chemické složení samobarvících drahokamů jsou uvedeny v tabulce 3-3.
Tabulka 3-3 Běžné barevné prvky, chemické složení a barvy barevných drahokamů
| Barevné prvky | Název drahého kamene | Chemické složení | Barva |
|---|---|---|---|
| Iron | Olivine | (Mg, Fe)2 (SiO4) | Zelená |
| Almandine | Fe3Al2 (SiO4)3 | Červená | |
| Chrom | Uvarovit | Ca3Cr2 (SiO4)3 | Zelená |
| Cuprum | Malachit | Cu2Co3(OH)2 | Zelená |
| Chryzokol | (CuAl)2H2Si2O5(OH)4 - nH2O | Zelená - modrá | |
| Tyrkysová | CUAl6(PO4)4(OH)8.5H2O | Nebesky modrá - Zelená | |
| Azurit | 2CuCO3 - Cu(OH)2 | Modrá | |
| Mangan | Spessartine-Garnet | Mn3Al2(SiO4)3 | Orange |
| Rodochrozit | MnCO3 | Růžová - červená | |
| Rodonit | (Mn, Ca, Fe) - 5(Si5O15) | Růžová - červená |
Kopírování @ Sobling.Jewelry - Výrobce šperků na zakázku, továrna na šperky OEM a ODM
Některé barevné drahé kameny mohou za určitých podmínek měnit barvu. Například tyrkys a malachit mohou měnit barvu při vystavení vysokým teplotám v důsledku odpařování molekul vody v jejich složení; rodochrozit, karbonátový drahokam, se může rozkládat, když se setká s kyselinami (například kyselinou chlorovodíkovou nebo sírovou), a jeho barva se podle toho také změní.
(2) Alochromatický-barvaed
Barva drahého kamene je způsobena stopovými nebo drobnými příměsovými prvky mimo vlastní chemické složení minerálů, tzv. alochromatickou barvou. Takové drahé kameny se označují jako alochromaticky zbarvené drahé kameny.
Mezi drahými kameny existuje mnoho odrůd drahých kamenů s různými barvami. Pokud v chemickém složení drahého kamene nejsou žádné příměsi, je bezbarvý a průhledný; pokud obsahuje příměsi různých barvicích prvků, může vytvářet různé barvy.
Pokud je čistý korund bezbarvý, stává se rubínem, pokud obsahuje malé množství chromových iontů; pokud obsahuje malé množství železa a titanu, mění se v modré nebo zelené drahokamy. Mezi podobné drahé kameny patří smaragd, spinel, turmalín, jadeit, chalcedon, nefrit atd. Běžné barevné prvky, chemické složení a alochromaticky zbarvené drahé kameny jsou uvedeny v tabulce 3-4.
Tabulka 3-4 Běžné barevné prvky, chemické složení a alochromaticky zbarvené drahé kameny
| Barevné prvky | Název drahého kamene | Chemické složení | Barva |
|---|---|---|---|
| Chrom | Ruby | Al2O3 | Červená |
| Emerald | Buďte na .3Al2(Si6O18) | Zelená | |
| Alexandrit | BeAl2O4 | Červeno-zelená | |
| Spinel | MgAl2O4 | Červená | |
| Chalcedon | SiO2 | Zelená | |
| Iron | Akvamarín | Buďte na .3Al2Si6O18 | Modrá |
| Turmalín | (Na, K, Ca) (Al, Fe3+, Cr)6(BO3)3Si6O18(OH)4 | Zeleno-hnědá | |
| Spinel | MgAl2O4 | Žlutý | |
| Nefrit | Ca2(Mg, Fe2+) 5 (Si4O11) 2 (OH)2 | Zelená | |
| Vanad | Tanzanit | Ca2Al3(SiO4)3(OH) | Fialovomodrá |
| Zelený beryl | Buďte na .3Al2Si6O18 | Zelená | |
| Titan | Benitoit | BaTiSi3O9 | Modrá |
| Sapphire | Al2O3 | Modrá | |
| Mangan | Červený beryl | Buďte na .3Al2Si6O18 | Červená |
| Rodochrozit | MnCO3 | Růžová | |
| Kobalt | Přírodní spinel | MgAl2O4 | Modrá |
| Syntetický spinel | MgAl2O4 | Modrá | |
| Nikl | Zelený chalcedon | SiO2 | Zelená |
(3) Pseudo-barvaed
Barvy, které pseudobarvy vytvářejí, nesouvisejí s chemickým složením minerálů drahých kamenů. Přesto jsou způsobeny strukturními a kompozičními změnami, které jsou důsledkem mechanických směsí nebo vzniku minerálů. Pseudobarvy nejsou barvy samotných minerálů, ale spíše barvy způsobené zvláštními strukturami vzniklými vnějšími vlivy. Například krásné interferenční barvy vznikající interferencí odraženého a dopadajícího světla, jako je fluorescenční efekt labradoritu a efekt hry barev opálu. Zbarvení způsobené inkluzemi také spadá do pseudobarvení, například černé diamanty, způsobené mnoha černými neprůhlednými grafitovými inkluzemi uvnitř diamantu.
2. Barevné ionty v drahých minerálech
Chemické prvky, které vytvářejí barvy drahokamů, mohou být hlavními nebo vedlejšími složkami. Prvky přechodných kovů, zejména přechodné kovy čtvrté periody titan, vanad, chrom, mangan, železo, kobalt, nikl a měď, se často označují jako chromofory nebo barvicí ionty. Těchto osm prvků zaujímá v periodické tabulce po sobě jdoucí pozice s atomovými čísly od 22(Ti) do 29(Cu). Základní vlastnosti těchto prvků jsou uvedeny v tabulce 3-5.
Tabulka 3-5 Základní vlastnosti osmi přechodových prvků
| Název prvku | Titan | Vanad | Chrom | Mangan | Iron | Kobalt | Nikl | Měď |
|---|---|---|---|---|---|---|---|---|
| Symbol prvku | Ti | V | Cr | Mn | Fe | Co | Ni | Cu |
| Atomové číslo | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 |
| Hlavní oxidační stavy | +2, +3, +4 | +2, +3, +4, +5 | +2, +3, +6 | +2, +3, +4, +6 | +2, +3, +6 | +2, +3 | +2, +3 | +1, +2 |
| Valenční elektronová konfigurace | 3d24s2 | 3d34s2 | 3d54s1 | 3d54s2 | 3d64s2 | 3d74s2 | 3d84s2 | 3d104s1 |
Těchto osm přechodných kovových prvků má následující vlastnosti:
① Valenční elektrony jsou obsazeny v d orbitalech předposlední slupky v pořadí a obecný vzorec pro valenční elektronovou konfiguraci atomů přechodných prvků je (n-1)d1-10nS1-2, proto se tyto prvky nazývají také d blokové prvky.
② U přechodných kovů, protože d orbitaly předposlední slupky jsou spojeny s vnějšími s orbitaly a d orbitaly ještě nedosáhly stabilní struktury, se mohou s elektrony i d elektrony podílet na vazbě částečně nebo zcela, což vede k řadě proměnlivých oxidačních stavů přechodných kovů, přičemž různé oxidy mají v drahých kamenech různé barvy.
③ Ionty se obecně vyznačují barvou, protože v d orbitalech jsou nespárované jednoduché elektrony a energetické hladiny těchto elektronů v excitovaném a základním stavu jsou relativně blízko, což umožňuje excitaci viditelnou světelnou energií. Různé excitační podmínky mohou také způsobit, že drahé kameny vykazují různé barvy.
Pokud jsou všechny spinové elektrony v iontu spárovány, například ionty s valenční elektronovou konfigurací d0, d10, d10s2, elektrony jsou ve stabilním stavu a nejsou snadno excitovány, což vede k tomu, že iont nemá barvu; C+, Cr6+ a další nemají barvu a nemohou vytvářet barvu v drahých kamenech.
Těchto osm přechodných kovových prvků tvoří barevné složení běžných přírodních barevných drahých kamenů. Různé chromofory vytvářejí v různých drahých kamenech různé barvy a stejný chromofor může také vytvářet různé barvy. Běžné přírodní drahé kameny a chromofory jsou uvedeny v tabulce 3-6.
Tabulka 3-6 Barvy podle iontů přechodných kovů v běžných přírodních drahokamech a odrůdách drahokamů
| Chromofor | Běžné barvy | Odrůdy drahokamů |
|---|---|---|
| Iont titanu (Ti) | Modrá | Safír, benitoit, topaz |
| Ion vanadu (V) | Zelená | Syntetická změna barvy korundu, essonitu, smaragdu |
| Ionty chromu (Cr) | Červená, zelená | Rubín, korund, smaragd, pyrop, nefrit |
| Iont manganu (Mn) | Růžová, červená | Spessartin, rodolit, červený beryl |
| Ionty železa (Fe) | Modrá, zelená, žlutá | Safír, olivín, akvamarín, turmalín, spinel |
| Iont kobaltu (Co) | Modrá | Syntetický spinel, staurolit kobaltové barvy |
| Ionty niklu (Ni) | Zelená | Zelený chalcedon |
| Ionty mědi (Cu) | Modrá, modrozelená | Malachit, tyrkys, azurit |
Různé ionty chromoforů vytvářejí v drahých kamenech různé barvy, což vede k absorpčním spektrům s odlišnými vlastnostmi. Pro běžné chromoforové ionty mají absorpční spektra typický identifikační význam.
(1) Absorpční spektrum chromových iontů
Absorpční spektrum chromových iontů se vyznačuje především mnoha úzkými absorpčními čarami v červené oblasti, přičemž dvě nejsilnější se nacházejí v tmavě červené oblasti a další dvě v oranžové oblasti. Žlutozelená oblast má široký absorpční pás a její šířka, poloha a intenzita souvisí s hloubkou barvy drahokamu. V modré oblasti může být několik úzkých pásů, zatímco fialová oblast je plně absorbovaná. Chromové ionty vytvářejí především červenou a zelenou barvu, které se u různých drahokamů liší, a absorpční spektra vykazují určité rozdíly. Například rubíny mají tři absorpční čáry v červené oblasti, široký absorpční pás ve žlutozelené oblasti, tři absorpční čáry v modré oblasti a plnou absorpci ve fialové oblasti; smaragdy mají absorpční čáry v červené oblasti, slabý absorpční pás v oranžovožluté oblasti, slabé absorpční čáry v modré oblasti a plnou absorpci ve fialové oblasti; alexandrit má absorpční čáry v červené oblasti, absorpční pás ve žlutozelené oblasti, jednu absorpční čáru v modré oblasti a plnou absorpci ve fialové oblasti. Absorpční spektra těchto tří drahokamů jsou znázorněna na obrázku 3-9.

(2) Charakteristiky absorpčního spektra iontů železa
Ionty železa vytvářejí v různých drahokamech různé barvy a mají silný barvicí účinek, ale absorpční spektrum iontů železa se značně liší. Když je drahokam zelený, vytváří absorpci v červené zóně, a když je červený, vytváří absorpční rys, kterému dominuje modrá zóna, přičemž hlavní charakteristická absorpční linie se nachází v zelené a modré zóně. Například ionty železa v olivínu se jeví jako olivově zelené, přičemž absorpční spektrum vykazuje hlavně tři úzké absorpční pásy v modré oblasti při 453 nm, 473 nm a 493 nm; červený almandin má typické absorpční spektrum železa se třemi silnými úzkými absorpčními pásy při 504 nm, 520 nm a 573 nm ve žlutozelené oblasti, v průmyslu běžně označované jako "železné okno". Kromě toho existují slabé úzké absorpční pásy při 423nm, 460nm, 610nm a 680~690nm; absorpční spektrum žlutého safíru má tři úzké absorpční pásy v modré oblasti při 450nm, 460nm, 470nm (obr. 3-10).
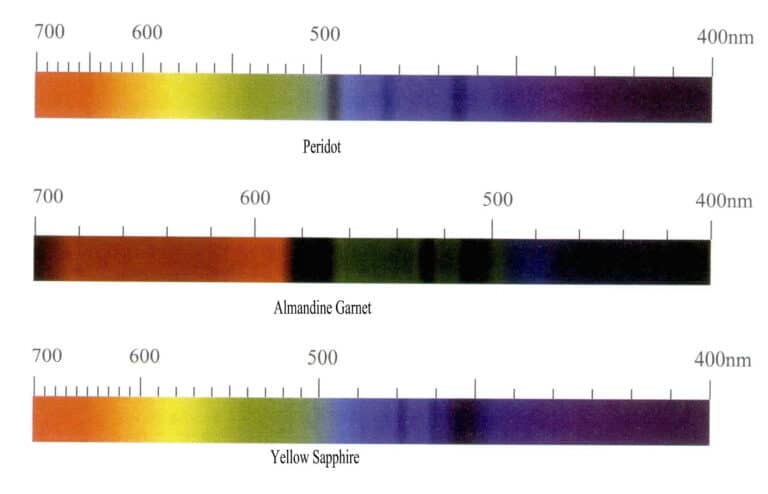
(3) Absorpční spektrální charakteristiky iontů manganu
Ionty manganu tvoří v drahých kamenech především růžovou, oranžovou a červenou barvu, přičemž absorpční spektrum vykazuje především silnou absorpci ve fialové oblasti, která zasahuje do ultrafialové oblasti, a určitou absorpci v modré oblasti. Například charakteristiky absorpčního spektra růžového rodochrozitu mají tři absorpční pásy při 410nm, 450nm, 540nm; linie absorpčního spektra spessartinu mají především 410nm, 420nm, 430nm tři absorpční pásy a absorpční linie při 460nm, 480nm a 520nm. Někdy se mohou vyskytovat dvě absorpční čáry 504nm, 573nm (obrázek 3-11).

(4) Absorpční spektrum kobaltových iontů
Ionty kobaltu mají silný barvicí účinek, v drahých kamenech se obvykle objevují v jasně modré barvě, přičemž absorpční spektrum vykazuje především tři silné a široké absorpční pásy ve žlutozelené oblasti. Vzhledem k nízkému výskytu kobaltu v zemské kůře existuje jen velmi málo přírodních drahých kamenů zbarvených kobaltovými ionty. Absorpční spektrum kobaltových iontů indikuje také syntetické drahé kameny, jako je syntetický modrý spinel a kobaltové sklo. Syntetický modrý spinel má tři silné absorpční pásy ve žlutozelené a oranžovožluté oblasti, přičemž nejužší je absorpční pás v zelené oblasti; absorpční čáry kobaltového skla mají především tři silné absorpční pásy ve žlutozelené a oranžovožluté oblasti, přičemž nejužší je absorpční pás ve žluté oblasti (obrázek 3-12).

3. Zbarvení prvků vzácných zemin
Výzkum vlivu stopových prvků vzácných zemin na barvu drahých kamenů je stále důkladnější. Barvy prvků vzácných zemin jsou živější a jejich fyzikálně-chemické vlastnosti jsou také velmi stabilní. Prvky vzácných zemin, jako je apatit a fluorit, mohou také zbarvovat přírodní drahé kameny. Do syntetických a optimálně upravených drahých kamenů lze přidávat různé prvky vzácných zemin a získat tak různě barevné drahé kameny, například žlutou z ceru a modrou z neodymu.
Prvky vzácných zemin, které barví drahé kameny, jsou především lanthanoidy a aktinoidy v periodické tabulce chemických prvků a barvy, které mohou vytvářet, jsou uvedeny v tabulce 3-7.
Tabulka 3-7 Prvky vzácných zemin a jejich barvy v běžných drahých kamenech
| Symbol prvku | La | Ce | Nd | Pr | Dy | Sm | Er | Tm | U |
|---|---|---|---|---|---|---|---|---|---|
| Celé jméno | Lanthan | Cer | Neodym | Praseodym | Dysprosium | Samarium | Erbium | Thulium | Uran |
| Barva | Bezbarvý | Žlutý | Modrá | Zelená | Světle žlutá | Světle žlutá | Růžová | Světle zelená | Stříbrnobílý |
Prvky vzácných zemin mají charakteristická absorpční spektra, která často tvoří jedinečné jemné čáry. Například žlutý apatit často obsahuje prvek vzácné zeminy Ce s charakteristickými jemnými absorpčními čarami ve žluté oblasti. Uran však nevytváří jasně žlutou barvu; může vytvářet výrazné absorpční spektrální čáry. Například v zeleném zirkonu se může objevit více než deset absorpčních čar v různých barevných zónách (obr. 3-13).

Oddíl III Barvy vytvářené krystalovými vadami a barevnými centry
V přírodě se minerály dělí na krystaly a nekrystaly na základě různých stupňů krystalizace. Většina drahých kamenů, jako jsou rubíny, safíry, diamanty, smaragdy a křemen, jsou krystaly; některé organické drahé kameny, například jantar a korály, jsou nekrystalické. Krystalické struktury mají mřížkovou strukturu, kde jsou jejich vnitřní částice (atomy, ionty nebo molekuly) uspořádány v pravidelném periodickém vzoru v trojrozměrném prostoru, a krystaly mohou samovolně vytvářet mnohostěny; nekrystaly jsou amorfní tělesa s nemřížkovou strukturou, která nemohou vytvářet mnohostěny, jako je sklo, kalafuna a pryskyřice.
Nejtypičtějším příkladem rozdílu mezi krystaly a amorfními pevnými látkami je křemen a sklo. Přírodní křemen vzniká z roztaveného materiálu SiO2 v magmatu, které chladne v dutinách zemské kůry. Vnější vrstva běžných křemenných koulí je achát, který nevykazuje krystalický tvar, zatímco vnitřní vrstva představuje krystalický tvar křemene. Hlavními chemickými složkami skla i křemene jsou SiO2; křemen je krystal s uspořádanými ionty křemíku a kyslíku, zatímco sklo je amorfní pevná látka s chaoticky uspořádanými ionty křemíku a kyslíku, které postrádají pravidelnost, jak ukazuje obrázek 3-14.
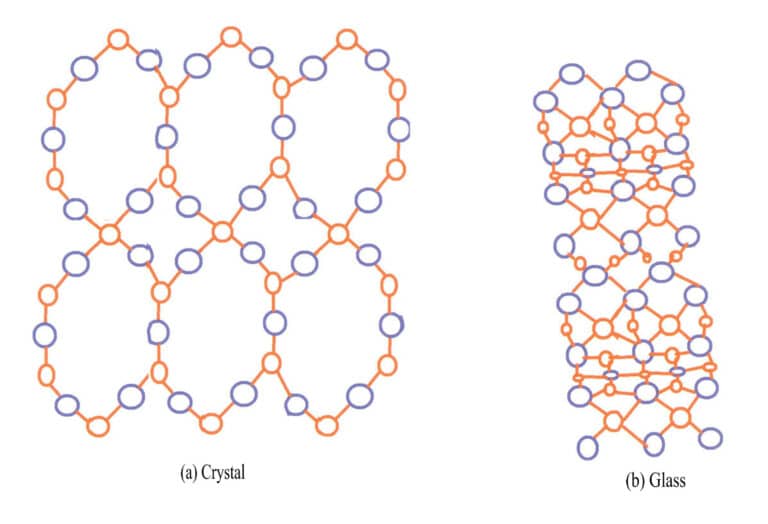
Většina krystalů drahých kamenů je zbarvena díky iontům nečistot, například rubíny, smaragdy a turmalíny. Některé drahé kameny, přestože postrádají chromoforem ionty, jsou barevné v důsledku defektů v jejich krystalové struktuře. Přírodní drahé kameny vznikající v přírodě mohou měnit barvu v důsledku vnějších podmínek, jako je ozařování a ionizace, které mění krystalovou strukturu. Nejběžnějším příkladem je záhněda, která získává barvu v důsledku vzniku barevných center z vakancí vyvolaných zářením. Uměle ozářený záhnědový křemen má podobný princip vzniku jako přírodní záhnědový křemen, s tím rozdílem, že umělé záření vytváří barvu rychle.
1. Vady a typy krystalů
Jev, při kterém se uspořádání částic odchyluje od pravidel mřížkové struktury (částice se periodicky translačně opakují v trojrozměrném prostoru) v lokálním rozsahu krystalové struktury drahokamu, se nazývá mřížková vada. Příčiny souvisejí s tepelnými vibracemi částic v krystalu drahokamu, vnějším napětím, vysokou teplotou a tlakem, ozařováním, difuzí, iontovou implantací a dalšími podmínkami.
Například u diamantů vykrystalizovaných ve vysokoteplotním a vysokotlakém prostředí svrchního pláště, kdy jsou rychle přeneseny hostitelským magmatem (kimberlitem nebo lamproitem) do blízkosti zemského povrchu, může rychlá změna teplotních a tlakových podmínek a vzájemné srážky mezi krystaly a okolními horninami snadno vést k lokálním změnám ve struktuře intruzivních diamantových krystalů, což vede k mřížkovým defektům, které mění barvu původně bezbarvých diamantů a vytvářejí hnědožluté, hnědé a růžové diamanty.
Přítomnost krystalových vad má významný vliv na vlastnosti krystalů. Ve skutečnosti mají krystaly více či méně defektů. Mírné množství určitých bodových defektů může výrazně zvýšit vodivost polovodičových materiálů a luminiscenci luminiscenčních materiálů, což hraje příznivou roli. Naproti tomu defekty, jako jsou dislokace, mohou způsobit náchylnost materiálů k lámání a snížit pevnost v tahu krystalů téměř bez mřížkových defektů na zlomek.
V ideálně dokonalém krystalu jsou atomy přísně uspořádány v pravidelné periodické mřížce v určitých bodech prostoru. Během skutečného růstu a tvorby krystalů se však vlivem růstového prostředí, jako je teplota, tlak a koncentrace složek prostředí, může morfologie krystalu po růstu někdy od ideální krystalové struktury odchýlit. Jakoukoli odchylku od ideální krystalové struktury lze nazvat krystalovou vadou. Krystalové defekty významně ovlivňují fyzikální a chemické vlastnosti krystalů a s krystalovými defekty souvisí mnoho oborů, například iontové dopování v materiálové vědě. Barva drahých kamenů do značné míry souvisí s krystalovými vadami v nich. To je jedna z příčin barvy drahých kamenů - barevná centra.
Existuje mnoho typů defektů krystalové struktury, které lze rozdělit do čtyř kategorií podle rozsahu jejich rozložení v trojrozměrném prostoru: bodové defekty, čárové defekty, povrchové defekty a objemové defekty.
(1) Bodové vady
V ideálním krystalu jsou některé atomy nahrazeny jinými, některé jsou dopovány nebo vznikají vakance. Některé atomy v krystalu jsou nahrazeny nebo chybí v důsledku vnějších atomů a tyto změny narušují periodické uspořádání pravidelné mřížky krystalu, způsobují změny v potenciálovém poli částic a vedou k neúplnosti krystalové struktury, omezené na určité polohy, ovlivňující pouze několik blízkých atomů. Vliv bodových defektů na krystal je minimální a mezi běžné typy bodových defektů patří polohové defekty mřížky, defekty složení a nábojové defekty (obrázek 3-15).
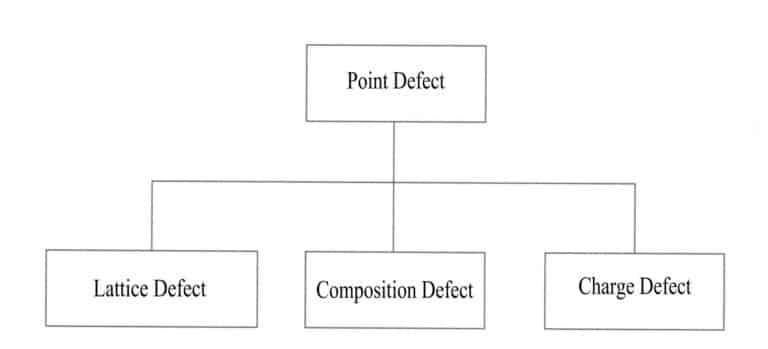
(2) Závady na vedení
Čárové vady jsou ve dvou směrech velmi malé a v jiném směru se většinou prodlužují. Jsou také známé jako jednorozměrné defekty a skládají se především z různých dislokací. Na dislokace lze pohlížet jako na součin lokálního mřížkového skluzu podél určité atomové roviny. Skluz neproniká celou mřížkou; krystalová vada končí uvnitř mřížky, což způsobuje neuspořádané uspořádání částic na hranici mezi sklouznutou a nesklouznutou částí mřížky, známé jako dislokace. Tato hranice, čára průsečíku mezi sklouznutou a nesklouznutou částí, se nazývá dislokační čára. Existují dva základní typy dislokací: když je krystal vystaven tlakovým silám, rovina skluzu částic tvoří dislokační čáru s neklouzavou rovinou a dislokační čára je kolmá ke směru skluzu, tzv. hranová dislokace, nazývaná také klínovitá dislokace; v důsledku smykového napětí dochází ke skluzu mezi rovinami a protínající se dislokační čáry ve skluzové části krystalu jsou rovnoběžné se směrem skluzu, označované jako šroubová dislokace (obrázek 3-16).
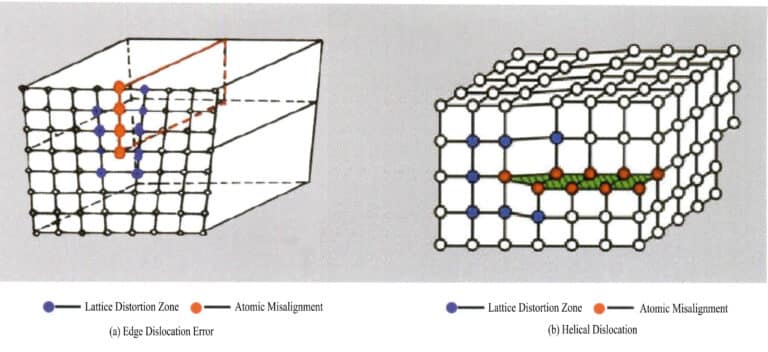
(3) Povrchové vady
Nejjednodušší povrchovou vadou je stohovací vada, která se dělí na vnitřní stohovací vady (kdy je odstraněna krystalová rovina) a vnější stohovací vady (kdy je do krystalu vložena atomární vrstva). Tyto vady se vyskytují v rozmezí několika atomových vzdáleností na obou stranách určité roviny podél mřížky nebo mezi zrny. Zahrnují především stohovací poruchy a rozhraní uvnitř krystalů a mezi nimi, jako jsou maloúhlové hranice zrn, doménové stěny a dvojčatové a mezikrystalové hranice.
(4) Objemové vady
Objemovými vadami se rozumí vady, které se vyskytují v různé míře ve všech třech směrech, což jsou trojrozměrné vady, jako jsou vložené trhliny, síťové struktury, rodinné struktury, dvojčata a různé inkluze drahých kamenů.
2. Barevná centra v drahých kamenech
Barevná centra jsou zvláštním případem mřížkových defektů, obecně se jedná o mřížkové defekty v drahých kamenech, které mohou selektivně absorbovat viditelnou světelnou energii a vytvářet barvu, patřící k nejtypičtějším strukturním typům barev. V některých případech se mohou nespárované elektrony, které produkují barvu, objevit také v iontech nepřechodných prvků nebo v krystalových defektech vzniklých v důsledku nedostatku elektronů, což jsou právě barevná centra. Bodové defekty v iontových krystalech mohou způsobit absorpci viditelného světla, v důsledku čehož se původně průhledné krystaly jeví jako barevné; tyto typy bodových defektů, které mohou absorbovat viditelné světlo, se obvykle označují jako barevná centra. Mnoho typů přírodních drahých kamenů vytváří barvu z barevných center, například fialový fluorit, kouřový křišťál a zelené diamanty.
V procesu optimalizace drahých kamenů mohou mít některé přírodní a umělé drahé kameny také barevná centra vytvořená zářením, jako jsou modré, žluté, červené, zelené diamanty a modré topasy, které mění barvu v důsledku záření, a modré topasy, mezi nimiž jsou některé barvy relativně stabilní a mizí pouze při zahřátí; některé barvy jsou nestabilní a mohou vyblednout i při pokojové teplotě. Tento typ barevného centra způsobujícího barvu úzce souvisí s krystalovou strukturou drahého kamene, jako jsou zelené diamanty, kde je příčinou barvy přítomnost vakancí v krystalové struktuře, ale tento strukturní defekt lze odstranit i ozářením, čímž se diamant stane bezbarvým. Běžnými typy barevných center v drahých kamenech jsou "elektronová barevná centra" a "děrová barevná centra".
(1) Centrum elektronové barvy (F centrum)
Elektronová barevná centra jsou barevná centra, která vznikají při výskytu elektronů ve vakancích krystalových defektů způsobených aniontovými vakancemi v krystalové struktuře drahého kamene. Pokud aniont chybí, vakance se stává kladně nabitou elektronovou pastí, která zachycuje elektrony. Pokud vakance zachytí elektron a naváže ho na tuto vakanci, elektron se excituje a selektivně absorbuje určitou vlnovou délku energie, čímž se zbarví. Proto se elektronové barevné centrum skládá z aniontové vakance a elektronu vázaného elektrickým polem této vakance.
Fialový fluorit je barva vytvářená elektronickými barevnými centry. Fluorit (CaF2) patří do izometrické krystalové soustavy, přičemž každý Ca2+ připojené ke dvěma F– [Obrázek 3-17 (a)]. V některých případech je F– ve fluoritu může opustit svou normální polohu. Na původním místě F– a aby byla zachována elektrická neutralita krystalu, musí toto volné místo obsadit záporně nabitá entita. Záporně nabitou entitou obsazující toto volné místo se stane elektron z určitého atomu v krystalu [obrázek 3-17 (b)]. Tím vznikne "barevné centrum", známé jako elektronické barevné centrum. Ve fluoritu elektronická barevná centra absorbují viditelné světlo, čímž vzniká fialová barva.
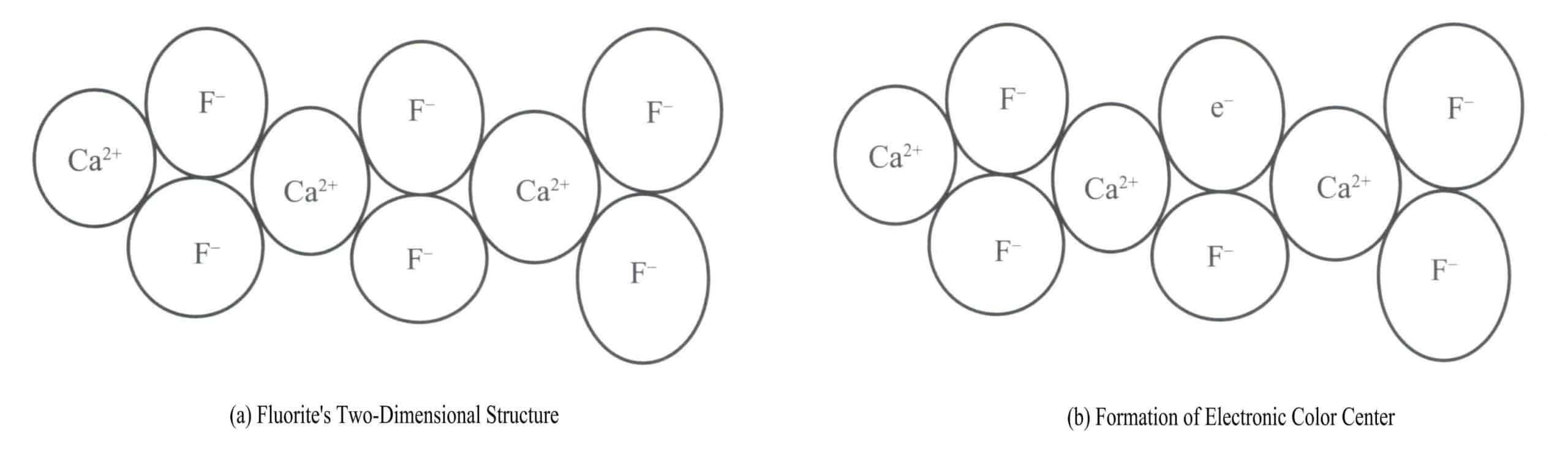
(2) Středy barev otvorů (V středy)
Barevné centrum vakance vzniká působením vnějších faktorů, kdy kationty vytvářejí elektronové vakance. To znamená, že elektrony jsou vytlačovány ze svých původních pozic a zanechávají za sebou nespárovaný elektron. Důvodem barvy je, že když se v krystalu vytvoří kationtové vakance, aby se dosáhlo nábojové rovnováhy, anionty v blízkosti kationtové vakance uvolňují elektrony pod vlivem vnější energie a vytvářejí nepárové elektrony, které absorbují viditelné světlo a vytvářejí barvu. Například v ozářených diamantech a modrém topazu dodává ozáření energii k aktivaci elektronů, což způsobuje přemístění iontů nebo atomů v mřížce, a tím vznik strukturních defektů a barevných center v důsledku ozáření.
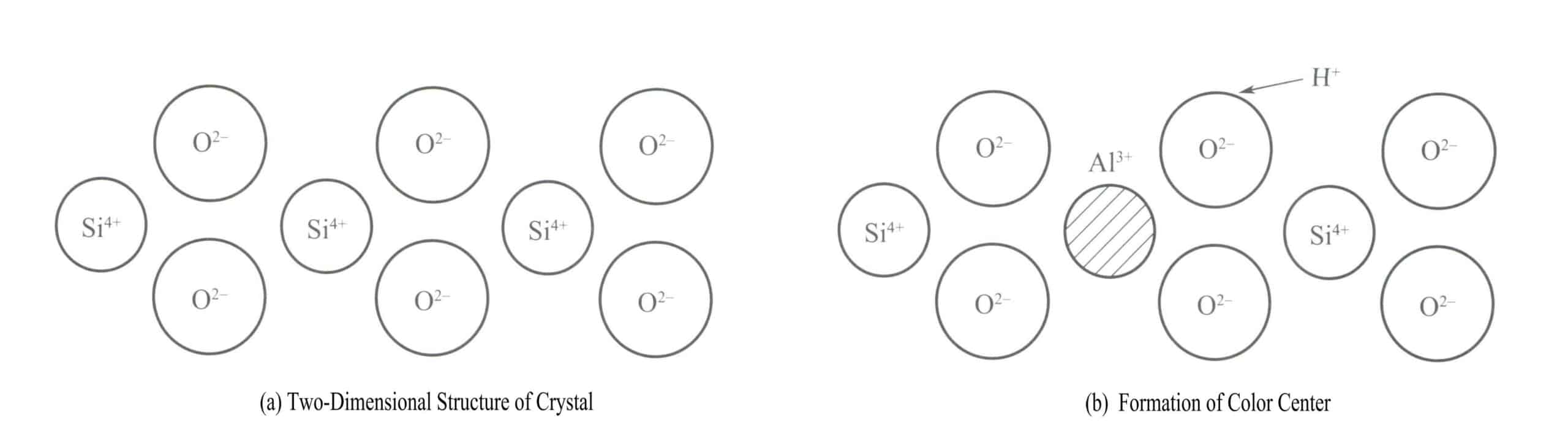
Klasickým příkladem barevného centra v křišťálu je zbarvení záhnědy. Krystalovou strukturu křemene tvoří křemíko-kyslíkový čtyřstěn, přičemž křemík je ve čtyřkoordinačním stavu, jak ukazuje dvourozměrné strukturní schéma na obrázku 3-18(a). Každých 10 000 Si4+ atomy mají jeden nahrazený Al3+a když Al3+ nahrazuje Si4+ v krystalu, Al3+ musí být obklopen některými alkalickými ionty (např. Na+ nebo H+), aby byla zachována elektrická neutralita. Přesto jsou tyto ionty často v určité vzdálenosti od Al3+.
Při ozařování křemene rentgenovým zářením, zářením γ a dalšími zdroji záření se energie sousedních atomů kyslíku s Al3+ se zvýší, což umožní, aby byl jeden z elektronů v páru vyhozen ze své normální polohy. H+ zachytí tento elektron a vytvoří H . Vysokoenergetické záření způsobí, že O2- s větším počtem valenčních elektronů uvolní elektron a vytvoří [A1O4]4- a barevný střed [A1O4]4- atomový shluk absorbuje viditelné světlo a vytváří barvu, čímž vzniká kouřový křemen.
[A1O4]5-→ [A1O4]4-+e– (3-1)
H+ +e–→ H (3-2)
H+ zachycuje elektrony a stává se H, který je bezbarvý a neabsorbuje viditelné světlo. Pokud je intenzita ozařování vysoká a je dostatek Al3+ v krystalu lze křemen ozářit do černé barvy. Vzhledem k tomu, že v místě, kde je elektron vyražen, se často nachází vakance, označuje se tento typ barevného centra jako "vakanční barevné centrum".
Během geologické historie vzniká přírodní kouřový krystal většinou dlouhodobým ozářením nízkými dávkami radioaktivních materiálů. Zahříváním lze barvu odstranit; když se tento kouřový krystal zahřeje na teplotu kolem 400 ℃, vyvržené elektrony se vrátí do původních poloh, všechny elektrony se spárují a křemen se opět stane bezbarvým; je-li znovu ozářen, může se opět stát kouřovým [obrázek 3-18 (b)].
Ametyst má stejná barevná centra vakance, ale jeho příměsí je železo místo hliníku. Když je příměs Fe 3+ nahrazuje Si4+ v křemeni dochází při ozáření vysokoenergetickým zářením k následujícím změnám:
[FeO4]5- → [FeO4]4- +e– (3-3)
H+ +e–→ H (3-4)
Podobně jako u principu vzniku kouřového krystalu vzniká fialová barva v důsledku tvorby [FeO4]4- barevná centra otvorů po ozáření. Při zahřátí tento ametyst zežloutne a stane se citrínem a při dalším zahřívání vybledne na bezbarvý. Obecně je teplota zahřívání poměrně nízká, kolem 400 ℃. Fialovou barvu tepelně upraveného ametystu lze obnovit opětovným ozářením barevných center. Na tomto principu se syntetizuje také syntetický ametyst.
V některých drahých kamenech může několik shluků atomů nečistot rovněž tvořit barevná centra a vykazovat barvu. Například při růstu berylu a při radioaktivním ozařování, může ztratit elektron a stát se , čímž vznikne červenozelený absorpční pás, který vytváří modrou barvu. V diamantech existuje mnoho barevných center, z nichž většina je způsobena vznikem vakancí nebo dislokací ve struktuře za vnějších podmínek, a barvy jsou obecně velmi stabilní.
Studium barevných center je poměrně náročné a vyžaduje různé techniky, jako je spektroskopie a elektronová paramagnetická rezonance. Předchozí výzkumy ukazují, že některé typické charakteristiky barev indukovaných barevnými centry jsou poměrně jasné. Tabulka 38 shrnuje barvy a příčiny barvy indukované barevným centrem u běžných drahých kamenů.
Tabulka 3-8 Barvy a příčiny barevného středu u běžných drahých kamenů
| Typy drahých kamenů | Barva | Příčina |
|---|---|---|
| Diamond | Zelená | Uhlíkové volno GR1 barevný střed v diamantu |
| Žlutý | Chybějící struktura diamantových agregátů N3 | |
| Orange | Natomy a vady barevného středu H3, H4 | |
| Crystal | Barva kouře | Volná pracovní místa vytvořená Al3+ nahrazením Si4+ , související s radiací |
| Žlutý | Související s Al3+, může být také generován zářením | |
| Fialová | Fe3+ nahrazuje volné pracovní místo, které vzniklo po Si4+ | |
| Drahokam korund | Žlutý | Barva je nestabilní, důvod strukturálních vad není znám. |
| Topaz | Modrá | Barva je stabilní, důvod strukturálních vad není znám. |
| Žlutý | Barva je stabilní, příčina strukturálních vad není známa. | |
| Hnědočervené | Barva je nestabilní, příčina strukturálních vad není známa. | |
| Turmalín | Červená | Související s Mn3+ , může být také způsobena zářením |
| Beryl | Modrá | Souvisí s CO32- , může být také způsobena ozářením |
| Fluorit | Fialová | Elektronické e- nahrazuje F- a vytváří |
Princip barevných center se používá také ke zlepšení barvy přírodních drahých kamenů při zušlechťování drahých kamenů. Většina metod využívá ke změně barvy drahých kamenů ozařování. Některá barevná centra jsou relativně stabilní, zatímco některé odrůdy drahých kamenů rychle blednou, takže tato metoda vylepšování je pro tyto drahé kameny méně významná. Tabulka 3-9 uvádí některé barvy vytvářené barevnými centry, včetně stabilních barevných center, nestabilních barevných center a barev vytvářených dalšími možnými faktory.
Tabulka 3-9 Barvy vytvořené barevnými centry
| V podstatě stabilní ve světle | Ametyst, fluorit (fialovo-červený), ozářené diamanty (zelený, žlutý, hnědý, černý, modrý, růžový); některé přírodní nebo ozářené topasy (modré). |
|---|---|
| Na světle rychle bledne | lithium-cesiový zelený beryl (tmavě modrý); některé ozářené topasy (hnědý nebo hnědý); ozářený safír (žlutý); ultrafialově ozářený fialový sodalit (fialově červený). |
| Další barvy, které mohou barevná centra produkovat | Sylvín (modrý); halit (modrý nebo žlutý); zirkon (hnědý); kalcit (žlutý); baryt, celestin (modrý); amazonit (modrý až zelený) |