Что такое химическое золочение и как оно работает?
Химическое золотое покрытие: Техники, решения и применение в ювелирном деле
Введение:
Что такое химическое золотое покрытие? Это процесс, используемый для нанесения тонкого слоя золота на различные материалы, улучшающий их внешний вид и долговечность. Как это работает? Химическое золочение предполагает использование специальных растворов с ионами золота и восстановителями. В традиционных методах часто используется цианид, но есть и безцианидные варианты. Почему стоит выбрать химическое золотое покрытие? Оно обеспечивает равномерное и высококачественное покрытие, которое идеально подходит для ювелирных и других декоративных изделий. Если вы занимаетесь изготовлением ювелирных изделий, дизайном или розничной торговлей, понимание этих методов может повысить качество вашей продукции.

Оглавление
Раздел I Цианистое химическое золотое покрытие
1. Обзор
С учетом высокой плотности электронных компонентов, сложности линейного дизайна, микрофабрикации схем и независимости электрических свойств химическое золочение, которое решает проблему сложности процесса покрытия, стало неизбежным способом золотого покрытия. Однако химическое золочение имеет следующие недостатки:
① Медленная скорость;
② Узкие условия использования и рабочий диапазон, что повышает сложность управления;
③ Поверхность материала должна быть тщательно очищена;
④ Срок службы гальванического раствора короткий (подвержен самоокислительным реакциям);
⑤ Толщина покрытия очень чувствительна к условиям перемешивания.
Поэтому химическое золочение должно выполняться на специальном оборудовании. Обычно используемый состав раствора для химического золочения приведен в таблице 1-24. Он готовится путем сочетания различных координационных солей золота и восстановителей.
Таблица 1-24 Типы координационных солей золота и восстановителей в растворе для химического золочения
| Редуцирующий агент | KAu(CN)2 | KAu(CN)4 | Na3Au(SO2)2 | HAuCl4 - 3H2O | HAuCl4 ・ 3H2O | AuCN | KAu(CN)4 | KAu ・ O2 | KAu(OH)4 | AuI | Не определено |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Гипофосфит натрия | 57,58 | 71 | 77 | ||||||||
| Формальдегид | 71 | 78 | |||||||||
| Биазид | 59 | 71 | 76 | 78 | |||||||
| Борогидрид | 60,61 | 72 | 78 | 79 | |||||||
| Метилборан | 60 | 69 | 74 | 75 | 79 | 80 | |||||
| Гидроксиламин | 62 | ||||||||||
| Неопубликованный | 63 | 73 | 81 | ||||||||
| Тиомочевина | 64 | ||||||||||
| Гидроксид аммония | 65 | ||||||||||
| Калий-натрий тартрат тетрагидрат (комбинированный) | 66 | 70 | |||||||||
| N,N-диметиламид | 82 | ||||||||||
| N,N-диметилглицин | 67 | ||||||||||
| Нет | 68 |
Таблица 1-25 Функции компонентов в растворе для химического золочения
| Компонент | Назначение | Название соединения |
|---|---|---|
| Ион золота | Поставка металлического золота | KAu(CN)2、KAu(CN)4AUCN, Na3Au(SO2)2. HAuCl4 - 3H2O、KAu ・ O2 |
| Редуцирующий агент | Восстановители для осаждения золота | Калия натрия тартрат тетрагидрат, борогидрид, амин боран, формальдегид, гипофосфит, N,N-диметилглицин, аскорбиновая кислота |
| Органические хелатирующие агенты | Буферное действие для предотвращения быстрого осаждения золота | ЭДТА, цитрат калия, винная кислота |
| Стабилизатор | Маскировка активных ядер для предотвращения разложения гальванического раствора | Тиомочевина, цианид металла, ацетилацетон |
| Активатор | Замедляющее действие замедляющего хелатирующего агента | Янтарная кислота |
| Буферный агент | Поддерживать определенный уровень pH | Фосфаты, цитраты, тартраты |
| Поверхностно-активное вещество | Легко смачивайте детали с покрытием | Алифатические сульфонаты, сульфаты спирта |
2. Гипофосфитный раствор для золотого покрытия
Когда основной металл и золото в гальваническом растворе вступают в реакцию вытеснения, металл с более низким электрохимическим потенциалом ионизируется легче, чем золото. Во время реакции, как только поверхность основного металла полностью покрывается золотом, реакция немедленно прекращается, поэтому можно получить только тонкий слой золотого покрытия толщиной 0,1~0,3 мкм. Этот раствор для нанесения покрытия, или раствор Брукшира, является старым раствором для нанесения покрытия и представляет собой основной состав продаваемых в настоящее время химических растворов для нанесения золотого покрытия. Характеристики раствора: базовый слой для нанесения золотого покрытия должен быть никелевым для реакции вытеснения; золото не может быть нанесено на медный материал методом вытеснения.
(1) Состав и условия применения гипофосфитного раствора для химического золотого покрытия
В таблице 1-26 приведен типичный состав гипофосфитного раствора для химического золочения.
Таблица 1-26 Состав и условия применения гипофосфитного раствора для химического золотого покрытия
| Состав и условия эксплуатации | Серийный номер | ||||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | |
| Цианид золота калия/(г/л) | 2 | 2 | 20 | 2 | 2 |
| Гипофосфит натрия/(г/л) | 10 | 10 | 10 | 10 | 10 |
| Цианид калия /(г/л) | 0.2 | 0.2 | 80 | 0.4 ① | 0.2 |
| Температура/°C | 96 | 96 | 96 | 96 | 96 |
| pH | 13.5 | 7.5 | 13.5 | 13.5 | 7.1 |
| Скорость нагрузки/(см2/см3) | 0.25 | 0.25 | 0.25 | 0.25 | 0.25 |
| Скорость нанесения покрытия/[мг/(см2- h)] | 9.8 | 9.85 | 12.3 | 8.2 | 3.86 |
(2) Влияние никеля на скорость осаждения гипофосфитного гальванического раствора
В растворе для химического золочения с гипофосфитом в качестве восстановителя активные ионы металлов (Ni2+) добавляются. Металл (никель) и золото в незначительных количествах осаждаются на поверхности покрываемых деталей, создавая большую химическую движущую силу и увеличивая скорость нанесения золотого покрытия. Принцип работы показан на схеме рис. 1-25.
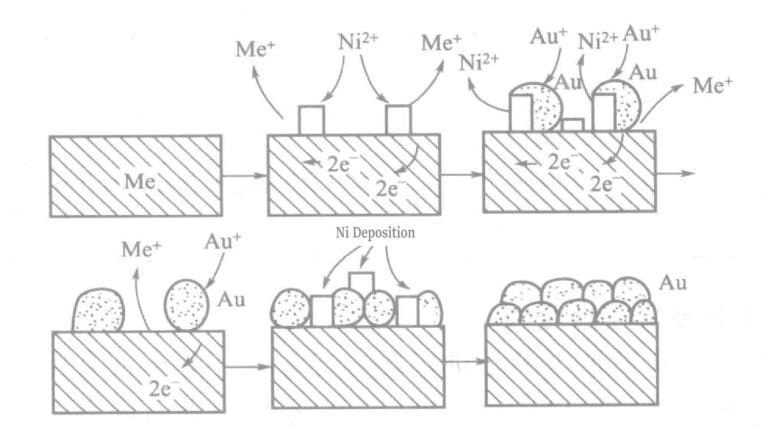
Таблица 1-27 Состав и условия работы гипофосфитного раствора для золотого покрытия
| Состав и условия эксплуатации | I | II | Состав и условия эксплуатации | I | II |
|---|---|---|---|---|---|
| Цианид золота калия/(г/л) | 2, 5, 7 | 2, 5, 7 | Цианид калия /(г/л) | - | 2 |
| Цитрат натрия/(г/л) | 75 | 75 | H2NNH2 - H2O / (г/л) | - | 2 |
| Гипофосфит натрия/(г/л) | 15 | 15 | pH | 8.5 | 4.3 |
| ЭДТА-2Na/(г/л) | - | - | Температура/℃ | 70, 90 | 70, 90 |
| Хлорид натрия/(г/л) | - | 5 |
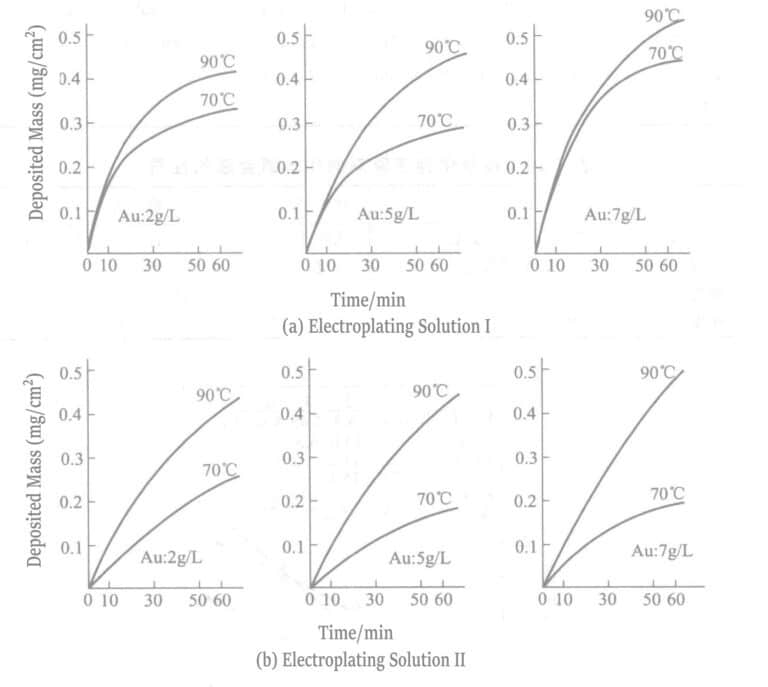
3. Раствор борогидридной соли для гальванических покрытий
(1) Состав Свойства химического раствора борогидрида калия для золотого покрытия
В 1969 году Окинака и др. предложили использовать раствор для нанесения покрытия с борогидридными соединениями в качестве восстановителя. Состав и условия применения боргидридных растворов для химического золочения приведены в таблицах 1-28, а свойства золотых слоев, покрытых этими растворами, - в таблицах 1-29. Толщина слоев, нанесенных в разное время с помощью различных растворов, показана на рис. 1-27. Суммарные результаты применения восстановителей - борогидрида калия и диметиламиноборана - приведены в табл. 1-30.
Таблица 1-28 Состав и условия работы раствора химического золотого покрытия на основе борогидрида калия
| Состав и эксплуатация | Серийный номер | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| Цианид золота калия/(г/л) | 0. 02моль/л (5,8 г/л) | 0. 03моль/л (8,6 г/л) | 0. 005моль/л (1. 45г/л) |
| Цианид калия | 0. 2моль/л (13,0 г/л) | 0. 2моль/л (13,0 г/л) | 0. лмоль/л (6,5 г/л) |
| Гидроксид калия | 0. 2моль/л (11,2 г/л) | 0. 2моль/л (22,4 г/л) | 0. 2моль/л (11,2 г/л) |
| Борогидрид калия | 0. 4моль/л (21,6 г/л) | 0. 8 ммоль/л (43,1 г/л) | 0. 2моль/л (10,8 г/л) |
| Температура/°C | 75 | 75 | 75 |
Таблица 1-29 Свойства раствора для химического золочения с восстановителем борогидридом калия
| Природа | Данные | Природа | Данные |
|---|---|---|---|
| Прочность скрепления | Отличная прочность сцепления металлического слоя | Пористость | Отсутствие пор размером более 1 мкм на однородной поверхности |
| Внешний вид | Тускло-желтый | Чистота | 99. 9% |
| Плотность | Содержание золота 19. 3 г/см3 | Значение сопротивления | 0. 03Ω/см2 ( Au: 1 мкм) |
| Твердость | Твердость нупа 60〜80 | Паяемость | Превосходно |
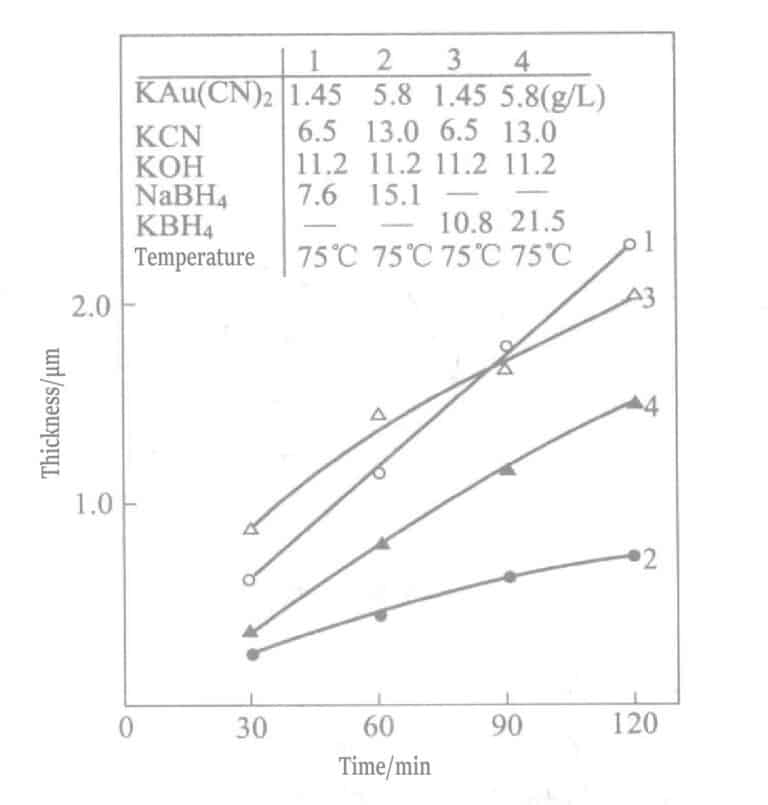
Таблица 1-30 Функции компонентов в химическом растворе борогидрида калия для золотого покрытия
| Влияющие факторы | Раствор борогидрида калия для гальванических покрытий | Раствор для нанесения покрытия DMAB (диметиламиноборан) |
|---|---|---|
| Влияние концентрации золота | Когда концентрация золота достигает 0,002 моль/л, скорость осаждения резко возрастает и снижается выше этого уровня. | Скорость осаждения линейно возрастает при концентрации золота 0,01 моль/л, но не оказывает влияния выше этого значения. |
| Действие цианистого калия |
Нестабильный раствор для нанесения покрытия при концентрации ниже 0,005 моль/л. Золото не выпадает в осадок при концентрации выше 0,2 моль/л. |
То же, что и слева |
| Влияние борогидрида калия | BH не стабилен при комнатной температуре. Добавление гидроксида калия повышает стабильность ванны, а скорость выпадения осадка уменьшается с увеличением концентрации. | ДМАБ стабилен при комнатной температуре, скорость выпадения осадка увеличивается с увеличением количества гидроксида калия. |
| Концентрация восстанавливающего агента | Увеличение скорости выпадения осадков с ростом концентрации | |
| Влияние температуры ванны для нанесения покрытия | Увеличьте скорость выпадения осадков на 10℃ и разлагайте при температуре 85℃. |
(2) Влияние скорости нанесения покрытия и ионов тяжелых металлов
Добавление следовых количеств ионов тяжелых металлов (свинца, таллия и т. д.) в раствор для химического золочения значительно увеличивает скорость осаждения. Макинтайр объяснил этот эффект следующим образом. Из-за низкого потенциала осаждения каталитический эффект адсорбированных атомов свинца, как показано в механизмах (1-4) и (1-5), способствует зарождению.
Pb2+ + 2e– → Pbобъявление (1-4)
2Au(CN)2– + Pbобъявление → 2Au + Pb2+ + 4CN– (1-5)
Из-за большой разницы в рабочих функциях меди, золотых материалов и ионов свинца свинец восстанавливается и осаждается при потенциале, более положительном, чем термодинамический окислительно-восстановительный потенциал, образуя монослой. Благодаря каталитической реакции адсорбированных атомов свинца, как показано в (1-4) и (1-5), реакция восстановления Au(CN) протекает быстро, эффективно способствуя осаждению золота.
Зависимость между концентрацией свинца и скоростью осаждения в растворе боргидрида калия для восстановления золотого покрытия показана на рис. 1-28, а состав раствора для покрытия приведен в табл. 1-31. Свинец добавляется в виде нитрата свинца. На рис. 1-28 показано, что концентрация добавляемого свинца в растворе может составлять только около 20 мл/л, и добавление большего количества не дает никакого эффекта.
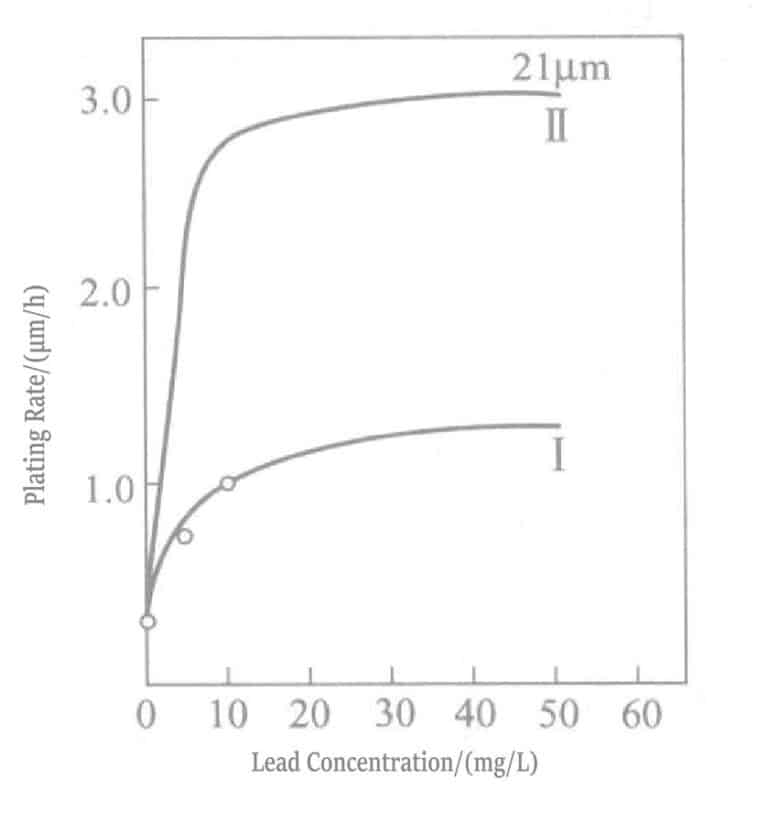
Таблица 1-31 Состав и условия работы раствора борогидрида калия для золотого покрытия
| Состав и условия эксплуатации | I | II | Состав и условия эксплуатации | I | II |
|---|---|---|---|---|---|
| Цианид золота калия/(г/л) | 2 | 2 | Цианид калия /(г/л) | 10 | 10 |
| Калий борогидрид/(г/л) | 2 | 10 | ЭДТА-2Na/(г/л) | 5 | 5 |
| Цианид калия/(мг/л) | 5 | 5 | Температура раствора для нанесения покрытия/°C | 75 | 75 |
Таблица 1-32 Состав раствора для золотого покрытия BMAB
| Состав и условия эксплуатации | Концентрация | Состав и условия эксплуатации | Концентрация |
|---|---|---|---|
| Цианид золота калия/(г/л) | 2 | Цианид калия /(г/л) | 30 |
| БМАБ/(г/л) | 10 | ЭДТА-2Na/(г/л) | 5 |
| Цианид калия/(мг/л) | 5 | рН | 13.6 |
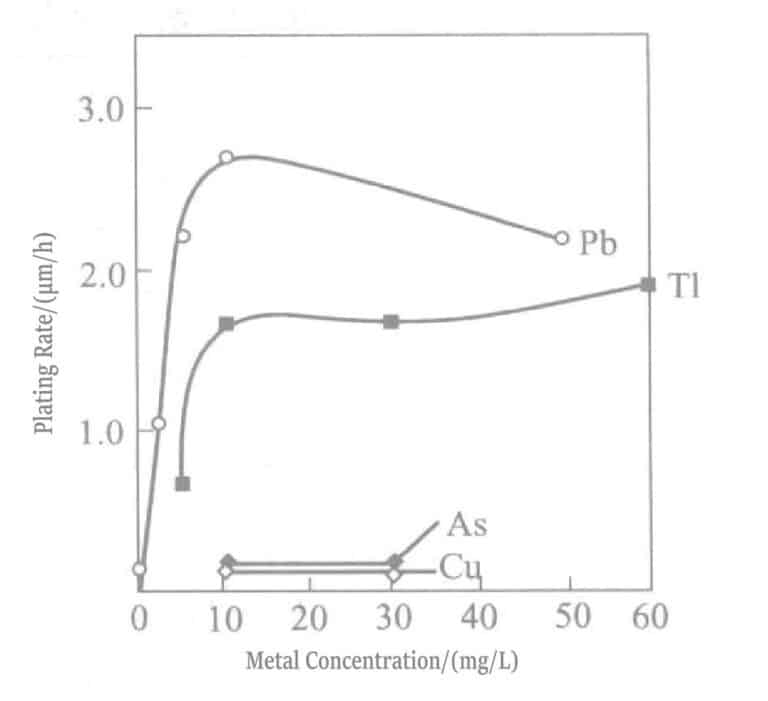
Таблица 1-33 Состав раствора цианида золота(III) калия для химического золотого покрытия
| Состав | Параметры | Состав | Параметры |
|---|---|---|---|
| KAu(CN)4/(г/л) | 4 | KOH/(мг/л) | 11.2 |
| KBH4/(г/л) | 3 | Температура/℃ | 70 |
| PbCl2/ (мг/л) | 0.5 |
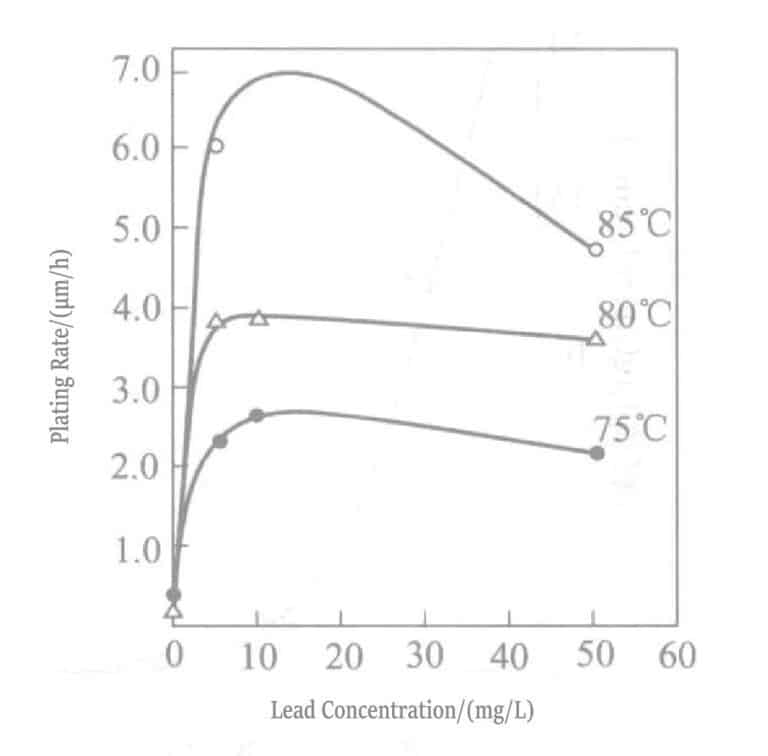
Рисунок 1-30 Влияние температуры и концентрации свинца на скорость осаждения золота
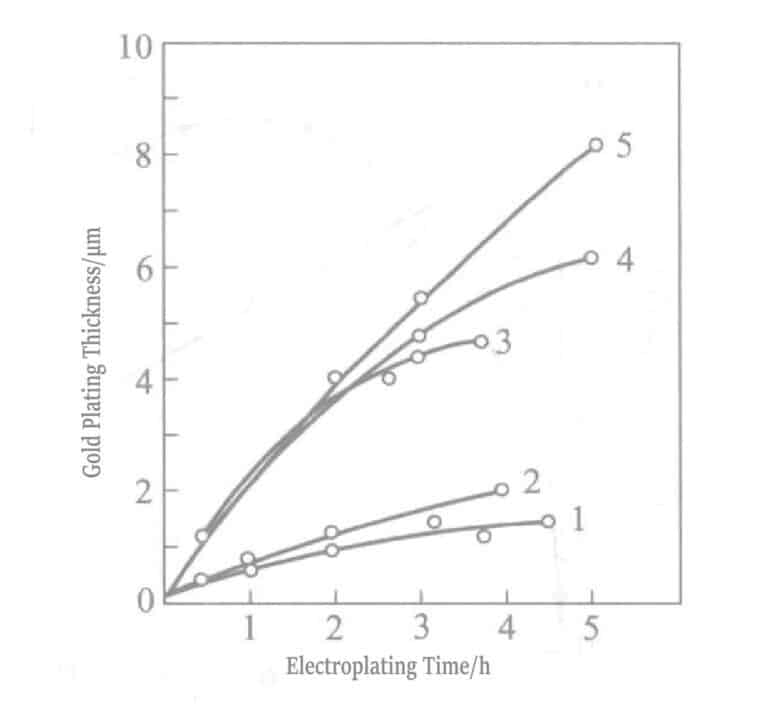
Рисунок 1-31 Зависимость между временем нанесения покрытия и толщиной слоя золотого покрытия
1 - Нет перемешивания Au+ жидкость; 2 - Не перемешивать Au3+ жидкость; 3 - перемешивание Au3+ жидкость; 4 - пополнение запасов Au3+ жидкость; и 5 - обновление Au3+ жидкость
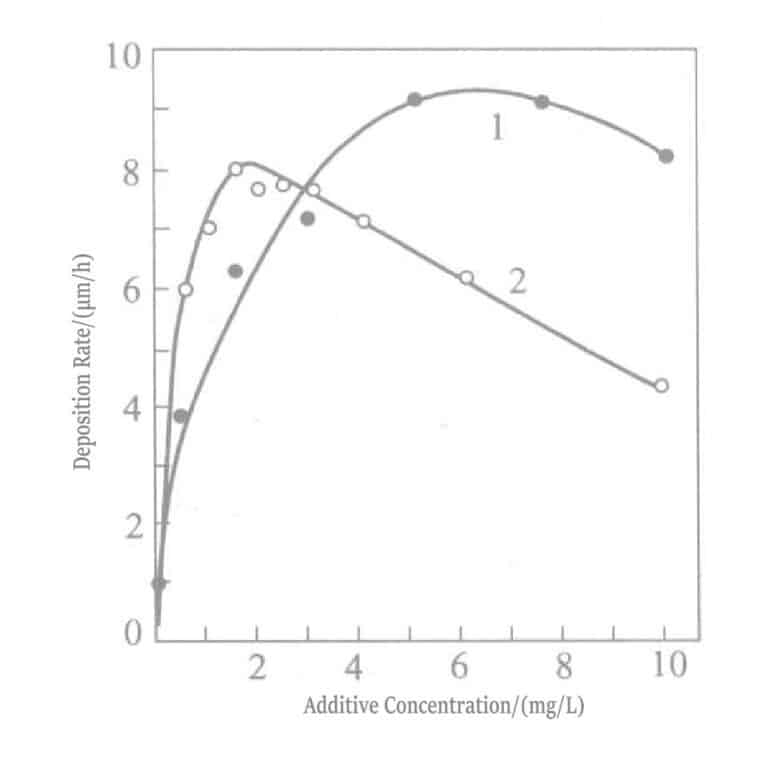
Рисунок 1-32 Влияние добавленных концентраций свинца и таллия на скорость золотого покрытия
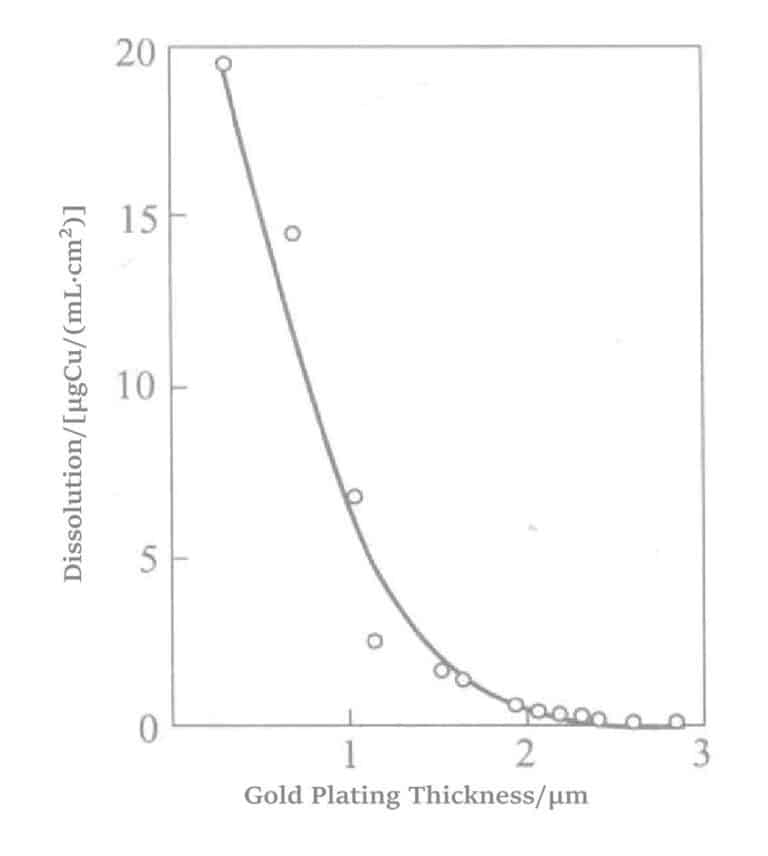
Рисунок 1-33 Пористость слоя электролитического золотого покрытия
Процесс химического золочения кристаллизованного стекла (SiO2 46% + Al2O3 16% + MgO 17% + K2O 10% + F 4% + B2O3 7% ) показан на рисунке 1-34.
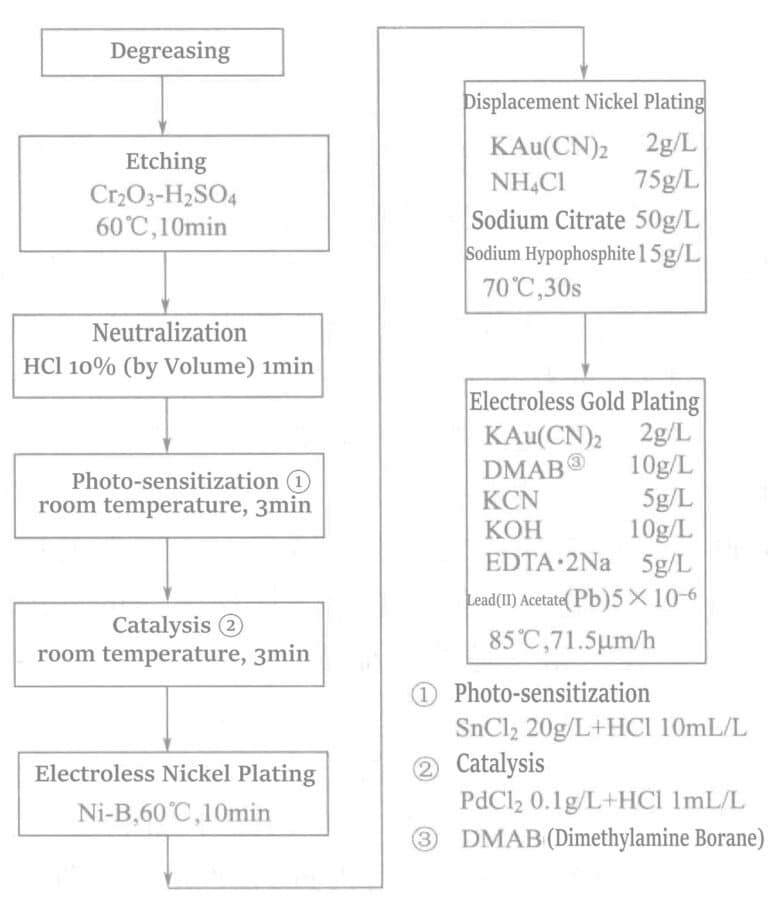
4. Механизм реакции химического раствора боргидридной соли для золотого покрытия
Линь Чжунфу и др. предположили, что растворы боргидрида калия и ДМАБ (диметиламиноборана) для золотого покрытия, приведенные в таблице 1-34, могут стать практичными растворами для золотого покрытия после добавления стабилизаторов.
(1) Состав двух гальванических растворов: В таблице 1-34 представлены две композиции.
Таблица 1-34 Химические растворы борогидрида калия и ДМАБ для гальванических покрытий
| Состав гальванического раствора | Раствор борогидрида калия для гальванических покрытий | Раствор для нанесения покрытия DMAB |
|---|---|---|
| Цианид золота калия/(моль/л) | 0.02 | 0.02 |
| Цианид калия/(моль/л) | 0.2 | 0.02 |
| Гидроксид калия/(моль/л) | 0.2 | 0.8 |
| Калий борогидрид/(моль/л) | 0.4 | - |
| ДМАБ/(моль/л) | - | 0.4 |
| Температура/°C | 75 | 85 |
| Скорость нанесения покрытия/(мкм/ч) | 0.7 | 0.4 |
(2) Механизм реакции: В растворе боргидрида калия для золотого покрытия, BH4– сам по себе не производит восстановительного эффекта, но промежуточный BH3OH– продукта его гидролиза BO2– выступает в качестве восстановителя.
BH4– + H2O → BH3OH–+ H2 (1-6)
BH3OH– + H2O → BO2– + 3H2 (1-7)
BH3OH– + 3OH– → BO2– + 3/2 H2 + 2H2O + 3e– (1-8)
Au(CN)2– + e– → Au + 2CN– (1-9)
BH3OH– + 3Au(CN)2– + 3OH– → BO2– + 3/2 H2 + 2H2O + 3Au + 6CN – (1-10)
Реакции гидролиза по уравнениям (1-6) и (1-7) были проанализированы с помощью полярографии. Результат показывает, что реакция (1-7) протекает в 500 раз быстрее, чем реакция (1-6). Таким образом, коэффициент использования борогидрида калия в реакции золочения очень низок. При типичных условиях нанесения покрытия эффективная скорость утилизации не превышает 2%~3%, при этом большая часть восстановителя остается неэффективной из-за гидролиза.
Вышеуказанная реакция гидролиза протекает быстро при низком pH (кислотно-катализируемая реакция), и скорость осаждения золота возрастает при низкой концентрации гидроксида калия. Чтобы предотвратить естественное разложение раствора для золотого покрытия, концентрацию гидроксида калия необходимо поддерживать на уровне не ниже 0,1 моль/л. Зависимость между скоростью осаждения золота и концентрацией гидроксида калия показана на рисунке 1-35.
![Рисунок 1-35 Кривая изменения скорости нанесения покрытия в зависимости от концентрации гидроксида калия [KAu(CN)2 0,02 моль/л, KCN (сплошная линия) 0,2 моль/л, KCN (пунктирная линия) 0,1 моль/л, 80 °C].](https://sobling.jewelry/wp-content/uploads/2025/11/Page_58_docsmall.com_副本-768x801.jpg)
Рисунок 1-35 Кривая изменения скорости нанесения покрытия в зависимости от концентрации гидроксида калия
[KAu(CN)2 0,02 моль/л, KCN (сплошная линия) 0,2 моль/л, KCN (пунктирная линия) 0,1 моль/л, 80 °C].
![Рисунок 1-36 Влияние концентрации гидроксида калия на скорость нанесения покрытия в растворе ДМАБ, ДМАБ [KAu(CN)2 0,02моль/л, KCN 0,2моль/л, ДМАБ 0,4моль/л, 75℃].](https://sobling.jewelry/wp-content/uploads/2025/11/Page_58_docsmall.com_副本1-768x560.jpg)
Рисунок 1-36 Влияние концентрации гидроксида калия на скорость осаждения в растворе ДМАБ, ДМАБ
[KAu(CN)2 0,02моль/л, KCN 0,2моль/л, DMAB 0,4моль/л, 75℃]
(CH3)2NH2 - BH3 + OH– → (CH3)2NH2 + BH3OH– (1-11)
(3) Проблемы с раствором для нанесения покрытия на основе борогидрида калия и раствором для нанесения покрытия на основе ДМАБ
На рисунке 1-37 показано, что скорость нанесения покрытия изменяется в зависимости от концентрации ионов меди и никеля в растворе для нанесения покрытия. Когда концентрация ионов никеля составляет 10-5моль/л, скорость осаждения начинает снижаться, а когда концентрация ионов никеля достигает 10-3моль/л, гальванический раствор разлагается. Ионы меди практически не влияют на скорость осаждения. На начальной стадии золотого покрытия ионы золота и никеля вступают в реакцию вытеснения, следовые количества ионов никеля растворяются, и скорость покрытия замедляется.

Рисунок 1-37 Влияние ионов меди и ионов никеля на скорость нанесения покрытия
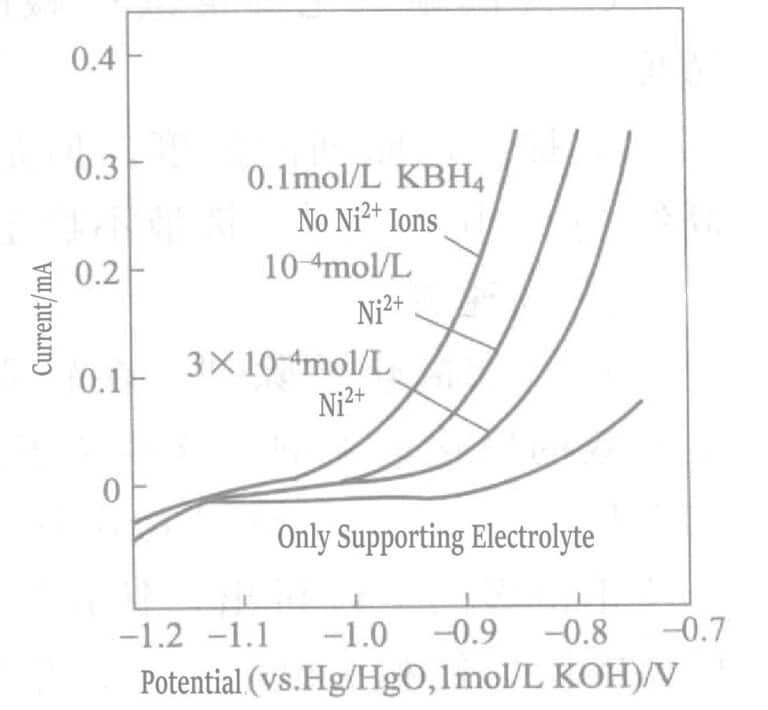
Рисунок 1-38 Влияние следовых ионов никеля на ток анодного окисления BH3OH
(Золотой вращающийся электрод, 2000 об/мин, 75℃, KOH 0,2 ммоль/л, KCN 0,1 ммоль/л)
Влияние добавления следовых количеств ионов никеля на BH3OH– Анодный ток окисления показан на рис. 1-38. Добавление следовых ионов никеля значительно ингибирует реакцию окисления восстановителя BH3OH– на золотом вращающемся дисковом аноде. Это объясняется тем, что ионы никеля существуют в виде цианистой лигандной соли Ni(CN)42- и этот комплексный ион преимущественно адсорбируется на поверхности золота, препятствуя его осаждению.
Для нестабильных базовых слоев (например, нитрида алюминия) нельзя использовать сильнощелочные растворы. pH раствора зависит от природы восстановителя, что является самым большим недостатком растворов борогидрида калия и DMAB.
Что касается вышеупомянутых проблем, за исключением того, что pH раствора для нанесения покрытия не может быть изменен, другие аспекты могут быть улучшены.
(4) Улучшить раствор боргидрида калия для золотого покрытия и раствор DMAB для золотого покрытия
① Увеличение скорости нанесения покрытия
- a. Измените основной состав раствора для нанесения покрытия и условия работы, чтобы увеличить скорость нанесения покрытия.
- b. Увеличьте скорость перемешивания.
- c. Повысьте температуру раствора для нанесения покрытия.
- d. Уменьшить концентрацию свободного цианида.
- e. Уменьшите концентрацию щелочи в растворе борогидрида калия и увеличьте концентрацию щелочи в растворе DMAB.
- f. Увеличьте концентрацию восстановителя. Однако, когда скорость нанесения покрытия без специальных добавок увеличивается примерно на 2 мкм/ч или более, раствор для нанесения покрытия становится нестабильным и склонным к разложению.
② Высокоскоростной раствор для нанесения покрытия
- a. Добавьте поляризационные элиминаторы. В растворах для мягкого золотого покрытия Pb2+ , T1+ Ионы свинца являются эффективными устранителями поляризации. Эти ионы сильно адсорбируются на поверхности золота, что приводит к так называемому явлению UPD (under potential deposition), когда свинец осаждается при потенциале, гораздо более положительном, чем Pb2+ / Pb равновесный потенциал и таллий осаждается при потенциале более положительном, чем T1+ /T1 равновесный потенциал. Осажденные свинец, таллий и Au(CN)2– вступает в реакции вытеснения, в результате чего реакция осаждения золота смещается в сторону более положительного потенциала (ослабление поляризации). С другой стороны, добавление этих ионов в растворы для химического осаждения золота, аналогично электролитическому осаждению, смещает Au(CN)2– восстановительный потенциал в положительном направлении, что приводит к увеличению скорости нанесения покрытия, которая может достигать около 10 мкм/ч. Растворы для нанесения покрытия с добавлением Pb2+ , T1+ ионов приведены в таблицах 1-35 и 1-36.
Таблица 1-35 Раствор борогидрида калия с добавлением Pb2+
| Решение 1 | Решение 1 | ||
|---|---|---|---|
| Цианид золота с калием | 5 г/л | Коллоидный | 2 г/л |
| Цианид калия | 8 г/л | Решение 2 | |
| Цитрат натрия | 50 г/л | Борогидрид калия | 200 г/л |
| ЭДТА | 5 г/л | Гидроксид натрия | 120 г/л |
| Хлорид свинца | 0,5 г/л | ||
Таблица 1-36 Раствор борогидрида калия для металлизации с добавлением T1+
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Цианид золота с калием | Отрегулируйте по мере необходимости | Борогидрид калия | 5. 4 ~ 10. 8 г/л |
| Цианид калия | 6,5 г/л | Температура | 70 〜 80℃ |
| Гидроксид калия | 11,2 г/л | Скорость нанесения покрытия | <10 мкм/ч |
| Сульфат таллия | 5 〜 100 мг/л |
Au(CN)4– + 2e– → Au(CN)2– + 2CN– (1-12)
![Рисунок 1-39 Влияние добавления хлорида свинца на поляризационную кривую реакции восстановления Au(CN)2- [вращающийся золотой электрод, KAu(CN)2 0. 009моль/л, KOH 0. 2моль/л].](https://sobling.jewelry/wp-content/uploads/2025/11/Page_61_docsmall.com_副本-768x578.jpg)
Рисунок 1-39 Влияние добавления хлорида свинца на Au(CN)2--поляризационная кривая реакции восстановления [Вращающийся золотой электрод, KAu(CN)2 0. 009моль/л, KOH 0. 2моль/л]
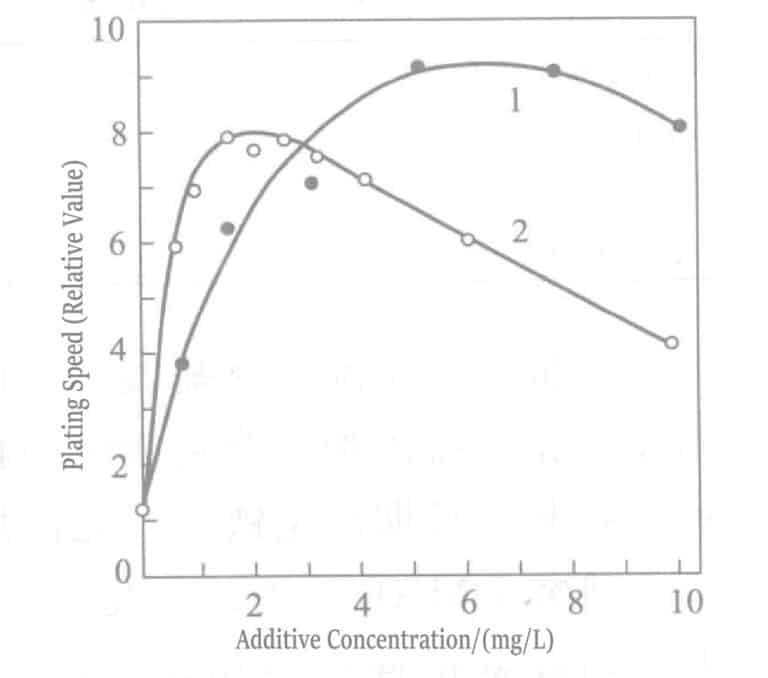
Рисунок 1-40 Влияние концентрации хлорида таллия (кривая 1) и хлорида свинца (кривая 2) на скорость золотого покрытия в растворе борогидрида калия
- b. Добавление стабилизаторов. Добавление органических стабилизаторов, снижающих каталитическую активность золота, повышение температуры раствора для нанесения покрытия и изменение концентрации восстановителя может повысить скорость нанесения покрытия. Например, скорость нанесения покрытия в растворах, содержащих аминоуксусную кислоту, гидроксиэтилэтилендиаминтетрауксусную кислоту, диазотриуксусную кислоту или производные янтарной кислоты, может достигать высокой скорости 12~23 мкм/ч при 90℃. Однако при высоких температурах реакция гидролиза восстановителя значительно ускоряется, что затрудняет контроль над раствором для нанесения покрытия. Добавление следовых количеств стабилизатора п-диметиламиноазобензола не влияет на стабильность гальванического раствора и может увеличить обычную концентрацию BH4- в 2 раза, повышая скорость гальванического покрытия до 5 мкм/ч. Другие эффективные стабилизаторы включают этиленгликоль. Этиловый эфир, диэтиленгликоль? этиловый эфир и полиэтиленимин.
- c. Используйте комплексные соли цианида трехвалентного золота. Растворы для гальванического покрытия с комплексными солями цианида трехвалентного золота, например, с добавлением хлорида свинца или хлорида титана, как показано в таблице 1-33, подробно описаны в таблице 1-37.
Таблица 1-37 Цианид калия золота(III) Борогидрид калия Раствор для металлизации
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Золото(III) калия | 3 г/л | Хлорид свинца | 0. 5 мг/л |
| Гидроксид калия | 11,2 г/л | Температура | 70℃ |
| Борогидрид калия | 3 г/л |
Преимущество комплексного солевого раствора цианида трехвалентного золота заключается в том, что KAuO2 и KAu(OH)4 могут использоваться в качестве дополнительных добавок к солям золота, предотвращая чрезмерное накопление свободных цианид-ионов в гальваническом растворе, снижая скорость гальванического покрытия и способствуя долгосрочной стабильной скорости гальванического покрытия. Скорость нанесения покрытия в растворе без добавок составляет 2~8 мкм/ч.
Исследование электрохимического поведения, структуры и свойств гальванического раствора DMAB показало, что подобно гальваническому раствору борогидрида калия, KAu(CN)2 используется только при приготовлении раствора для золотого покрытия, а растворенный гидроксид золота в растворе гидроксида калия добавляется в качестве добавки, чтобы избежать накопления свободных цианид-ионов. Состав раствора для нанесения покрытия приведен в таблице 1-38.
Таблица 1-38 Раствор для нанесения покрытия DMAB (гидроксид золота, растворенный в растворе гидроксида калия)
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Цианид золота с калием | 0,013 ~ 0,018 ммоль/л | Добавка | Небольшое количество |
| DMAB | 0,07 〜 0,1 моль/л | pH | 13.1 ~ 13.4 |
| Гидроксид калия | 0,09 〜 0,15 ммоль/л | Температура | 70 〜 75℃ |
| Цианид калия | 0,007 ~ 0,01 ммоль/л | Скорость нанесения покрытия | 2 мкм/ч |
(5) Повышение стабильности раствора для гальванического покрытия.
Использование добавок может увеличить скорость нанесения покрытия и стабильность раствора, но образующиеся примеси приведут к разложению раствора.
Такие вещества, как ЭДТА и этаноламин, добавляемые в гальванический раствор, образуют прочные комплексные ионы с ионами металлических примесей, ингибируя реакцию между металлическими примесями и BH4– и BH3OH–Таким образом, повышается стабильность гальванического раствора. Состав раствора борогидрида калия с добавлением ЭДТА и этаноламина приведен в таблице 1-39.
Таблица 1-39 Раствор борогидрида калия для металлизации с добавлением ЭДТА и этаноламина
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Цианид золота с калием | 1,45 г/л | ЭДТА | 5 г/л |
| Цианид калия | 11 г/л | Этаноламин | 50 мл/л |
| Гидроксид калия | 11,2 г/л | Температура | 72℃ |
| Борогидрид калия | 10,8 г/л | Скорость нанесения покрытия | 1. 5 мкм/ч |
Таблица 1-40 Раствор для металлизации с двумя восстановителями (гидразин и DMAB)
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Цианид золота с калием | 0. 005моль/л | DMAB | 0. 05моль/л |
| Цианид калия | 0. 035моль/л | Гидразин | 0. 25моль/л |
| Гидроксид калия | 0. 8моль/л | Температура | 80℃ |
| Карбонат калия | 0. 45моль/л | Скорость нанесения покрытия на никелевый базовый слой (начальная стадия) | 2. 6 мкм/ч |
| Ацетат свинца | 15X10-6 | На золото (фиксированная стоимость) | 7. 8 мкм/ч |
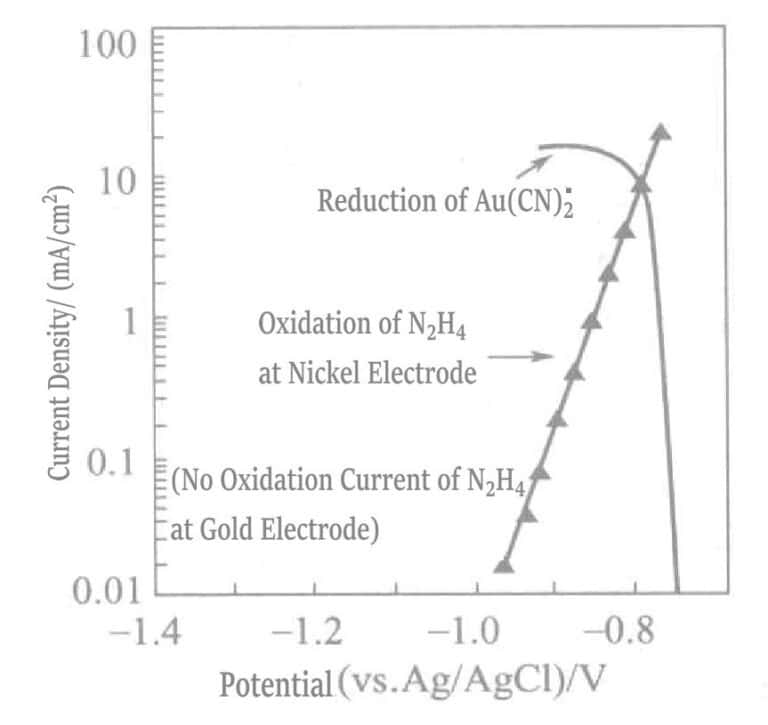
Рис. 1-41 Поляризационные кривые реакции анодного окисления гидразина на никелевом электроде и реакции катодного восстановления Au(CN)2-.
(KOH 0. 8моль/л, KCN 0. 035моль/л, N2H4 0. 05моль/л, 80℃)
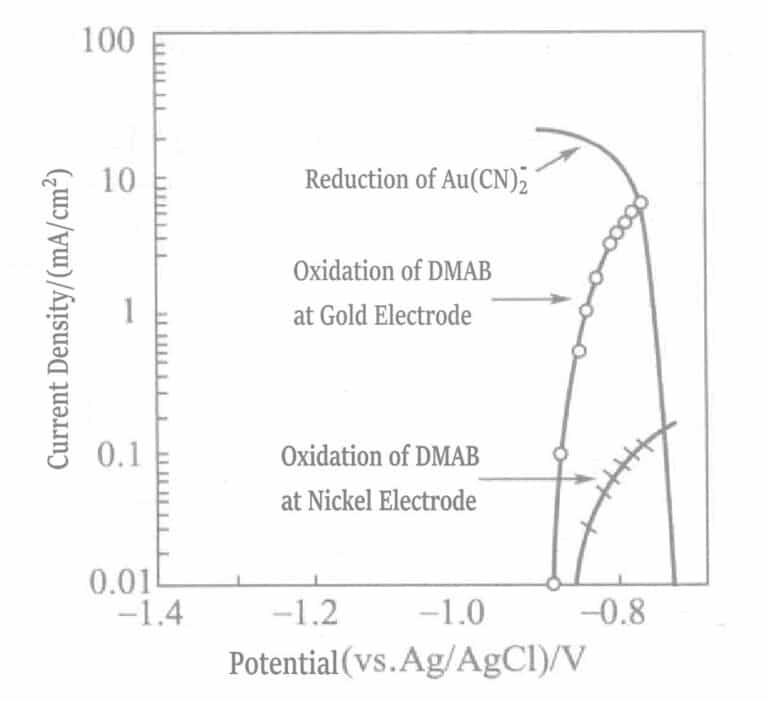
Рис. 1-42 Поляризационные кривые реакции анодного окисления DMAB на никелевом и золотом электродах и реакции катодного восстановления Au(CN)2-
(KOH 0. 8моль/л, KCN 0. 035моль/л, DMAB 0. 05моль/л, 80℃)
В гальваническом растворе, содержащем только восстановитель гидразин, золото может осаждаться исключительно за счет каталитического эффекта никелевого базового слоя. Когда базовый слой полностью покрывается золотом, осаждение золота прекращается, и в этот момент толщина слоя золотого покрытия зависит от концентрации свободного цианида в гальваническом растворе. Несмотря на то, что максимальная толщина покрытия в этом растворе ограничена (около 2 мкм), слой покрытия получается достаточно плотным, чтобы соответствовать требованиям, предъявляемым к ключевым соединениям под давлением.
Кроме гидразина, в растворе для каталитического золочения материала имеется множество других доступных восстановителей; см. табл. 1-41.
Таблица 1-41 Другие растворы для гальванического покрытия с восстановителем
| Редуцирующий агент | pH | Температура/℃ |
|---|---|---|
| Гипофосфит | 7 〜 7. 5 | 93 |
| 7. 5 〜 13. 5 | 96 | |
| 3 〜 4 | 70 〜 80 | |
| Гидразин | 7 〜 7. 5 | 92 〜 95 |
| 5. 8 〜 5. 9 | 95 | |
| 11. 7 | 95 | |
| Гидроксиламин | 2. 3 〜 2. 8 | 70 〜 85 |
| Цианоборогидрид натрия (NaBH3CN) | 3.5 | 90 |
| Гидразинилборан (N2H4 ・ BH3) | >13 | 60 |
| Тиомочевина | 6. 5 〜 7. 0 | 83 〜 90 |
| 4.2 | 80 ~ 85 | |
| Аскорбиновая кислота | 8 | 63 |
| Трихлорид титана | 5 | 75 |
Копирайт @ Sobling.Jewelry - Пользовательские ювелирные изделия производителя, OEM и ODM ювелирный завод
5. Химическое покрытие золотым сплавом
(1) Золото-серебряный сплав:
Химическое покрытие сплавом золото-серебро может быть достигнуто путем непрерывного добавления раствора цианистого калия в раствор борогидрида золота. Ag(CN)2– восстанавливается легче, чем Au(CN)2–. При приготовлении нового гальванического раствора серебро выпадет в осадок первым, если смешать эти два вещества, и сплав нельзя будет гальванизировать.
При непрерывном добавлении небольшого количества цианистого серебра калия по каплям в раствор для нанесения покрытия, поддерживая относительно низкий уровень конденсации [молярное соотношение Au:Ag (26:10~(26:0.5)], можно осадить слой покрытия из сплава золото-серебро с содержанием серебра 80%~20%. В этом гальваническом растворе осаждение серебра является продуктом реакции замещения золота, которое осаждается первым, и Ag(CN)2–, в растворе.
(2) Золото-медный сплав:
В обычном химическом растворе для меднения на основе ЭДТА и формальдегидного восстановителя только цианистый калий может покрыть сплав золота с медью. Изменяя концентрацию цианистого золота с калием, можно регулировать массовую долю меди в покрывающем слое золотого сплава в пределах 1%~94%.
(3) Золото-оловянный сплав:
Для химического покрытия золота и оловянных сплавов используется раствор SnCl2 метод восстановителя. Состав и диапазон концентраций раствора для нанесения покрытия приведены в таблице 1-42.
Таблица 1-42 Раствор для нанесения покрытия из сплава золото-олово
| Состав и условия эксплуатации | Параметры | Состав и условия эксплуатации | Параметры |
|---|---|---|---|
| Цианид золота(III) калия | 4〜10 г/л | Триолефин | 0. 05 ~ 0. 5 г/л |
| Цианид калия | 5〜15 г/л | Температура | Комнатная температура |
| Гидроксид калия | 60〜100 г/л | Скорость нанесения покрытия | 1,5 мкм/ч (без добавления триолефина) |
| Хлорид калия | 40〜60 г/л | 5 мкм/ч (добавление триолефина 0,5 г/л) |
(4) Золото-индиевый сплав:
Раствор для нанесения покрытия из золото-индиевого сплава готовится путем добавления Ih2(SO4)3 и ЭДТА в раствор борогидрида. Содержание индия в слое покрытия составляет 1%~4%. При комнатной температуре тонкий слой покрытия из сплава золота и индия, нанесенный на активированный палладием n-GaAs, после термообработки при температуре 350℃ имеет контактное сопротивление, превосходящее сопротивление чистого золота.
(5) Золото-никелевые, золото-кобальтовые сплавы:
Уэмаки разработал растворы для гальванических покрытий из сплавов золота-никеля и золота-кобальта 18~22K. pH 3~5, слой гальванического покрытия из цианистого химического раствора золота с добавлением восстановителя гипофосфита натрия имеет физические свойства, такие как твердость и износостойкость, уступающие свойствам гальванических слоев из сплавов золота, содержащих никель и кобальт.
Раздел II Безцианидное химическое золотое покрытие
1. Обзор
При золочении вытеснительного типа в качестве движущей силы реакции покрытия используется разность потенциалов между потенциалом окисления металла основного слоя и потенциалом восстановления ионов золота. В отличие от этого, химическое золочение восстановительного типа использует разность потенциалов между потенциалом окисления восстановителя и потенциалом восстановления ионов золота в качестве движущей силы реакции покрытия.
Электроны, участвующие в реакции восстановления ионов золота, обеспечиваются либо за счет реакции окисления металла основного слоя (вытесняющее золотое покрытие), либо за счет реакции окисления восстанавливающего агента (восстановительное золотое покрытие).
Другие методы включают: ① Добавление солей тяжелых металлов в вытесняющий раствор для золотого покрытия, при этом поверхность металла базового слоя адсорбирует тяжелые металлы, смещая потенциал в направлении, облегчающем восстановление ионов золота; ② Добавление восстановителя в вытесняющий раствор для золотого покрытия, что позволяет окислительно-восстановительным реакциям происходить одновременно для нанесения более толстого слоя золота; ③ В растворах для золотого покрытия, содержащих восстановители, благородный металл базового слоя действует как восстановитель и подвергается окислению с помощью катализатора, осуществляя каталитическое химическое золотое покрытие базового слоя.
В качестве лигандов в растворах для химического золочения обычно используется цианид, который образует очень устойчивые комплексы с ионами золота (константа устойчивости K=4×1028). В настоящее время многие полупроводниковые компоненты перешли на использование почти нейтральных, малоцианистых или бесцианистых растворов для золотого покрытия, таких как сульфитные или тиосульфатные растворы для золотого покрытия и бесцианистые химические растворы для золотого покрытия с тиоловыми лигандами серии RSH.
2. Химическое золотое покрытие вытесняющего типа
Как правило, прочность связи между толстослойным электролитическим золотым покрытием восстановленного типа и основным слоем цветных металлов относительно низкая. Поэтому перед нанесением толстого слоя золота необходимо выполнить электролитическое золочение со смещением.
В растворе для золотого покрытия вытесняющего типа основной металл базового слоя растворяется (окисляется) в растворе электролита, высвобождая электроны. Ионы золота в растворе, напротив, принимают электроны и осаждаются (восстанавливаются) на неметаллической поверхности. Образование золотых лигандов снижает концентрацию ионов золота в растворе, сдвигая восстановительный потенциал в отрицательном направлении, как показано в таблице 1-43.
Таблица 1-43 Лиганды и восстановительные потенциалы ионных комплексов золота
| Лиганды | Лиганд | Д/В |
|---|---|---|
| H2O |
Au(H2O)2+ Au(H2O)43+ |
1.68 1.50 |
| Cl- |
AuCl2 - AuCl4 - |
1.15 0.92 |
| SCN- |
Au(SCN)2 - Au(SCN)4 - |
0.67 0.64 |
| I- |
AuI2- AuI4- |
0.58 0.57 |
| NH3 | Au(NH)43+ | 0.56 |
| OH- | Au(OH)4 - | 0.48 |
| Тиомочевина | Au(Thu)2+ | 0.38 |
| S2O32- | Au(S2O3)23- | 0.15 |
| SO32- | Au(SO3)23- | 0.06 |
| R-SH | Au(R-S)2- | -0. 3 〜 - 0. 5 |
| CN- | Au(CN)2 - | -0.65 |
Таблица 1-43 показывает, что помимо цианидов, другие лиганды, такие как тиолы, сульфиты и тиосульфаты, также могут образовывать устойчивые комплексы с ионами золота и демонстрировать отрицательные потенциалы.
В растворе для вытеснения золота сульфитной системой, кроме сульфитных ионов, могут быть использованы лиганды, такие как полиаминополикарбоновые кислоты и их соли, водорастворимые амины, соли аминов, соли триацетата этилендиамина, стабилизаторы, такие как соли тетраалкиламмония, тетра(метиленфосфонат) этилендиамина, сахара и тиоловые соединения. Концентрация ионов аммония, хлорид-ионов, сульфат-ионов, бромид-ионов или йодид-ионов должна поддерживаться в определенном диапазоне и не быть слишком высокой; в противном случае в гальваническом растворе могут образоваться аммонийные (комплексные)-золотые лиганды, окислительно-восстановительный потенциал которых более положителен, чем у сульфита натрия. Если гальванический раствор стоит или находится в процессе золочения, сульфит натрия может окислять и восстанавливать золото, вызывая нестабильность гальванического раствора.
Сукцинат тиола, ацетилцистеин, цистеин и другие соединения тиолового ряда и ионы золота могут образовывать стабильные лиганды в растворах для золочения, не содержащих цианидов. Сукцинат тиола [HOOCCH(SH)-CH2COOH] и восстановительный потенциал лиганда иона золота, то есть Au(HOOCCHSCH2COOH)2– + e– ⇌Au(s) + 2 ( HOOCCH - SCH2COOH)–Поэтому правильное значение стандартного электродного потенциала для реакции получить сложно. Измеренный потенциал восстановления раствора для осаждения составляет около -0,3~0,5 В. Тиоловый сукцинатный лиганд золота существует в форме [Au(HOOC - CHSCH2COOH)2]–, с золотом в состоянии окисления +1.
HAuCl4 + 3H2O → Au(OH)3 + 4HCl (1-13)
Au(OH)3 + 4[HOOCCH(SH)CH2 COOH] → [Au(HOOCCH-S-CH2COOH)4 ]– + 3H2O+H+ (1-14)
[Au( HOOCCH-S-CH2COOH)4]– → [Au(HOOCCH-S-CH2COOH)2]– + HOOCH2ЧОК-ЧОК-ЧОК-ЧОК2COOH (1-15)
Таблица 1-44 Безцианидный раствор для вытесняющего золотого покрытия
| Состав и условия эксплуатации | Сульфитная система | Система меркаптосукциновой кислоты | ||
|---|---|---|---|---|
| Хлорат золота натрия/(моль/л) | 0.05 | |||
| Тиосульфат натрия/(моль/л) | 0.028 | 0.015 | ||
| Меркаптосукцинат золота/(моль/л) | 0.01 | |||
| Сульфит натрия/(моль/л) | 0.52 | 0.1 | ||
| Меркаптосукциновая кислота/(моль/л) | 0.25 | 0.25 | ||
| Цитрат натрия/(моль/л) | 0.22 | |||
| Ацетилцистеин/(моль/л) | 0.03 | |||
| Тетраметиламмоний хлорид/(моль/л) | 0.8 | |||
| ЭДТА/ (моль/л) | 0.015 | |||
| ЭДТА - 2Na/(моль/л) | 0.02 | |||
| Аминотрис(метиленфосфоновая кислота)/(моль/л) | 0.1 | |||
| Карбоксиметилцеллюлоза натрия/(г/л) | 10 | |||
| pH | 7.0 | 7.0 | 1,5 (корректируется соляной ) | 7.0 |
| Температура /℃ | 60 | 85 | 80 ~ 90 | |
3. Химический толстый слой золотого покрытия восстановленного типа
В растворах для золотого покрытия с тиосульфатом в качестве лиганда сульфит натрия предотвращает разложение тиосульфат-ионов. В NaAuCl4 В растворах, содержащих соли трехвалентного золота, моновалентное золото восстанавливается под действием избытка тиосульфата. В слабощелочные растворы для золотого покрытия обычно добавляют буферы pH, такие как хлорид аммония, тетраборат натрия и борная кислота.
Тиоловые соединения могут образовывать с ионами золота лиганды, которые обладают отличной стабильностью и действуют как восстановители. К таким тиоловым соединениям относятся, в частности, L-цистеин и 2-этанамин тиола. В таблице 1-45 приведены состав и условия работы нецианистых растворов для химического золотого покрытия восстановленного типа с использованием тиосульфата натрия и тиоловых соединений в качестве лигандов.
Таблица 1-45 Безцианидный раствор для золотого покрытия восстановительного типа
| Состав и условия эксплуатации | Тиосульфатная система | Тиоловая система | |||
|---|---|---|---|---|---|
| Хлорат золота/(г/л) | 0.01 | ||||
| Натрий золотохлористый/(г/л) | 0.0125 | 0.0125 | |||
| Сульфит золота натрия/(г/л) | 0.02 | ||||
| Меркаптосукцинат золота/(г/л) | 0.01 | ||||
| Меркаптосукциновая кислота/(г/л) | 0.27 | ||||
| Тиосульфат натрия/(г/л) | 0.1 | 0.17 | 0.1 | ||
| Сульфит натрия/(г/л) | 0.1 | 0.4 | |||
| Сульфит аммония/(г/л) | 0.43 | ||||
| ЭДТА ・ 2Na/(г/л) | 0.19 | ||||
| Триэтаноламин/(г/л) | 0.034 | ||||
| Хлорид аммония/(г/л) | 0.05 | ||||
| Тетраборат натрия/(г/л) | 0.13 | ||||
| Дигидрогенфосфат калия/(г/л) | 0.15 | ||||
| Тиомочевина/(г/л) | 0.0033 | ||||
| Гидрохинон/(г/л) | 0.002 | ||||
| Аскорбиновая кислота/(г/л) | 0.25 | ||||
| Гидразин/(г/л) | 0.3 | ||||
| L-цистеин/(г/л) | 0.08 | ||||
| 2-аминоэтилмеркаптан/(г/л) | 0.2 | ||||
| Бензотриазол калия/(г/л) | 0.05 | ||||
| pH | 7.5 | 7.0 | 8.0 | 7.0 | 7.5 |
| Температура/℃ | 60 | 80 | 70 | 80 | 80 |
4. Каталитическое химическое золотое покрытие базового слоя
Каталитическое химическое золотое покрытие базового слоя - это метод химического золотого покрытия восстановительного типа с использованием восстановителя. Восстанавливающий агент обладает каталитической активностью только на поверхности подложки, слоя основного металла (никеля), и не обладает каталитической активностью на поверхности осажденного золота. Слой каталитического химического золотого покрытия более гладкий, плотный и имеет меньше или меньше пор, чем слой золотого покрытия вытесняющего типа.
В растворах тиосульфата и сульфита для химического золочения золото может быть осаждено на никелевую поверхность без добавления других восстановителей. На поверхности никеля сульфит восстанавливает только тиосульфатный комплекс золота и не действует на поверхность золота, поэтому такой способ химического золочения называется каталитическим. Одновременно на поверхности базового никелевого слоя происходит реакция смещения золотого покрытия. Таким образом, восстановитель сульфит проходит различные реакции окисления под влиянием состава основного никелированного слоя и условий предварительной обработки. Концентрация тиосульфатного лиганда натрия или pH гальванического раствора влияет на различные соотношения реакций вытеснения и восстановления, максимальную толщину слоя золотого покрытия, внешний вид, пористость и адгезию, поэтому необходимо выбрать подходящий состав гальванического раствора и условия золотого покрытия.
5. Стабильность безцианидного химического раствора для золотого покрытия
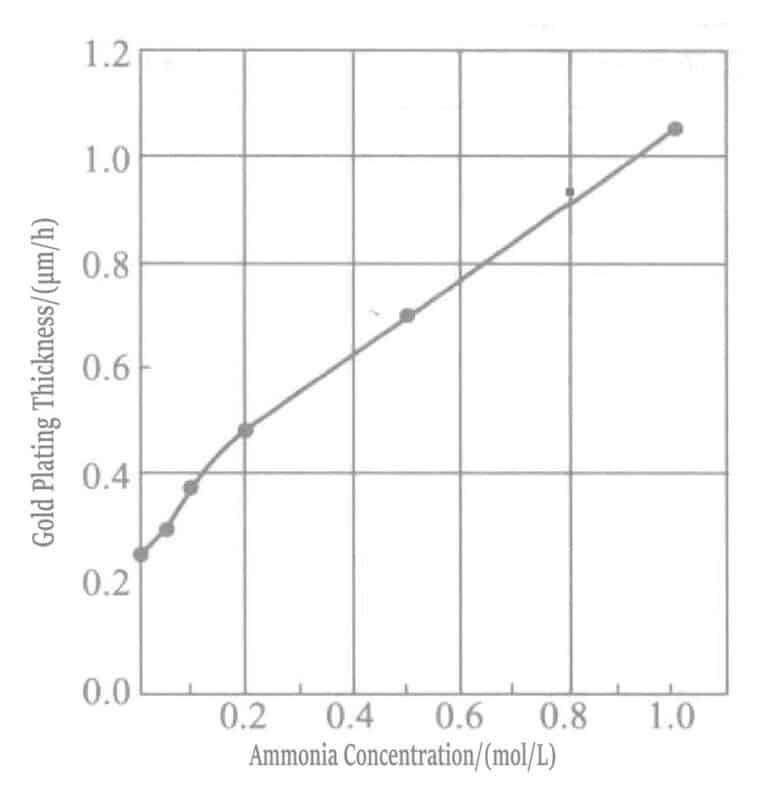
Увеличение концентрации аммиачной воды ускоряет скорость осаждения слоя золотого покрытия. В растворах с высокой концентрацией аммиака меркаптосукцинат выступает в качестве восстановителя, и реакция восстановления протекает одновременно с реакцией вытеснения.
Загрязнение ионами меди или железа является основной причиной нестабильности нецианистых растворов для химического золочения. Медь, растворенная в порах никелевого слоя, и железо из подложки легко способствуют нестабильности раствора для химического золочения.
Причины: ① Ионы золота принимают электроны, высвобождающиеся при окислении этих металлов, увеличивая скорость восстановления. ② Ионы меди или железа катализируют реакцию окисления сульфита или тиола, ускоряя скорость реакции, что вызывает дефекты на поверхности слоя химического золотого покрытия и снижает производительность сварки и прочность соединения. В растворах для химического золочения растворение и загрязнение этих металлов следует подавлять путем добавления лигандов, образующих устойчивые комплексы с этими растворенными и загрязненными ионами металлов.
6. Не содержащий цианидов химический раствор для золотого покрытия
(1) Соли тетрахлороаурата (III) и слабовосстанавливающие амин-борановые растворы для золотого покрытия
Соли тетрахлороаурата (III) (NaAuCl4) легко восстанавливаются до золота. Эфирно-замещенные борановые восстановители третичных аминов можно использовать с NaAuCl4 для формирования раствора автокаталитического покрытия, или восстановители, такие как триметиламинобораны, метилморфолинобораны и диизопропиламинобораны, вместе со стабилизаторами, такими как тиолы и йодистые соединения.
(2) Раствор для золотого покрытия с сульфитной солью золота:
В настоящее время используется большое количество моновалентных сульфитных растворов золота, в которых в качестве восстановителей используются гипофосфиты, формальдегид, гидразин, тетрагидроборат и DMAB. Золотосульфитная соль [Na3Au(SO3)2] нестабилен в воде и требует добавления стабилизаторов, таких как 1,2-диаминоэтан и бромид калия.
(3) Тиосульфатный раствор для золотого покрытия
① Раствор для золотого покрытия с тиомочевиной и ее производными в качестве восстановителей:
Комбинация моновалентного тиосульфата золота и раствора для нанесения покрытия из тиомочевины обладает хорошей стабильностью, не выделяет водородный газ при нейтральном pH и не имеет пористости. Состав раствора для нанесения покрытия приведен в таблице 1-46 (раствор для нанесения покрытия A).
Таблица 1-46 Тиосульфатный раствор для золотого покрытия
| Состав и условия эксплуатации | Раствор для нанесения покрытия A | Раствор для нанесения покрытия B |
|---|---|---|
| NaAuCl4 / (моль/л) | 0.1 | 0.0125 |
| Na2S2O3/(моль/л) | 0.08 | 0.1 |
| Na2SO3 /(моль/л) | 0.4 | 0.1 |
| Na2B4O7/ (моль/л) | 0.1 | - |
| NH4Cl/(моль/л) | - | 0.05 |
| Тиомочевина/(моль/л) | 0.1 | - |
| L-аскорбат натрия/(моль/л) | - | 0.25 |
| pH | 9.0 | 6.0 |
| Температура/℃ | 80 | 60 |
| Скорость нанесения покрытия/(мкм/ч) | 1. 9 〜 2. 3 | 1. 5 〜 2. 0 |
② Раствор для золотого покрытия с аскорбиновой кислотой в качестве восстановителя:
В тиосульфатном гальваническом растворе с L-аскорбиновой кислотой натрия в качестве восстановителя присутствует сульфит натрия, который может стабильно покрывать золото. Состав раствора для нанесения покрытия приведен в таблице 1-46 (раствор для нанесения покрытия B).
Эффективными восстановителями в растворах тиосульфата натрия, помимо тиомочевины и аскорбата натрия, являются тартрат натрия, гликолевая кислота и гипофосфорная кислота.
③ Механизм реакции тиосульфатного раствора:
Соль золота реагирует с тиосульфатом с образованием Au(S2O3)23-. Когда в растворе нет тиосульфата, присутствует только сульфит и образуется Au(SO3)23-. Уравнение реакции выглядит следующим образом:
Au3++ 2S2O3 2- + H2O ⇌ Au(S2O3)23- + SO4 2- + 2H+ (1-16)
Au3+ + 3SO32- + H2O ⇌ Au(SO3 )23- + SO42- + 2H+ (1-17)
Au+ + 2SO32- ⇌ Au(SO3)23- K=1010 (1-18)
Au+ + 2S2O32- ⇌ Au(S2O3)23- K = 1026 (1-19)

Рисунок 1-44 Сравнение катодных поляризационных кривых реакций осаждения золота в сульфитных и тиосульфатных растворах
(NH4Cl 0. 1моль/л, Na2SO3 0. 2моль/л)
Тиосульфат обладает более сильной комплексообразующей способностью с моновалентным золотом, чем сульфит, поэтому моновалентное золото труднее осадить из растворов, содержащих тиосульфат натрия, чем из растворов, содержащих сульфит.
В растворе сульфитного золотого покрытия с восстановителем аскорбатом из-за разницы в катодных поляризационных кривых между комплексными ионами сульфита золота и комплексными ионами тиосульфата золота скорость осаждения золота составляет лишь 1/10 от скорости осаждения в растворе тиосульфата натрия. На рис. 1-45 показаны катодные и анодные поляризационные кривые аскорбат-сульфита и тиосульфата золота.
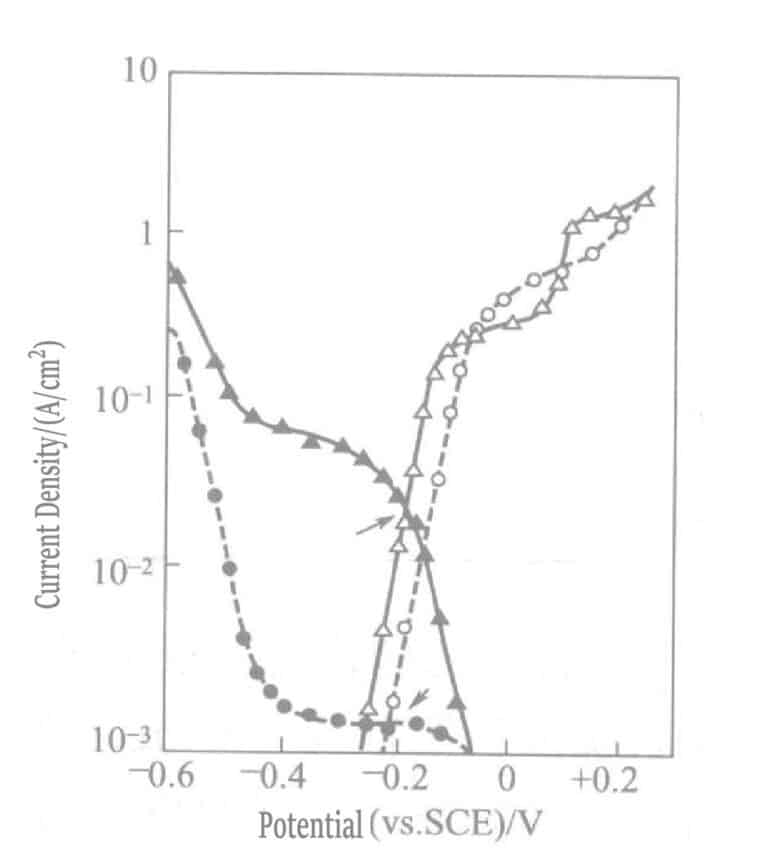
Рисунок 1-45 Катодные и анодные поляризационные кривые аскорбиновой кислоты, сульфитного раствора и тиосульфата золота
(золотой электрод, NH4Cl 0. 1mol/L, pH 6. 0, 60℃. Кривая "●" раствор для нанесения покрытия: Na2SO3 0,2 моль/л и NaAuCl4 0,01моль/л; кривая "▴" - тот же раствор для нанесения, что и раньше, с добавлением Na2S2O3 0. 1моль/л; Кривая "○" раствор для нанесения покрытия: Na2SO3 0. 2моль/л и аскорбат натрия 0. лмоль/л; Кривая "△", раствор, как и ранее, с добавлением Na2S2O3 0,1 ммоль/л)
Принцип реакции тиосульфатного раствора для электроосаждения золота зависит от степени окисления восстановителя, и местные реакции протекают следующим образом.
Катодная реакция:
Au(S2O3)23- + 2e– → Au + 2S2O32- (1-20)
Анодная реакция:
Раствор для нанесения тиомочевины
CS(NH2)2 + 5H2O → CO(NH2)2 + H2SO4 + 8H+ + 8e– (1-21)
Продукт реакции CO(NH2)2 это мочевина.
Раствор аскорбиновой кислоты
C6H8O6 → C6H6O6 + 2H+ + 2e–
7. Раствор для золотого покрытия с добавлением сахара и сульфитной соли золота
После добавления сахаристых соединений в раствор сульфита золота он может оставаться стабильным в течение длительного времени, а слой золотого покрытия получается хорошим. Состав раствора для нанесения покрытия следующий.
Соли сульфита золота: сульфит золота калия, сульфит золота натрия, сульфит золота аммония и др.
Сульфиты: сульфит калия, сульфит натрия, сульфит аммония и др.
Корректор pH: Отрегулируйте pH 6~9 с помощью различных буферов.
Стабилизаторы: водорастворимые аминные соединения, этилендиамин, диэтилентриамин, триэтилентетрамин и т.д.; водорастворимые аминокислоты или соли, этилендиаминтетрауксусная кислота, триэтилентетрамин гексауксусная кислота, транс-1,2-циклогександиаминтетрауксусная кислота или соли и т.д.; водорастворимые органофосфаты или соли, аминотрис(метиленфосфоновая кислота), 1-гидроксиэтилиден-1,1-дифосфоновая кислота, этилендиаминтетра(метиленфосфоновая кислота), диэтаноламин, пентакис(метиленфосфоновая кислота) или соли и др.Также могут быть добавлены водорастворимые ароматические нитросоединения, такие как моно-, ди- и три-нитробензоловая кислота, моно- и ди-нитросалициловая кислота, нитробензол дикарбоновая кислота, моно-, ди- и три-нитрофенол, динитроаминофенол, моно-, ди- и три-нитробензол и др.
К сахарам, помимо крахмала, также можно отнести гексозы, глюкозу, маннозу, галактозу и другие моносахариды, эритрит, пентитол, гексанол и другие сахарные спирты, глюкаровую и другие альдаровые кислоты, глюконовую, гексатоновую и другие альдоновые кислоты, олигосахариды и т.д. Эти соединения сахара могут повысить стабильность раствора для нанесения покрытия и расширить диапазон плотности тока в зоне яркого покрытия.
Результаты нанесения покрытия приведены в таблице 1-47.
Таблица 1-47 Различные сульфитные ванны для золотого покрытия, условия эксплуатации и влияние добавок
| Серийный номер | Различные сульфитные ванны для золотого покрытия и условия эксплуатации | Аддитивный эффект |
|---|---|---|
| No. 1 |
Золото сульфит натрия 10 г/л Сульфит натрия 65 г/л Цитрат тринатрия 65 г/л Этилендиаминтетраметиленфосфоновая кислота (EDTMP) 85 г/л pH 7 Температура 60℃ Общий ток 0,2A Подложка для образцов: сплав 42Fe-Ni Метод идеальной плотности тока с сильным перемешиванием |
Электролиз 1080 ℃, гальванический раствор разлагается, образуя черные частицы. Появление гальванического слоя при различных плотностях тока приводит к образованию пятен и ожогов. |
| No.1 Добавьте карбоксиметилцеллюлозу натрия (КМЦ) 10 г/л в раствор для нанесения покрытия. Остальные условия те же, что и для №1 | Электроосаждение 1740℃, разложение гальванического раствора, черные частицы. Внешний вид слоя покрытия улучшен, а пятна и ожоги явно уменьшены. | |
| No. 2 |
Золото сульфит натрия 10 г/л Сульфит натрия 130 г/л Цитрат тринатрия 65 г/л Цитрат триаммония 65 г/л п-Нитро(бензол)фенол 1 г/л pH 7 Температура 40℃ Общий ток 0,2A Подложка для образцов: медь Сильное перемешивание |
Сгорели участки с высокой плотностью тока, внешний вид слоя покрытия очень плохой, появляются диффузные пятна |
| Раствор для нанесения покрытия №2 с крахмалом 5 г/л, остальные условия такие же, как у №2. | Отсутствие горения в области высокой плотности тока, хороший внешний вид слоя покрытия в широком диапазоне плотности тока, стабильный раствор для нанесения покрытия. | |
| No. 3 |
Сульфит золота натрия 10 г/л Сульфит натрия 100 г/л Борат натрия 50 г/л Борная кислота 100 г/л п-Нитро(бензол)фенол 1 г/л pH 7 Температура 40℃ Общий ток 0,2A Подложка для образцов: медь Сильное перемешивание |
Плохой внешний вид слоя покрытия |
| Добавьте 5 г/л крахмала в раствор для осаждения №3, остальные условия такие же, как у №3. | Хороший внешний вид слоя покрытия в широком диапазоне плотности тока, стабильный раствор для нанесения покрытия. | |
| No. 4 |
Сульфит золота натрия 12 г/л Сульфит натрия 100 г/л Фосфит 3 г/л Этилендиамингидрат 30 г/л pH 7 Температура 60°C Общий ток 0,2A Подложка для образцов: сплав 42Fe-Ni Сильное перемешивание |
Сгоревшая область с высокой плотностью тока, внешний вид слоя покрытия очень плохой |
| No.4 добавьте крахмал 5 г/л в раствор для нанесения покрытия, остальные условия такие же, как у No.4. | Хороший внешний вид гальванического слоя и стабильность гальванического раствора в широком диапазоне плотности тока. | |












