Co to jest pozłacanie chemiczne i jak działa?
Złocenie chemiczne: Techniki, rozwiązania i zastosowania w jubilerstwie
Wprowadzenie:
Czym jest pozłacanie chemiczne? Jest to proces osadzania cienkiej warstwy złota na różnych materiałach, poprawiający ich wygląd i trwałość. Jak to działa? Złocenie chemiczne polega na stosowaniu specjalnych roztworów z jonami złota i środkami redukującymi. Tradycyjne metody często wykorzystują cyjanek, ale istnieją również opcje wolne od cyjanku. Dlaczego warto wybrać złocenie chemiczne? Oferuje jednolite, wysokiej jakości wykończenie, które idealnie nadaje się do biżuterii i innych przedmiotów dekoracyjnych. Niezależnie od tego, czy jesteś producentem biżuterii, projektantem czy sprzedawcą detalicznym, zrozumienie tych technik może podnieść jakość Twoich produktów.

Spis treści
Sekcja I Złocenie chemiczne cyjankiem
1. Przegląd
Wraz z wysoką gęstością komponentów elektronicznych, złożonością projektowania linii, mikrofabrykacją obwodów i niezależnością właściwości elektrycznych, chemiczne złocenie, które rozwiązuje złożoność procesu powlekania, stało się nieuniknionym sposobem złocenia. Złocenie chemiczne ma jednak następujące wady:
① Wolna prędkość;
② Wąskie warunki użytkowania i zakres działania, zwiększające trudności w zarządzaniu;
③ Powierzchnia materiału musi być dokładnie czysta;
④ Żywotność roztworu galwanicznego jest krótka (podatność na reakcje samoodtleniania);
⑤ Grubość powłoki jest bardzo wrażliwa na warunki mieszania.
Dlatego też, chemiczne złocenie musi być przeprowadzane przy użyciu specjalnego sprzętu. Powszechnie stosowany skład roztworu do chemicznego powlekania złotem przedstawiono w tabeli 1-24, przygotowany przez połączenie różnych soli koordynacyjnych złota i środków redukujących.
Tabela 1-24 Rodzaje soli koordynacyjnych złota i środków redukujących w roztworze do chemicznego powlekania złotem
| Środek redukujący | KAu(CN)2 | KAu(CN)4 | Na3Au(SO2)2 | HAuCl4 - 3H2O | HAuCl4 ・ 3H2O | AuCN | KAu(CN)4 | KAu ・ O2 | KAu(OH)4 | AuI | Nie określono |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Hipofosforyn sodu | 57,58 | 71 | 77 | ||||||||
| Formaldehyd | 71 | 78 | |||||||||
| Biazyd | 59 | 71 | 76 | 78 | |||||||
| Borohydryd | 60,61 | 72 | 78 | 79 | |||||||
| Metyloboran | 60 | 69 | 74 | 75 | 79 | 80 | |||||
| Hydroksyloamina | 62 | ||||||||||
| Niepublikowane | 63 | 73 | 81 | ||||||||
| Tiomocznik | 64 | ||||||||||
| Wodorotlenek amonu | 65 | ||||||||||
| Winian sodowo-potasowy czterowodny (połączony) | 66 | 70 | |||||||||
| N,N-dimetyloamid | 82 | ||||||||||
| N,N-dimetyloglicyna | 67 | ||||||||||
| Brak | 68 |
Tabela 1-25 Funkcje składników w roztworze do chemicznego powlekania złotem
| Komponent | Cel | Nazwa związku |
|---|---|---|
| Złoty jon | Dostawa metalicznego złota | KAu(CN)2、KAu(CN)4、AUCN、 Na3Au(SO2)2. HAuCl4 - 3H2O、KAu ・ O2 |
| Środek redukujący | Środki redukujące do osadzania złota | Czterowodny winian sodowo-potasowy, borohydryt, aminoboran, formaldehyd, podfosforyn, N,N-dimetyloglicyna, kwas askorbinowy |
| Organiczne czynniki chelatujące | Działanie buforowe zapobiegające szybkiemu osadzaniu się złota | EDTA, cytrynian potasu, kwas winowy |
| Stabilizator | Maskowanie aktywnych jąder, aby zapobiec rozkładowi roztworu galwanicznego | Tiomocznik, cyjanek metalu, acetyloaceton |
| Aktywator | Spowalniający efekt moderującego czynnika chelatującego | Kwas bursztynowy |
| Czynnik buforujący | Utrzymanie określonego pH | Fosforany, cytryniany, winiany |
| Środek powierzchniowo czynny | Łatwość zwilżania powlekanych części | Sulfoniany alifatyczne, siarczany alkoholi |
2. Hipofosforynowy roztwór do powlekania złotem
Gdy metal podstawowy i złoto w roztworze galwanicznym ulegają reakcji wypierania, metal o niższym potencjale elektrochemicznym jonizuje się łatwiej niż złoto. Podczas reakcji, gdy powierzchnia metalu nieszlachetnego zostanie całkowicie pokryta złotem, reakcja natychmiast się zatrzymuje, więc można uzyskać tylko cienką warstwę złota o grubości 0,1 ~ 0,3 μm. Ten roztwór galwaniczny lub roztwór Brookshire'a jest starym roztworem galwanicznym i jest podstawowym składem obecnie sprzedawanych chemicznych roztworów do powlekania złotem. Charakterystyka roztworu galwanicznego: warstwa bazowa do złocenia musi być niklowa dla reakcji wypierania; złoto nie może być wypierane na materiale miedzianym.
(1) Skład i warunki stosowania chemicznego roztworu do złocenia z podfosforynem
Tabela 1-26 przedstawia typowy skład chemicznego roztworu do złocenia z podfosforynem.
Tabela 1-26 Skład i warunki stosowania roztworu do pozłacania chemicznego z hipofosforynem
| Skład i warunki pracy | Numer seryjny | ||||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | |
| Cyjanek złota potasu/(g/L) | 2 | 2 | 20 | 2 | 2 |
| Hipofosforyn sodu/(g/L) | 10 | 10 | 10 | 10 | 10 |
| Cyjanek potasu /(g/L) | 0.2 | 0.2 | 80 | 0.4 ① | 0.2 |
| Temperatura/°C | 96 | 96 | 96 | 96 | 96 |
| pH | 13.5 | 7.5 | 13.5 | 13.5 | 7.1 |
| Szybkość obciążenia/(cm2/cm3) | 0.25 | 0.25 | 0.25 | 0.25 | 0.25 |
| Szybkość powlekania/[mg/(cm2- h)] | 9.8 | 9.85 | 12.3 | 8.2 | 3.86 |
(2) Wpływ niklu na szybkość osadzania roztworu do powlekania podfosforynem
W chemicznym roztworze do powlekania złotem z podfosforynem jako środkiem redukującym, aktywne jony metali (Ni2+). Metal (nikiel) i złoto osadzają się w śladowych ilościach na powierzchni powlekanych części, tworząc dużą chemiczną siłę napędową i zwiększając prędkość powlekania złotem. Zasadę działania przedstawiono na schemacie modelu na rysunku 1-25.
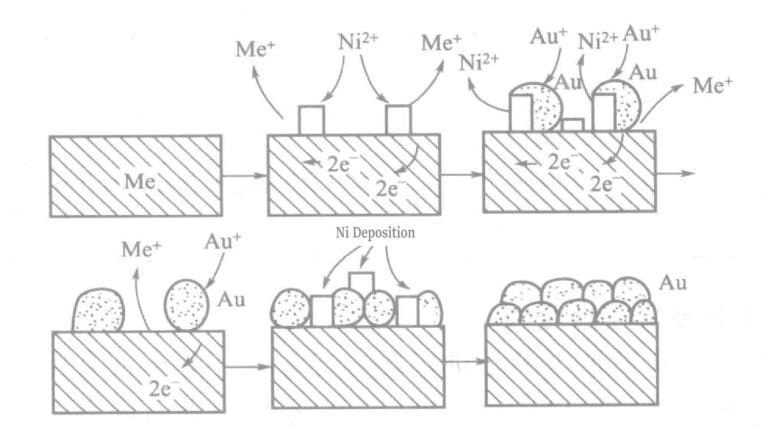
Tabela 1-27 Skład i warunki pracy roztworu do powlekania złotem hipofosforynowym
| Skład i warunki pracy | I | II | Skład i warunki pracy | I | II |
|---|---|---|---|---|---|
| Cyjanek złota potasu/(g/L) | 2, 5, 7 | 2, 5, 7 | Cyjanek potasu /(g/L) | - | 2 |
| Cytrynian sodu/(g/l) | 75 | 75 | H2NNH2 - H2O /(g/L) | - | 2 |
| Podfosforyn sodu/(g/L) | 15 | 15 | pH | 8.5 | 4.3 |
| EDTA-2Na/(g/L) | - | - | Temperatura/℃ | 70, 90 | 70, 90 |
| Chlorek sodu/(g/L) | - | 5 |
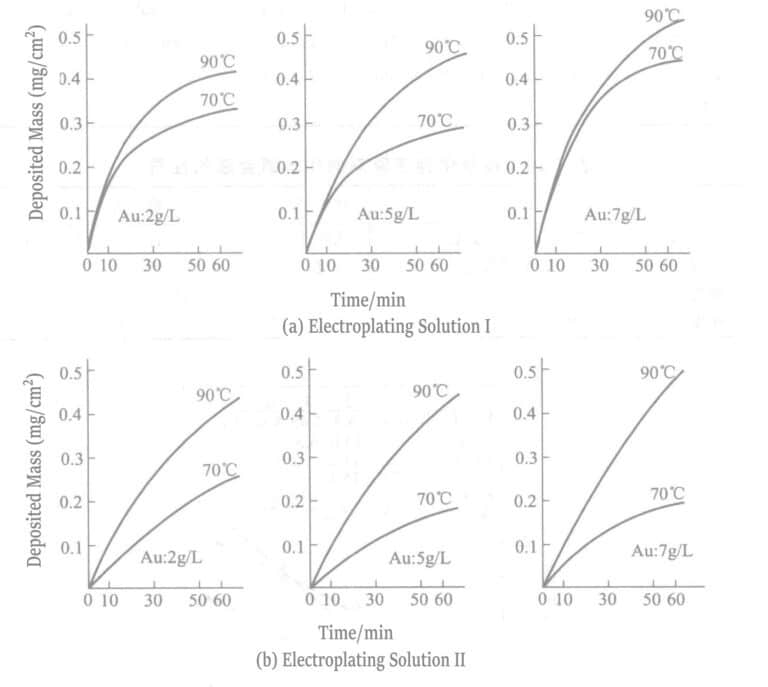
3. Roztwór do powlekania solą boro-wodorkową
(1) Skład i właściwości chemicznego roztworu do złocenia borowodorku potasu
W 1969 r. Okinaka i in. zaproponowali zastosowanie roztworu galwanicznego ze związkami boro-wodorkowymi jako środkiem redukującym. Skład i warunki boro-wodorkowego chemicznego roztworu do powlekania złotem przedstawiono w tabelach 1-28, a właściwości warstw złota powlekanych tymi roztworami przedstawiono w tabelach 1-29. Grubość warstw galwanicznych pokrytych w różnym czasie różnymi roztworami galwanicznymi pokazano na rysunku 1-27. Podsumowanie wyników stosowania środków redukujących borohydryku potasu i boranu dimetyloaminy przedstawiono w tabeli 1-30.
Tabela 1-28 Skład i warunki pracy chemicznego roztworu do powlekania złotem boro-wodorku potasu
| Skład i działanie | Numer seryjny | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| Cyjanek złota potasu/(g/L) | 0. 02mol/L(5.8g/L) | 0. 03mol/L(8.6g/L) | 0. 005mol/L(1.45g/L) |
| Cyjanek potasu | 0. 2mol/L(13.0g/L) | 0. 2mol/L(13.0g/L) | 0. lmol/L (6.5g/L) |
| Wodorotlenek potasu | 0. 2mol/L(11.2g/L) | 0. 2mol/L(22.4g/L) | 0. 2mol/L(11.2g/L) |
| Dwuwodnik potasu | 0. 4mol/L(21.6g/L) | 0. 8mol/L(43.1g/L) | 0. 2mol/L(10.8g/L) |
| Temperatura/°C | 75 | 75 | 75 |
Tabela 1-29 Właściwości chemicznego roztworu do złocenia z czynnikiem redukującym boro-wodorkiem potasu
| Natura | Dane | Natura | Dane |
|---|---|---|---|
| Siła wiązania | Doskonała siła wiązania warstwy metalu | Porowatość | Brak porów większych niż 1 μm na jednolitej powierzchni |
| Wygląd | Matowy żółty | Czystość | 99. 9% |
| Gęstość | Zawartość złota 19. 3g/cm3 | Wartość rezystancji | 0. 03Ω/cm2 (Au: 1 μm) |
| Twardość | Twardość Nup 60〜80 | Lutowność | Doskonały |
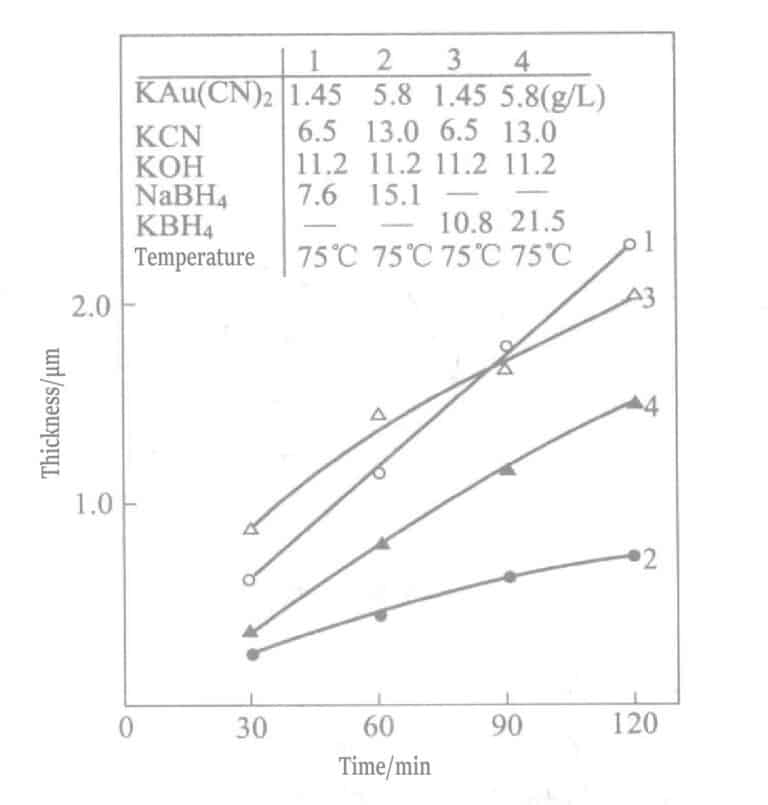
Tabela 1-30 Funkcje składników w chemicznym roztworze do pozłacania boro-wodorku potasu
| Czynniki wpływające | Roztwór galwaniczny boro-wodorku potasu | Roztwór galwaniczny DMAB (dimetyloaminoboran) |
|---|---|---|
| Wpływ stężenia złota | Gdy stężenie złota osiągnie 0,002 mol/l, szybkość wytrącania gwałtownie wzrasta i spada powyżej tej wartości. | Szybkość wytrącania wzrasta liniowo przy stężeniu złota 0,01 mol/l, ale nie ma wpływu powyżej tej wartości. |
| Skutki cyjanku potasu |
Niestabilny roztwór galwaniczny poniżej 0,005 mol/l. Złoto nie wytrąca się powyżej 0,2 mol/l. |
Tak samo jak po lewej |
| Wpływ borohydryku potasu | BH nie jest stabilny w temperaturze pokojowej. Dodanie wodorotlenku potasu poprawia stabilność kąpieli, a szybkość wytrącania maleje wraz ze wzrostem stężenia. | DMAB jest stabilny w temperaturze pokojowej, szybkość wytrącania wzrasta wraz ze wzrostem wodorotlenku potasu. |
| Stężenie czynnika redukującego | Wzrost szybkości opadów wraz ze wzrostem stężenia | |
| Wpływ temperatury kąpieli galwanicznej | Zwiększyć szybkość opadów o 10 ℃ i rozłożyć w temperaturze 85 ℃. |
(2) Wpływ prędkości powlekania i jonów metali ciężkich
Dodanie śladowych ilości jonów metali ciężkich (ołowiu, talu itp.) do roztworu do chemicznego powlekania złotem znacznie zwiększa szybkość osadzania. Mcintyre wyjaśnił ten efekt w następujący sposób. Ze względu na niski potencjał osadzania, efekt katalityczny zaadsorbowanych atomów ołowiu, jak pokazano w mechanizmach (1-4) i (1-5), sprzyja zarodkowaniu.
Pb2+ + 2e- → Pbreklama (1-4)
2Au(CN)2- + Pbreklama → 2Au + Pb2+ + 4CN- (1-5)
Ze względu na dużą różnicę funkcji pracy między miedzią, materiałami złotymi i jonami ołowiu, ołów jest redukowany i osadzany przy potencjale bardziej dodatnim niż termodynamiczny potencjał redoks, tworząc monowarstwę. Ze względu na katalityczną reakcję zaadsorbowanych atomów ołowiu, jak w (1-4) i (1-5), ) reakcja redukcji Au(CN) zachodzi szybko, skutecznie promując osadzanie złota.
Zależność między stężeniem ołowiu a szybkością osadzania w roztworze do powlekania złotem redukującym borohydryd potasu przedstawiono na rysunku 1-28, a skład roztworu do powlekania przedstawiono w tabeli 1-31. Ołów jest dodawany w postaci azotanu ołowiu. Rysunek 1-28 pokazuje, że stężenie dodatku ołowiu w roztworze galwanicznym może wynosić tylko około 20 ml/l, a dodanie większej ilości nie ma żadnego wpływu.
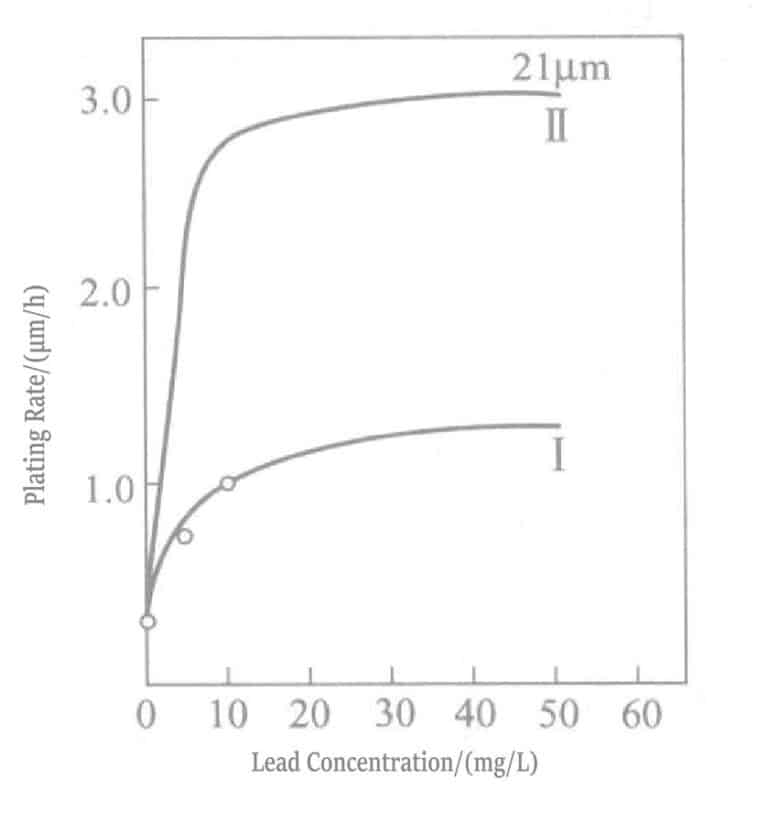
Tabela 1-31 Skład i warunki pracy roztworu do powlekania złotem boro-wodorku potasu
| Skład i warunki pracy | I | II | Skład i warunki pracy | I | II |
|---|---|---|---|---|---|
| Cyjanek złota potasu/(g/L) | 2 | 2 | Cyjanek potasu /(g/L) | 10 | 10 |
| Dwuwodzian potasu/(g/L) | 2 | 10 | EDTA-2Na/(g/L) | 5 | 5 |
| Cyjanek potasu/(mg/L) | 5 | 5 | Temperatura roztworu galwanicznego/°C | 75 | 75 |
Tabela 1-32 Skład roztworu do powlekania złotem BMAB
| Skład i warunki pracy | Koncentracja | Skład i warunki pracy | Koncentracja |
|---|---|---|---|
| Cyjanek złota potasu/(g/L) | 2 | Cyjanek potasu /(g/L) | 30 |
| BMAB/(g/L) | 10 | EDTA-2Na/(g/L) | 5 |
| Cyjanek potasu/(mg/L) | 5 | рH | 13.6 |
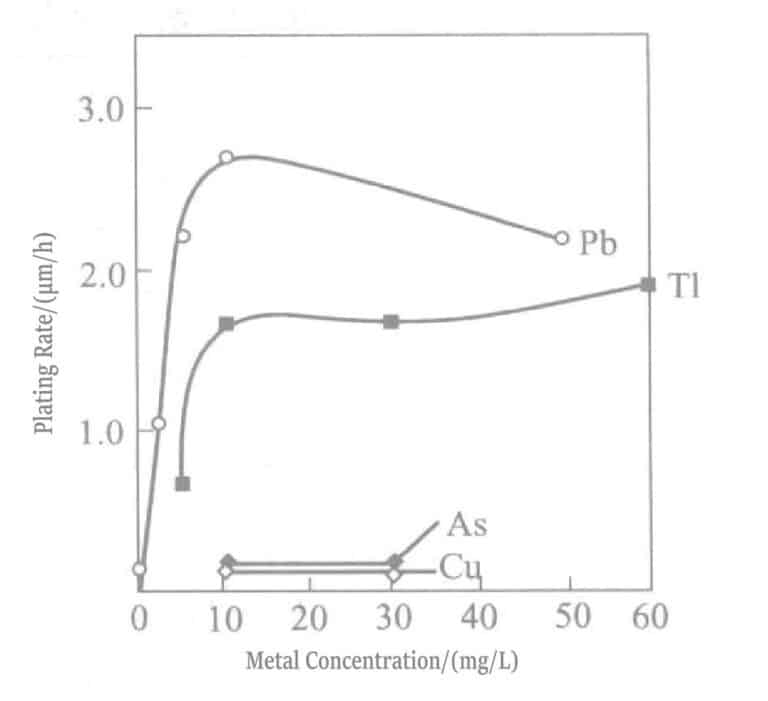
Tabela 1-33 Skład chemicznego roztworu cyjanku złota(III) potasu do powlekania złotem
| Skład | Parametry | Skład | Parametry |
|---|---|---|---|
| KAu(CN)4/(g/l) | 4 | KOH/(mg/L) | 11.2 |
| KBH4/(g/l) | 3 | Temperatura/℃ | 70 |
| PbCl2/(mg/L) | 0.5 |
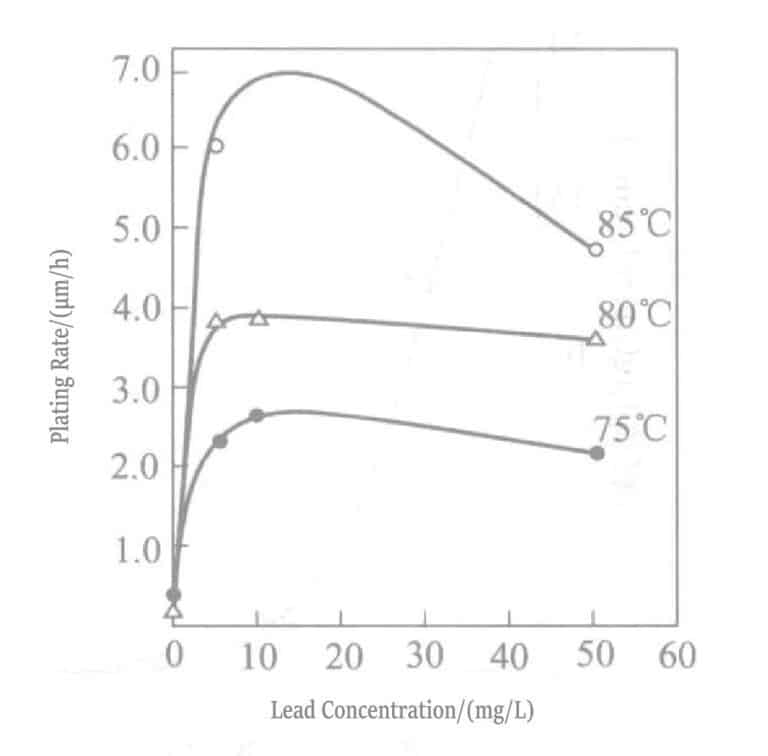
Rysunek 1-30 Wpływ temperatury i stężenia ołowiu na szybkość wytrącania złota
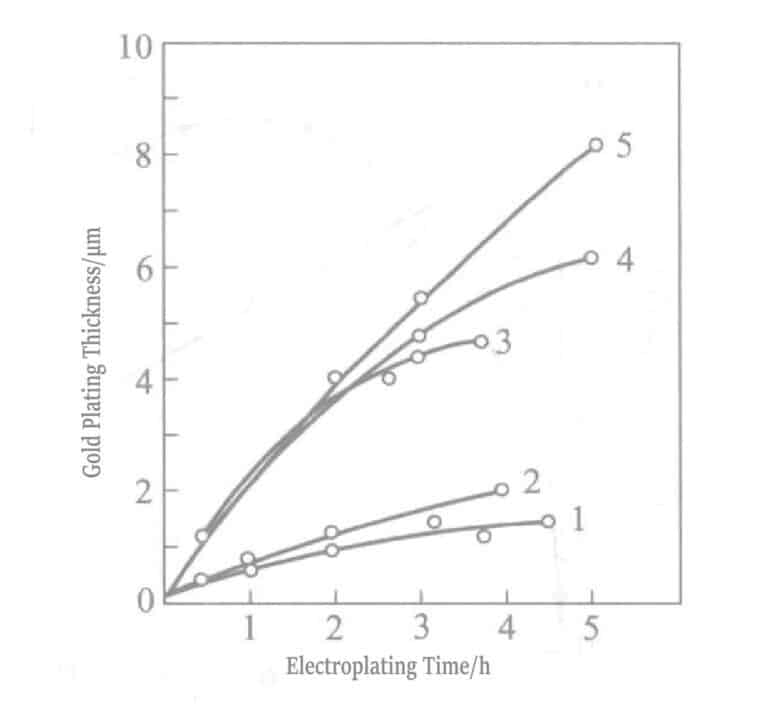
Rysunek 1-31 Zależność między czasem powlekania a grubością pozłacanej warstwy
1 - Brak mieszania Au+ ciecz; 2 - Brak mieszania Au3+ ciecz; 3 - mieszanie Au3+ płyn; 4 - Uzupełnianie Au3+ płyn; oraz 5 - Odnawianie Au3+ płyn
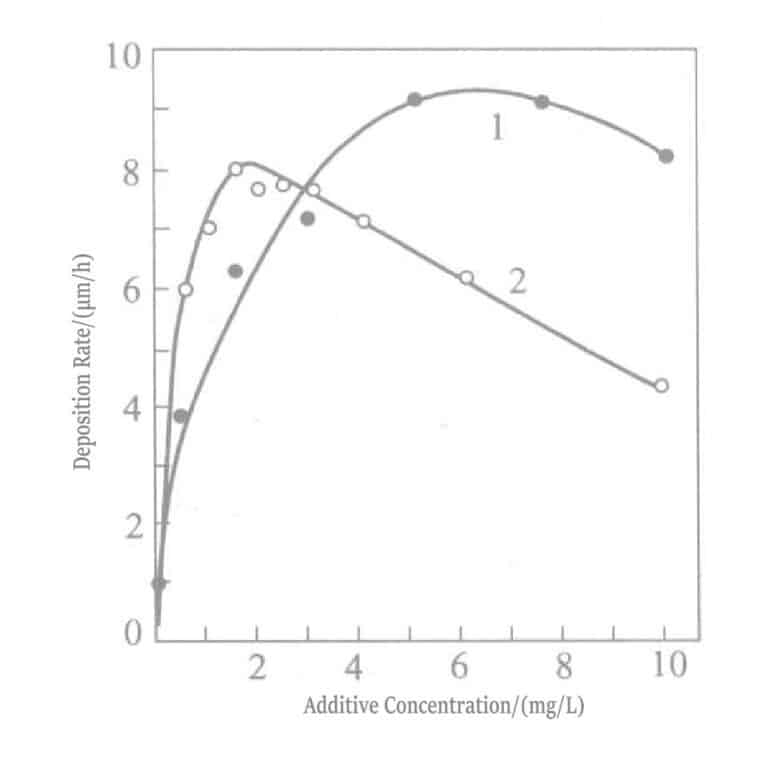
Rysunek 1-32 Wpływ dodanych stężeń ołowiu i talu na szybkość powlekania złotem
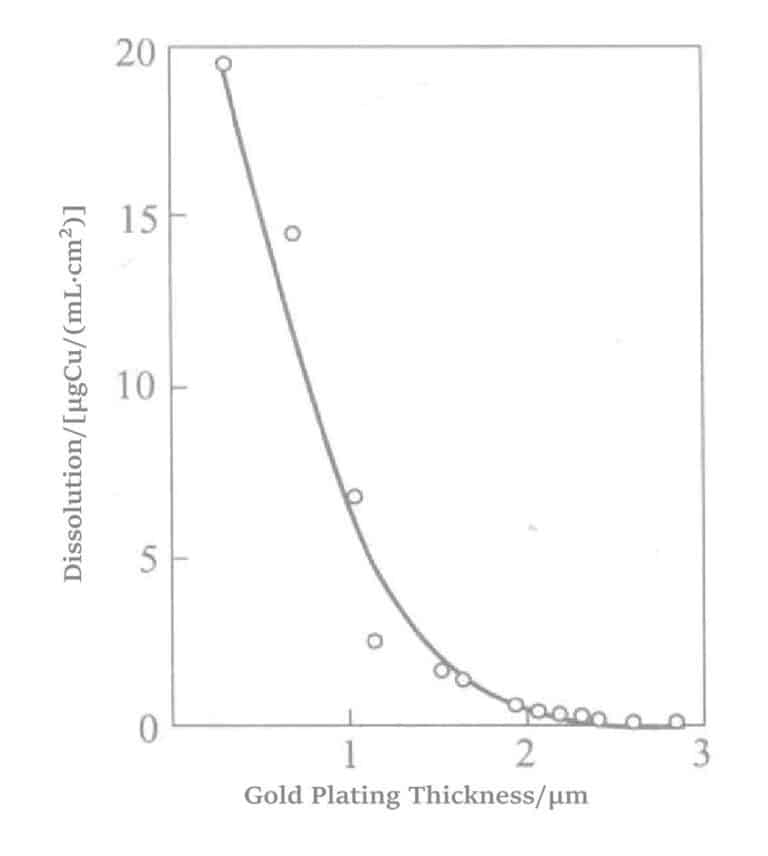
Rysunek 1-33 Porowatość warstwy złocenia bezprądowego
Proces chemicznego złocenia krystalizowanego szkła (SiO2 46% + Al2O3 16% + MgO 17% + K2O 10% + F 4% + B2O3 7% ) przedstawiono na rysunku 1-34.
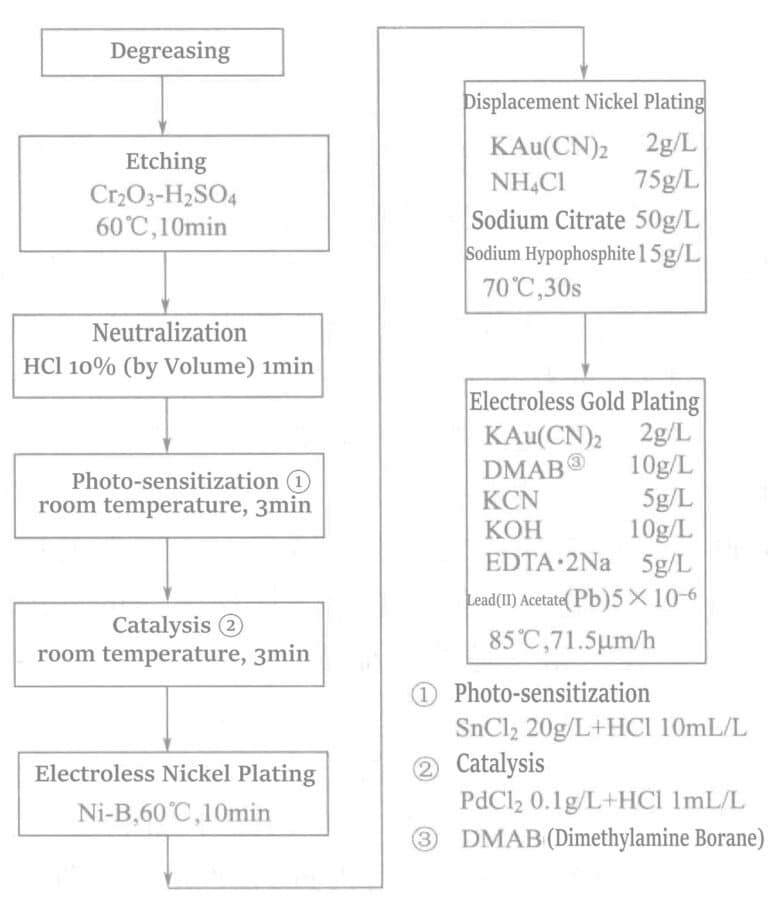
4. Mechanizm reakcji chemicznego roztworu soli boro-wodorkowej do powlekania złotem
Lin Zhongfu i in. zaproponowali, że roztwory do powlekania złotem borohydryku potasu i DMAB (dimetyloaminoboranu) w tabeli 1-34 mogą stać się praktycznymi roztworami do powlekania złotem po dodaniu stabilizatorów.
(1) Skład dwóch roztworów galwanicznych: Tabela 1-34 przedstawia dwa składy.
Tabela 1-34 Roztwory do powlekania chemicznego boro-wodorku potasu i DMAB
| Skład roztworu galwanicznego | Roztwór galwaniczny borohydryku potasu | Roztwór galwaniczny DMAB |
|---|---|---|
| Cyjanek złota potasu/(mol/l) | 0.02 | 0.02 |
| Cyjanek potasu/(mol/l) | 0.2 | 0.02 |
| Wodorotlenek potasu/(mol/l) | 0.2 | 0.8 |
| Dwuwodzian potasu/(mol/l) | 0.4 | - |
| DMAB/(mol/L) | - | 0.4 |
| Temperatura/°C | 75 | 85 |
| Prędkość powlekania/(μm/h) | 0.7 | 0.4 |
(2) Mechanizm reakcji: W roztworze boro-wodorku potasu do powlekania złotem, BH4- sam w sobie nie wywołuje efektu redukującego, ale pośredni BH3OH- produktu hydrolizy BO2- działa jako czynnik redukujący.
BH4- + H2O → BH3OH-+ H2 (1-6)
BH3OH- + H2O → BO2- + 3H2 (1-7)
BH3OH- + 3OH- → BO2- + 3/2 H2 + 2H2O + 3e- (1-8)
Au(CN)2- + e- → Au + 2CN- (1-9)
BH3OH- + 3Au(CN)2- + 3OH- → BO2- + 3/2 H2 + 2H2O + 3Au + 6CN - (1-10)
Reakcje hydrolizy równań (1-6) i (1-7) analizowano za pomocą polarografii. Wynik pokazuje, że reakcja (1-7) jest 500 razy szybsza niż reakcja (1-6). Dlatego stopień wykorzystania borohydryku potasu w reakcji powlekania złotem jest bardzo niski. W typowych warunkach galwanizacji efektywny stopień wykorzystania nie przekracza 2%~3%, przy czym większość środka redukującego pozostaje nieskuteczna z powodu hydrolizy.
Powyższa reakcja hydrolizy przebiega szybko przy niskim pH (reakcja katalizowana kwasem), a szybkość osadzania złota jest szybka, gdy stężenie wodorotlenku potasu jest niskie. Aby zapobiec naturalnemu rozkładowi roztworu do powlekania złotem, stężenie wodorotlenku potasu musi być utrzymywane na poziomie co najmniej powyżej 0,1 mol/l. Zależność między szybkością osadzania złota a stężeniem wodorotlenku potasu przedstawiono na rysunku 1-35.
![Figure 1-35 Curve of plating rate variation with potassium hydroxide concentration [KAu(CN)2 0.02 mol/L, KCN (solid line) 0.2 mol/L, KCN (dashed line) 0.1 mol/L, 80 °C]](https://sobling.jewelry/wp-content/uploads/2025/11/Page_58_docsmall.com_副本-768x801.jpg)
Rysunek 1-35 Krzywa zmian szybkości powlekania w zależności od stężenia wodorotlenku potasu
[KAu(CN)2 0,02 mol/l, KCN (linia ciągła) 0,2 mol/l, KCN (linia przerywana) 0,1 mol/l, 80 °C].
![Figure 1-36 Effect of potassium hydroxide concentration on the plating rate of DMAB plating solution, DMAB [KAu(CN)2 0.02mol/L, KCN 0.2mol/L, DMAB 0.4mol/L, 75℃]](https://sobling.jewelry/wp-content/uploads/2025/11/Page_58_docsmall.com_副本1-768x560.jpg)
Rysunek 1-36 Wpływ stężenia wodorotlenku potasu na szybkość powlekania roztworu do powlekania DMAB, DMAB
[KAu(CN)2 0.02mol/L, KCN 0.2mol/L, DMAB 0.4mol/L, 75℃].
(CH3)2New Hampshire2 - BH3 + OH- → (CH3)2New Hampshire2 + BH3OH- (1-11)
(3) Problemy z roztworem do powlekania boro-wodorkiem potasu i roztworem do powlekania DMAB
Rysunek 1-37 pokazuje, że szybkość powlekania zmienia się wraz ze stężeniem jonów miedzi i niklu w roztworze do powlekania. Gdy stężenie jonów niklu wynosi 10-5mol/L, szybkość galwanizacji zaczyna spadać, a gdy stężenie jonów niklu osiąga 10-3mol/L, roztwór galwaniczny ulega rozkładowi. Jony miedzi nie mają prawie żadnego wpływu na szybkość powlekania. Na początkowym etapie powlekania złotem jony złota i niklu ulegają reakcji wypierania, śladowe ilości jonów niklu rozpuszczają się, a szybkość powlekania spada.

Rysunek 1-37 Wpływ jonów miedzi i niklu na szybkość powlekania
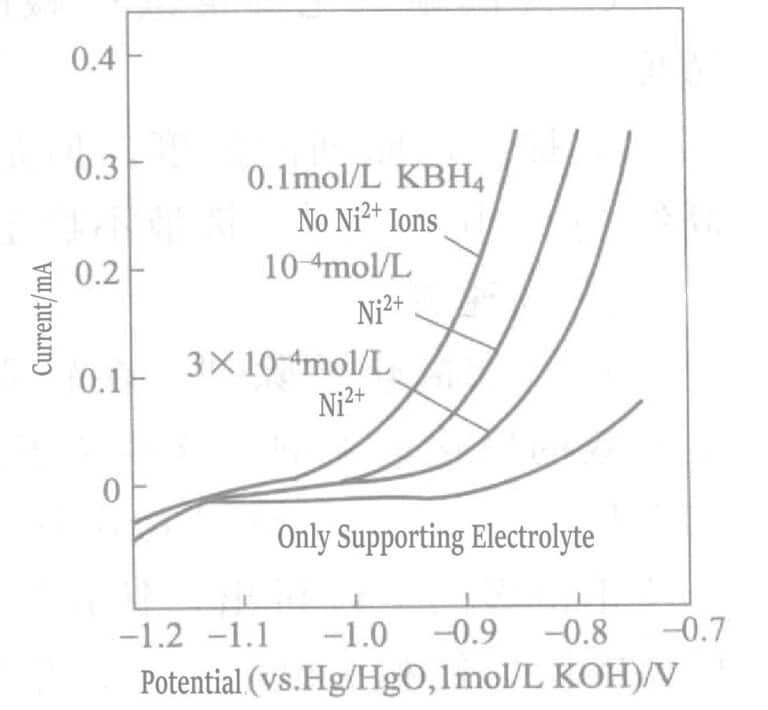
Rysunek 1-38 Wpływ śladowych jonów niklu na anodowy prąd utleniania BH3OH
(Złota elektroda rotacyjna, 2000r/min, 75℃, KOH 0,2mol/L, KCN 0,1mol/L)
Wpływ dodania śladowych ilości jonów niklu na BH3OH- anodowego prądu utleniania pokazano na rysunku 1-38. Dodatek śladowych jonów niklu znacząco hamuje reakcję utleniania czynnika redukującego BH3OH- na złotej obrotowej anodzie dyskowej. Dzieje się tak, ponieważ jony niklu występują w postaci soli ligandu cyjankowego Ni(CN)42- , a ten jon kompleksowy preferencyjnie adsorbuje się na powierzchni złota, utrudniając jego osadzanie.
Niestabilne warstwy bazowe (takie jak azotek glinu) nie mogą wykorzystywać silnie alkalicznych roztworów. pH roztworu galwanicznego zależy od rodzaju środka redukującego, co jest największą wadą roztworów galwanicznych borohydryku potasu i DMAB.
W odniesieniu do powyższych kwestii, z wyjątkiem tego, że nie można zmienić pH roztworu galwanicznego, można poprawić inne aspekty.
(4) Ulepszony roztwór do powlekania złotem boro-wodorku potasu i roztwór do powlekania złotem DMAB
① Zwiększenie prędkości galwanizacji
- a. Zmiana podstawowego składu roztworu galwanicznego i warunków pracy w celu zwiększenia szybkości galwanizacji.
- b. Zwiększyć prędkość mieszania.
- c. Zwiększyć temperaturę roztworu galwanicznego.
- d. Zmniejszenie stężenia wolnego cyjanku.
- e. Zmniejszyć stężenie alkaliów w roztworze do powlekania borohydryku potasu i zwiększyć stężenie alkaliów w roztworze do powlekania DMAB.
- f. Zwiększenie stężenia środka redukującego. Jednakże, gdy szybkość powlekania bez specjalnych dodatków wzrasta o około 2 μm/h lub więcej, roztwór do powlekania staje się niestabilny i podatny na rozkład.
② Roztwór do szybkiego galwanizowania
- a. Dodać eliminatory polaryzacji. W miękkich roztworach do powlekania złotem, Pb2+ , T1+ są skutecznymi eliminatorami polaryzacji. Jony te silnie adsorbują się na powierzchni złota, powodując tak zwane zjawisko UPD (under potential deposition), w którym ołów osadza się przy potencjale znacznie bardziej dodatnim niż Pb2+ / Pb, a tal osadza się na potencjale bardziej dodatnim niż T1+ /T1. Osadzony ołów, tal i Au(CN)2- ulega reakcji wypierania, powodując przesunięcie reakcji osadzania złota do bardziej dodatniego potencjału (osłabienie polaryzacji). Z drugiej strony, dodanie tych jonów do chemicznych roztworów złota, podobnie jak w przypadku powlekania elektrolitycznego, przesuwa Au(CN)2- potencjał redukcji w kierunku dodatnim, co skutkuje zwiększoną szybkością galwanizacji, która może osiągnąć około 10 μm/h. Roztwory galwaniczne z dodatkiem Pb2+ , T1+ przedstawiono w tabelach 1-35 i 1-36.
Tabela 1-35 Roztwór do powlekania boro-wodorkiem potasu z dodatkiem Pb2+
| Rozwiązanie 1 | Rozwiązanie 1 | ||
|---|---|---|---|
| Cyjanek złota potasowego | 5 g/l | Koloidalny | 2g/l |
| Cyjanek potasu | 8g/L | Rozwiązanie 2 | |
| Cytrynian sodu | 50g/l | Dwuwodnik potasu | 200g/L |
| EDTA | 5 g/l | Wodorotlenek sodu | 120 g/l |
| Chlorek ołowiu | 0,5 g/l | ||
Tabela 1-36 Roztwór galwaniczny boro-wodorku potasu z dodatkiem T1+
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Cyjanek złota potasowego | Dostosuj według potrzeb | Dwuwodnik potasu | 5. 4 ~ 10. 8g/L |
| Cyjanek potasu | 6,5 g/l | Temperatura | 70 〜 80℃ |
| Wodorotlenek potasu | 11,2 g/l | Szybkość powlekania | <10μm/h |
| Siarczan talu | 5 〜 100mg/L |
Au(CN)4- + 2e- → Au(CN)2- + 2CN- (1-12)
![Figure 1-39 Effect of adding lead chloride on the Au(CN)2- reduction reaction polarization curve of the [Rotating gold electrode, KAu(CN)2 0. 009mol/L, KOH 0. 2mol/L]](https://sobling.jewelry/wp-content/uploads/2025/11/Page_61_docsmall.com_副本-768x578.jpg)
Rysunek 1-39 Wpływ dodania chlorku ołowiu na Au(CN)2--reduction reaction polarization curve [Rotating gold electrode, KAu(CN)2 0. 009mol/L, KOH 0. 2mol/L]
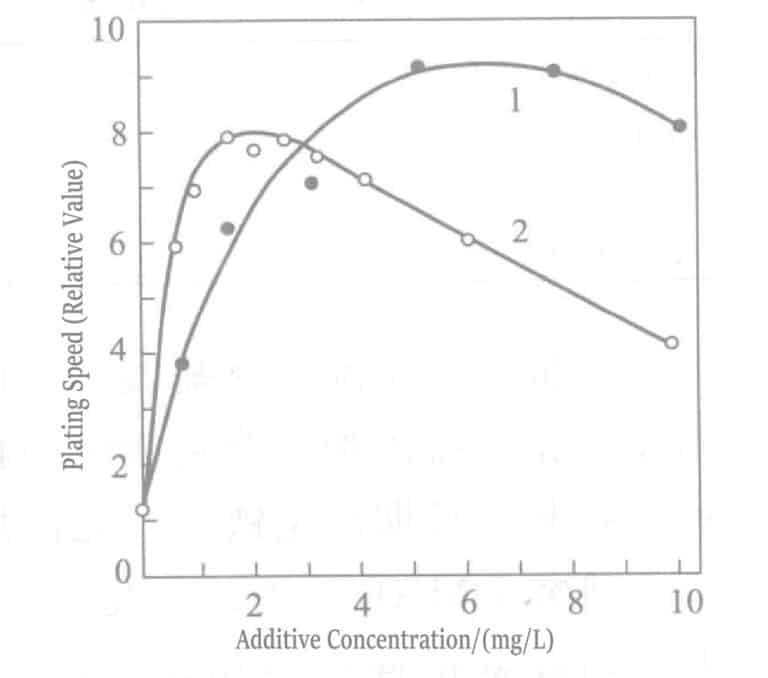
Figure 1-40 Effect of thallium chloride (curve 1) and lead chloride (curve 2) concentration on the gold plating rate of potassium borohydride plating solution
- b. Adding stabilizers. Adding organic stabilizers that reduce the catalytic activity of gold, increasing the plating solution temperature, and changing the concentration of the reducing agent can improve the plating speed of the solution. For example, the plating speed of plating solutions containing amino acetic acid, hydroxyethyl ethylenediaminetetraacetic acid, and diazotriacetic acid or succinic acid derivatives can reach a high rate of 12~23μm/h at 90℃. However, at high temperatures, the hydrolysis reaction of the reducing agent accelerates significantly, making the plating solution difficult to control. Adding trace amounts of p-dimethylamino azobenzene stabilizer does not affect the stability of the plating solution and can increase the usual usage concentration of BH4- by 2 times, raising the plating speed to 5μm/h. Other effective stabilizers include ethylene·glycol. Ethyl·ether, diethylene glycol? ethyl ether, and polyethyleneimine.
- c. Use trivalent gold cyanide complex salts. Plating solutions with trivalent gold cyanide complex salts, such as those with added lead chloride or titanium chloride, as shown in Table 1-33, is detailed in Table 1-37.
Table 1-37 Potassium Gold(III) Cyanide Potassium Borohydride Plating Solution
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Potassium gold(III) | 3 g/l | Lead chloride | 0. 5mg/L |
| Wodorotlenek potasu | 11,2 g/l | Temperatura | 70℃ |
| Dwuwodnik potasu | 3 g/l |
The advantage of trivalent gold cyanide complex salt plating solution is that KAuO2 and KAu(OH)4 can be used as supplementary gold salt additives, avoiding excessive accumulation of free cyanide ions in the plating solution, reducing the plating rate, and favoring long-term stable plating rate. The plating rate of additive-free the plating solution is 2~8μm/h.
The study of the electrochemical behavior, structure, and properties of the DMAB plating solution shows that similar to the potassium borohydride plating solution, KAu(CN)2 only is used when preparing the gold plating solution, and dissolved gold hydroxide in potassium hydroxide solution is added as a supplement to avoid the accumulation of free cyanide ions. The composition of the plating solution is shown in Table 1-38.
Table 1-38 DMAB Plating Solution (Gold Hydroxide Dissolved in Potassium Hydroxide Solution)
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Cyjanek złota potasowego | 0.013 ~ 0.018mol/L | Dodatek | Niewielka ilość |
| DMAB | 0.07 〜 0.1 mol/L | pH | 13.1 ~ 13.4 |
| Wodorotlenek potasu | 0.09 〜 0.15mol/L | Temperatura | 70 〜 75℃ |
| Cyjanek potasu | 0.007 ~ 0.01mol/L | Szybkość powlekania | 2μm/h |
(5) Improve the stability of the plating solution.
Using additives can increase the plating rate and the stability of the plating solution, but the impurities produced will cause the plating solution to decompose.
Substances such as EDTA and ethanolamine added to the plating solution form strong, complex ions with metal impurity ions, inhibiting the reaction between metal impurities and BH4- and BH3OH-, thereby, improving the stability of the plating solution. The composition of the potassium borohydride plating solution with added EDTA and ethanolamine is shown in Table 1-39.
Table 1-39 Potassium Borohydride Plating Solution with Added EDTA and Ethanolamine
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Cyjanek złota potasowego | 1.45g/L | EDTA | 5 g/l |
| Cyjanek potasu | 11 g/L | Ethanolamine | 50mL/L |
| Wodorotlenek potasu | 11,2 g/l | Temperatura | 72℃ |
| Dwuwodnik potasu | 10.8g/L | Szybkość powlekania | 1. 5μm/h |
Table 1-40 Plating Solution with Two Reducing Agents (Hydrazine and DMAB)
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Cyjanek złota potasowego | 0. 005mol/L | DMAB | 0. 05mol/L |
| Cyjanek potasu | 0. 035mol/L | Hydrazine | 0. 25mol/L |
| Wodorotlenek potasu | 0. 8mol/L | Temperatura | 80℃ |
| Węglan potasu | 0. 45mol/L | Plating rate On the Nickel Base Layer (Initial Stage) | 2. 6μm/h |
| Lead acetate | 15X10-6 | On the gold (fixed value) | 7. 8μm/h |
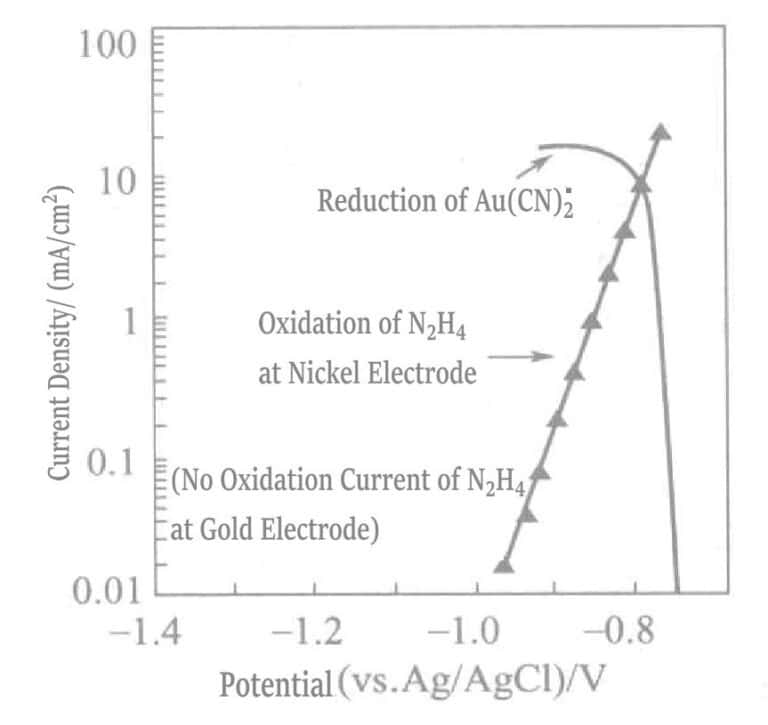
Figure 1-41 Polarization curves of the anodic oxidation reaction of hydrazine on the nickel electrode and the cathodic reduction reaction of Au(CN)2-.
(KOH 0. 8mol/L, KCN 0. 035mol/L, N2H4 0. 05mol/L, 80℃)
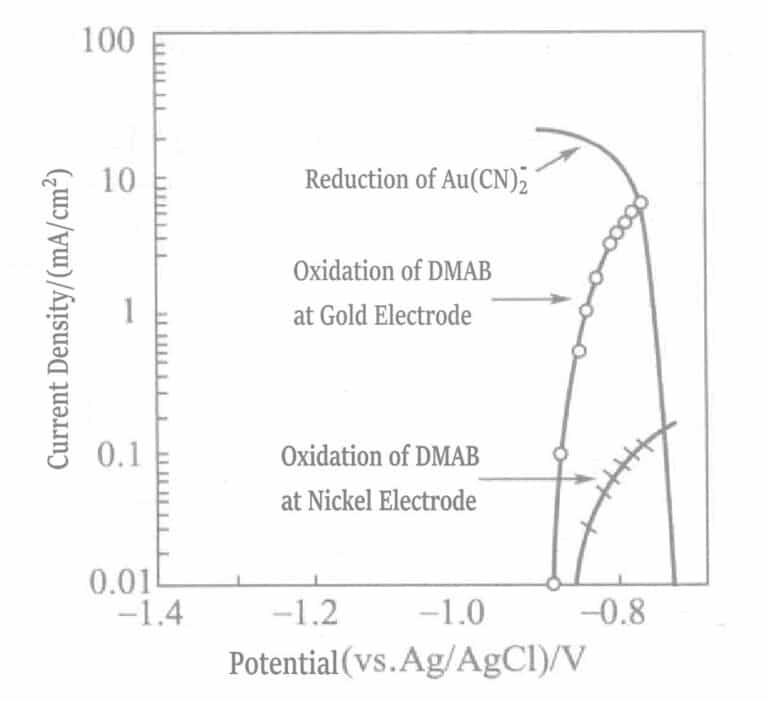
Figure 1-42 Polarization curves of the anodic oxidation reaction of DMAB on nickel and gold electrodes and the cathodic reduction reaction of Au(CN)2-
(KOH 0. 8mol/L, KCN 0. 035mol/L, DMAB 0. 05mol/L, 80℃)
In a plating solution containing only the reducing agent hydrazine, gold can be deposited solely relying on the catalytic effect of the nickel base layer. When the base layer is completely covered by gold, gold deposition stops, and at this point, the thickness of the gold plating layer depends on the concentration of free cyanide in the plating solution. Although the maximum plating thickness of this plating solution is limited (about 2μm), the plating layer is dense enough to meet the requirements of key pressure bonding.
Besides hydrazine, many other available reducing agents are available in the material catalytic gold plating solution; see Table 1-41.
Table 1-41 Other Reducing Agent Plating Solutions
| Środek redukujący | pH | Temperatura/℃ |
|---|---|---|
| Hypophosphite | 7 〜 7. 5 | 93 |
| 7. 5 〜 13. 5 | 96 | |
| 3 〜 4 | 70 〜 80 | |
| Hydrazine | 7 〜 7. 5 | 92 〜 95 |
| 5. 8 〜 5. 9 | 95 | |
| 11. 7 | 95 | |
| Hydroksyloamina | 2. 3 〜 2. 8 | 70 〜 85 |
| Sodium cyanoborohydride (NaBH3CN) | 3.5 | 90 |
| Hydrazinylborane (N2H4 ・ BH3) | >13 | 60 |
| Tiomocznik | 6. 5 〜 7. 0 | 83 〜 90 |
| 4.2 | 80 ~ 85 | |
| Ascorbic acid | 8 | 63 |
| Titanium trichloride | 5 | 75 |
Copywrite @ Sobling.Jewelry - Producent biżuterii na zamówienie, fabryka biżuterii OEM i ODM
5. Chemical Gold Alloy Plating
(1) Gold-silver alloy:
A chemical gold-silver alloy plating can be achieved by continuously adding potassium silver cyanide solution to the borohydride gold plating solution. Ag(CN)2- is more easily reduced than Au(CN)2-. When preparing a new plating solution, silver will precipitate first if the two are mixed, and the alloy cannot be plated.
By continuously adding small amounts of potassium silver cyanide dropwise into the plating solution, maintaining a relatively low condensation [molar ratio of Au:Ag (26:10~(26:0.5)] A gold-silver alloy plating layer with a silver content of 80%~20% can be precipitated. In this plating solution, the precipitation of silver is a replacement reaction product of the gold that precipitates first and the Ag(CN)2-, in solution.
(2) Gold-Copper Alloy:
In conventional coordination-based EDTA and formaldehyde reducing agent chemical copper plating solution, only potassium gold cyanide can plate a gold-copper alloy. By changing the potassium gold cyanide concentration, the copper mass fraction in the gold alloy plating layer can be adjusted from 1%~94%.
(3) Gold-Tin Alloy:
Gold and tin alloy chemical plating solution use the SnCl2 reducing agent method. The composition and concentration range of the plating solution are shown in Table 1-42.
Table 1-42 Gold-Tin Alloy Plating Solution
| Skład i warunki pracy | Parametry | Skład i warunki pracy | Parametry |
|---|---|---|---|
| Cyjanek złota(III) potasu | 4〜10g/L | Triolefin | 0. 05 ~ 0. 5g/L |
| Cyjanek potasu | 5〜15g/L | Temperatura | Temperatura pokojowa |
| Wodorotlenek potasu | 60〜100g/L | Szybkość powlekania | 1.5μm/h (no triolefin addition) |
| Stannous chloride | 40〜60g/L | 5μm/h (triolefin addition 0.5g/L) |
(4) Gold-indium alloy:
The gold-indium alloy plating solution is prepared by adding Ih2(SO4)3 and EDTA to a borohydride solution. The indium content in the plating layer is 1%~4%. At room temperature, a thin gold-indium alloy plating layer deposited on palladium-activated n-GaAs, after 350℃ heat treatment, has a contact resistance superior to pure gold.
(5) Gold-nickel, gold-cobalt alloys:
Uemaki developed 18~22K bright gold-nickel and gold-cobalt alloy plating solutions. pH 3~5, the gold alloy plating layer of cyanide chemical gold plating solution with added reducing agent sodium hypophosphite has physical properties such as hardness and wear resistance inferior to those of gold alloy electroplating layers containing nickel and cobalt.
Section II Cyanide-Free Chemical Gold Plating
1. Przegląd
Displacement-type gold plating uses the potential difference between the oxidation potential of the base layer metal and the reduction potential of gold ions as the plating reaction driving force. In contrast, reduction-type chemical gold plating uses the potential difference between the oxidation potential of the reducing agent and the reduction potential of gold ions as the plating reaction driving force.
The electrons involved in the reduction reaction of gold ions are provided either by the oxidation reaction of the base layer metal (displacement-type gold plating) or by the oxidation reaction of the reducing agent (reductive gold plating).
Other methods include: ① Adding heavy metal salts to the displacement-type gold plating solution, where the base layer metal surface adsorbs the heavy metals, shifting the potential in the direction that makes gold ions easier to reduce; ② Adding a reducing agent to the displacement-type gold plating solution, allowing redox reactions to occur simultaneously to plate thicker gold; ③ In gold plating solutions containing reducing agents, the base layer noble metal acts as a reducing agent and undergoes oxidation with a catalyst, performing base layer catalytic chemical gold plating.
Ligands in chemical gold plating solutions commonly use cyanide, which forms very stable complexes with gold ions (stability constant K=4×1028). Currently, many semiconductor components have switched to using near-neutral, low-cyanide, or cyanide-free gold plating solutions, such as sulfite or thiosulfate gold plating solutions and cyanide-free chemical gold plating solutions with thiol RSH series ligands.
2. Displacement-Type Chemical Gold Plating
Generally, the bonding strength between the reduced-type thick-layer electroless gold plating and the base layer of base metals is relatively poor. Therefore, displacement-type electroless gold plating must be performed before plating a thick gold layer.
In the displacement-type gold plating solution, the base layer’s base metal dissolves (oxidizes) in the electrolyte solution, releasing electrons. In contrast, the gold ions in the solution accept electrons and deposit (reduce) on the non-metal surface. The formation of gold ligands reduces the concentration of gold ions in the plating solution, shifting the reduction potential in the negative direction, as shown in Table 1-43.
Table 1-43 Ligands and Reduction Potentials of Gold Ion Complexes
| Ligands | Ligand | E/V |
|---|---|---|
| H2O |
Au(H2O)2+ Au(H2O)43+ |
1.68 1.50 |
| Cl- |
AuCl2 - AuCl4 - |
1.15 0.92 |
| SCN- |
Au(SCN)2 - Au(SCN)4 - |
0.67 0.64 |
| I- |
AuI2- AuI4- |
0.58 0.57 |
| New Hampshire3 | Au(NH)43+ | 0.56 |
| OH- | Au(OH)4 - | 0.48 |
| Tiomocznik | Au(Thu)2+ | 0.38 |
| S2O32- | Au(S2O3)23- | 0.15 |
| SO32- | Au(SO3)23- | 0.06 |
| R-SH | Au(R-S)2- | -0. 3 〜 - 0. 5 |
| CN- | Au(CN)2 - | -0.65 |
Table 1-43 shows that besides cyanides, other ligands such as thiols, sulfites, and thiosulfates can also form stable complexes with gold ions and exhibit negative potentials.
In the sulfite system displacement-type gold plating solution, besides sulfite ions, ligands such as polyamine polycarboxylic acids and their salts, water-soluble amines, amine salts, ethylenediamine triacetate salts, stabilizers like tetraalkylammonium salts, ethylenediamine tetra (methylene phosphonate), sugars, and thiol compounds can also be used. The concentrations of ammonium ions, chloride ions, sulfate ions, bromide ions, or iodide ions must be maintained within a specific range and not be too high; otherwise, ammonium (complex)–gold ligands may form in the plating solution, whose redox potential is more positive than sodium sulfite. When the plating solution is left standing or during gold plating, sodium sulfite may oxidize and reduce gold, causing instability in the plating solution.
Thiol succinate, acetylcysteine, cysteine, and other thiol series compounds and gold ions can form stable ligands in cyanide-free gold-plating solutions. Thiol succinate [HOOCCH(SH)-CH2COOH] and the reduction potential of the gold ion ligand, that is, Au(HOOCCHSCH2COOH)2- + e- ⇌Au(s) + 2 ( HOOCCH – SCH2COOH)-, the correct value of the standard electrode potential for the reaction is difficult to obtain. The measured reduction potential of the plating solution is about -0.3~0.5V. The thiol succinate gold ligand exists in the form of [Au(HOOC – CHSCH2COOH)2]-, with gold in the +1 oxidation state.
HAuCl4 + 3H2O → Au(OH)3 + 4HCl (1-13)
Au(OH)3 + 4[HOOCCH(SH)CH2 COOH] → [Au(HOOCCH—S—CH2COOH)4 ]- + 3H2O+H+ (1-14)
[Au( HOOCCH—S—CH2COOH)4]- → [Au(HOOCCH—S—CH2COOH)2]- + HOOCH2CHOOCCH—S—S—CHCOOHCH2COOH (1-15)
Table 1-44 Cyanide-Free Displacement Gold Plating Solution
| Skład i warunki pracy | Sulfite system | Mercaptosuccinic acid system | ||
|---|---|---|---|---|
| Sodium gold chlorate/(mol/L) | 0.05 | |||
| Sodium thiosulfate/(mol/L) | 0.028 | 0.015 | ||
| Gold mercaptosuccinate/(mol/L) | 0.01 | |||
| Sodium sulfite/(mol/L) | 0.52 | 0.1 | ||
| Mercaptosuccinic acid/(mol/L) | 0.25 | 0.25 | ||
| Trisodium citrate/(mol/L) | 0.22 | |||
| Acetylcysteine/(mol/L) | 0.03 | |||
| Tetramethylammonium chloride/(mol/L) | 0.8 | |||
| EDTA/( mol/L) | 0.015 | |||
| EDTA - 2Na/(mol/L) | 0.02 | |||
| Amino tris(methylenephosphonic acid)/(mol/L) | 0.1 | |||
| Sodium carboxymethyl cellulose/(g/L) | 10 | |||
| pH | 7.0 | 7.0 | 1.5 (Adjusted with hydrochloric ) | 7.0 |
| Temperatura /℃ | 60 | 85 | 80 ~ 90 | |
3. Reduced-Type Chemical Thick Gold Plating Layer
In gold plating solutions with thiosulfate as the ligand, sodium sulfite prevents the decomposition of thiosulfate ions. In NaAuCl4 plating solutions containing trivalent gold salts, monovalent gold is reduced by excess thiosulfate. In weakly alkaline gold plating solutions, pH buffers such as ammonium chloride, sodium tetraborate, and boric acid are commonly added.
Thiol compounds can form ligands with gold ions that have excellent stability and act as reducing agents. These thiol compounds include L-cysteine and 2-ethanamine thiol, among others. Table 1-45 lists the composition and operating conditions of cyanide-free reduced-type chemical gold plating solutions using sodium thiosulfate and thiol compounds as ligands.
Table 1-45 Cyanide-Free Reduction-Type Gold Plating Solution
| Skład i warunki pracy | Thiosulfate system | Thiol system | |||
|---|---|---|---|---|---|
| Gold chlorate/(g/L) | 0.01 | ||||
| Sodium gold chlorate/(g/L) | 0.0125 | 0.0125 | |||
| Sodium gold sulfite/(g/L) | 0.02 | ||||
| Gold mercaptosuccinate/(g/L) | 0.01 | ||||
| Mercaptosuccinic acid/(g/L) | 0.27 | ||||
| Sodium thiosulfate/(g/L) | 0.1 | 0.17 | 0.1 | ||
| Sodium sulfite/(g/L) | 0.1 | 0.4 | |||
| Ammonium sulfite/(g/L) | 0.43 | ||||
| EDTA ・ 2Na/(g/L) | 0.19 | ||||
| Trietanoloamina/(g/L) | 0.034 | ||||
| Chlorek amonu/(g/l) | 0.05 | ||||
| Tetraboran sodu/(g/L) | 0.13 | ||||
| Potassium dihydrogen phosphate/(g/L) | 0.15 | ||||
| Tiomocznik/(g/L) | 0.0033 | ||||
| Hydroquinone/(g/L) | 0.002 | ||||
| Ascorbic acid/(g/L) | 0.25 | ||||
| Hydrazine/(g/L) | 0.3 | ||||
| L-cysteine/(g/L) | 0.08 | ||||
| 2-aminoethyl mercaptan/(g/L) | 0.2 | ||||
| Potassium benzotriazole/(g/L) | 0.05 | ||||
| pH | 7.5 | 7.0 | 8.0 | 7.0 | 7.5 |
| Temperatura/℃ | 60 | 80 | 70 | 80 | 80 |
4. Base Layer Catalytic Chemical Gold Plating
Base layer catalytic chemical gold plating is a reduction-type chemical gold plating method using a reducing agent. The reducing agent only has catalytic activity on the surface of the substrate, the base metal (nickel) layer, and has no catalytic activity on the deposited gold surface. The catalytic chemical gold plating layer is smoother, denser, and has fewer or smaller pores than the displacement-type gold plating layer.
In thiosulfate and sulfite chemical gold plating solutions, gold can be deposited on the nickel surface without adding other reducing agents. On the nickel surface, sulfite only reduces the thiosulfate gold complex and does not act on the gold surface, so it is called a base layer catalytic type of chemical gold plating. A displacement gold plating reaction also occurs simultaneously on the surface of the base nickel plating layer. Therefore, the reducing agent sulfite undergoes different oxidation reactions influenced by the composition of the base nickel plating layer and pretreatment conditions. The concentration of the thiosulfate sodium ligand or the pH of the plating solution affects the different ratios of displacement and reduction reactions, the maximum thickness of the gold plating layer, appearance, porosity, and adhesion, so it is necessary to select an appropriate plating solution composition and gold plating conditions.
5. Stability of Cyanide-Free Chemical Gold Plating Solution
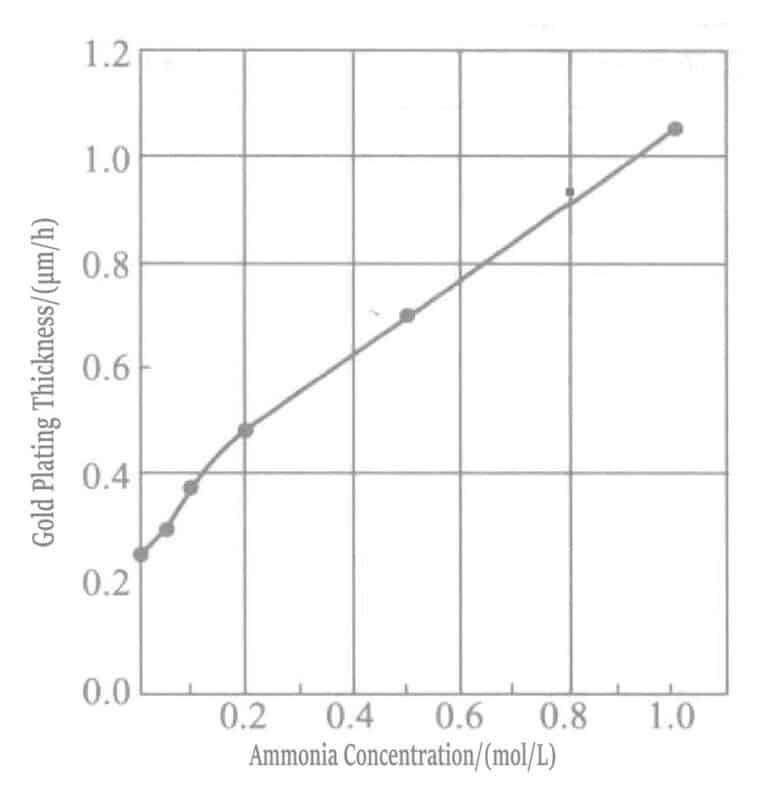
Increasing the concentration of ammonia water accelerates the deposition rate of the gold plating layer. In plating solutions with high ammonia concentration, mercapto succinate acts as a reducing agent, and a reduction reaction occurs simultaneously with the displacement reaction.
The contamination of copper or iron ions is the main cause of instability in cyanide-free chemical gold plating solutions. Copper dissolved from the nickel plating layer’s pores and iron from the substrate easily promote the instability of the chemical gold plating solution.
Reasons: ① Gold ions accept electrons released when these metals oxidize, increasing the reduction rate. ② Copper ions or iron ions catalyze the oxidation reaction of sulfite or thiol, accelerating the reaction rate, which causes defects on the surface of the chemical gold plating layer and reduces welding performance and bonding strength. In chemical gold plating solutions, the dissolution and contamination of these metals should be suppressed by adding ligands that form stable complexes with these dissolved and contaminated metal ions.
6. Cyanide-Free Chemical Gold Plating Solution
(1) Tetrachloroaurate (III) salts and weakly reducing amine borane gold plating solutions
Tetrachloroaurate (III) salts (NaAuCl4) are easily reduced to deposit gold. Ether-substituted tertiary amine borane reducing agents can be used with NaAuCl4 to form an autocatalytic plating solution, or reducing agents such as trimethylamine borane, methylmorpholine borane, and diisopropylamine borane, along with stabilizers like thiols and iodide compounds.
(2) Gold plating solution with gold sulfite salt:
Currently a large number of monovalent gold sulfite plating solutions are used, with hypophosphites, formaldehyde, hydrazine, tetrahydroborate and DMAB as reducing agents. Gold sulfite salt [Na3Au(SO3)2] is unstable in water and requires the addition of stabilizers such as 1,2-diaminoethane and potassium bromide.
(3) Thiosulfate gold plating solution
① Gold plating solution with thiourea and its derivatives as reducing agents:
The combination of monovalent gold thiosulfate and thiourea plating solution has good stability, does not produce hydrogen gas around neutral pH, and has no porosity. The composition of the plating solution is shown in Table 1-46 (Plating Solution A).
Table 1-46 Thiosulfate Gold Plating Solution
| Skład i warunki pracy | Plating Solution A | Plating Solution B |
|---|---|---|
| NaAuCl4 / (mol/L) | 0.1 | 0.0125 |
| Na2S2O3/(mol/L) | 0.08 | 0.1 |
| Na2SO3 /(mol/L) | 0.4 | 0.1 |
| Na2B4O7/( mol/L) | 0.1 | - |
| NH4Cl/(mol/L) | - | 0.05 |
| Thiourea/(mol/L) | 0.1 | - |
| Sodium L-ascorbate/(mol/L) | - | 0.25 |
| pH | 9.0 | 6.0 |
| Temperatura/℃ | 80 | 60 |
| Plating rate/(μm/h) | 1. 9 〜 2. 3 | 1. 5 〜 2. 0 |
② Gold plating solution with ascorbic acid as a reducing agent:
In the thiosulfate plating solution with L-ascorbic acid sodium as the reducing agent, sodium sulfite is present, which can stably plate gold. The composition of the plating solution is shown in Table 1-46 (Plating Solution B).
Effective reducing agents in sodium thiosulfate plating solutions, besides thiourea and sodium ascorbate, include sodium tartrate, glycolic acid, and hypophosphorous acid.
③ Reaction mechanism of thiosulfate plating solution:
Gold salt reacts with thiosulfate to produce Au(S2O3)23-. When there is no thiosulfate in the solution, only sulfite is present and formed Au(SO3)23-. The reaction equation is as follows:
Au3++ 2S2O3 2- + H2O ⇌ Au(S2O3)23- + SO4 2- + 2H+ (1-16)
Au3+ + 3SO32- + H2O ⇌ Au(SO3 )23- + SO42- + 2H+ (1-17)
Au+ + 2SO32- ⇌ Au(SO3)23- K=1010 (1-18)
Au+ + 2S2O32- ⇌ Au(S2O3)23- K = 1026 (1-19)

Figure 1-44 Comparison of cathodic polarization curves of gold deposition reactions in sulfite and thiosulfate plating solutions
(NH4Cl 0. 1mol/L, Na2SO3 0. 2mol/L)
Thiosulfate has a stronger complexing ability with monovalent gold than sulfite, so monovalent gold is more difficult to deposit from plating solutions containing sodium thiosulfate than those containing sulfite.
In the sulfite gold plating solution with the reducing agent ascorbate, due to the difference in cathodic polarization curves between gold sulfite complex ions and gold thiosulfate complex ions, the gold deposition rate is only 1/10 of that in the sodium thiosulfate plating solution. Figure 1-45 shows ascorbate sulfite and thiosulfate gold’s cathodic and anodic polarization curves.
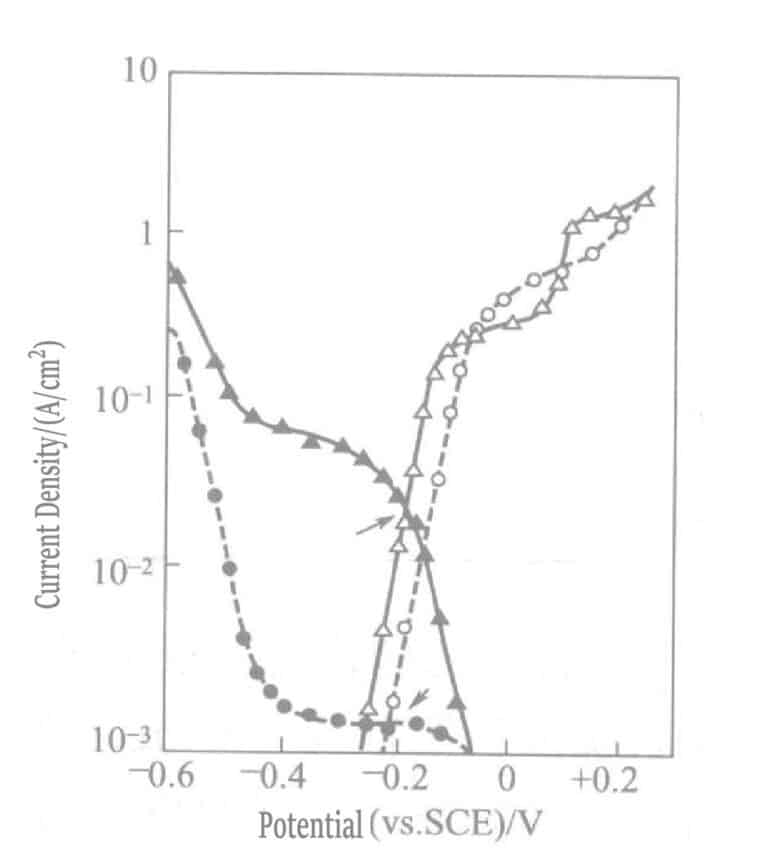
Figure 1-45 Cathodic and anodic polarization curves of ascorbic acid, sulfite plating solution, and thiosulfate gold
(Gold electrode, NH4Cl 0. 1mol/L, pH 6. 0, 60℃. Curve "●" plating solution: Na2SO3 0.2mol/ L and NaAuCl4 0.01mol/L; Curve "▴" same plating solution as before, with the addition of Na2S2O3 0. 1mol/L; Curve "○" plating solution: Na2SO3 0. 2mol/L and sodium ascorbate 0. lmol/L; Curve "△" solution, same as before, with the addition of Na2S2O3 0.1mol/L)
The reaction principle of thiosulfate electroless gold plating solution refers to the oxidation state of the reducing agent, and the local reactions are as follows.
Cathodic reaction:
Au(S2O3)23- + 2e- → Au + 2S2O32- (1-20)
Anodic reaction:
Thiourea plating solution
CS(NH2)2 + 5H2O → CO(NH2)2 + H2SO4 + 8H+ + 8e- (1-21)
The reaction product CO(NH2)2 is urea.
Ascorbic acid plating solution
C6H8O6 → C6H6O6 + 2H+ + 2e-
7. Gold Plating Solution of Sugar Additive with Gold Sulfite Salt
After adding saccharide compounds to the gold sulfite plating solution, it can remain stable for a long time, and the gold plating layer is good. The composition of the plating solution is as follows.
Gold sulfite salts: potassium gold sulfite, sodium gold sulfite, ammonium gold sulfite, etc.
Sulfites: potassium sulfite, sodium sulfite, ammonium sulfite, etc.
pH adjuster: Adjust to pH 6~9 with various buffers.
Stabilizers: water-soluble amine compounds, ethylenediamine, diethylenetriamine, triethylenetetramine, etc.; Water-soluble amino acids or salts, ethylenediamine tetraacetic acid, triethylenetetramine hexaacetic acid, trans-1,2-cyclohexane diamine tetraacetic acid or salts, etc.; water-soluble organophosphates or salts, amino tris (methylenephosphonic acid), 1-hydroxyethylidene-1,1-diphosphonic acid, ethylenediaminetetra(methylene phosphonic acid), diethanolamine, pentakis(methylene phosphonic acid) or salts, etc.; water-soluble aromatic nitro compounds can also be added, such as mono-, di-, and tri-nitrobenzol acid, mono- and di-nitrosalicylic acid, nitrobenzene dicarboxylic acid, mono-, di-, and tri-nitrophenol, dinitroaminophenol, mono-, di-, and tri-nitrobenzene, etc.
Sugars other than starch can also include hexoses, glucose, mannose, galactose and other monosaccharides, erythritol, pentitol, hexanol and other sugar alcohols, glucaric acid and other aldaric acids, gluconic acid, hexatonic acid and other aldonic acids, oligosaccharides, etc. These sugar compounds can increase the stability of the plating solution and expand the current density range of the bright plating area.
The plating results are shown in Table 1-47.
Table 1-47 Various Sulfite Gold Plating Baths, Operating Conditions, and Effects of Additives
| Numer seryjny | Various Sulfite Gold Plating Baths and Operating Conditions | Additive Effect |
|---|---|---|
| Nr 1 |
Gold sodium sulfite 10g/L Sodium sulfite 65g/L Trisodium citrate 65g/L Ethylenediaminetetramethylenephosphonic acid (EDTMP) 85g/L pH 7 Temperature 60℃ Total current 0.2A Specimen substrate:42Fe-Ni alloy Ideal current density method with strong stirring |
Electrolysis 1080 ℃, electroplating solution decomposition, producing black particles. Appearance of plating layer with different current densities produces spots and scorching. |
| No.1 Add sodium carboxymethyl cellulose (CMC) 10g/L to the plating solution. Other conditions are the same as No.1 | Electrodeposition 1740℃, plating solution decomposition, black particles. The appearance of plating layer is improved, and spots and scorching are obviously reduced. | |
| Nr 2 |
Gold sodium sulfite 10g/L Sodium sulfite 130g/L Trisodium citrate 65g/L Triammonium citrate 65g/L p-Nitro(benzene)phenol 1g/L pH 7 Temperature 40℃ Total current 0.2A Specimen substrate: copper Strong stirring |
High current density areas burnt, plating layer appearance is very poor, appear diffuse spots |
| No.2 plating solution with starch 5g/L, other conditions are the same as No.2. | No burning in high current density area, good appearance of plating layer in wide current density range, stable plating solution. | |
| Nr 3 |
Sodium gold sulfite 10g/L Sodium sulfite 100g/L Disodium borate 50g/L Boric acid 100g/L p-Nitro(benzene)phenol 1g/L pH 7 Temperature 40℃ Total current 0.2A Specimen substrate: copper Strong stirring |
Poor appearance of plating layer |
| Add 5g/L starch to No.3 plating solution, other conditions are the same as No.3. | Good appearance of plating layer in wide range of current density, stable plating solution. | |
| Nr 4 |
Sodium gold sulfite 12g/L Sodium sulfite 100g/L Phosphite 3g/L Ethylenediamine hydrate 30g/L pH 7 Temperature 60°C Total current 0.2A Specimen substrate:42Fe-Ni alloy Strong stirring |
High current density area burnt, plating layer appearance is extremely poor |
| No.4 add starch 5g/L to the plating solution, other conditions are the same as No.4. | Good appearance of plating layer and stability of plating solution in wide range of current density. | |