Apa Metode dan Aplikasi Utama Pelapisan Platinum dalam Industri Modern?
Teknik Pelapisan Platinum: Solusi, Paduan, dan Aplikasi untuk Perhiasan
Pendahuluan:
Ingin tahu tentang pelapisan platina? Panduan ini mencakup semuanya, mulai dari dasar hingga teknik tingkat lanjut. Pelajari tentang solusi pelapisan yang berbeda, termasuk opsi berbasis klorida dan sulfat, dan temukan cara meningkatkannya. Jelajahi solusi pelapisan tipis dan tebal untuk berbagai aplikasi. Penasaran dengan paduan platinum? Kami membahas yang populer seperti Pt-Au, Pt-Co, dan Pt-Ir. Selain itu, pelajari juga pelapisan kimiawi untuk aplikasi yang unik. Baik Anda seorang perancang perhiasan, peritel, atau pembuat khusus, tinjauan komprehensif ini akan membantu Anda menyempurnakan produk Anda dengan pelapisan platina.

Daftar Isi
Bagian I Tinjauan Umum
Platinum memiliki nomor atom 78 dalam tabel periodik, dengan simbol unsur Pt, massa atom relatif 195,7, densitas 21,09 g/cm3 (20 ℃), dan titik leleh 1768 ℃.
Beberapa parameter utama platinum ditunjukkan pada Tabel 3-1.
Tabel 3-1 Beberapa Parameter Utama Platinum
| Parameter karakteristik | Nilai karakteristik |
|---|---|
|
Nama unsur, simbol unsur, nomor atom Klasifikasi Grup, Periode Kepadatan, kekerasan Warna Massa atom relatif Jari-jari atom Jari-jari ikatan kovalen Valensi kimia Struktur kristal titik leleh titik didih Panas penguapan Panas pembubaran Kapasitas panas spesifik Konduktivitas Konduktivitas termal |
Platinum 、 Pt 、 78 Logam Transisi 10(Ⅷ),6 21090kg / m3, 3.5 Putih keabu-abuan 195.084 135pm 128pm 2、4 Kubik yang berpusat pada wajah 2041. 4K( 1768.3℃) 4098K (3825℃) 510kJ/mol 19.6kJ/mol 130J/(kg - K) 9. 66X 106m ・Ω 71. 6W/(m ・ K) |
Bagian II Elektroplating Platinum
Tabel 3-2 Aplikasi Industri Pelapisan Pt Plating
| Produk | Bahan | Ketebalan pelapisan / μm | Produk | Bahan | Ketebalan pelapisan / μm |
|---|---|---|---|---|---|
|
Komponen Kedirgantaraan Komponen Penerbangan Baki Sekat Pengaman Elektroda |
Superalloy yang mengandung Niobium SUS347 Titanium SUS316 |
10 10 5 10 |
Elektroda Elektroda Elektroda - |
Titanium Jaring titanium Kawat Tungsten - |
2〜7 2〜7 10 - |
Tabel 3-3 Garam Platinum Khas
| Garam bervalensi 2, 4 | Garam platinum yang khas |
|---|---|
| Garam Pt (II) |
Asam kloroplatinat: H2PtCl6 - 6H2O Diammine platinum nitrit: Pt (NH3)2(TIDAK2)2 Platinum nitrit sulfat: H2Pt (NO2)2SO4 |
| Garam Pt (Ⅳ) | Natrium hidroksiplatinat: Na2Pt (OH)6 - 2H2O |
1. Berbagai Solusi Pelapisan Platinum
Tabel 3-4 Berbagai Komposisi Larutan Pelapisan Pt dan Kondisi Proses
| Komposisi dan kondisi proses | Klorida | Amonium sulfit | DNS | Garam hidroksibasa | Asam fosfat | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nomor 1 | Nomor 2 | Nomor 3 | Nomor 4 | Nomor 5 | Nomor 6 | Nomor 7 | Nomor 8 | No. 9 | No. 10 | No. 11 | No. 12 | No. 13 | No. 14 | |
| Asam kloroplatinat H2PtCl6/ (g/L) | 10 〜50 | |||||||||||||
| Amonium kloroplatinat (NH4)2PtCl6/ (g/L) | 15 | |||||||||||||
| Diammine platinum nitrit Pt (NH3)2(TIDAK2)2/ (g/L) | 8~16. 5 | 20 | 6~20 | 8 | 6~20 | 16.5 | ||||||||
| Platinum nitrit sulfat H2Pt (NO2)2SO4/ (g/L) | 10 | |||||||||||||
| Natrium hidroksiplatinat Na2Pt (OH)6 ・ 2H2O / (g/L) | 20 | 18.5 | ||||||||||||
| Asam hidroksiplatinat H2Pt (OH)6/ (g/L) | 20 | |||||||||||||
| Kalium hidroksiplatinat K2Pt (OH)6/ (g/L) | 20 | |||||||||||||
| Platinum klorida PtCl4- 5H2O / (g/L) | 7.5 | |||||||||||||
| Amonia (28%) / (g/L) | ||||||||||||||
| Asam klorida/(g/L) | 180~300 | |||||||||||||
| Natrium sitrat/(g/L) | 100 | 20~25 | ||||||||||||
| Amonium klorida/(g/L) | 4~5 | |||||||||||||
| Amonium nitrat/(g/L) | 100 | |||||||||||||
| Natrium nitrit/(g/L) | 10 | |||||||||||||
| Asam fluoroborat/(g/L) | 50~100 | |||||||||||||
| Natrium fluoborat / (g/L) | 80~120 | |||||||||||||
| Asam sulfonat/(g/L) | 20~100 | |||||||||||||
| Asam fosfat/(g/L) | 80 | 10~100 | ||||||||||||
| Asam sulfat/(g/L) | 10~100 | pH2 | ||||||||||||
| Natrium asetat/(g/L) | 70 | |||||||||||||
| Natrium karbonat/(g/L) | 100 | |||||||||||||
| Natrium hidroksida/(g/L) | 10 | 5.1 | ||||||||||||
| Natrium oksalat/(g/L) | 5.1 | |||||||||||||
| Natrium sulfat/(g/L) | 30.8 | |||||||||||||
| Kalium hidroksida / (g/L) | 15 | |||||||||||||
| Amonium Hidrogen Fosfat) (g/L) | 20 | |||||||||||||
| Natrium hidrogen fosfat/(g/L) | 100 | |||||||||||||
| Kalium sulfat/(g/L) | 40 | |||||||||||||
| Suhu larutan pelapisan / ° C | 45~90 | 80~90 | 90~95 | 70~90 | 65~100 | 75~100 | 75~100 | 80~90 | 30~70 | 75 | 65~80 | 75 | 70~90 | 70~90 |
| Kepadatan arus/(A/dm2) | 3.0 | 0.5~1.0 | 0.3~2.0 | 2~5 | 0.2~2 | 0.5~0.3 | 0.5~0.3 | 0.5 | 2.5 | 0.8 | 0.8 | 0.75 | 0.3~1 | 0.3~1 |
| Efisiensi saat ini/% | 15~20 | 70~10 | 10 | 14~18 | 15 | 15 | 15 | 35~40 | 10~15 | 100 | 80 | 100 | 10~50 | 15~50 |
(1) Larutan pelapisan klorida
Larutan pelapisan Pt pertama yang berhasil secara teknis menggunakan asam kloroplatinat (H2PtCl6・6H2O) sebagai garam dasar. Elektroda Pt yang dapat larut digunakan, dan kondisinya adalah 10 ~ 15g / L asam kloroplatinat, 180 ~ 300g / L asam klorida, suhu larutan pelapisan 45 ~ 90 ℃, kerapatan arus 2,5 ~ 3,5A / dm2, dan efisiensi arus katoda 15% ~ 20%. Film pelapisan yang diperoleh dari larutan ini dapat mencapai 20μm tanpa retakan dan keuletan yang baik. Namun, pH harus dikontrol dalam kisaran sempit untuk mencegah hidrolisis larutan pelapisan. Ketika pH larutan pelapisan mulai terhidrolisis, pH mencapai 2,2.
(2) Larutan Pelapisan Diamminonitrit
Untuk memastikan konsentrasi Pt divalen dan mencegahnya teroksidasi menjadi Pt(Ⅳ), senyawa amina dalam jumlah yang sesuai perlu ditambahkan untuk membentuk kompleks dengan Pt(II). Komponen dasar dari larutan pelapisan ini adalah diamminonitritoplatinum Pt(NH3)2(TIDAK2)2, sering disebut sebagai garam Pt-P (II). Larutan pelapisan menggunakan garam ini ditemukan oleh W. Keitel pada tahun 1931 (larutan pelapisan No. 3 pada Tabel 3-4). Ketika konsentrasi nitrit dalam larutan meningkat, hal ini mempengaruhi disosiasi kompleks Pt, sehingga mempengaruhi perilaku larutan pelapisan. Setelah mendidih, NH4OH ditambahkan untuk bereaksi dengan NaNO3 untuk menghasilkan NH4TIDAK2 untuk mengembalikan efisiensi arus awal, menghasilkan, yang kemudian terurai menjadi gas nitrogen dan hidrogen. Dengan cara ini, hampir semua komponen non-logam dari garam Pt-P dalam larutan pelapisan menjadi gas dan menghilang, sehingga umur larutan pelapisan lebih panjang dibandingkan dengan larutan pelapisan klorida. Keuntungan dari larutan pelapisan ini adalah penyesuaian komponennya relatif mudah.
A. B. Triper dan yang lainnya menggunakan PR sebagai sumber daya, mencapai kecepatan elektroplating 5μm/jam. Kondisinya adalah: 5 ~ 6A / dm2, Waktu elektrolisis katoda 5 detik dan waktu elektrolisis anoda 2 detik. Larutan pelapisan No. 4 pada Tabel 4-3 diusulkan dalam paten Lacroix tahun 1967 di Prancis. Larutan pelapisan ini dapat menghasilkan ketebalan lapisan hingga 7,5μm. Larutan pelapisan No. 5 berasal dari paten AS (US PAT. 2984603, 2984604), diusulkan pada tahun 1961, yang melibatkan penambahan asam sulfonat ke dalam larutan pelapisan garam Pt-P. No. 6 mengandung asam fosfat, sedangkan No. 7 menggunakan asam fosfat-sulfat sebagai larutan dasar, yang diusulkan dalam paten Prancis tahun 1960 (Fr PAT. 1299226). Mereka menggunakan anoda yang tidak larut dan secara fleksibel menerapkan metode penting seperti pengadukan dan pengocokan.
No. 8 menggunakan natrium asetat dan natrium karbonat untuk menggantikan garam amonium, sehingga mencapai efisiensi arus maksimum dan meningkatkan stabilitas larutan pelapisan. Lapisan yang diperoleh dari larutan ini halus dan rata, dengan ketebalan pelapisan hingga 10μm tanpa lubang kecil atau retakan.
Di Jepang, solusi pelapisan ini digunakan secara luas dalam industri. Di bawah ini adalah salah satu contohnya:
|
Platinum (Diammineplatinum Nitrit) Amonium nitrat Natrium nitrit Amonium hidroksida |
10 gram/L 100g / L 10 gram/L 35g / L |
Suhu Larutan Kepadatan arus Efisiensi saat ini - |
90~92℃ 1A/dm2 10%~20% - |
(3) Larutan Pelapisan Asam Nitrosulfat Platinum
Larutan pelapisan ini tidak mengandung komponen amonia atau amina tetapi menggunakan asam nitrosulfat platinum[H2Pt (OH)6 - 2H2O] sebagai bahan dasar. Persiapan larutan pelapisan melibatkan penggunaan garam nitro, garam kalium platinum klorida, atau asam sulfat platinum ([K2Pt (NO2)3Cl, K2Pt (NO2)2Cl2 atau K2Pt (NO2)2SO4]). Densitas arus yang rendah digunakan untuk pelapisan yang cerah, dan asam sulfat ditambahkan untuk menyesuaikan pH di bawah 2,0. Komposisi yang representatif ditunjukkan pada Tabel 3-4, No. 9. Larutan pelapisan ini dapat menghasilkan lapisan pelapisan yang relatif tebal.
(4) Larutan Pelapisan Garam Logam Asam Hidroksiplatinat Basa
Dalam larutan pelapisan alkali yang khas, garam natrium atau kalium dari asam hidroksiplatinat seperti Na2Pt (OH)6 atau K2Pt (OH)6 digunakan. Komposisi larutan pelapisan yang representatif ditunjukkan pada Tabel 3-4, No. 11. Suhu larutan pelapisan 75 ℃, kerapatan arus 0,8A / dm2, dan efisiensi saat ini dapat mencapai 100%, dan anoda menggunakan bahan Ni atau baja tahan karat.
No. 10 diusulkan oleh A.R. Powell pada tahun 1913, dan paten Inggris diperoleh (Brit PAT. 363569). Lapisan cerah yang sebanding dengan larutan pelapisan Rh dapat
diperoleh dari larutan pelapisan ini. Ketika konsentrasi Pt di bawah 3g/L, efisiensi arus turun tajam. Kepadatan arus bisa mencapai 2,5A/dm2 ketika konsentrasinya tinggi (12g / L). Pada suhu larutan 65 ~ 70 ° C, efisiensi saat ini dapat mencapai sekitar 80%. Namun demikian, peningkatan suhu lebih lanjut tidak meningkatkan efeknya secara signifikan.
(5) Larutan Pelapisan Fosfat
Pada awal tahun 1855, Roseleuer mengusulkan skema fosfat. Larutan pelapisan ini menggunakan garam koordinasi Pt klorida tetravalen, garam fosfat logam alkali, dan garam amonium sebagai garam konduktif. Pada tahun 1949, W. Pfanhauser mengusulkan solusi pelapisan No. 14, yang, dalam kondisi ini, dapat menghasilkan lapisan 0,5μm.
Druve melaporkan hasil percobaan dengan menggunakan larutan pelapisan yang sama. Kelemahan terbesar larutan pelapisan ini adalah kesulitan dalam penyesuaian. Endapan yang terbentuk ketika larutan pelapisan yang baru disiapkan harus larut dalam waktu yang lama. Amonium fosfat harus digunakan untuk menghindari pelapisan berpori dan kenyal. Amonium fosfat membantu melarutkan kompleks platina. Dalam kondisi tertentu, garam kuning yang tidak larut terbentuk pada permukaan anoda dalam larutan pelapisan, menjadi lapisan isolasi yang diperkirakan sebagai garam amonium hidroksiplatinat.
(6) Pelapisan Platinum Berbasis Sulfat
Pelapisan platina pada titanium atau tantalum tidak bermasalah meskipun tidak cerah, tetapi ketika melapisi platina pada benda-benda dekoratif, kecerahan menjadi masalah penting, dan keretakan juga menjadi masalah yang tidak dapat diabaikan. Masashi dan yang lainnya mengusulkan untuk menggunakan larutan pelapisan sulfat untuk mengatasi masalah ini. Karakteristik larutan pelapisan ini adalah melarutkan garam platinum ke dalam sulfat, menambahkan sulfit ke dalam larutan, dan menyesuaikan pH hingga kurang dari 2 dengan asam sulfat. Karena penambahan sulfit dapat membuat potensi platinum lebih negatif daripada ion hidrogen, ini memastikan kandungan hidrogen yang rendah pada lapisan pelapisan platinum, sehingga menghasilkan tekanan internal yang rendah dan kecerahan pada lapisan pelapisan. Namun, jika konsentrasi sulfit terlalu tinggi, platina dapat berkurang. Jika pH>2, sulfit mudah terhidrolisis. Juga pH <2 akan membantu menstabilkan kompleks platina.
Perlakuan awal untuk pelapisan adalah basa → penghilangan lemak elektrolitik → pencelupan asam, dan elektrolisis katodik selama 2 menit.
Proses pelapisan ditunjukkan pada Tabel 3-5.
Tabel 3-5 Kondisi Proses Pelapisan Platina dalam Seri Asam Sulfat
| Komposisi dan kondisi proses | Nomor 1 | Nomor 2 |
|---|---|---|
|
HAuCl4 (dihitung sebagai Au) K2SO4 K2SO3 pH (disesuaikan dengan asam sulfat) suhu Kepadatan arus Waktu pelapisan Ketebalan pelapisan Lapisan pelapisan |
10 gram/L 50 gram/L 1.0g / L 1.0 75℃ 2A/dm2 60 menit 7 μm Kecerahan |
10 gram/L 100g / L 2,0g/L 2.0 65℃ 1 A/dm2 100 menit 5 / μm Penampilan cantik, ikatan yang baik |
Pada Tabel 3-5 No.1, lapisan dikroik Pt-Au dapat diperoleh dengan melapisi emas kilat pada substrat, melapisi platina 7μm secara tebal, dan melapisi emas 2μm pada platina.
2. Solusi Pelapisan Tipis
3. Solusi Pelapisan Tebal
(1) Pelapisan Dekoratif
Seperti yang disebutkan sebelumnya, produk berlapis platinum seperti bingkai kacamata dan kotak arloji telah muncul karena penekanan pada merek platinum itu sendiri. Ketebalan pelapisan produk berlapis platina pada umumnya di bawah 5μm.
Baru-baru ini, teknologi baru lainnya telah muncul di bidang benda-benda dekoratif, yaitu electroforming.
Ketebalan produk yang dibentuk secara elektro umumnya 100 ~ 150μm, dan membuatnya berongga dapat mengurangi berat dan menurunkan biaya. Saat pelapisan dengan larutan pelapisan biasa menggunakan metode pelapisan listrik konvensional, retakan akan muncul setelah ketebalan pelapisan melebihi 10μm, sehingga secara teknis menantang.
(2) Aplikasi Industri
Pelapisan Pt pada komponen baja tahan karat untuk penerbangan telah digunakan secara praktis. Prosesnya adalah sebagai berikut:
Tabel 3-6 Kinerja Bahan Anoda Pt
| Properti | Pt | Ti | Nb | Ta |
|---|---|---|---|---|
|
Kepadatan (20 ℃) / (g / cm3) Titik leleh/°C Kekerasan (setelah perlakuan panas) Konduktivitas termal/[W/(m-K)] Resistivitas/μΩ-cm Koefisien muai panjang linier (x105)/[mm/(mm-K)]
|
21. 45 1769 37〜42 (Vickers) 71. 6 10. 6 9. 1 |
4. 54 1668 120 (Brennel) 16.8 48 8. 5 |
8. 57 2468 84 (Vickers) 67. 4 13. 1 7. 1 |
16. 6 2996 E-60 (Rockwell) 54. 8 12.4 6. 5 |
Umumnya, ketebalan lapisan pelapisan Pt adalah sekitar 2μm, sehingga densitas arusnya tinggi. Dalam kondisi seperti korsleting saat katoda dihubungi, dan operasi yang melibatkan amonium bifluorida, asam fluoroborat, alkali kuat, dan larutan sianida tinggi, konsumsi Pt semakin cepat. Oleh karena itu, memperpanjang masa pakainya sebanyak mungkin diperlukan, yang dapat dicapai dengan meningkatkan rasio area anoda-ke-katoda. Saat melapisi Pt pada elektroda Ti, Ti pertama-tama dapat dikeraskan dengan sandblasting, kemudian diaktifkan dengan asam untuk menghilangkan lapisan oksida permukaan, diikuti dengan pelapisan Pt.
Proses penuaan yang khas dari anoda Ti berlapis Pt adalah: (1) Film oksida Ti pada lubang jarum pelapisan Pt dihancurkan; (2) Ti mulai larut; (3) antarmuka Pt-Ti mengalami korosi sumuran saat pelarutan berlangsung, dan film Pt terkelupas. Pada saat ini, jika terjadi selama pelapisan emas, maka akan menyebabkan peningkatan mendadak dalam penyimpangan ketebalan pelapisan emas. Ketika menghadapi masalah seperti itu dalam praktiknya, memeriksa anoda adalah yang terbaik.
4. Peningkatan Lain pada Solusi Pelapisan
(1) Perbaikan pada Perlakuan Awal
Ada juga metode untuk meningkatkan daya rekat antara natrium dan paduannya dengan lapisan pelapisan platina dengan meningkatkan proses pra-perlakukan. Kamata mengusulkan dalam sebuah paten bahwa pelapisan serangan asam dilakukan dalam larutan pelapisan serangan asam pH = 1, diikuti dengan pelapisan ketebalan yang diperlukan dari lapisan platina dalam larutan pelapisan alkali. Komponen utama dari larutan pelapisan serangan asam adalah 0,3 ~ 3g / L asam kloroplatinat (dihitung sebagai platina) dan ion halida 5% ~ 15% (fraksi massa). pH harus dikontrol di bawah 1; jika tidak, aktivitas titanium akan menurun, menyebabkan daya rekat yang buruk. Misalkan konsentrasi ion halida terlalu rendah. Dalam hal ini, penghilangan film pasif pada permukaan titanium mungkin tidak sempurna, yang pada gilirannya mempengaruhi daya rekat lapisan pelapisan. Kondisi untuk pelapisan mogok adalah suhu larutan pelapisan 40 ~ 80 ℃ dan kepadatan arus 5 ~ 25A / dm2. Kondisi pelapisan dan hasil pelapisan platina ditunjukkan pada Tabel 3-7.
Tabel 3-7 Kondisi Pelapisan Platinum dan Hasilnya (nilai konsentrasi dalam tanda kurung)
| Nomor seri | Solusi pelapisan dampak | Solusi pelapisan platinum | Ketebalan pelapisan / μm | Tes pengupasan | ||
|---|---|---|---|---|---|---|
| Ion platinum/(g/L) | Ion halogen (fraksi massa)/% | Ion platinum/(g/L) | pH | |||
|
1 2 3 4 5 6 7 8 9 |
H2PtCl6 (0. 1) H2PtCl6 (0. 1) H2PtCl6 (0. 1) H2PtCl6 (1. 0) H2PtCl6 (1. 0) H2PtCl6 (1.0) H2PtCl6 (5.0) H2PtCl6 (5.0) H2PtCl6( 5. 0) |
HCl (5) HCl (5) HCl (5) HCl (10) HCl (10) HCl (10) HCl (20) HCl (20) HCl (20) |
K2Pt (OH)6 (5) K2Pt (OH)6 (10) K2Pt (OH)6 ⑸ Platinum dinitrat (5) Platinum dinitrate (10) Platinum dinitramide (20) K2Pt (OH)6 ⑸ K2Pt (OH)6 (10) K2Pt (OH)6 (20) |
12. 0 13. 0 13. 5 12. 0 13. 0 13. 5 12.0 13. 0 13. 5 |
10 15 20 10 15 20 10 15 20 |
Bagus. Bagus. Bagus. Bagus. Bagus. Bagus. Bagus. Bagus. Bagus. |
(2) Plating Platinum Using a Neutral Plating Solution
Using a nearly neutral plating solution is beneficial for pattern plating, as it avoids using alkali metals such as Na, preventing the adverse effects caused by the accumulation of alkali metals. The platinum plating solution proposed by Otani meets this condition. Table 3-8 shows the composition of the plating solution and its process condition tests.
Table 3-8 Composition and Process Conditions of Neutral Platinum Plating Solution Test
| Bahan-bahan dan kondisi prosesnya | Nomor 1 | Nomor 2 | Nomor 3 |
|---|---|---|---|
|
Dinitrodiammine platinum(Pt concentration)/(g/L) Glisin/(mol/L) Iminodiacetic acid/(mol/L) Diaminotriacetic acid/(mol/L) pH Suhu/°C Kepadatan arus/(A/dm2) Precipitation speed/(μm/min) Efisiensi saat ini/%
|
12 0. 57 - - 5.0 70 1. 0 0. 3 80 |
12 - 0. 3 - 5. 0 70 1. 0 0. 2 65 |
12 - 0. 1 0. 1 5. 0 70 1. 0 0. 1 65 |
Since this plating solution is close to neutral, it is favorable for pattern plating and will not adversely affect the counter-plating film.
Kamata from Japan also studied the effect of alkaline earth metals as brighteners. It was found that alkaline earth metals, such as Ca, Ba, Mg, etc., have a brightening effect on alkaline plating solutions. The suitable concentration of alkaline earth ions is (2×100)×10-6. The degree of brightness is also controlled by varying the concentration of alkaline earth metal ions added.
The main components and operating conditions of the plating solution are as follows:
| Main components of plating solution |
KOH 40g/L Pt [added in the form of K2Pt (OH)6] 20g/L Ca [added in the form of CaCl2 aqueous solution] Adequate amount |
| Operating conditions |
рH 13.5 Temperature 80℃ Current density 3A/dm2 Base metal Calendered copper plate Plating thickness 20μm |
Table 3-9 Effect of Ca Ion Concentration on the Brightness of the Pt Plating Layer
| Ca ion concentration/x10-6 | Penampilan | Ca ion concentration/x10-6 | Penampilan |
|---|---|---|---|
|
0 0. 1 0. 3 0. 5 0. 7 1. 0 |
Non-glossy Non-glossy Non-glossy Non-glossy Non-glossy Semi-glossy |
1. 5 2. 0 2. 5 3. 0 5. 0 - |
Semi-glossy Semi-glossy Semi-glossy Semi-glossy Mirror Bright - |
Copywrite @ Sobling.Jewelry - Produsen perhiasan khusus, pabrik perhiasan OEM dan ODM
Section III Platinum Alloy Plating
(1) Platinum-Iridium Alloy
Electroplated Pt-Ir alloy can be used on electrodes for soda ash production and electroplating.
The plating process conditions for the alloy proposed by Kamada et al. are shown in Table 3-10.
Table 3-10 Electroplating Pt-Ir Alloy Process Conditions
| Komposisi dan kondisi proses | Nomor 1 | Nomor 2 |
|---|---|---|
|
Sodium iridium hexachloride Asam borat Disodium malonate Sodium tetrachloroplatinate Potassium oxalate Sodium tetrabromoplatinate pH Suhu Kepadatan arus |
10 gram/L 40 gram/L 0,02 mol/L 0. 5~3g/L - - 5 85℃ 0. 5 A/dm2 |
10 gram/L 40 gram/L - - 0,02 mol/L 0. 5〜3g/L 2 85℃ 0. 5 A/dm2 |
The electroplating steps are to first flash plate 1μm gold on the brass sheet, then plate gold off, and finally plate a Pt-Ir alloy on top. The coating obtained by this method has good hardness, adhesion, heat resistance, and metal wire bonding connectivity, with a current efficiency reaching 100%.
Regarding this plating solution, if the pH is too low, the current density is too small to be practical; if the pH is too high, hydroxide precipitates are easily formed. If the temperature is too low, the alloy is difficult to deposit; if the temperature is too high, the plating solution evaporates quickly, which is unfavorable for maintaining the plating solution. If the current density is too low, the deposition rate is too slow; if the current density is too high, the cathodic reaction is mainly hydrogen evolution.
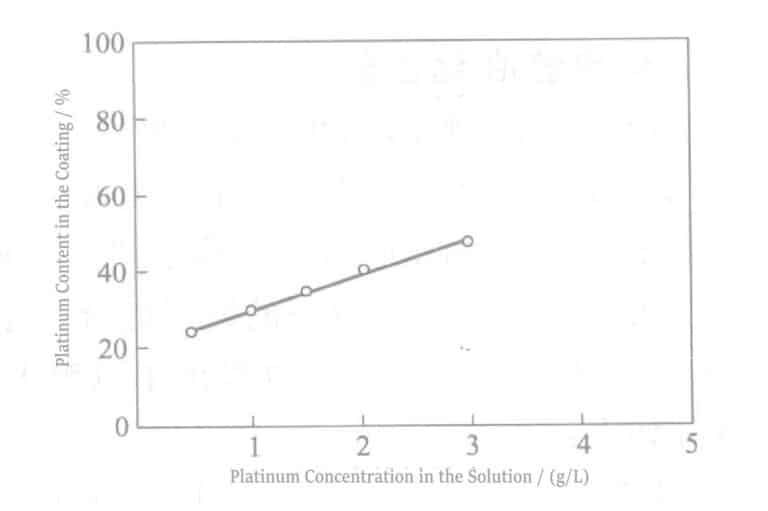
At the same time, the alloy composition in the plating film can also be controlled by adjusting the metal concentration ratio in the plating solution. Figure 3-1 shows the variation of alloy coating composition with the metal concentration ratio in the plating solution.
As can be seen from the figure, within the experimental concentration range, the Pt-Ir composition ratio in the plating layer has a linear relationship with the metal ion concentration ratio in the plating solution.
(2) Electroplating of Platinum-Iron Alloy
Alloys containing Fe are generally used as magnetic materials. The higher the recording density, the better. Platinum-iron alloys have high magnetic anisotropy, good corrosion resistance, and wear resistance and are expected to improve the performance of magnetic films.
Katsutsugu Koda proposed a plating solution formula with good stability that allows continuous electroplating. Since trivalent iron ions in the plating solution tend to form gels, this is detrimental to the appearance of the plating layer and reduces the concentration of divalent iron, negatively affecting the plating solution’s stability. Trivalent iron is generated based on the following reaction:
Pt4+ + 2e-→ Pt2+
2Fe2+ → 2Fe3+ + 2e-
From the above formula, from the perspective of considering the stability of iron ions, tetravalent platinum ions play a negative role, which led to the invention of divalent platinum to replace tetravalent platinum. The practice has proven that divalent platinum can be used for electroplating.
Table 3-11 shows the process conditions and results of binary Pt-Fe alloy electroplating. From the table, it can be seen that the metal atomic ratio of the Pt-Fe alloy coating obtained in No. 1~No. 3. It is close to. When the atomic ratio of the alloy is 50%, it is optimal as a magnetic film for recording.
Table 3-11 Process Conditions for Pt-Fe Binary Alloy Plating and Their Results
| Komposisi dan kondisi proses | Nomor 1 | Nomor 2 | Nomor 3 | Nomor 4 | Nomor 5 | |
|---|---|---|---|---|---|---|
| Platinum salt | Jenis | Pt(NH3)2(TIDAK2)2 | [Pt(NH3)4]Cl2 | Pt(NH3)2(TIDAK2)2 | Pt(NH3)2(TIDAK2)2 | Na[Pt(C2O4)2 |
| Konten | 5 gram/L | 5 gram/L | 5 gram/L | 5 gram/L | 10 gram/L | |
| Iron Salt | Jenis | FeSO4 - 7H2O | FeSO4 - 7H2O | FeSO4 - 7H2O | FeSO4 - 7H2O | FeSO4 - 7H2O |
| Konten | 2 gram/L | 30g / L | 30g / L | 10 gram/L | 20 gram/L | |
| Antioxidants | Jenis | Sodium sulfite | Hydroxyammonia chloride | L-Ascorbic acid | Citric acid hydrate | Hydroxyammonia sulfate |
| Konten | 5 gram/L | 3g / L | 3g / L | 40 gram/L | 50 gram/L | |
| Agen pengompleks | Jenis | Triammonium citrate | EDTA-2Na | Triammonium citrate | EDTA-2Na | Sodium oxalate |
| Konten | 50 gram/L | 10 gram/L | 15 gram/L | 2 gram/L | 30g / L | |
| Aditif | Jenis | - | Potassium dihydrogen phosphate | Potassium dihydrogen phosphate | Potassium ascorbyl phosphate | - |
| Konten | - | 15 gram/L | 15 gram/L | 5 gram/L | - | |
| Temperature of plating solution | 40℃ | 30℃ | 60℃ | 50℃ | 70℃ | |
| pH | 8 | 2 | 3 | 4 | 8 | |
| Kepadatan arus | 1A/dm2 | 2A/dm2 | 1A/dm2 | 1A/dm2 | 1.5A/dm2 | |
| Plating composition (atomization) | Pt | 51% | 49% | 55% | 72% | 37% |
| Fe | 49% | 51% | 45% | 28% | 63% | |
| Appearance of plated layer | O | O | O | O | O | |
(3) Electroplating of Platinum-Cobalt Alloy
The Pt-Co alloy film has a very high magnetic recording density, which is very attractive for the large capacity of magnetic recording media. Especially when its atomic ratio is 1:1, the performance is optimal.
Koda also researched Pt-Co alloys (see Table 3-12).
Table 3-12 Process Conditions and Results of Pt-Co Binary Alloy Plating
| Komposisi dan kondisi proses | Nomor 1 | Nomor 2 | Nomor 3 | Nomor 4 | Nomor 5 | |
|---|---|---|---|---|---|---|
| Platinum salt | Jenis | Pt(NH3)2(TIDAK2)2 | [Pt(NH3)4]Cl2 | Pt(NH3)2(TIDAK2)2 | Pt(NH3)2(TIDAK2)2 | Na[Pt(C2O4)2 |
| Konten | 2 gram/L | 5 gram/L | 5 gram/L | 2 gram/L | 10 gram/L | |
| Iron Salt | Jenis | CoSO4 - 7H2O | CoSO4 - 7H2O | CoSO4 - 7H2O | CoSO4 - 7H2O | CoSO4 - 7H2O |
| Konten | 30g / L | 30g / L | 2 gram/L | 45g/L | 20 gram/L | |
| Buffer(1) | Jenis | EDTA-2Na | Triammonium citrate | Triammonium citrate | Asam borat | Ammonium oxalate |
| Konten | 30g / L | 5 gram/L | 50 gram/L | 30g / L | 30g / L | |
| Buffer(2) | Jenis | Triammonium citrate | - | - | EDTA-2Na | - |
| Konten | 5 gram/L | - | - | 2 gram/L | - | |
| Conductive salt | Jenis | Sulfamic acid | Ammonium sulfate | Ammonium sulfate | Sulfamic acid | Ammonium sulfate |
| Konten | 15 gram/L | 15 gram/L | 15 gram/L | 20ml/L | 15 gram/L | |
| Antiprecipitant | Jenis | - | Amonia | - | - | - |
| Konten | - | 3g / L | - | - | - | |
| Temperature of plating solution | 60℃ | 50℃ | 40℃ | 50℃ | 70℃ | |
| pH | 3 | 2 | 4 | 3 | 4 | |
| Kepadatan arus | 1A/dm2 | 2A/dm2 | 4A/dm2 | 3A/dm2 | 4A/dm2 | |
| Plating composition (atomization) | Pt | 65% | 49% | 30% | 40% | 37% |
| Fe | 35% | 51% | 70% | 60% | 63% | |
| Appearance of plated layer | O | O | O | O | O | |
The alloy atomic ratio of the coating obtained from No. 2 in Table 3-11 is about 50%.
Hu Zhongmin et al. also proposed a plating Pt-Co alloy formula. Its main components are as follows:
|
Pt(NH3)2(TIDAK2)2 (as Co) 0.2~15g/L CoSO4 (as cobalt) 5~70g/L (Maintain Co:Pt=30:1) |
|
pH 1.2 (adjusted with NH2SO3H) Temperature 70℃ Current density 2A/dm2
|
(4) Platinum-Rhodium Alloy
Because Pt-W alloy coating has higher oxidation catalytic ability than Pt coating, people’s interest in Pt-W alloy plating has been aroused. Matsunori Sawada et al. proposed a platinum-tungsten alloy formula that can achieve a uniform appearance, good catalytic ability, and good plating solution stability.
A stable plating solution is obtained by adding organic acids or organic acid salts to the main components and then aging the mixture.
The organic acids used can be acetic acid, citric acid, oxalic acid, tartaric acid, etc. Representative components and concentrations are as follows:
H2PtCl4 2g/L(as Pt)
Na2WO4 • 2H2O 25g/L(as W)
Sodium citrate 5g/L
Citric acid 5g/L
Sodium sulfate 15g/L
Aging conditions 60℃×8h
Plating conditions 65℃ ,6mA/cm2 , 10min
Plating material Stainless steel wire mesh with a diameter of 0.3mm
Pre-plating treatments are:
Electrolytic degreasing→Water rinse→Hydrochloric acid soaking→Water rinse→Flash gold plating→Sulfuric acid soaking→Water rinse→Electroplating Pt-W Alloy
Suppose no aging treatment is applied and plating is done immediately using the prepared plating solution. In that case, the co-deposition of tungsten will be unstable, especially since the initial tungsten deposition will be low. The plating solution will gradually stabilize with continued use, and tungsten co-deposition will increase. A stable tungsten-containing plating layer can be obtained if the above aging treatment is used.
(5) Electroplating Platinum-Nickel Alloy
Hu Zhongmin proposed the main components of the electroplating Pt-Co alloy formula as follows:
(5) Electroplating Platinum-Nickel Alloy
Hu Zhongmin proposed the main components of the electroplating Pt-Co alloy formula as follows:
|
Pt(NH3)2(TIDAK2)2 (as Pt) 0.2~15g/L Nickel sulfamate (as Ni) 5~70g/L (maintain Ni:Pt=30:1) Sulfamic acid Adequate amount |
|
pH 1~1.4 (adjusted with sulfamic acid) Temperature 70°C Current density 2A/dm2 |
Section IV Chemical Plating of Platinum
In addition to being used in jewelry, catalysis, and heat-resistant materials, platinum can also be used as a thin film electrode for semiconductor components. Obtaining platinum thin films through chemical plating is a new approach. The reducing agents are generally hydrazine or hydrazine hydrate; hypophosphite is sometimes used.
Raitian refines platinum salts by passing carbon dioxide into a solution of hexaammineplatinum complex [Pt(NH3)6(OH)4], causing the platinum salt to precipitate and achieving stable and high-speed platinum electroplating.
The specific refining method is to pass carbon dioxide into a solution of hexaammineplatinum complex [Pt(NH3)6(OH)4] for about 3 hours to obtain a platinum salt precipitate. Then, filter, wash, dry the precipitate and dissolve the carbonate with an organic acid to obtain refined platinum salt for electroplating. The purpose of using organic salts is to avoid contamination by inorganic ions. Halide ions tend to adsorb onto the plated parts, reducing the deposition rate and causing the platinum film to darken. The presence of sulfate and nitrate ions can also cause appearance issues with the plating. The organic acids used are sulfonic acids, such as methanesulfonic or ethanesulfonic acid, or low molecular weight organic carboxylic acids, such as acetic or propionic acid.
To facilitate the volatilization and removal of carbon dioxide, the solution can be kept under reduced pressure when dissolving the platinum carbonate precipitate with organic acid.
Plating solution and process conditions:
Pt(NH3)6(CH3COO)4 (as Pt dissolved in acetic acid) 3g/L
Hydrazine hydrate 3mL/L
Glycerol ester (leveling agent) 20×10-6
pH (Adjusted with ammonia) 11
Temperature 60℃
Plated parts Aluminum oxide plate (activated)
Deposition speed 1.8μm/h
The leveling agent can be polyoxyethylene dodecyl ether, and the reducing agent can be replaced with hypophosphite.
Also using hydrazine hydrate as the reducing agent, Koslov Alexander’s formula is:
Pt(NH3)2(TIDAK2)2 (as Pt) 2g/L
Hydrazine hydrate (reducing agent) 3g/L
NH2OH – HC1(as stabilizer) Adequate amount
pH (adjusted with acetic acid) 3
Temperature 50℃
Deposition speed 0. 1μm/h
Table 3-13 Chemical Plating Pt Test
| Item | Test 1 | Test 2 | Test 3 |
|---|---|---|---|
| Test Characteristics | The ion-exchange membrane soaked in 5% (NH4)4PtCl2 solution was placed in a solution of 1g/L sodium hydroboride+1mg/L magnesium carbonate at 50℃ for 1h. | Ion exchange membrane soaked in 5% (NH4)4PtCl2 solution was placed in a solution of 1g/L sodium hydroboride + 10mg/L magnesium sulfate at 30℃ for 1h. |
HPtCl4 1g / L Sodium hydroboride 1g/L Calcium carbonate 10ml/L 80℃,1h Reaction of plate Al in the above solution by immersion |
| Base material | Cation exchange membrane | Cation exchange membrane | Aluminum plate |
| Platinum thickness | 0. 1mm | 0. 1mm | 0. 1mm |
| Platinum particle diameter | Below 10μm | Below 10μm | Below 10μm |
| Surface resistance | 10Ω/cm | 10Ω/cm | 10Ω/cm |
In this reaction, alkaline earth metals are required; they can dissolve with the reducing agent (as in Experiment 1, Experiment 2) or be added to the plating solution (as in Experiment 3). However, the mechanism of action of alkaline earth metals is unclear. The better the compactness of the plating layer, the fewer defects, such as cracks in the plating layer, which can ensure a relatively low resistance and thus guarantee the quality of the electrode.
Kenji Takahashi proposed a chemical plating scheme using tetravalent platinum ammonium salt as the main salt. The general form of the platinum salt is [Pt(NH3)6X]. In the formula X can be a halide ion, OH- group, SO42-, etc.
Its composition is:
Platinum salt (tetravalent platinum ammonium salt) (in platinum) 0. 5〜5.0g/L
Ammonia (28%) 10〜100g / L
Water and hydrazine (reducing agent) 0. 5〜5g/L
рH 10〜12. 5
Plating solution temperature 50〜70℃