Proč mají drahé kameny více barev?
Úvod do teorie krystalového pole & teorie molekulových orbitalů & teorie energetických pásů
Barvy drahých kamenů jsou bohaté a rozmanité a mají jedinečné kouzlo, které lidé odjakživa milují. Kvalita drahých kamenů do značné míry závisí na jejich barvě. Barva drahého kamene je důležitým ukazatelem při hodnocení drahých kamenů a většina optimalizačních úprav drahých kamenů zahrnuje změnu nebo zlepšení jejich barvy. Proto je pochopení příčin zbarvení drahých kamenů zásadním předpokladem pro optimalizační ošetření drahých kamenů. Pouze na základě znalosti toho, jak drahé kameny získávají svou barvu, lze určit, zda lze drahý kámen optimalizovat, jaké optimalizační schéma přijmout a jaký experimentální plán stanovit. Existuje pět běžných teorií zbarvení drahých kamenů: klasická mineralogická teorie, teorie krystalového pole, teorie molekulových orbitalů, teorie energetických pásů a fyzikální optické efekty. Tyto teorie tvoří teorie zbarvení běžných přírodních drahých kamenů a níže je uveden stručný úvod do těchto pěti teorií zbarvení.
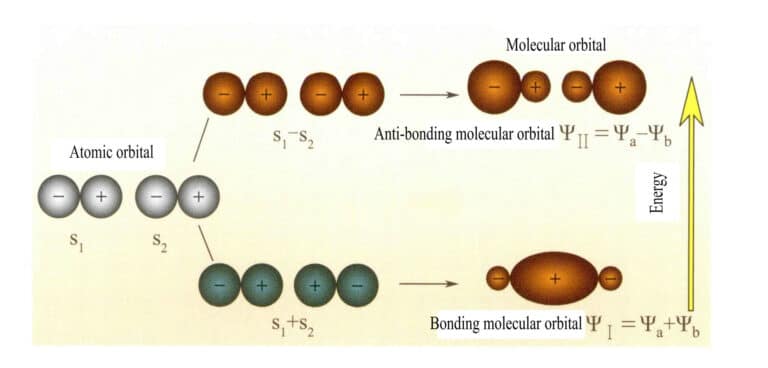
Molekulové orbitaly tvořené dvěma s atomovými orbitaly
Obsah
Oddíl I Teorie krystalového pole
Ve 30. letech 20. století navrhli vědci teorii krystalového pole, která vysvětluje vlastnosti krystalů. Teorie krystalového pole je teorie, která studuje chemické vazby přechodných prvků (komplexů). Vysvětluje fyzikální a chemické vlastnosti přechodných prvků a lanthanoidů kombinací některých hledisek elektrostatické teorie, kvantové mechaniky a teorie grup (teorie, která studuje symetrii hmoty) se zaměřením na vliv ligandů na d a f orbitaly centrálních iontů. V 50. letech 20. století lidé aplikovali teorii krystalového pole na komplexy a navrhli teorii ligandového pole. Teorie ligandového pole je pokrokem teorie krystalového pole; bere v úvahu jak vliv elektrického pole ligandu na centrální ion, tak vyplňující účinek elektronů ligandu na centrální ion, takže je úplnější než teorie krystalového pole. Mezi oběma teoriemi však není zásadní rozdíl a při studiu anorganických minerálů se obecně nerozlišují.
1. Základní pojmy teorie krystalového pole
Ionty přechodných kovů jsou v krystalovém poli okolních aniontů nebo dipólových molekul. Teorie krystalového pole je elektrostatický model, který nahlíží na krystal jako na elektrostatickou interakci mezi kladnými a zápornými ionty, kde kladně nabitý kationt se nazývá centrální ion a záporně nabitý aniont se nazývá ligand.
Použití teorie krystalového pole k vysvětlení barvy minerálů drahých kamenů zahrnuje především d elektrony nebo f elektronovou energii iontů přechodných prvků. Například d orbitaly mají pět typů: dxy, dxz, dyz, d , a d . Těchto pět d orbitalů má ve volném stavu iontu různé prostorové rozložení, ale mají stejnou energii. Pod vlivem ligandového pole však podléhají významným změnám. Pět energeticky degenerovaných d orbitalů centrálního atomu se rozštěpí pod vlivem záporného elektrického pole vytvořeného okolními ligandy. Některé d orbitaly mají zvýšenou energii, zatímco jiné mají sníženou energii. V důsledku rozštěpení energetických hladin d orbitalů se elektrony v d orbitalech centrálního atomu přeskupí a přednostně obsadí orbitaly s nižší energií, čímž se sníží celková energie systému a komplex se stane stabilnějším.
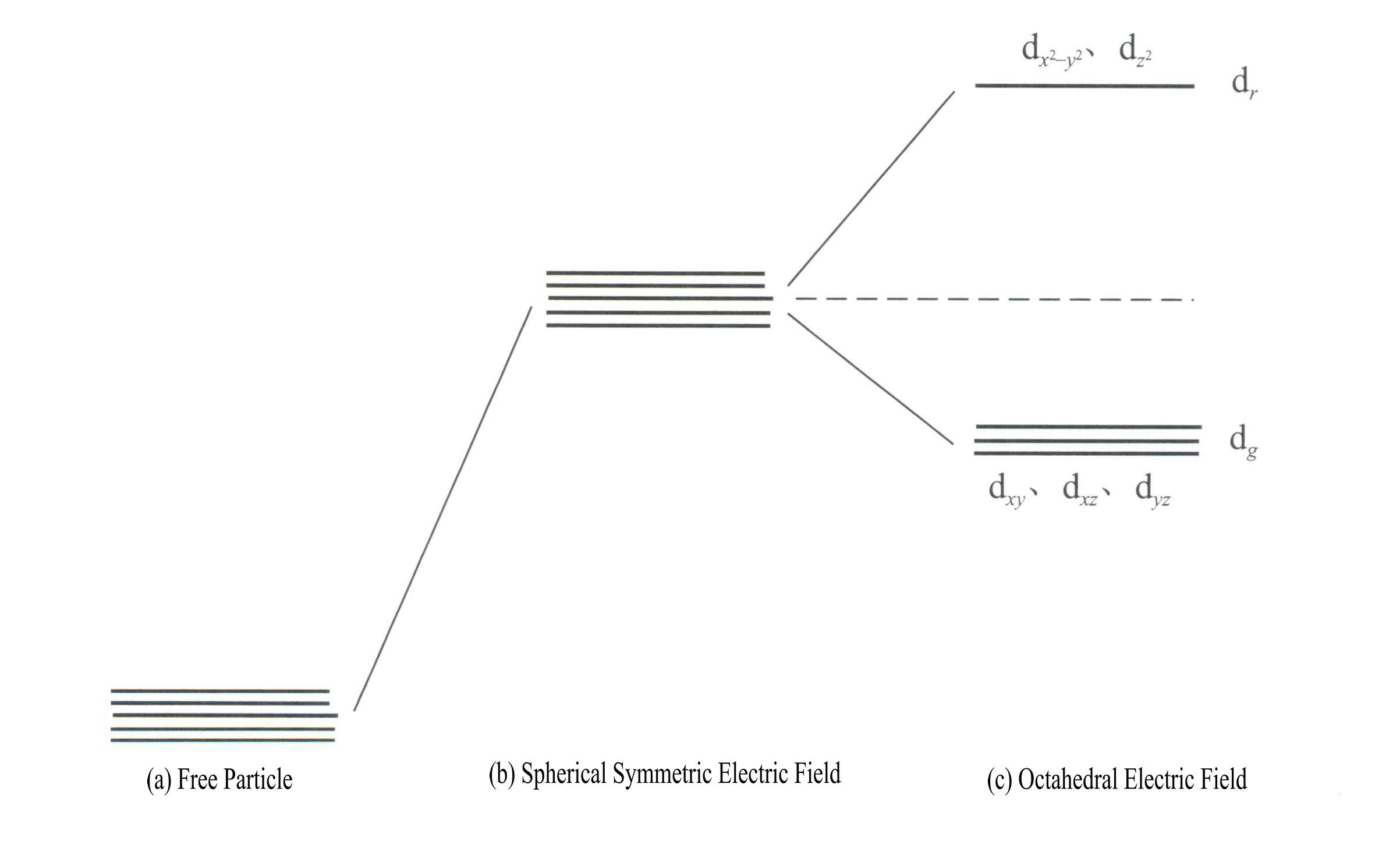
Energie d orbitalů je stejná, když neexistuje elektrické pole [obrázek 3-19 (a)]; při sféricky symetrickém elektrostatickém poli mají d orbitaly zvýšenou energii, ale nerozštěpí se [obrázek 3-19 (b)]; když je ligandové pole oktaedrické, rozštěpí se na dr a dg. Z nich dr se skládají z orbitalů d a d , které mají vyšší energii; orbitaly d s nižší energií se skládají z dg se skládají z orbitalů dxy, dxz, dyz.
Ionty přechodných kovů jsou v krystalovém poli okolních aniontů nebo dipólových molekul. Teorie krystalového pole je elektrostatický model, který nahlíží na krystal jako na elektrostatickou interakci mezi kladnými a zápornými ionty, kde kladně nabitý kationt se nazývá centrální ion a záporně nabitý aniont se nazývá ligand.
Použití teorie krystalového pole k vysvětlení barvy minerálů drahých kamenů zahrnuje především d elektrony nebo f elektronovou energii iontů přechodných prvků. Například d orbitaly mají pět typů: dxy, dxz, dyz, d , a d . Těchto pět d orbitalů má ve volném stavu iontu různé prostorové rozložení, ale mají stejnou energii. Pod vlivem ligandového pole však podléhají významným změnám. Pět energeticky degenerovaných d orbitalů centrálního atomu se rozštěpí pod vlivem záporného elektrického pole vytvořeného okolními ligandy. Některé d orbitaly mají zvýšenou energii, zatímco jiné mají sníženou energii. V důsledku rozštěpení energetických hladin d orbitalů se elektrony v d orbitalech centrálního atomu přeskupí a přednostně obsadí orbitaly s nižší energií, čímž se sníží celková energie systému a komplex se stane stabilnějším.
Energie d orbitalů je stejná, když neexistuje elektrické pole [obrázek 3-19 (a)]; při sféricky symetrickém elektrostatickém poli mají d orbitaly zvýšenou energii, ale nerozštěpí se [obrázek 3-19 (b)]; když je ligandové pole oktaedrické, rozštěpí se na dr a dg. Z nich dr se skládají z orbitalů dx2– y2 a dz2
, s vyšší energií; nižší energie dg se skládají z orbitalů dxy, dxz, dyz. [Obrázek 3-19 (c)]
Rozdíl mezi nejvyšší a nejnižší energetickou hladinou po rozštěpení orbitalu d se nazývá separační energie △ . Separační energie vzniklé při různých konfiguracích ligandových polí nejsou stejné (obr. 3-20). Jejich energetické pořadí je následující:
Čtvercové pole > osmistěnné pole > čtyřstěnné pole

I u polí stejné konfigurace se mohou lišit v důsledku rozdílů v ligandech a centrálních iontech; čím je větší, tím je krystal stabilnější. O velikosti separační energie krystalu rozhodují především následující tři faktory:
(1) Krystaly tvořené stejným přechodným prvkem; pokud jsou ligandy stejné, platí, že čím větší je náboj centrálního iontu, tím větší je separační energie △ . Čím vyšší je kladný náboj centrálního iontu, tím větší je přitažlivost ligandů, což vede k menší vzdálenosti mezi centrálním iontem a jádrem ligandu, a čím větší je odpudivá síla krystalového pole vytvářená ligandy na elektrony, tím větší je separační energie △ .
(2) U krystalů tvořených různými ionty se stejným kladným nábojem a stejnými ligandy platí, že čím větší je poloměr centrálního iontu, tím dále jsou d orbitaly od jádra a tím větší je separační energie △ .
(3) U krystalů tvořených stejným centrálním iontem a různými ligandy se separační energie liší v důsledku rozdílné síly krystalového pole ligandu. Různé ligandy mají různé intenzity pole a separační energie △ se mění v závislosti na intenzitě pole ligandu.
Separační energie slouží ke kvalitativnímu vysvětlení stability krystalů; není nutné získat absolutní hodnotu △ , protože stačí znát relativní hodnoty krystalu za různých podmínek.
Na základě relativní energie rozdělených d orbitalů lze vypočítat celkovou energii iontů přechodných kovů v d orbitalech. Tato energie je nižší než před štěpením, a poskytuje tak krystalu dodatečnou energii, známou jako energie stabilizace krystalového pole, označovanou symbolem CFSE. V tabulce 3-10 jsou uvedeny stabilizační energie iontů obsahujících dn elektronů za různých podmínek.
Tabulka 3-10 Energie stabilizace krystalového pole při různých ligandech (Wu Ruihua, 1994)
| dn | Slabé pole | Silné pole | ||||
|---|---|---|---|---|---|---|
| dn | Čtverec | Pravidelný osmistěn | Pravidelný tetraedr | Čtverec | Pravidelný osmistěn | Pravidelný tetraedr |
| d0 | 0 | 0 | 0 | 0 | 0 | 0 |
| d1 | 5.14 | 4 | 2.67 | 5.14 | 4 | 2.67 |
| d2 | 10.28 | 8 | 5.34 | 10.28 | 8 | 5.34 |
| d3 | 14.56 | 12 | 3.56 | 14.56 | 12 | 8.01 |
| d4 | 12.28 | 6 | 1.78 | 19.70 | 16 | 10.68 |
| d5 | 0 | 0 | 0 | 24.84 | 20 | 8.90 |
| d6 | 5.14 | 4 | 2.67 | 29.12 | 24 | 6.12 |
| d7 | 10.28 | 8 | 5.34 | 26.84 | 18 | 5.34 |
| d8 | 14.56 | 12 | 3.56 | 24.56 | 12 | 3.56 |
| d9 | 12.28 | 6 | 1.70 | 12.28 | 6 | 1.78 |
| d10 | 0 | 0 | 0 | 0 | 0 | 0 |
2. Barevné charakteristiky iontů přechodných kovů
V jeho barevných drahých kamenech je barva většiny drahých kamenů způsobena ionty přechodných kovů a barva drahých kamenů souvisí s tím, zda barvicí ionty obsahují nespárované elektrony na d nebo f orbitalech. Barevné vlastnosti iontů přechodných kovů zahrnují především následující aspekty:
(1) Zbarvení iontů přechodných kovů souvisí s elektronickými stavy d orbitalu nebo f orbitalu. Pokud jsou elektrony orbitalu d nebo f zaplněné nebo prázdné, drahokam nevykazuje barvu. Například Cr6+, Ce4+a Cu+.
(2) Různé barvicí ionty vykazují ve stejném materiálu drahého kamene různé barvy. Vzhledem k rozdílným separačním energiím různých barvicích iontů se mohou i ve stejném materiálu projevovat různými barvami. Například Fe2+ vytváří ve spinelu mírně šedomodrou barvu, zatímco Cr3+ produkuje červenou barvu.
(3) Barevné ionty téhož prvku v různých valenčních stavech mají často ve stejném materiálu drahého kamene různé barvy. Protože energie potřebná pro přechody d-elektronů centrálního iontu je různá, jsou absorbované vlnové délky světla různé, což vede k různým barvám. Například kastrum obsahující Mn2+ má jemně růžový odstín, zatímco beryl obsahující Mn2+ představuje jasně červenou barvu, známou jako červený beryl.
(4) Barevné ionty téhož prvku ve stejném valenčním stavu mají často různé barvy, když jsou v různých konfiguracích ligandů. Například Co2+ v tetraedrické konfiguraci spinelu vykazuje charakteristickou "diamantově modrou" barvu, zatímco v oktaedrické konfiguraci kalcitu se jeví jako růžový. Fe2+ v oktaedricky koordinovaném olivínu vykazuje charakteristickou olivově zelenou barvu, zatímco v deformovaném kubicky koordinovaném almandinu se jeví jako sytě červená.
(5) Stejný typ barevných iontů má stejný valenční stav a koordinační geometrii, ale různé sousední koordinační atomy vykazují různé barvy. Například v tetraedrické koordinaci Co2+, ve sfaleritu, Co2+ je spojen se sírou, což se projevuje zeleně, zatímco ve spinelu je Co2+ je připojen ke kyslíku a zobrazuje se modře.
(6) Stejný typ barevných iontů se stejným valenčním stavem, koordinační geometrií a sousedními atomy má v různých drahých kamenech různé barvy. Deformace koordinační geometrie způsobená rozdílným chemickým složením drahých kamenů mění povahu chemických vazeb mezi centrálním iontem a koordinačními ligandy, čímž se mění přechodová energie elektronů d. Například Cr3+ v rubínu je červený, ve smaragdu zelený a v alexandritu vykazuje proměnlivé barvy. Důvodem těchto změn v Cr3+ souvisí s jeho vlastnostmi a sousedními koordinačními ligandy, přičemž analýza specifických vlastností je následující.
① Cr3+ Charakteristika:
Cr3+ má vnější elektronovou slupku 3s23p63d3s 11 elektrony ve vnější slupce, které patří do nepravidelné (8-18) elektronové struktury.
Tato struktura má menší stínicí účinek na jádro než struktura s 8elektronovou slupkou, což vede k tomu, že Cr3+ má větší efektivní kladný náboj a zároveň menší iontový poloměr, což tvoří základní charakteristiku Cr3+: silné kladné elektrické pole a prázdné d orbitaly. Cr3+ může poskytnout šest prázdných orbitalů pro šest koordinačních ligandů s prostorovou konfigurací oktaedrickou, patřící do d2sp3 hybridizace (obrázek 3-21).
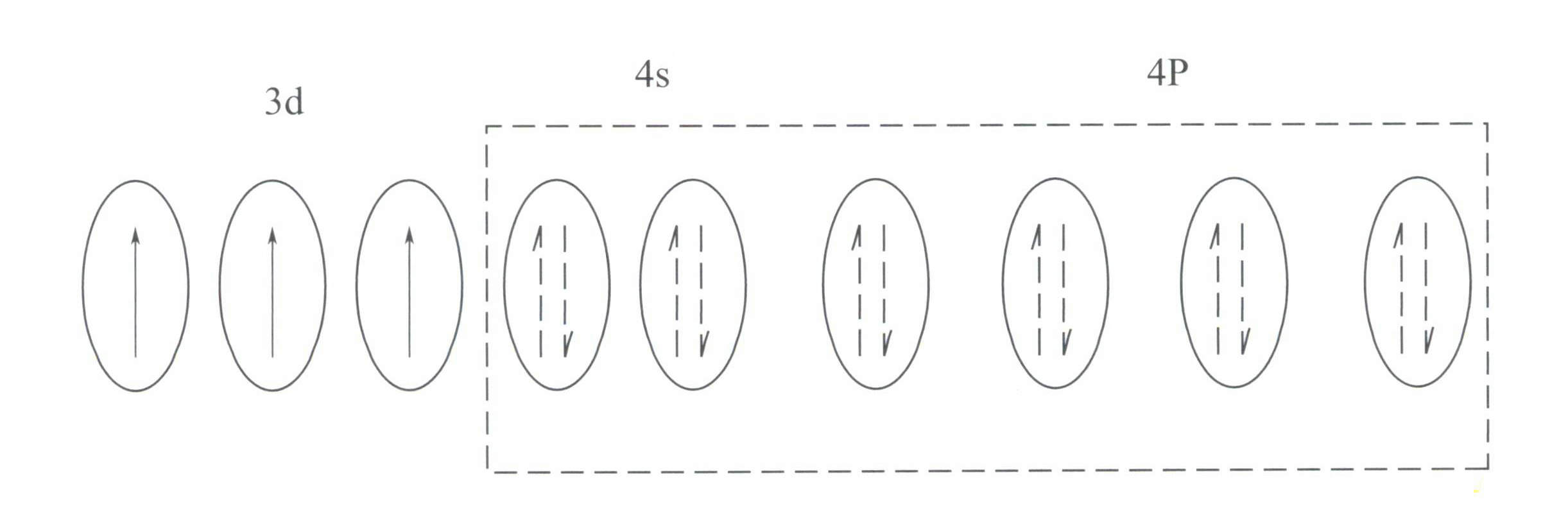
Podle teorie krystalového pole jsou v oktaedrickém poli d orbitaly Cr3+ se může rozdělit na nižší energii dƐ a vyšší energie dr oběžná dráha. Protože tři d elektrony Cr3+ jsou všechny v dƐ a všechny jsou jednoduché elektrony, může ve viditelném světle docházet k d-d přechodům, které způsobují, že drahokamy obsahující Cr3+ vykazovat barvu.
② Mechanismus barvení Cr3+:
V rubínu Hlavní chemickou složkou rubínu je Al2O3. Když několik procent Cr3+ nahrazuje Al3+, vytváří jasně červenou barvu. Ve struktuře rubínu je díky většímu poloměru Cr3+ v porovnání s poloměrem Al3+, Cr3+ vstupuje do mřížky korundu a snižuje symetrii kolem oxidu hlinitého.
D orbitaly Cr3+ a když se elektrony v excitovaném stavu vracejí z D nebo C do základního stavu A, musí nejprve projít B, čímž se uvolní teplo. Z B se vracejí do A za doprovodu luminiscence a vyzařují červenou fluorescenci. Při tomto procesu elektrony absorbují světelnou energii, což způsobuje, že rubín absorbuje D fialové (400 nm) a C žlutozelené (555 nm) viditelné spektrum (obrázek 3-22) a vytváří absorpční pás.

Při průchodu bílého světla rubínem jsou fotony ve spektru od fialové po žlutozelenou absorbovány, zatímco téměř všechno červené světlo a část modrého světla prochází, což dává rubínu sytě červenou barvu s nádechem do fialova, známou jako holubí krev.
Rubíny vykazují krátkou absorpci na úrovni B, která se projevuje červenou fluorescencí. Tato absorpce na úrovni B, která způsobuje červenou fluorescenci, činí barvu rubínu živější; čím vyšší je obsah chromových iontů, tím silnější je fluorescence.
Ionty železa v drahém kameni mohou potlačovat fluorescenci absorpce na úrovni B, což vysvětluje jev, kdy se rubíny s příměsí železa jeví tmavší.
③ Cr3+ Mechanismus zbarvení smaragdů
Hlavní chemickou složkou smaragdu je Be3Al2Si6O18, Cr3+, která nahrazuje Al3+ ve smaragdové mřížce a Cr3+ je také obklopen oktaedrem složeným ze šesti iontů kyslíku, kde Cr3+Délka vazby -O je také velmi podobná délce vazby v rubínech. Ve srovnání s rubíny však mají smaragdy o dva ionty více, Be2+ a Si4+. Ve struktuře smaragdů se zvyšuje kovalentní charakter vazeb mezi oxidy kovů, zatímco iontové vlastnosti slábnou.
Drobné změny, jako jsou chemické vazby, vedou k mírnému snížení obsahu Cr3+C a D hladiny, což vede k mírnému posunu absorpčního pásu (Obrázek 3-23), který ve spektru výrazně blokuje propustnost modrofialového (425 nm) a oranžovožlutého (608 nm) světla a zároveň zvyšuje propustnost modrozeleného světla, čímž vzniká charakteristická smaragdově zelená barva.

Absorpce dioptázy na úrovni B se téměř nezměnila. Pokud nečistota železo nemá ve smaragdové složce "inhibiční" účinek, silná červená fluorescence způsobuje, že charakteristická smaragdová zeleň září ještě jasněji.
④ Cr3+ Barevný mechanismus alexandritu:
Barva alexandritu je rovněž způsobena Cr3+ nahrazující Al3+ v deformované oktaedrické koordinaci. Vzhledem k chemickému složení alexandritu, který je BeAL2O4, povaha chemických vazeb mezi jeho kovovými ionty a kyslíkem leží mezi rubínem a smaragdem. Proto také jeho absorpční pásy leží mezi pásy rubínu a smaragdu, přičemž pravděpodobnosti přenosu modro-fialového a oranžovo-žlutého světla jsou přibližně stejné, což znemožňuje určit, zda převažuje červené nebo modro-zelené světlo (obrázek 3-24).
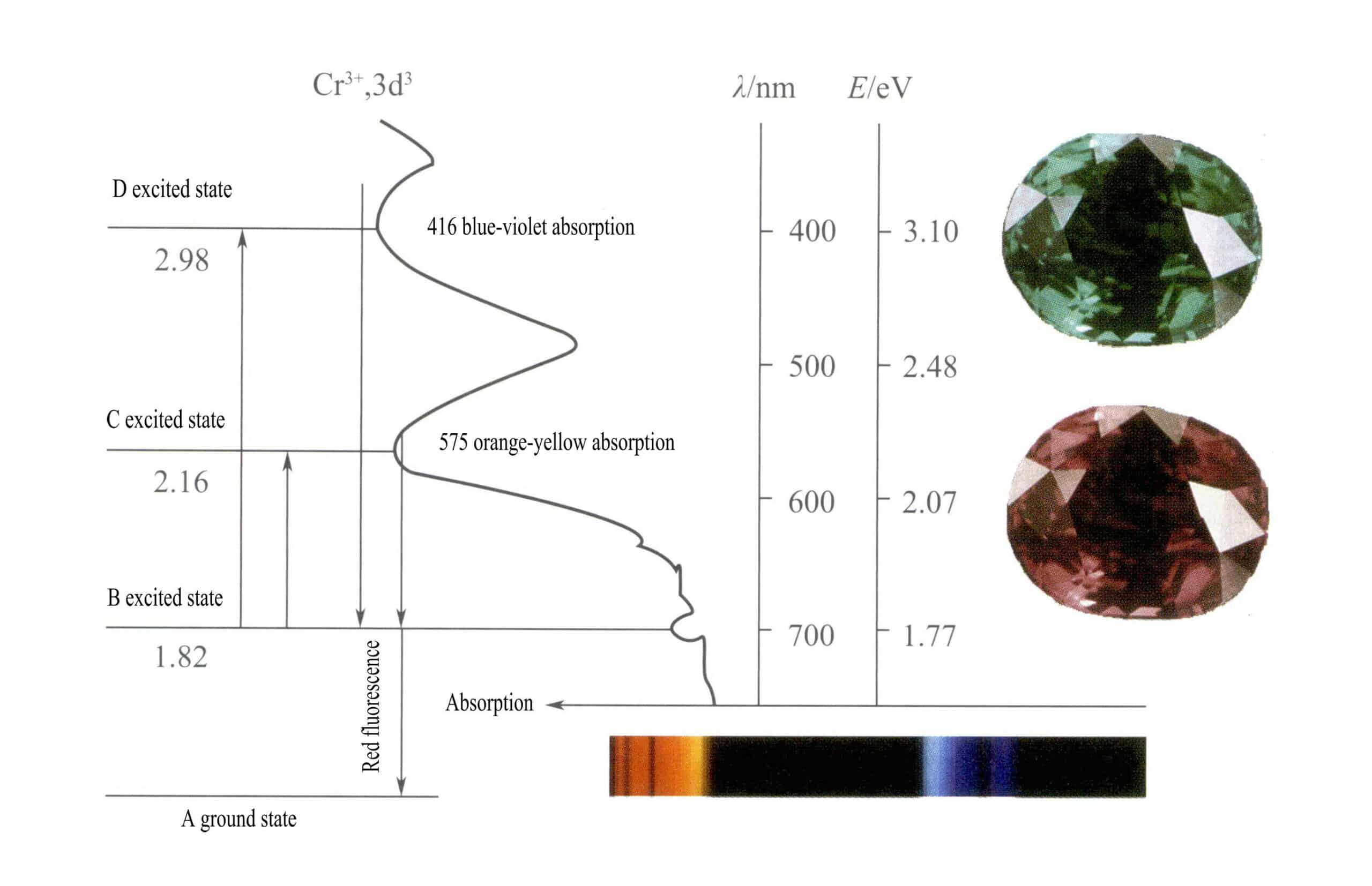
Proto může barva alexandritu záviset pouze na rozložení energie a barevném rozsahu dopadajícího světla, což vede k "efektu změny barvy" alexandritu, tj. jeví se zelený v denním světle s vysokým podílem modré složky světla a červený v žárovkovém světle s vysokým podílem červené složky světla. Proto se alexandritu často říká "smaragd ve dne a rubín v noci".
"Efekt změny barvy" se objevuje u mnoha druhů drahých kamenů, například u korundu měnícího barvu a granátu měnícího barvu. V současné době se uměle syntetizovaný korund měnící barvu vyrábí na principu změny barvy, přičemž se používá V3+ jako barvicí iont pro syntézu.
3. Barvy drahých kamenů
Z chemického složení minerálů drahých kamenů lze odvodit barvy, které vytvářejí složky přechodných kovů. Například tyrkys obsahující Cu2+ musí být modrá, zatímco Cu+ je bezbarvý. Tabulka 3-11 uvádí barvy, které vytvářejí běžné složky přechodných kovů v přírodních minerálech drahých kamenů.
Tabulka 3-11 Barvy vytvářené složkami přechodných kovů v přírodních drahých kamenech
| Prvek | Barva | Běžné minerály |
|---|---|---|
| Cer (Ce) | Žlutý | Parisite |
| Chrom (Cr) | Červená, zelená, oranžová atd. | Crocoisite, Red Crocoisite, Uvarovite |
| Kobalt (Co) | Modrá | Syntetický spinel |
| Měď (Cu) | Modrá, zelená | Azurit, chryzokol, tyrkysový malachit, dioptáz |
| Železo (Fe) | Červená, zelená, žlutá | Almandin, olivín, goethit |
| Mangan (Mn) | Růžová, oranžová | Rodonit, spessartin |
| Nikl (Ni) | Zelená | Bunsenit, chalcedon |
Barvu většiny drahých kamenů způsobují příměsi přechodných kovů, které obsahují. Například rubíny vypadají červeně díky stopovému množství Cr3+. Barvu drahého kamene ovlivňují různé faktory způsobené ionty nečistot. Nečistoty proto mohou u různých drahých kamenů vyvolat různé barvy. Například Cr3+ v rubínech se objevuje červená a ve smaragdech zelená.
Stejné nečistoty nemusí nutně způsobit stejnou barvu drahého kamene. Například zelenou barvu většiny smaragdů způsobuje Cr, zatímco zelená barva některých smaragdů je částečně nebo zcela způsobena vanadem (V).
Teorii krystalového pole lze použít nejen k vysvětlení barev drahých kamenů, které jsou tvořeny složkami nebo příměsemi přechodných kovů, ale také barev, které jsou tvořeny strukturními defekty (barevnými centry); konkrétní proces vzniku barev je uveden v kapitole 3.3 této knihy.
Vysvětlení barev minerálů drahých kamenů pomocí teorie krystalového pole má také nedostatky, které se projevují především v následujících aspektech:
(1) Elektrony centrálního iontu d nejsou zcela lokalizovány ve svých původních orbitalech. Mohou se objevit i v okolí koordinačních atomů, což svědčí o kovalentní interakci mezi centrálním atomem a ligandy.
(2) Uvažuje pouze elektrostatickou iontovou interakci mezi centrálním atomem a ligandy a zcela ignoruje kovalentní vazebné interakce mezi centrálním atomem a ligandy. Ve fyzikálním výzkumu se výsledky kvantitativních výpočtů často výrazně liší od skutečné situace.
(3) Příčiny barvy minerálů drahých kamenů mohou být vedle interakce mezi centrálním iontem a ligandy způsobeny také kombinací účinků strukturních defektů a krystalového pole.
Oddíl II Teorie molekulových orbitalů
Mulliken a Hund původně navrhli teorii molekulových orbitalů (MO teorie). Díky neustálému zkoumání mnoha vědců se vyvinula ve vyspělou teorii. Molekulové orbitaly (MO) lze získat lineárními kombinacemi atomových orbitalů, což je běžně používaná metoda konstrukce molekulových orbitalů. Z n atomových orbitalů lze získat n molekulových orbitalů a koeficienty lineárních kombinací lze určit pomocí variační metody nebo jiných metod. Molekulové orbitaly tvořené dvěma atomovými orbitaly s energetickými hladinami nižšími než atomové orbitaly se nazývají vazebné orbitaly; orbitaly s energetickými hladinami vyššími než atomové orbitaly se nazývají antivazebné orbitaly; orbitaly s energetickými hladinami blízkými atomovým orbitálům jsou obecně nevazebné orbitaly.
Teorie molekulových orbitalů je teorie používaná k vysvětlení otázek, jako je vznik, struktura a vlastnosti molekul. Lze jí také vysvětlit některé příčiny barev drahých kamenů, které byly vyvinuty na základě teorie krystalového pole a teorie molekulových orbitalů přechodných kovů. Molekulární orbitaly jsou přirozeným rozšířením atomových orbitalů. V molekule již elektrony nepatří konkrétnímu atomu, ale pohybují se v celém molekulovém rozsahu; proto se pohyb elektronů v molekule popisuje pomocí molekulových orbitalů.
1. Základní pojmy teorie molekulových orbitalů
Teorie molekulových orbitalů tvrdí, že poté, co atomy vytvoří molekulu, elektrony již nepatří do původních atomových orbitalů, jak navrhuje teorie krystalového pole, ale pohybují se v rámci určitých molekulových orbitalů. Molekulární orbitaly tvoří molekulu stejně jako atomové orbitaly tvoří atom. Valenční elektrony již nejsou považovány za lokalizované v rámci jednotlivých atomů, ale pohybují se v celé molekule. Rozložení elektronů v molekule lze řešit podle principů rozložení elektronů v atomech (princip minimální energie a Hundovo pravidlo).
Lineární kombinace atomových orbitalů v molekule tvoří molekulové orbitaly. Počet molekulových orbitalů se rovná počtu atomových orbitalů před kombinací. Kombinace atomových orbitalů do efektivních molekulových orbitalů musí dodržovat následující tři zásady:
(1) Princip shody symetrie: Pouze atomové orbitaly se stejnou symetrií mohou tvořit molekulové orbitaly.
(2) Princip energetické blízkosti: Pouze atomové orbitaly s podobnou energií se mohou spojit do efektivních molekulových orbitalů.
(3) Princip maximálního překryvu: Čím větší je překryv atomových orbitalů, tím více klesá energie výsledných molekulových orbitalů a tím stabilnější je výsledná chemická vazba.
Molekulový orbital ψ je vlnová funkce jednoho elektronu. Lze ji znázornit jako lineární kombinaci atomových orbitalů, přičemž každému orbitalu odpovídá určitá energie, která je součtem kinetické a potenciální energie elektronu pohybujícího se v molekulovém elektrickém poli. Dva atomové orbitaly, a a b, prostřednictvím překrývajících se lineárních kombinací vytvářejí dva molekulové orbitaly ψI a ψII :
ψI=ψa + ψb (3-5)
ψII = ψa - ψb (3-6)
Když jsou molekulové orbitaly s elektrony zaplněny jako první, vazebné orbitaly ψI jsou naplněny jako první. Když elektrony zaplňují molekulové orbitaly se stejnou energií, měly by podle Hundova pravidla co nejvíce obsazovat i různé molekulové orbitaly se stejným směrem spinu.
Molekulární orbitaly ψI získané sečtením dvou atomových orbitálních funkcí (rovnice 3-5) se nazývají vazebné molekulové orbitaly. Molekulové orbitaly ψII získané odečtením dvou atomových orbitálních funkcí (rovnice 3-6) se nazývají antivazebné molekulové orbitaly. Energie vazebných molekulových orbitalů je nižší než energie antivazebných molekulových orbitalů a nižší než energie původních dvou atomových orbitalů. Stejně jako v případě zaplňování atomových orbitalů se tedy i při zaplňování molekulových orbitalů elektrony nejprve umístí do vazebných orbitalů a molekulový orbital může pojmout dva elektrony s opačnými spiny. Když elektrony zaplňují molekulové orbitaly se stejnou energií, měly by podle Hundova pravidla obsadit pokud možno také různé molekulové orbitaly se stejným směrem spinu. Molekulové orbitaly tvořené dvěma s atomovými orbitaly jsou znázorněny na obrázku 3-25.

p Orbitaly a d orbitaly mohou také tvořit molekulové orbitaly různých energetických hladin; například kombinace dvouatomových molekulových orbitalů v O2 molekul je poměrně složitý.
Při experimentech byly změřeny magnetické vlastnosti těchto dvou jednotlivých elektronů, což poskytlo silnou podporu pro teorii molekulárních orbitalů. Na rozdíl od molekul složených ze stejných atomů mají molekuly složené ze dvou nebo více různých atomů složitější molekulové orbitální energetické hladiny, ale princip je stejný.
2. Charakteristiky zbarvení přenosu náboje
Tato teorie molekulových orbitalů, kde celá molekula sdílí elektrony, je také považována za přechod elektronů z jednoho atomového orbitalu na druhý, známý jako přenos náboje. K přenosu náboje může docházet při interakcích kov-kov (M-M), nekov-nekov (L-L) a nekov-kov (L-M). Mezi nimi jsou L-L, M-L tyto dva typy vazeb často především kovalentní vazby. O2 patří k přenosu náboje L-L, což je kovalentní vazba.
(1) Přenos náboje kov-kov (M - M Charge Transfer)
K tomuto typu přenosu náboje obvykle dochází mezi ionty běžných přechodných kovů. Většina příčin zbarvení barevných drahých kamenů vzniká přenosem náboje mezi kovy. Přenos náboje M-M zahrnuje především následující typy: Fe2+ - Fe3+/Fe3+ - Fe2+; Ti3+ - Ti4+ / Ti4+- T3+ ;Fe2+ - T4+/Fe3+ - T3+; Mn2+ - Mn4+/Mn3+ - Mn3+ . Přenos náboje mezi kovy se dělí na dva typy: přenos náboje mezi homojadernými atomy a přenos náboje mezi heterojadernými atomy.
① Přenos náboje mezi izoelektronickými atomy
K přenosu náboje mezi izoelektronickými atomy dochází mezi dvěma atomy téhož přechodného kovového prvku v různých oxidačních stavech. Například Fe2+ a Fe3+ podléhají přenosu náboje za různých redoxních podmínek, absorbují energii a vytvářejí barvu. Modrofialová barva iolitu vzniká přenosem náboje iontů železa v různých oxidačních stavech. Fe3+ a Fe2+ jsou v tetraedrické, resp. oktaedrické poloze se dvěma ligandy spojenými hranami. Když na iolit svítí viditelné světlo, jeden elektron d Fe2+ absorbuje světlo o určité energii a přechází na Fe3+absorbuje žluté světlo o vlnové délce 588 nm a vytváří modrofialovou barvu. Akvamarín, zelený turmalín a další mohou rovněž vykazovat barvu způsobenou přenosem náboje mezi ionty železa.
② Přenos náboje mezi heteroatomy
Modré safíry jsou nejtypičtějším příkladem barvy, která vzniká přenosem náboje mezi dvěma typy iontů přechodných kovů. Koordinační polyedry iontů přechodných kovů jsou spojeny hranami nebo stěnami, což usnadňuje přenos náboje mezi kovy.
Například v safírech, kde ionty železa a titanu vstupují do spojených oktaedrů, existují Fe i Ti ve dvou oxidačních stavech:
Fe2+ + Ti4+ nízká energie (3-7)
Fe3+ + Ti3+ vysoká energie (3-8)
Přechod z rovnice (3-7) do rovnice (3-8) vyžaduje absorpci určitého množství světelné energie, což vede k širokému absorpčnímu pásmu, které se pohybuje od žluté po červenou. Naproti tomu většina modrého světla drahým kamenem prochází, což mu dodává modrý vzhled.
Přenos náboje mezi různými valenčními stavy má silnou směrovost a drahé kameny, které vykazují barvu díky tomuto mechanismu, často vykazují pleochroismus. Například akvamarín zbarvený Fe2+→ Fe3+ přenos náboje se projevuje barevně striktně podél směru optické osy. Obrázek 3-26 ukazuje, že akvamarín se v rovinách b a c jeví jako žlutý. Současně nedochází k žádnému takovému přenosu podél směru osy a, což má za následek žádnou absorpci světla, a tedy žádnou barvu podél směru osy a.
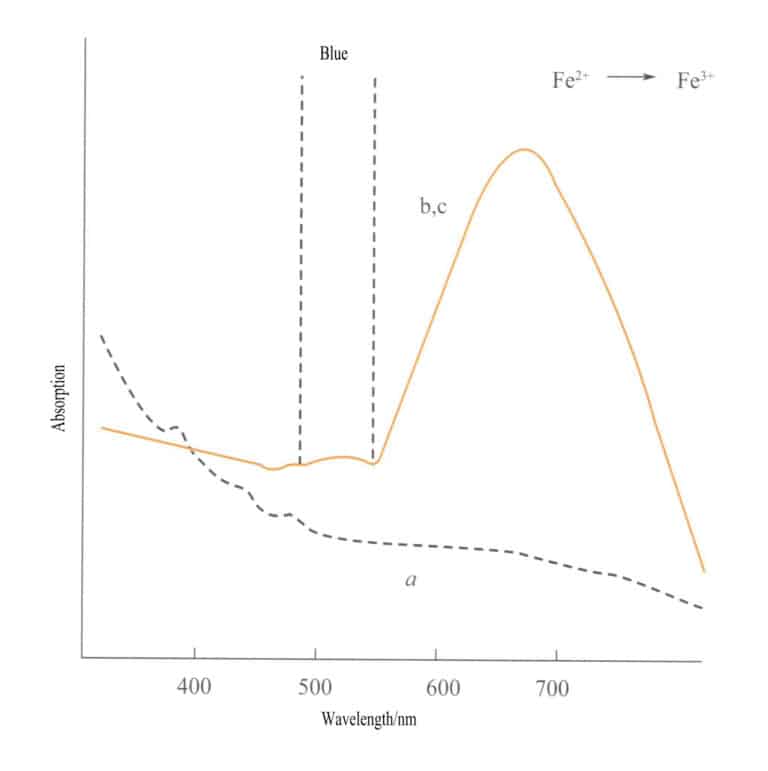
(2) Přenos náboje z nekovu na kov (L-M)
K tomuto typu přenosu náboje L-M často dochází mezi kyslíkem a ionty kovů a některé drahé kameny obsahující kyslík jsou zbarveny přenosem náboje z nekovu na kov, například O2–→ Fe3+, O2- →Cr6+, O2-→Mn6+, O →V5+.
V absorpčním spektru jednoduchých oxidů železa (obr. 3-27) se v infračervené oblasti objevují dva slabé absorpční pásy ilmenitu, hematitu a lepidokrocitu (elektronické přechody d - d). V krátkovlnné oblasti se objevuje silný absorpční pás, který vytváří O2-→Fe3+ a tento absorpční pás určuje charakteristické barvy těchto sloučenin: červenohnědou, hnědou a žlutohnědou.
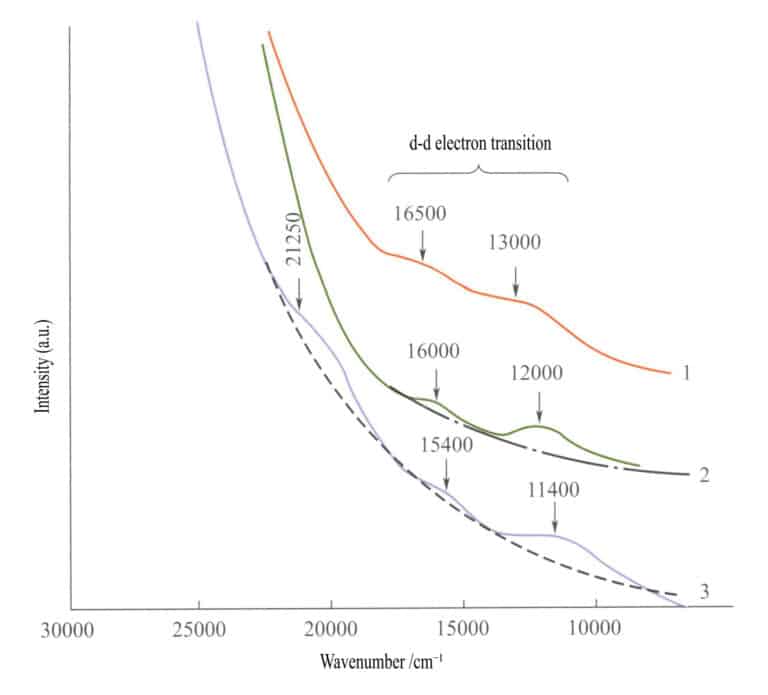
1 - ilmenit; 2 - hematit; 3 - lepidokrocit
Žlutý beryl získává svou barvu z O2–→ Fe3+ přenos náboje. Ve struktuře žlutého berylu je O2–→ Fe3+ silná absorpce přenosu náboje může přesahovat z ultrafialového konce do modrého konce viditelného spektra, přičemž absorbuje fialovou a modrou barvu, což vede ke žluté barvě.
Safír, který má zcela odlišné koordinační prostředí než beryl, může také vytvářet stejné spektrální absorpční pásy jako beryl, což má za následek žlutou barvu, která je rovněž výsledkem působení O2–→ Fe3+ přenos náboje.
Podle teorie krystalového pole některé minerály drahých kamenů neobsahují nespárované elektrony a nemohou vytvářet barvu. Například elektronické vrstvy krokoitu (PbCrO4), Pb2+, Cr6+a O2– jsou plné. Přesto je u CrO42- atomového klastru jsou "molekulární orbitaly", které odpovídají excitovaným stavům při O2-→Cr6+ přenos, vytváření absorpčních pásů a oranžové barvy.
L→M Přenos náboje zahrnuje také přenos síry na kov, jako je tomu u běžného pyritu; tento optický jev způsobený přenosem je snáze pochopitelný, pokud se o něm diskutuje pomocí pásové teorie.
(3) Přenos náboje z nekovu na nekov (L-L)
Molekulární orbitální teorie naznačuje, že tmavě modrá barva lapisu lazuli je způsobena excitačními energetickými hladinami S3- atomová skupina.
V grafitu jsou kruhy šesti atomů uhlíku uspořádány ve vrstvách. Podél této vrstvy se elektrony mohou do určité míry volně pohybovat, což má za následek silnou absorpci světla, anizotropii a vodivost.
Některé organické drahé kameny, jako je jantar a perly, mají elektrony, které se pohybují a excitují v atomových skupinách organických pigmentů na společných molekulárních orbitalech, což způsobuje absorpci viditelného světla a vytváří barvu. Například "medová žluť" jantaru, barvy korálů a některých mušlí a barevných perel.
Barevné mechanismy běžných drahých kamenů jsou uvedeny v tabulce 3-12.
Tabulka 3-12 Klasifikace barevných mechanismů běžných drahých kamenů
| Přenos náboje kov - kov | Fe2+ - Fe3+ /Fe3+ - Fe2+ : iolit (modrý), berthierit (modrý), magnetit (černý) atd. |
| Fe2+ -Ti4+/Fe3+ - Ti3+ : Kyanit (modrý), Safír (modrý) | |
| Mn2+-Mn4+/Mn3+-Mn3+: Manganit (černý), Bixbyit (černý) | |
| Přenos náboje z nekovu na kov | O2- -Fe3+: Zlatožlutý beryl, zlatožlutý safír, ilmenit, hematit, lepidokrocit atd. |
| O2- - Cr6+: Crocoite (oranžový) | |
| O2- -V5+:Vanadinit (oranžový) | |
| Síra na kov: pyrit, markazit atd. (viz polovodič s mezerou) | |
| Nekovový - nekovový přenos náboje | S3-: Lapis lazuli (modrý) |
| Π elektronická: grafitová (černá) | |
| Barvy některých organických drahých kamenů, jako je jantar a korál. |
Kopírování @ Sobling.Jewelry - Výrobce šperků na zakázku, továrna na šperky OEM a ODM
Oddíl III Teorie energetických pásem
Teorie energetických pásů je kvantově mechanický model pro studium materiálů s drahými kameny, který je dalším rozšířením teorie molekulových orbitalů. Studium teorie energetických pásů může lépe vysvětlit mechanismus zbarvení některých přírodně zbarvených drahých kamenů.
1. Základní pojmy teorie energetických pásů
Teorie energetických pásů je přibližná teorie používaná ke studiu zákonitostí pohybu elektronů v pevných látkách. Pevné látky se skládají z atomů, které zahrnují atomová jádra a vnější elektrony, které jsou v neustálém pohybu. Pásová teorie předpokládá, že elektrony v pevných látkách nejsou vázány na konkrétní atom, ale jsou společné pro celý krystal a pohybují se v periodickém potenciálovém poli trojrozměrného prostoru krystalu. Rozsah pohybu elektronů je v rámci periodického potenciálového pole mřížky, což umožňuje, aby prostorové rozložení elektronových orbitů přesáhlo rozložení molekul a dosáhlo maxima. Energetické hladiny jednotlivých elektronů jsou rozšířeny do energetických pásů.
Pásmová teorie se zabývá především přechody elektronů mezi nelokálními stavy, kde by všechny valenční elektrony měly patřit celé mřížce pevné látky. Podle pásové teorie lze pevné materiály rozdělit do různých energetických pásů podle toho, zda jsou atomové orbitaly zaplněny: zaplněný pás je tvořen energetickými hladinami atomových orbitalů, které jsou plně obsazeny elektrony, což představuje nízkoenergetický pás; prázdný pás je tvořen energetickými hladinami, které nejsou plně obsazeny elektrony, což představuje vysokoenergetický pás. Energetický rozdíl mezi těmito dvěma typy pásů se nazývá "pásmová mezera" (obrázek 3-28).
Pokud jsou všechny energetické pásy materiálu zaplněny, jedná se o nevodič; pokud jsou částečně zaplněny elektrony, jedná se o vodič. Mřížkové defekty vnášejí do krystalu další energetické hladiny, které umožňují elektronům vstoupit do těchto energetických hladin, což vede k podmíněné vodivosti.
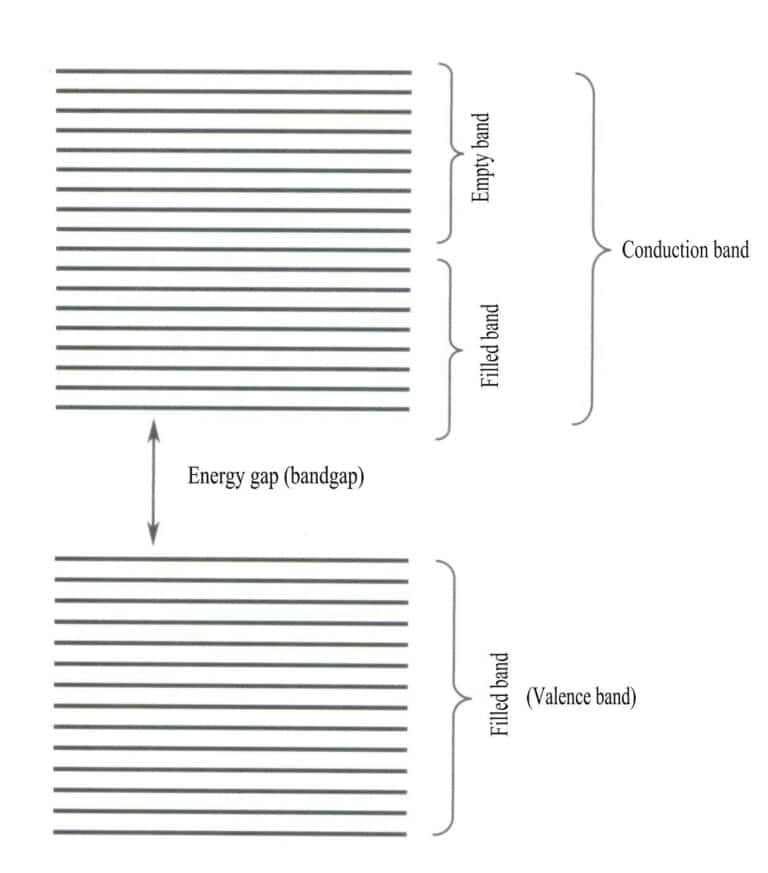
2. Charakteristiky přechodů mezi pásy
Některé minerály drahých kamenů obsahují prvky ze skupiny IV A periodické tabulky, například diamant a moissanit, které se vážou především kovalentně. Existují také další minerály, jako je sulfid kademnatý (CdS), jejichž barvy lze vysvětlit pomocí pásové teorie.
Elektrony absorbují světelnou energii a pohybují se mezi valenčním a vodivostním pásem, čímž vytvářejí "vnitřní pásové přechody". Pravděpodobnost přechodů úzce souvisí s rozdílem energií mezi valenčními a vodivostními pásy, známým jako energie pásmové mezery (Eg) (obrázek 3-29).

Na obrázku 3-29 (a) je typický pásový diagram polovodiče. Podle velikosti energie pásové mezery krystalu je lze rozdělit na tři typy: široká pásová mezera, úzká pásová mezera a střední pásová mezera. Široká pásová mezera má energii pásové mezery větší než energie viditelného světla; když energie pásové mezery přesahuje energii viditelného světla, viditelné světlo není absorbováno a zcela prochází, takže minerál je bezbarvý. Například energie pásové mezery diamantu Eg je přibližně 5,5 eV, takže je bezbarvý.
Energie pásu úzkopásmových materiálů je menší než energie viditelného světla, takže veškeré viditelné světlo je pohlceno, což vede k tmavě šedozeleným nebo černým barvám. Například energie pásové mezery galenitu je Eg méně než 0,4eV, což se jeví jako olověná šeď. Pokud má tento "úzkopásmový polovodič" vhodný geometrický tvar, vykazuje usměrňovací a zesilovací vlastnosti.
Energie materiálů se středním pásmovým rozpětím je přesně v oblasti viditelného světla a drahokamové minerály mají různé barvy. Jejich barevná posloupnost je znázorněna na obrázku 3-29 (c), od červenožluté přes zelenomodrou až po fialovou. Například energie pásové mezery (Eg) sulfidu kademnatého (CdS) je přibližně 2,5eV, který absorbuje modré a fialové světlo a jeví se jako žlutý. Pásová energie cinabaru je přibližně 2eV, což propouští pouze červené světlo, a proto se jeví jako červený. Energie pásu orpimentu je přibližně 2,5 eV, takže se jeví jako žlutý.
Další kategorií přírodních drahokamových minerálů vysvětlovanou pásmovou teorií je barva materiálů se širokým pásmem, které obsahují nečistoty. Například v případě diamantu s příměsemi je energie pásové mezery diamantu Eg přibližně 5,5eV a viditelné světlo není při průchodu diamantem absorbováno; čistý diamant je bezbarvý, ale situace se mění, když obsahuje příměsi.
(1) Barevný mechanismus žlutých diamantů
Atomy dusíku nahrazují pozice atomů uhlíku. Protože atomy dusíku mají o jeden elektron více než atomy uhlíku, vytváří tento elektron navíc v pásové mezeře příměsovou energetickou hladinu, známou jako donorová energetická hladina, přičemž atomy dusíku působí jako "dárci".
Existence této úrovně nečistoty snižuje energii pásmové mezery na 4eV[ [Obrázek 3-30 (a)]. Může být i nižší, což umožňuje absorbovat ultrafialové světlo a trochu 3eV fialového světla, což způsobuje, že diamant vypadá žlutě.
Tento efekt je silný; jeden atom dusíku na každých sto tisíc atomů uhlíku může způsobit, že diamant bude sytě žlutý. Zmenšení pásmové mezery však stále nestačí k tomu, aby byl diamant vodivý při pokojové teplotě.
(2) Mechanismus vzniku barvy u modrých diamantů
Protože má bór o jeden elektron méně než uhlík, tvoří "akceptorovou hladinu" v pásové mezeře diamantu. Nemá sice elektrony navíc, ale může přijímat elektrony z valenčního pásu diamantu, čímž vytváří ve valenčním pásu díry [obrázek 3-30 (b)] a vytváří příměsový energetický pás asi 0,4 eV nad valenčním pásem, známý jako akceptorová hladina.

Akceptorová energetická hladina není jednoduchá; jedná se o složitou strukturu příměsových energetických pásů, které mohou vytvářet modrou barvu. Akceptorová energetická hladina vytváří "díry" ve valenčním pásu, což umožňuje tomuto "děrovému" modrému diamantu typu II b vést elektrický proud.
Jeden atom boru na každý milion atomů uhlíku může tvořit modrou barvu. Vzhledem k vyššímu obsahu hliníku v tomto modrém diamantu a k tomu, že hliník má o jeden elektron vnější vrstvy méně než uhlík, se dříve předpokládalo, že hliník hraje roli akceptoru. Přesto současné experimenty prokázaly, že je to bór, nikoliv hliník.
Vodivé modré diamanty typu II b jsou přirozeně modré a jejich vodivost je jedním z rozdílů od ozářených modrých diamantů (barevných center). Tato vlastnost se často používá k rozlišení obou typů diamantů. Žluté diamanty s donorovým dusíkem však nevedou elektrický proud, takže tuto metodu nelze použít k jejich odlišení od ozářených žlutých diamantů.
3. Minerály drahých kamenů zbarvené pásovými přechody
Teorie energetických pásů může částečně vysvětlit vznik barev přírodních drahých kamenů. Vzhledem k tomu, že pásmová energie je přirozenou vlastností krystalu a nemění se vlivem vnějších podmínek, je barva drahých kamenů dobře stabilní. Vodivost krystalu lze určit na základě toho, zda jsou energetické pásy v krystalu zaplněny elektrony. V tabulce 3-13 jsou uvedeny typy barev drahých kamenů, které lze vysvětlit pomocí pásové teorie, a jejich vodivostní vlastnosti.
Tabulka 3-13 Typy barev drahokamů vysvětlené pásmovou teorií a jejich vodivost
| Vodiče (kovové barvy a kovový lesk) | Prvek | Měď, zlato, železo, stříbro, rtuť atd. |
| Slitina | Amalgám, Meteorit nikl železo | |
| Polovodiče | Úzká mezera mezi pásmy | Neprůhledný šedý až černý: altait, galenit |
| Neprůhledná kovová barva: kobaltín, markazit, pyrit, smaltit | ||
| Mírná pásmová mezera | Červená: cinabar, proustit, pyrargyrit | |
| Oranžová: Realgar | ||
| Žlutá barva: Sulfid kademnatý, realgar, síra. | ||
| Široká pásmová propust | Bezbarvé: diamant, sfalerit | |
| Polovodiče s širokým pásmem obsahující nečistoty | Dárcovská nečistota: Diamant dopovaný dusíkem (žlutý) | |
| Nečistoty v hostiteli: diamant obsahující bór (modrá) |
Barva drahých kamenů způsobená pásovými přechody souvisí se strukturou a typem vazby v době vzniku drahého kamene. Má jen malý vztah k pozdějším nečistotám a krystalovým vadám. Velikost energie pásové mezery drahých kamenů je pevně daná. Nemění se s vlastnostmi materiálu drahého kamene, takže konvenční optimalizační metody obecně nemohou zlepšit barvu drahých kamenů.
Oddíl IV Fyzikální optické účinky
Většina přírodních drahých kamenů může způsobovat selektivní absorpci světla a různé drahé kameny absorbují viditelné světlo různých vlnových délek, což vede k různým barvám. Kromě selektivní absorpce světla může vnitřní struktura krystalů drahých kamenů způsobovat také fyzikální optické efekty, které vedou k různým barvám drahých kamenů.
1. Minerály drahých kamenů související s fyzikálními optickými jevy
Barvy vznikající fyzikálními optickými jevy vznikají v důsledku disperze, interference, difrakce a dalších příčin světla způsobených strukturou nebo složením krystalu a inkluzí. Jedná se pouze o optický efekt, který lze vysvětlit pomocí fyzikální optické teorie. Různé drahé kameny mohou při stejných optických efektech vytvářet různé barvy. Kromě běžných stopových prvků, které způsobují barvu, souvisejí příčiny barev vytvářených fyzikálními optickými efekty především s vnitřní strukturou a fyzikálními vlastnostmi drahých kamenů. Typy minerálů drahých kamenů, které způsobují barvy v důsledku fyzikálních optických efektů, jsou uvedeny v tabulce 3-14.
Tabulka 3-14 Typy drahých kamenů způsobené fyzikálními optickými efekty
| Funkce | Optické vlastnosti a barva | Drahokamové minerály |
|---|---|---|
| Disperze Rozptyl | Třpytivé | "Oheň" v disperzních drahých kamenech, jako jsou diamanty, zirkon, rutil a titaničitan stroncia. |
| Modrá | Měsíční kámen, modrý křemen, opál | |
| Fialová | Fluorit (rozptyl mikrokrystalů vápníku) | |
| Červená | Rubínové sklo, rozptyl mikrokrystalů mědi nebo zlata | |
| Bílá | Mléčný křemen | |
| Efekt kočičího oka | akvamarín kočičí oko, pyroxen kočičí oko atd. | |
| Efekt hvězdného světla | Různé hvězdné efekty korundu a granátu | |
| Luster | Lesk perel, apofylitu atd. | |
| Sparkle | Třpyt aventurínu, obsidiánu atd. | |
| Interferenční difrakce | Čisté spektrální barvy tenké vrstvy | Duha chalkopyritu, odbarvená vrstva v trhlině křemene irisové barvy |
| Interferenční účinky | Změna barvy opálu, efekt labradoritu | |
| Zařazení | Modrá | Dumortierit v křemeni |
| Zelená | Zelený chalcedon a niklové žilky v zeleném chalcedonu, fuchsit v hvězdném křemeni | |
| Orange | Hydratovaný oxid železitý v ohnivém opálu a chalcedonu tělové barvy | |
| Červená | Hematitové vločky v ortoklasu |
2. Interferenční a difrakční efekty
(1) Interferenční účinky
K interferenčním jevům dochází, když se dva světelné paprsky šíří po stejné optické dráze nebo v paralelních směrech. Běžným interferenčním jevem u drahých kamenů je iridescence. Například u iridiscenčního křemene závisí interferenční barvy na tloušťce vrstvy, indexu lomu vrstvy a charakteru dopadajícího světla.
Interferenční barvy perel vznikají soustředným střídavým vrstvením dvou látek s různými indexy lomu (aragonitu a nacru), kdy se dopadající světlo odráží od ploch mezi střídajícími se vrstvami a odražené světlo interferuje s dopadajícím světlem a vytváří nádherné interferenční barvy.
(2) Difrakční efekty
Difrakce je fyzikální jev, při kterém se světelné vlny při setkání s překážkami odchylují od svého původního přímočarého šíření. Ve fyzice dochází při průchodu překážkami, jako jsou štěrbiny, malé otvory nebo disky, k různým stupňům ohybu a rozptylu světelných vln. Je-li mezi zdrojem světla a pozorovací obrazovkou umístěna překážka, objeví se na pozorovací obrazovce světlé a tmavé oblasti, jejichž hranice nejsou ostré a vytvářejí složitý obrazec světla a tmy. Tento jev se nazývá difrakce. K těmto jevům může dojít vždy, když světelné vlny narazí na překážky na své dráze šíření. Nejdůležitějším faktorem při vzniku difrakce je přítomnost periodicky rozmístěných difrakčních mřížek v minerálech drahých kamenů.
① Změna barvy opálu
V opálu mají kuličky oxidu křemičitého obsahující vodu stejný průměr a jsou uspořádány v pravidelné střídavé vrstevnaté struktuře, která vytváří periodicky rozmístěné difrakční mřížky. Když do opálu vstoupí světlo, dochází k difrakci a změně barvy (obrázky 3-31, 3-32). Druhy barev a stupeň změny barvy závisí především na mezirovinných vzdálenostech naskládaných křemenných kuliček.
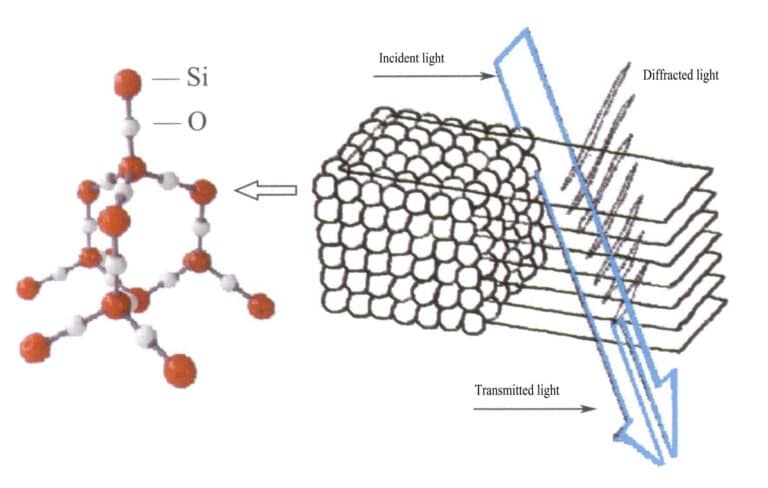

Například opál s plochou destičkou s kubickou strukturou s centrovaným povrchem a mřížkovou roztečí 3×10-10m vykazuje barvy od zelené po červenou; tento typ opálu s roztečí mřížek 2,5×10-10m zobrazuje barvy od modré po žlutou.
② Labradoritový efekt
Labradorit vykazuje také podobné efekty jako opál (obrázek 3-33). Labradorit je také známý jako spektrolit, protože se může blýskat barevným slunečním světlem. Různé typy labradoritu z Finska mohou vykazovat řadu spektrálních barev, což je jev známý jako "labradoritový efekt". Efekt změny barvy u labradoritu je způsoben malými mezivrstvami taveniny plagioklasu s různým složením. Nepatrné rozdíly v indexu lomu mezi různými živci způsobují interferenci a difrakci světla, což vede k luminiscenci a změně barvy. Barvy, které tato struktura vytváří, souvisejí s relativní tloušťkou vrstev a jejich indexy lomu. Příležitostně vykazuje difrakční jevy také andradit z Mexika.

3. Rozptyl a inkluze
(1) Rozptyl
K rozptylu obecně dochází, pokud je vnitřní struktura drahokamových materiálů nepravidelná nebo pokud velikost složek přesahuje hranice difrakčních podmínek. Barevné efekty způsobené rozptylem souvisejí s velikostí a tvarem částic drahokamového materiálu. Při interakci dopadajícího světla s nepravidelně uspořádanými částicemi menšími, než je vlnová délka viditelného světla, jsou prošlé vysokoenergetické světelné vlny silnější než nízkoenergetické světelné vlny, což znamená, že ve většině případů lze pozorovat pouze fialovou a modrou barvu. Například SiO2 malé kuličky v opálu mají průměr menší než vlnová délka viditelného světla, a pokud se velikost rozptylujících částic blíží vlnové délce viditelného světla, mohou se objevit i rozptylové barvy.
Například fialový fluorit vzniká radioaktivním ozářením, při kterém se vyloučí atomy fluoru, což vede ke kondenzaci atomů vápníku, které se vážou s atomy fluoru do hexagonálních destiček o velikosti srovnatelné s vlnovou délkou viditelného světla. Interakce mezi vápenatými destičkami a světelnými vlnami způsobuje rozptyl. Absorbuje některé světelné vlny a vytváří silný absorpční pík v oblasti zeleného až červeného světla, což umožňuje průchod fialového světla a vznik fialové barvy.
Protože částice kovových prvků stejné velikosti mohou vytvářet podobné barevné efekty a různé kovové částice mohou vytvářet různé barvy, jsou některé imitace drahokamů vyráběny s využitím této vlastnosti.
Například "rubínové" sklo se vyrábí přidáním částic mědi nebo zlata do skla, čímž se získá červená barva podobná barvě rubínů. Pokud materiál drahokamu obsahuje inkluze, mikrotrhliny nebo bublinky větší, než je vlnová délka viditelného světla, světelné vlny interagují s těmito rozptylujícími částicemi, což způsobuje rekombinaci rozptýlených světelných vln a vytváří průsvitné mléčné světlo. Například některé imitace měsíčního kamene.
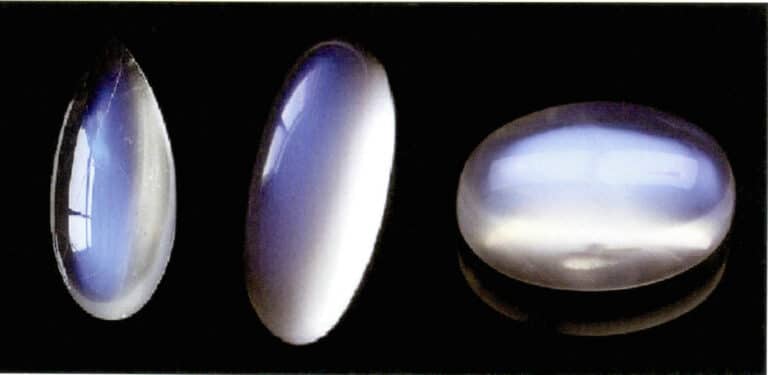
Efekt měsíčního světla měsíčního kamene vzniká také rozptylem světla (obrázek 3-34). Měsíční kámen je alkalický živec, kompozit tvořený střídajícími se paralelními vrstvami živce bohatého na draslík a sodík. Tloušťka mezivrstev se obvykle pohybuje v rozmezí 50 ~ 1000 nm, přičemž tenčí vrstvy jsou schopny vytvářet rozptyl. Stejná barva rozptylu se může vyskytovat také u plagioklasu, známá jako "labradoritový efekt".
Speciálně orientované uspořádání rozptylujících částic může vyvolat charakteristické optické efekty. Například pokud jsou rozptylující částice v paralelní vláknité formě, vytvářejí efekty kočičího oka nebo hvězdy, jako jsou hvězdné safíry a křemenné kočičí oči. Pokud jsou rozptylující částice dostatečně velké, aby je bylo možné rozlišit pouhým okem, mohou vytvářet "efekt zlatého kamene", jako je sluneční kámen (obrázek 3-35) a zlaté sklo.

(2) Inkluze
Barevné a optické jevy způsobené inkluzemi jsou zvláštním typem rozptylu. Barevné inkluze zasazené do téměř bezbarvých hlavních krystalů se projeví barvou inkluzí, jako je například nikl obsahující páskovaný chalcedon a vodu obsahující oxid železitý (FeO - H2O) chalcedon tělové barvy; barva ortoklasu z Madagaskaru a některých kordieritů je tvořena o něco většími, ale stále mikroskopickými inkluzemi hematitu, které vytvářejí červené odstíny; submikroskopické inkluze hydroxidu železitého často barví ohnivý opál.
Diamanty často vykazují různé barvy v důsledku přítomnosti četných inkluzí. Diamanty zbarvené inkluzemi mohou být černé, oranžovočervené a hnědočervené. Pokud diamant obsahuje nespočet tmavých neprůhledných minerálních inkluzí, jeví se jako černý; při zkoumání silným procházejícím světlem lze pozorovat mnoho tmavých inkluzí a diamant se jeví jako tmavě šedý; dalším typem jsou sekundární inkluze, které se vyskytují v trhlinách diamantu. Když se trhliny vyvinou a vyplní těmito barevnými inkluzemi, diamant se jeví jako hnědočervený nebo oranžovočervený, což je také známé jako "oxidovaný" diamant.
4. Disperze
Jev rozkladu bílého světla na různé spektrální barvy v objektu se nazývá disperze. Disperze drahých kamenů označuje vlastnost rozptylu světla na různé vlnové délky spektrálních barev při průchodu skloněnými rovinami průhledných drahých kamenů. Vzhledem k různým vlnovým délkám monochromatického světla, které tvoří bílé světlo šířící se různými rychlostmi a indexy lomu v různých materiálech, může být bílé světlo za určitých podmínek rozloženo na různé spektrální barvy. Velikost disperzní hodnoty drahého kamene je dána jeho fyzikálními vlastnostmi; každý drahý kámen má svou vlastní disperzní hodnotu, která se s vlastnostmi drahého kamene nemění. Jedinečný půvab diamantů úzce souvisí s jejich vysokou hodnotou disperze (0,044).
Většina simulantů diamantů má vyšší disperzní hodnotu, například disperzní hodnota zirkonu je 0,039 a disperzní hodnota syntetického moissanitu 0,104. Srovnání hodnot disperze diamantů a jejich běžných simulantů drahých kamenů je uvedeno v tabulce 3-15.
Tabulka 3-15 Srovnání hodnot rozptylu diamantů a jejich běžných simulantů drahých kamenů
| Název drahého kamene | Hodnota rozptylu |
|---|---|
| Diamond | 0.044 |
| Zirkon | 0.039 |
| Korund | 0.018 |
| Spinel | 0.020 |
| Topaz | 0.014 |
| Beryl | 0.014 |
| Crystal | 0.014 |
| Syntetický rutil | 0.280 |
| Syntetický titanistan stroncia | 0.190 |
| Syntetický moissanit | 0.104 |
Disperze se běžně označuje jako "oheň" drahých kamenů. Například diamanty mají vysokou hodnotu disperze a jejich oheň je velmi výrazný, což zvyšuje již tak královský status diamantů a ukazuje jejich jedinečný půvab.
Existuje mnoho typů barev, které vznikají fyzikálními optickými jevy a které lze všechny vysvětlit pomocí fyzikální optické teorie. Kromě disperze, která je přirozenou vlastností samotného drahokamu, jsou ostatní jevy způsobeny strukturálními změnami po vzniku drahokamu a rozdíly v mechanických inkluzích. Pochopení různých příčin barev drahých kamenů poskytuje teoretický základ pro optimalizaci úpravy přírodních a syntetických drahých kamenů.